文档内容
第四章 生物大分子
第一节 糖类
第1课时 糖类的组成和分类 单糖
糖类是生命中的另一种基础有机化学物质。本节内容分为三部分,第- - 部分葡萄糖与果糖,第
二部分蔗糖与麦芽糖,第三部分淀粉与纤维素,课文中穿插了单糖的性质、二糖的水解对比探究实
验、化学方法水解淀粉条件的研究等系列实验。通过课堂内的实验探究,使学生认识和体会单糖、
二糖、多糖性质的研究过程,理解葡萄糖、果糖、蔗糖、麦芽糖、淀粉的结构。教学设计时要高效
地利用教科书、课外资料、生动的录像和图片,充分调动学生已有的生活经验,如学生对葡萄糖、
蔗糖、淀粉的感性认识,以及烃的衍生物中已有的醛类、醇类知识,进行类推、延伸、替代、变
换、重组、迁移等思维方式的训练,以使学生的思维对象由单官能团的化合物、小分子的化合物自
然地过渡到多官能团的化合物和高分子化合物,形成糖类完整、系统的知识体系,理解糖类在生命
活动过程中的重要作用。
课程目标 学科素养
1. 了解糖类的概念、分类及结构特点。 a. 宏观辨识与与微观探析:了解糖类的概念、分类
2. 熟知葡萄糖的结构和性质,学会葡萄糖 及结构特点。
的检验方法。 b. 变化观念与科学探究:熟知葡萄糖的结构和性
质,学会葡萄糖的检验方法。
教学重点: 葡萄糖的组成、典型性质及应用
教学难点: 从官能团典型性质的角度认识糖类物质与醛、酮、醇物质的关系
讲义 教具
【新课导入】
糖类是一类重要的有机化合物,在自然界中分布广泛,日常食用的蔗糖、粮食中的淀粉、植物茎叶
中的纤维素、人体血液中的葡萄糖等均属于糖类。糖类在生命活动中起着重要作用,是生物体所需
能量的主要来源,也是重要的能量储存物质,如植物体内的淀粉和动物体内的糖原。糖类还是很多
生物体的结构成分,如植物细胞壁的主要成分纤维素。
[展示]葡萄糖、蔗糖、麦芽糖、纤维素、淀粉图片。任务一:糖类的组成和分类
1. 观察葡萄糖、蔗糖、麦芽糖、纤维素、淀粉的分子式,分析糖类的组成。
2. 糖类与碳水化合物的关系
3. 糖类的定义
4. 糖类的分类
【讲解】
1. 糖类都是由碳、氢、氧三种元素组成的,组成通式为C (H O) 。
n 2 m
2. 随着化学的发展,人们发现并不是所有糖的组成都符合上述通式,如脱氧核糖(C H O),而
5 10 4
某些符合此通式的物质却不属于糖类,如乙酸(C HO)。因此,碳水化合物这一名称并不准确,
2 4 2
但因沿用已久,目前仍在使用。
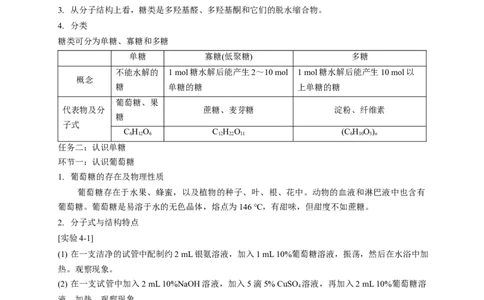
3. 从分子结构上看,糖类是多羟基醛、多羟基酮和它们的脱水缩合物。
4. 分类
糖类可分为单糖、寡糖和多糖
单糖 寡糖(低聚糖) 多糖
不能水解的 1 mol糖水解后能产生2~10 mol 1 mol糖水解后能产生10 mol以
概念
糖 单糖的糖 上单糖的糖
葡萄糖、果
代表物及分 蔗糖、麦芽糖 淀粉、纤维素
糖
子式
C H O C H O (C H O)
6 12 6 12 22 11 6 10 5 n
任务二:认识单糖
环节一:认识葡萄糖
1. 葡萄糖的存在及物理性质
葡萄糖存在于水果、蜂蜜,以及植物的种子、叶、根、花中。动物的血液和淋巴液中也含有
葡萄糖。葡萄糖是易溶于水的无色晶体,熔点为146 ℃,有甜味,但甜度不如蔗糖。
2. 分子式与结构特点
[实验4-1]
(1) 在一支洁净的试管中配制约2 mL银氨溶液,加入1 mL 10%葡萄糖溶液,振荡,然后在水浴中加
热。观察现象。
(2) 在一支试管中加入2 mL 10%NaOH溶液,加入5滴5% CuSO 溶液,再加入2 mL 10%葡萄糖溶
4
液,加热。观察现象。
[实验现象]
(1)试管壁上形成银镜。
(2)溶液有砖红色沉淀产生。
[实验结论]
(1)葡萄糖具有还原性,属于还原糖
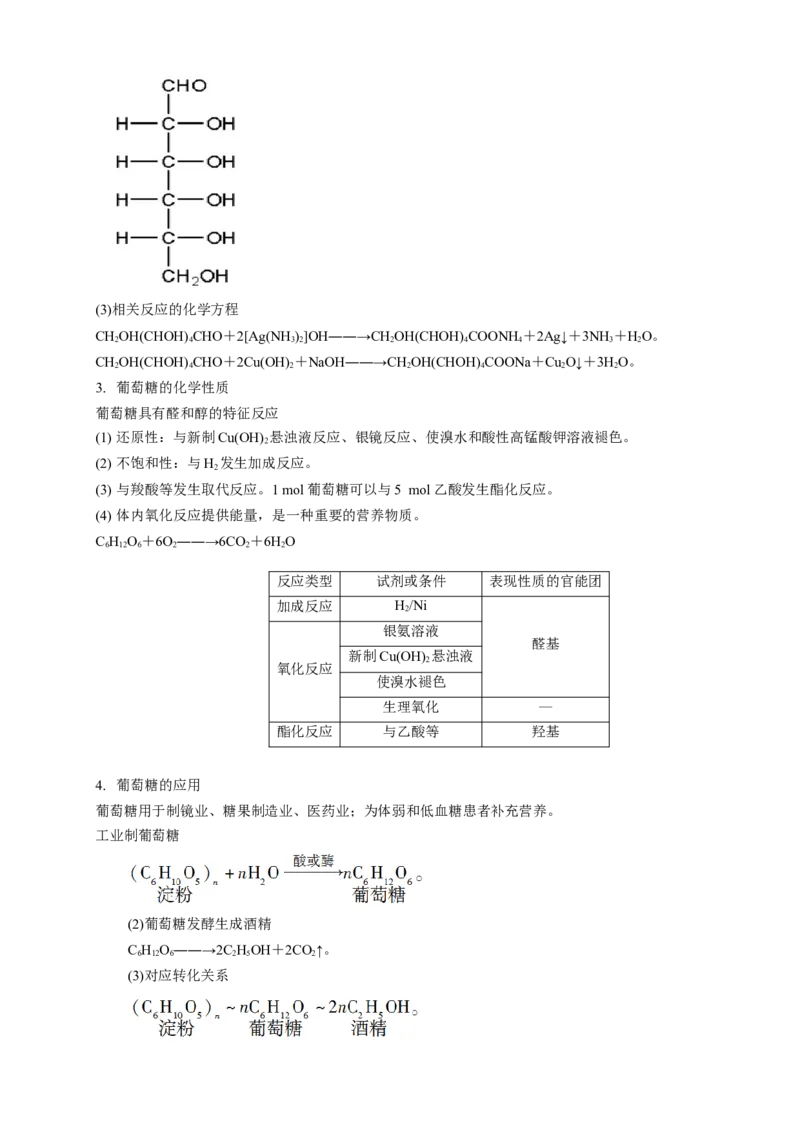
(2)葡萄糖的结构
分子式为C H O,分子中含有醛基和羟基,属于醛糖。结构简式为CHOH(CHOH) CHO。
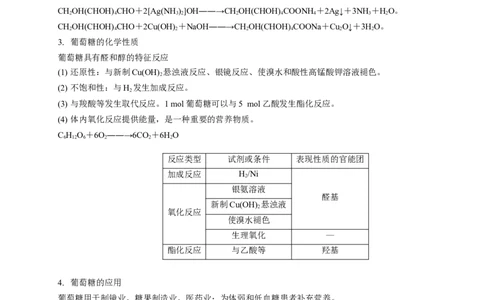
6 12 6 2 4(3)相关反应的化学方程
CHOH(CHOH) CHO+2[Ag(NH)]OH――→CHOH(CHOH) COONH+2Ag↓+3NH +HO。
2 4 3 2 2 4 4 3 2
CHOH(CHOH) CHO+2Cu(OH) +NaOH――→CHOH(CHOH) COONa+Cu O↓+3HO。
2 4 2 2 4 2 2
3. 葡萄糖的化学性质
葡萄糖具有醛和醇的特征反应
(1) 还原性:与新制Cu(OH) 悬浊液反应、银镜反应、使溴水和酸性高锰酸钾溶液褪色。
2
(2) 不饱和性:与H 发生加成反应。
2
(3) 与羧酸等发生取代反应。1 mol葡萄糖可以与5 mol乙酸发生酯化反应。
(4) 体内氧化反应提供能量,是一种重要的营养物质。
C H O+6O――→6CO+6HO
6 12 6 2 2 2
反应类型 试剂或条件 表现性质的官能团
加成反应 H/Ni
2
银氨溶液
醛基
新制Cu(OH) 悬浊液
2
氧化反应
使溴水褪色
生理氧化 —
酯化反应 与乙酸等 羟基
4. 葡萄糖的应用
葡萄糖用于制镜业、糖果制造业、医药业;为体弱和低血糖患者补充营养。
工业制葡萄糖
(2)葡萄糖发酵生成酒精
C H O――→2C HOH+2CO↑。
6 12 6 2 5 2
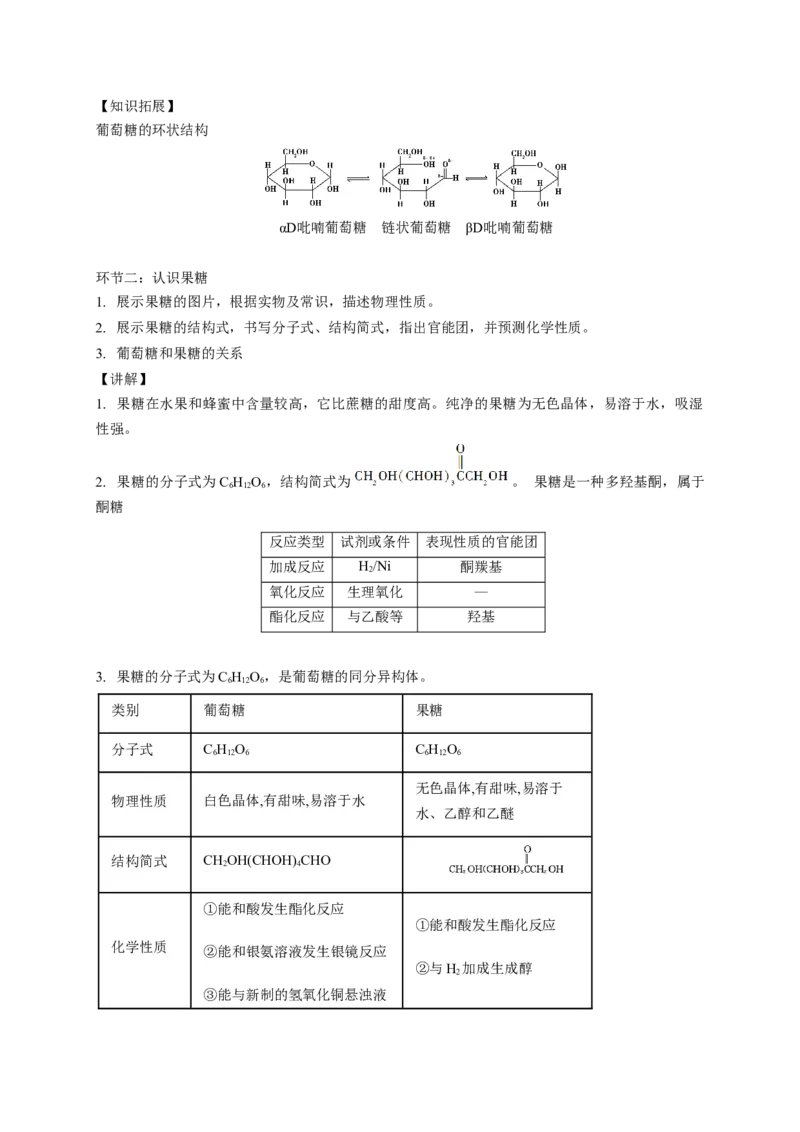
(3)对应转化关系【知识拓展】
葡萄糖的环状结构
αD吡喃葡萄糖 链状葡萄糖 βD吡喃葡萄糖
环节二:认识果糖
1. 展示果糖的图片,根据实物及常识,描述物理性质。
2. 展示果糖的结构式,书写分子式、结构简式,指出官能团,并预测化学性质。
3. 葡萄糖和果糖的关系
【讲解】
1. 果糖在水果和蜂蜜中含量较高,它比蔗糖的甜度高。纯净的果糖为无色晶体,易溶于水,吸湿
性强。
2. 果糖的分子式为C H O ,结构简式为 。 果糖是一种多羟基酮,属于
6 12 6
酮糖
反应类型 试剂或条件 表现性质的官能团
加成反应 H/Ni 酮羰基
2
氧化反应 生理氧化 —
酯化反应 与乙酸等 羟基
3. 果糖的分子式为C H O,是葡萄糖的同分异构体。
6 12 6
类别 葡萄糖 果糖
分子式 C H O C H O
6 12 6 6 12 6
无色晶体,有甜味,易溶于
物理性质 白色晶体,有甜味,易溶于水
水、乙醇和乙醚
结构简式 CHOH(CHOH) CHO
2 4
①能和酸发生酯化反应
①能和酸发生酯化反应
化学性质
②能和银氨溶液发生银镜反应
②与H 加成生成醇
2
③能与新制的氢氧化铜悬浊液反应产生红色沉淀
④与H 加成生成醇
2
相互关系 互为同分异构体
用途 用于制镜、糖果、医药等行业 主要用于食品工业
环节三:核糖与脱氧核糖
1.核糖与脱氧核糖分别是生物体的遗传物质核糖核酸(RNA)与脱氧核糖核酸(DNA)的重要组成
部分。它们都是含有5个碳原子的单糖——戊糖。均为醛糖,具有还原性。
2.糖类分子与手性
(1)手性碳原子:在分子中连有4个不同的原子或原子团的碳原子叫做不对称碳原子,也叫手性碳原
子。
(2)手性分子:含有手性碳原子存在不能重叠、互为镜像的对映异构体的分子称手性分子:如
为手性分子。
环节四:知识建构单糖
1. 糖类是由C、H、O三种元素组成的一类有机化合物。下列物质不属于糖类的是
A. 葡萄糖 B. 果糖 C. 纤维素 D. 蛋白质
【答案】D【解析】
A.葡萄糖是单糖,属于糖类,故A错误;
B.蔗糖是二糖,属于糖类,故B错误;
C.纤维素是多糖,属于糖类,故C错误;
D.蛋白质不属于糖类,故D正确。
故选D。
2. 糖类、油脂、蛋白质都是与生命息息相关的物质,下列有关说法正确的是
A. 葡萄糖和蔗糖是同系物,淀粉和纤维素是同分异构体
B. 淀粉、纤维素、油脂、蛋白质都是高分子化合物,都能发生水解反应
C. “春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”“泪”分别是纤维素和油脂
D. 通过灼烧时产生的气味可以鉴别蚕丝和棉纱
【答案】D
【解析】
A.同系物是指结构相似分子组成相差若干个 原子团的有机物,葡萄糖和蔗糖结构不相似,不
是同系物;纤维素和淀粉都是多糖,分子式都可用 表示,但两者的n不同,它们不是同
分异构体,故A错误;
B.油脂相对分子质量较小,不属于高分子化合物,故B错误;
C.“丝”中含有的物质是蛋白质,“泪”指的是液态石蜡,液态石蜡属于烃,故C错误;
D.蛋白质灼烧具有烧焦羽毛的气味,纤维素灼烧没有烧焦羽毛的气味,蚕丝的成分是蛋白质、棉纱
的成分是纤维素,所以可以用灼烧的方法鉴别,故D正确;
故选D。
3. 下列说法中不正确的是
A. 符合通式 的物质一定是葡萄糖
B. 葡萄糖由C、H、O三种元素组成
C. 糖类是人类维持生命的六大类营养素之一
D. 纤维素不能作为人类的营养食物
【答案】A
【解析】A.满足这个通式的不一定是葡萄糖,如甲醛 ,故A错误;
B.葡萄糖所含的元素是C、H、O,故B正确;
C.糖类是六大类营养素之一,故C正确;
D.人体内无纤维素酶,纤维素不能作为人类的营养食物,故D正确。
故选A。
4. 新版人民币的发行,引发了人们对有关人民币中化学知识的关注。下列表述不正确的是
A. 制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素
B. 用于人民币票面文字等处的油墨中所含有的 是一种磁性物质
C. 某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是葡萄糖
D. 防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料
【答案】C
【解析】
A.棉花、优质针叶木等原料的主要成分是纤维素,故A正确;
B. 是一种磁性物质,故B正确;
C.遇碘变蓝的是淀粉,不是葡萄糖,故C错误;
D.树脂属于有机高分子材料,故D正确。
故选C。
5. 下列有关化合物X的叙述正确的是
A. X分子只存在2个手性碳原子
B. X分子能发生氧化、取代、消去反应
C. X分子中所有碳原子可能在同一平面上
D. 1 mol X与足量NaOH溶液反应,最多消耗3 mol NaOH
【答案】B
【解析】
分子中连接 ,且相邻的2个碳原子连接4个不同的原子或原子团,为手性碳原子,共 3
个,故A错误;
B.含有羟基,可发生氧化反应,取代反应、消去反应,故B正确;
C.含有饱和碳原子,具有甲烷的结构特征,则所有的原子不在同一个平面上,故C错误;
D.能与氢氧化钠反应的为酯基、溴原子,则 1 mol X与足量NaOH溶液反应,最多消耗2 mol NaO
H,故D错误。
故选:B。通过选择贴近生活实际的素材,认识常见的糖类——葡萄糖、蔗糖、麦芽糖、淀粉和纤维素。
了解糖类的概念、分类及结构特点。从官能团典型性质的角度认识糖类物质与醛、酮、醇物质的关
系,培养宏观辨识与与微观探析的核心素养;熟知葡萄糖的结构和性质,学会葡萄糖的检验方法。
培养变化观念与科学探究;