文档内容
第四章 生物大分子
第一节 糖类
第一课时 糖类的组成和分类
课题: 4.1.1 糖类的组成和分类 课时 2 授课年级 高二
《普通高中化学课程标准(2017年版)》对本节课作出了明确的【内容要求】:
根据2022年版义务教育化学课程标准,对糖类的教学要求如下:
糖类的概念和分类:要求学生了解糖类的定义,掌握单糖、二糖、多糖等基本分类,并
能够识别各种糖类的结构特点。
糖类的性质和制备:要求学生了解糖类的物理性质和化学性质,如还原性、水解反应
等,同时掌握糖类的制备方法,如淀粉的水解制备葡萄糖等。
课标要 糖类在生物体内的作用:要求学生了解糖类在生物体内的代谢过程,如葡萄糖的氧化分
解,以及糖类在生物体中的功能,如能量供应、细胞识别等。
求
糖类与人类生活:要求学生了解糖类在人类饮食中的作用,如糖类的摄入与血糖水平的
调节,以及糖类与健康的关系,如糖尿病的发生机制等。
糖类的应用:要求学生了解糖类在工业、医药等领域的应用,如葡萄糖酸钙在补钙剂中
的应用,以及淀粉在造纸、纺织等领域的应用。
总的来说,2022年版义务教育化学课程标准对糖类的要求不仅包括糖类的基本概念、分
类和性质,还包括糖类在生物体内的作用、与人类生活的关系以及在实际应用中的重要性。
这些要求旨在帮助学生建立全面的糖类知识体系,提高学生的科学素养。
糖类第1课时,由光合作用视频引出糖的概念,进而关注其组成和结构特点;根据已有知
识结构(主要源于生物学认知)对常见的各类别糖的了解是并列的,可以将各类糖的典型代表物
统筹学习,然后再仔细对比各自分子结构异同。为了加深对醛基官能团的了解,并基于实验证
据,引导学生完成教材[实验4-1],并对该实验延伸补充,将果糖、核糖与脱氧核糖作对比实验,进
行探究,完善了官能团性能从书面认知到用实验认识,从实验现象到实验结论的推理论证。
在糖类性质的学习中,注重联系以前学习的醛类、醇类等知识,进行类推、迁移,紧紧抓住
结构决定性质的学科思维。在讲授糖类的各种典型代表物之间的转化,以及选学内容葡萄糖链
状和环状的转化过程中,将糖类学习融入有机化学学习的基本方式中,熟练掌握分子结构、官
能团与性质之间的联系。在书写糖分子的结构式时,如学生基础较好,还可以关注手性。最后
教材
组织学生讨论糖尿病的发现与检测,提高学生将所学知识应用于日常生活的积极性,将所学知
分析 识用于解决生活实际问题。
学到糖的第2课时,从糖的分类入手,自然引出二糖、多糖等概念,然后给学生分享典型
的二糖、多糖等,从宏观辨识到微观探析,探析二糖的还原性等性质。在探究过程中,学生自己
讨论,设计方案,操作完成实验,体会一套完整的实验方案。探究完二糖的水解反应后,引导学
生书写水解反应的化学方程式,体会用化学用语表达化学反应的过程。水解反应探究之后,逆
向思维,探究单糖的脱水缩合过程,形成完整而严谨的实验思路,感知变化观点与创新思想。
在学习多糖的过程中,沿用之前探究单糖和二糖的思路,层层递进,从宏观辨识到微观探析,
除了探究糖类的水解反应以及水解产物是否具有还原性,还拓展多糖其他的一些性质,比如淀
粉遇碘变蓝、纤维素的酯化反应等。始终注意引导学生关注物质的用途,体会学科价值。
1.知道糖类的元素组成和分类,了解单糖、寡糖(主要讨论二糖)和多糖的典型代表物质及
教学目
其化学式。从组成的角度对糖类进行分类,从结构的角度认识有机化合物中醛基、羟基的特
标
性,发展学生的宏观辨识与微观探析素养水平。2.通过分组实验,探究并掌握葡萄糖的特征反应,认识有机化合物中醛基、羟基的特性,类
比学习有醛基的核糖、脱氧核糖等单糖。对比学习果糖,并能在一定指导下进行规范实验操
作,培养并提升实验动手操作能力,发展学生的证据推理、科学探究与创新意识素养水平。
3.学有余力的学生初步了解葡萄糖的环状结构和糖类分子的手性,发展学生的证据推理、
科学探究与创新意识素养水平。
4.结合葡萄糖的组成、结构和性质,认识糖类在生产、生活中的重要应用,并能对有关饮
食、健康等实际问题进行分析、讨论和评价,发展学生的科学态度与社会责任素养水平。
重点:单糖的典型代表物葡萄糖的组成、结构、化学性质及应用。
教学
难点:从官能团的角度理解糖类与所学过的醛、酮、醇类物质的关系,用实验的方法、手
重、难
段和基于证据推理的思想认识它们之间的关系,初步掌握含多官能团有机物的性质的一般学习
点
过程。
证据推理与模型认知:了解糖类的组成与分类,单糖、二糖和多糖的区别与联系,培养学
生辨识记忆、分析解释、简单设计的学科能力,落实宏观辨识与微观探析、证据推理与模型认
知、科学探究与创新意识及科学态度与社会责任的学科核心素养。
宏观辨识与微观探析:在具备分析解释和简单设计的关键学科能力基础上,结合典型例题
核心素
的真实问题情境,考查葡萄糖中官能团和淀粉水解的知识,落实宏观辨识与微观探析、科学探
养
究与创新意识的学科核心素养。
概括关联与推论预测:在糖类的试题情境中,运用辨识记忆、说明论证及简单设计等综合
能力解决问题,培养宏观辨识与微观探析、科学探究与创新意识,并发展科学态度与社会责任
的学科核心素养。
学生在必修阶段的学习中,已经初步了解了糖类的组成和结构通式,通过实验展示认识了
葡萄糖的主要化学性质,还初步学习了二糖和多糖的水解及其产物。通过本册教材第三章对醇
学情分 和醛的学习,学生知道糖类是一种多官能团的有机化合物,具有羟基和醛基或酮羰基的化学性
析 质。学生已经具备了进一步学习糖类知识的基础。糖类与学生生活息息相关,社会上关于无糖
食品的新闻也层出不穷,本节课宜结合生活实际与社会热点问题授课,能够增加课堂的趣味性,
以及更好地落实核心素养。
教学过程
教学环
教学活动 设计意图
节
【导入】糖类是一类重要的有机化合物,在生命活动中起着重要作用,是生 以日常生活
物体所需能量的主要来源,是重要的能量储存物质,也是很多生物体的结构 中常见的一
成分。(PPT图片和视频展示) 些产品为例
引入新课,
【教师】播放PPT,引起学生对糖类的学习兴趣
吸引学生的
活动一、糖类的组成和分类 好奇心。
【任务一】糖类
【学生活动1】阅读教材P ,总结糖类的基本概念?
100
【学生】阅读教材,分组讨论与交流,小组代表回答
【教师】评价、强调,补充
总结:
1.组成:一般由碳、氢、氧三种元素组成,大多数糖符合通式C (H O) 又叫
m 2 n
碳水化合物。 教师知识讲
解,学生认
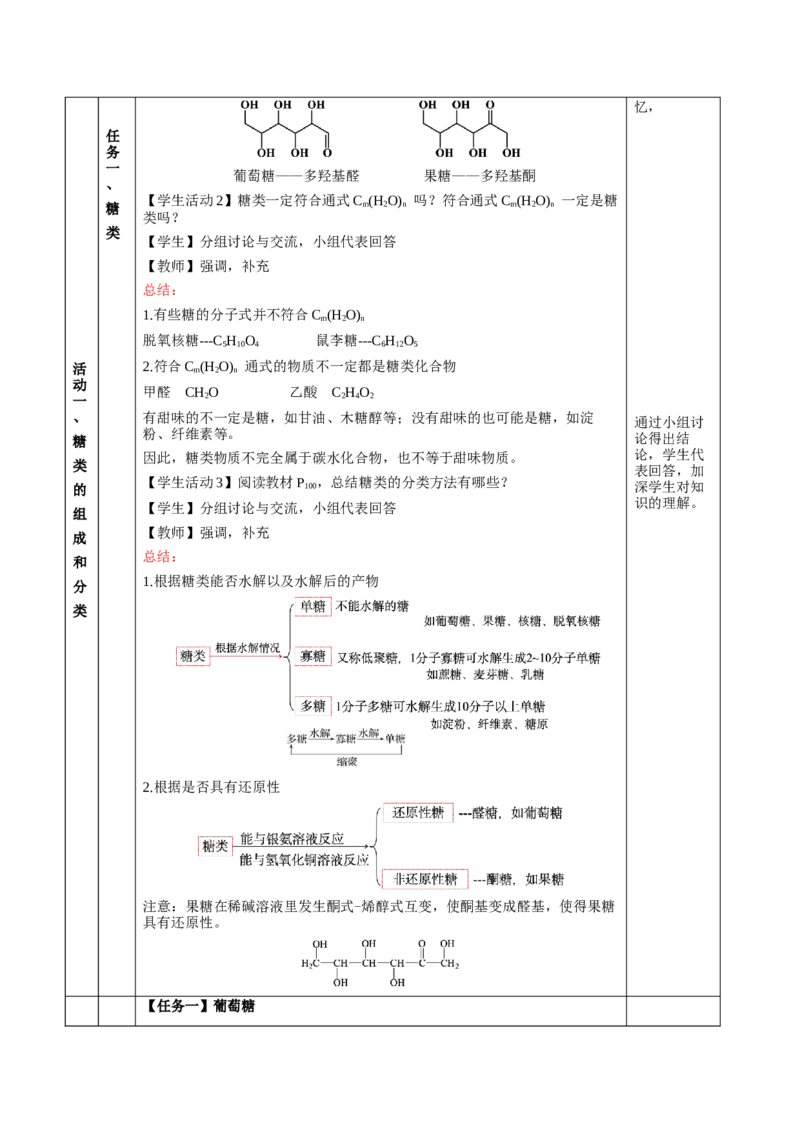
2.定义:从分子结构上看,糖类是多羟基醛、多羟基酮和它们的脱水缩合物。
真听讲并记忆,
任
务
一
葡萄糖——多羟基醛 果糖——多羟基酮
、
【学生活动2】糖类一定符合通式C (H O) 吗?符合通式C (H O) 一定是糖
糖 m 2 n m 2 n
类吗?
类
【学生】分组讨论与交流,小组代表回答
【教师】强调,补充
总结:
1.有些糖的分子式并不符合C (H O)
m 2 n
脱氧核糖---C H O 鼠李糖---C H O
5 10 4 6 12 5
活 2.符合C (H O) 通式的物质不一定都是糖类化合物
m 2 n
动
甲醛 CHO 乙酸 C HO
一 2 2 4 2
、 有甜味的不一定是糖,如甘油、木糖醇等;没有甜味的也可能是糖,如淀
通过小组讨
粉、纤维素等。
糖 论得出结
因此,糖类物质不完全属于碳水化合物,也不等于甜味物质。 论,学生代
类
表回答,加
的
【学生活动3】阅读教材P
100
,总结糖类的分类方法有哪些?
深学生对知
识的理解。
【学生】分组讨论与交流,小组代表回答
组
【教师】强调,补充
成
总结:
和
1.根据糖类能否水解以及水解后的产物
分
类
2.根据是否具有还原性
注意:果糖在稀碱溶液里发生酮式-烯醇式互变,使酮基变成醛基,使得果糖
具有还原性。
【任务一】葡萄糖【学生活动1】阅读教材P ,总结葡萄糖的基本概念?
101
任 【学生】阅读教材,小组代表回答
务
【教师】评价、强调,补充
一
总结:
、
1.存在:水果、蜂蜜,以及植物的种子、叶、根、花中;动物的血液和淋巴液
葡
中也含有葡萄糖。 培养学生总
萄
结归纳的能
糖 2.分子结构---多羟基醛:CHOH(CHOH) CHO
2 4 力。
3.物理性质:
易溶于水的无色晶体, 熔点146℃,有甜味,但甜度不如蔗糖。
【学生活动2】根据葡萄糖的结构预测其化学性质?
【学生】阅读教材,小组代表回答
【教师】评价、强调,补充
总结:1.醛基:
老师讲解,
(1)弱氧化剂氧化
学生认真听
(2)与高锰酸钾、溴水等强氧化剂反应 讲。
(3)还原反应(加成反应)
2.羟基:
(1)置换反应---与活泼金属反应
(2)氧化反应---醇羟基的氧化
(3)取代反应---酯化反应/与HX反应/分子间脱水
(4)消去反应
【学生活动3】阅读教材P 【实验4-1】探究葡萄糖的化学性质?
101
【学生】观看实验视频,推测其化学性质,小组代表回答
【教师】评价、强调,补充
总结:一、葡萄糖与新制的银氨溶液反应
观看实验,
然后总结归
纳。
老师讲解,
1.反应条件:水浴加热、碱性条件
学生认真听
2.应用: ①工业制镜或热水瓶胆镀银等 讲。
②医学用于检验尿糖
二、葡萄糖新制Cu(OH) 悬浊液反应
21.反应条件:加热煮沸、碱性条件
2.应用: 医学用于检验尿糖
结论:葡萄糖能被银氨溶液、新制Cu(OH) 悬浊液等弱氧化剂氧
2
化,表现出强的还原性,葡萄糖中含有醛基,是一种还原性糖。
活 三 、生物酶作用
动
二 通过小组讨
、 论得出结
单 a.葡萄糖易于被人体吸收,经酶的催化反生氧化反应放出热量,提供 论,学生代
糖 了维持生命活动所需要的能量。 表回答,加
任
深学生对知
氧务 b.低血糖的患者可利用静脉注射葡萄糖溶液的方式来迅速补充营养。 识的理解。
二
、 【知识扩展】阅读教材P 资料卡片葡萄糖的环状结构,链状葡萄糖转化为环
102
果 状葡萄糖的反应属于什么反应类型?
糖
总结:
环化反应:是可逆的。
任务二、果糖 循序渐进的
推进课程,
【学生活动1】阅读教材P ,总结果糖的基本概念?
102 根据学生的
【学生】阅读教材,小组代表回答 掌握情况,
可作相应调
【教师】评价、强调,补充
整。
总结:1.存在:果糖于水果和蜂蜜中含量较高,它比蔗糖的甜度高。
2.分子结构---多羟基酮:CHOH(CHOH) COCH OH
2 3 2
3.物理性质:
纯净的果糖为无色晶体,易溶于水,乙醇和乙醚,吸湿性强,熔点
103~105℃,最甜的糖。
【学生活动2】阅读教材P ,总结果糖的化学性质和用途?
102
【学生】阅读教材,小组代表回答
【教师】评价、强调,补充
通过小组讨
任 1.化学性质:果糖分子中含有酮羰基和醇羟基,同样具有酮和醇的性质。碱性
论得出结
务 条件下,果糖会发生异构化反应生成葡萄糖---还原性糖
三 加深学生对
2.用途:广泛用于食品和医药的生成中。
知识的理
、
解,培养学
任务三、核糖和脱氧核糖
核 生总结归纳
糖 【学生活动1】阅读教材P 102 ,总结核糖和脱氧核糖的基础知识? 的能力。
和 【学生】阅读教材,小组代表回答
脱
【教师】评价、强调,补充
氧
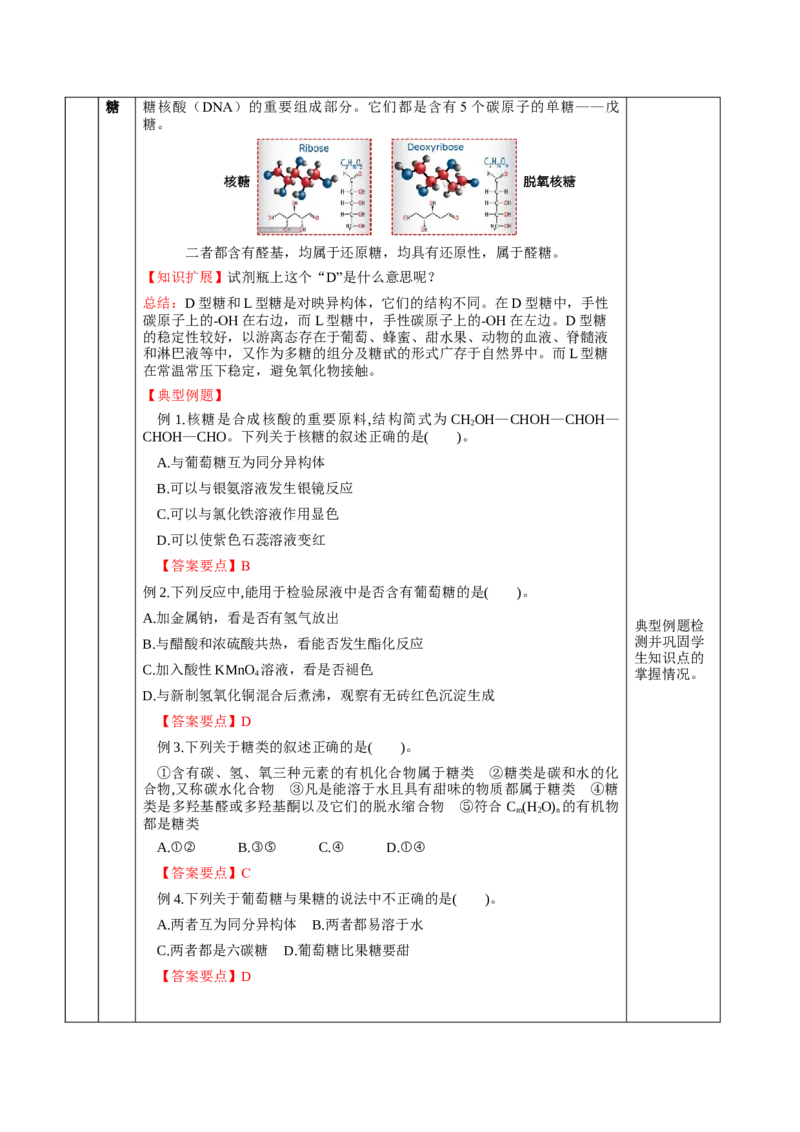
核 核糖与脱氧核糖分别是生物体的遗传物质核糖核酸(RNA)与脱氧核糖 糖核酸(DNA)的重要组成部分。它们都是含有5个碳原子的单糖——戊
糖。
二者都含有醛基,均属于还原糖,均具有还原性,属于醛糖。
【知识扩展】试剂瓶上这个“D”是什么意思呢?
总结:D型糖和L型糖是对映异构体,它们的结构不同。在D型糖中,手性
碳原子上的-OH在右边,而L型糖中,手性碳原子上的-OH在左边。D型糖
的稳定性较好,以游离态存在于葡萄、蜂蜜、甜水果、动物的血液、脊髓液
和淋巴液等中,又作为多糖的组分及糖甙的形式广存于自然界中。而L型糖
在常温常压下稳定,避免氧化物接触。
【典型例题】
例1.核糖是合成核酸的重要原料,结构简式为CHOH—CHOH—CHOH—
2
CHOH—CHO。下列关于核糖的叙述正确的是( )。
A.与葡萄糖互为同分异构体
B.可以与银氨溶液发生银镜反应
C.可以与氯化铁溶液作用显色
D.可以使紫色石蕊溶液变红
【答案要点】B
例2.下列反应中,能用于检验尿液中是否含有葡萄糖的是( )。
A.加金属钠,看是否有氢气放出
典型例题检
B.与醋酸和浓硫酸共热,看能否发生酯化反应 测并巩固学
生知识点的
C.加入酸性KMnO
4
溶液,看是否褪色
掌握情况。
D.与新制氢氧化铜混合后煮沸,观察有无砖红色沉淀生成
【答案要点】D
例3.下列关于糖类的叙述正确的是( )。
①含有碳、氢、氧三种元素的有机化合物属于糖类 ②糖类是碳和水的化
合物,又称碳水化合物 ③凡是能溶于水且具有甜味的物质都属于糖类 ④糖
类是多羟基醛或多羟基酮以及它们的脱水缩合物 ⑤符合 C (H O) 的有机物
m 2 n
都是糖类
A.①② B.③⑤ C.④ D.①④
【答案要点】C
例4.下列关于葡萄糖与果糖的说法中不正确的是( )。
A.两者互为同分异构体 B.两者都易溶于水
C.两者都是六碳糖 D.葡萄糖比果糖要甜
【答案要点】D课堂总
结
4.1.1糖类的组成和分类
一、糖的分类
1.单糖:不能水解的糖
板书
常见单糖有葡萄糖、果糖、核糖、脱氧核糖
设计
2.寡糖:能水解为2-10分子的糖
常见的有二糖,如蔗糖、麦芽糖等
3.多糖:能水解为十个以上的单糖的糖
常见多糖有纤维素、淀粉等
二、葡萄糖的结构与性质
1.官能团:羟基、醛基
2.与氢氧化铜悬浊液的反应:
3.与银氨溶液反应:
三、果糖、核糖与脱氧核糖
1.各自的结构式
本节课通过设置四个教学环节,引发学生主动思考、发现问题;通过分组实验,学生在动手
中完成对新知的学习;通过小组讨论,层层递进解决新知中的疑难问题;通过设计实验,进一步加
深学生对葡萄糖检验的理解;在[作业设计]环节,通过撰写报告,激发学生拓展思维,多方位认识
糖类在生产、生活中的要应用,关注糖类对能源、饮食、健康等实际问题的影响。教学设计
教学
充分发挥了学生的主体性,努力实现了情境、问题、思维的有效统一,提升了学生学习知识并
反思 运用知识解决实际问题的能力。教学过程中也发现个别小组的学生实验目的不够清晰、实验
操作有待规范、小组分工合作协同性有待提高等情况,需要教具有一定的预判预估能力,并有
针对性地进行指导,以促进学生学习能力的提升和核心素养发展。