文档内容
4.1.2 原子结构与元素的性质
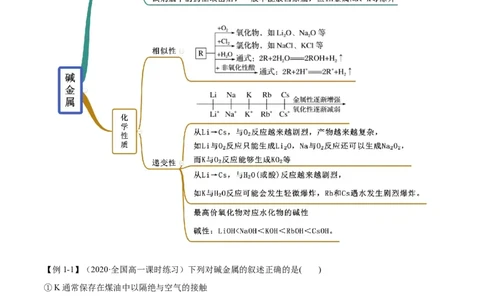
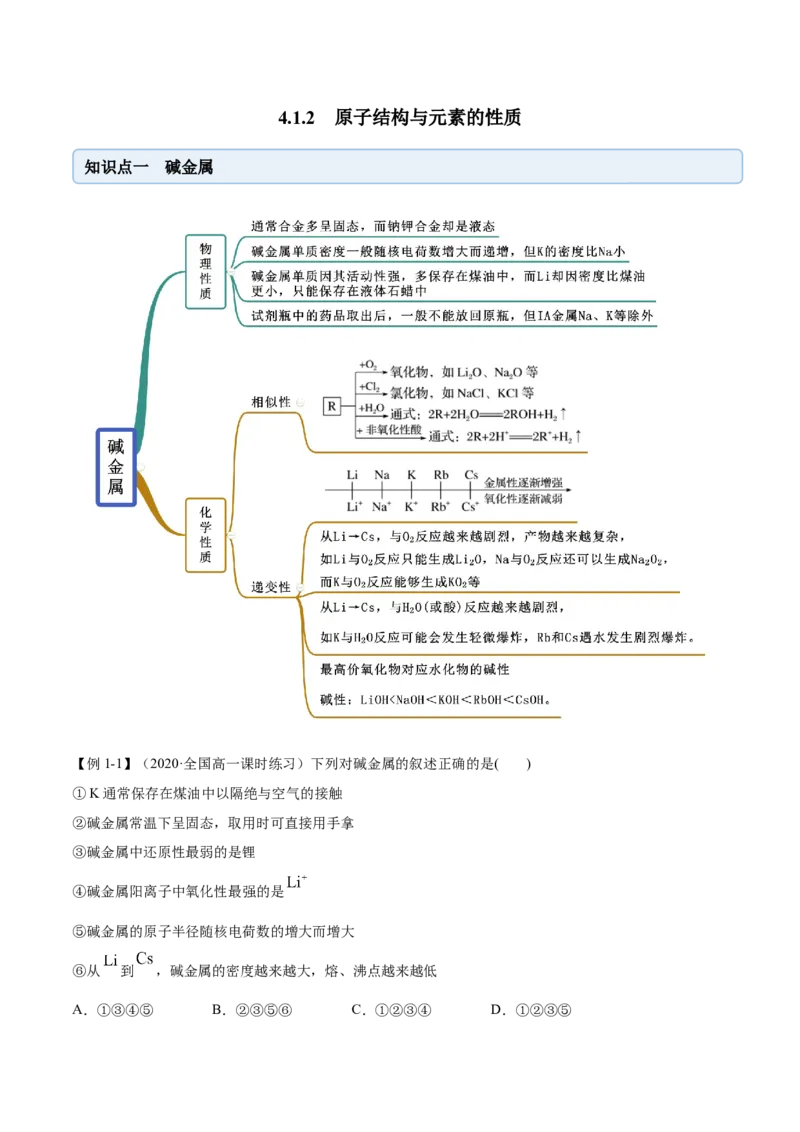
知识点一 碱金属
【例1-1】(2020·全国高一课时练习)下列对碱金属的叙述正确的是( )
①K通常保存在煤油中以隔绝与空气的接触
②碱金属常温下呈固态,取用时可直接用手拿
③碱金属中还原性最弱的是锂
④碱金属阳离子中氧化性最强的是
⑤碱金属的原子半径随核电荷数的增大而增大
⑥从 到 ,碱金属的密度越来越大,熔、沸点越来越低
A.①③④⑤ B.②③⑤⑥ C.①②③④ D.①②③⑤【例1-2】(2020·全国高一课时练习)2019年诺贝尔化学奖颁给几位在锂离子电池研发领域作出突出贡献
的科学家。已知锂单质的化学性质与钠类似,但活泼性比钠略差,其密度为 ,锂元素的焰
色反应呈紫红色。将绿豆大的锂投入水中,下列实验现象合理的有( )
①锂沉入水中
②锂浮在水面上
③水中没有气泡产生
④在反应后的溶液中加入几滴石蕊试液,溶液变红色
⑤反应剧烈,发出紫红色火焰
⑥锂四处游动
A.②⑥ B.①③ C.②③⑤ D.②④⑤⑥
【一隅三反】
1.(2020·全国高一课时练习)以下关于锂、钠、钾、铷、铯的叙述不正确的是( )
① 氢氧化物中碱性最强的是CsOH
② 单质熔点最高的是铯
③ 它们的密度依次增大
④ 其单质的还原性依次增强
⑤ 它们对应离子的氧化性依次增强
⑥ 单质与水反应的剧烈程度依次增加
⑦ 单质与相同浓度、相同体积的盐酸反应的剧烈程度依次增加
A.① ⑤ ⑦ B.② ⑥
C.② ③ ⑤ D.② ③ ④
2.(2020·河北涿鹿中学高一月考)以下关于锂、钠、钾、铷、铯的叙述正确的是( )
①氢氧化物中碱性最强的是CsOH ②单质熔点最高的是铯 ③它们都是热和电的良导体 ④它们的密度
依次增大,且都比水轻 ⑤它们的还原性依次增强 ⑥它们对应阳离子的氧化性依次增强
A.①③ B.②⑤ C.②④⑥ D.①③⑤
3.(2020·自贡市田家炳中学高一期中)关于碱金属的叙述正确的是
A.随核电荷数的增加,碱金属单质与水反应的剧烈程度增大
B.随核电荷数的增加,碱金属单质熔、沸点升高
C.随核电荷数的减小,碱金属原子的还原性增强D.随核电荷数的减小,碱金属单质的密度增大
4.(2020·全国高一课时练习)下列关于碱金属元素的说法正确的是( )
A.碱金属元素中,锂原子失去电子的能力最强
B.碱金属单质可将铜从其盐溶液中置换出来
C.金属钾具有强还原性, 具有强氧化性
D.常温下Cs与水反应会发生爆炸
5.(2019·全国高一课时练习)2019年诺贝尔化学奖颁给几位在锂离子电池研发领域做出贡献的科学家,
锂单质化学性质与钠类似,活泼性比钠略弱。它的密度为0.534g/cm3,锂元素的焰色为紫红色,将绿豆大
的锂投入水中,下列实验现象合理的有( )
①锂沉入水中
②锂浮在水面上
③水中有大量气泡
④ 反应后在水中加入几滴石蕊试液,溶液变红
⑤反应剧烈,发出紫红色火焰
⑥锂四处游动
A.②③ B.①③
C.②③⑤ D.②④⑤⑥
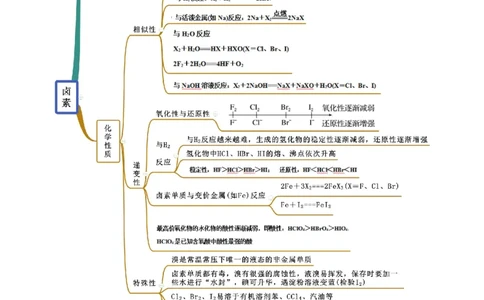
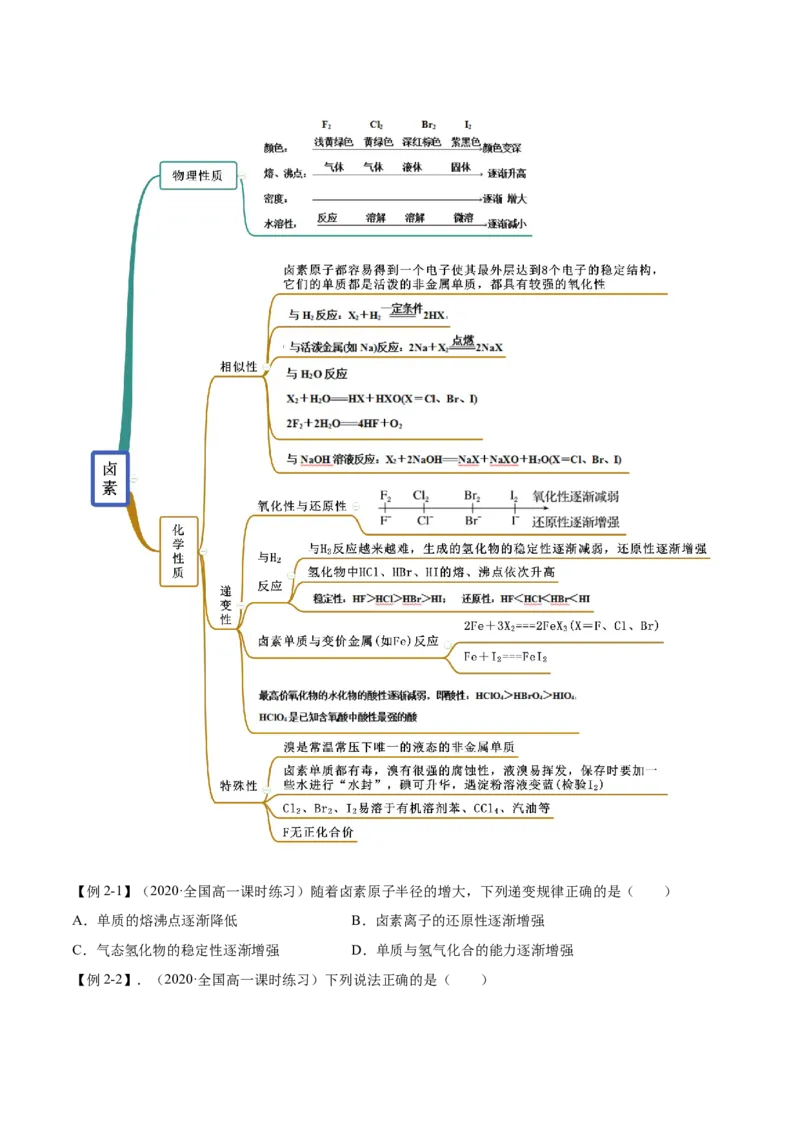
知识点二 卤素【例2-1】(2020·全国高一课时练习)随着卤素原子半径的增大,下列递变规律正确的是( )
A.单质的熔沸点逐渐降低 B.卤素离子的还原性逐渐增强
C.气态氢化物的稳定性逐渐增强 D.单质与氢气化合的能力逐渐增强
【例2-2】.(2020·全国高一课时练习)下列说法正确的是( )A.还原性:
B.热稳定性:
C.向少量KI溶液中滴入足量溴水,振荡后再加入 ,则静置后有机层呈橙红色
D.密度:
【一隅三反】
1.(2020·全国高一课时练习)氯、溴、碘单质的化学性质相似,原因是
A.均为有色单质 B.均为双原子分子
C.原子最外层电子数均为7 D.均可从海洋中提取
2.(2020·呼和浩特开来中学高一期末)在含有NaBr和NaI的溶液中通入足量的 ,然后把溶液蒸干并
将剩余残渣灼烧,最后留下的物质是
A.NaCl和NaBr的混合物 B.NaCl和
C.NaCl D.NaCl、 和
3.(2020·全国高一课时练习)向 溶液中滴加少量溴水,溶液变为黄色。下列说法正确的是
A.由于所得溶液中存在 ,所以溶液变为黄色
B.向所得溶液中加入硫氰化钾溶液,可判断是否生成了
C.向所得溶液中加入氢氧化钾溶液,不能判断是否生成了
D.向所得溶液中加入淀粉 溶液,不能判断是否生成了
4.(2020·上海静安)向NaBr、NaI、NaSO 的混合溶液中,通入一定量的氯气后,将溶液蒸干并充分灼
2 3
烧,得到固体物质中一定有
A.NaCl、NaSO B.NaCl、NaBr、NaSO
2 4 2 4
C.NaCl、NaSO 、I D.NaCl、NaI、NaSO
2 4 2 2 4
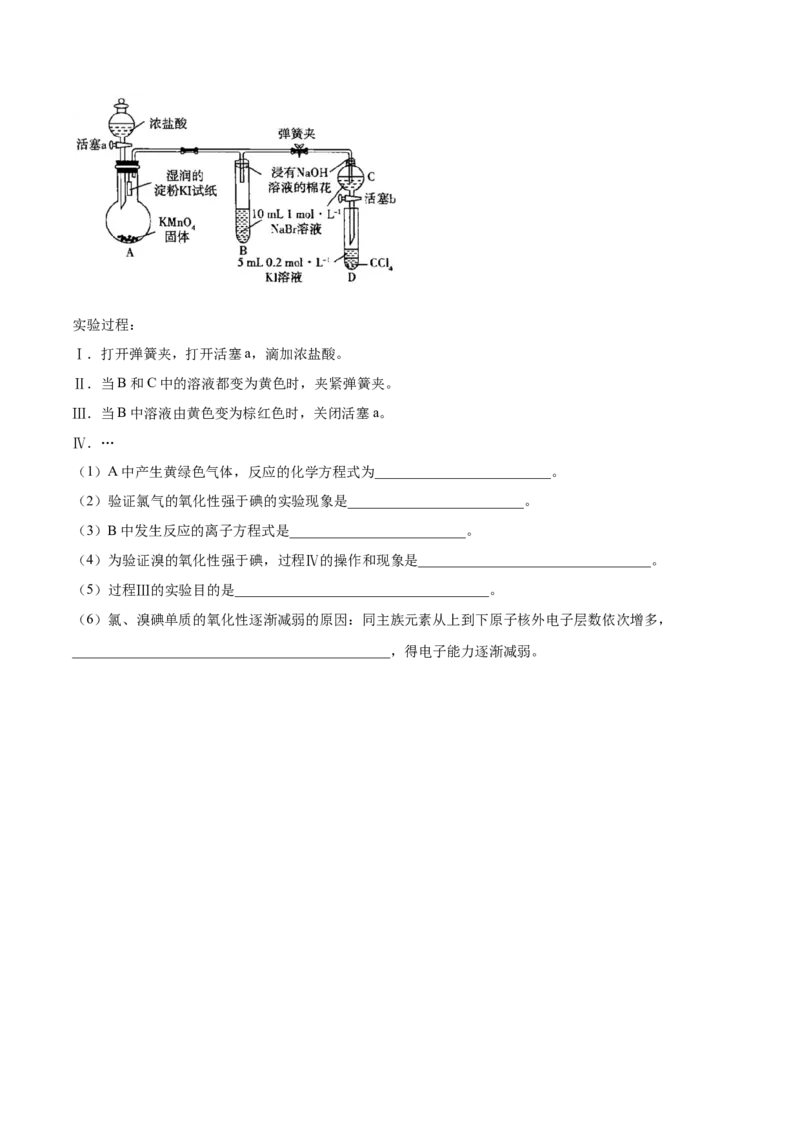
5.(2020·全国高一课时练习)为验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹
持装置已略去,装置气密性已检验)。实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.…
(1)A中产生黄绿色气体,反应的化学方程式为_________________________。
(2)验证氯气的氧化性强于碘的实验现象是_________________________。
(3)B中发生反应的离子方程式是_________________________。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是_________________________________。
(5)过程Ⅲ的实验目的是____________________________________。
(6)氯、溴碘单质的氧化性逐渐减弱的原因:同主族元素从上到下原子核外电子层数依次增多,
_____________________________________________,得电子能力逐渐减弱。