文档内容
4.1.2 原子结构与元素的性质
【题组一 碱金属】
1.(2020·全国高一课时练习)下列各项中的叙述I和叙述II都正确,但叙述II不能用于对叙述I进行解释
的是( )
选项 叙述I 叙述II
A 金属钠和钾都容易用小刀切开 钠和钾的硬度都较小
B 金属钠和钾都可用煤油密封保存 钠和钾都不与煤油反应,且密度都比煤油的大
金属钠和钾分别在空气中燃烧,钾的反应相对较
C 钾的金属性比钠的强
快
D 金属钠和钾分别与水反应,钾的反应相对较快 钾的密度比钠的小
【答案】D
【解析】A. 金属钠和钾都容易用小刀切开,钠和钾的硬度都较小,A项正确;
B. 金属钠和钾都可用煤油密封保存,钠和钾都不与煤油反应,且密度都比煤油的大,B项正确;
C. 金属钠和钾分别在空气中燃烧,钾的反应相对较快,钾的金属性比钠的强,C项正确;
D. 金属钠和钾分别与水反应,钾反应相对较快的原因是钾的金属性比钠的强,或者说钾原子比钠原子更
易失去电子,D项错误;
答案选D。
2.(2020·全国高一课时练习)可能存在的第119号未知元素,有人称为“类钫”,它位于碱金属族,根
据元素周期表结构及元素性质变化趋势,下列关于碱金属某些元素原子结构和性质的判断,错误的是(
)
①锂与水反应比钠剧烈 ②金属单质都可以密封保存在煤油中
③锂的氧化物暴露在空气中易吸收二氧化碳 ④锂的阳离子的最外层电子数和钠的相同
⑤“类钫”单质是强还原剂 ⑥“类钫”在化合物中显+1价
⑦推测“类钫”单质的密度应该大于 ⑧“类钫”单质有较高的熔点
A.①②④⑧ B.①②③⑦ C.③④⑤⑧ D.①③④⑥
【答案】A
【解析】①金属性: ,元素的金属性越强,对应的单质与水反应越剧烈,则钠与水反应比锂与水
反应剧烈,①错误;②锂的密度小于煤油的密度,若用煤油保存锂,则达不到隔绝空气和水的目的,②错误;
③锂的氧化物( )是碱性氧化物,在空气中易吸收二氧化碳,生成碳酸锂,③正确;
④原子失去最外层电子后,次外层变成最外层,故锂离子最外层有2个电子,钠离子最外层有8个电子,
二者数目不等,④错误;
⑤“类钫”属于碱金属,碱金属单质都具有强还原性,可作强还原剂,⑤正确;
⑥碱金属元素原子最外层都只有1个电子,在反应中容易失去这个电子显+1价,⑥正确;
⑦碱金属单质的密度从上到下逐渐增大(K反常),推测“类钫”单质的密度应该大于钫的,密度大于
,⑦正确;
⑧碱金属单质的熔点较低且从上到下熔点逐渐降低,所以“类钫”单质的熔点很低,⑧错误。
故选A。
3.(2020·全国高一课时练习)下列关于碱金属的性质叙述正确的是( )
A.单质均为银白色,密度均小于水 B.单质与水反应时都能生成碱和氢气
C.单质在空气中燃烧的生成物都是过氧化物D.单质的还原性逐渐减弱
【答案】B
【解析】A.Cs略带金色光泽,Li、Na、K的密度小于水的密度,Rb、Cs的密度大于水的密度,故A错
误;
B.碱金属单质都能与水反应,生成相应的碱和 ,故B正确;
C.随着核电荷数的增大,碱金属越来越活泼,碱金属单质在空气中燃烧的产物越来越复杂,Li在空气中
燃烧的主要产物为 ,且为氧化物,故C错误;
D.从Li到Cs,单质的还原性逐渐增强,故D错误。
故选B。
4.(2020·全国高一课时练习)下列说法不正确的是( )
A.碱金属元素在自然界中以化合态形式存在
B.金属铷投入水中会发生爆炸式反应,生成氢氧化物和氢气
C.碱金属与氧气反应,生成物都不随反应条件或反应物的用量变化而变化
D.金属铯的密度大于钠,而钠的熔点高于铯
【答案】C
【解析】A.碱金属元素在自然界中均以化合态形式存在,A正确;B.金属铷的金属性很强,因此金属铷投入水中会发生爆炸式反应,生成氢氧化物和氢气,B正确;
C.除锂之外的碱金属与氧气反应,生成物都随反应条件的变化而变化,C错误;
D.碱金属从锂到铯,密度呈增大趋势,熔沸点依次降低,故金属铯的密度大于钠,而钠的熔点高于铯,D
正确;故答案为:C。
5.(2020·全国高一课时练习)以下关于锂、钠、钾、铷、铯的叙述不正确的是( )
①对应的氢氧化物中,碱性最强的是
②单质熔点最高的是铯
③与 反应均可得到多种氧化物
④单质的密度依次增大
⑤单质的还原性依次增强
⑥对应阳离子的氧化性依次增强
A.①③⑤ B.②④⑥ C.②③④⑥ D.①⑤
【答案】C
【解析】①元素的金属性越强,其最高价氧化物对应水化物的碱性越强,由于金属性最强的元素是Cs,所
以对应的氢氧化物中碱性最强的是CsOH,①正确;
②碱金属单质的熔、沸点随着原子序数的增加而降低,所以单质熔点最低的是铯,②错误;
③Li与O 反应只能得到LiO,③错误;
2 2
④碱金属单质的密度随着原子序数的增加而增大,但K例外,K的密度小于Na,④错误;
⑤碱金属元素随原子序数的增加,原子半径逐渐增大,失电子能力增强,所以其单质的还原性依次增强,
⑤正确;
⑥由于碱金属元素的原子半径逐渐增大,原子核吸引电子的能力逐渐减弱,失电子能力增强,所以它们对
应阳离子的氧化性依次减弱,⑥错误。
故叙述②③④⑥不正确,故答案为:C。
6.(2020·全国高一课时练习)钫( )是一种具有放射性的元素,原子序数为87,其原子最外层电子
数是1。下列有关 元素的说法不正确的是( )
A. 是第六周期第Ⅰ 族元素 B. 的原子核外有87个电子
C. 在化合物中一般显 价 D.其阳离子半径小于原子半径
【答案】A【解析】A. 的原子序数为 ,为第七周期第Ⅰ 族元素,其原子最外层电子数是1,A错误;
B.原子中,质子数=核外电子数=原子序数,则 的原子核外有87个电子,B正确;
C. 原子的最外层电子数为1,在化学反应中易失去最外层的1个电子,故形成化合物时一般显 价,
C正确;
D.同一种元素的阳离子由于失去最外层电子,故其半径小于其原子半径,D正确;
故答案为:A。
7.(2020·全国高一课时练习)下列说法错误的是( )
A.锂在空气中燃烧只会生成氧化锂
B.锂很软,用小刀可以切割
C.锂的熔点比铯的高
D.锂可以保存在煤油或液体石蜡中
【答案】D
【解析】A. 锂较其他碱金属活泼性差,在氧气中燃烧只生成氧化锂,故A正确;
B. 碱金属都很软,均可用小刀切割,故B正确;
C. 碱金属从 熔点逐渐降低,故C正确;
D. 金属锂的密度比煤油的小,所以不能保存在煤油中,故D错误。
综上所述,答案为D。
【题组二 卤素】
1.(2020·全国高一课时练习)下列叙述正确的有( )
①卤素原子的最外层均有7个电子,次外层均有8个电子
②Li、Na、K的原子半径和密度随原子序数的增加而增大
③碱金属元素和卤素在自然界中都只以化合态形式存在
④液溴易挥发,在存放液溴的试剂瓶中应加水液封
⑤如图所示,若a、b、c中分别盛放浓盐酸、 固体、淀粉KI溶液,则通过实验可证明氧化性:A.5句 B.4句 C.3句 D.2句
【答案】C
【解析】①F原子次外层是2个电子,故①错误;②K单质的密度反常,比Na的小,故②错误;③碱金
属元素和卤素分别是活泼的金属元素和非金属元素,易与多种物质发生反应,在自然界中没有游离态,故
③正确;④液溴易挥发,存放液溴需加水液封,故④正确;⑤
和 ,根据氧化剂的氧化
性强于氧化产物的氧化性,氧化性: ,故⑤正确,因此共有3句正确,故C正确。
综上所述,答案为C。
2.(2020·浙江)钾、铷、铯在过量的氧气中燃烧均生成黄色的超氧化物(如KO )。 下列说法不正确的是
2
( )
A.在450℃ 、15MPa 的压力下, Na 与 O 反应也能够得纯净的 NaO ,常温下NaO 的稳定性比 NaO
2 2 2 2 2
好
B.CsO 具有强氧化性,能与水反应生成O,其中水作还原剂
2 2
C.4KO +2CO = 2K CO+3O ,因此可用来作氧气源
2 2 2 3 2
D.KO 与水反应后的溶液呈强碱性
2
【答案】B
【解析】A.钠在空气中燃烧生成NaO,在高温下才能得纯净的 NaO ,可见常温下NaO 比NaO 稳定,
2 2 2 2 2 2
故A正确;
B.CsO 具有强氧化性,能与水反应生成O,其中CsO 既是氧化剂,又是还原剂,而水既不是氧化剂,又
2 2 2
不是还原剂,故B错误;
C.由4KO +2CO = 2K CO+3O 可知,可利用KO 作供氧剂,故C正确;
2 2 2 3 2 2
D.KO 与水反应生成KOH和O,所得溶液呈强碱性,故D正确;
2 2
故答案为B。
3.(2019·上海宝山·)甲、乙、丙三种溶液中各含有Cl-、Br-、I-中的一种卤素离子,向甲溶液中加入淀粉
溶液和氯水,变成橙色,再加入乙溶液,溶液颜色没有明显变化。则甲、乙、丙三种溶液分别含有的离子是( )
A.Cl-、Br-、I- B.Br-、Cl-、I- C.Br-、I-、Cl- D.I-、Br-、Cl-
【答案】B
【解析】向甲中加淀粉溶液和氯水,溶液变为橙色,发生Cl+2Br-=Br +2Cl-,则甲中含有溴离子;再加入
2 2
乙溶液,颜色无明显变化,因氯气能氧化碘离子,则乙中不含碘离子,即乙中含氯离子;甲、乙、丙三种
溶液各含有一种离子,则丙中含碘离子,所以甲、乙、丙依次含有Br-、Cl-、I-,故选B。
4.(2020·上海外国语大学附属宏达高级中学月考)下列物质能使湿润的淀粉碘化钾试纸变蓝色的是
A.HO B.Cl C.NH D.HCl
2 2 3
【答案】B
【解析】能使湿润的淀粉碘化钾试纸变蓝色,说明该气体能氧化KI生成碘单质,碘单质才能使淀粉变蓝,
则该气体具有氧化性,则气体是Cl,HO、NH 、HCl均不能氧化KI,故答案选B。
2 2 3
5.(2020·福建省晋江市养正中学高一月考)向 、 、 混合液中,通入一定量氯气后,将
溶液蒸干并充分灼烧,得到固体剩余物质的组成不可能是
A. B.
C. 、 、 D.
【答案】D
【解析】Br−、I−的还原性由弱到强为Br−<I−,向含有NaCl、NaBr、NaI的混合溶液中通入一定量氯气发生:
2NaI+Cl=2NaCl+I、2NaBr+Cl=2NaCl+Br ,Br 易挥发、I 易升华,
2 2 2 2 2 2
A.当氯气过量时,发生反应2NaI+Cl=2NaCl+I、2NaBr+Cl=2NaCl+Br ,加热过程中,Br 易挥发、
2 2 2 2 2
I 易升华,最后剩余固体是NaCl,故A不选;
2
B.当氯气少量时,发生反应2NaI+Cl=2NaCl+I,部分2NaBr+Cl=2NaCl+Br 反应,加热过程中,碘
2 2 2 2
升华,所以固体是NaCl、NaBr,故B不选;
C.当氯气少量时,只发生部分2NaI+Cl=2NaCl+I 反应,加热过程中,碘升华,所以固体是NaCl、
2 2
NaBr、NaI,故C不选;
D.当加入氯气,氯气先和碘离子反应,后和溴离子反应,所以固体是中不可能是NaCl、NaI,故D选;
故答案选D。
6.(2020·全国高一单元测试)下列能够检验出KI中是否含有Br-的实验是( )
A.加入足量的新制氯水,溶液变色则有Br-
B.加入酸性KMnO 溶液,观察溶液颜色是否褪去
4C.加入少量的碘水,再加入CCl 振荡,有机层有色,则有Br-
4
D.加入足量FeCl 溶液,用CCl 萃取后,取无色的水层并加入AgNO 溶液,有淡黄色沉淀生成,则含有
3 4 3
Br-
【答案】D
【解析】A. 加入足量的新制氯水,Br-、I-都能被Cl 氧化生成溴和碘,溶于水都有颜色,所以溶液变色不
2
能证明有Br-存在,A不正确;
B. 加入酸性KMnO 溶液,能将Br-、I-氧化,溴水、碘水都有颜色,不能观察溶液颜色褪去,B不正确;
4
C. 碘水与Br-不反应,有机层有色是因为碘溶于四氯化碳,实验现象与Br-无关,C不正确;
D. 加入足量FeCl 溶液,将I-全部氧化为I,用CCl 萃取后,取无色的水层并加入AgNO 溶液,有淡黄色
3 2 4 3
沉淀生成,证明生成了AgBr,从而证明含有Br-,D正确。
故选D。
7.(2020·广东天河·华南师大附中高三专题练习)下列关于物质的保存不正确的是
A.漂白粉可露置于空气中保存 B.金属钠应用煤油液封
C.液溴应用水封存 D.AgI、AgBr应保存在棕色瓶中
【答案】A
【解析】A.漂白粉中的次氯酸钙能与空气中的二氧化碳反应,生成碳酸钙和次氯酸,次氯酸见光易分解,
从而使漂白粉失效,故漂白粉需密闭保存,故A符合题意;
B.钠能分别与水和氧气等反应,钠的密度比水的小比煤油的大,所以少量的金属钠应保存在煤油中,隔
绝空气,故B不符合题意;
C.液溴易挥发、密度大于水,在水中溶解度较小,所以少量的液溴通常保存在棕色的玻璃瓶中,并采用
水封,故C不符合题意;
D.AgI、AgBr见光易分解,保存时应避光,用棕色瓶保存,故D不符合题意。
故答案选A。
8.下列物质与其用途相符合的是( )
①Cl-做消毒剂 ②AgBr-制胶卷,感光纸 ③AgI-人工降雨 ④加碘食盐-预防甲状腺肿大⑤淀粉-检验I
2 2
的存在 ⑥NaClO-漂白纺织物 ⑦Na-K合金--快中子反应堆导热剂
A.②③④⑤⑥ B.①②③④⑤ C.②③④⑤⑦ D.全部
【答案】D
【解析】①Cl 能与水反应生成次氯酸,次氯酸可作消毒剂,用于杀菌消毒,故①正确;
2
②AgBr不稳定,易分解生成银,可用来制胶卷、感光纸,故②正确;
③AgI易与空气中水蒸气结合形成晶核,有利水汽粒子的碰撞增大,从而形成雨,故③正确;④碘元素是预防甲状腺肿大的主要元素,故④正确;
⑤淀粉遇碘单质变蓝色,可用来检验碘单质,故⑤正确;
⑥NaClO与二氧化碳、水反应生成次氯酸,次氯酸具有强氧化性,可用于漂白纺织物,故⑥正确;
⑦根据钠钾合金熔点低,可作为冷却剂应用于实验室的快中子反应器中的导热剂,故⑦正确;
故选:D。
9.(2019·师宗县第二中学高一期末)下列说法正确的是( )
A.碘易升华,可保存在酒精中
B.液溴应保存在棕色磨口玻璃塞的试剂瓶中,并加少量水进行水封
C.新制的氯水可长期保存在无色玻璃瓶中
D.碘易溶于酒精,所以可用酒精从碘水中萃取碘
【答案】B
【解析】A.碘溶于酒精,得到是酒精溶液,故A错误;
B.液溴易挥发应保存在棕色磨口玻璃塞的试剂瓶中,并加少量水进行水封,故B正确;
C.新制氯水中的次氯酸见光容易分解,不能保存在无色玻璃瓶中,应该盛放在棕色瓶中,故C错误;
D.萃取利用物质在互不相溶的溶剂中溶解度不同进行分离的方法,酒精是和水互溶不能分层,不能萃取
分离,故D错误;
故选B。
10.在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。所用仪器如下图:
(1)连接上述仪器的正确顺序(填各接口处的字母):__________接__________;__________接
__________;__________接__________;__________接__________。
(2)饱和食盐水的作用是吸收__________;NaOH溶液的作用是__________。
(3)写出该气体发生装置中化学方程式:____________________。
(4)如果将过量二氧化锰与20mL 12 mol·L-1盐酸混合加热,充分反应后生成的氯气明显少于0.06mol其主
要原因有:①____________________;②____________________。
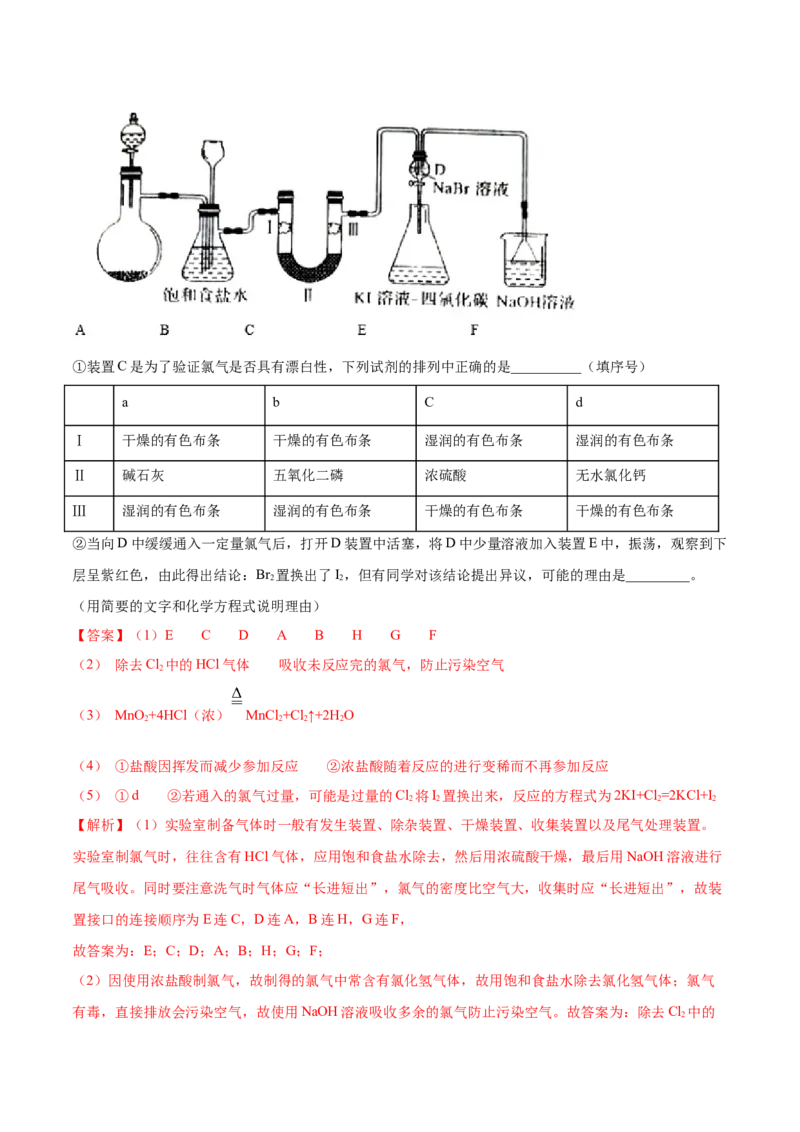
(5)某兴趣小组的同学拟采用以下装置(夹持及加热仪器已略)来探究氯、溴、碘的相关性质。请回答:①装置C是为了验证氯气是否具有漂白性,下列试剂的排列中正确的是__________(填序号)
a b C d
Ⅰ 干燥的有色布条 干燥的有色布条 湿润的有色布条 湿润的有色布条
Ⅱ 碱石灰 五氧化二磷 浓硫酸 无水氯化钙
Ⅲ 湿润的有色布条 湿润的有色布条 干燥的有色布条 干燥的有色布条
②当向D中缓缓通入一定量氯气后,打开D装置中活塞,将D中少量溶液加入装置E中,振荡,观察到下
层呈紫红色,由此得出结论:Br 置换出了I,但有同学对该结论提出异议,可能的理由是_________。
2 2
(用简要的文字和化学方程式说明理由)
【答案】(1)E C D A B H G F
(2) 除去Cl 中的HCl气体 吸收未反应完的氯气,防止污染空气
2
(3) MnO +4HCl(浓) MnCl +Cl↑+2H O
2 2 2 2
(4) ①盐酸因挥发而减少参加反应 ②浓盐酸随着反应的进行变稀而不再参加反应
(5) ①d ②若通入的氯气过量,可能是过量的Cl 将I 置换出来,反应的方程式为2KI+Cl =2KCl+I
2 2 2 2
【解析】(1)实验室制备气体时一般有发生装置、除杂装置、干燥装置、收集装置以及尾气处理装置。
实验室制氯气时,往往含有HCl气体,应用饱和食盐水除去,然后用浓硫酸干燥,最后用NaOH溶液进行
尾气吸收。同时要注意洗气时气体应“长进短出”,氯气的密度比空气大,收集时应“长进短出”,故装
置接口的连接顺序为E连C,D连A,B连H,G连F,
故答案为:E;C;D;A;B;H;G;F;
(2)因使用浓盐酸制氯气,故制得的氯气中常含有氯化氢气体,故用饱和食盐水除去氯化氢气体;氯气
有毒,直接排放会污染空气,故使用NaOH溶液吸收多余的氯气防止污染空气。故答案为:除去Cl 中的
2HCl气体;吸收未反应完的氯气,防止污染空气;
(3)二氧化锰跟浓盐酸反应制氯气的产物还有二氯化锰和水,反应方程式为MnO +4HCl(浓)
2
MnCl +Cl↑+2H O,故答案为:MnO +4HCl(浓) MnCl +Cl↑+2H O;
2 2 2 2 2 2 2
(4)浓盐酸具有挥发性,加热的条件下挥发程度增大,是使制得的氯气减少的原因之一;随着反应的进
行,盐酸溶质不断被消耗,浓盐酸逐渐变稀,变为稀盐酸时反应停止,这也是使制得的氯气减少的原因之
一;故答案为:①盐酸因挥发而减少参加反应;②浓盐酸随着反应的进行变稀而不再参加反应;
(5)①要验证氯气是否具有漂白性,应将干燥的氯气通过干燥的有色布条,故Ⅲ处应放置干燥的有色布
条。U形管中应盛放固体干燥剂,要与Ⅲ形成对比实验,Ⅰ处应放置湿润的有色布条,故选d,故答案为:
d;
②通过现象I 被置换出来,可能是过量的氯气将I 置换出来的,不能确定是溴置换出的碘,反应的方程式
2 2
为2KI+Cl =2KCl+I ,故答案为:若通入的氯气过量,可能是过量的Cl 将I 置换出来,反应的方程式为
2 2 2 2
2KI+Cl =2KCl+I 。
2 2
11.(2020·安徽省明光中学高二开学考试)海水中溴含量约为65mg·L-1,从海水中提取溴的工艺流程如图:
(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是_____。
(2)步骤Ⅱ通入热空气吹出Br ,利用了溴的______(填字母)。
2
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数:
________Br +________ =________ +_Br-+_CO ↑
2 2
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水
溶液反应的化学方程式:______。
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是______(填字母)。
A.稀硫酸 B.四氯化碳 C.烧碱溶液 D.水
【答案】(1)富集溴元素 (2) C (3) 3 3 1 5 3(4) SO +Br +2H O==H SO +2HBr (5) B
2 2 2 2 4
【解析】(1)步骤Ⅰ中获得低浓度的溴,步骤Ⅱ又将之转变成化合态的溴,主要是想实现浓度的增大,所以
目的是富集溴元素。答案为:富集溴元素;
(2)步骤Ⅱ通入热空气,使溶液的温度升高,溴从溶液中挥发,即吹出Br ,利用了溴的挥发性,故选C。
2
答案为:C;
(3)步骤Ⅱ涉及的离子反应中,Br 中一部分生成 ,溴元素的价态升高5价;Br 中一部分生成Br-,溴
2 2
元素的价态降低1价,依据化合价升高与降低的总数相等的原则,方程式中应为3Br +___ =
2
+5Br-+_ CO↑;再依据电荷守恒和质量守恒,便可得到配平的离子方程式:3Br +3 = +5Br-
2 2
+3CO ↑。答案为:3;3;1;5;3;
2
(4)溴与二氧化硫水溶液发生氧化还原反应,生成硫酸和氢溴酸,化学方程式为:
SO +Br +2H O==H SO +2HBr。答案为:SO +Br +2H O==H SO +2HBr;
2 2 2 2 4 2 2 2 2 4
(5)实验室分离溴还可以用溶剂萃取法,四个选项的物质中,稀硫酸、烧碱溶液、水都能与原来的溶液互溶,
液体不分层,所以不能作萃取剂,四氯化碳的密度比水大、难溶于水,且溴在其中的溶解度比在水中大得
多,所以可以用作溴的萃取剂的是B。答案为:B。
12.(2020·商丘市第一高级中学高三期中)氢溴酸在医药和石化工业上有广泛用途。如图是模拟工业制备
氢溴酸的流程图:
回答下列问题:
(1)混合①中发生反应的离子方程式为____。
(2)混合②中加入试剂a是____。
(3)工业氢溴酸常带有淡淡的黄色,可能的原因是:①含Fe3+,②含Br ,③含Fe3+和Br ,只用下列一种试剂
2 2
就能分析产生淡黄色的原因,该试剂是_____(填写字母)。
a.KMnO 溶液 b.NaOH溶液 c.KSCN溶液 d.淀粉KI溶液 e.CCl
4 4
(4)加入NaSO 的目的是除去过量的Br ,但要防止过量,原因是____(请用离子方程式表示)。
2 3 2(5)实验室制取Br 的反应为:2NaBr+3HSO +MnO 2NaHSO+MnSO +Br ↑+2H O,制取Br 最好选用如图
2 2 4 2 4 4 2 2 2
装置中的____(填写字母,固定和加热装置均已省略)。简述检验图所选装置气密性的方法_____。
【答案】(1)SO +Br +2H O=4H++2Br-+SO2-
2 2 2 4
(2) BaCl 溶液
2
(3) e
(4) SO 2-+2H+=SO↑+H O
3 2 2
(5) C 关闭分液漏斗活塞,将烧瓶上的导气管连接一段橡皮管并伸入水中,用手焐热烧瓶,若导管
末端有气泡产生,冷却后导管中上升一段水柱,证明装置气密性良好
【解析】(1) Br 与SO 反应生成氢溴酸和硫酸,发生的离子方程式为SO +Br +2H O=4H++2Br-+SO2-。
2 2 2 2 2 4
(2)由流程图可知,混合②后过滤生成硫酸钡,滤液蒸馏产生NaCl溶液,故钡离子、氯离子应是加入试剂a
引入的,试剂a是BaCl 溶液。
2
(3) CCl 与溶液混合后分层,有机层在下层,水层在上层,若有机层无色,水层为黄色,则原因为①;若有
4
机层为橙色,水层为无色,则原因为②;若有机层为橙色、水层为黄色,则原因为③;故答案选e。
(4)Na SO 过量,能与HBr反应生成二氧化硫、溴化钠、水,离子反应方程式为SO 2-+2H+=SO↑+H O。
2 3 3 2 2
(5)实验室制取Br 的反应为:2NaBr+3HSO +MnO 2NaHSO+MnSO +Br ↑+2H O,该反应为固体、液体
2 2 4 2 4 4 2 2
混合加热制备气体,应选择装置C;该装置检查气密性的方法为关闭分液漏斗活塞,将烧瓶上的导气管连
接一段橡皮管并伸入水中,用手焐热烧瓶,若导管末端有气泡产生,冷却后导管中上升一段水柱,证明装
置气密性良好。