文档内容
4.1.2 化学电源(学案)
1.能写出电极反应和电池反应的方程式。
2.了解常见化学电池的种类及其工作原理。
3.理解金属发生电化学腐蚀的原因,金属腐蚀的危害,防止金属腐蚀的措施。
1.写出电极反应和电池反应的方程式。
构成原电池的条件________________________________________________
知识点一、化学电源
1、电极方程式的书写
一般来讲,书写原电池的电极反应式应注意如下四点:
1.准确判断原电池的正负极
如果电池的正负极判断失误,则电极反应式必然写错,这是正确书写电极反应式的前提。一般
而言,较活泼的金属成为原电池的负极,但不是绝对的。如将铜片和铝片同时插入浓硝酸中组成原
电池时,铜却是原电池的负极被氧化,因为铝在浓硝酸中表面发生了钝化。此时,其电极反应式为:
负极:Cu-2e- ==Cu2+ 正极:2NO -+4H++2e-==2NO +2H O
3 2 2
又如将镁铝合金放入6mol/L的NaOH溶液中构成原电池时,尽管镁比铝活泼,但镁不和NaOH
溶液反应,所以铝成为负极,其电极反应式为:负极:2Al+8OH—-6e-==2AlO -+4H O 正极:
2 2
6HO+6e-==3H +6OH-
2 2
2.高度注意电解质的酸碱性
在正、负极上发生的电极反应不是孤立的,它往往与电解质溶液紧密联系。如氢—氧燃料电池
有酸式和碱式两种,在酸溶液中负极反应式为:2H-4e-==4H+ 正极反应式为:O+4H++4e-=2H O;如
2 2 2
是在碱溶液中,则不可能有H+出现,在酸溶液中,也不可能出现OH-。又于CH、CHOH等燃料
4 3
电池,在碱溶液中C元素以CO2-离子形式存在,而不是放出CO。
3 2
3.牢牢抓住总的反应方程式
从理论上讲,任何一个自发的氧化还原反应均可设计成原电池。而两个电极反应相加即得总的
反应方程式。所以,对于一个陌生的原电池,只要知道总反应方程式和其中的一个电极反应式,即可迅速写出另一个电极反应式。
4.不能忽视电子转移数相等
在同一个原电池中,负极失去的电子数必等于正极得到的电子数,所以在书写电极反应式时,
要注意电荷守恒。这样可以避免由电极反应式写总反应方程式,或由总反应方程式改写成电极反应
式所带来的失误,同时,也可避免在有关计算中产生误差。
(1)一次电池:放电之后不能充电,内部的氧化还原反应是不可逆的。
干电池:一次电池中电解质溶液制成胶状,不流动。
碱性锌锰电池
构成:负极是________,正极是_____________,电解质是KOH
负极:_____________________正极:_____________________
总反应式:_______________________________
特点:比能量较高,储存时间较长,可适用于大电流和连续放电。
(2)二次电池
①铅蓄电池
放电电极反应
负极:_____________________;正极:___________________________
总反应式:Pb(s)+PbO (s)+2HSO (aq)=2PbSO (s)+2HO(l)
2 2 4 4 2
②镍一镉碱性蓄电池
负极:________________________________;
正极:________________________________________________
总反应式:Cd +2NiO(OH)+2H O 2Ni(OH) + Cd(OH)
2 2 2
(3)燃料电池
酸性电解质 碱性电解质
电池 电极反应
H→H+,C→CO,水提供氧 H→H O,C→CO2-,OH—提供氧
2 2 3
负极
氢氧燃
正极
料电池
总反应
负极
甲烷燃
正极
料电池
总反应
负极
甲醇燃
正极
料电池
总反应负极
乙醇燃料
正极
电池
总反应
熔融碳酸盐电解质 固体氧化物电解质
电池 电极反应
H→H O,C→CO,CO2—提供氧 H→H O,C→CO,O2—提供氧
2 2 3 2 2
负极
氢氧燃
正极
料电池
总反应
负极
甲烷燃
正极
料电池
总反应
负极
甲醇燃
正极
料电池
总反应
负极
乙醇燃料
正极
电池
总反应
除氢气外,烃、肼、甲醇、氨、煤气等液体或气体,均可作燃料电池的燃料;除纯氧气外,空气中
的氧气也可作氧化剂。
燃料电池的能量转化率高于80%,远高于燃烧过程(仅30%左右),有利于节约能源。燃料电池
有广阔的发展前途。
知识点二、析氢腐蚀与吸氧腐蚀
以钢铁的腐蚀为例进行分析:
类型 析氢腐蚀 吸氧腐蚀
条件 水膜酸性较强 (pH≤4.3 ) 水膜酸性很弱或呈中性
电极 负极 Fe-2e-===Fe2+
反应 正极 2H++2e-===H ↑ O+2HO+4e-===4OH-
2 2 2
总反应式 Fe+2H+===Fe2++H↑ 2Fe+O+2HO===2Fe(OH)
2 2 2 2
联系 吸氧腐蚀更普遍
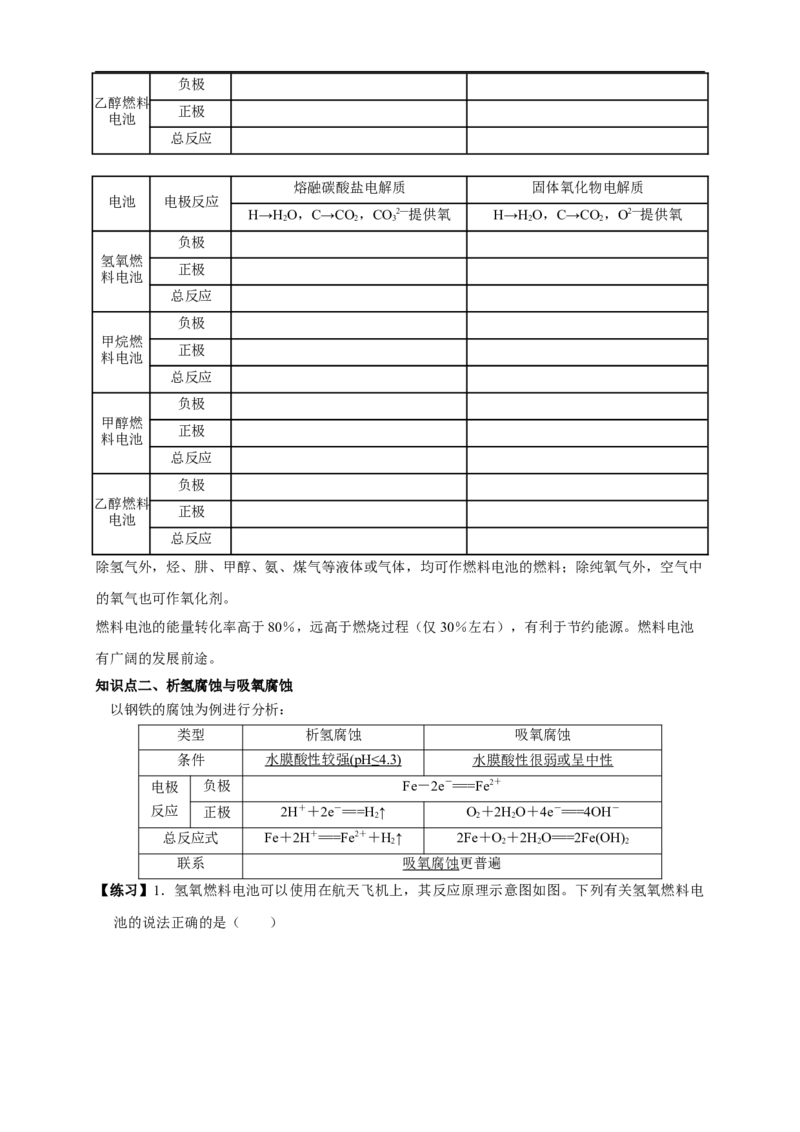
【练习】1.氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图。下列有关氢氧燃料电
池的说法正确的是( )A.该电池中电极b是正极,发生还原反应
B.外电路中电流由电极a通过导线流向电极b
C.该电池的总反应为2H O═2H +O
2 2 2
D.该电池工作时电能转化为化学能
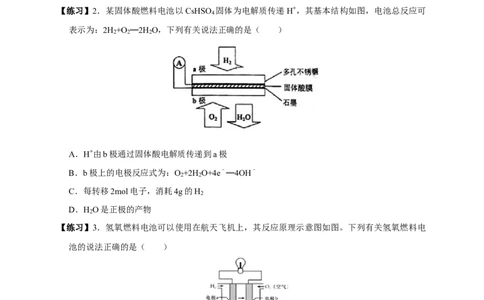
【练习】2.某固体酸燃料电池以CsHSO 固体为电解质传递H+,其基本结构如图,电池总反应可
4
表示为:2H +O ═2H O,下列有关说法正确的是( )
2 2 2
A.H+由b极通过固体酸电解质传递到a极
B.b极上的电极反应式为:O +2H O+4e﹣═4OH﹣
2 2
C.每转移2mol电子,消耗4g的H
2
D.H O是正极的产物
2
【练习】3.氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图。下列有关氢氧燃料电
池的说法正确的是( )
A.该电池工作时电能转化为化学能
B.该电池中电极b是负极
C.外电路中电子由电极b通过导线流向电极a
D.该电池是绿色环保电池
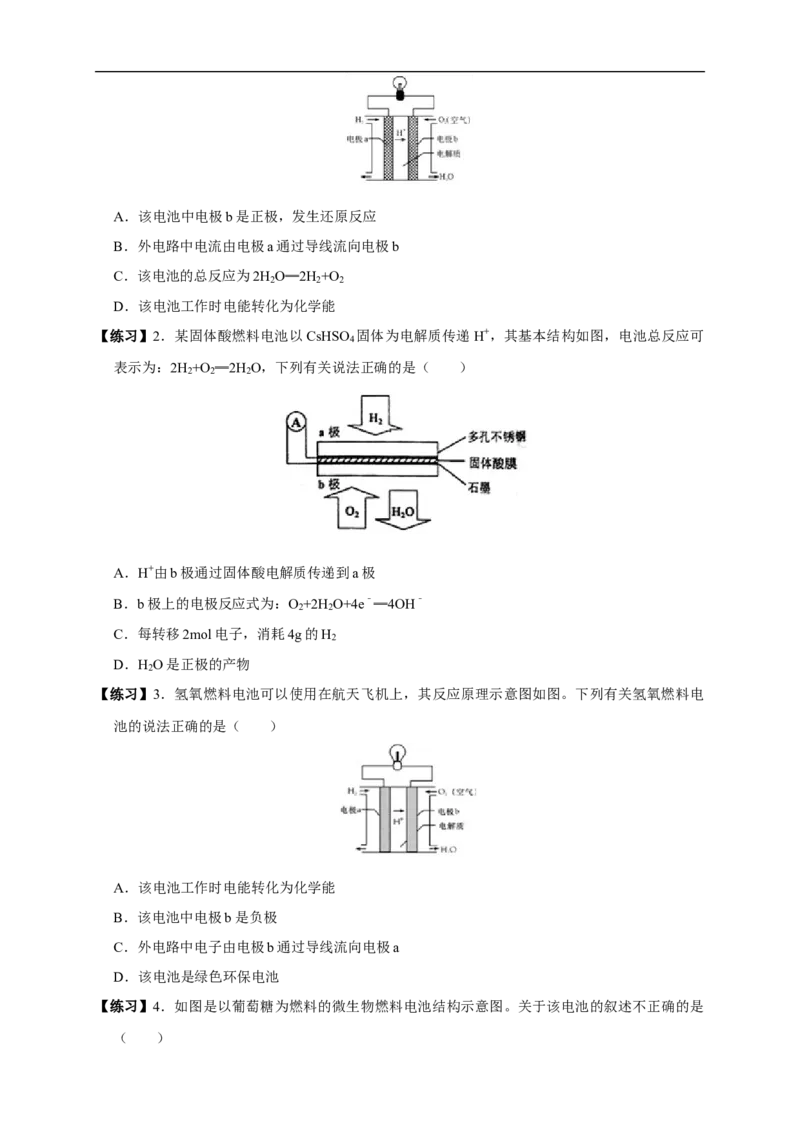
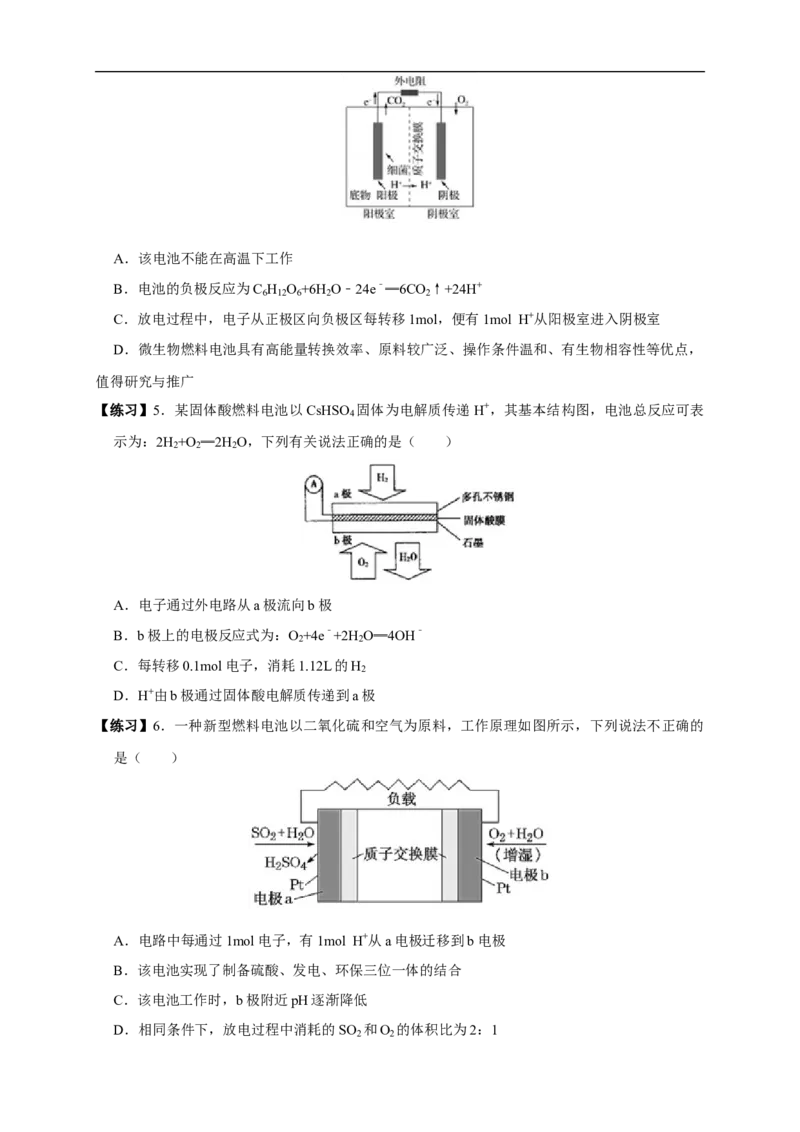
【练习】4.如图是以葡萄糖为燃料的微生物燃料电池结构示意图。关于该电池的叙述不正确的是
( )A.该电池不能在高温下工作
B.电池的负极反应为C H O +6H O﹣24e﹣═6CO ↑+24H+
6 12 6 2 2
C.放电过程中,电子从正极区向负极区每转移1mol,便有1mol H+从阳极室进入阴极室
D.微生物燃料电池具有高能量转换效率、原料较广泛、操作条件温和、有生物相容性等优点,
值得研究与推广
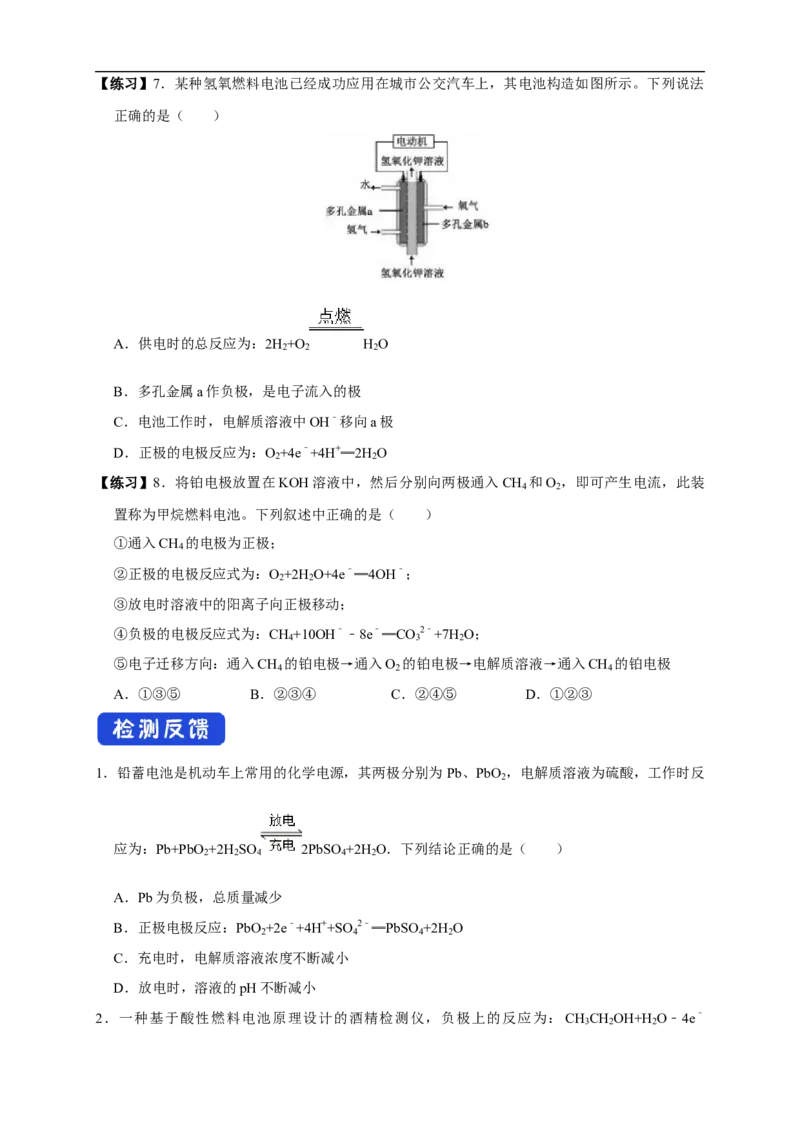
【练习】5.某固体酸燃料电池以CsHSO 固体为电解质传递H+,其基本结构图,电池总反应可表
4
示为:2H +O ═2H O,下列有关说法正确的是( )
2 2 2
A.电子通过外电路从a极流向b极
B.b极上的电极反应式为:O +4e﹣+2H O═4OH﹣
2 2
C.每转移0.1mol电子,消耗1.12L的H
2
D.H+由b极通过固体酸电解质传递到a极
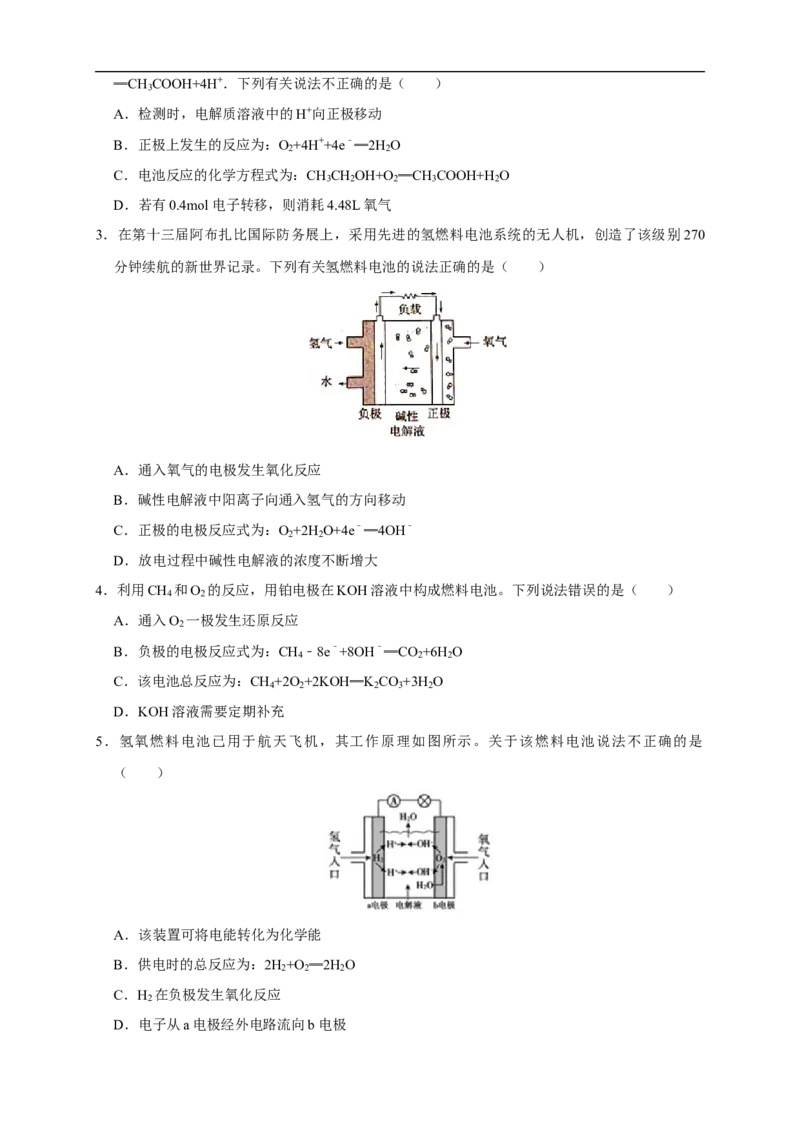
【练习】6.一种新型燃料电池以二氧化硫和空气为原料,工作原理如图所示,下列说法不正确的
是( )
A.电路中每通过1mol电子,有1mol H+从a电极迁移到b电极
B.该电池实现了制备硫酸、发电、环保三位一体的结合
C.该电池工作时,b极附近pH逐渐降低
D.相同条件下,放电过程中消耗的SO 和O 的体积比为2:1
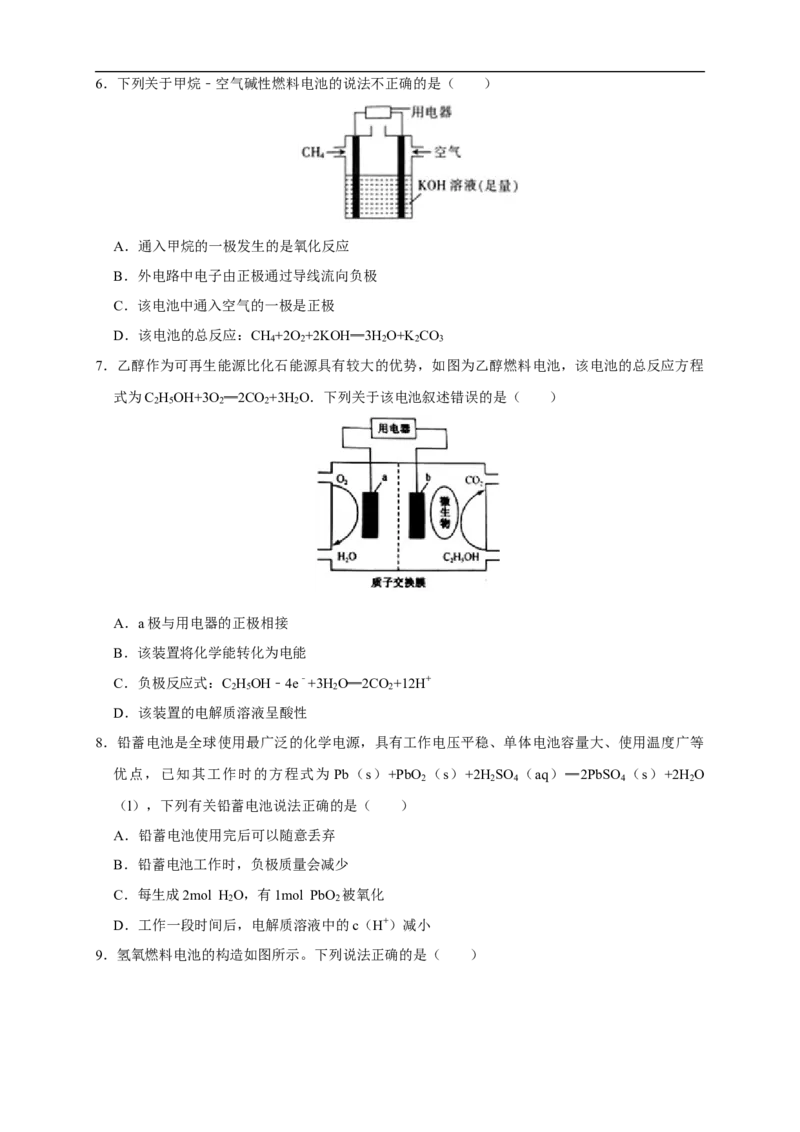
2 2【练习】7.某种氢氧燃料电池已经成功应用在城市公交汽车上,其电池构造如图所示。下列说法
正确的是( )
A.供电时的总反应为:2H +O H O
2 2 2
B.多孔金属a作负极,是电子流入的极
C.电池工作时,电解质溶液中OH﹣移向a极
D.正极的电极反应为:O +4e﹣+4H+═2H O
2 2
【练习】8.将铂电极放置在KOH溶液中,然后分别向两极通入CH 和O ,即可产生电流,此装
4 2
置称为甲烷燃料电池。下列叙述中正确的是( )
①通入CH 的电极为正极;
4
②正极的电极反应式为:O +2H O+4e﹣═4OH﹣;
2 2
③放电时溶液中的阳离子向正极移动;
④负极的电极反应式为:CH +10OH﹣﹣8e﹣═CO 2﹣+7H O;
4 3 2
⑤电子迁移方向:通入CH 的铂电极→通入O 的铂电极→电解质溶液→通入CH 的铂电极
4 2 4
A.①③⑤ B.②③④ C.②④⑤ D.①②③
1.铅蓄电池是机动车上常用的化学电源,其两极分别为Pb、PbO ,电解质溶液为硫酸,工作时反
2
应为:Pb+PbO +2H SO 2PbSO +2H O.下列结论正确的是( )
2 2 4 4 2
A.Pb为负极,总质量减少
B.正极电极反应:PbO +2e﹣+4H++SO 2﹣═PbSO +2H O
2 4 4 2
C.充电时,电解质溶液浓度不断减小
D.放电时,溶液的pH不断减小
2.一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH CH OH+H O﹣4e﹣
3 2 2═CH COOH+4H+.下列有关说法不正确的是( )
3
A.检测时,电解质溶液中的H+向正极移动
B.正极上发生的反应为:O +4H++4e﹣═2H O
2 2
C.电池反应的化学方程式为:CH CH OH+O ═CH COOH+H O
3 2 2 3 2
D.若有0.4mol电子转移,则消耗4.48L氧气
3.在第十三届阿布扎比国际防务展上,采用先进的氢燃料电池系统的无人机,创造了该级别270
分钟续航的新世界记录。下列有关氢燃料电池的说法正确的是( )
A.通入氧气的电极发生氧化反应
B.碱性电解液中阳离子向通入氢气的方向移动
C.正极的电极反应式为:O +2H O+4e﹣═4OH﹣
2 2
D.放电过程中碱性电解液的浓度不断增大
4.利用CH 和O 的反应,用铂电极在KOH溶液中构成燃料电池。下列说法错误的是( )
4 2
A.通入O 一极发生还原反应
2
B.负极的电极反应式为:CH ﹣8e﹣+8OH﹣═CO +6H O
4 2 2
C.该电池总反应为:CH +2O +2KOH═K CO +3H O
4 2 2 3 2
D.KOH溶液需要定期补充
5.氢氧燃料电池已用于航天飞机,其工作原理如图所示。关于该燃料电池说法不正确的是
( )
A.该装置可将电能转化为化学能
B.供电时的总反应为:2H +O ═2H O
2 2 2
C.H 在负极发生氧化反应
2
D.电子从a电极经外电路流向b电极6.下列关于甲烷﹣空气碱性燃料电池的说法不正确的是( )
A.通入甲烷的一极发生的是氧化反应
B.外电路中电子由正极通过导线流向负极
C.该电池中通入空气的一极是正极
D.该电池的总反应:CH +2O +2KOH═3H O+K CO
4 2 2 2 3
7.乙醇作为可再生能源比化石能源具有较大的优势,如图为乙醇燃料电池,该电池的总反应方程
式为C H OH+3O ═2CO +3H O.下列关于该电池叙述错误的是( )
2 5 2 2 2
A.a极与用电器的正极相接
B.该装置将化学能转化为电能
C.负极反应式:C H OH﹣4e﹣+3H O═2CO +12H+
2 5 2 2
D.该装置的电解质溶液呈酸性
8.铅蓄电池是全球使用最广泛的化学电源,具有工作电压平稳、单体电池容量大、使用温度广等
优点,已知其工作时的方程式为 Pb(s)+PbO (s)+2H SO (aq)═2PbSO (s)+2H O
2 2 4 4 2
(l),下列有关铅蓄电池说法正确的是( )
A.铅蓄电池使用完后可以随意丢弃
B.铅蓄电池工作时,负极质量会减少
C.每生成2mol H O,有1mol PbO 被氧化
2 2
D.工作一段时间后,电解质溶液中的c(H+)减小
9.氢氧燃料电池的构造如图所示。下列说法正确的是( )A.a是电池正极
B.电池工作时,H 在电池内部燃烧
2
C.b电极的电极反应为O +4e﹣+4H+═2H O
2 2
D.电子由a沿导线流向b,再由b通过电解质溶液流回a
【课前复习答案】能自发进行的氧化还原反应发生;活泼性不同的两电极;形成闭合回路
【知识点填空答案】
Zn;MnO ;Zn-2e-+2OH-=Zn(OH) ;MnO +e-+H O=MnOOH+OH-;
2 2 2 2
Zn+2MnO +2H O=2MnOOH+Zn(OH) ;Pb-2e-+SO 2-=PbSO;PbO +2e-+4H++SO 2-=PbSO+
2 2 2 4 4 2 4 4
2HO;Cd+2OH--2e-=Cd(OH) ;2NiO(OH)+2H O+2e-=2Ni(OH) +2OH-
2 2 2 2
H+2e-=2H+ 2H++2OH-=2H O
2 2
O+4H++4e-=2H O O+2H O+4e-=4OH-
2 2 2 2
2H+O =2H O 2H+O =2H O
2 2 2 2 2 2
CH-8e-+2H O=8H++CO CH–8e-+10OH-=CO 2-+7H O
4 2 2 4 3 2
O+4H++4e-=2H O O+2H O+4e-=4OH-
2 2 2 2
CH+2O =CO +2H O CH+2OH-+2O =CO 2-+3H O
4 2 2 2 4 2 3 2
CHOH-6e-+H O=6H++CO CHOH-6e-+8OH-=CO 2-+6H O
3 2 2 3 3 2
O+4H++4e-=2H O O+2H O+4e-=4OH-
2 2 2 2
2CHOH+3O -=2CO +4H O 2CHOH+3O +4OH-=2CO 2-+6H O
3 2 2 2 3 2 3 2
C HOH-12e-+3H O=12H++2CO C HOH-12e-+16OH-=2CO 2-+11H O
2 5 2 2 2 5 3 2
O+4H++4e-=2H O O+2H O+4e-=4OH-
2 2 2 2
C HOH-+3O -=2CO +3H O C HOH-+3O +4OH-=2CO 2-+5H O
2 5 2 2 2 2 5 2 3 2
H+CO 2—2e-=H O+CO H+O2—2e-=H O
2 3 2 2 2 2
O+4e-+2CO =2CO 2- O+4e-=2O2-
2 2 3 2
2H+O =2H O 2H+O =2H O
2 2 2 2 2 2
CH+4CO 2—8e-=2H O+5CO CH+4CO 2—8e-=2H O+5CO
4 3 2 2 4 3 2 2
O+4e-+2CO =2CO 2- O+4e-=2O2-
2 2 3 2
CH+2O =CO +2H O CH+2O =CO +2H O
4 2 2 2 4 2 2 2
CHOH+3CO 2—6e-=2H O+4CO CHOH+3CO 2—6e-=2H O+4CO
3 3 2 2 3 3 2 2
O+4e-+2CO =2CO 2- O+4e-=2O2-
2 2 3 22CHOH+3O -=2CO +4H O 2CHOH+3O -=2CO +4H O
3 2 2 2 3 2 2 2
C HOH+6CO 2—12e-=3H O+7CO C HOH+6O2—12e-=3H O+2CO
2 5 3 2 2 2 5 2 2
O+4e-+2CO =2CO 2- O+4e-=2O2-
2 2 3 2
C HOH-+3O -=2CO +3H O C HOH-+3O -=2CO +3H O
2 5 2 2 2 2 5 2 2 2
【练习答案】ADDCACCB
【检测反馈答案】BDCBABCDC