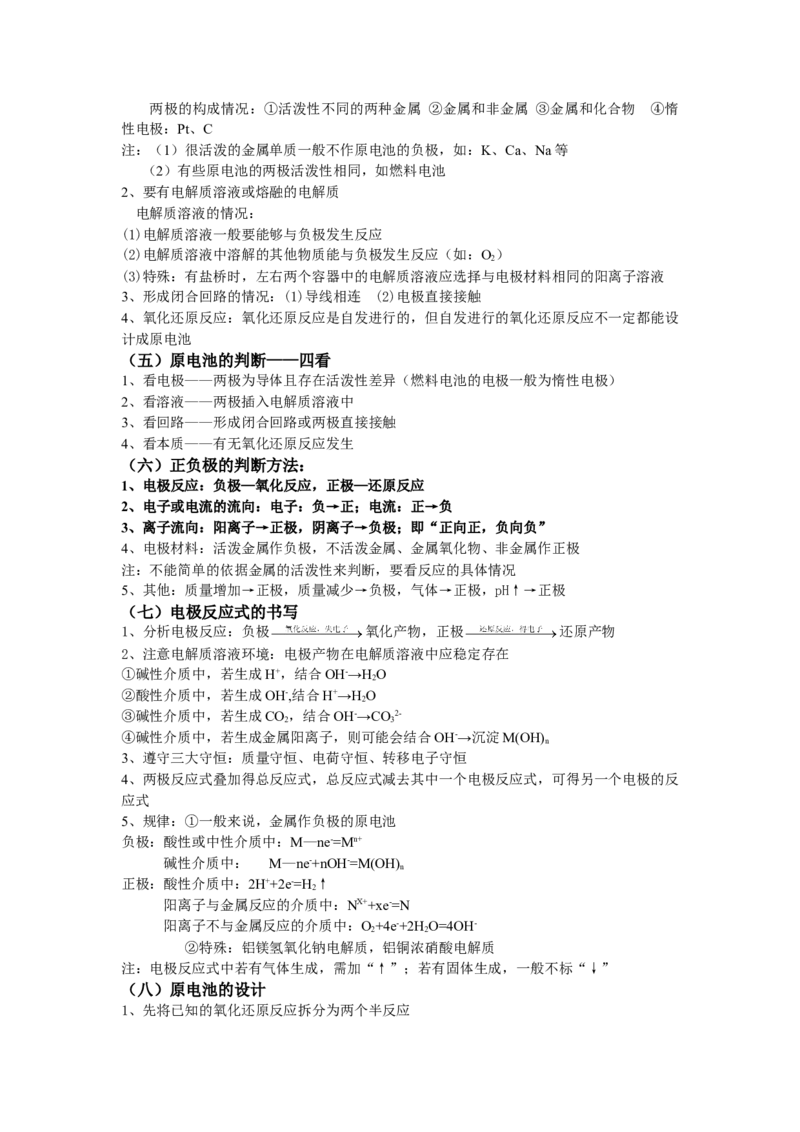文档内容
第一节 原电池
一、原电池的工作原理
(一)定义:将化学能转化能电能的装置
(二)本质:氧化还原反应
(三)工作原理:以铜-锌原电池为例
电极:Zn—负
极,Cu—正极
工作原理:负极→失
电子→
发生氧
化反应
→电子
通过导
线流向
正极→
正极→
得电子
→发生
还原反
应
溶液中:阴离子→
负极,
阳离子
→正极
外电路—电子导
电,内
电路—
离子导
电
电极反应: 总反应: Zn+Cu2+=Zn2++Cu
注: 1、盐桥的作用:(1)成分:含琼胶的KCl饱和溶液
(2)作用:①构成通路,代替两溶液直接接触 ②平衡电荷:K+→
正极,Cl-→负极
(3)优点:隔离氧化剂和还原剂,不同区域实现电子定向移动,产
生持续、稳定的电流
2、电子只能在两极和外电路中流动,不可能进入溶液中。即“电子不下水,离子不上岸”
3、溶液中是由电解质溶液中的阴阳离子定向移动形成闭合回路的
(四)条件:两极一液一连线,氧化还原是条件
1、两个能导电的电极——正极和负极:两极的构成情况:①活泼性不同的两种金属 ②金属和非金属 ③金属和化合物 ④惰
性电极:Pt、C
注:(1)很活泼的金属单质一般不作原电池的负极,如:K、Ca、Na等
(2)有些原电池的两极活泼性相同,如燃料电池
2、要有电解质溶液或熔融的电解质
电解质溶液的情况:
(1)电解质溶液一般要能够与负极发生反应
(2)电解质溶液中溶解的其他物质能与负极发生反应(如:O)
2
(3)特殊:有盐桥时,左右两个容器中的电解质溶液应选择与电极材料相同的阳离子溶液
3、形成闭合回路的情况:(1)导线相连 (2)电极直接接触
4、氧化还原反应:氧化还原反应是自发进行的,但自发进行的氧化还原反应不一定都能设
计成原电池
(五)原电池的判断——四看
1、看电极——两极为导体且存在活泼性差异(燃料电池的电极一般为惰性电极)
2、看溶液——两极插入电解质溶液中
3、看回路——形成闭合回路或两极直接接触
4、看本质——有无氧化还原反应发生
(六)正负极的判断方法:
1、电极反应:负极—氧化反应,正极—还原反应
2、电子或电流的流向:电子:负→正;电流:正→负
3、离子流向:阳离子→正极,阴离子→负极;即“正向正,负向负”
4、电极材料:活泼金属作负极,不活泼金属、金属氧化物、非金属作正极
注:不能简单的依据金属的活泼性来判断,要看反应的具体情况
5、其他:质量增加→正极,质量减少→负极,气体→正极,pH↑→正极
(七)电极反应式的书写
1、分析电极反应:负极 氧化产物,正极 还原产物
2、注意电解质溶液环境:电极产物在电解质溶液中应稳定存在
①碱性介质中,若生成H+,结合OH-→HO
2
②酸性介质中,若生成OH-,结合H+→HO
2
③碱性介质中,若生成CO,结合OH-→CO2-
2 3
④碱性介质中,若生成金属阳离子,则可能会结合OH-→沉淀M(OH)
n
3、遵守三大守恒:质量守恒、电荷守恒、转移电子守恒
4、两极反应式叠加得总反应式,总反应式减去其中一个电极反应式,可得另一个电极的反
应式
5、规律:①一般来说,金属作负极的原电池
负极:酸性或中性介质中:M—ne-=Mn+
碱性介质中: M—ne-+nOH-=M(OH)
n
正极:酸性介质中:2H++2e-=H ↑
2
阳离子与金属反应的介质中:NX++xe-=N
阳离子不与金属反应的介质中:O+4e-+2H O=4OH-
2 2
②特殊:铝镁氢氧化钠电解质,铝铜浓硝酸电解质
注:电极反应式中若有气体生成,需加“↑”;若有固体生成,一般不标“↓”
(八)原电池的设计
1、先将已知的氧化还原反应拆分为两个半反应2、根据原电池的电极反应特点,结合两个半反应,找出正负极材料及电解质溶液
3、按要求画出原电池装置图
(九)应用
1、形成原电池,可以加快氧化还原反应的反应的速率
2、通过原电池的电极,可以比较金属活泼性强弱
3、设计化学电源
4、保护金属设备:被保护金属作正极
二、化学电源
(一)分类:
一次电池:就是放电后不可再充电的电池。随着使用,一次电池中能发生氧化还原反应的
物质逐渐被消耗,当这些物质被消耗到一定程度时,电池就不能继续使用了。
一次电池中电解质溶液制成胶状,不流动,也叫做干电池。
二次电池:又称可充电电池或蓄电池,是一类放电后可以再充电而反复使用的电池。即它
在放电时所进行的氧化还原反应,在充电时可以逆向进行(一般通过充电器将
交流电转变为直流电进行充电),使电池恢复到放电前的状态。这样可以实现
将化学能转变为电能(放电),再由电能转变为化学能(充电)的循环。
燃料电池:是一种连续的将燃料和氧化剂的化学能直接转换成电能的化学电池。
(二)优点:
1、化学电池的能量转化效率较高,供能稳定可靠
2、可以制成各种形状、大小和容量不同的电池及电池组
3、方便携带,易于维护
(三)判断电池优劣的主要标准:
1、比能量:电池单位质量或单位体积所能输出电能的多少
2、比功率:输出功率的大小
3、电池可储存时间的长短
(四)一次电池——普通锌锰电池、碱性锌锰电池、锌银电池
1、普通锌锰干电池
(1)电极材料及电极反应:负极:锌筒 Zn-2e-=Zn2+
正极:石墨 2NH ++2MnO+2e-=2NH↑+Mn O+HO
4 2 3 2 3 2
总反应:Zn+2MnO +2NH Cl=ZnCl+2NH↑+Mn O+HO
2 4 2 3 2 3 2
(2)电解质:MnO 、NH Cl、ZnCl、淀粉等调成糊状
2 4 2
(3)缺点:新电池会自动放电,锌皮腐蚀逐渐变薄、放电后电压下降较快、电量小、易气
胀或漏液、存放时间缩短不易长时间连续使用
(4)优点:制作简单,价格便宜
2、碱性锌锰电池
(1)电极材料及电极反应:负极:锌筒 Zn-2e-+2OH-=Zn(OH)
2
正极:MnO 2MnO +2e-+2HO=2MnO(OH)(氢氧化氧锰)+2OH-
2 2 2
(MnO 作为正极反应物,得电子被还原为
2
MnO(OH))
总反应: Zn+2MnO +2HO=2MnO(OH)+Zn(OH)
2 2 2
(2)电解质:将NH Cl换成湿的KOH
4
(3)优点:比能量和可储存时间均有所提高,是普通干电池的升级换代产品(五)二次电池(可充电电池)
举例:铅酸蓄电池
1、电极材料:负极:Pb 正极:PbO 电解质:HSO
2 2 4
2、电极反应式:负极:Pb-2e-+SO2-=PbSO 正极:PbO +4H++2e-+SO2-
4 4 2 4
=PbSO+2HO
4 2
总反应:Pb+PbO+2H SO =2PbSO+2HO
2 2 4 4 2
3、工作特点:电压稳定,使用方便,安全可靠,价格低廉;但比能量低,笨重,废弃电池
污染环境
4、接线方式:充电时,待充电电池的负极要接电源的负极,待充电电池的正极要接电源的
正极,即正接正,负接负
注:放电:化学能转化为电能;充电:电能转化为化学能
(六)燃料电池
1、工作原理
连续将氢气、烃、肼、甲醇、氨、煤气等液体或气体燃料和氧化剂的化学能转换为电
能。电极本身不包含活性物质,不参与氧化还原反应。工作时,燃料和氧化剂连续地由外
部供给,在电极上不断地进行反应,生成物不断被排除
2、特点:
(1)燃料电池中,燃料(还原性气体等)作负极,发生氧化反应,氧化剂(通常为氧气)
作正极发生还原反应
(2)燃料电池的电极材料一般为惰性电极,具有很强的催化活性,如铂电极、活性炭电极
等
(3)燃料电池在使用过程中,并没有发生燃料与氧化剂之间的直接燃烧,而是在两极之间
发生了放电,将化学能转化
为电能
(4)燃料的燃烧是一种剧烈的氧化还原反应,而燃料电池则是平稳的氧化还原反应
(5)燃料直接燃烧时,大量的热能释放到空气中,利用率低;燃料电池工作时,能量转化
率较高,是一种高效、环境友好的发电装置
(6)燃料电池的反应物并不储存在电池内部,而是由外设装备提供燃料和氧化剂
3、燃料电池与一般化学电池的区别
一般化学电池的活性物质储存在电池内部,故而限制了电池的容量,而燃料电池的电
极本身不包含活性物质,只是一个催化转化元件。它工作时,燃料和氧化剂连续地由外部
供给,在电极上不断地进行反应,生成物不断地被排除,于是电池就连续不断地提供电能
4、优点
燃料电池的能量转化率超过80%,远高于普通燃烧过程(能量转化率仅30%多),可
以持续使用,噪音低,不污染环境。既有利于节约能源,又绿色环保,具有广阔的发展前
景,被誉为“绿色发电站”
5、种类
(1)氢氧燃料电池
电解质 酸性 中性 碱性
负极反 H-2e-=2H+ H-2e-=2H+ H-2e-+2OH-=2HO
2 2 2 2
应
正极反 O+4e-+4H+=2HO O+4e-+2HO=4OH- O+4e+2HO=4OH-
2 2 2 2 2 2
应
总反应 2H+O =2HO
2 2 2
(2)甲烷燃料电池
电解质 HSO KOH
2 4负极反
CH-8e-+2H O=CO+8H+ CH-8e-+10OH-=CO2-+7H O
应 4 2 2 4 3 2
正极反
O+4e-+4H+=2HO O+4e-+2HO=4OH-
应 2 2 2 2
总反应 CH+2O =CO+2HO CH+2O +2OH-=CO2-+3HO
4 2 2 2 4 2 3 2
(3)甲醇燃料电池
电解质 HSO KOH
2 4
负极反
CHOH-6e-+H O=CO+6H+ CHOH-6e-+8OH-=CO2-+6H O
应 3 2 2 3 3 2
正极反
O+4e-+4H+=2HO O+4e-+2HO=4OH-
应 2 2 2 2
总反应 2CHOH+3O =2CO+4HO 2CHOH+3O +4OH-=2CO2-+6HO
3 2 2 2 3 2 3 2
(4)熔融盐电池
例如:用LiCO 和NaCO 的熔融盐混合物作电解质的燃料电池,CO为燃料,空气与CO
2 3 2 3 2
的混合气为助燃气,制得在650℃下工作的燃料电池,在工作过程中,电解质熔融
盐的组成、浓度不变
电极反应式:负极:2CO+2CO2--4e-=4CO 正极:O+2CO +4e-=2CO2- 总反
3 2 2 2 3
应:2CO+O =2CO
2 2
6、燃料电池中常见正极反应式的书写
(1)在酸性溶液中:O+4e-+4H+=2HO
2 2
(2)在碱性或中性溶液中,O+4e-+2HO=4OH-
2 2
(3)在熔融碳酸盐中,O+2CO +4e-=2CO2-
2 2 3
(4)在可传导O2-的晶体电解质中(例如:掺杂(Y O)氧化钇的(ZrO)氧化锆晶体):
2 3 2
O+4e-=2O2-
2
注:燃料电池的总反应就是各种物质的燃烧反应,但不写反应条件