文档内容
第四章 物质结构 元素周期律
第一节 原子结构与元素周期表
第四课时 原子结构与元素的性质—卤素
【学习目标】1.通过阅读教材和实验探究,认识卤族元素性质的递变规律,并能用原子结构理论初步
加以解释同主族元素性质的递变规律,掌握元素性质与原子结构的关系,培养宏观辨识与微观探析的化学
核心素养。
2.通过分析卤族元素的相关性质的图表信息,尝试运用比较、归纳等方法对信息进行加工,培养分
析、处理数据的能力,体会事物变化过程中量变引起质变的规律,落实证据推理与模型认知的化学核心素
养。
【学习重点】卤族元素性质的相似性和递变性
【学习难点】原子结构与卤族元素性质的关系
【课前预习】
旧知回顾:1.指出ⅦA族元素的元素符号及名称,并分别画出原子结构示意图。
2.碱金属都能与水反应,反应的通式为 。随着核电荷数的增加,碱
金属与水反应越来越 ,生成的ROH(最高价氧化物对应的水化物)的碱性越来越 。
新知预习:1.卤族元素为第 族的元素,包括 。最外层电子
数都是 ,容易 一个电子形成最外层8电子我的结构。
2.卤族元素性质相似,如均能与氢气化合的通式为 ,与水反应的通
式为 ( 除外)。从上到下,随核电荷数的增加,也表现出递变
性如氢化物稳定性: ;还原性:
;酸性: 。最高价氧化物对应水化物的酸性逐渐 (除
外),即 等。
【课中探究】
情景导入:
【溴和碘的发现之旅】
1824年,法国化学家巴拉尔(1802—1876)在研究盐湖中植物的时候,将从大西洋和地中海沿岸采集到
的黑角菜燃烧成灰,然后用浸泡的方法得到一种灰黑色的浸取液。他往浸取液中加入
氯水和淀粉,溶液即分为两层:下层显蓝色(这是由于淀粉与溶液中的碘生成了化合
物);上层显棕黄色。为什么会出现这种现象呢?经巴拉尔的研究,认为可能有两种
情况:一是氯与溶液中的碘形成新的氯化碘,这种化合物使溶液呈棕黄色;二是氯把溶液中的新元素置换出来了,因而使上层溶液呈棕黄色。于是巴拉尔想了些办法,试图把新的化合物分
开,但都没有成功。所以他断定这是一种与氯、碘相似的新元素。1825年,德国海德堡大学学生罗威把家
乡克罗次纳的一种矿泉水通入氯气,产生一种红棕色的物质。这种物质用乙醚提取后,再将乙醚蒸发,则
得到红棕色的液溴。所以罗威也是独立发现溴的化学家。
一、卤素原子的结构特点及物理性质
活动一、卤素的概念及原子结构
任务一、查看元素周期表,阅读教材P102页中间自然段,思考什么是卤素元素?其原子结构有何特
点?可得到什么结论?
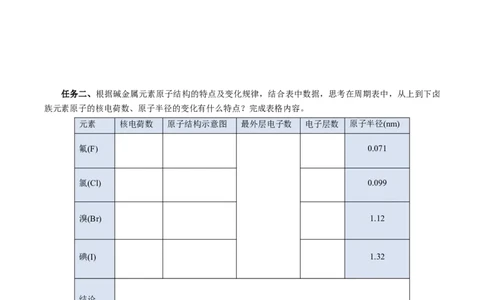
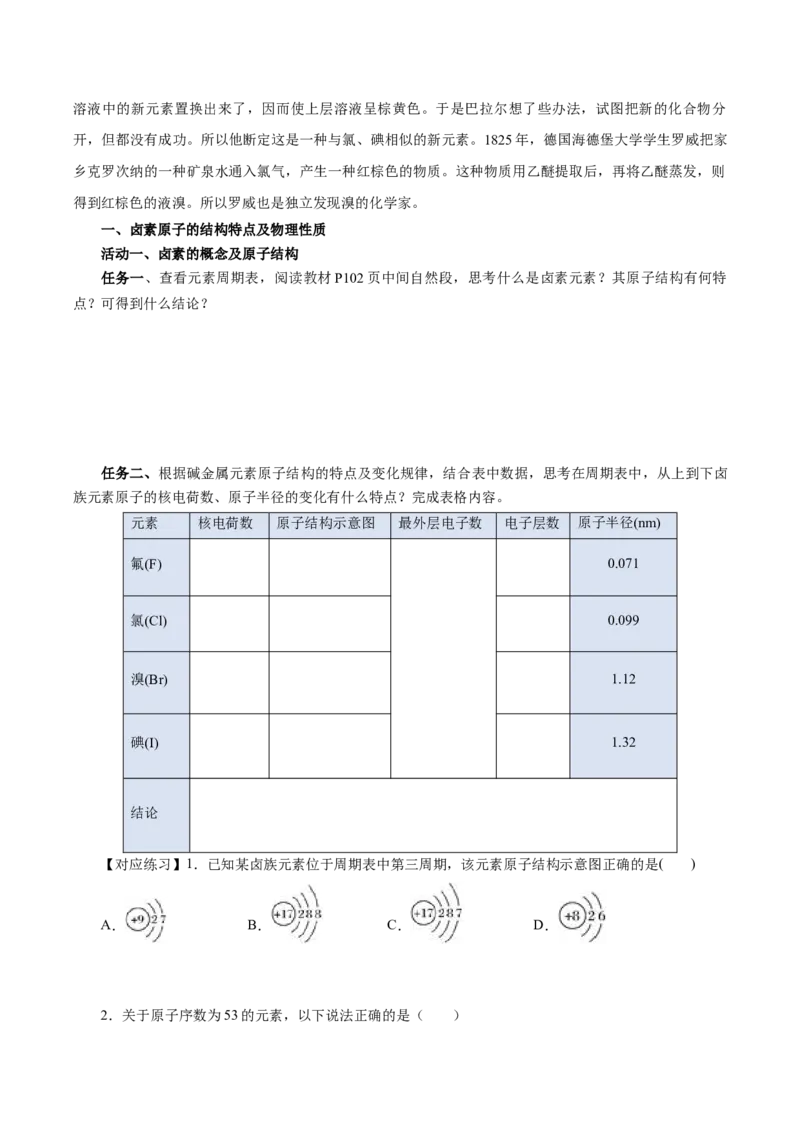
任务二、根据碱金属元素原子结构的特点及变化规律,结合表中数据,思考在周期表中,从上到下卤
族元素原子的核电荷数、原子半径的变化有什么特点?完成表格内容。
元素 核电荷数 原子结构示意图 最外层电子数 电子层数 原子半径(nm)
氟(F) 0.071
氯(Cl) 0.099
溴(Br) 1.12
碘(I) 1.32
结论
【对应练习】1.已知某卤族元素位于周期表中第三周期,该元素原子结构示意图正确的是( )
A. B. C. D.
2.关于原子序数为53的元素,以下说法正确的是( )A.位于第六周期 B.是金属元素
C.最外电子层含有6个电子 D.属于卤族元素
活动二、卤素单质的物理性质及变化规律
任务一、结合教材P102页表4-3(下表)种数据内容,归纳总结卤素单质的物理性质具有哪些相似性
和递变性?
卤素单质 颜色(常态) 密度 熔点/℃ 沸点/℃
淡黄绿色(气体) 1.69 g·L-1(15 ℃) -219.6 -188.1
F( )
2
黄绿色(气体) 3.214 g·L-1(0 ℃) -101 -34.6
Cl( )
2
深红棕色(液体) 3.119 g·cm-3(20 ℃) -7.2 58.78
Br ( )
2
紫黑色(固体) 4.93 g·cm-3 113.5 184.4
I ( )
2
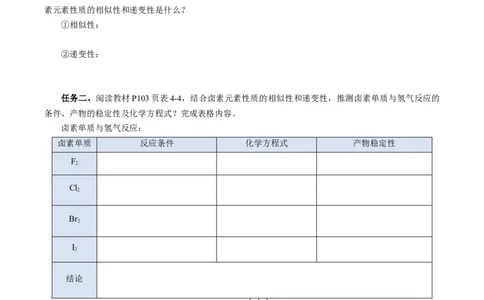
①相似性(原子结构的相似性):
②递变性(原子结构的递变性决定):
任务二、回顾氯气的溶解性,展示液溴(水封)、碘水样品,讨论交流 Cl 、Br 、I 的物理性质具有
2 2 2
哪些特殊性?完成表格内容。
气体 物理性质
F
2
Cl
2
Br
2
I
2
【对应练习】1.砹(At)是原子序数最大的卤族元素,对砹及其化合物的叙述,不正确的是
A.与H 化合的能力:At Br-
C.卤素单质的密度从F→I 随相对分子质量增大而增大
2 2
D.F 可以从NaCl溶液中置换出Cl
2 2
5.类推是一种常采用的科研和学习方法,下列类推结论合理的是( )
A.由单质铁和氯气反应生成FeCl ,推出单质铁和碘单质反应生成FeI
3 3
B.由元素周期表中从上到下,卤族元素单质熔沸点逐渐升高,推出碱金属元素单质熔沸点逐渐升高
C.最高价氧化物的水化物的酸性,由N的强于P的,推出F的强于Cl的
D.由Na在常温下与水剧烈反应,推出K在常温下也能与水剧烈反应
6.向NaBr、NaI混合液中,通入一定量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成
不可能是( )
A.NaCl,NaI B.NaCl,NaBr
C.NaCl,NaBr,NaI D.NaCl
7.已知常温下,浓盐酸与高锰酸钾反应可以生成氯气。如图甲、乙、丙三处分别是沾有NaBr溶液的
棉花、润湿的淀粉-KI试纸、润湿的品红试纸,下列说法正确的是( )
A.该实验通过现象可以证明氧化性:
B.沾有品红溶液的试纸会褪色,若再对丙微热则恢复红色C.甲的现象也可以证明 的还原性强于
D. 与NaBr溶液反应的实质与 与NaBr溶液反应类似
8.碘(I)在元素周期表中位于ⅦA族,是人体必需的微量元素之一。
(1)131I可用于治疗甲亢。131I的原子核内中子数为_______。
53 53
(2)①碘元素的非金属性比氯元素的弱,其原因是由于同主族元素从上到下原子核外电子层数依次
增多,___________逐渐增大,___________能力逐渐减弱。
②下列事实能够用“碘的非金属性比氯的弱”来解释的是________(填序号)。
a.碘单质的熔点高于氯单质
b.高氯酸的酸性强于高碘酸
c.Cl 与H 的化合比I 与H 的化合更容易
2 2 2 2
(3)氢碘酸是HI的水溶液,是一种酸性比盐酸强的酸。
资料:ⅰ.盐酸和氢碘酸均可使氢氧化铁溶解,后者得到的产物中含有I。
2
ⅱ.KI溶液不能溶解氢氧化铁,KI溶液与FeCl 溶液反应的产物中含有I。
3 2
①盐酸与氢氧化铁发生反应的离子方程式是Fe(OH) +3H+=Fe3++3HO;氢碘酸与氢氧化铁发生反
3 2
应的离子方程式是_______________________________________。
② 结 合 上 述 资 料 , 由 物 质 性 质 解 释 ① 中 两 反 应 的 异 同 :
________________________________________。