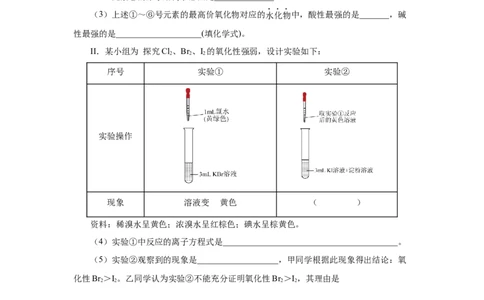
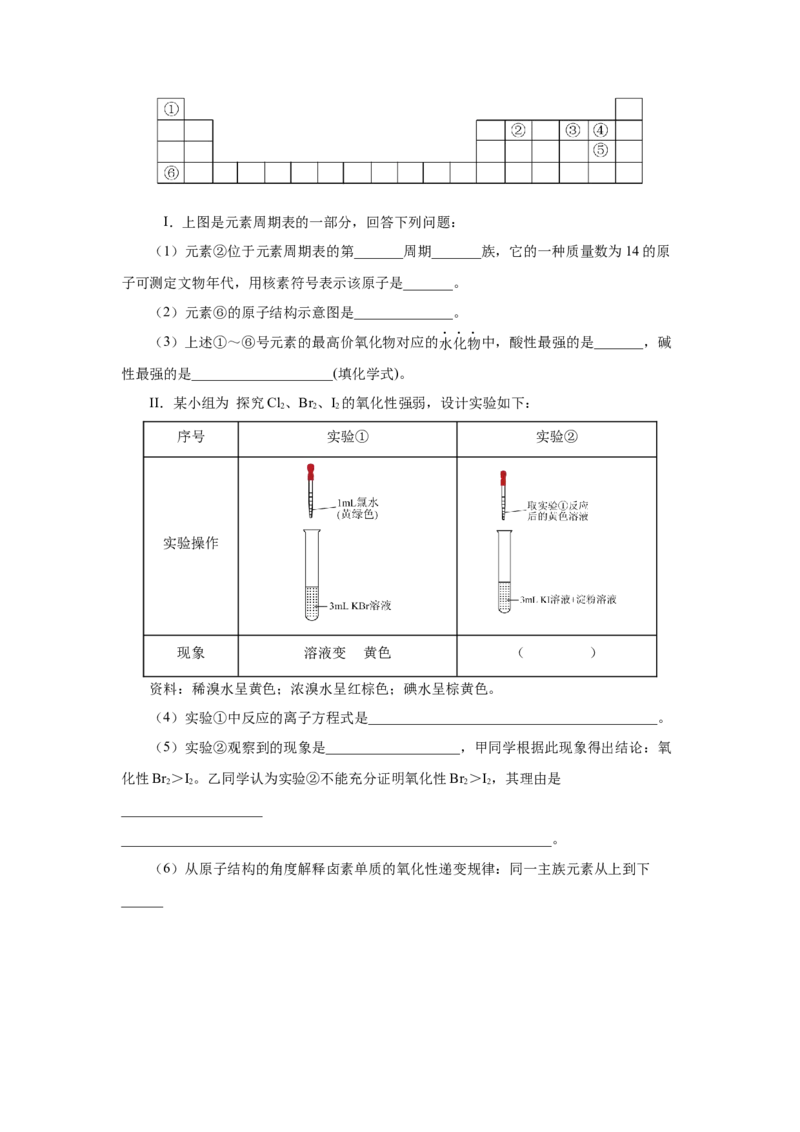
文档内容
第四章 物质结构 元素周期律
第一节 原子结构与元素周期表 课时作业
第四课时 原子结构与元素的性质—卤族元素
基础达标
1.下列关于卤素的叙述正确的是( )
A.卤素是典型的非金属元素,其单质不能与其他非金属单质化合
B.卤素单质越活泼,其熔、沸点就越高
C.卤素各单质都能与水剧烈反应
D.卤素的单质都能与氢气反应,且气态氢化物的稳定性随单质氧化性的增强而增强
2.关于元素周期表下列说法不正确的是( )
A.元素周期表有七个横行即七个周期,十八个纵行,十八个族
B.第IA族又名碱金属,随着核电荷数的増大,金属性越来越强
C.第VIIA族又称卤素,随着核电荷数的增大,单质的颜色越来越深
D.第三周期主族元素中,简单离子半径最小的是
3.氯、溴、碘单质的化学性质相似,主要原因是( )
A.单质均有颜色 B.均为双原子分子
C.原子最外层电子数均为7 D.均为非金属元素
4.核电荷数为1~18的元素中,下列叙述正确的是( )
A.最外层只有1个电子的元素一定不是非金属元素
B.最外层只有2个电子的元素一定是金属元素
C.原子核外各层电子数相等的元素一定是非金属元素
D.核电荷数为17的元素的原子容易获得1个电子
5.下列对卤素的说法不符合递变规律的是( )
A.F、Cl、Br 、I 的氧化性逐渐减弱
2 2 2 2
B.HF、HCl、HBr、HI的热稳定性逐渐减弱
C.F-、Cl-、Br-、I-的还原性逐渐增强
D.卤素单质按F、Cl、Br 、I 的顺序,颜色逐渐变浅,密度逐渐增大
2 2 2 2
6.下列操作能达到实验目的的是( )
A.检验钠和钾:分别取小粒投入含酚酞的水中,观察溶液颜色变化
B.检验氯化钠、溴化钾、碘化钾溶液:分别滴加溴水,再加入四氯化碳,振荡,观
察颜色C.除去氯化钾中的少量碘化钾:溶于水,并通入足量氯气,加热蒸干
D.证明钾比钠活泼:向氯化钠水溶液中加入一小粒钾,观察现象
7.如图是卤素单质(F 、Cl 、Br 、I)的沸点与相对分子质量的关系图,下列说法错误
2 2 2 2
的是 ( )
A.单质①是最活泼的非金属单质
B.单质②能使品红溶液褪色
C.保存少量的单质③时加少量水进行水封
D.单质④的氢化物在卤素氢化物中沸点最高
8.下列说法不正确的是( )
A.俄国化学家门捷列夫制作了第一张元素周期表
B.元素在周期表中的位置,反映了元素的原子结构和性质
C.随核电荷数增加,碱金属单质熔、沸点升高
D.随核电荷数增加,卤素单质的氧化性逐渐减弱
9.下列关于碱金属或卤族元素的叙述中,正确的是( )
A.碱金属单质都可保存在煤油中
B.随着核电荷数的增加,碱金属单质、卤素单质的熔沸点依次升高,密度依次增大
C.碱金属单质的金属性很强,均易与氧气发生反应,加热时生成氧化物R O
2
D.砹(At)是第六周期的卤族元素,根据卤素性质的递变规律,还原性:HAt>HI
10.甲、乙两种非金属元素:①甲比乙容易与氢气化合;②甲原子能与乙的阴离子发生置
换反应;③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性
强;④与某金属反应时,甲原子得电子数目比乙的多;⑤甲单质的熔、沸点比乙单质的低。能
说明甲比乙的非金属性强的是( )
A.只有④ B.只有⑤ C.①②③ D.①②③④⑤
能力提升
11.卤族元素是最活泼的一族非金属元素,下列关于卤族元素的说法正确的是( )
A.卤素单质的最外层电子数都是7
B.从上到下,卤素原子的电子层数依次增多,原子半径依次减小
C.从F到I,原子核对最外层电子的吸引能力依次减弱,原子得电子能力依次减弱
D.卤素单质与H 化合的难易程度为F