文档内容
第一节 原子结构与元素周期表
第4课时 原子结构与元素的性质——卤族元素
基础巩固
1.下列关于元素非金属性强弱的判断方法正确的是 ( )
A.根据非金属单质与氢气化合的难易程度及气态氢化物的稳定性
B.非金属氧化物对应水化物酸性的强弱或单质间的置换反应
C.HCl的酸性强于HS,故非金属性Cl>S
2
D.ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强
2.下列有关第ⅦA族元素说法不正确的是( )
A.原子最外层电子数都是7 B.从上到下原子半径逐渐增大
C.单质从F 到I,颜色逐渐加深 D.单质从F 到I,密度逐渐增大,熔沸点逐渐降低
2 2 2 2
3.氯、溴、碘单质的化学性质相似,主要原因是( )
A.单质均有颜色 B.均为双原子分子
C.原子最外层电子数均为7 D.均为非金属元素
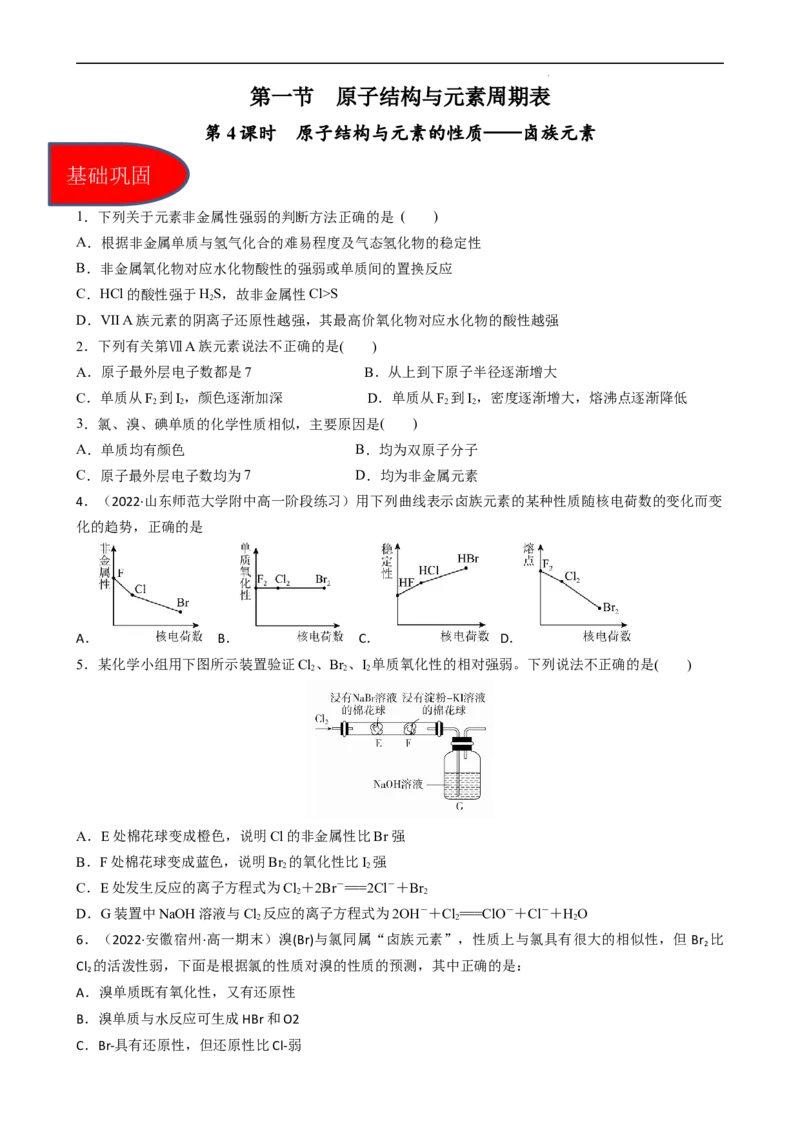
4.(2022·山东师范大学附中高一阶段练习)用下列曲线表示卤族元素的某种性质随核电荷数的变化而变
化的趋势,正确的是
A. B. C. D.
5.某化学小组用下图所示装置验证Cl、Br 、I 单质氧化性的相对强弱。下列说法不正确的是( )
2 2 2
A.E处棉花球变成橙色,说明Cl的非金属性比Br强
B.F处棉花球变成蓝色,说明Br 的氧化性比I 强
2 2
C.E处发生反应的离子方程式为Cl+2Br-===2Cl-+Br
2 2
D.G装置中NaOH溶液与Cl 反应的离子方程式为2OH-+Cl===ClO-+Cl-+HO
2 2 2
6.(2022·安徽宿州·高一期末)溴(Br)与氯同属“卤族元素”,性质上与氯具有很大的相似性,但Br 比
2
Cl 的活泼性弱,下面是根据氯的性质对溴的性质的预测,其中正确的是:
2
A.溴单质既有氧化性,又有还原性
B.溴单质与水反应可生成HBr和O2
C.Br-具有还原性,但还原性比Cl-弱
学科网(北京)股份有限公司D.溴蒸气与氢气反应比氯气与氢气反应剧烈
7.(2022·全国·高一课时练习)下列关于卤族元素(X)及其化合物叙述错误的是
A.单质均有颜色,随原子序数递增颜色加深
B.HX随原子序数递增稳定性逐渐减弱
C.单质均能与水反应生成HX和HXO
D.碘蒸气为紫色,碘水为黄褐色,碘的四氯化碳溶液呈紫红色
8.依据下列说法来判断相应元素的金属性、非金属性强弱,不合理的是( )
A.卤素单质Cl、Br 、I 的氧化性强弱
2 2 2
B.气态氢化物 NH 、HO、HF的稳定性
3 2
C.碱金属单质 Li、Na、K 与水反应的剧烈程度
D.1 mol Na、Mg、Al 分别与足量盐酸反应时失去电子数的多少
9.(2022·四川成都·高二开学考试)随着原子序数的递增,碱金属与卤族元素的变化规律正确的是
A.单质的熔沸点和密度均逐渐增大 B.最高氧化物对应的水化物酸或碱性都逐渐增强
C.原子的半径均逐渐增大 D.单质的化学活泼性均逐渐增强
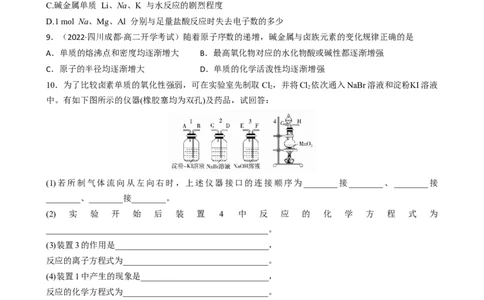
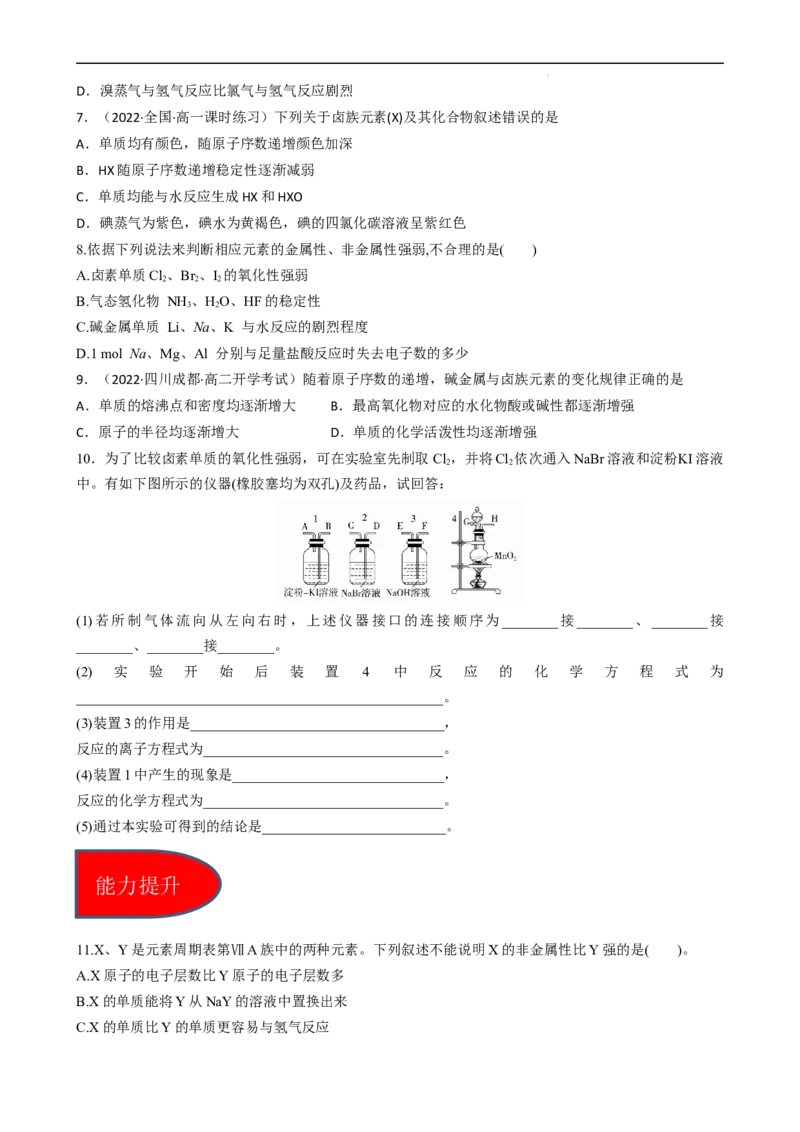
10.为了比较卤素单质的氧化性强弱,可在实验室先制取Cl,并将Cl 依次通入NaBr溶液和淀粉KI溶液
2 2
中。有如下图所示的仪器(橡胶塞均为双孔)及药品,试回答:
(1)若所制气体流向从左向右时,上述仪器接口的连接顺序为________接________、________接
________、________接________。
(2) 实 验 开 始 后 装 置 4 中 反 应 的 化 学 方 程 式 为
____________________________________________________。
(3)装置3的作用是____________________________________,
反应的离子方程式为__________________________________。
(4)装置1中产生的现象是______________________________,
反应的化学方程式为__________________________________。
(5)通过本实验可得到的结论是__________________________。
能力提升
11.X、Y是元素周期表第ⅦA族中的两种元素。下列叙述不能说明X的非金属性比Y强的是( )。
A.X原子的电子层数比Y原子的电子层数多
B.X的单质能将Y从NaY的溶液中置换出来
C.X的单质比Y的单质更容易与氢气反应
学科网(北京)股份有限公司D.同浓度下X的最高价氧化物对应的水化物比Y的最高价氧化物对应的水化物的酸性强
12.(2022·全国·高一课时练习)1940年,意大利化学家西格雷发现了第 85号元素,它被命名为“砹
(At)”。砹(At)是卤族元素中位于碘后面的元素,推测砹的结构和性质正确的是
A.与H2化合的能力: B.砹在常温下是白色固体
C.砹原子的最外层上有7个电子 D.砹易溶于水,难溶于四氯化碳
13.若能发现第117号元素X,它的原子结构与卤族元素相似,电子排布有7个电子层,且最外层有7个
电子。下列叙述中正确的是( )
A.此X元素的气态氢化物的化学式为HX,在常温下很稳定
B.其单质带有金属光泽,具有强氧化性,可与KI发生置换反应生成I
2
C.其单质的分子式为X,易溶于有机溶剂
2
D.AgX是一种有色的易溶于水的化合物
14.溴化碘(IBr)的化学性质很像卤素的单质,它能与大多数金属、非金属化合生成卤化物,它也能与水
发生以下反应:IBr+HO===HBr+HIO,下列有关IBr的叙述中,不正确的是( )
2
A.在很多反应中IBr是强氧化剂
B.IBr与水反应时既作氧化剂,又作还原剂
C.IBr与AgNO 溶液反应会生成AgBr沉淀
3
D.IBr与NaOH溶液反应时,生成NaBr和NaIO
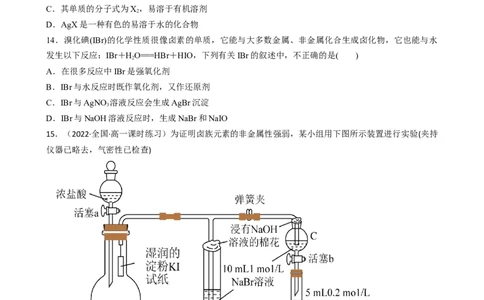
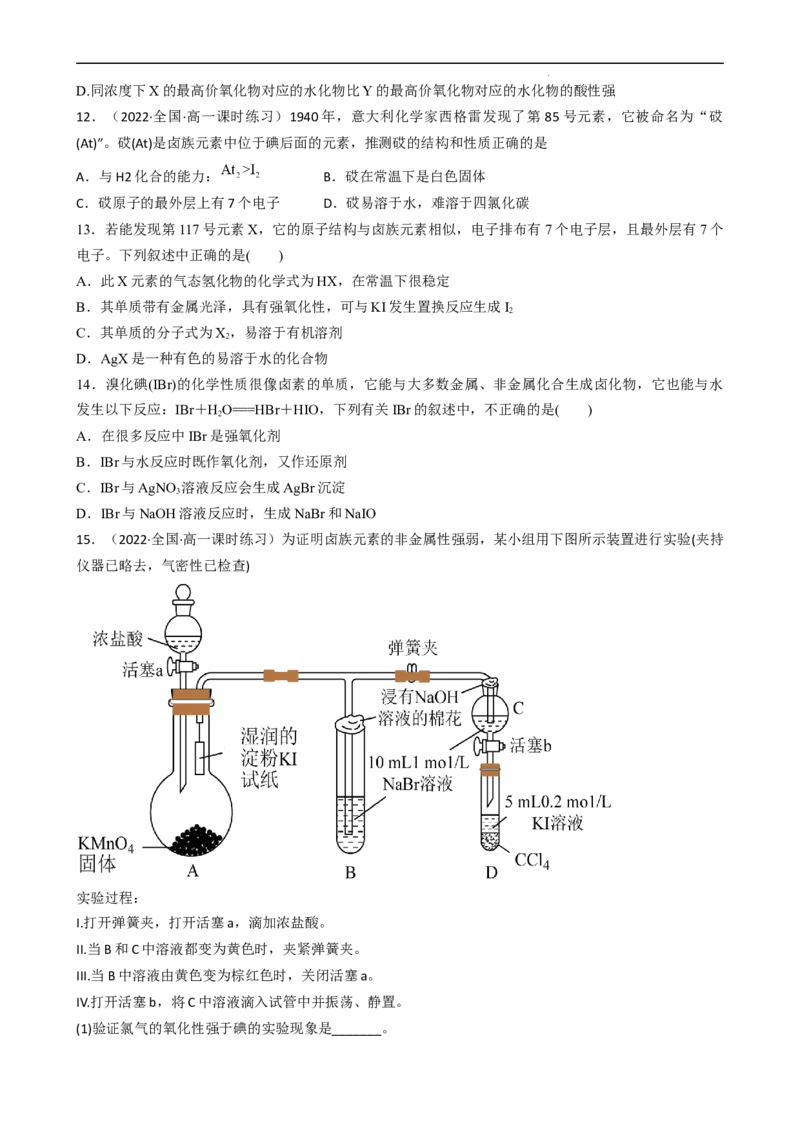
15.(2022·全国·高一课时练习)为证明卤族元素的非金属性强弱,某小组用下图所示装置进行实验(夹持
仪器已略去,气密性已检查)
实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中溶液都变为黄色时,夹紧弹簧夹。
III.当B中溶液由黄色变为棕红色时,关闭活塞a。
IV.打开活塞b,将C中溶液滴入试管中并振荡、静置。
(1)验证氯气的氧化性强于碘的实验现象是_______。
学科网(北京)股份有限公司(2)B中溶液发生反应的离子方程式是_______。
(3)为验证溴的氧化性强于碘,过程IV中试管中的现象是_______。
(4)试管B管口塞有浸有NaOH溶液的棉花的目的是_______。
学科网(北京)股份有限公司学科网(北京)股份有限公司