文档内容
第四章《化学反应与电能》导学案
第一节 原电池的工作原理
第二课时 化学电源
【学习目标】
1. 知道化学电源的分类方法。
2. 熟悉几种常见化学电源的组成和工作原理。
3. 了解化学电源广泛的应用及废旧电池对环境的危害,培养良好的环保意识。
【学习重难点】
重点:
(1)化学电池的工作原理;
(2)燃料电池电极反应式的书写
难点:掌握几种典型化学电池的电极反应
【课前预习】
旧知回顾
一、原电池的知识总结
1.定义:将 化学能 转化为电能的装置叫做 原电池 _ 。
2.组成条件
(1)两个活泼性不同的电极
【注意】①其中一个相对较活泼,另一个相对较不活泼,如:金属与金属、金属与非金属、非金属与非金
②燃料电池中两极可同选石墨或铂
(2)电解质溶液
(3)电极用导线相连并插入电解液构成闭合回路
(4)自发的氧化还原反应
3.原电池中电子流向、电流的流向及离子的迁移方向
外电路中电子的流向:负极——导线——正极
外电路中电流的流向:正极——导线——负极
内电路中离子的迁移:阴离子移向负极,阳离子移向正极溶液。
【课中探究】
情境导入:
化学电源作为一种能量转换装置,在日常生活中具有广泛的应用。它可以为我们提供
电力,如手机、笔记本电脑等电子设备都需要电池来供电。随着科技的发展,电池的性能
和安全性也在不断提高。我们也可以进一步思考化学电源在电动汽车中的应用,它作为电动汽车的动力来源,能够将化学能转化为电能,为车辆提供动力。
随着电动汽车的普及和发展,它对环境的贡献不容忽视。电动汽车相较于传统燃油汽
车,可以减少燃油排放和环境污染,符合环保意识和社会发展趋势。化学电源在电动汽车
中的应用和推广具有重要意义,它可以促进环保意识的普及和可持续发展。
一、化学电源的分类及概念
活动一、生活中的化学电源
任务1:引导学生认识化学电源,且了解化学电源的分类。
【讨论1】
讨论生活中的化学电源有哪些?按照特点化学电源怎么分类?
【答题要点】
1.生活中有干电池,汽车的铅酸蓄电池,手机、电动汽车的锂电池等。
2.化学电源的分类:化学电源可以分为一次电池、二次电池和燃料电池等
①一次电池:也叫做干电池,放电后不可再充电
②二次电池:又称可充电电池或蓄电池,放电后可以再充电使活性物质获得再生
③燃料电池:连续地将燃料和氧化剂的化学能直接转化为电能的化学电源
【讨论2】
了解生活中的电池的工作特点,那么怎么判断电池的优劣指标呢?
【答题要点】
1.比能量:单位质量或单位体积所能输出电能的多少,单位是(W·h)·kg-1或(W·h)·L-1。
2.比功率:单位质量或单位体积所能输出功率的大小,单位是W·kg-1或W·L-1。
3.电池的可储存时间的长短。
【讨论3】电池使用需要注意哪些?可以直接掩埋处理吗?
使用后的废弃电池中含有汞、镉、铬、铅等大量的重金属和酸碱等有害物质,随处丢
弃会给土壤、水源等造成严重的污染。废弃电池要进行回收利用。
【对应训练1】下列电池不属于化学电池的是( )
A.碱性干电池 B.铅蓄电池 C.燃料电池 D.太阳能电池
【答案】D
【解析】常见的电源:碱性干电池、蓄电池、燃料电池,可以将化学能转化为电能,而太阳能电池是太阳能转化为电能的装置,不是化学电池,故选D。
【对应训练2】下列有关电池的说法错误的是( )
A.手机中用的锂离子电池属于二次电池
B.甲醇燃料电池可把化学能转化为电能
C.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
D.铅蓄电池使用一段时间后,电解质溶液的酸性减弱,导电能力下降
【答案】C
【解析】A项,手机中用的锂离子电池是一类放电后可以再充电而反复使用的电池,属于
二次电池,A正确;B项,甲醇燃料电池是一种连续的将燃料和氧化剂的化学能直接转化
为电能的化学电源,B正确;C项,铜锌原电池工作时,锌为负极,铜为正极,电子沿外
电路从负极锌流向正极铜,C错误;D项,铅蓄电池使用一段时间后电解质硫酸消耗,酸
性减弱,导电能力下降,D正确;故选C。
二、一次电池(锌锰电池)
活动一:引导学生分小组讨论锌锰干电池的使用场景及不足?
任务1:结合生活中的化学电源使用情况,分析锌锰干电池的电池类别。
【答题要点】
1.一次电池:也叫做干电池,放电后不可再充电。常见的一次电池有普通锌锰干电池、碱
性锌锰干电池、纽扣式银锌电池等。
2. 锌锰干电池的结构:
常见的锌锰干电池的构造如图所示。其中,石墨棒作正极,氯化铵糊作电解质溶液,锌筒
作负极。这种电池放电之后不能充电(内部的氧化还原反应无法逆向进行),属于一次电
池。
3.生活中使用锌锰干电池时的弊端:酸性锌锰干电池即使不用,放置过久,锌筒也会因酸
性的NH Cl溶液腐蚀,造成漏液而失效,还会导致电器设备的腐蚀。
4
任务2:在已掌握的原电池原理,及电极反应式的书写知识基础上,引导学生书写锌锰干
电池的两极反应式。
【答题要点】负极:Zn﹣2e- === Zn2+
正极:2MnO + 2 + 2e- === 2MnO(OH) + 2NH ↑
2 NH+ 3
4
总反应:Zn + 2MnO + 2 === Zn2+ + 2MnO(OH) + 2NH ↑
2 NH+ 3
4
活动二、一次电池——碱性锌锰电池
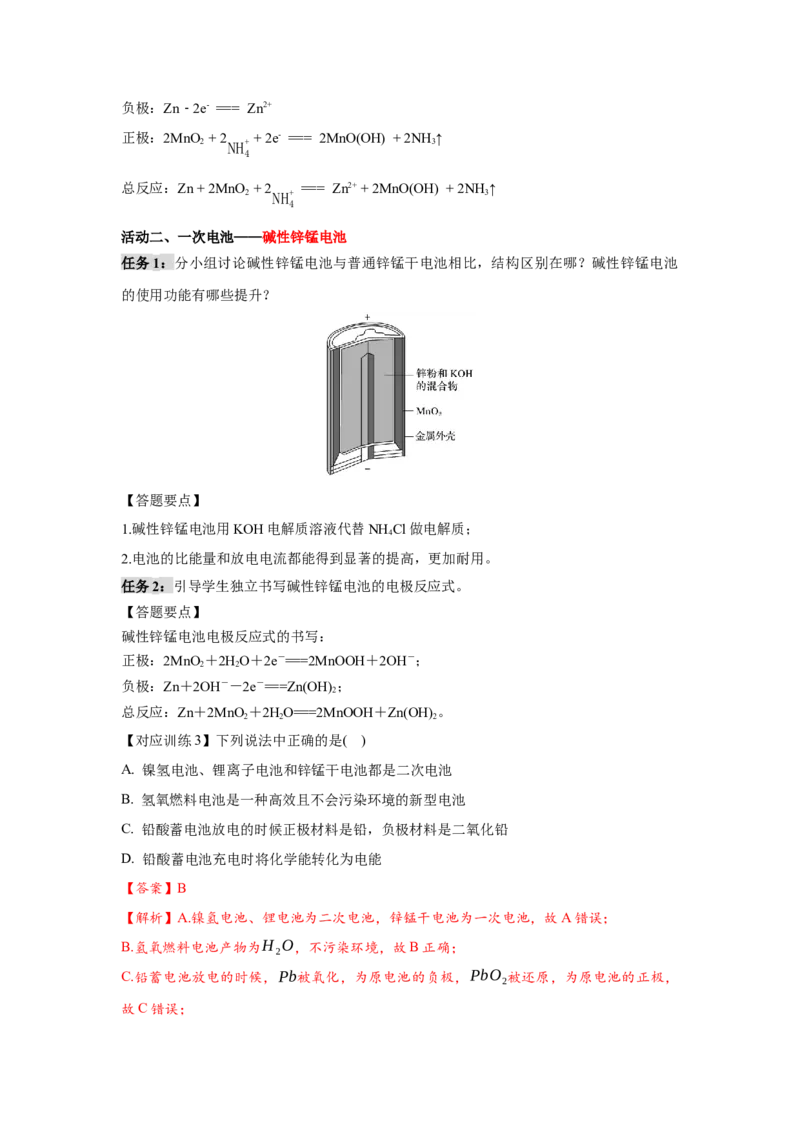
任务1:分小组讨论碱性锌锰电池与普通锌锰干电池相比,结构区别在哪?碱性锌锰电池
的使用功能有哪些提升?
【答题要点】
1.碱性锌锰电池用KOH电解质溶液代替NH Cl做电解质;
4
2.电池的比能量和放电电流都能得到显著的提高,更加耐用。
任务2:引导学生独立书写碱性锌锰电池的电极反应式。
【答题要点】
碱性锌锰电池电极反应式的书写:
正极:2MnO +2HO+2e-===2MnOOH+2OH-;
2 2
负极:Zn+2OH--2e-===Zn(OH) ;
2
总反应:Zn+2MnO +2HO===2MnOOH+Zn(OH) 。
2 2 2
【对应训练3】下列说法中正确的是( )
A. 镍氢电池、锂离子电池和锌锰干电池都是二次电池
B. 氢氧燃料电池是一种高效且不会污染环境的新型电池
C. 铅酸蓄电池放电的时候正极材料是铅,负极材料是二氧化铅
D. 铅酸蓄电池充电时将化学能转化为电能
【答案】B
【解析】A.镍氢电池、锂电池为二次电池,锌锰干电池为一次电池,故A错误;
B.氢氧燃料电池产物为H O,不污染环境,故B正确;
2
C.铅蓄电池放电的时候,Pb被氧化,为原电池的负极,PbO 被还原,为原电池的正极,
2
故C错误;D.铅蓄电池充电时是将电能转化为化学能,故D错误;
三、二次电池(铅酸蓄电池)
活动一、阅读课本,熟悉二次电池的概念,了解铅酸蓄电池的工作原理。。
任务1:阅读课本,总结二次电池的概念,并举例生活常见的二次电池。
【答题要点】
1.二次电池又称可充电电池或蓄电池,放电后可以再充电使活性物质获得再生,是一类放
电后可以再充电而反复使用的电池。
2.生活中可以手机电池,笔记本电池以及汽车发动机的使用电池均属于二次电池。
任务2:分小组讨论铅酸蓄电池的构成,并判断正负极。
【答题要点】
1.铅酸蓄电池的构成;
铅酸蓄电池是一种常见的二次电池,深灰色所示的正极板,板上覆盖有二氧化铅。浅灰色
所示的负极板上覆盖有铅单质。硫酸作为电解质溶液。
2.正负极分判断:铅蓄电池是最常见的二次电池,负极材料是Pb,正极材料是PbO 。
2
任务3:老师引导学生思考铅酸蓄电池的工作原理的充放电规律。
【老师总结】
1.二次电池的充电规律
a.充电时电极的连接:充电的目的是使电池恢复其供电能力,是原电池的逆反应,因此负
极应与电源的负极相连得电子,称阴极,正极接电源的正极后作阳极。
b.工作时的电极反应式:同一电极上的电极反应式,在充电与放电时,形式上恰好是相反
的;同一电极周围的溶液,充电与放电时pH的变化趋势也恰好相反。
2.图解二次电池的的工作原理
任务4:小组讨论铅酸蓄电池的电极反应式,并总结书写电极反应式的方法。
【答题要点】
1.电极反应式的书写
①放电时的反应
负极:Pb(s)+SO(aq)-2e-===PbSO(s);
4
正极:PbO (s)+4H+(aq)+SO(aq)+2e-===PbSO(s)+2HO(l)。
2 4 2总反应式:Pb(s)+PbO (s)+2HSO (aq) ==2PbSO (s)+2HO(l)
2 2 4 4 2
②充电时的反应
阴极:PbSO+2e-===Pb+ SO2- ;
4 4
阳极:PbSO+2HO-2e-===PbO+4H++ SO2-
4 2 2 4
总反应:2PbSO + 2HO === Pb + PbO +4H+ +
2SO2-
4 2 2 4
【总结】铅酸蓄电池是二次可充电电池,引导学生熟悉铅酸蓄电池的整体工作原理的总反应式。
Pb(s)+PbO (s)+2HSO (aq) 2PbSO (s)+2HO(l)
2 2 4 4 2
2. 二次电池电极反应式的书写方法
a.标:先标出原电池总反应式电子转移的方向和数目,找出参与负极和正极反应的物质。
b.写:写出一个比较容易书写的电极反应式(书写时一定要注意电极产物是否与电解质溶液
共存)
c.减:在电子守恒的基础上,总反应式减去写出的电极反应式即得另一电极反应式。
充电时的电极反应与放电时的电极反应过程相反。
【对应训练4】下列关于铅蓄电池的说法中正确的是( )
A.在放电时,正极发生的反应是Pb+SO2-=PbSO+2e-
4 4
B.在放电时,该电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是PbSO +2e-=Pb+ SO 2-
4 4
【答案】B
【解析】A 项,电池放电时正极发生还原反应,电极反应为 PbO +4H++2e-+SO2-
2 4
=PbSO+2H O;C项,电池充电时硫酸的浓度应不断增大;D项,电池充电时阳极应发生
4 2
氧化反应。
活动二、锂电池半自主学习
任务1:生活中熟悉的手机电池,笔记本电池均属于锂电池,分小组展开讨论,并总结锂
电池的优势及工作原理。
【答题要点】
老师投屏给出:转移1mol电子时,消耗金属的质量图
Li的摩尔质量是7g/mol,当转移1mol的电子时需要锂的质量7g,和其他金属比较,有着电池
质量小、体积小、储存和运输能量大优点。
任务2:根据二次电池电极反应式的书写方法,让学生自主写出锂电池的放电的电极反应式。
【答题要点】
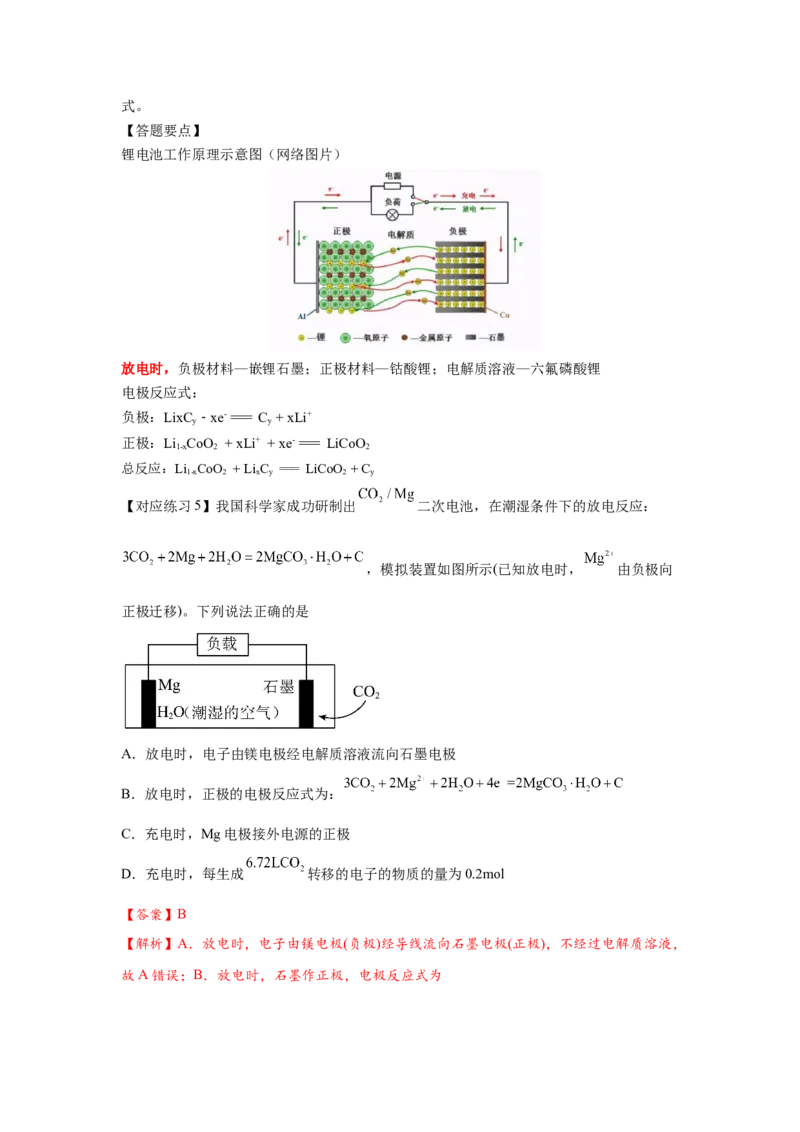
锂电池工作原理示意图(网络图片)
放电时,负极材料—嵌锂石墨;正极材料—钴酸锂;电解质溶液—六氟磷酸锂
电极反应式:
负极:LixC ﹣xe- === C + xLi+
y y
正极:Li CoO + xLi+ + xe- === LiCoO
1-x 2 2
总反应:Li CoO + LiC === LiCoO + C
1-x 2 x y 2 y
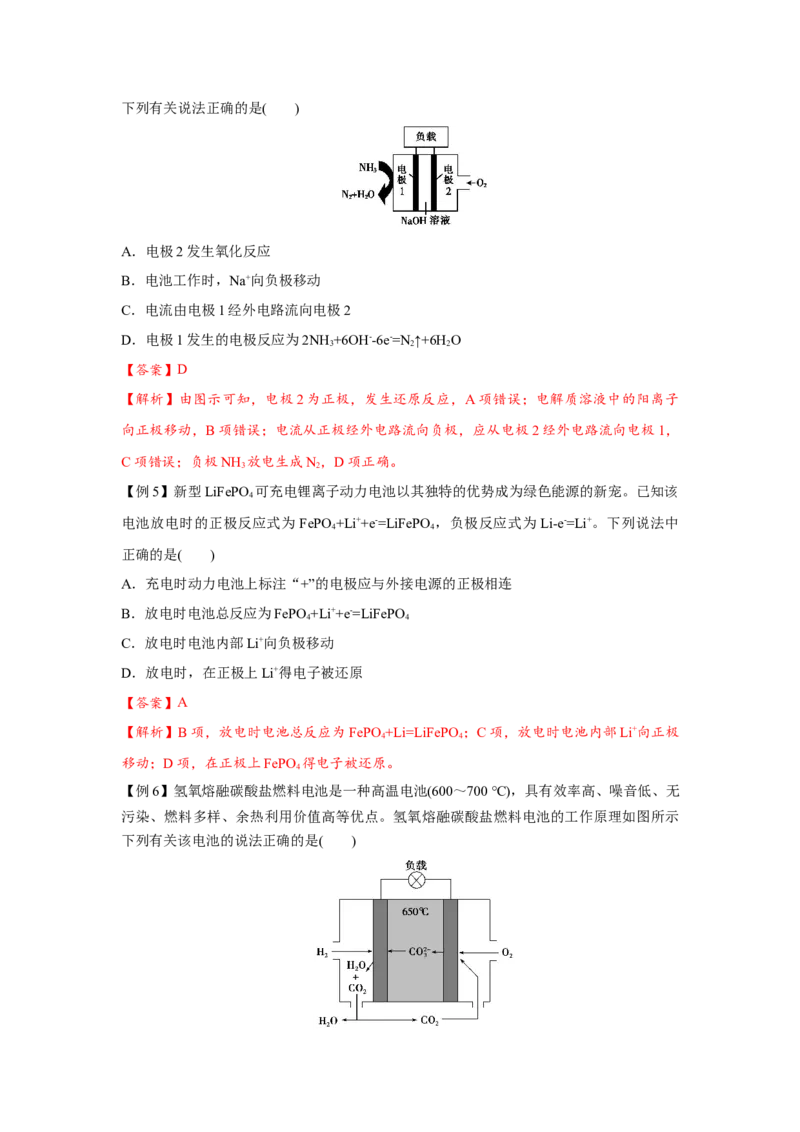
【对应练习5】我国科学家成功研制出 二次电池,在潮湿条件下的放电反应:
,模拟装置如图所示(已知放电时, 由负极向
正极迁移)。下列说法正确的是
A.放电时,电子由镁电极经电解质溶液流向石墨电极
B.放电时,正极的电极反应式为:
C.充电时,Mg电极接外电源的正极
D.充电时,每生成 转移的电子的物质的量为0.2mol
【答案】B
【解析】A.放电时,电子由镁电极(负极)经导线流向石墨电极(正极),不经过电解质溶液,
故A错误;B.放电时,石墨作正极,电极反应式为,故B正确;C.充电时,Mg作阴极,连接
电源的负极,故C错误;D.题目未给标准状况,无法使用22.4L/mol计算气体的物质的量,
故D错误;故答案选B。
四、燃料电池
活动一、讲解实现氢气与氧气反应将化学能转化为电能的过程
任务1:思考讨论氢氧燃料电池的构成条件
【答题要点】一般用酸溶液或碱溶液作电解质溶液,以Pt作电极,负极室通入氢气,正极
室通入氧气,用导线外接用电器形成闭合回路,即可实现化学能转化为电能。
任务2:氢氧燃料电池是目前最成熟的燃料电池,可分为酸性和碱性两种,引导学生书写
不同环境下的氢氧燃料电池的电极反应式。
【答题要点】
1.酸性条件:
负极: 2H - 4e- === 4H+ 正极:O + 4H+ + 4e- === 2H O
2 2 2
总反应:2H +O === 2H O
2 2 2
2.碱性条件:
负极:2H +4OH- - 4e- === 4H O 正极:O +2HO + 4e- === 4OH-
2 2 2 2
总反应:2H +O === 2H O
2 2 2
任务3:根据氢氧燃料电池的工作原理,书写甲烷燃料电池的电极反应式。
【答题要点】
1.酸性条件
负极:CH-8e-+2H O=CO+8H+
4 2 2
正极:O+4e-+4H+=2H O
2 2
总反应:CH+2O =CO +2H O
4 2 2 2
2.碱性条件
负极:CH-8e-+10OH-=CO 2-+7H O
4 3 2
正极:O+4e-+2H O=4OH-
2 2
总反应:CH+2O +2OH-=CO 2-+3H O
4 2 3 2【对应训练6】燃料电池是利用燃料(如CO、H 、CH 等)与氧化剂反应,将反应物的化学
2 4
能转化为电能的装置,通常用氢氧化钾作电解质。回答下列问题:
(1)已知某燃料电池的总反应为CH+2O +2KOH=K CO+3H O,电池中有一极的电极反应式
4 2 2 3 2
为CH+10OH--8e-=CO 2-+7H O,该电极是燃料电池的 (填“正”或“负”)极,另
4 3 2
一个电极上的电极反应式为 。
(2)随着电池不断放电,电解质溶液的碱性逐渐 (填“增强”“减弱”或“不变”)
(3)通常情况下,甲烷燃料电池的能量利用率 (填“大于”“小于”或“等于”)甲烷
燃烧的能量利用率。
【答案】(1)负 4HO+2O+8e-=8OH- (2)减弱 (3)大于
2 2
【解析】(1)根据电极反应式可知,甲烷失去电子,作电池的负极,正极反应式可以用电池
总反应式减去负极反应式得到。(2)从电池总反应可知反应过程消耗KOH,所以溶液的碱性
减弱。
课 后 作 业 练 习
【例1】 下列有关电池的说法错误的是( )
A.手机中用的锂离子电池属于二次电池
B.甲醇燃料电池可把化学能转化为电能
C.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
D.铅蓄电池使用一段时间后,电解质溶液的酸性减弱,导电能力下降
【答案】C
【解析】A项,手机中用的锂离子电池是一类放电后可以再充电而反复使用的电池,属于
二次电池,A正确;B项,甲醇燃料电池是一种连续的将燃料和氧化剂的化学能直接转化
为电能的化学电源,B正确;C项,铜锌原电池工作时,锌为负极,铜为正极,电子沿外
电路从负极锌流向正极铜,C错误;D项,铅蓄电池使用一段时间后电解质硫酸消耗,酸
性减弱,导电能力下降,D正确;故选C。
【例2】下列有关装置的说法正确的是A. 装置Ⅰ中Mg为原电池的负极
B. 装置Ⅱ为一次电池
C. 装置Ⅲ可构成原电池
D. 装置Ⅳ工作时,电子由锌通过导线流向碳棒
【答案】D
【解析】
A.镁与氢氧化钠溶液不反应,铝能够与氢氧化钠溶液反应,装置Ⅰ中铝为负极,镁为正极,
故A错误;
B.铅蓄电池是二次电池,可以放电充电,故B错误;
C.装置Ⅲ中的两个材料相同、都是Zn,不能构成原电池,故C错误;
D.装置Ⅳ为干电池,锌为负极,碳棒为正极,工作时,原电池中电子由负极沿导线流向正
极,因此电子由锌通过导线流向碳棒,故D正确。
【例 3】微型纽扣电池在现代生活中有广泛应用,有一种锌银电池,其总反应为
Ag O+Zn+H O=Zn(OH) +2Ag。下列叙述中正确的是( )。
2 2 2
A.在使用过程中,电池负极区溶液的pH逐渐增大
B.在使用过程中,电子由Ag O经外电路流向Zn
2
C.Zn是负极,Ag O是正极
2
D.Zn发生还原反应,Ag O发生氧化反应
2
【答案】C
【解析】根据电池反应可知,Zn失电子被氧化,Ag O得电子被还原,故Zn是负极,Ag O
2 2
是正极;负极在反应时消耗OH-,则负极区溶液的pH应逐渐减小;原电池工作时,电子由
负极经外电路流向正极,即电子由Zn经外电路流向Ag O;在原电池中,负极发生氧化反
2
应,正极发生还原反应。
【例4】瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池的工作原理如图所示,下列有关说法正确的是( )
A.电极2发生氧化反应
B.电池工作时,Na+向负极移动
C.电流由电极1经外电路流向电极2
D.电极1发生的电极反应为2NH +6OH--6e-=N ↑+6H O
3 2 2
【答案】D
【解析】由图示可知,电极2为正极,发生还原反应,A项错误;电解质溶液中的阳离子
向正极移动,B项错误;电流从正极经外电路流向负极,应从电极2经外电路流向电极1,
C项错误;负极NH 放电生成N,D项正确。
3 2
【例5】新型LiFePO 可充电锂离子动力电池以其独特的优势成为绿色能源的新宠。已知该
4
电池放电时的正极反应式为 FePO +Li++e-=LiFePO ,负极反应式为Li-e-=Li+。下列说法中
4 4
正确的是( )
A.充电时动力电池上标注“+”的电极应与外接电源的正极相连
B.放电时电池总反应为FePO +Li++e-=LiFePO
4 4
C.放电时电池内部Li+向负极移动
D.放电时,在正极上Li+得电子被还原
【答案】A
【解析】B项,放电时电池总反应为FePO +Li=LiFePO ;C项,放电时电池内部Li+向正极
4 4
移动;D项,在正极上FePO 得电子被还原。
4
【例6】氢氧熔融碳酸盐燃料电池是一种高温电池(600~700 ℃),具有效率高、噪音低、无
污染、燃料多样、余热利用价值高等优点。氢氧熔融碳酸盐燃料电池的工作原理如图所示
下列有关该电池的说法正确的是( )A.电池工作时,熔融碳酸盐只起到导电的作用
B.负极反应式为H-2e-+CO===CO +HO[来源:学#科#网Z#X#X#K]
2 2 2
C.该电池可利用工厂中排出的CO,减少温室气体的排放
2
D.电池工作时,外电路中流过0.2 mol电子,消耗3.2 g O
2
【答案】B
【解析】根据图示,在氢氧熔融碳酸盐燃料电池中,通入氢气的电极为负极,负极发生氧
化反应,电极反应式为H -2e-+CO===CO +HO,通入氧气的电极为正极,正极发生还
2 2 2
原反应,电极反应式为O +2CO +4e-===2CO,总反应为2H +O===2H O。根据上述分
2 2 2 2 2
析,电池工作时,熔融碳酸盐参与了电极反应,故A错误;负极发生氧化反应,电极反应
式为H -2e-+CO===CO +HO,故B正确;根据总反应,该电池工作时没有消耗二氧化
2 2 2
碳,不能减少温室气体的排放,故C错误;电池工作时,外电路中流过0.2 mol电子,消耗
0.5 mol氧气,质量为16 g O,故D错误。
2
【例7】.下列有关四个常用电化学装置的叙述中,正确的是
图Ⅰ碱性锌锰电池 图Ⅱ铅蓄电池 图Ⅲ 图Ⅳ氢氧燃料电池
A. 图Ⅰ所示电池中,MnO 是正极,电极反应式是2H O+2e-=H ↑+2OH-
2 2 2
B. 图Ⅱ所示电池放电过程中,当外电路通过1mol电子时,理论上负极板的质量增加96g
C. 图Ⅲ所示装置没有形成原电池
D. 图Ⅳ所示电池中,不管KOH溶液换成H SO 溶液还是Na SO 溶液,电池总反应式
2 4 2 4
不变
【答案】D
【解析】A.图Ⅰ所示电池中,正极上MnO 得电子发生还原反应,电极反应式是:
2
MnO +H O+e-=MnO(OH)+OH- ,故A错误;
2 2
B. 图 Ⅱ 所 示 电 池 放 电 过 程 中 , 当 外 电 路 通 过 1mol电 子 时 , 负 极 反 应
Pb-2e-+SO2-=PbSO ,理论上负极板增加的的质量(是0.5mol的硫酸根的质量)即增加
4 4
48g,故B错误;C.图Ⅲ所示装置满足原电池形成条件,形成了原电池 ,故C错误;
D.图Ⅳ所示电池中,不管KOH溶液换成H SO 溶液还是Na SO 溶液,电池总反应式都
2 4 2 4
为:2H +O =2H O,故D正确。
2 2 2
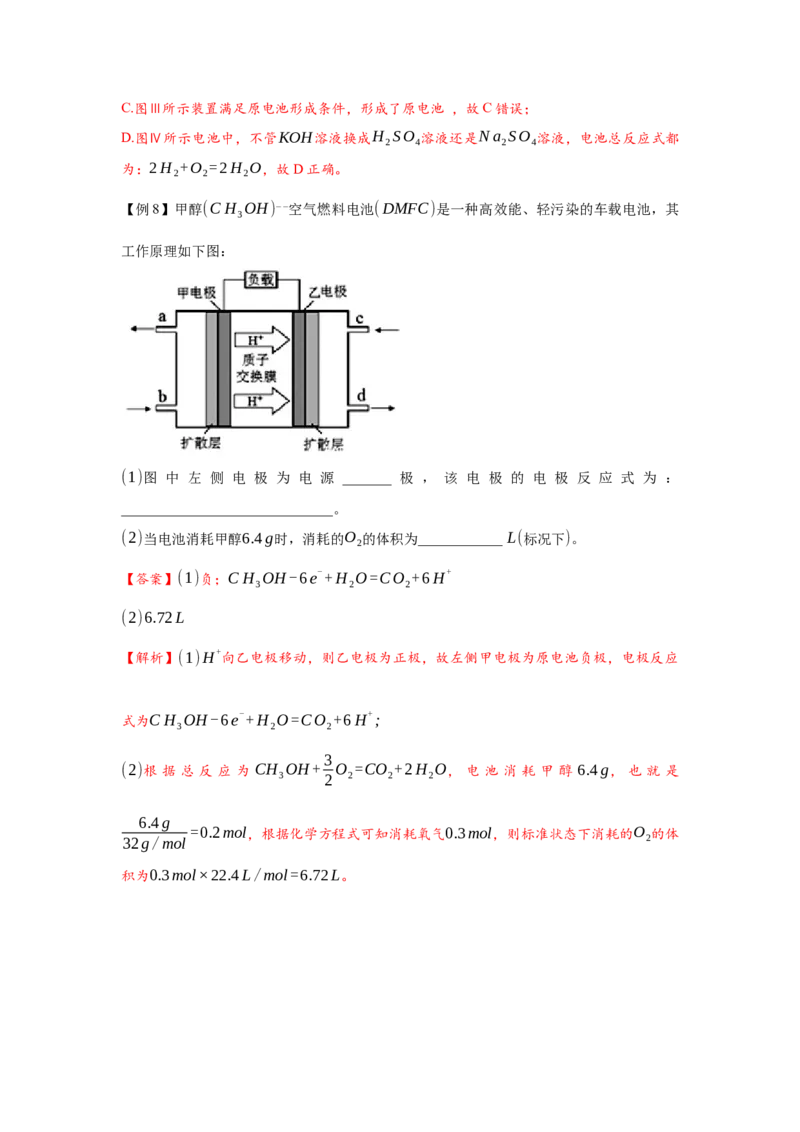
【例8】甲醇(CH OH) __ 空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其
3
工作原理如下图:
(1)图 中 左 侧 电 极 为 电 源 _______ 极 , 该 电 极 的 电 极 反 应 式 为 :
______________________________。
(2)当电池消耗甲醇6.4g时,消耗的O 的体积为____________ L(标况下)。
2
【答案】(1)负;CH OH-6e-+H O=CO +6H+
3 2 2
(2)6.72L
【解析】(1)H+
向乙电极移动,则乙电极为正极,故左侧甲电极为原电池负极,电极反应
式为CH OH-6e-+H O=CO +6H+;
3 2 2
3
(2)根 据 总 反 应 为 CH OH+ O =CO +2H O, 电 池 消 耗 甲 醇 6.4g, 也 就 是
3 2 2 2 2
6.4g
=0.2mol,根据化学方程式可知消耗氧气0.3mol,则标准状态下消耗的O 的体
32g/mol 2
积为0.3mol×22.4L/mol=6.72L。