文档内容
第四章 物质结构 元素周期律
第一节 原子结构与元素周期表
第二课时 元素周期表 核素、同位素
【学习目标】1.通过阅读教材、讨论交流,了解核素、同位素的含义,认识同位素在生产、生活中的
应用,初步学会利用各概念之间的关系解答有关问题。
2.通过对元素周期表发现史资料的收集整理、交流汇报,了解元素周期表的形成过程,并能运用归
纳、概括等方法对信息进行加工,体验科学探究的过程,进一步学习科学探究的方法。
3.通过阅读教材、归纳总结,知道周期和族的概念,会描述元素周期表的结构,知道元素在周期表
中的位置与原子结构的关系,初步学会推导元素在周期表中的位置的基本方法。
【学习重点】元素周期表的结构,核素、同位素的概念
【学习难点】元素周期表中元素的排列与原子核外电子排布的关系
【课前预习】
旧知回顾:1.原子序数是元素在元素周期表中的顺序,原子序数与元素的原子结构之间存在如下的关
系: 原子序数 = 核电荷数 = 质子数 = 核外电子数 。
2.在多电子的原子里,原子的核外电子在不同的区域运动,将这些不同的区域简化为 电子层 。离核
较近的 电子层 中的电子能量 低 ,由内向外分别用 K 、 L 、 M 、 N 、 O 、 P 、 Q 来表示。
新知预习:1.元素周期表的编排原则:按 原子序数 递增的顺序从左到右排列,把 电子层数 相同的
元素排成一横行。把不同横行中 最外层电子数相同 相等的元素,按 电子层数递增 递增的顺序从上到下
排成一纵行。
2.元素周期表的结构:周期表中有 7 个横行,叫做周期。周期的序数就是该周期元素的原子具有的
电子 层数 。第一、二、三周期称为 短周期 ;四、五、六、七周期称为 长周期 。周期表有 1 8 个纵
行,称为族,主族元素的族序数后标 A ,副族元素的族序数后标 B 。第8、9、10三纵行称为第Ⅷ族,
第18纵行称为0族。
【课中探究】
情景导入:历史上,为了寻求各种元素及其化合物间的内在联系核规律性,人们进行了许多尝试。
1869年俄国化学家门捷列夫绘制出第一张元素周期表是化学科学发展中一个重要的里程碑。118号元素发
现之后,科学界一直在讨论一个问题,元素周期表第七周期已经被填满,是否证明所有化学元素已经被集
齐了呢?(见PPT视频)
一、元素周期表
活动一、元素周期表的发展历程
任务一、阅读教材P98页“科学史话”,思考元素周期表的发展历程有哪些?完成表格内容。【答案要点】
诞生 1869年,俄国化学家门捷列夫编制出第一张元素周期表
编制 将元素按照相对原子质量由小到大依次排列,并将化学性质相似的元素放在一起
意义 揭示了元素间的内在联系,成为化学发展史上的重要里程碑之一
演变 元素周期表中为未知元素留下的空位先后被填满
现行 排序依据由相对原子质量改为原子的核电荷数
任务二、讨论交流:阅读教材P94页内容,思考现行元素周期表的编排原则是什么?
【答案要点】①原子序数:按照元素在周期表中的顺序给元素编号;原子序数=核电荷数=质子数=
核外电子数。
②元素周期表中元素的排列方式:将电子层数相同的元素按照原子序数递增的顺序由左向右排成横
行,再把不同横行中最外层电子数相同的元素,按电子层数递增的顺序由上向下排成纵列。
【对应练习】1.下列说法中不正确的是( )
A.元素的原子序数等于核电荷数
B.元素所在周期序数等于该元素原子的电子层数
C.元素原子的质子数等于核外电子数
D.元素所在周期序数等于该元素原子的最外层电子数
【答案】D
【解析】A.在原子中质子数=核电荷数=原子序数,所以元素的原子序数等于核电荷数,故A正确;
B.原子核外有几个电子层,该元素就位于第几周期,即元素所在周期序数等于该元素原子的电子层数,
故B正确;C.原子呈电中性,则原子中质子数=核外电子数,故C正确;D.元素所在周期序数等于该元
素原子的电子层数,主族元素的族序数等于最外层电子数,故D错误;故答案选D。
2.任何科学真理的发现,都不是一帆风顺的,门捷列夫的元素周期表奠定了现代化学和物理学的理
论基础。下列关于元素周期表的叙述正确的是( )
A.周期表中有7个主族、8个副族
B.目前使用的元素周期表中,最长的周期含有32种元素
C.短周期元素是指1~20号元素
D.原子的最外层电子数都等于该元素所在的族序数
【答案】B
【解析】A.周期表中有7个主族、7个副族,A错误;B.目前使用的元素周期表中,最长的周期为
第六周期,含有32种元素,B正确;C.短周期元素是指第一、二、三周期的元素,即1~18号元素,C错
误;D.主族元素的原子,原子的最外层电子数等于该元素所在的族序数,D错误;故选B。
活动二、探究元素周期表的结构
任务一、观察元素周期表,结合教材P95页“思考与讨论”,思考周期序数与原子核外电子排布有何
关系?完成表格内容。
【答案要点】①周期序数与原子核外电子排布的关系:
周期序数 起止元素 包括元素种数 核外电子层数1 H~He 2 1
2 Li~Ne 8 2
3 Na~Ar 8 3
4 K~Kr 18 4
5 Rb~Xe 18 5
6 Cs~Rn 32 6
7 Fr~Og 32 7
②结论:由上得到元素的周期序数等于原子核外电子层数。元素周期表的前三周期统称为短周期,其
余周期统称为长周期。显然短周期元素就是指前18号元素。
任务二、讨论交流:观察元素周期表,思考元素周期表的结构(周期、族)有何特点?完成表格内
容。
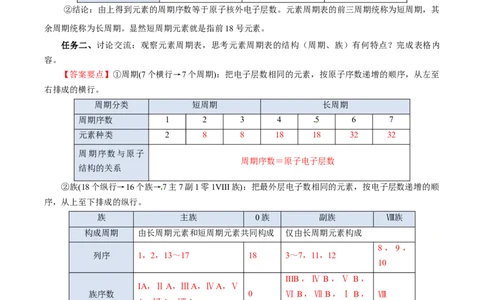
【答案要点】①周期(7个横行→7个周期):把电子层数相同的元素,按原子序数递增的顺序,从左至
右排成的横行。
周期分类 短周期 长周期
周期序数 1 2 3 4 5 6 7
元素种类 2 8 8 18 18 32 32
周期序数与原子
周期序数=原子电子层数
结构的关系
②族(18个纵行→16个族→7主7副1零1Ⅷ族):把最外层电子数相同的元素,按电子层数递增的顺
序,从上至下排成的纵行。
族 主族 0族 副族 Ⅷ族
构成周期 由长周期元素和短周期元素共同构成 仅由长周期元素构成
8,9,
列序 1,2,13~17 18 3~7,11,12
10
ⅢB,Ⅳ B,Ⅴ B,
ⅠA,ⅡA,ⅢA,ⅣA,Ⅴ
族序数 0 Ⅵ B,Ⅶ B,Ⅰ B, Ⅷ
A,ⅥA,ⅦA
ⅡB
族序数与原子 主族序数=原子最外层电
结构关系 子数
第ⅠA族(除氢):碱金属元素;第ⅦA族:卤族元素;0族:稀有气体元
常见族的别称
素
③同周期相邻主族元素的原子序数之差。
周期 ⅡA ⅢA
2、3 n n+14、5 n n+11
6、7 n n+25
任务三、问题探究:元素周期表还有哪些其它表现特征?
【答案要点】①元素周期表中的方格中的符号的意义:
②元素周期表的特殊位置:
A.过渡元素:元素周期表中从ⅢB族到ⅡB族10列元素,都是金属元素。
B.镧系:元素周期表第六周期第ⅢB族中,从57号元素到71号元素共15种元素。
C.锕系:元素周期表第七周期第ⅢB族中,从89号元素到103号元素共15种元素。
D.ⅡA , ⅢA不紧邻,最外层电子为1—2的不一定是ⅠA 、 ⅡA主族,也可能是过渡元素。
【对应练习】1.下列关于元素周期表的叙述正确的是( )
A.元素周期表揭示了化学元素间的内在联系,是化学发展史上的重要里程碑之一
B.元素所在的周期数等于它的电子层数,所在的族序数等于它的最外层电子数
C.元素周期表有7个横行即7个周期,18个纵列即18个族
D.某种元素的相对原子质量取整数值,就是其原子序数
【答案】A
【解析】A.门捷列夫研制出的元素周期表,不仅揭示了元素间的内在联系和变化规律,也为发现新
元素及探究物质的用途提供了依据,其价值非凡,A正确;B.周期数=电子层数,主族序数=最外层电子
数,对于副族及第Ⅷ族元素,族序数不一定等于相应原子的最外层电子数,B错误;C.元素周期表中的
8、9、10三个纵列合在一起叫做第Ⅷ族,故共有16个族,C错误;D.元素的原子序数等于元素的核电荷
数或对应原子的质子数,D错误;故选A。
2.2018年IUPAC(国际纯粹与应用化学联合会)制作了新版周期表,包含118种元素。下列有关元素周
期表说法正确的是( )
A.元素周期表中只有第ⅡA元素原子最外层电子数为2
B.元素周期表有18个族
C.第ⅠA族的元素全部是金属元素
D.元素周期表中含元素种类最多的族是第ⅢB族
【答案】D
【解析】A.He最外层有2个电子,但属于稀有气体元素,在0族,故A错误;B.元素周期表有7
个主族、7个副族、1个0族和1个VIII族,共16个族,故C错误;C.第ⅠA族的H元素是非金属,故
C错误;D.元素周期表中含元素种类最多的族为ⅢB族,含锕系和镧系元素,故D正确。故选D。
3.下列关于过渡元素及其单质的说法正确的是( )
A.过渡元素包括12列元素B.过渡元素中既含有金属元素,也含非金属元素
C.所有的过渡元素的单质都具有良好的导电性
D.过渡金属元素的单质比较稳定,与空气和水不发生反应
【答案】C
【解析】A.过渡元素包括第3~12列共10列元素,故A错误;B.过渡元素中只含有金属元素,不含
非金属元素,故B错误;C.过渡元素中只含有金属元素,单质都具有良好的导电性,故C正确;D.多
数过渡金属元素的单质比较稳定,与空气和水反应缓慢或不发生反应,故D错误;选C。
二、核素 同位素
活动一、元素和核素
任务一、阅读教材P96页内容,观察表4-1,思考核素和元素的定义是什么?
1 H2 H
【答案要点】①核素:具有一定数目质子和一定数目中子的一种原子,其符号为 X。例如:1 1
3 H
1 都是氢元素的不同核素。决定核素种类的是质子数与中子数,与核外电子无关。
②元素:具有相同质子数(核电荷数)和不同中子数的一类原子的总称。决定元素种类的是质子数,与
中子数和核外电子无关。
任务二、根据教材P96页表4-1,回答氢元素的三种核素有核特点?完成表格内容。
【答案要点】①氢元素的三种核素比较:
原子 氢元素的原子核
原子符号(X)
名称 质子数(Z) 中子数(N)
氕 H
氘 H或D
氚 H或T
②结论:元素周期表中涉及的元素有118种,但核素多于118种。并不是所有原子均有中子数,氕无
中子。
【对应练习】1.核素是具有一定数目质子和一定数目中子的一种原子。下列说法错误的是( )
A.H、H、H+和H 是氢元素的四种不同粒子
2
B.Ca和Ca、石墨和金刚石均为同素异形体
C.H和H是不同的核素
D.12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同
【答案】B
【解析】A项中的四种微粒是氢元素的四种不同粒子,H和H是质子数均为1,中子数不等的不同的
氢原子,它们是不同的核素,12C和14C由于其质子数均为6,而中子数分别为6和8,故它们互为同位素,
同理,Ca和Ca也互为同位素,其物理性质不同,但化学性质几乎完全相同;金刚石与石墨是由碳元素组
成的不同的单质,它们互为同素异形体。
2.美国夏威夷联合天文中心的科学家发现了新型氢微粒,这种新粒子是由3个氢原子核(只含质子)和2个电子构成,对于这种微粒,下列说法正确的是( )
A.该微粒为电中性 B.它是氢元素的一种新的核素
C.它的化学式为H D.它比一个普通H 分子多一个氢原子核
3 2
【答案】D
【解析】A.这种氢粒子是由3个氢原子核(只含质子)和2个电子构成的,所以该粒子带一个单位
的正电荷,A错误;B.这种氢粒子是是由3个氢原子核(只含质子)和2个电子构成,故该离子为化学式为
H+,该微粒是一个离子,而不是原子,核素是一种原子,故不是氢元素的一种新的核素,B错误;C.这
3
种氢粒子是由3个氢原子核(只含质子)和2个电子构成,该微粒可表示为H+,C错误;D.普通氢分子
3
2个原子核,这种氢粒子是由3个氢原子核构成,它比一个普通H 分子多一个氢原子核,D正确;故答案
2
为:D。
活动二、探究同位素的概念、特点及用途
任务一、阅读教材P96-97页内容,结合“化学与职业”栏目,回答同位素的定义、特点是什么?有何
用途?
【答案要点】①概念:质子数相同而中子数不同的同一元素的不同原子互称为同位素(即同一元素的不
同核素互称为同位素),如H、H、H互为同位素。
②特点:同位素在元素周期表中占有相同的位置,化学性质几乎完全相同,物理性质略有差异;同一
元素的不同核素的中子数不同,质量数也不相同;天然存在的同位素,相互间保持一定的比率。
③用途:在考古工作中用于测定文物的年代;H、H用于制造氢弹;利用放射性同位素释放的射线育
种、给金属探伤、诊断和治疗疾病等。
任务二、讨论交流:元素、核素、同位素、同素异形体的区别与联系是什么,完成表格内容。
【答案要点】
元素 核素 同位素 同素异形体
质子数相同的一类 质子数、中子数都 质子数相同、中子 同种元素形成的不
本质
原子 一定的原子 数不同的核素 同单质
范畴 同类原子 原子 原子 单质
只有种类,没有个 化学反应中的最小 化学性质几乎完全 元素相同、性质不
特性
数 微粒 相同 同
决定因
质子数 质子数、中子数 质子数、中子数 组成元素、结构
素
H、H、H互称同 O 与O 互为同素
2 3
举例 H、C、O三种元素 H、H、H三种核素
位素 异形体
联系【对应训练】1.稀土有工业“黄金”之称。下列有关稀土元素 与 的说法不正确的是( )
A.元素Y的原子序数为39 B. 与 的性质相同
C.核素 的原子核内有52个中子 D. 与 互为同位素
【答案】B
【解析】A.原子序数=质子数,故元素Y的原子序数为39,A项正确;B. 与 互为同位素,
物理性质不同,B项错误;C. 指质子数为39,则中子数=91-39=52,C项正确;D. 指质子数为
39,中子数为51的Y原子, 指质子数为39,中子数为52的Y原子, 与 是两种不同的原子,互
为同位素,D项正确;答案选B。
2.2021年,“中国天眼”正式对全球开放,其“眼镜片”主要成分是高性能碳化硅新型材料,它能
探测到宇宙边缘的中性氢,重现宇宙早期图像。下列有关说法正确的是( )
A.其塔架所用钢材的组成元素都是金属元素
B.其射电板所用铝合金具有较强的抗腐蚀性
C.中性氢原子构成的氢气有三种同素异形体
D.硅位于元素周期表第三周期ⅥA族
【答案】B
【解析】A.钢材的组成元素除了铁元素外,还有碳元素,故A错误;B.铝合金表面有一层致密的
氧化膜,具有较强的抗腐蚀性,故B正确;C.同种元素组成的不同单质为同素异形体,中性氢原子构成
的氢气只有一种单质,故C错误;D.硅元素位于元素周期表第三周期ⅣA族,故D错误;答案B。
【课后巩固】1.下列有关元素周期表的说法中错误的是( )
A.元素原子的最外层电子数等于该元素所在的族序数
B.元素周期表中从ⅢB族到ⅡB族10个纵列的元素都是金属元素
C.除He外的所有稀有气体元素原子的最外层电子数都是8
D.ⅡA族与ⅢA族之间隔着10个纵列
【答案】A
【解析】A.只有主族元素原子的最外层电子数等于该元素所在的族序数,过渡元素的族序数大多等
于其价电子数,不是最外层电子数,选项A错误;B.元素周期表中从IIIB族到IIB族10个纵行的元素都
是过渡元素,过渡元素全部为金属元素,选项B正确;C.稀有气体元素原子中,只有氦原子的最外层电
子数为2,其余的均为8,选项C正确;D.ⅡA族、ⅢA族分别位于元素周期表的第2纵列和第13纵
列,即ⅡA族与ⅢA族之间隔着10个纵列(第3列~第12列),选项D正确;答案选A。
2.下列关于元素周期表的叙述正确的是( )
A.在元素周期表中共有18个纵行,18个族 B.同族元素的最外层电子数一定相同
C.同周期元素的电子层数相同 D.元素周期表有7个周期,8个主族【答案】C
【解析】A.周期表共有18个纵行,16个族,其中第Ⅷ族包括第8、9、10三个纵行,A项错误;B.
对于0族元素、副族元素及第Ⅷ族元素来说,同族元素原子的最外层电子数不一定相同,B项错误;C.
同周期元素具有相同的电子层数,C项正确;D.元素周期表有7个周期,7个主族,D项错误;答案选
C。
3.已知X、Y、Z三种主族元素在元素周期表中的位置如图所示。设 X的原子序数为a,则下列说法不
正确的是( )
Y
X
Z
A.Y的原子序数可能为a-17 B.Y与Z的原子序数之和可能为2a
C.Z的原子序数可能为a+31 D.X、Y、Z可能均为短周期元素
【答案】D
【解析】A.若Y为第三周期元素,则 X、Z分别为第四、五周期元素,X的原子序数为a,则Y的
原子序数为a-17,A正确;B.若Y为第三周期元素,则 X 、Z分别为第四、五周期元素,X的原子序数
为a,则Y的原子序数为 a-17,Z的原子序数为a+17,则Y与乙的原子序数之和为2a,B正确;C.若 Y
为第四周期元素,则 X、Z分别为第五、六周期元素,X 的原子序数为a,则Y的原子序数为a-17,Z的
原子序数为a+31,C正确;D.由图中X、Y、Z三种主族元素在周期表中的相对位置可知,X、Y、Z三
种主族元素处于过渡元素右侧,Y 不可能是第一周期元素,则Z一定处于长周期,D错误; 故选D。
4.元素M、R形成的简单离子M2-与R+的核外电子数之和为20,下列说法正确的是( )
A.M原子的质子数一定大于R原子的质子数
B.M可能存在16M、18M两种核素
C.M2-与R+的电子层结构不可能相同
D.两种离子结合可形成MR型化合物
【答案】B
【解析】从离子的核外电子数之和为20,可推出M、R两种原子的质子数之和为19,则R为Na、M
为O或R为Li、M为S,以此来解答。A.若M为O,R为Na,O的质子数为8小于Na的为11,A错
误;B.氧元素含有16O、17O和18O三种核素,若M为O时则成立,B正确;C.若M为O,R为Na,则
O2-和Na+均具有10电子,具有相同的电子层结构,C错误;D.简单离子M2-与R+形成的化合物为MR ,
2
不可能为MR型化合物,D错误;故答案为:B。
5.钷 广泛用于量规、光电池等。 的最外层电子数是2,下列说法不正确的是( )
A. 的原子核外有61个电子 B. 与 互为同位素
C. 属于金属元素 D. 的中子数为147【答案】D
【解析】A.原子的质子数等于核外电子数,故 的原子核外有61个电子,故A正确;B. 与
的质子数相同、中子数不同,故互为同位素,故B正确;C. 属于金属元素,故C正确;D.
的中子数为147-61=86,故D错误;故选D。
6.13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,Kurt等人由此
获得2002年诺贝尔化学奖。下面有关13C、15N叙述正确的是( )
A.13C与15N有相同的中子数 B.13C 与12C 互为同素异形体
60 60
C.13C与14C的性质完全相同 D.14N与15N互为同位素
【答案】D
【解析】A.13C与15N的中子数分别为7、8,A错误;B.同素异形体是同一种元素形成的不同的单
质,因排列方式而具有不同性质的的单质,13C 与12C 的排列相同,B错误;C.13C与14C互为同位素,
60 60
化学性质基本一样,物理性质不同,C错误;D.同位素具有相同的质子数不同的中子数核素的互称,14N
与15N质子数都是7,中子数分别为7、8,D正确;故选D。
7.某位同学为1~18号元素设计了一种扇形图(如下图),其实就是目前仍在使用的扇形周期表的一部
分,下列有关说法不正确的是( )
A.每个小扇区就是长式周期表的一个族
B.此扇形周期表中只显示了三个周期
C.扇形周期表拆下扇子顶螺丝可以转换为现行的长式周期表
D.扇形周期表考虑镧系和锕系应有九个周期
【答案】D
【解析】A.第一个小扇区表示H、Li、Na,最外层电子相同,为一个族,Be和Mg最外层电子数相
同,也为一个族,同理类推,每个小扇区就是长式周期表的一个族,A正确;B.由元素在扇形周期表中
的位置可知,H和He位于第一周期,Li、Be、B、C、N、O、F、Ne位于第二周期,Na、Mg、Al、Si、
P、S、Cl、Ar位于第三周期,此扇形周期表中只显示了三个周期,B正确;C.扇形周期表拆下扇子顶螺
丝后可观察到有三个横行,为三个周期,8个竖行,为八个主族,故可以转换为现行的长式周期表的一部
分,C正确;D.元素周期表有7个周期,其中镧系元素属于第六周期,是第IIB族, 锕系元素属于第七
周期,也是第IIB族,D错误;故选D。
8.下表标出的是元素周期表的一部分元素,回答下列问题:(1)属于第二周期元素的有_______、__________、________ (填元素符号), 属于第ⅢA 族的有
________(填元素符号),属于第 IA 族的有__________ 、_______(填元素符号)。
(2)C 元素在元素周期表中的位置是第_____周期第____族。B 元素在元素周期表中的位置是第_____
周期第____族。
【答案】C O F Al Na K 3 VA 2 ⅥA
【解析】根据元素在周期表中的分布,A是F,B是O,C是P,D是C,E是Ar,F是Cl, G是S,
H是P,I是Mg,J是Na,K是Ca,L是K,M是过渡金属元素,N是Br,结合元素周期表的结构分析解
答。
(1)属于第二周期元素的有D、B、A三种元素,分别为C、O、F;属于第ⅢA 族的是H,为Al元
素;属于第 IA 族的有J、L两种元素,分别为Na、K,故答案为:C;O;F;Al;Na;K;
(2)C是P元素,在元素周期表中的位置是第3周期第VA族。B 是O元素,在元素周期表中的位置是
第2周期第ⅥA族,故答案为:3;VA;2;ⅥA。