文档内容
第四章《物质结构 元素周期律》教学设计
第一节 原子结构与元素周期表
第四课时 原子结构与元素的性质—卤素
课题: 4.1.4 原子结构与元素的性质—卤素 课时 1 授课年级 高一
认识元素性质与元素在元素周期表中位置的关系,结合有关数据核实验事实认识元素性质
课标 呈周期性变化的规律,建构元素周期律。以第三周期的钠、镁、铝、硅、硫、氯,以及卤素元
要求 素为例,了解同周期核同主族元素性质的递变规律。体会元素周期律(表)在学习元素化合物
知识与科学研究中的重要作用。
本节内容是高中化学人教版(2019版)必修第一册第四章第一节《原子建构与元素周期
表》内容,本节教学的主要目的是帮助学生能够从原子结构的角度进一步认识元素周期表的实
质,未学习元素周期律打下基础。
本节内容新教材与旧教材基本相似,没有大的变化,但稍有调整,因此教学中可以按照旧
教材的思路展开教学。教材先介绍原子结构、质量数概念,然后介绍核外电子排布规律、原子
结构示意图。教材通过“思考与讨论”,引导学生观察稀有气体元素的原子核外电子排布,发
现规律,从而归纳1-20号元素的原子核外电子排布,这样的呈现方式,重在启发学生思考、培
养逻辑思维能力。再引入元素周期表,学生在初中已了解概貌,教材中这部分内容编写的目的
是要使学生了解和熟悉元素周期表的结构。本节采用“思考与讨论”的方式,让学生发现、归
纳原子结构与元素周期表的关系,重点讨论准确表达族序数与原子核外电子排布的关系,为后
面讨论元素性质打下基础。初步了解元素周期表的结构后,结合原子结构示意图分析元素原子
结构与元素在周期表位置的关系;从同族元素原子结构示意图出发,比较最外层电子数,并突
出最外层电子数相同,认识族的概念,然后介绍核素和同位素的有关知识。再以碱金属和卤素
元素为代表,通过比较原子结构(电子层数、最外层电子数)的异同,突出最外层电子数的相
同,并通过实验和事实,探究同族元素性质的相似性和递变性,通过观察、交流和归纳,得出
结论,形成元素性质与原子核外电子排布的关系。
本节内容教学重点是元素周期表的结构和元素在元素周期表中的位置及其性质的递变规
律,教学难点是原子结构与元素性质的关系。体现“构”“位”“性”的关系,教材的呈现重
视知识的逻辑性,在“构”“位”的基础上,以“演绎、归纳”的方式得出性质及其变化规
教材 律。从原子结构和元素周期表出发演绎元素的性质,再以理论和事实为依据,归纳得出同主族
元素性质的变化规律。元素周期表的发现过程,充分体现了科学研究方法、观念和科学精神,
分析
教材在本节特别重视化学史情境的创设。通过节引言、元素周期表的引人段落、科学史话、研
究与实践等形式,呈现周期表的发现过程和意义。例如,在元素周期表的引人段落,以门捷列
夫编制第一张周期表引入,并特别强调其是“在前人研究的基础上”编制出来的;在科学史话
“元素周期表的发展”中,简述了门捷列夫周期表之前的基础和之后的发展;在研究与实践
“认识元素周期表”中,还以学生体验的形式,通过关注周期表发展过程中的不同形式,引导
学生认识和理解周期表。这条化学史情境线索的呈现,能使学生发现和体会科学家的研究方法
和科学态度。教材还突出了周期表能使学生能通过周期表的位置和元素的原子结构预测元素的
性质,发现新元素的重要作用。如卤族元素是通过“思考与讨论”栏目,采用“预测—验证
(事实)—分析—结论”的思路归纳出来的。学生可以通过这样的过程体会元素周期表的作
用。同时,教材还在“方法导引”中介绍了“预测”这一科学方法,有利于学生认识到科学方
法对以及和学习的意义。本节内容共分 4个课时完成。第一课时“原子结构 核外电子排
布”,第二课时“元素周期表 核素、同位素”,第三课时“原子结构与元素的性质—碱金
属”,第四课时“原子结构与元素的性质—卤素”。
本课时是第四课时“原子结构与元素的性质—卤素”的内容。这一课时是以卤素元素的结
构和性质的关系进一步讨论原子结构与元素的性质的相似性及递变性。初步掌握根据原子结构
的特点,推测元素的化学性质。
本节课以卤素元素为代表,呈现同族元素性质的相似性,引导学生从中发现规律。在前面
的学习中,学生已经学习了原子结构和元素周期表,本课时依托于元素周期表中的典型的非金
属元素----卤族元素,诠释了原子结构与元素性质的关系。教材重点阐述了元素的非金属性与
元素在周期表中的位置和原子结构的关系,目的是帮助学生提高应用周期表分析问题和解决问题的能力,进一步建构“构”“位”“性”的关系,形成结构决定性质的观念。教学时可以从
上节课学习的同主族元素原子结构的相似性出发,继续以周期表的纵向结构为线索,学习卤族
元素的性质,由此进一步明确同族元素的原子结构(电子层数、最外层电子数)的异同,进一
步明确同族元素性质的相似性和递变性,认识元素性质与原子核外电子排布的关系。
1.通过阅读教材和实验探究,认识卤族元素性质的递变规律,并能用原子结构理论初步加
以解释同主族元素性质的递变规律,掌握元素性质与原子结构的关系,培养宏观辨识与微观探
教学 析的化学核心素养。
目标 2.通过分析卤族元素的相关性质的图表信息,尝试运用比较、归纳等方法对信息进行加
工,培养分析、处理数据的能力,体会事物变化过程中量变引起质变的规律,落实证据推理与
模型认知的化学核心素养。
教学 重点:卤族元素性质的相似性和递变性
重、 难点:原子结构与卤族元素性质的关系
难点
宏观辨识与微观探析:从微观上进一步理解同主族元素原子核外电子排布的相似性和递变
规律,宏观上明确元素性质与微观上的原子核外电子排布之间的关系,理解结构决定性质,性
质反映结构的基本规律。
核心
科学探究与创新意识:通过完成卤族元素性质的探究实验,进一步体验科学探究在化学学
素养 科的学习中的重要地位,了解科学探究的基本方法,培养初步的科学探究能力。
证据推理与模型认知:建立同主族元素原子结构变化的微观模型,进一步理解根据该模型
及相关数据信息进行元素性质推理的科学思想。
学生在第二章中已经学习过卤族的代表氯及其化合物的性质,在上几节课中又学习过同主
学情 族元素原子结构的相似性和递变性等知识,同时具备一定的对图表信息加工、处理和实验探究
分析 的能力,但对卤族元素性质的相似性和差异性尚不清晰,缺乏规律性的认识,还需要通过进一
步的学习体验探究的过程,形成科学的思维方法。
教学过程
教学 设计意
教学活动
环节 图
【回顾1】指出ⅦA族元素的元素符号及名称,并分别画出原子结构示意图。
回顾旧
【学生】板书: ⅦA族: F(氟) 、Cl(氯) 、Br(溴) 、I 知,预
习新
知,创
设卤素
(碘) 元素发
现史情
【回顾2】碱金属与水反应有哪些相似性和递变性? 境,激
发学习
【学生1】板书:相似性—碱金属都能与水反应,通式为 2R + 2H O===2ROH + H ↑
2 2 兴趣和
环
。 探究的
节
欲望。
一 【学生2】递变性:随着核电荷数的增加,碱金属与水反应越来越剧烈,生成的 ROH
培养科
、
生 (最高价氧化物对应的水化物)的碱性越来越强。 学态度
情 活 与社会
【预习1】什么是卤族元素?原子结构有何特点?
景 情 责任的
导 境 【学生1】卤族元素为第 VIIA 族的元素,包括 氟(F)、氯(Cl)、溴(Br)、碘(I)、砹 化学核
入 心素
(At) 。【学生2】最外层电子数都是 7 ,容易 得到 一个电子形成最外层8电子我
养。
的结构。【预习2】简述卤素元素性质的相似性和递变性?
【学生1】卤族元素性质的相似性:均能与氢气化合的通式为 X+H O==2HX ,与水反
2 2
应的通式为 X+H O==HX+HXO ( F 除外)。
2 2
【学生2】卤族元素性质的递变性:从上到下,随核电荷数的增加,也表现出递变性
如氢化物稳定性:HF>HCl>HBr>HI ;还原性:HFHBrO>HIO 等。
4 4 4
【引入】溴和碘的发现之旅:1824年,法国化学家巴拉尔(1802—1876)在研究盐湖中
植物的时候,将从大西洋和地中海沿岸采集到的黑角菜燃烧成
灰,然后用浸泡的方法得到一种灰黑色的浸取液。他往浸取液中
加入氯水和淀粉,溶液即分为两层:下层显蓝色(这是由于淀粉与
溶液中的碘生成了化合物);上层显棕黄色。为什么会出现这种现
象呢?经巴拉尔的研究,认为可能有两种情况:一是氯与溶液中
的碘形成新的氯化碘,这种化合物使溶液呈棕黄色;二是氯把溶
液中的新元素置换出来了,因而使上层溶液呈棕黄色。于是巴拉
尔想了些办法,试图把新的化合物分开,但都没有成功。所以他
断定这是一种与氯、碘相似的新元素。1825年,德国海德堡大学学生罗威把家乡克
罗次纳的一种矿泉水通入氯气,产生一种红棕色的物质。这种物质用乙醚提取后,再
将乙醚蒸发,则得到红棕色的液溴。所以罗威也是独立发现溴的化学家。
【过渡】上节课我们研究的是典型的金属元素——碱金属元素,本节课我们来研究一
下典型的非金属元素—卤族元素。
回归教
【问题1】查看元素周期表,阅读教材P102页中间自然段,思考什么是卤素元素?
材,从
宏观上
其原子结构有何特点?可得到什么结论?
认识卤
【学生1】元素周期表中第ⅦA族元素称卤族元素(简称卤素),包括氟(F)、氯 族元
素。
(Cl)、溴(Br)、碘(I)、砹(At)、ti´an(Ts)六种元素(后两种具有放射性)。
【学生2】其原子结构具有相似性:最外层电子数都是7(大于4),从上到下即由
F→I,随着核电荷数增加,电子层数增多。
【教师】评价、强调:卤素是化学性质非常活泼的非金属,在自然界中都以化合态存 宏微结
合认识
在。
卤素原
【问题2】根据碱金属元素原子结构的特点及变化规律,结合表中数据,思考在周期 子结构
特点,
表中,从上到下卤族元素原子的核电荷数、原子半径的变化有什么特点?完成表格内
为后续
容。 探究卤
素的性
【教师】投影表格、观察巡视。
质奠定
【学生】完成表格内容、展示交流: 基础,
体现结
原子结构示 最外层电 电子 构决定
活 元素 核电荷数 原子半径(nm)
性质的
意图 子数 层数
活 思想。
动 氟(F) 9 2 0.071
一 7
、 氯(Cl) 17 3 0.099
卤
素的
溴(Br) 35 4 1.12
环 概
节
念
二 巩固与
、 及 评价,
碘(I) 53 5 1.32
发现问
氧原
题,调
卤 子 控课
①最外层电子数相等(均为7);②从上到下,电子层数依次增加;
堂,提
素 结 结论
高效
③从上到下,原子半径依次增大。
原 构 率。
【教师】评价、强调:根据上面的原子结构示意图可知,随着原子的核电荷数递增,
子
核外电子层数逐渐增加,但是最外层电子数都是7个。
的
【对应练习1】已知某卤族元素位于周期表中第三周期,该元素原子结构示意图正确
结
的是( )
构
特 A. B. C. D.
点
及 【答案】C
物 【解析】该卤族元素是氯元素,位于元素周期表的第三周期ⅦA族,有三个电子
层,为2、8、7排列,故C正确;答案:C
理
【对应练习2】关于原子序数为53的元素,以下说法正确的是( )
性
A.位于第六周期 B.是金属元素
质
C.最外电子层含有6个电子 D.属于卤族元素
【答案】D
【解析】原子序数为53的元素比零族54号元素氙少一个质子,而氙位于第五周期,
所以53号元素位于第五周期、第ⅦA族,最外层含有7个电子,属于卤族元素,而
卤族元素均是非金属元素,答案选D。
【过渡】卤族元素(简称卤素)是典型的非金属元素,它们在自然界中都以化合态存
在。
下面我们先来学习卤素的物理性质。
回归检
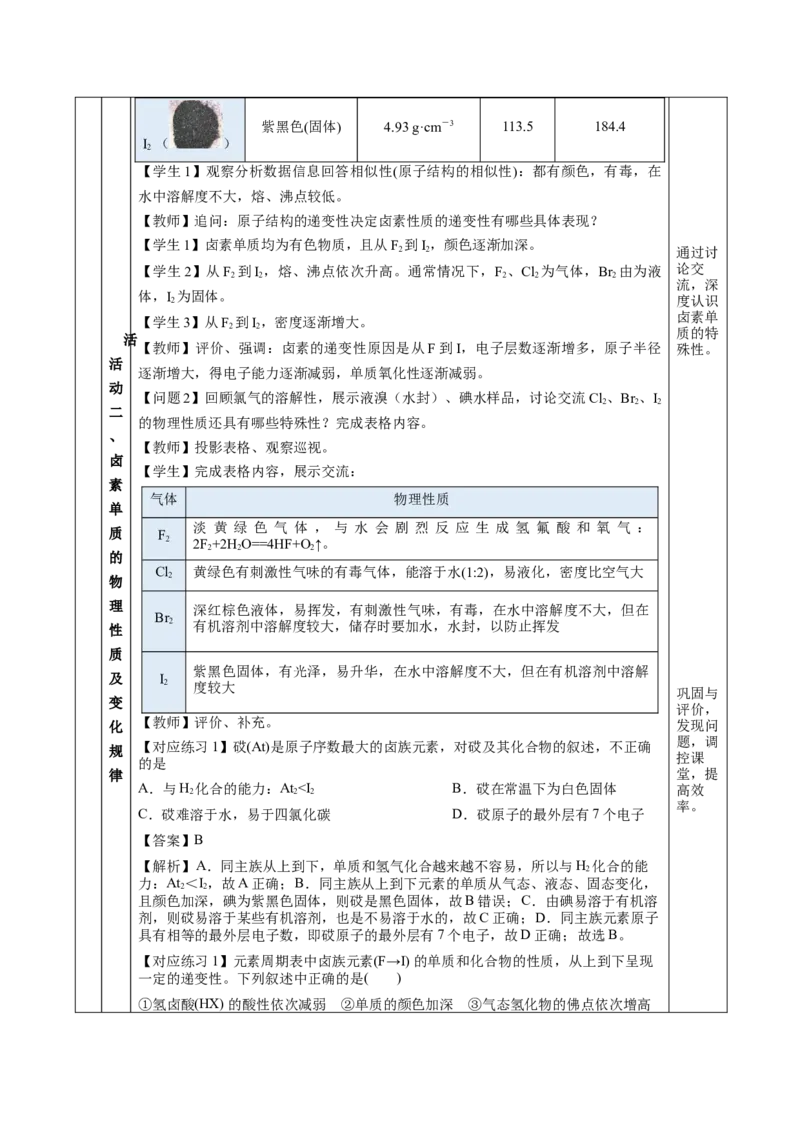
【问题1】结合教材P102页表4-3(下表)种数据内容,归纳总结卤素单质的物理性
测,通
质具有哪些相似性和递变性? 过分析
一个数
【教师】投影、引导分析。
据信
卤素单质 颜色(常态) 密度 熔点/℃ 沸点/℃ 息,认
识卤素
物理性
淡黄绿色(气体) 1.69 g·L-1(15 ℃) -219.6 -188.1 质的相
F 2 ( ) 似性和
递变
性。
黄绿色(气体) 3.214 g·L-1(0 ℃) -101 -34.6
Cl( )
2
3.119 g·cm-3(20
深红棕色(液体) -7.2 58.78
Br ( ) ℃)
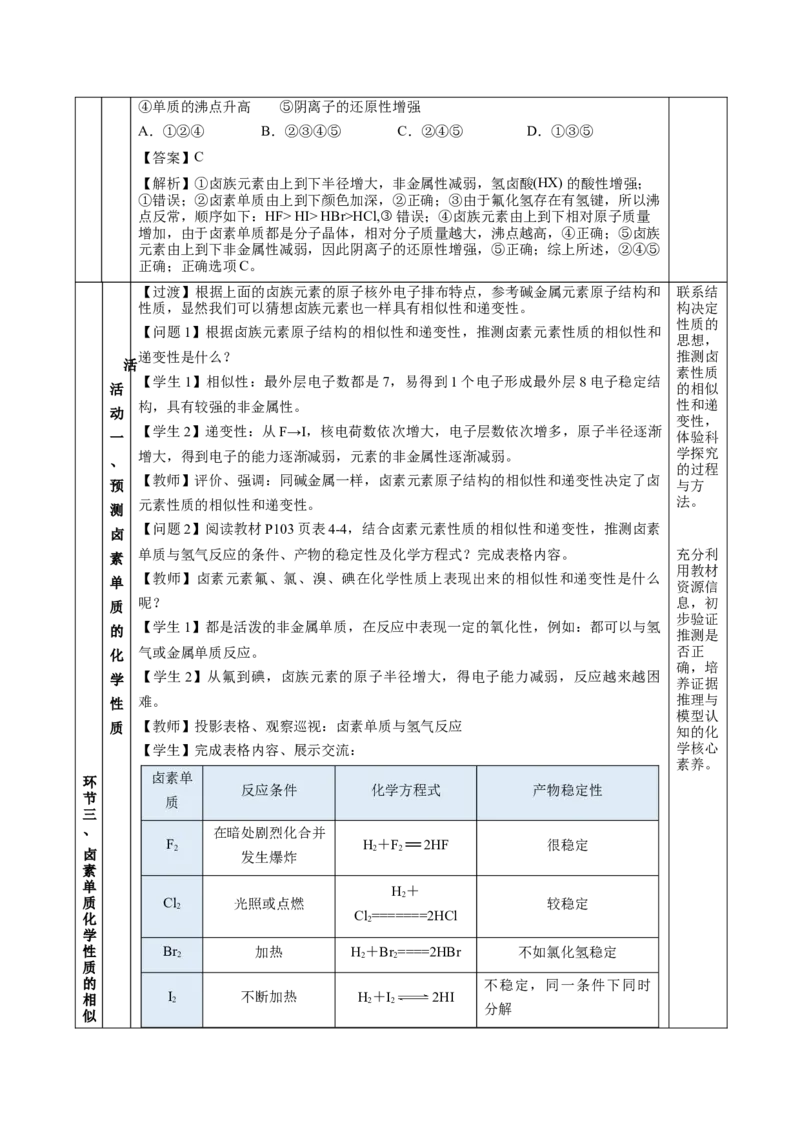
2紫黑色(固体) 4.93 g·cm-3 113.5 184.4
I ( )
2
【学生1】观察分析数据信息回答相似性(原子结构的相似性):都有颜色,有毒,在
水中溶解度不大,熔、沸点较低。
【教师】追问:原子结构的递变性决定卤素性质的递变性有哪些具体表现?
【学生1】卤素单质均为有色物质,且从F 到I,颜色逐渐加深。
2 2 通过讨
【学生2】从F 到I ,熔、沸点依次升高。通常情况下,F 、Cl 为气体,Br 由为液 论交
2 2 2 2 2
流,深
体,I
2
为固体。
度认识
卤素单
【学生3】从F 到I,密度逐渐增大。
2 2 质的特
活
【教师】评价、强调:卤素的递变性原因是从F到I,电子层数逐渐增多,原子半径 殊性。
活
逐渐增大,得电子能力逐渐减弱,单质氧化性逐渐减弱。
动
【问题2】回顾氯气的溶解性,展示液溴(水封)、碘水样品,讨论交流Cl、Br 、I
2 2 2
二
的物理性质还具有哪些特殊性?完成表格内容。
、
【教师】投影表格、观察巡视。
卤
【学生】完成表格内容,展示交流:
素
气体 物理性质
单
淡 黄 绿 色 气 体 , 与 水 会 剧 烈 反 应 生 成 氢 氟 酸 和 氧 气 :
质 F
2 2F+2H O==4HF+O ↑。
2 2 2
的
Cl 黄绿色有刺激性气味的有毒气体,能溶于水(1:2),易液化,密度比空气大
物 2
理
深红棕色液体,易挥发,有刺激性气味,有毒,在水中溶解度不大,但在
Br
性 2 有机溶剂中溶解度较大,储存时要加水,水封,以防止挥发
质
紫黑色固体,有光泽,易升华,在水中溶解度不大,但在有机溶剂中溶解
及 I
2 度较大
巩固与
变
评价,
化 【教师】评价、补充。 发现问
题,调
规 【对应练习1】砹(At)是原子序数最大的卤族元素,对砹及其化合物的叙述,不正确
控课
的是
律 堂,提
A.与H 化合的能力:At HI> HBr>HCl,③错误;④卤族元素由上到下相对原子质量
增加,由于卤素单质都是分子晶体,相对分子质量越大,沸点越高,④正确;⑤卤族
元素由上到下非金属性减弱,因此阴离子的还原性增强,⑤正确;综上所述,②④⑤
正确;正确选项C。
【过渡】根据上面的卤族元素的原子核外电子排布特点,参考碱金属元素原子结构和 联系结
性质,显然我们可以猜想卤族元素也一样具有相似性和递变性。 构决定
性质的
【问题1】根据卤族元素原子结构的相似性和递变性,推测卤素元素性质的相似性和
思想,
递变性是什么? 推测卤
活
素性质
【学生1】相似性:最外层电子数都是7,易得到1个电子形成最外层8电子稳定结
活 的相似
构,具有较强的非金属性。 性和递
动
变性,
【学生2】递变性:从F→I,核电荷数依次增大,电子层数依次增多,原子半径逐渐
一 体验科
增大,得到电子的能力逐渐减弱,元素的非金属性逐渐减弱。 学探究
、
的过程
【教师】评价、强调:同碱金属一样,卤素元素原子结构的相似性和递变性决定了卤
预 与方
元素性质的相似性和递变性。 法。
测
【问题2】阅读教材P103页表4-4,结合卤素元素性质的相似性和递变性,推测卤素
卤
素 单质与氢气反应的条件、产物的稳定性及化学方程式?完成表格内容。 充分利
用教材
【教师】卤素元素氟、氯、溴、碘在化学性质上表现出来的相似性和递变性是什么
单
资源信
质 呢? 息,初
步验证
的
【学生1】都是活泼的非金属单质,在反应中表现一定的氧化性,例如:都可以与氢
推测是
化 气或金属单质反应。 否正
确,培
学 【学生2】从氟到碘,卤族元素的原子半径增大,得电子能力减弱,反应越来越困
养证据
性 难。 推理与
模型认
质 【教师】投影表格、观察巡视:卤素单质与氢气反应
知的化
【学生】完成表格内容、展示交流: 学核心
素养。
环 卤素单
反应条件 化学方程式 产物稳定性
节
质
三
、 在暗处剧烈化合并
F H+F=2HF 很稳定
卤 2 发生爆炸 2 2
素
单 H+
2
质 Cl 光照或点燃 较稳定
2
化 Cl 2 =======2HCl
学
性 Br 加热 H+Br ====2HBr 不如氯化氢稳定
2 2 2
质
的 不稳定,同一条件下同时
相 I 2 不断加热 H 2 +I 2 2HI
分解
似性 从F 到I ,与H 化合越来越难,生成的氢化物稳定性逐渐减弱,元素
2 2 2
和 结论
递 的非金属性逐渐减弱。
变
【教师】评价、强调:由氟到碘,反应逐渐变得困难;反应生成的氢化物的稳定性逐
性
渐减弱;非金属性逐渐减弱。
巩固与
【对应练习1】下列关于F、Cl、Br、I的比较,不正确的是( )
评价,
发现问
A.它们的原子核外电子层数随核电荷数的增加而增多
题,调
B.单质的氧化性随核电荷数的增加而减弱 控课
堂,提
C.它们的氢化物的稳定性随核电荷数的增加而增强
高效
率。
D.单质的颜色随核电荷数的增加而加深
【答案】C
【解析】A项,F、Cl、Br、I的原子核外电子层数分别为2、3、4、5,随核电荷数
的增加而增多,正确;B项,F、Cl、Br、I原子半径增大,原子核对电子的引力逐渐
减小,单质的氧化性随核电荷数的增加而减弱,正确;C项,元素的非金属性越强,
其氢化物的稳定性越强,非金属性F>Cl>Br>I, F、Cl、Br、I原子半径增大,与
氢原子的作用力逐渐减小,它们的氢化物的稳定性随核电荷数的增加而减弱,错误;
D项,单质的颜色分别是浅黄绿色、黄绿色、深红棕色和紫黑色,单质的颜色随核电
荷数的增加而加深,正确。
【对应练习2】下列有关碱金属、卤素原子结构和性质的描述正确的是( )
A.随着核电荷数的增加,碱金属单质熔、沸点依次降低,密度依次减小
B.碱金属单质的金属性很强,均易与氧气发生反应,加热时生成氧化物R O
2
C.根据同主族元素性质的递变规律推测At与H 化合较难
2
D.根据F、Cl、Br、I的非金属性依次减弱,可推出HF、HCl、HBr、HI的还原性及
热稳定性依次减弱
【答案】C
【解析】A项,碱金属单质的熔点、沸点均随着核电荷数的递增而降低,碱金属单质
的密度随着核电荷数的递增而逐渐增大,但是钠钾反常,错误;B项,碱金属金属性
随原子序数的递增依次增强,碱金属单质与氧气加热条件下反应,锂生成LiO、钠生
2
成NaO、钾铷铯生成过氧化物、超氧化物等,错误;C项,同主族元素从上到下非
2 2
金属逐渐减弱,I 与H 需要持续加热才能化合,由此可推知At与H 更难化合,正
2 2 2
确;D项,根据F、Cl、Br、I的非金属性依次减弱,可推出HF、HCl、HBr、HI的
热稳定性依次减弱,HF、HCl、HBr、HI的还原性依次增强,错误。
活【过渡】化学实验是科学探究的重要环节,为了证明卤素单质化学性质的相似性和递
变性,我们来进行进一步的实验探究。
【问题1】结合教材P104页【实验4-1】完成实验,观察比较卤素单质间的置换反应
通过实
的实验现象,并分析其原理,完成表格内容。
验探
【教师】演示实验或指导学生实验或观看视频,并投影表格:卤素单质间的置换反应 究,进
一步验
的实验探究
证推测
【学生】观察实验现象或完成实验后,填写表格内容、展示交流: 是否正
确,培实验内容 操作方法 实验现象 化学方程式或解释 养宏观
辨识与
将少量氯水滴入盛有KBr 无 色 变 橙 Cl 2 + 2KBr===2KCl + 微观探
Br
活 溶液的试管中,用力振荡 色,后上层 2 析的化
氯置换溴
试管,再滴加CCl 4 振 无色,下层 溴单质溶于 CCl 呈橙 学核心
4
荡。 橙红色。 红色 素养,
体验科
将少量氯水滴入盛有KI 无色变棕褐 Cl+2KI===2KCl+I 学探究
2 2
溶液的试管中,用力振荡 色,后上层 的过程
氯置换碘
试管,再滴加CCl 4 振 无色,下层 碘单质溶于 CCl 4 呈紫 与方
荡。 紫红色。 红色 法。
将少量溴水滴入盛有KI 无色变棕褐 Br +2KI===2KBr+I
2 2
溶液的试管中,用力振荡 色,后上层
溴置换碘
试管,再滴加CCl 4 振 无色,下层 碘单质溶于 CCl 4 呈紫
荡。 紫红色。 红色
活
①氯能从可溶的溴化物和碘化物水溶液中置换出溴和碘,溴能置换
活
出碘,即氯比溴和碘活泼,溴比碘活泼,即卤素单质的氧化性顺序
动
通过归
结论 由强到弱依次是:Cl>Br >I ;卤素离子的还原性顺序由强到弱依次
二 2 2 2 纳和总
是:I->Br->Cl-. 结,进
、
一步明
实 ②Br 2 、I 2 难溶于水,易溶于CCl 4 。 确卤素
验 【教师】评价、强调:所以随着核电荷数的增加,卤族元素单质的氧化性,按照 元素性
F、Cl、Br 、I 的顺序依次减弱。 质的相
探 2 2 2 2 似性和
【问题2】归纳总结:卤素元素化学性质的相似性和递变性有哪些?完成表格内容。 递变性
究
的具体
【教师】投影表格:卤族元素性质的相似性,引导分析。
卤 表现。
【学生】完成表格内容,展示交流:
素
元素 F Cl Br I
单
质 最外层电子数 均为7
的 最高正价 均为7(F除外)
化
最低负价 均为-1
学
最高价氧化物对应水化物 无 HClO HBrO HIO
4 4 4
性
质 气态氢化物 HF HCl HBr HI
自然界中状态 均以化合态形式存在
【教师】评价、投影:卤素单质化学性质的递变性。
通过对
【学生】完成表格内容、展示交流: 卤素单
质特殊
化学性质 规律(按F、Cl、Br、I顺序)
性的认
原子得电子能力 逐渐减弱 识,深
度理解
非金属性 逐渐减弱 卤素单
质性质
单质的氧化性 逐渐减弱 的变化
规律。
阴离子的还原性 逐渐增强
最高价氧化物对应水化物的酸性 逐渐减弱单质与氢气化合的难易程度 越来越难
氢化物的稳定性 逐渐减弱
【教师】评价、补充。
【问题3】讨论交流:结合所学知识,你认为卤素还有哪些特殊性?
【学生1】在常温下Br 是唯一的液态非金属单质,易挥发,在保存液溴时要加一些
2
水进行“水封”。
【学生2】碘为紫黑色固体,易升华,淀粉遇I 变蓝。
2
【学生3】氟是最活泼的非金属,没有正化合价,氟单质与盐溶液反应时,先与水反
应产生HF和O:2F+2HO=4HF+O。
2 2 2 2
【学生4】氢化物性质:氢化物的稳定性逐渐减弱,还原性逐渐增强,其水溶液的酸
性逐渐增强,即:稳定性:HF>HCl>HBr>HI;还原性:HF<HCl<HBr<HI;酸
巩固与
性:HF<HCl<HBr<HI。 评价,
发现问
【教师】、评价、总结。 题,调
控课
【对应练习1】向KI溶液中加入氯水,发生Cl +2I-=2Cl-+I 。下列说法不正确
2 2 堂,提
的是( )
高效
A.Cl 水导电但Cl 不是电解质 率。
2 2
B.停止反应后,取少量溶液滴加淀粉溶液,溶液变蓝
C.溶液颜色变化说明
D.实验结果说明,氯的非金属性强于碘
【答案】C
【解析】A项,Cl 水导电是Cl 与HO反应生成了HCl和HClO,电解质是化合物而
2 2 2
Cl 是单质不是是电解质,正确;B项,向KI溶液中加入氯水,发生Cl+2I-=2Cl
2 2
-+I,有碘单质生成,淀粉遇碘变蓝,所以取少量溶液滴加淀粉溶液,溶液变蓝,
2
正确;C项,对于反应Cl+2I-=2Cl-+I,其中氯元素化合价降低,得电子,碘元
2 2
素化合价升高,失电子,用单线桥表示为 ,错误;D项,根据
反应Cl+2I-=2Cl-+I,氧化性:Cl>I,所以非金属性:Cl>I,正确。
2 2 2 2
【对应练习2】验证氧化性强弱Cl>Br >I,设计如下实验。(已知:稀溴水呈黄
2 2 2
色;浓溴水呈红棕色;碘水呈棕黄色;忽略氧气的影响)
实验① 实验② 实验③ 实验④溶液变为浅黄绿色 溶液变为黄色 溶液变为棕黄色 溶液变为蓝色
下列说法不正确的是( )
A.实验①设计目的为:排除实验②③④水稀释的影响
B.实验②发生反应为:2Br-+Cl=Br +2Cl-
2 2
C.实验③的现象可以证明氧化性:Cl>I
2 2
D.实验④能证明氧化性:Br >I
2 2
【答案】D
【解析】A项,实验采用控制变量方法,因此实验①为对照实验,可排除实验②③④
中水稀释对溶液颜色变化的影响,正确;B项,将Cl 水滴入KBr溶液中,发生置换
2
反应:2Br-+Cl=Br +2Cl-,由于产生的溴水浓度较小,因此看到溶液变为黄
2 2
色,正确;C项,将1 mL氯水加入KI溶液中,发生反应:Cl+2I-=I+2Cl-,产
2 2
生的I 使溶液变为棕黄色,在反应中氧化剂是Cl,氧化产物是I,故可证明物质的
2 2 2
氧化性:Cl>I,正确;D项,②反应后的溶液中可能含有过量的Cl 及反应产生的
2 2 2
Br ,因此取②反应后的溶液加入KI淀粉混合溶液中,溶液变为蓝色,可能发生反
2
应:Cl+2I-=I+2Cl-,也可能发生反应:Br +2I-=I+2Br-,I 遇淀粉溶液变
2 2 2 2 2
为蓝色,该实验不能证明氧化性:Br >I,错误。
2 2
1.(易)教材作业:P106页练习3、4、5、6、8
2.(易)卤族元素随原子核电荷数的增加,下列叙述不正确的是( )
A.原子半径依次增大 B.元素的非金属性依次减弱
C.单质的氧化性依次减弱 D.氢化物的稳定性依次增强
【答案】D
【解析】卤素单质(F →I)与氢气发生化合反应由易到难(反应由F 与H 不需要
2 2 2 2
任何条件,到H 与I 加热才化合,并且化合生成的HI同时分解),生成的氢化物稳定
2 2
性逐渐减弱。
3.(易)下列关于碱金属元素和卤素的说法中错误的是( )
A.随核电荷数的增大,碱金属元素和卤素的原子半径都逐渐增大
B.碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子能力最
强
C.钾与水的反应比钠与水的反应更剧烈
D.单质溴与水的反应比氯气与水的反应更剧烈
【答案】D
【解析】由于Cl比Br非金属性强,故Cl 与HO的反应比Br 与HO的反应更剧
2 2 2 2
烈,故D项错误。
4.(中)关于卤素(用X表示)的下列叙述正确的是( )
A.卤素单质与水反应均可用X+HO=HXO+HX表示
2 2
B.还原性:Cl->Br-
及时巩
C.卤素单质的密度从F→I 随相对分子质量增大而增大 固、消
2 2
化所
D.F 可以从NaCl溶液中置换出Cl
2 2 学,促
【答案】C 进掌握【解析】A.F 与水反应的化学方程式为2F+2HO=4HF+O,A错误;B.因 必备知
2 2 2 2
为单质的氧化性:Cl>Br ,故还原性:Cl-