文档内容
第四章 化学反应与电能
课题
第一节 原电池
第一课时
1、复习原电池的化学原理,掌握形成原电池的基本条件。
知识与技能 2、常识性介绍日常生活中常用的化学电源。并能从电极反应的角度认识常
见电源的化学原理
1、通过拆分干电池和学会自制简易电池培养学生观察能力与分析
思维能力,并通过了解电池的化学组成而增强环保意识。
教 学 过程与方法 2、通过化学化学电源的使用史实引导学生以问题为中心的学习方
目 标 法。学会发现问题、解决问题的方法。加深理解实践→认识→
再实践→再认识的辨证唯物主义的思维方法
1、通过原电池的发明、发展史,培养学生实事求是勇于创新的科
情感态度 学
与价值观 态度。
2、激发学生的学习兴趣与投身科学追求真理的积极情感。
教学
电极反应的书写
重点
教学
电极反应的书写
难点
教
学科网(北京)股份有限公司
学
设
想
本节课是对原电池原理的应用,同时了解生活实际,有利于用化学知识来解决
教
材 生活中的实际问题
分
析
学生已经学了氧化还原反应的理论和原电池知识,为学习化学电源做了思想上
学
情 和能力上的准备。 对原电池的工作原理有神秘感和探索欲望。要充分利用学生的
分
好奇心和求知欲,设计层层实验和问题情境,使学生在自主实验、积极思考和相
析
互讨论中自己发现问题、分析问题和解决问题。
教学环节 设计意图
教 学 内 容
教师活动 学生活动【提问】
组成原电池的条件:
①有两种活动性不同的金属(或一种是非金属导
体)作电极
②电极均插入电解质溶液中 复习引入新课
③两极相连形成闭合回路
立即用多媒体展示相应的原电池图片,使学生的认
识直观、清晰。
再很自然地引出利用原电池的原理我们已经制作使
用的化学电池。
【引课】第二节 化学电源
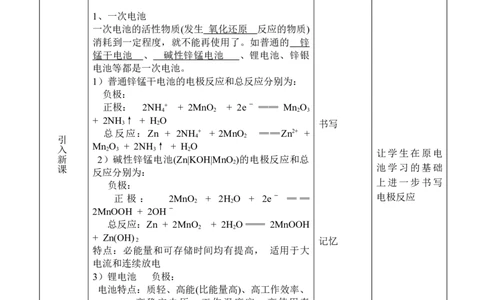
1、一次电池
一次电池的活性物质(发生 氧化还原 反应的物质)
消耗到一定程度,就不能再使用了。如普通的 锌
锰干电池 、 碱性锌锰电池 、锂电池、锌银
电池等都是一次电池。
1)普通锌锰干电池的电极反应和总反应分别为:
负极:
正极: 2NH + + 2MnO + 2eˉ ══ Mn O
4 2 2 3
+ 2NH ↑ + H O
3 2 书写
总反应:Zn + 2NH + + 2MnO ══Zn2+ +
引 4 2
Mn O + 2NH ↑ + H O
入 2 3 3 2 让学生在原电
新 2)碱性锌锰电池(Zn|KOH|MnO )的电极反应和总
2
课 池学习的基础
反应分别为:
上进一步书写
负极:
正 极 : 2MnO + 2H O + 2eˉ ═ ═ 电极反应
2 2
2MnOOH + 2OHˉ
总反应:Zn + 2MnO + 2H O ══ 2MnOOH
2 2
+ Zn(OH)
2 记忆
特点:必能量和可存储时间均有提高, 适用于大
电流和连续放电
3)锂电池 负极:
电池特点:质轻、高能(比能量高)、高工作效率、
高稳定电压、工作温度宽、高使用寿
命,广泛应用于军事和航空领域。
4)锌银电池 (电解液KOH溶液)
负极( Zn ): Zn - 2 e ˉ + 2 O H ˉ
== Zn(OH)
2
正极( A g O ): A g O + 2e ˉ + H O ═
2 2 2
2Ag + 2 O H ˉ
理解
总反应: Zn + A g O + H O ═ 2Ag +
2 2
Zn(OH)
2
特点:比能量大、电压稳定、储存时间长、适宜小
电流连续放电。
学科网(北京)股份有限公司2、二次电池
二次电池又称充电电池或蓄电池,放电后可以再充
电,使活性物质获得
再生,恢复工作能力,实现电池的多次重复使用。
最典型的为铅蓄电池,
铅蓄电池放电时的电极反应和总反应分别为:
(电解液H SO 溶液)
2 4
负极( P b ): Pb - 2 e ˉ + SO 2 ˉ ═ PbSO
4 4
正极( PbO ):PbO + 2 e ˉ + 4H + + SO 2 ˉ ═
2 2 4
PbSO + 2H O
4 2
总反应 Pb + PbO 2 + 2H 2 SO 4 ═ 2PbSO 4 + 书写
2H O
2 通 过 以 上 实
铅蓄电池充电时的电极反应和总反应分别为:
例,引导学生
阳极:PbSO + 2H O -2eˉPbO + 4H+ + SO 2ˉ
4 2 2 4
分析,归纳总
阴极: PbSO + 2eˉ == Pb + SO 2ˉ
4 4
结规律,培养
总 反 应 : 2PbSO + 2H O ═ Pb + PbO +
4 2 2
2H SO
学生归纳总结
2 4
优点:电压稳定、使用方便、安全可靠、价 的能力
格低廉
缺点:比能量低、笨重,废弃电池污染环境
3、燃料电池——是一种连续地将燃料和氧化剂的
导
化学能直接转化成电能的化学电源又称连续电池
学
达 燃料电池的规律:① 燃料通入负极,助燃剂
标
氧气通入正极
② 电极材料一般不参加化
学反应,只起传导电子的作用。
燃料电池与前几种电池的差别:① 氧化剂与
还原剂在工作时不断补充;
② 反应产物不断排出;③能量转化率高(超
过80%),普通的只有30%,有利于节约能源。
1)氢氧燃料电池
让学生学以之
(1) 特点: ① 高效、低污染,原料来源广泛
用,根据已学
② 电极材料不参加电池反应
总结 知识来解决实
(2) 总反应式:2H + O == 2H O
2 2 2
负极:2H - 4eˉ == 4H+; 际问题
2
正极:O + 2H O + 4eˉ == 4OHˉ
2 2
注意:电解质溶液不同,电极反应不同。 让学掌握基本
当为碱性溶液时:
的原电池的电
负极:2H + 4OHˉ - 4eˉ== 4H O
2 2 极 反 应 的 书
正极:O + 2H O + 4eˉ == 4OHˉ
2 2 写,并学会应
当为酸性溶液时: 负极:2H - 4eˉ == 4H+
2
用
正极:O + 4H+ + 4eˉ == 2H O
2 2
学科网(北京)股份有限公司2)甲烷氢氧燃料电池
当为酸性溶液时:
负极: CH 4 - 8 e ˉ + 2H 2 O == CO 2 + 8H + 培养学生的发
正极: 2O + 8 e ˉ + 8H + == 4H O
2 2 散思维,有一
当为碱性溶液时:
定的设计能力
负极: CH - 8 e ˉ + 10OH ˉ == CO 2 ˉ + 7H O
4 3 2
正极: 2O + 8 e ˉ + 4H O == 8OH ˉ
2 2
3)甲醇氢氧燃料电池
当为酸性溶液时:
培养学生的归
负极: 2CH OH - 12e ˉ + 2H O == 2CO + 12H +
导 3 2 2
学 正极: 3O + 12 e ˉ + 12H + == 6H O 纳总结的能力
2 2
达
当为碱性溶液时:
标
负极: 2CH OH - 12e ˉ + 16OH ˉ == 2CO 2 ˉ +
3 3
12H O 正极: 3O + 12 e ˉ + 6H O == 12OH ˉ
2 2 2
当电解质为熔融碳酸盐时: 培养学生的解
负极: 2CH 3 OH - 12e ˉ + 6 CO 3 2 ˉ == 8 CO 2 + 4 H 2 O 决问题的能力
正极: 3O + 12 e ˉ + 6 CO == 6 CO 2 ˉ
2 2 3
当电解质为固体氧化物时:
负极: 2CH OH - 12e ˉ + 12 O 2 ˉ == 2 CO + 4 H O
3 2 2
正极: 3O + 12 e ˉ == 6 O 2 ˉ
2
作
业
设
计
一、
化学电源
板
一、一次电池
书
设 二、二次电池
计
三、燃料电池
学科网(北京)股份有限公司学科网(北京)股份有限公司