文档内容
第四章 化学反应与电能
课题 第一节 原电池
第一课时
1、让学生了解原电池的工作原理和构成条件
知识与技能
2、能够写出电极反应式和电池反应方程式
1、通过分组实验培养学生实验设计、动手操作、观察、分析、推理等
能力
过程与方法
2、通过实验引导学生学会发现问题、分析问题和解决问题的科学探究
教 学
目 标 精神和创新能力
1、通过学生实验,激发学生学习的兴趣,培养学生探究和合作学习的
情感态度 精神
与价值观
2、通过原电池的发明、发展史,培养学生实事求是、勇于探究、创新
的科学态度
教学
原电池的工作原理;原电池电极的判定及电极反应式的书写
重点
教学
原电池的工作原理及电极反应式的书写
难点
教
学科网(北京)股份有限公司
学
设
想
本节课是新课标人教版化学必修 2第二章第二节《化学能与电能》的部分教学内
容,是教学大纲和考纲要求的重要知识点,是电化学中的基础内容也是核心内容,也
教 是高中化学的教学难点之一,是多数高中学生掌握不好的一部分知识。本节教材起着
材
承前启后的作用,它融合了之前所学的氧化还原反应、金属的性质、电解质溶液等知
分
析 识,在学习过程中还涉及到物理中电学的相关知识,能培养学生创造性思维;又将为
以后学好化学选修1《化学与生活》中金属腐蚀与防护,以及化学选修 4《化学反应原
理》中的第四节 《电化学基础》等知识打下基础。
学生已经学了氧化还原反应的理论、有关金属的性质、电解质溶液等知识,为学习
学 原电池做了思想上和能力上的准备。学生初次接触电化学知识,对原电池的工作原理
情
有神秘感和探索欲望。要充分利用学生的好奇心和求知欲,设计层层实验和问题情
分
析
境,使学生在自主实验、积极思考和相互讨论中自己发现问题、分析问题和解决问
题。
教学环节 设计意图
教 学 内 容
教师活动设计 学生活动设计[引入新课]请同学们分享一则故事
[课件]以一件生活中的事例——格林 思考
太太的两颗假牙(一颗黄金制作,一
颗不锈钢制作)导致格林太太头痛、 引入病例分析激发
失眠、心情烦躁等症状,格林太太为 学生探究科学的兴
什么会出现这样的症状呢?与她的假 趣。
牙有关吗?学习本节内容,便能解决
此问题。
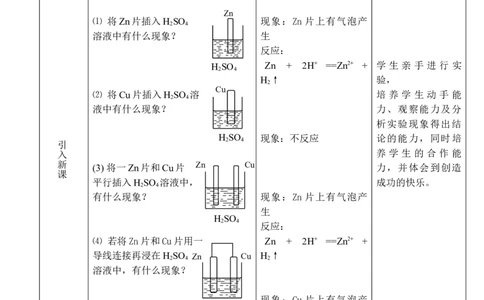
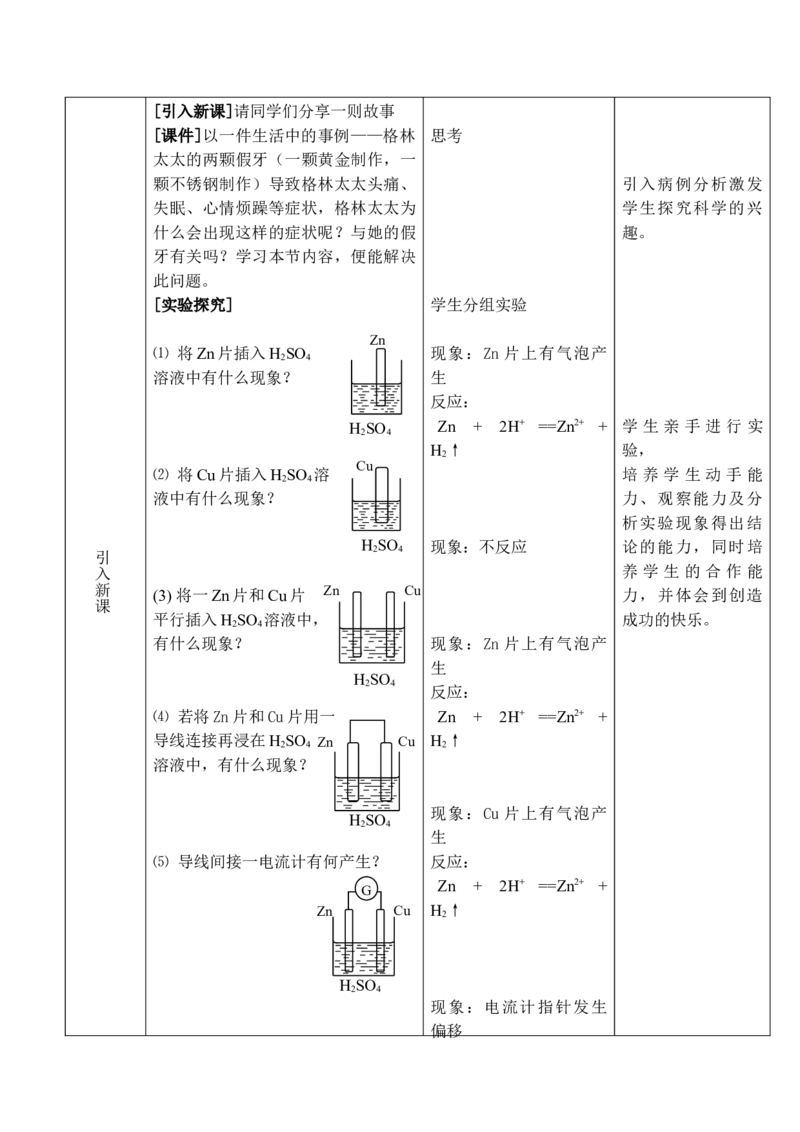
[实验探究] 学生分组实验
Zn
⑴ 将Zn片插入H SO 现象:Zn 片上有气泡产
2 4
溶液中有什么现象? 生
反应:
H SO Zn + 2H+ ==Zn2+ + 学 生 亲 手 进 行 实
2 4
H ↑ 验,
2
Cu
⑵ 将Cu片插入H SO 溶 培 养 学 生 动 手 能
2 4
液中有什么现象? 力、观察能力及分
析实验现象得出结
H SO 现象:不反应 论的能力,同时培
2 4
引
入 养 学 生 的 合 作 能
新 (3) 将一Zn片和Cu片 Zn Cu 力,并体会到创造
课
平行插入H SO 溶液中, 成功的快乐。
2 4
有什么现象? 现象:Zn 片上有气泡产
生
H SO
2 4
反应:
⑷ 若将Zn片和Cu片用一 Zn + 2H+ ==Zn2+ +
导线连接再浸在H SO Zn Cu H ↑
2 4 2
溶液中,有什么现象?
现象:Cu 片上有气泡产
H SO
2 4
生
⑸ 导线间接一电流计有何产生? 反应:
Zn + 2H+ ==Zn2+ +
G
Zn Cu H ↑
2
H SO
2 4
现象:电流计指针发生
偏移
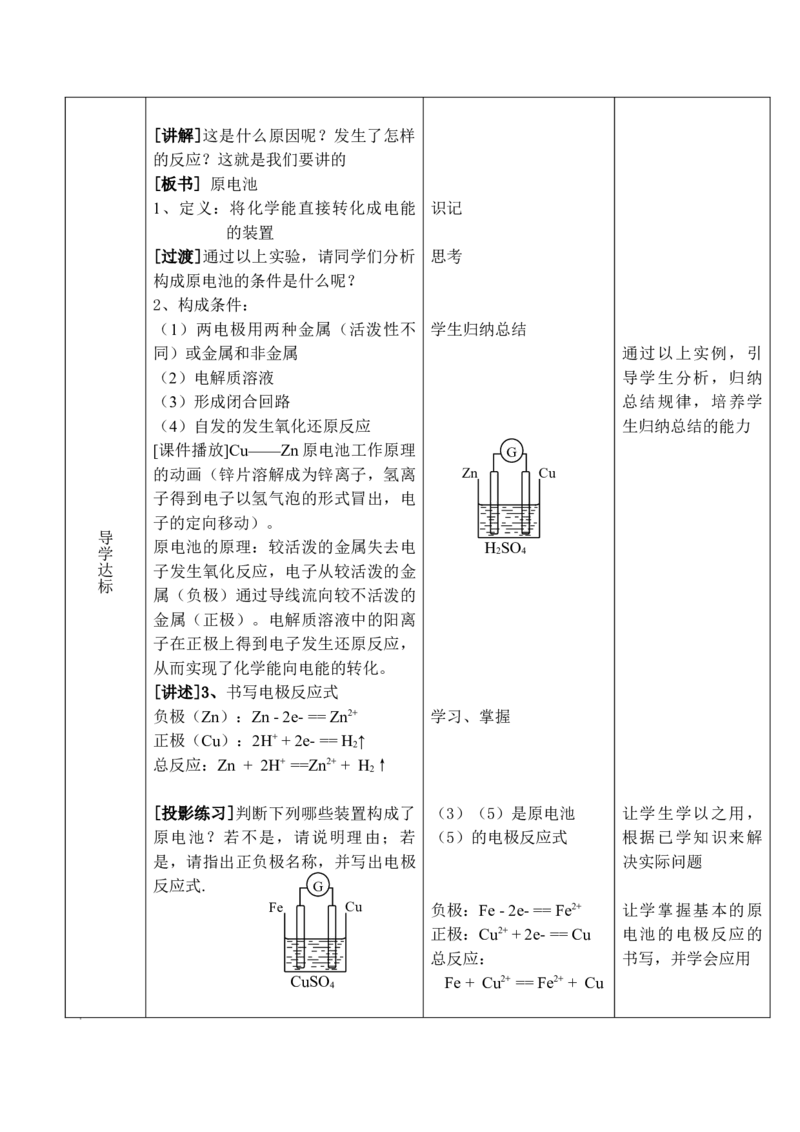
学科网(北京)股份有限公司[讲解]这是什么原因呢?发生了怎样
的反应?这就是我们要讲的
[板书] 原电池
1、定义:将化学能直接转化成电能 识记
的装置
[过渡]通过以上实验,请同学们分析 思考
构成原电池的条件是什么呢?
2、构成条件:
(1)两电极用两种金属(活泼性不 学生归纳总结
同)或金属和非金属 通过以上实例,引
(2)电解质溶液 导学生分析,归纳
(3)形成闭合回路 总结规律,培养学
(4)自发的发生氧化还原反应 生归纳总结的能力
[课件播放]Cu——Zn原电池工作原理
G
的动画(锌片溶解成为锌离子,氢离 Zn Cu
子得到电子以氢气泡的形式冒出,电
子的定向移动)。
导
原电池的原理:较活泼的金属失去电 H SO
学 2 4
达 子发生氧化反应,电子从较活泼的金
标
属(负极)通过导线流向较不活泼的
金属(正极)。电解质溶液中的阳离
子在正极上得到电子发生还原反应,
从而实现了化学能向电能的转化。
[讲述]3、书写电极反应式
负极(Zn):Zn - 2e- == Zn2+ 学习、掌握
正极(Cu):2H+ + 2e- == H ↑
2
总反应:Zn + 2H+ ==Zn2+ + H ↑
2
[投影练习]判断下列哪些装置构成了 (3)(5)是原电池 让学生学以之用,
原电池?若不是,请说明理由;若 (5)的电极反应式 根据已学知识来解
是,请指出正负极名称,并写出电极 决实际问题
反应式. G
Fe Cu 负极:Fe - 2e- == Fe2+ 让学掌握基本的原
正极:Cu2+ + 2e- == Cu 电池的电极反应的
总反应: 书写,并学会应用
CuSO Fe + Cu2+ == Fe2+ + Cu
4
学科网(北京)股份有限公司[讲述]4、根据原电池原理可以设计
原电池 负极:Cu
例:请结合组成原电池的条件,将氧 正极:比铁不活泼金属
化还原反应:Cu + 2Ag+ == Cu2+ + 或石墨 培养学生的发散思
2Ag 电解液:可溶性银盐 维,有一定的设计
电极反应式 : 能力
负极: Cu - 2e- == Cu2+
正极:2Ag+ + 2e- == 2Ag
[练习]设计原电池:
Fe + 2Fe3+ == 3Fe2+
[讲述]根据以上知识的学习,请同学
们完成下表
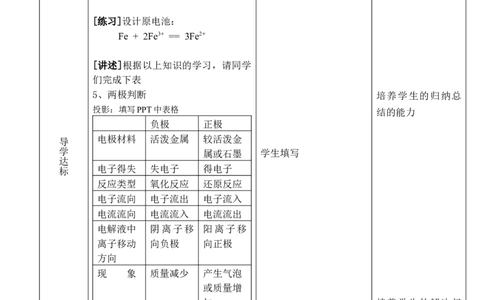
5、两极判断 培养学生的归纳总
投影:填写PPT中表格 结的能力
负极 正极
电极材料 活泼金属 较活泼金
导
学 属或石墨 学生填写
达
标 电子得失 失电子 得电子
反应类型 氧化反应 还原反应
电子流向 电子流出 电子流入
电流流向 电流流入 电流流出
电解液中 阴离子移 阳离子移
离子移动 向负极 向正极
方向
现 象 质量减少 产生气泡
或质量增
加 培养学生的解决问
讨论,回答
题的能力
格林太太的两个假牙相
[讨论]通过以上知识的学习,同学们
接触,再与口腔内的电
能否治疗格林太太的牙疼病呢?
解质构成了原电池,形
成了电流,导致格林太
太出现的症状
[过渡]我们学习原电池有什么应用
呢?
学科网(北京)股份有限公司6、原电池的应用
(1)原电池反应比普通氧化还原反
应速率快,如实验室制氢气 归纳总结 培养学生归纳总结
(2)利用工作原理判断金属性的强
的能力
弱
(3)制备各种各样的化学电源,包
括常见的干电池、蓄电池,以及我们
导 手机中使用的锂离子电池。还可以制
学
成水果电池。
达
标 [课堂小结]本节课通过实验探究了原
电池的原理以及组成原电池的条件。
要求同学们理解原电池的原理,能够
正确判断原电池的电极名称并写出电
极反应式,注意正、负极电极反应式
的书写要保证得失电子守恒。同时能
够依据组成原电池的条件判断那些装
置可以构成原电池。
作
业
1、课外实践活动:利用苹果、柑橘、柠檬等水果尝试制作原电池。
设
计 2、上网查询,发展中的化学电源种类及应用。
一、
二、 原电池
1、定义:将化学能直接转化成电能的装置
2、构成条件:
(1)电极用两种金属,活泼性不同
(2)电解质溶液;
(3)形成闭合回路。
板 (4)自发的发生氧化还原反应
书
3、书写电极反应式
设
负极(Zn):Zn - 2e- == Zn2+
计
正极(Cu):2H+ + 2e- == H ↑
2
总反应: Zn + 2H+ ==Zn2+ + H ↑
2
4、应用
(1)原电池反应比普通氧化还原反应速率快,如实验室制氢气
(2)利用工作原理判断金属性的强弱
(3)制备各种各样的化学电源,包括常见的干电池、蓄电池,以及我们手机中使用的
锂离子电池。还可以制成水果电池。
学科网(北京)股份有限公司学科网(北京)股份有限公司