文档内容
4.1原电池(分层作业)
1.随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是
A.利用电池外壳的金属材料
B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C.不使电池中渗泄的电解液腐蚀其他物品
D.回收其中石墨电极
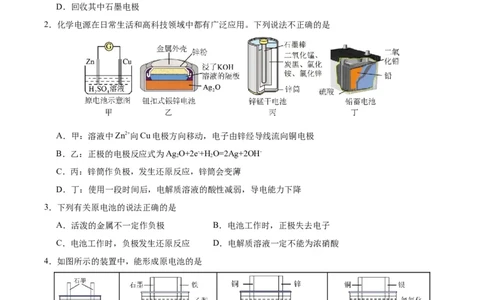
2.化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是
A.甲:溶液中Zn2+向Cu电极方向移动,电子由锌经导线流向铜电极
B.乙:正极的电极反应式为Ag O+2e-+H O=2Ag+2OH-
2 2
C.丙:锌筒作负极,发生还原反应,锌筒会变薄
D.丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
3.下列有关原电池的说法正确的是
A.活泼的金属不一定作负极 B.电池工作时,正极失去电子
C.电池工作时,负极发生还原反应 D.电解质溶液一定不能为浓硝酸
4.如图所示的装置中,能形成原电池的是
A B C D
A.A B.B C.C D.D
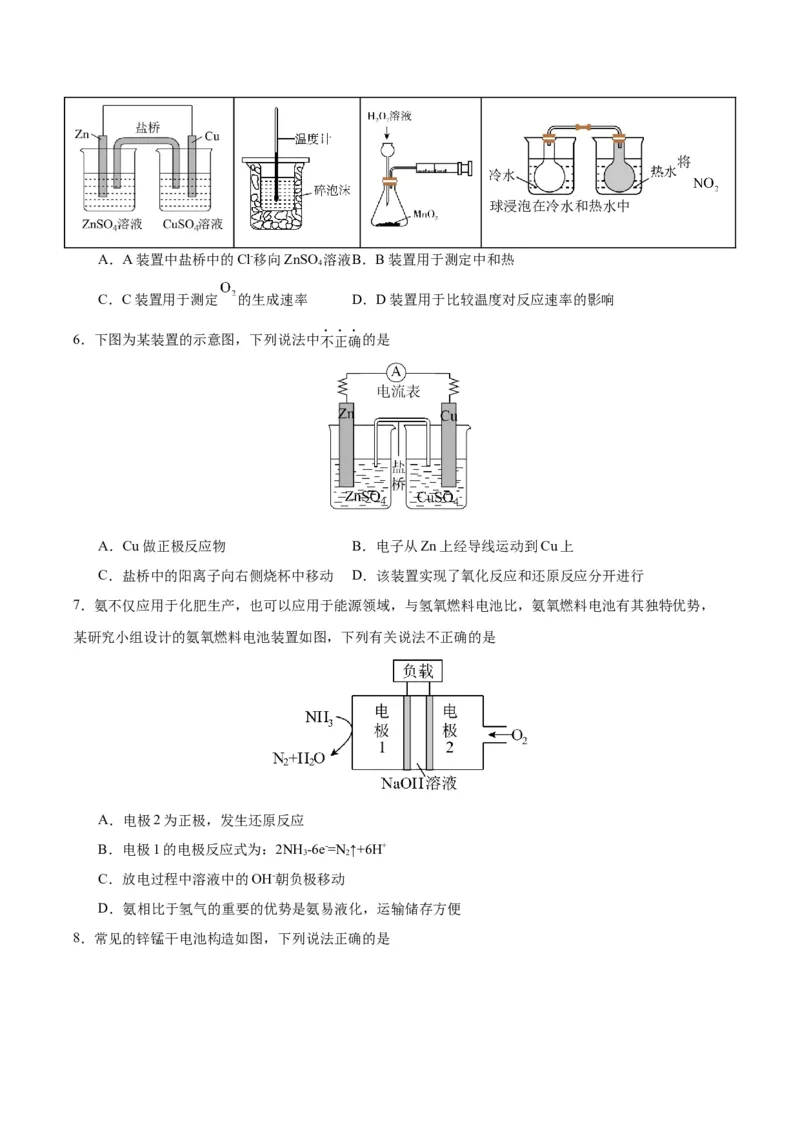
5.下列表述正确的是
A B C D将
球浸泡在冷水和热水中
A.A装置中盐桥中的Cl-移向ZnSO 溶液B.B装置用于测定中和热
4
C.C装置用于测定 的生成速率 D.D装置用于比较温度对反应速率的影响
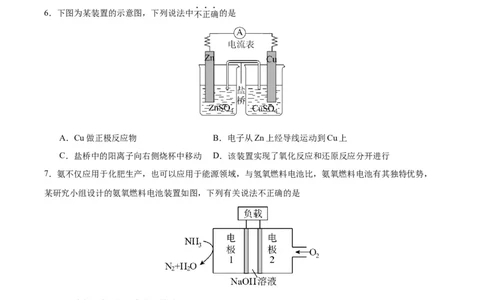
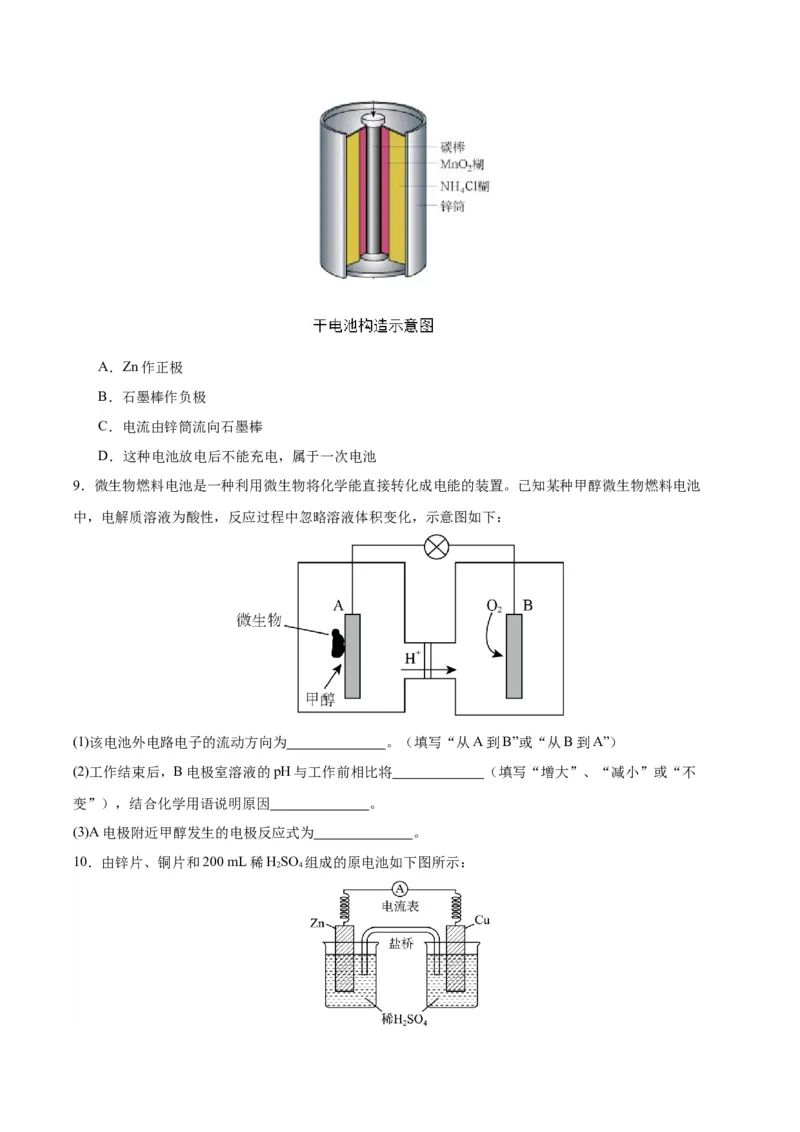
6.下图为某装置的示意图,下列说法中不正确的是
A.Cu做正极反应物 B.电子从Zn上经导线运动到Cu上
C.盐桥中的阳离子向右侧烧杯中移动 D.该装置实现了氧化反应和还原反应分开进行
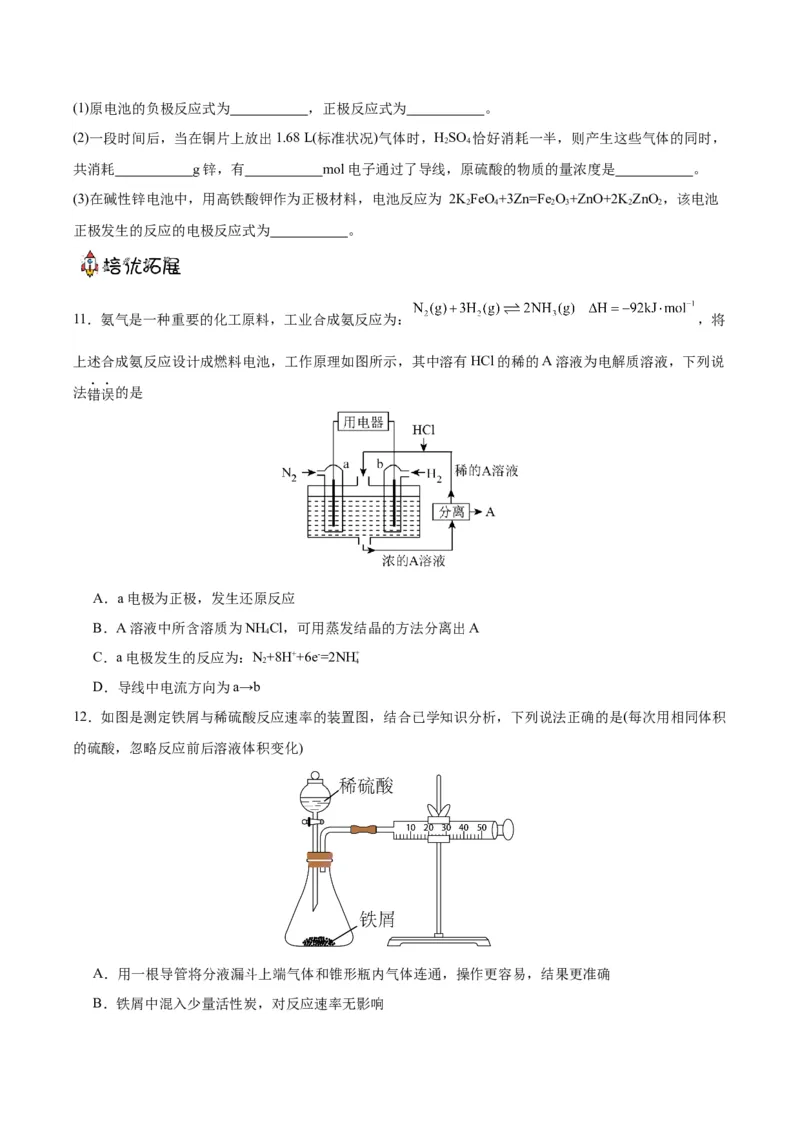
7.氨不仅应用于化肥生产,也可以应用于能源领域,与氢氧燃料电池比,氨氧燃料电池有其独特优势,
某研究小组设计的氨氧燃料电池装置如图,下列有关说法不正确的是
A.电极2为正极,发生还原反应
B.电极1的电极反应式为:2NH -6e-=N ↑+6H+
3 2
C.放电过程中溶液中的OH-朝负极移动
D.氨相比于氢气的重要的优势是氨易液化,运输储存方便
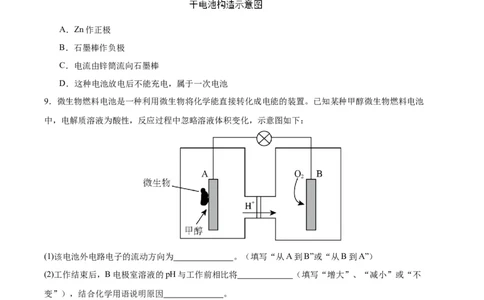
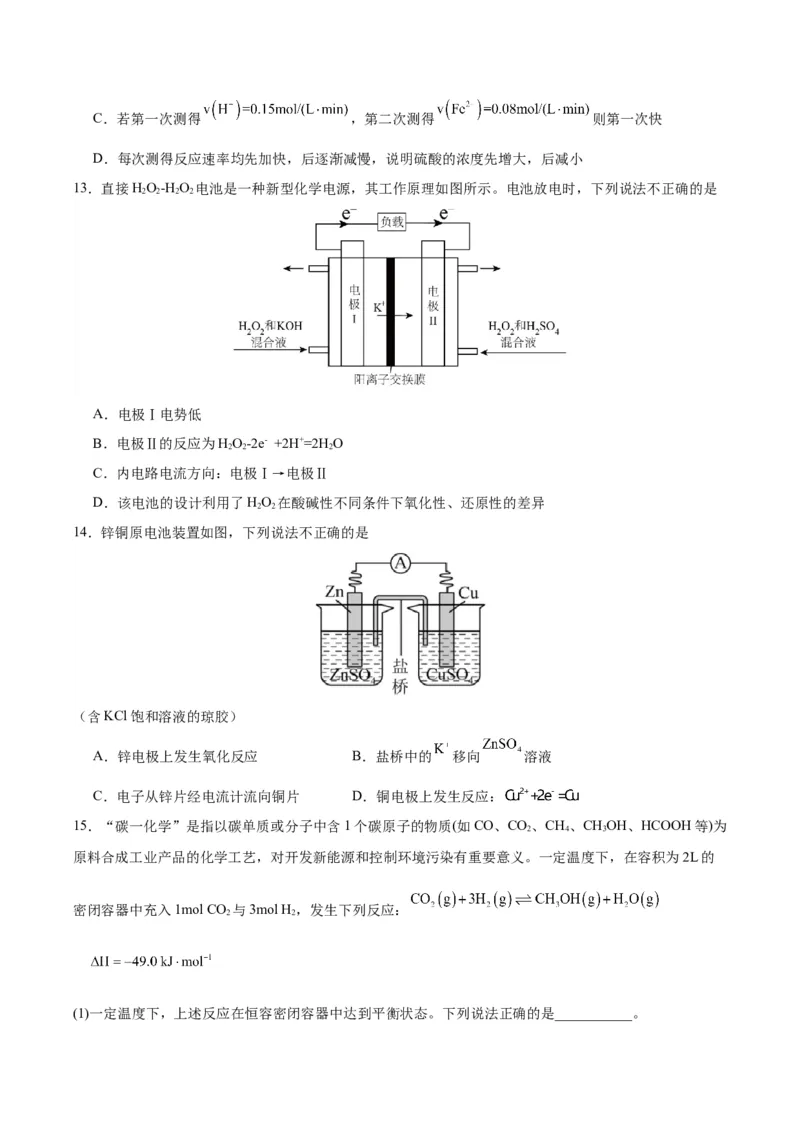
8.常见的锌锰干电池构造如图,下列说法正确的是A.Zn作正极
B.石墨棒作负极
C.电流由锌筒流向石墨棒
D.这种电池放电后不能充电,属于一次电池
9.微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池
中,电解质溶液为酸性,反应过程中忽略溶液体积变化,示意图如下:
(1)该电池外电路电子的流动方向为 。(填写“从A到B”或“从B到A”)
(2)工作结束后,B电极室溶液的pH与工作前相比将 (填写“增大”、“减小”或“不
变”),结合化学用语说明原因 。
(3)A电极附近甲醇发生的电极反应式为 。
10.由锌片、铜片和200 mL稀HSO 组成的原电池如下图所示:
2 4(1)原电池的负极反应式为 ,正极反应式为 。
(2)一段时间后,当在铜片上放出1.68 L(标准状况)气体时,HSO 恰好消耗一半,则产生这些气体的同时,
2 4
共消耗 g锌,有 mol电子通过了导线,原硫酸的物质的量浓度是 。
(3)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2KFeO+3Zn=Fe O+ZnO+2K ZnO,该电池
2 4 2 3 2 2
正极发生的反应的电极反应式为 。
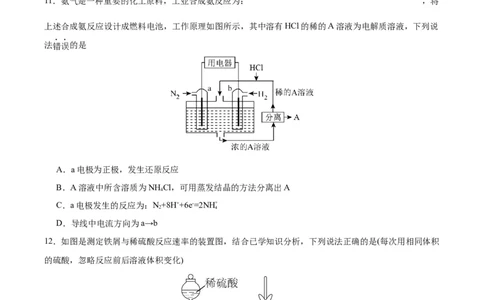
11.氨气是一种重要的化工原料,工业合成氨反应为: ,将
上述合成氨反应设计成燃料电池,工作原理如图所示,其中溶有HCl的稀的A溶液为电解质溶液,下列说
法错误的是
A.a电极为正极,发生还原反应
B.A溶液中所含溶质为NH Cl,可用蒸发结晶的方法分离出A
4
C.a电极发生的反应为:N+8H++6e-=2NH+
2 4
D.导线中电流方向为a→b
12.如图是测定铁屑与稀硫酸反应速率的装置图,结合已学知识分析,下列说法正确的是(每次用相同体积
的硫酸,忽略反应前后溶液体积变化)
A.用一根导管将分液漏斗上端气体和锥形瓶内气体连通,操作更容易,结果更准确
B.铁屑中混入少量活性炭,对反应速率无影响C.若第一次测得 ,第二次测得 则第一次快
D.每次测得反应速率均先加快,后逐渐减慢,说明硫酸的浓度先增大,后减小
13.直接HO-H O 电池是一种新型化学电源,其工作原理如图所示。电池放电时,下列说法不正确的是
2 2 2 2
A.电极Ⅰ电势低
B.电极Ⅱ的反应为HO-2e- +2H+=2H O
2 2 2
C.内电路电流方向:电极Ⅰ→电极Ⅱ
D.该电池的设计利用了HO 在酸碱性不同条件下氧化性、还原性的差异
2 2
14.锌铜原电池装置如图,下列说法不正确的是
(含KCl饱和溶液的琼胶)
A.锌电极上发生氧化反应 B.盐桥中的 移向 溶液
C.电子从锌片经电流计流向铜片 D.铜电极上发生反应:
15.“碳一化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO、CH、CHOH、HCOOH等)为
2 4 3
原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。一定温度下,在容积为2L的
密闭容器中充入1mol CO 与3mol H,发生下列反应:
2 2
(1)一定温度下,上述反应在恒容密闭容器中达到平衡状态。下列说法正确的是___________。A.加入催化剂,活化分子百分数不变
B.再额外通入适量H,H 的平衡转化率减小
2 2
C.充入少量氦气,CO 的平衡浓度减小
2
D.升高温度,正逆反应速率与CHOH的平衡浓度均减小
3
(2)若反应10min时达到平衡,H 的转化率为50%,则用CO 来表示反应从开始到平衡过程中的平均反应速
2 2
率是 。
(3)CO 还可与CH 制取,其原理为 。在密闭容器中通入等物质的量
2 4
的CH 与CO,在一定条件下发生反应,测得CH 的平衡转化率与温度及压强的关系如图所示,则压强
4 2 4
(填“>”或“<”) ; 时y点: (正) (填“>”、“”或“=”) (逆)。
(4)根据上述信息,在恒温恒容的密闭容器中通入 的混合气体,发生上述反应。下列
一定能说明该反应达到平衡状态的是___________。
A.混合气体的平均相对分子质量不再变化 B.
C.混合气体的密度不再变化 D.物质的总质量不再变化
(5)如图所示,甲醇燃料电池以甲醇为燃料,产生二氧化碳并实现化学能到电能的转化。则该电池中,甲醇
发生 反应,负极的电极反应式为 。