文档内容
4.1原电池(分层作业)
1.随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是
A.利用电池外壳的金属材料
B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C.不使电池中渗泄的电解液腐蚀其他物品
D.回收其中石墨电极
【答案】B
【解析】略
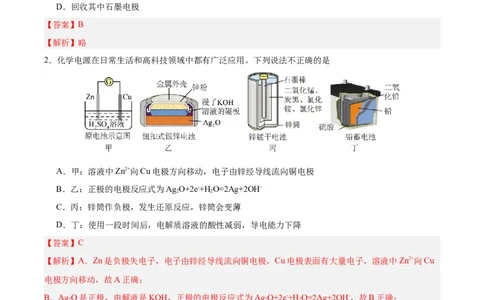
2.化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是
A.甲:溶液中Zn2+向Cu电极方向移动,电子由锌经导线流向铜电极
B.乙:正极的电极反应式为Ag O+2e-+H O=2Ag+2OH-
2 2
C.丙:锌筒作负极,发生还原反应,锌筒会变薄
D.丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
【答案】C
【解析】A.Zn是负极失电子,电子由锌经导线流向铜电极,Cu电极表面有大量电子,溶液中Zn2+向Cu
电极方向移动,故A正确;
B.Ag O是正极,电解液是KOH,正极的电极反应式为Ag O+2e-+H O=2Ag+2OH-,故B正确;
2 2 2
C.锌筒作负极,发生失电子的氧化反应,不是还原反应,故C错误;
D.铅蓄电池放电时总反应:Pb+PbO+2H SO =2PbSO+2H O,使用一段时间后,电解质溶液硫酸的浓度
2 2 4 4 2
减小,酸性减弱导电能力下降,故D正确;
故选C。
3.下列有关原电池的说法正确的是
A.活泼的金属不一定作负极 B.电池工作时,正极失去电子
C.电池工作时,负极发生还原反应 D.电解质溶液一定不能为浓硝酸【答案】A
【解析】A.原电池中,相对活泼的发生氧化反应的作负极,不一定是活泼金属,如Mg-NaOH-Al原电池
中,铝与氢氧化钠溶液发生自发的氧化还原反应,铝作负极,A正确;
B.原电池工作中,正极得电子,发生还原反应,B错误;
C.原电池工作中,正极得电子,发生还原反应,负极失去电子,发生氧化反应,C错误;
D.电解质溶液主要是起离子导体,传递电流的作用,可以是浓硝酸,D错误;
故选A。
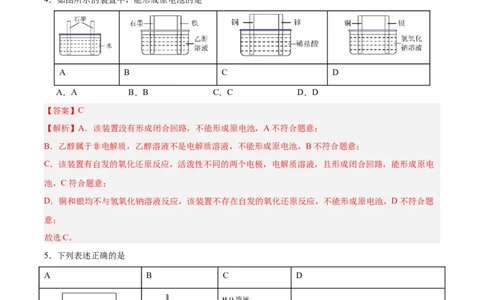
4.如图所示的装置中,能形成原电池的是
A B C D
A.A B.B C.C D.D
【答案】C
【解析】A.该装置没有形成闭合回路,不能形成原电池,A不符合题意;
B.乙醇属于非电解质,乙醇溶液不是电解质溶液,不能形成原电池,B不符合题意;
C.该装置有自发的氧化还原反应,活泼性不同的两个电极,电解质溶液,且形成闭合回路,能形成原电
池,C符合题意;
D.铜和银均不与氢氧化钠溶液反应,该装置不存在自发的氧化还原反应,不能形成原电池,D不符合题
意;
故选C。
5.下列表述正确的是
A B C D
将
球浸泡在冷水和热水中
A.A装置中盐桥中的Cl-移向ZnSO 溶液B.B装置用于测定中和热
4
C.C装置用于测定 的生成速率 D.D装置用于比较温度对反应速率的影响【答案】A
【解析】A.Zn比Cu活泼,Zn为负极,Zn极电极反应式为Zn-2e-=Zn2+,Cu为正极,Cu极电极反应式为
Cu2++2e-=Cu,盐桥中的阴离子Cl-移向ZnSO 溶液,A项正确;
4
B.测定中和热的装置中缺少了玻璃搅拌器,B项错误;
C.C装置中使用长颈漏斗,生成的O 会从长颈漏斗中逸出,注射器中不能准确测量生成的O 的体积,C
2 2
项错误;
D.NO 球中存在化学平衡2NO (g)⇌NO(g) ∆H<0,升高温度平衡逆向移动,颜色加深,降低温度平衡
2 2 2 4
正向移动,颜色变浅,用于探究温度对化学平衡的影响,不能探究温度对反应速率的影响,D项错误;
答案选A。
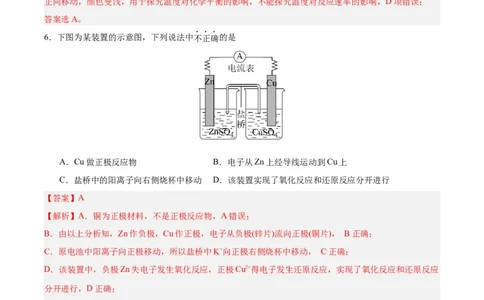
6.下图为某装置的示意图,下列说法中不正确的是
A.Cu做正极反应物 B.电子从Zn上经导线运动到Cu上
C.盐桥中的阳离子向右侧烧杯中移动 D.该装置实现了氧化反应和还原反应分开进行
【答案】A
【解析】A.铜为正极材料,不是正极反应物,A错误;
B.由以上分析知,Zn作负极,Cu作正极,电子从负极(锌片)流向正极(铜片), B正确;
C.原电池中阳离子向正极移动,所以盐桥中K+向正极右侧烧杯中移动, C正确;
D.该装置中,负极Zn失电子发生氧化反应,正极Cu2+得电子发生还原反应,实现了氧化反应和还原反应
分开进行,D正确;
故选A。
7.氨不仅应用于化肥生产,也可以应用于能源领域,与氢氧燃料电池比,氨氧燃料电池有其独特优势,
某研究小组设计的氨氧燃料电池装置如图,下列有关说法不正确的是A.电极2为正极,发生还原反应
B.电极1的电极反应式为:2NH -6e-=N ↑+6H+
3 2
C.放电过程中溶液中的OH-朝负极移动
D.氨相比于氢气的重要的优势是氨易液化,运输储存方便
【答案】B
【解析】A.电极2通入的氧气,根据氧元素的化合价只能降低判断,电极2做正极,发生还原反应,故
A正确;
B.电极1根据通入的氨气和出来的氮气与水利用电子、电荷、原子守恒及碱性溶液的环境书写电极反应
为:2NH -6e-+6OH-=N ↑+6H O,故B不正确;
3 2 2
C.原电池中阴离子向负极移动,C正确;
D.氨气易液化,氢气不易液化,因此氨相比于氢气的重要的优势是氨易液化,运输储存方便,D正确;
答案为B。
8.常见的锌锰干电池构造如图,下列说法正确的是
A.Zn作正极
B.石墨棒作负极
C.电流由锌筒流向石墨棒
D.这种电池放电后不能充电,属于一次电池【答案】D
【解析】A.放电时,Zn元素化合价由0价变为+2价,Zn电极上失电子发生氧化反应,做负极,故A错
误;
B.放电时,H元素化合价由+1价变为0价,所以石墨棒作正极,故B错误;
C.电流从电源的正极流向负极,即由石墨棒流向锌筒,故C错误;
D.常见锌锰干电池不能充电,所以属于一次电池,故D正确;
故选:D。
9.微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池
中,电解质溶液为酸性,反应过程中忽略溶液体积变化,示意图如下:
(1)该电池外电路电子的流动方向为 。(填写“从A到B”或“从B到A”)
(2)工作结束后,B电极室溶液的pH与工作前相比将 (填写“增大”、“减小”或“不
变”),结合化学用语说明原因 。
(3)A电极附近甲醇发生的电极反应式为 。
【答案】(1)从A到B
(2) 不变 B电极反应是O+4e-+4H+=2H O 当B电极消耗4mol氢离子同时,4mol氢离子通过离子
2 2
交换膜从A到B补充了消耗的氢离子,溶液总体积变化忽略不计,因此溶液pH不变
(3)CHOH-6e-+H O=CO+6H+
3 2 2
【解析】(1)该微生物的甲醇燃料电池中,通入甲醇(电极A)一极为负极,通入氧气(电极B)一极为
正极,该电池外电路电子的流动方向为负极到正极,即从A到B;
(2)电解质溶液为酸性,该电池的总反应式为:2CHOH+3O=2CO +4HO,总反应中并未消耗氢离
3 2 2 2
子,正极(电极B)反应式为:4H++O+4e-=2H O,当B电极消耗4mol氢离子同时,4mol氢离子通过
2 2
离子交换膜从A到B补充了消耗的氢离子,溶液总体积变化忽略不计,因此溶液pH不变;
(3)A电极为负极,发生氧化反应,甲醇失电子生成二氧化碳和氢离子,发生的电极反应式为:
CHOH-6e-+H O=CO+6H+。
3 2 210.由锌片、铜片和200 mL稀HSO 组成的原电池如下图所示:
2 4
(1)原电池的负极反应式为 ,正极反应式为 。
(2)一段时间后,当在铜片上放出1.68 L(标准状况)气体时,HSO 恰好消耗一半,则产生这些气体的同时,
2 4
共消耗 g锌,有 mol电子通过了导线,原硫酸的物质的量浓度是 。
(3)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2KFeO+3Zn=Fe O+ZnO+2K ZnO,该电池
2 4 2 3 2 2
正极发生的反应的电极反应式为 。
【答案】(1) Zn-2e-=Zn2+ 2H++2e-=H ↑
2
(2) 4.875 0.15 0.75 mol·L-1
(3)2FeO2- +6e—+5H O=Fe O+10OH-
4 2 2 3
【分析】由图可知,比铜金属性强的锌为原电池的负极,锌失去电子发生氧化反应生成锌离子,电极反应
式为Zn-2e-=Zn2+,铜为正极,氢离子在正极得到电子发生还原反应生成氢气,电极反应式为2H++2e-
=H ↑。
2
【解析】(1)由分析可知,负极的电极反应式为Zn-2e-=Zn2+,正极的电极反应式为2H++2e-=H ↑;
2
(2)由电极反应式可知,标准状况下铜片上放出1.68 L氢气时,反应转移电子和消耗氢离子的物质的量
1
1.68L 0.15mol× ×2
都为 ×2=0.15mol,则原硫酸的浓度为 2 =0.75mol/L,由得失电子数目守恒可
22.4L/mol
0.2L
1.68L
知,反应消耗锌的质量为 ×65g/mol=4.875g;
22.4L/mol
(3)由电池反应可知,高铁酸钾为原电池的正极,水分子作用下高铁酸根离子在正极得到电子发生还原
反应生成氧化铁和氢氧根离子,电极反应式为2FeO2- +6e—+5H O=Fe O+10OH-。
4 2 2 3
11.氨气是一种重要的化工原料,工业合成氨反应为: ,将
上述合成氨反应设计成燃料电池,工作原理如图所示,其中溶有HCl的稀的A溶液为电解质溶液,下列说法错误的是
A.a电极为正极,发生还原反应
B.A溶液中所含溶质为NH Cl,可用蒸发结晶的方法分离出A
4
C.a电极发生的反应为:N+8H++6e-=2NH+
2 4
D.导线中电流方向为a→b
【答案】B
【分析】由图可知,通入氮气的a电极为燃料电池的正极,酸性条件下氮气在正极得到电子发生还原反应
生成铵根离子,通入氢气的b电极为负极,氢气在负极失去电子发生氧化反应生成氢离子,放电得到的A
溶液为氯化铵溶液,浓溶液经冷却结晶、过滤得到氯化铵和可以循环使用的氯化铵的稀溶液。
【解析】A.由分析可知,通入氮气的a电极为燃料电池的正极,酸性条件下氮气在正极得到电子发生还
原反应生成铵根离子,故A正确;
B.氯化铵受热易分解,不能用蒸发结晶的方法分离得到,应用冷却结晶、过滤的方法得到氯化铵,故B
错误;
C.由分析可知,通入氮气的a电极为燃料电池的正极,酸性条件下氮气在正极得到电子发生还原反应生
成铵根离子,电极反应式为N+8H++6e-=2NH+ ,故C正确;
2 4
D.由分析可知,通入氮气的a电极为燃料电池的正极,通入氢气的b电极为负极,则导线中电流方向为
a→b,故D正确;
故选B。
12.如图是测定铁屑与稀硫酸反应速率的装置图,结合已学知识分析,下列说法正确的是(每次用相同体积
的硫酸,忽略反应前后溶液体积变化)A.用一根导管将分液漏斗上端气体和锥形瓶内气体连通,操作更容易,结果更准确
B.铁屑中混入少量活性炭,对反应速率无影响
C.若第一次测得 ,第二次测得 则第一次快
D.每次测得反应速率均先加快,后逐渐减慢,说明硫酸的浓度先增大,后减小
【答案】A
【解析】A.用导管将分液漏斗上端气体和锥形瓶内气体连通,可起到平衡气压和减小误差的作用,稀硫
酸更容易滴下,也能避免将加入硫酸的体积当做生成的氢气体积,选项A正确;
B.铁屑中混入少量活性炭,铁、C及稀硫酸构成原电池,能加快铁与稀硫酸的反应速率,选项B错误;
C.反应速率要用同一物质比较才能直接比较大小,若第二次v(Fe2+)=0.08mol/(L·min),则
v(H+)=2v(Fe2+)=2×0.08mol/(L·min)>0.15mol/(L·min),比第一次速率大,选项C错误;
D.反应速率先加快是因为该反应放热,温度升高,后减慢是因为硫酸浓度减小,选项D错误;
答案选A。
13.直接HO-H O 电池是一种新型化学电源,其工作原理如图所示。电池放电时,下列说法不正确的是
2 2 2 2
A.电极Ⅰ电势低
B.电极Ⅱ的反应为HO-2e- +2H+=2H O
2 2 2
C.内电路电流方向:电极Ⅰ→电极Ⅱ
D.该电池的设计利用了HO 在酸碱性不同条件下氧化性、还原性的差异
2 2【答案】B
【分析】原电池中,电解质溶液中的阳离子向正极移动。外电路中电子由负极流向正极;所以电极Ⅰ为负
极,失去电子,电极反应式为HO-2e- +2OH-=2H O+O;电极Ⅱ为正极,得电子,电极反应式为HO+2e-
2 2 2 2 2 2
+2H+=2H O;据此分析解题。
2
【解析】A.电极Ⅰ为负极,电势低,故A正确;
B.电极Ⅱ为正极,得电子,电极反应式为HO-2e- +2H+=2H O,故B错误;
2 2 2
C.电极Ⅰ为负极,电极Ⅱ为正极,内电路电流方向为电极Ⅰ→电极Ⅱ,故C正确;
D.HO 在不同的酸碱性条件下的氧化性、还原性不同,利用此可构建原电池,故D正确;
2 2
故答案选B。
14.锌铜原电池装置如图,下列说法不正确的是
(含KCl饱和溶液的琼胶)
A.锌电极上发生氧化反应 B.盐桥中的 移向 溶液
C.电子从锌片经电流计流向铜片 D.铜电极上发生反应:
【答案】B
【分析】由图可知,该装置为原电池,Zn比Cu活泼,Zn作负极,电极反应式为Zn−2e−=Zn2+,Cu作正
极,电极反应式为Cu2++2e−=Cu,据此作答。
【解析】A.Zn作负极,失电子,发生氧化反应,故A正确;
B.原电池工作时,阳离子向正极移动,因而K+移向硫酸铜溶液,故B错误;
C.原电池工作时,电子从负极(Zn)经电流计流向正极(Cu),故C正确;
D.Cu作正极,电极反应式为Cu2++2e−=Cu,故D正确;
故选B。
15.“碳一化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO、CH、CHOH、HCOOH等)为
2 4 3
原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。一定温度下,在容积为2L的
密闭容器中充入1mol CO 与3mol H,发生下列反应:
2 2(1)一定温度下,上述反应在恒容密闭容器中达到平衡状态。下列说法正确的是___________。
A.加入催化剂,活化分子百分数不变
B.再额外通入适量H,H 的平衡转化率减小
2 2
C.充入少量氦气,CO 的平衡浓度减小
2
D.升高温度,正逆反应速率与CHOH的平衡浓度均减小
3
(2)若反应10min时达到平衡,H 的转化率为50%,则用CO 来表示反应从开始到平衡过程中的平均反应速
2 2
率是 。
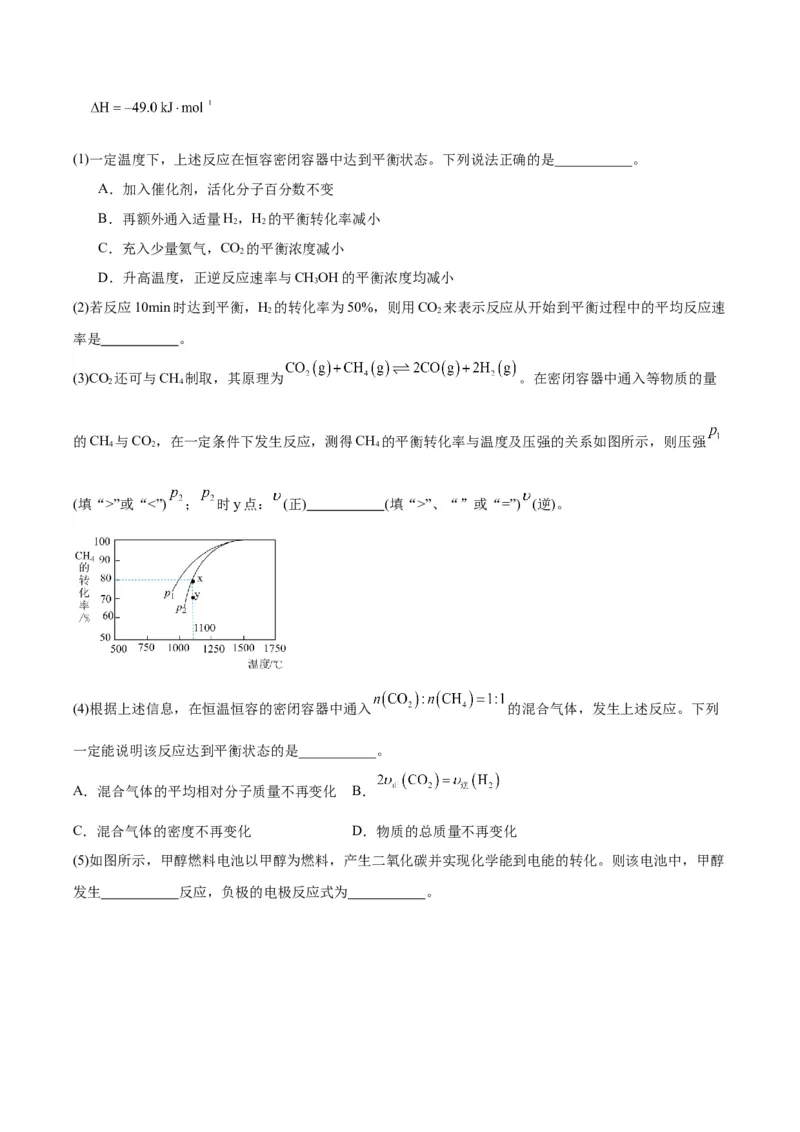
(3)CO 还可与CH 制取,其原理为 。在密闭容器中通入等物质的量
2 4
的CH 与CO,在一定条件下发生反应,测得CH 的平衡转化率与温度及压强的关系如图所示,则压强
4 2 4
(填“>”或“<”) ; 时y点: (正) (填“>”、“”或“=”) (逆)。
(4)根据上述信息,在恒温恒容的密闭容器中通入 的混合气体,发生上述反应。下列
一定能说明该反应达到平衡状态的是___________。
A.混合气体的平均相对分子质量不再变化 B.
C.混合气体的密度不再变化 D.物质的总质量不再变化
(5)如图所示,甲醇燃料电池以甲醇为燃料,产生二氧化碳并实现化学能到电能的转化。则该电池中,甲醇
发生 反应,负极的电极反应式为 。【答案】(1)B
(2)0.025mol•L-1•min-1
(3) < >
(4)B
(5) 氧化 CHOH+8OH--6e-=CO2- +6H O
5 3 2
【解析】(1)A.加入催化剂,降低了反应的活化能,活化分子数增加,活化分子百分数增加,A错误;
B.再额外通入适量H,平衡正向移动,但H 的平衡转化率减小,B正确;
2 2
C.充入少量氮气,恒容密闭容器,各物质的浓度不变,平衡不移动,CO 的平衡浓度不变,C错误;
2
D.升高温度,正逆反应速率均增大,平衡逆向移动,CHOH的平衡浓度减小,D错误,
3
故答案为:B;
(2)若反应10min时达到平衡,设CO 反应了xmol,则建立三段式:
2
CO(g) + 3H(g) ⇌ CHOH(g) + HO(g)
2 2 3 2
起始量(mol) 1 3
转化量(mol) x 3mol·50%
平衡量(mol)
1 3
由上可见: = (和方程式计量系数成比例)故:x=0.5mol,所以用CO 来表示反应从开始到平衡过
x 3×50% 2
△c 0.5mol
程中的平均反应速率ν(CO)= = =0.025mol•L-1•min-1,故答案为:0.025mol•L-1•min-1;
2 △t 2L·10min
(3)该反应正向为体积增大的方向,压强越大,CH 的转化率越小,已知相同温度下,P 条件下的转化率
4 1
大于P,则P 小于P,压强为P 时,在Y点反应未达到平衡,则反应正向移动,所以ν(正)大于ν(逆),故
2 1 2 2
答案为:<;>;
m
(4)A.混合气体的平均相对分子质量为M= ,反应过程中气体的总质量不变,气体的总物质的量也不
n变,则混合气体的平均相对分子质量始终不变,不能说明反应达到平衡状态,A错误;
B.2ν (CO)=ν (H ),说明正逆反应速率相等,反应达到平衡状态,B正确;
正 2 逆 2
C.反应过程中气体的总质量不变,容器的容积不变,则混合气体的密度始终不变,不能说明反应达到平
衡状态,C错误;
D.反应过程中气体的总质量不变,则气体的总质量不再变化不能说明反应达到平衡状态,D错误;
故答案为:B;
(5)该燃料电池中负极上甲醇失电子和NaOH反应生成碳酸钠和水,正极上氧气得电子生成氢氧根离
子,因此甲醇发生氧化反应;放电时电解质溶液中阴离子向负极移动、阳离子向正极移动,负极反应式为
CHOH+8OH--6e-=CO2- +6H O,故答案为:氧化;CHOH+8OH--6e-=CO2- +6H O。
5 3 2 5 3 2