文档内容
押广东卷第 15 题
化学反应速率与平衡 水溶液中的离子平衡
核心考点 考情统计 考向预测 备考策略
2023·广东卷,15
化学反应 考查反应机理和催化剂,平衡 1.化学平衡和反应速率的题
2022·广东卷,13,
速率与平 移动的影响因素,体现综合 目,应以分析图像为主,尤其
15
衡 性; 是曲线的分析。
2021·广东卷,14
考查溶液中的离子平衡,涉及 2.水溶液中的离子平衡,广
溶液中发生的反应,离子浓度 东卷大概率出现在原理大题,
水溶液中
大小比较,体现综合性和应用 选择题以基础为主,应回归基
的离子平 2021·广东卷,8
性。 本图像。
衡
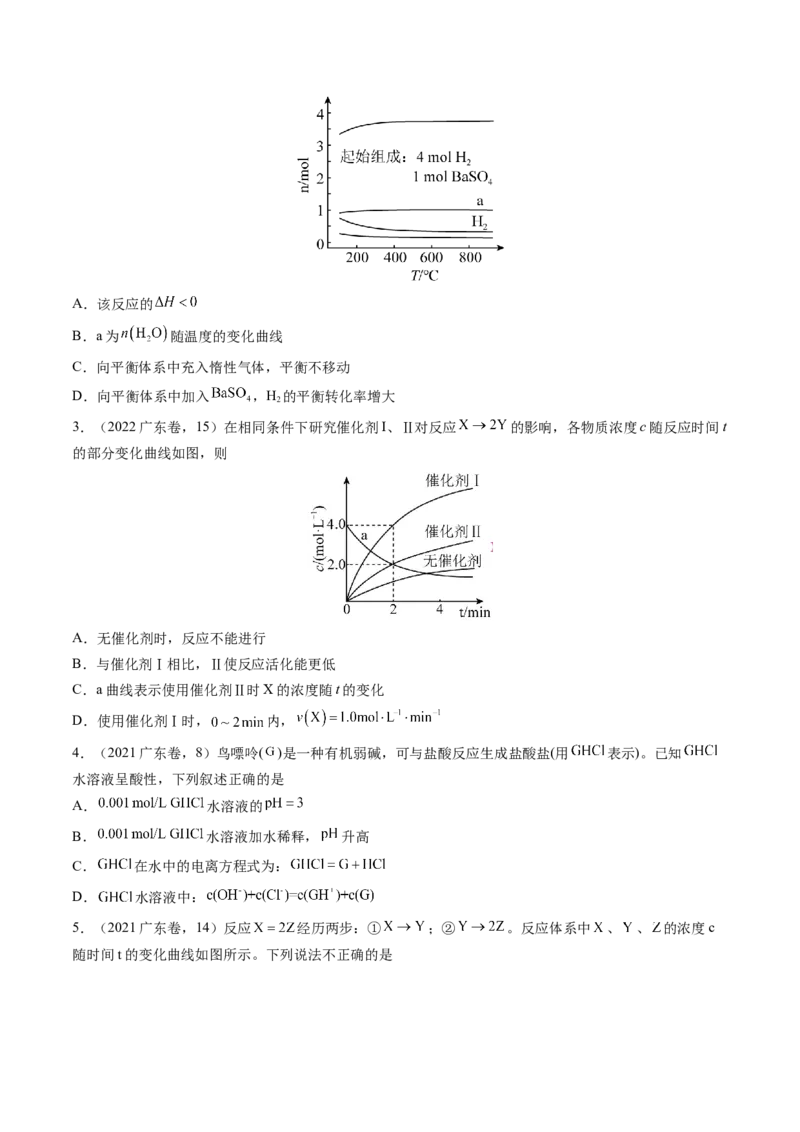
1.(2023广东卷,15)催化剂Ⅰ和Ⅱ均能催化反应 。反应历程(下图)中,M为中间产物。其
它条件相同时,下列说法不正确的是
A.使用Ⅰ和Ⅱ,反应历程都分4步进行 B.反应达平衡时,升高温度,R的浓度增大
C.使用Ⅱ时,反应体系更快达到平衡 D.使用Ⅰ时,反应过程中M所能达到的最高浓度更大
2.(2022广东卷,13)恒容密闭容器中, 在不同温度下达平衡
时,各组分的物质的量(n)如图所示。下列说法正确的是A.该反应的
B.a为 随温度的变化曲线
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入 ,H 的平衡转化率增大
2
3.(2022广东卷,15)在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反应时间t
的部分变化曲线如图,则
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时, 内,
4.(2021广东卷,8)鸟嘌呤( )是一种有机弱碱,可与盐酸反应生成盐酸盐(用 表示)。已知
水溶液呈酸性,下列叙述正确的是
A. 水溶液的
B. 水溶液加水稀释, 升高
C. 在水中的电离方程式为:
D. 水溶液中:
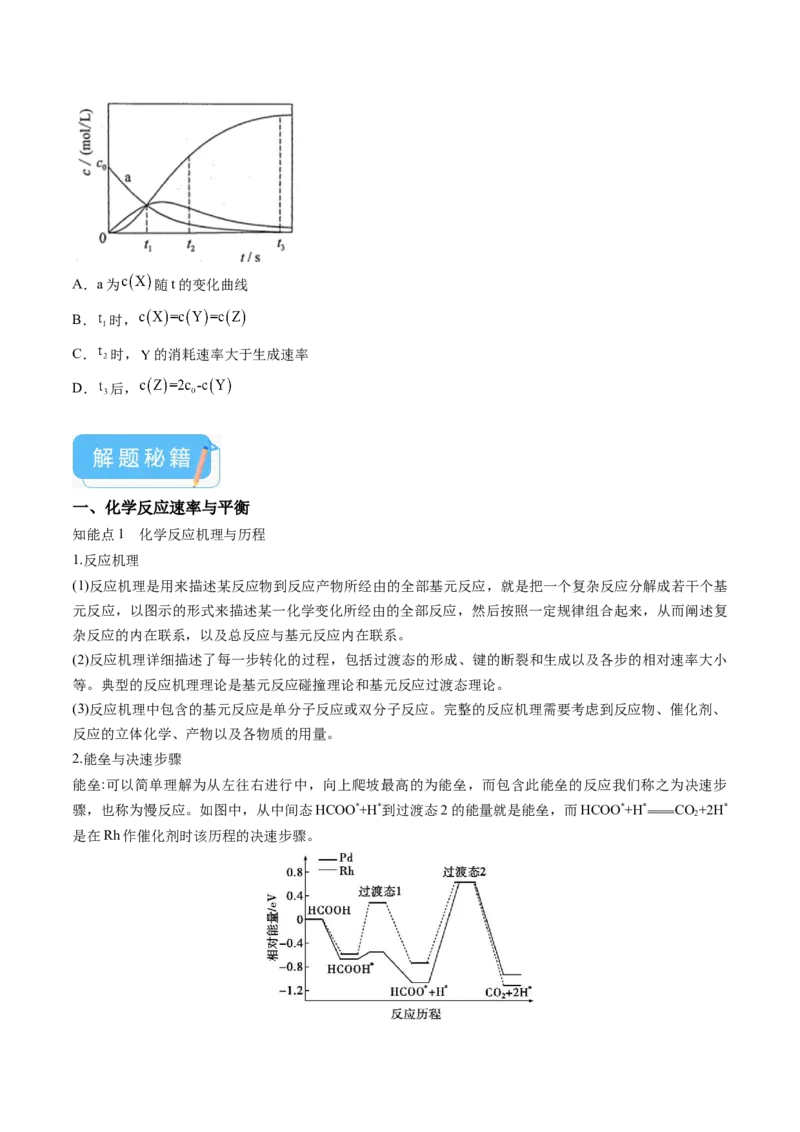
5.(2021广东卷,14)反应 经历两步:① ;② 。反应体系中 、 、 的浓度c
随时间t的变化曲线如图所示。下列说法不正确的是A.a为 随t的变化曲线
B. 时,
C. 时, 的消耗速率大于生成速率
D. 后,
一、化学反应速率与平衡
知能点1 化学反应机理与历程
1.反应机理
(1)反应机理是用来描述某反应物到反应产物所经由的全部基元反应,就是把一个复杂反应分解成若干个基
元反应,以图示的形式来描述某一化学变化所经由的全部反应,然后按照一定规律组合起来,从而阐述复
杂反应的内在联系,以及总反应与基元反应内在联系。
(2)反应机理详细描述了每一步转化的过程,包括过渡态的形成、键的断裂和生成以及各步的相对速率大小
等。典型的反应机理理论是基元反应碰撞理论和基元反应过渡态理论。
(3)反应机理中包含的基元反应是单分子反应或双分子反应。完整的反应机理需要考虑到反应物、催化剂、
反应的立体化学、产物以及各物质的用量。
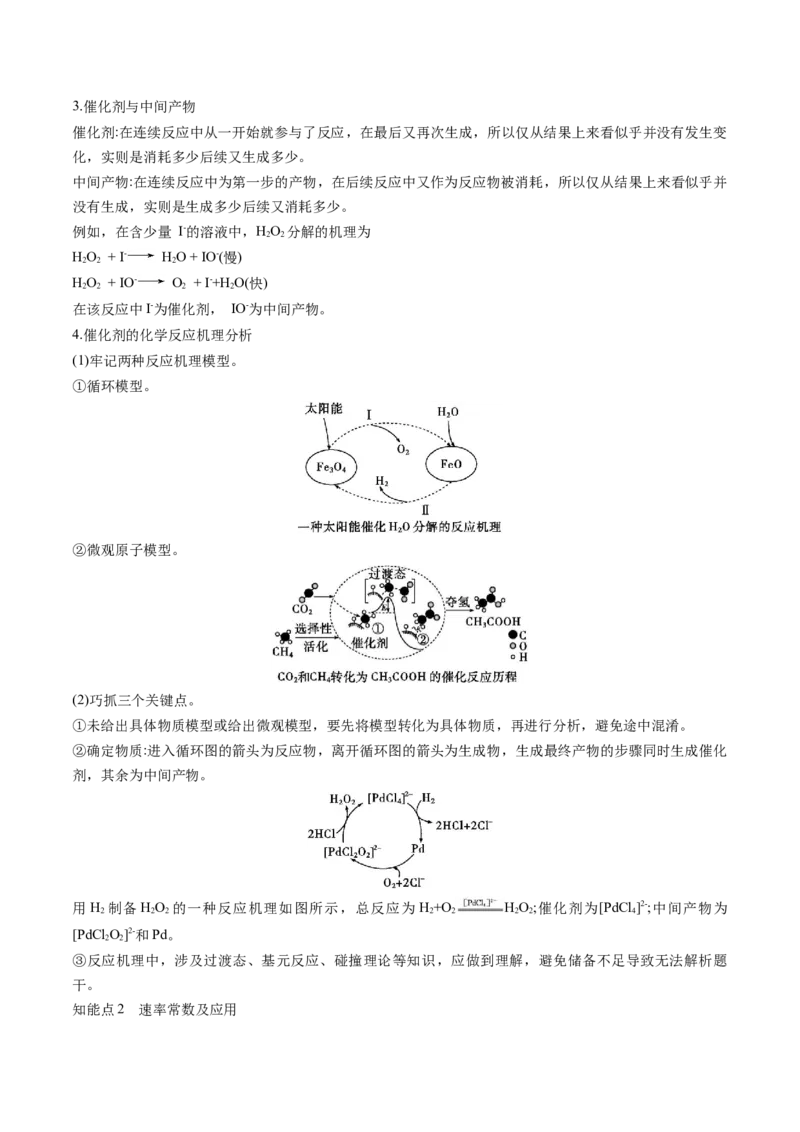
2.能垒与决速步骤
能垒:可以简单理解为从左往右进行中,向上爬坡最高的为能垒,而包含此能垒的反应我们称之为决速步
骤,也称为慢反应。如图中,从中间态HCOO*+H*到过渡态2的能量就是能垒,而HCOO*+H* CO+2H*
2
是在Rh作催化剂时该历程的决速步骤。3.催化剂与中间产物
催化剂:在连续反应中从一开始就参与了反应,在最后又再次生成,所以仅从结果上来看似乎并没有发生变
化,实则是消耗多少后续又生成多少。
中间产物:在连续反应中为第一步的产物,在后续反应中又作为反应物被消耗,所以仅从结果上来看似乎并
没有生成,实则是生成多少后续又消耗多少。
例如,在含少量 I-的溶液中,HO 分解的机理为
2 2
HO + I- HO + IO-(慢)
2 2 2
HO + IO- O + I-+H O(快)
2 2 2 2
在该反应中I-为催化剂, IO-为中间产物。
4.催化剂的化学反应机理分析
(1)牢记两种反应机理模型。
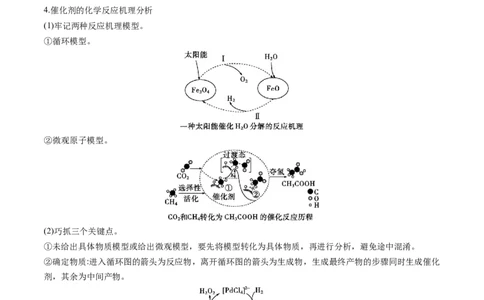
①循环模型。
②微观原子模型。
(2)巧抓三个关键点。
①未给出具体物质模型或给出微观模型,要先将模型转化为具体物质,再进行分析,避免途中混淆。
②确定物质:进入循环图的箭头为反应物,离开循环图的箭头为生成物,生成最终产物的步骤同时生成催化
剂,其余为中间产物。
用H 制备HO 的一种反应机理如图所示,总反应为 H+O HO;催化剂为[PdCl ]2-;中间产物为
2 2 2 2 2 2 2 4
[PdCl O]2-和Pd。
2 2
③反应机理中,涉及过渡态、基元反应、碰撞理论等知识,应做到理解,避免储备不足导致无法解析题
干。
知能点2 速率常数及应用1.设基元反应(能够一步完成的反应)为aA(g)+bB(g) cC(g)+dD(g),其速率可表示为v=k·ca(A)·cb(B),式
中的k称为反应速率常数或速率常数,它表示单位浓度下的化学反应速率,与浓度无关,但受温度、催化
剂、固体表面性质等因素的影响,通常反应速率常数越大,反应进行得越快。不同反应有不同的速率常
数。
2.正、逆反应的速率常数与平衡常数的关系
对于基元反应 aA(g)+bB(g) cC(g)+dD(g),v =k ·ca(A)·cb(B),v =k ·cc(C)·cd(D),平衡常数 K=
正 正 逆 逆
cc(C)·cd(D) k ·v k
正 逆 正
= ,反应达到平衡时v =v ,故K= 。
ca(A)·cb(B) k ·v 正 逆 k
逆 正 逆
知能点3 化学反应速率及平衡图像分析
1.速率与平衡图像常见类型
(1)速率变化图像。
对于反应mA(g)+nB(g) pC(g)+qD(g),ΔH>0。
①v 、v 同时突变。
正 逆
②v 、v 之一渐变。
正 逆
(2)平衡移动图像。
对于反应mA(g)+nB(g) pC(g)+qD(g),m+n>p+q,且ΔH>0。
①速率-时间图——注意断点。
②转化率(或含量)-时间图——先拐先平。(3)恒压(温)曲线。
分析时可沿横轴作一条平行于纵轴的虚线,即为等压线或等温线,然后分析另一条件变化对该反应的影
响。
2.陌生图像关键点的分析
(1)
(2)
(3)对于反应A(g)+2B(g) C(g)
(4)
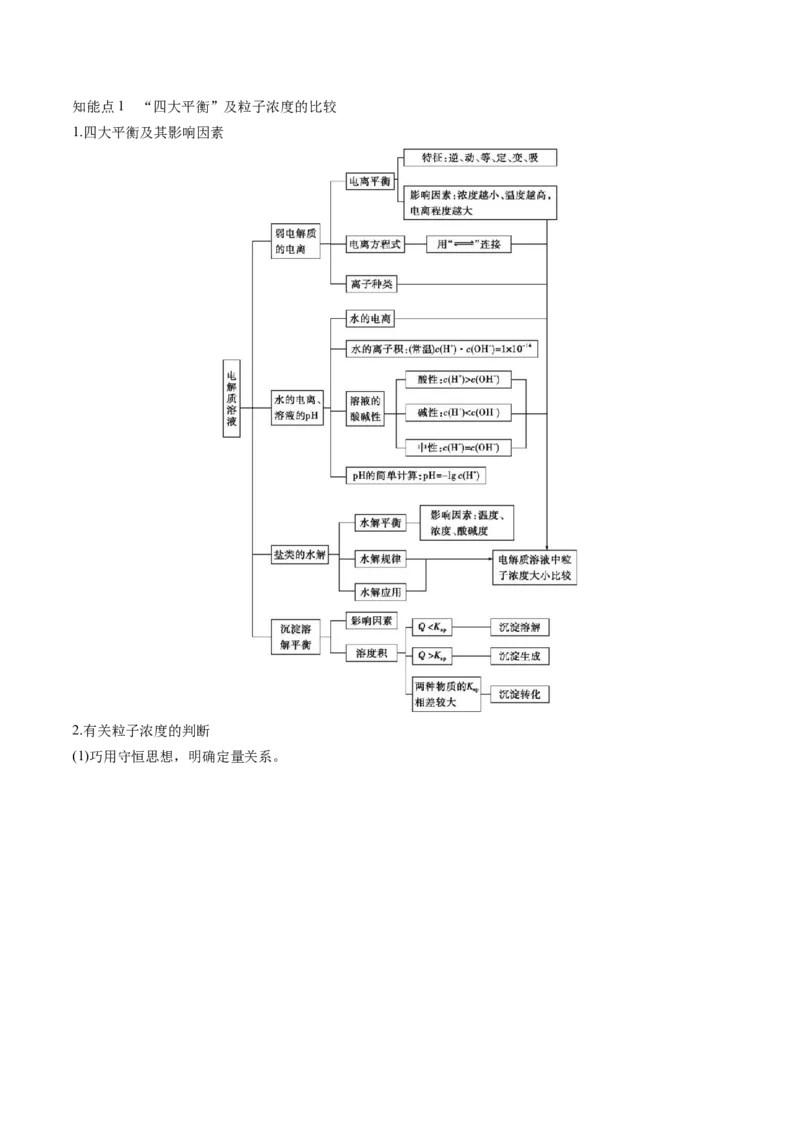
一、水溶液中的离子平衡知能点1 “四大平衡”及粒子浓度的比较
1.四大平衡及其影响因素
2.有关粒子浓度的判断
(1)巧用守恒思想,明确定量关系。(2)溶液中粒子浓度大小比较解题流程。
知能点2 K 、K、K、K 、K 之间的关系
w a b sp h
1.平衡常数之间的关系
已知:常温下,HS的电离常数为K 、K ,Cu(OH) 、CuS、Ag S的溶度积常数分别为K 、K ′、K ″。
2 a1 a2 2 2 sp sp sp
(1)水解常数与电离常数、水的离子积之间的关系。
K K
常温下的NaS溶液中,S2-的水解常数K = w ,HS-的水解常数K = w 。
2 h1 K h2 K
a2 a1
(2)水解常数与溶度积、水的离子积之间的关系。
K2
常温下的CuCl 溶液中,Cu2+的水解常数K= w。
2 h
K
sp
(3)平衡常数与电离常数、溶度积之间的关系。K '
①反应CuS(s)+2Ag+(aq) Cu2+(aq)+Ag S(s)的平衡常数K= sp 。
2 K ″
sp
K '
②反应CuS(s)+2H+(aq) Cu2+(aq)+H S(aq)的平衡常数K= sp 。
2 K ·K
a1 a2
(4)判断溶液的酸碱性。
NaHS溶液呈碱性,离子浓度大小顺序为c(Na+)>c(HS-)>c(OH-)>c(H+)>c(S2-)。
K
上述判断的理由是HS-的水解常数( w )大于其电离常数(K )。
K a2
a1
2.根据图形节点求算弱电解质的电离平衡常数
(1)由图形起点计算平衡常数。
(2)由图形交点计算平衡常数。
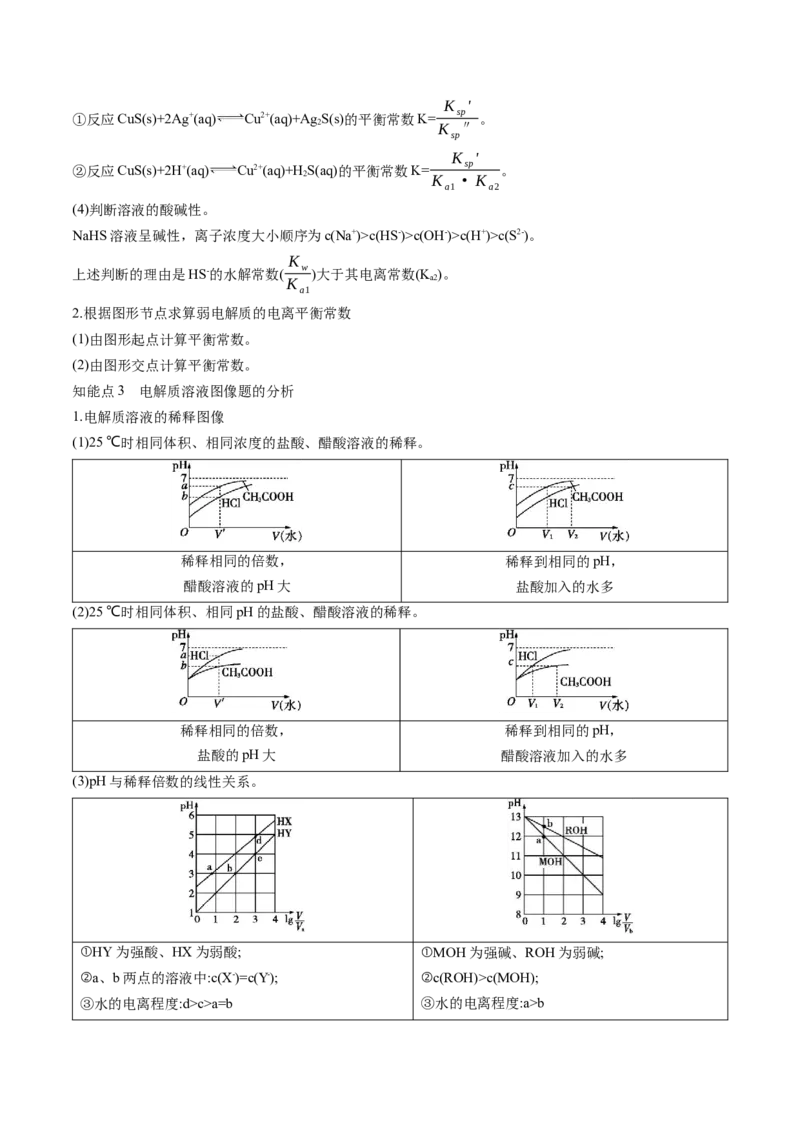
知能点3 电解质溶液图像题的分析
1.电解质溶液的稀释图像
(1)25 ℃时相同体积、相同浓度的盐酸、醋酸溶液的稀释。
稀释相同的倍数, 稀释到相同的pH,
醋酸溶液的pH大 盐酸加入的水多
(2)25 ℃时相同体积、相同pH的盐酸、醋酸溶液的稀释。
稀释相同的倍数, 稀释到相同的pH,
盐酸的pH大 醋酸溶液加入的水多
(3)pH与稀释倍数的线性关系。
①HY为强酸、HX为弱酸; ①MOH为强碱、ROH为弱碱;
②a、b两点的溶液中:c(X-)=c(Y-); ②c(ROH)>c(MOH);
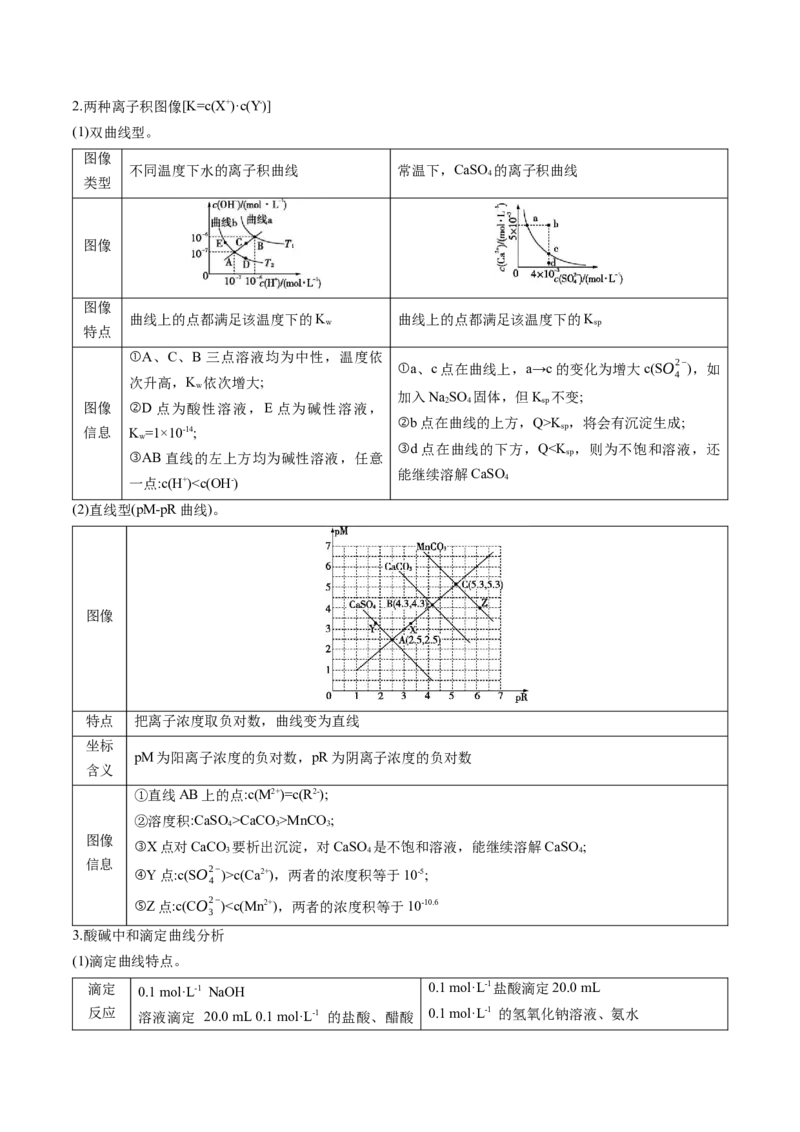
③水的电离程度:d>c>a=b ③水的电离程度:a>b2.两种离子积图像[K=c(X+)·c(Y-)]
(1)双曲线型。
图像
不同温度下水的离子积曲线 常温下,CaSO 的离子积曲线
4
类型
图像
图像
曲线上的点都满足该温度下的K 曲线上的点都满足该温度下的K
w sp
特点
①A、C、B三点溶液均为中性,温度依
①a、c点在曲线上,a→c的变化为增大c(SO2−
),如
4
次升高,K 依次增大;
w
加入NaSO 固体,但K 不变;
2 4 sp
图像 ②D 点为酸性溶液,E 点为碱性溶液,
②b点在曲线的上方,Q>K ,将会有沉淀生成;
信息 K =1×10-14; sp
w
③d点在曲线的下方,QCaCO >MnCO;
4 3 3
图像
③X点对CaCO 要析出沉淀,对CaSO 是不饱和溶液,能继续溶解CaSO;
3 4 4
信息
④Y点:c(SO2− )>c(Ca2+),两者的浓度积等于10-5;
4
⑤Z点:c(CO2− )7 强酸与弱碱反应时,终点pH<7
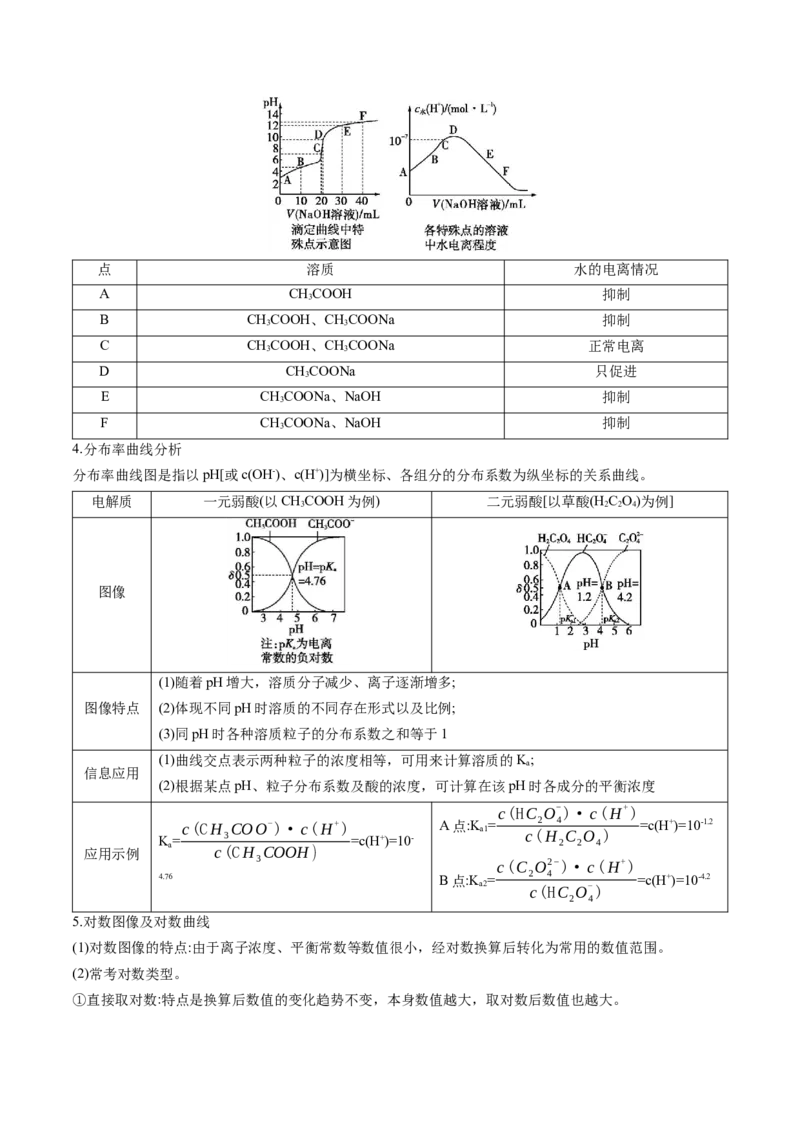
pH
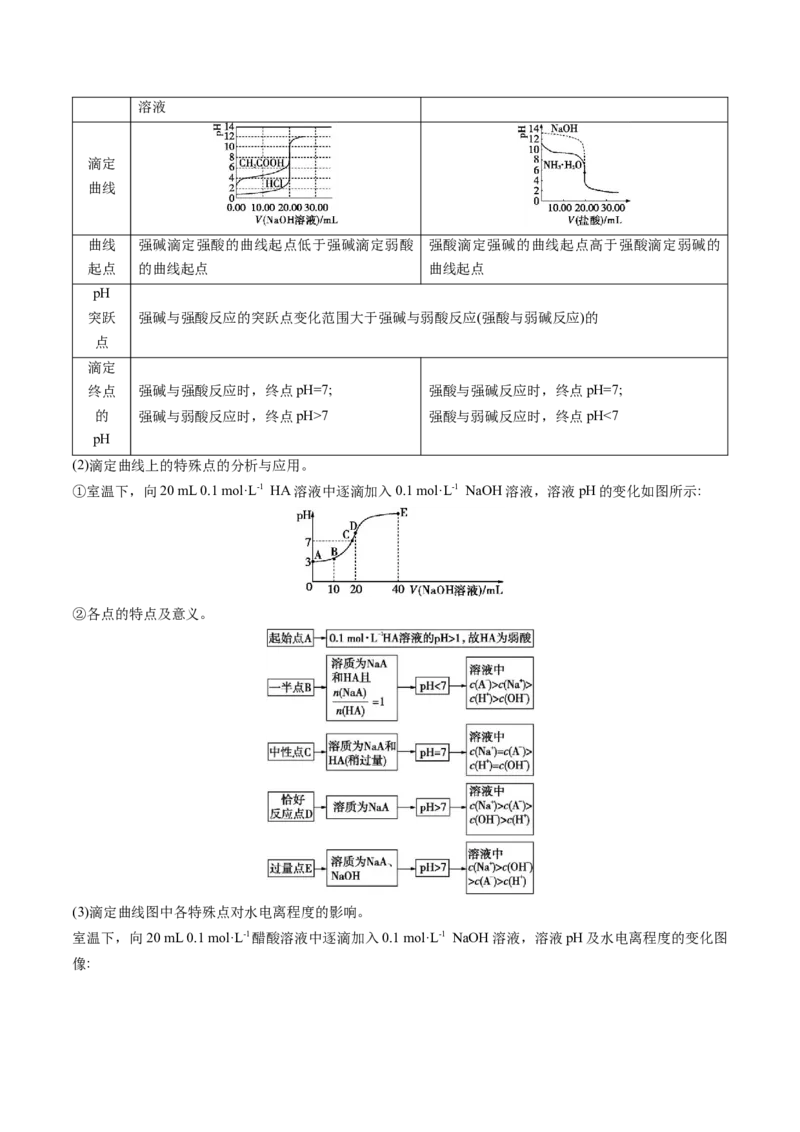
(2)滴定曲线上的特殊点的分析与应用。
①室温下,向20 mL 0.1 mol·L-1 HA溶液中逐滴加入0.1 mol·L-1 NaOH溶液,溶液pH的变化如图所示:
②各点的特点及意义。
(3)滴定曲线图中各特殊点对水电离程度的影响。
室温下,向20 mL 0.1 mol·L-1醋酸溶液中逐滴加入0.1 mol·L-1 NaOH溶液,溶液pH及水电离程度的变化图
像:点 溶质 水的电离情况
A CHCOOH 抑制
3
B CHCOOH、CHCOONa 抑制
3 3
C CHCOOH、CHCOONa 正常电离
3 3
D CHCOONa 只促进
3
E CHCOONa、NaOH 抑制
3
F CHCOONa、NaOH 抑制
3
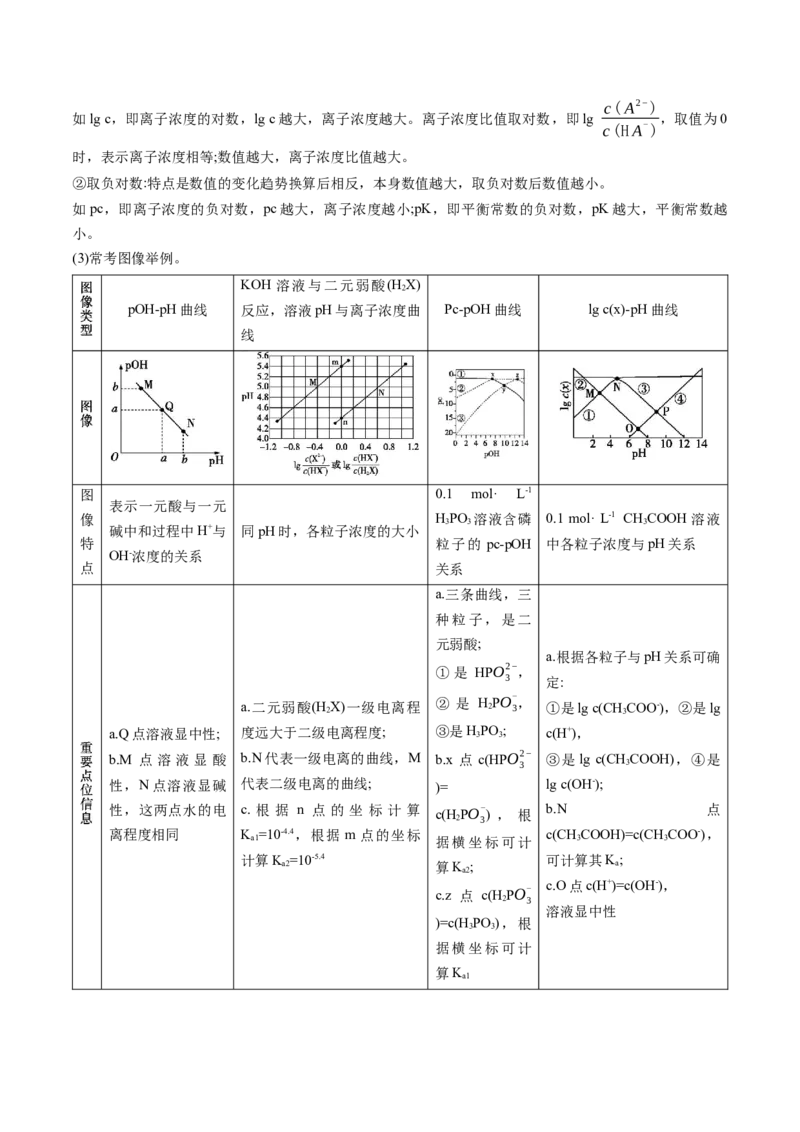
4.分布率曲线分析
分布率曲线图是指以pH[或c(OH-)、c(H+)]为横坐标、各组分的分布系数为纵坐标的关系曲线。
电解质 一元弱酸(以CHCOOH为例) 二元弱酸[以草酸(H C O)为例]
3 2 2 4
图像
(1)随着pH增大,溶质分子减少、离子逐渐增多;
图像特点 (2)体现不同pH时溶质的不同存在形式以及比例;
(3)同pH时各种溶质粒子的分布系数之和等于1
(1)曲线交点表示两种粒子的浓度相等,可用来计算溶质的K;
a
信息应用
(2)根据某点pH、粒子分布系数及酸的浓度,可计算在该pH时各成分的平衡浓度
c(HC O-)·c(H+)
应用示例 K a = c(CH c( 3 C C O H O C - O )· OH c( ) H+) =c(H+)=10- A点:K a1 = c( 2 H 4 2 C 2 O 4 ) =c(H+)=10-1.2
3 c(C O2−)·c(H+)
4.76 B点:K = 2 4 =c(H+)=10-4.2
a2 c(HC O-)
2 4
5.对数图像及对数曲线
(1)对数图像的特点:由于离子浓度、平衡常数等数值很小,经对数换算后转化为常用的数值范围。
(2)常考对数类型。
①直接取对数:特点是换算后数值的变化趋势不变,本身数值越大,取对数后数值也越大。c(A2−)
如lg c,即离子浓度的对数,lg c越大,离子浓度越大。离子浓度比值取对数,即lg ,取值为0
c(HA-)
时,表示离子浓度相等;数值越大,离子浓度比值越大。
②取负对数:特点是数值的变化趋势换算后相反,本身数值越大,取负对数后数值越小。
如pc,即离子浓度的负对数,pc越大,离子浓度越小;pK,即平衡常数的负对数,pK越大,平衡常数越
小。
(3)常考图像举例。
KOH 溶液与二元弱酸(H X)
2
pOH-pH曲线 反应,溶液pH与离子浓度曲 Pc-pOH曲线 lg c(x)-pH曲线
线
图 0.1 mol· L-1
表示一元酸与一元
像 HPO 溶液含磷 0.1 mol· L-1 CHCOOH 溶液
3 3 3
碱中和过程中H+与 同pH时,各粒子浓度的大小
特 粒子的 pc-pOH 中各粒子浓度与pH关系
OH-浓度的关系
点 关系
a.三条曲线,三
种粒子,是二
元弱酸;
a.根据各粒子与pH关系可确
① 是
HPO2−
,
3 定:
a.二元弱酸(H 2 X)一级电离程 ② 是 H 2 PO 3 - , ①是lg c(CH 3 COO-),②是lg
a.Q点溶液显中性; 度远大于二级电离程度; ③是H 3 PO 3 ; c(H+),
b.M 点 溶 液 显 酸 b.N代表一级电离的曲线,M b.x 点 c(HPO2− ③是 lg c(CHCOOH),④是
3 3
性,N点溶液显碱 代表二级电离的曲线; )= lg c(OH-);
性,这两点水的电 c. 根 据 n 点 的 坐 标 计 算 c(HPO-
) , 根
b.N 点
2 3
离程度相同 K =10-4.4,根据 m 点的坐标 c(CHCOOH)=c(CH COO-),
a1 据横坐标可计 3 3
计算K =10-5.4 可计算其K;
a2 算K ; a
a2
c.O点c(H+)=c(OH-),
c.z 点
c(HPO-
2 3
溶液显中性
)=c(H PO ),根
3 3
据横坐标可计
算K
a1考点一 化学反应速率与平衡
1.(2024届广东省省二模)液化石油气的主要成分C H 在光照条件下与Cl 反应,可得到各种氯代丙
3 8 2
烷。已知:
①C H 与Cl 反应的机理为自由基反应,包括以下几步:
3 8 2
Ⅰ.链引发:
Ⅱ.链传递: , ,……
Ⅲ.链终止: , ,……
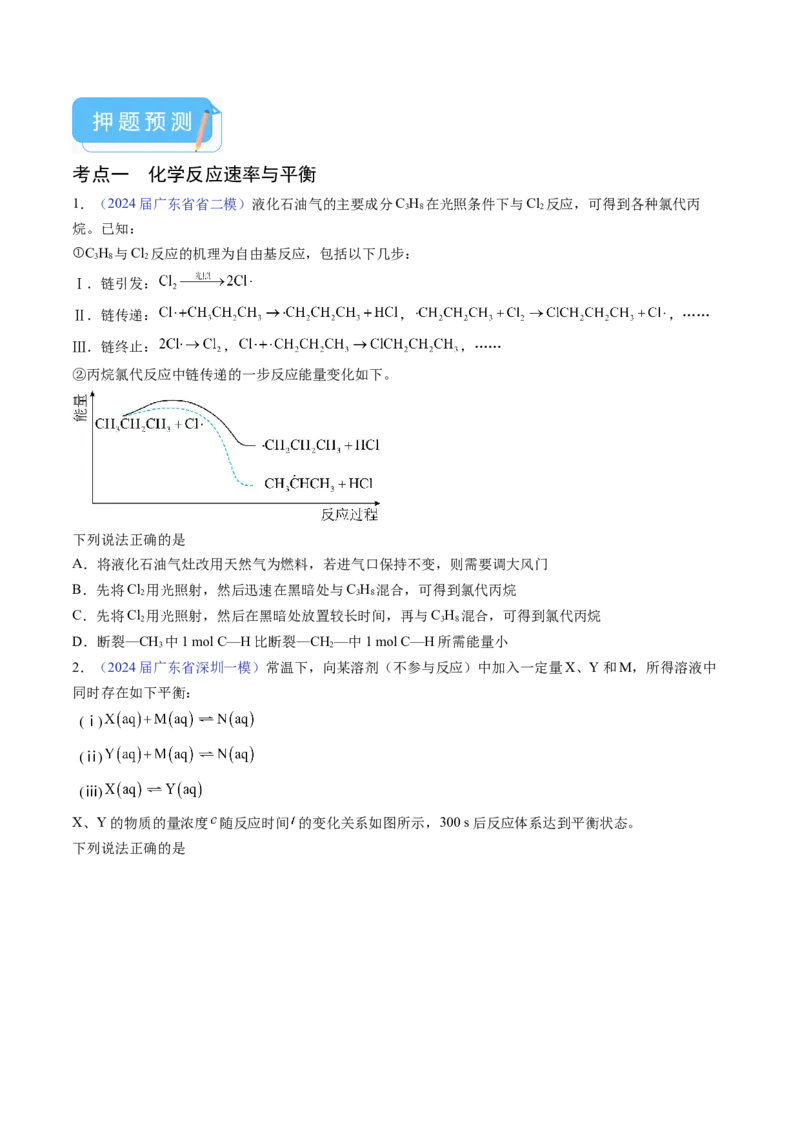
②丙烷氯代反应中链传递的一步反应能量变化如下。
下列说法正确的是
A.将液化石油气灶改用天然气为燃料,若进气口保持不变,则需要调大风门
B.先将Cl 用光照射,然后迅速在黑暗处与C H 混合,可得到氯代丙烷
2 3 8
C.先将Cl 用光照射,然后在黑暗处放置较长时间,再与C H 混合,可得到氯代丙烷
2 3 8
D.断裂—CH 中1 mol C—H比断裂—CH—中1 mol C—H所需能量小
3 2
2.(2024届广东省深圳一模)常温下,向某溶剂(不参与反应)中加入一定量X、Y和M,所得溶液中
同时存在如下平衡:
(ⅰ)
(ⅱ)
(ⅲ)
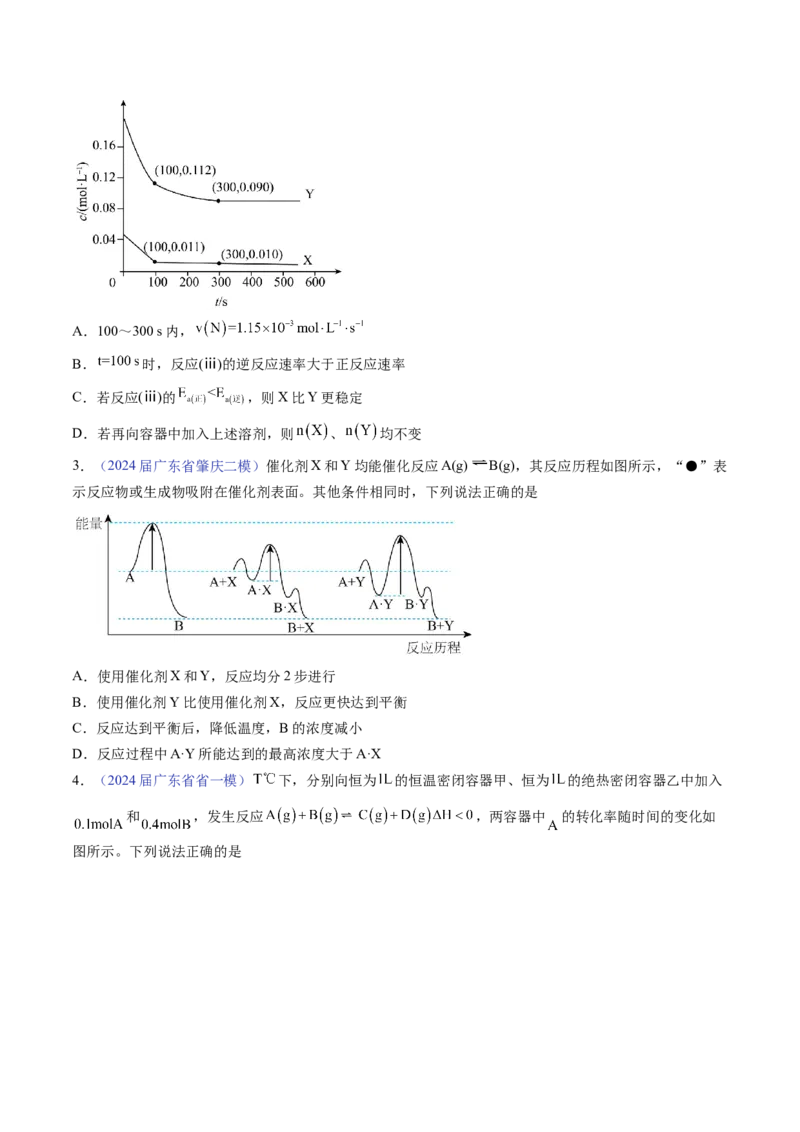
X、Y的物质的量浓度 随反应时间 的变化关系如图所示,300 s后反应体系达到平衡状态。
下列说法正确的是A.100~300 s内,
B. 时,反应(ⅲ)的逆反应速率大于正反应速率
C.若反应(ⅲ)的 ,则X比Y更稳定
D.若再向容器中加入上述溶剂,则 、 均不变
3.(2024届广东省肇庆二模)催化剂X和Y均能催化反应A(g) B(g),其反应历程如图所示,“●”表
示反应物或生成物吸附在催化剂表面。其他条件相同时,下列说法正确的是
A.使用催化剂X和Y,反应均分2步进行
B.使用催化剂Y比使用催化剂X,反应更快达到平衡
C.反应达到平衡后,降低温度,B的浓度减小
D.反应过程中A·Y所能达到的最高浓度大于A·X
4.(2024届广东省省一模) 下,分别向恒为 的恒温密闭容器甲、恒为 的绝热密闭容器乙中加入
和 ,发生反应 ,两容器中 的转化率随时间的变化如
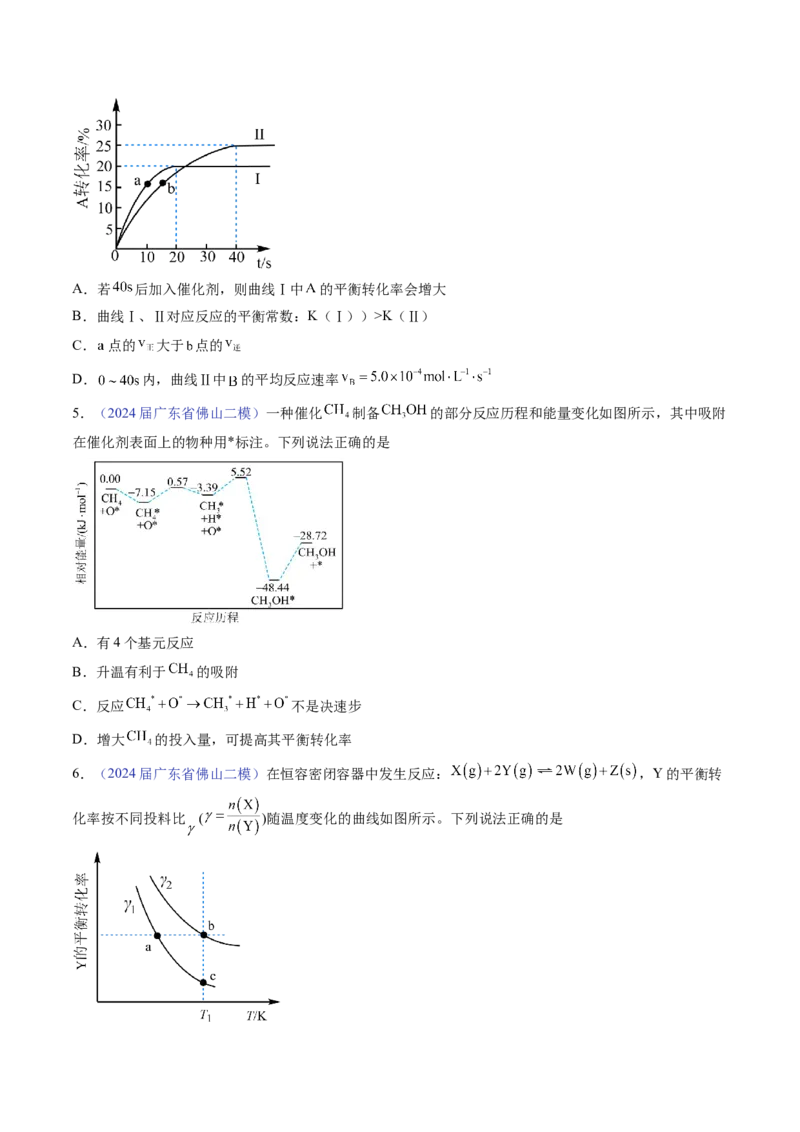
图所示。下列说法正确的是A.若 后加入催化剂,则曲线Ⅰ中 的平衡转化率会增大
B.曲线Ⅰ、Ⅱ对应反应的平衡常数:K(Ⅰ))>K(Ⅱ)
C. 点的 大于 点的
D. 内,曲线Ⅱ中 的平均反应速率
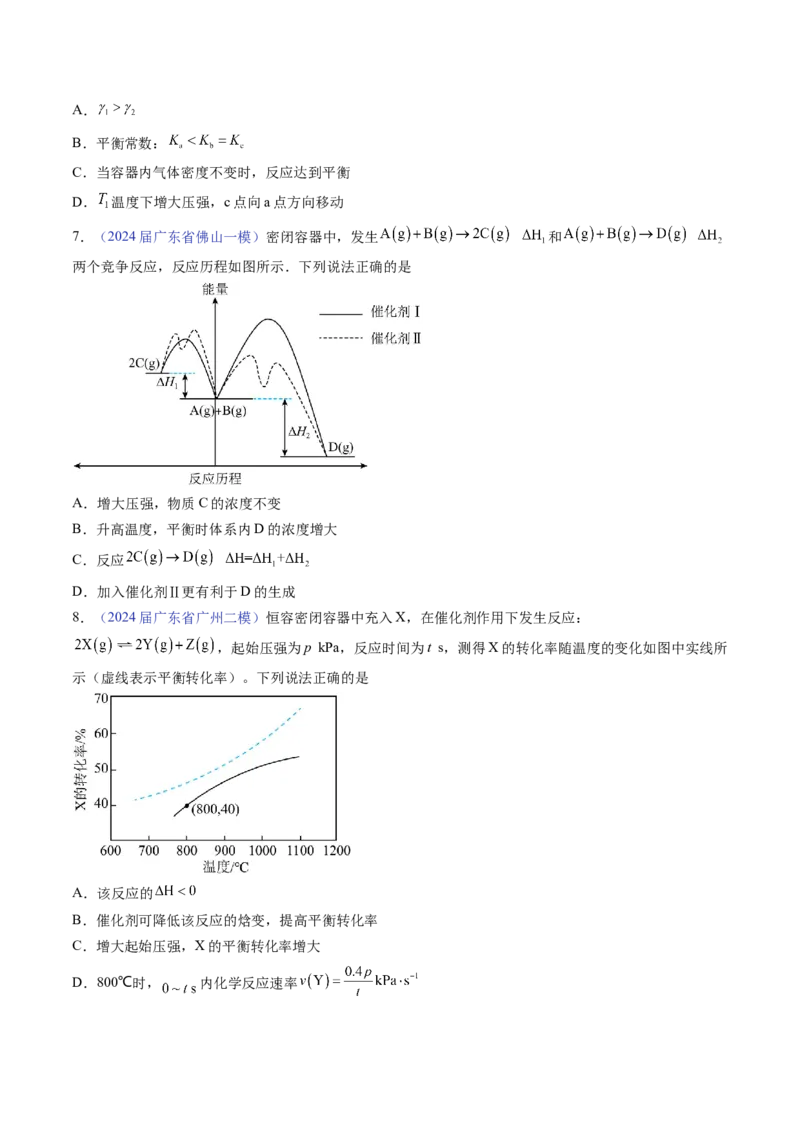
5.(2024届广东省佛山二模)一种催化 制备 的部分反应历程和能量变化如图所示,其中吸附
在催化剂表面上的物种用*标注。下列说法正确的是
A.有4个基元反应
B.升温有利于 的吸附
C.反应 不是决速步
D.增大 的投入量,可提高其平衡转化率
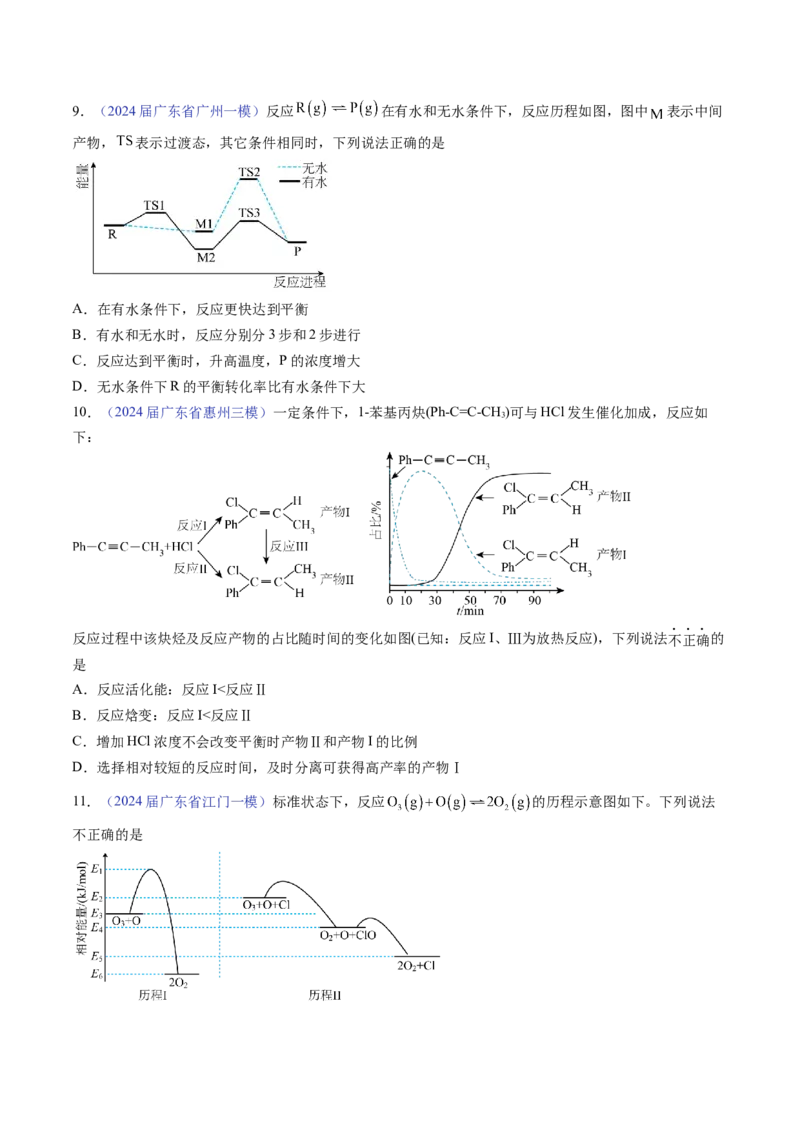
6.(2024届广东省佛山二模)在恒容密闭容器中发生反应: ,Y的平衡转
化率按不同投料比 ( )随温度变化的曲线如图所示。下列说法正确的是A.
B.平衡常数:
C.当容器内气体密度不变时,反应达到平衡
D. 温度下增大压强,c点向a点方向移动
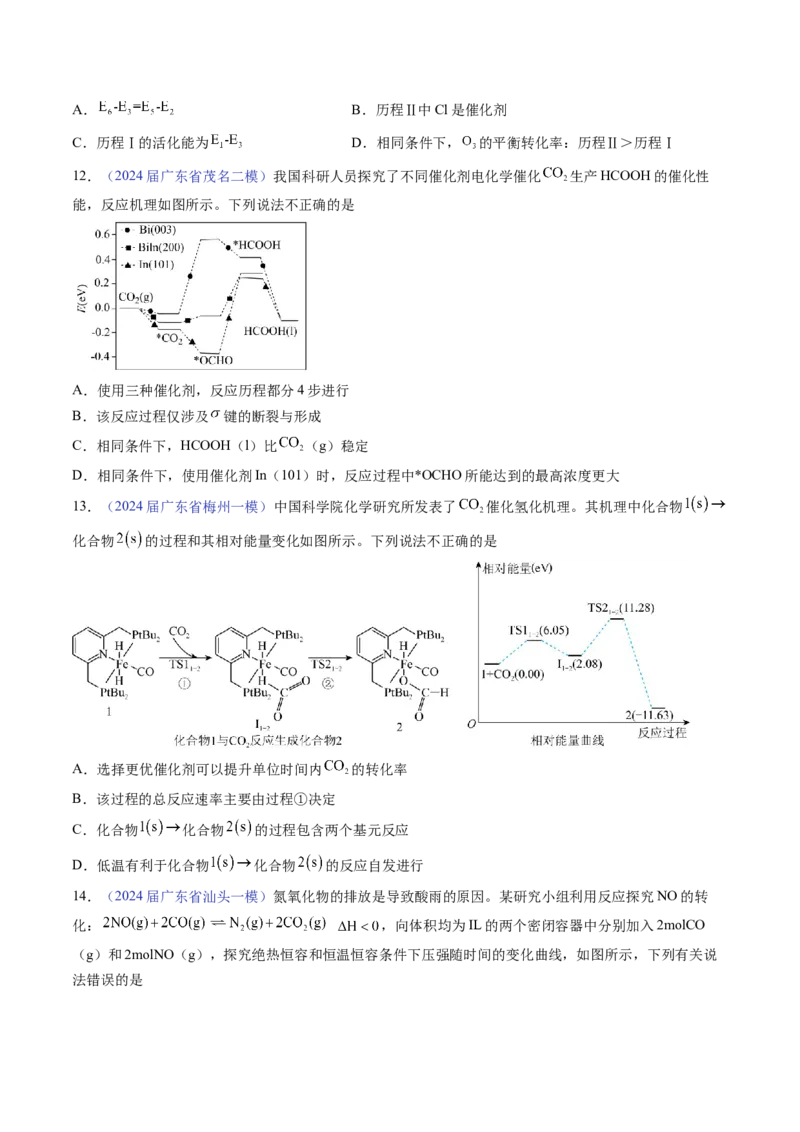
7.(2024届广东省佛山一模)密闭容器中,发生 和
两个竞争反应,反应历程如图所示.下列说法正确的是
A.增大压强,物质C的浓度不变
B.升高温度,平衡时体系内D的浓度增大
C.反应
D.加入催化剂Ⅱ更有利于D的生成
8.(2024届广东省广州二模)恒容密闭容器中充入X,在催化剂作用下发生反应:
,起始压强为p kPa,反应时间为t s,测得X的转化率随温度的变化如图中实线所
示(虚线表示平衡转化率)。下列说法正确的是
A.该反应的
B.催化剂可降低该反应的焓变,提高平衡转化率
C.增大起始压强,X的平衡转化率增大
D.800℃时, 内化学反应速率9.(2024届广东省广州一模)反应 在有水和无水条件下,反应历程如图,图中 表示中间
产物, 表示过渡态,其它条件相同时,下列说法正确的是
A.在有水条件下,反应更快达到平衡
B.有水和无水时,反应分别分3步和2步进行
C.反应达到平衡时,升高温度,P的浓度增大
D.无水条件下R的平衡转化率比有水条件下大
10.(2024届广东省惠州三模)一定条件下,1-苯基丙炔(Ph-C=C-CH )可与HCl发生催化加成,反应如
3
下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法不正确的
是
A.反应活化能:反应I<反应Ⅱ
B.反应焓变:反应I<反应Ⅱ
C.增加HCl浓度不会改变平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ
11.(2024届广东省江门一模)标准状态下,反应 的历程示意图如下。下列说法
不正确的是A. B.历程Ⅱ中Cl是催化剂
C.历程Ⅰ的活化能为 D.相同条件下, 的平衡转化率:历程Ⅱ>历程Ⅰ
12.(2024届广东省茂名二模)我国科研人员探究了不同催化剂电化学催化 生产HCOOH的催化性
能,反应机理如图所示。下列说法不正确的是
A.使用三种催化剂,反应历程都分4步进行
B.该反应过程仅涉及 键的断裂与形成
C.相同条件下,HCOOH(l)比 (g)稳定
D.相同条件下,使用催化剂In(101)时,反应过程中*OCHO所能达到的最高浓度更大
13.(2024届广东省梅州一模)中国科学院化学研究所发表了 催化氢化机理。其机理中化合物
化合物 的过程和其相对能量变化如图所示。下列说法不正确的是
A.选择更优催化剂可以提升单位时间内 的转化率
B.该过程的总反应速率主要由过程①决定
C.化合物 化合物 的过程包含两个基元反应
D.低温有利于化合物 化合物 的反应自发进行
14.(2024届广东省汕头一模)氮氧化物的排放是导致酸雨的原因。某研究小组利用反应探究NO的转
化: ,向体积均为IL的两个密闭容器中分别加入2molCO
(g)和2molNO(g),探究绝热恒容和恒温恒容条件下压强随时间的变化曲线,如图所示,下列有关说
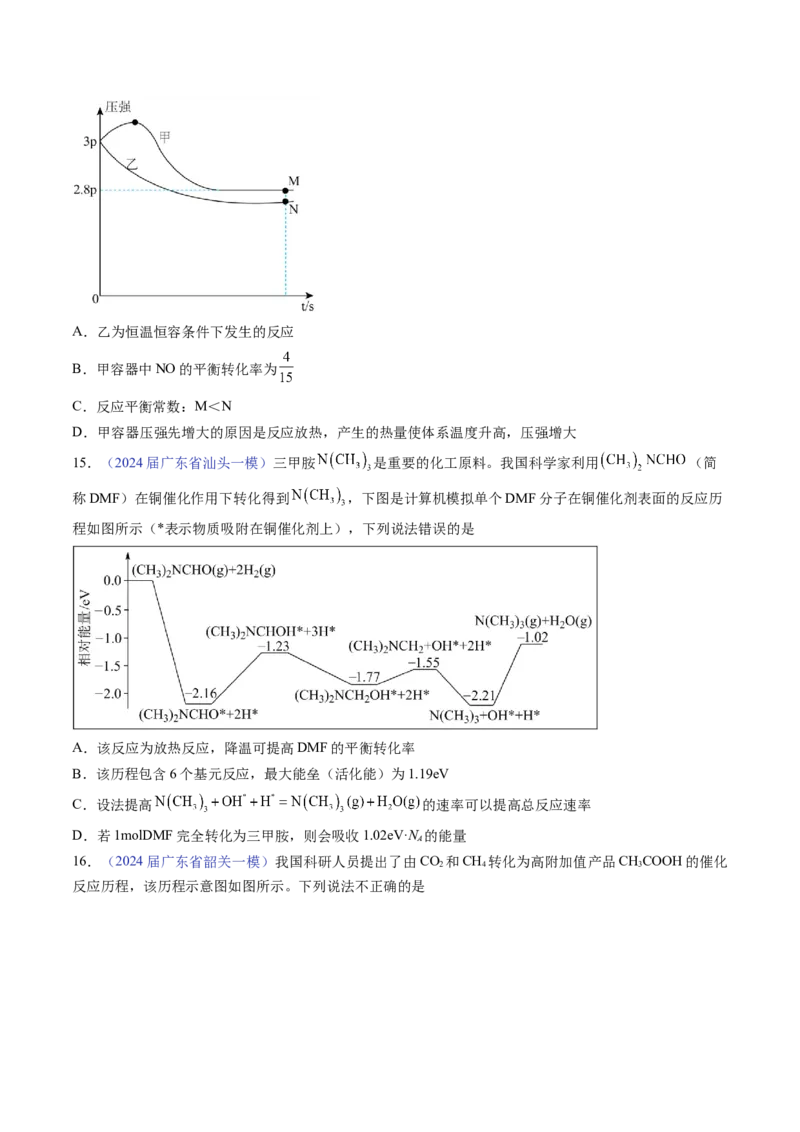
法错误的是A.乙为恒温恒容条件下发生的反应
B.甲容器中NO的平衡转化率为
C.反应平衡常数:M<N
D.甲容器压强先增大的原因是反应放热,产生的热量使体系温度升高,压强增大
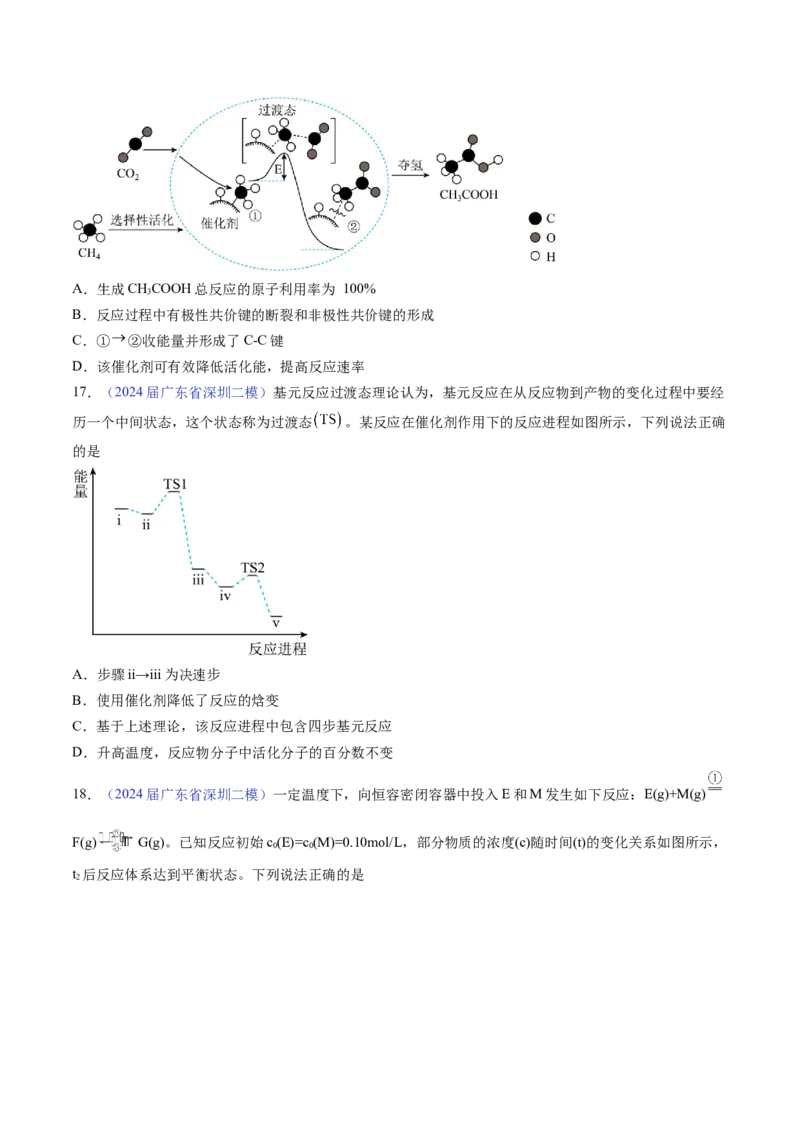
15.(2024届广东省汕头一模)三甲胺 是重要的化工原料。我国科学家利用 (简
称DMF)在铜催化作用下转化得到 ,下图是计算机模拟单个DMF分子在铜催化剂表面的反应历
程如图所示(*表示物质吸附在铜催化剂上),下列说法错误的是
A.该反应为放热反应,降温可提高DMF的平衡转化率
B.该历程包含6个基元反应,最大能垒(活化能)为1.19eV
C.设法提高 的速率可以提高总反应速率
D.若1molDMF完全转化为三甲胺,则会吸收1.02eV·N 的能量
A
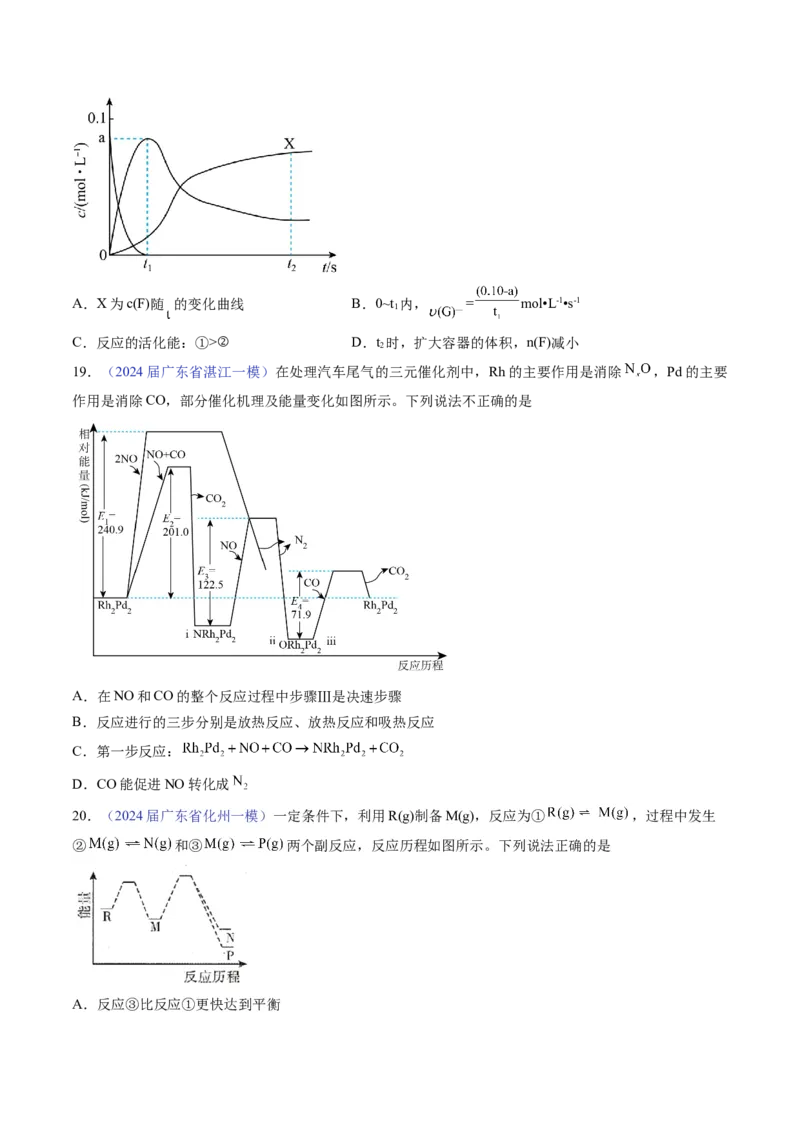
16.(2024届广东省韶关一模)我国科研人员提出了由CO 和CH 转化为高附加值产品CHCOOH的催化
2 4 3
反应历程,该历程示意图如图所示。下列说法不正确的是A.生成CHCOOH总反应的原子利用率为 100%
3
B.反应过程中有极性共价键的断裂和非极性共价键的形成
C.① ②收能量并形成了C-C键
D.该催化剂可有效降低活化能,提高反应速率
17.(2024届广东省深圳二模)基元反应过渡态理论认为,基元反应在从反应物到产物的变化过程中要经
历一个中间状态,这个状态称为过渡态 。某反应在催化剂作用下的反应进程如图所示,下列说法正确
的是
A.步骤ii→iii为决速步
B.使用催化剂降低了反应的焓变
C.基于上述理论,该反应进程中包含四步基元反应
D.升高温度,反应物分子中活化分子的百分数不变
18.(2024届广东省深圳二模)一定温度下,向恒容密闭容器中投入E和M发生如下反应:E(g)+M(g)
F(g) G(g)。已知反应初始c(E)=c (M)=0.10mol/L,部分物质的浓度(c)随时间(t)的变化关系如图所示,
0 0
t 后反应体系达到平衡状态。下列说法正确的是
2A.X为c(F)随 的变化曲线 B.0~t 内, = mol•L-1•s-1
1
C.反应的活化能:①>② D.t 时,扩大容器的体积,n(F)减小
2
19.(2024届广东省湛江一模)在处理汽车尾气的三元催化剂中,Rh的主要作用是消除 ,Pd的主要
作用是消除CO,部分催化机理及能量变化如图所示。下列说法不正确的是
A.在NO和CO的整个反应过程中步骤Ⅲ是决速步骤
B.反应进行的三步分别是放热反应、放热反应和吸热反应
C.第一步反应:
D.CO能促进NO转化成
20.(2024届广东省化州一模)一定条件下,利用R(g)制备M(g),反应为① ,过程中发生
② 和③ 两个副反应,反应历程如图所示。下列说法正确的是
A.反应③比反应①更快达到平衡B.温度越高,产物中M的纯度越高
C.一定时间内,使用合适的催化剂可减少体系中P的含量
D.增大R的浓度,反应①②③的 增大, 减小
考点二 水溶液中的离子平衡
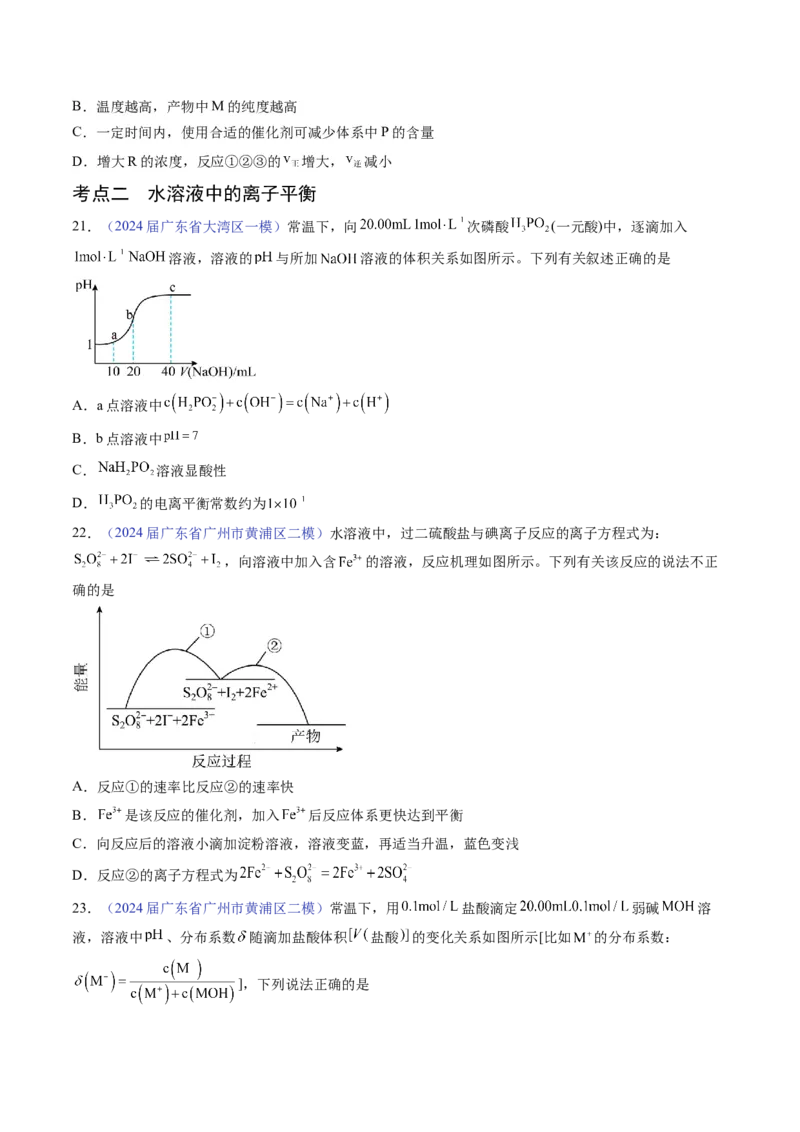
21.(2024届广东省大湾区一模)常温下,向 次磷酸 (一元酸)中,逐滴加入
溶液,溶液的 与所加 溶液的体积关系如图所示。下列有关叙述正确的是
A.a点溶液中
B.b点溶液中
C. 溶液显酸性
D. 的电离平衡常数约为
22.(2024届广东省广州市黄浦区二模)水溶液中,过二硫酸盐与碘离子反应的离子方程式为:
,向溶液中加入含 的溶液,反应机理如图所示。下列有关该反应的说法不正
确的是
A.反应①的速率比反应②的速率快
B. 是该反应的催化剂,加入 后反应体系更快达到平衡
C.向反应后的溶液小滴加淀粉溶液,溶液变蓝,再适当升温,蓝色变浅
D.反应②的离子方程式为
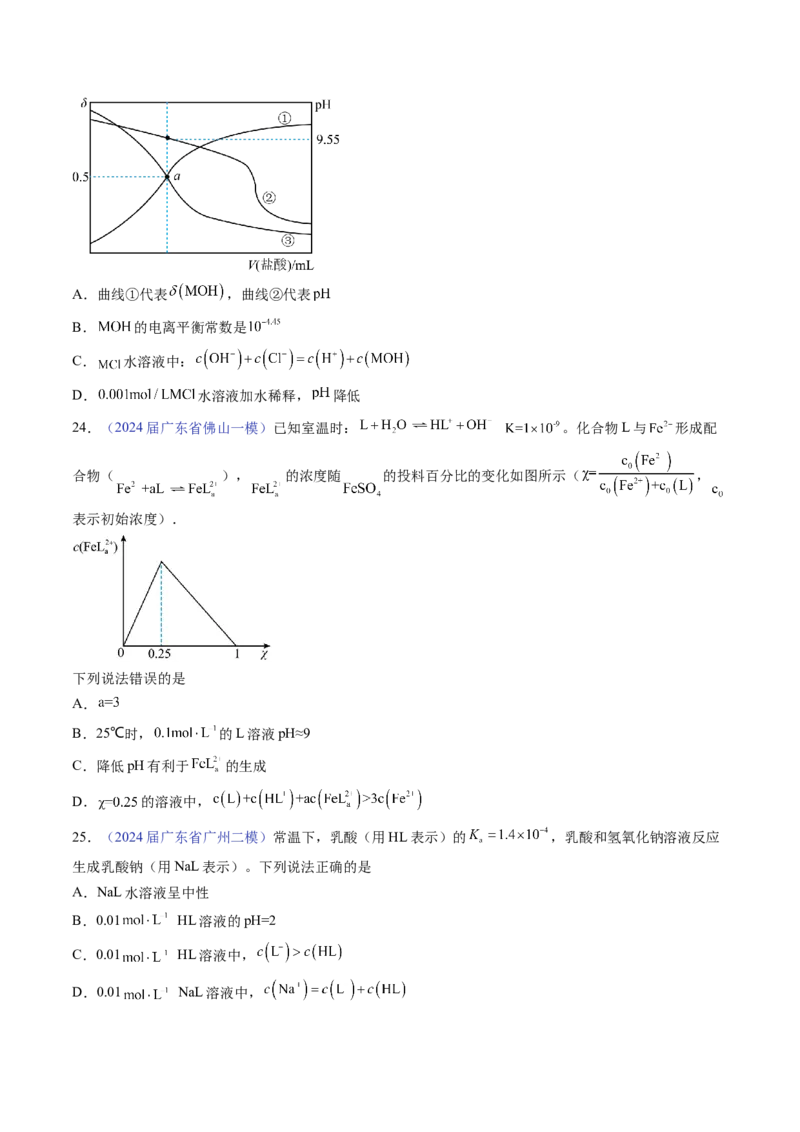
23.(2024届广东省广州市黄浦区二模)常温下,用 盐酸滴定 弱碱 溶
液,溶液中 、分布系数 随滴加盐酸体积 盐酸 的变化关系如图所示[比如 的分布系数:
],下列说法正确的是A.曲线①代表 ,曲线②代表
B. 的电离平衡常数是
C. 水溶液中:
D. 水溶液加水稀释, 降低
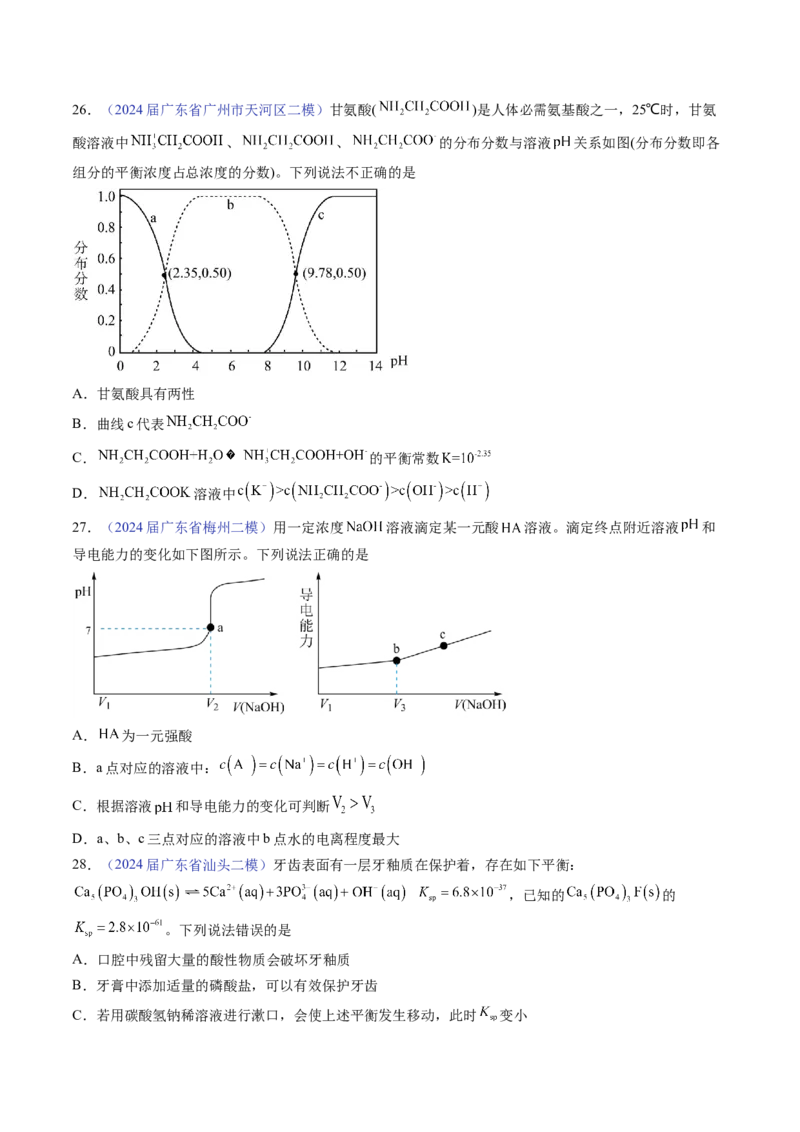
24.(2024届广东省佛山一模)已知室温时: 。化合物L与 形成配
合物( ), 的浓度随 的投料百分比的变化如图所示( ,
表示初始浓度).
下列说法错误的是
A.
B.25℃时, 的L溶液pH≈9
C.降低pH有利于 的生成
D. 的溶液中,
25.(2024届广东省广州二模)常温下,乳酸(用HL表示)的 ,乳酸和氢氧化钠溶液反应
生成乳酸钠(用NaL表示)。下列说法正确的是
A.NaL水溶液呈中性
B.0.01 HL溶液的pH=2
C.0.01 HL溶液中,
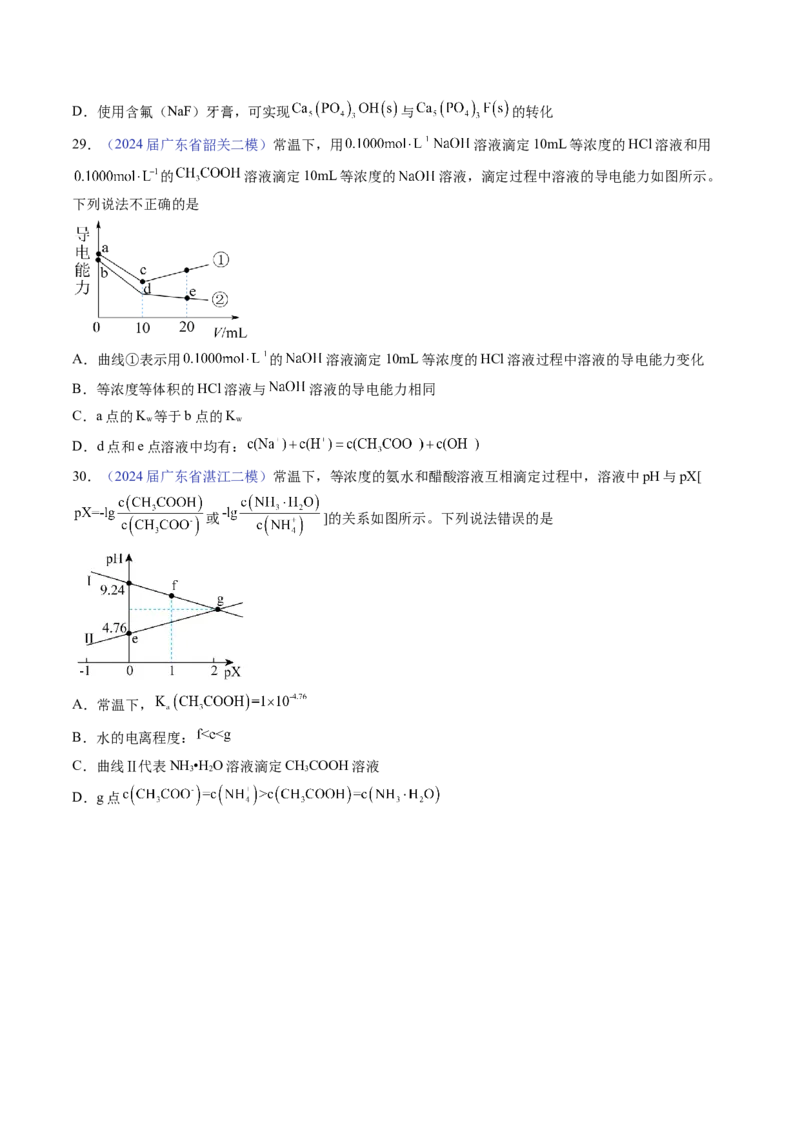
D.0.01 NaL溶液中,26.(2024届广东省广州市天河区二模)甘氨酸( )是人体必需氨基酸之一,25℃时,甘氨
酸溶液中 、 、 的分布分数与溶液 关系如图(分布分数即各
组分的平衡浓度占总浓度的分数)。下列说法不正确的是
A.甘氨酸具有两性
B.曲线c代表
C. 的平衡常数
D. 溶液中
27.(2024届广东省梅州二模)用一定浓度 溶液滴定某一元酸 溶液。滴定终点附近溶液 和
导电能力的变化如下图所示。下列说法正确的是
A. 为一元强酸
B.a点对应的溶液中:
C.根据溶液 和导电能力的变化可判断
D.a、b、c三点对应的溶液中b点水的电离程度最大
28.(2024届广东省汕头二模)牙齿表面有一层牙釉质在保护着,存在如下平衡:
,已知的 的
。下列说法错误的是
A.口腔中残留大量的酸性物质会破坏牙釉质
B.牙膏中添加适量的磷酸盐,可以有效保护牙齿
C.若用碳酸氢钠稀溶液进行漱口,会使上述平衡发生移动,此时 变小D.使用含氟(NaF)牙膏,可实现 与 的转化
29.(2024届广东省韶关二模)常温下,用 溶液滴定10mL等浓度的HCl溶液和用
的 溶液滴定10mL等浓度的 溶液,滴定过程中溶液的导电能力如图所示。
下列说法不正确的是
A.曲线①表示用 的 溶液滴定10mL等浓度的HCl溶液过程中溶液的导电能力变化
B.等浓度等体积的HCl溶液与 溶液的导电能力相同
C.a点的K 等于b点的K
w w
D.d点和e点溶液中均有:
30.(2024届广东省湛江二模)常温下,等浓度的氨水和醋酸溶液互相滴定过程中,溶液中pH与pX[
或 ]的关系如图所示。下列说法错误的是
A.常温下,
B.水的电离程度:
C.曲线Ⅱ代表NH •H O溶液滴定CHCOOH溶液
3 2 3
D.g点