文档内容
押广东卷第 18 题
工艺流程综合题
核心考点 考情统计 考向预测 备考策略
通过废液或矿石进行金属的
2023·广东卷,18 提炼或者制备特定的物质, 1.回归教材,熟悉教材流程,
物质制备
2022·广东卷,18 体现创新性和应用性; 掌握流程的基本分析思路。
通过废液或废矿的分离提 2.提高阅读理解能力,对新情
纯,得到相应的含特定元素 境进行分析解读,提取重要信
的物质,体现创新性和应用 息。
分离提纯 2021·广东卷,18
性。
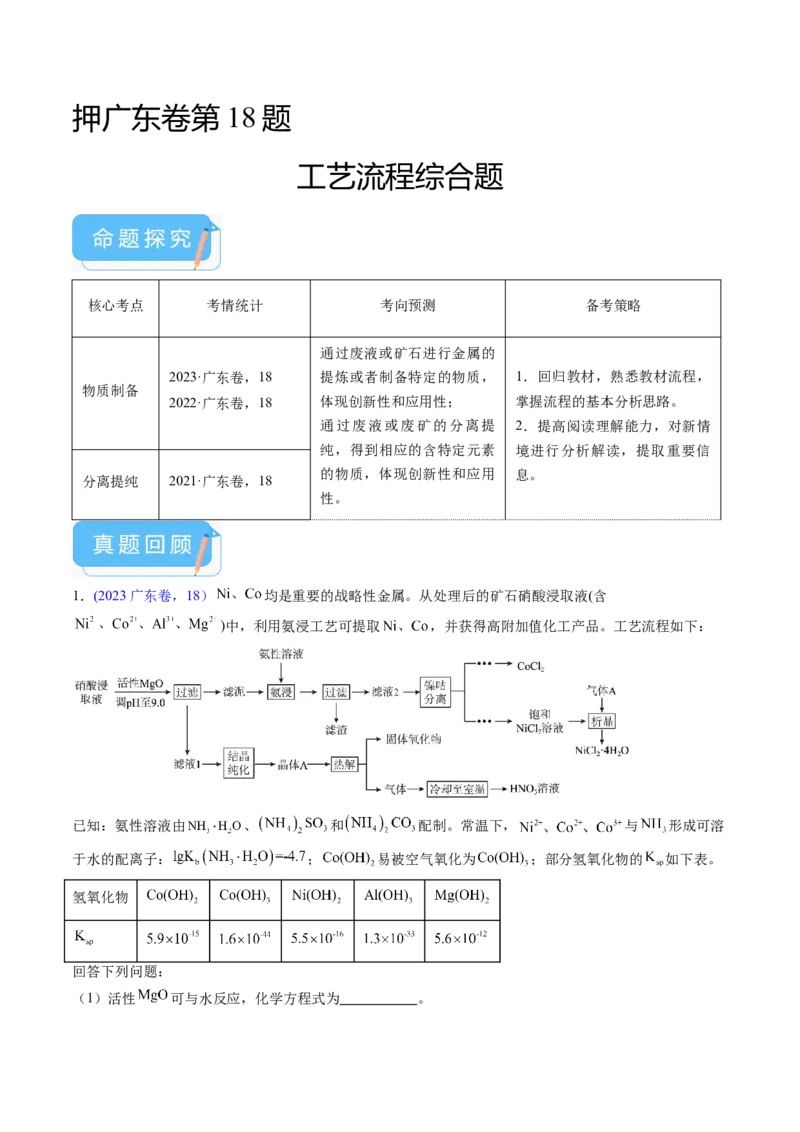
1.(2023广东卷,18) 均是重要的战略性金属。从处理后的矿石硝酸浸取液(含
)中,利用氨浸工艺可提取 ,并获得高附加值化工产品。工艺流程如下:
已知:氨性溶液由 、 和 配制。常温下, 与 形成可溶
于水的配离子: ; 易被空气氧化为 ;部分氢氧化物的 如下表。
氢氧化物
回答下列问题:
(1)活性 可与水反应,化学方程式为 。(2)常温下, 的氨性溶液中, (填“>”“<”或“=”)。
(3)“氨浸”时,由 转化为 的离子方程式为 。
(4) 会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱中,
出现了 的明锐衍射峰。
① 属于 (填“晶体”或“非晶体”)。
② 提高了 的浸取速率,其原因是 。
(5)①“析晶”过程中通入的酸性气体A为 。
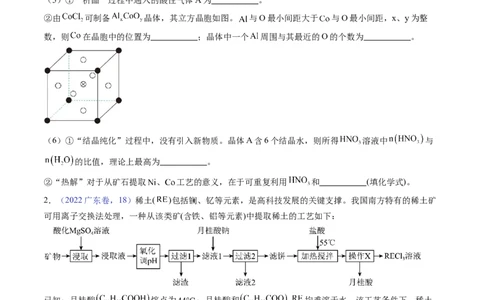
②由 可制备 晶体,其立方晶胞如图。 与O最小间距大于 与O最小间距,x、y为整
数,则 在晶胞中的位置为 ;晶体中一个 周围与其最近的O的个数为 。
(6)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得 溶液中 与
的比值,理论上最高为 。
②“热解”对于从矿石提取 工艺的意义,在于可重复利用 和 (填化学式)。
2.(2022广东卷,18)稀土( )包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿
可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
已知:月桂酸 熔点为 ;月桂酸和 均难溶于水。该工艺条件下,稀土
离子保持 价不变; 的 , 开始溶解时的pH为8.8;有关金属离子
沉淀的相关pH见下表。
离子
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
(1)“氧化调pH”中,化合价有变化的金属离子是_______。(2)“过滤1”前,用 溶液调pH至_______的范围内,该过程中 发生反应的离子方程式为_______。
(3)“过滤2”后,滤饼中检测不到 元素,滤液2中 浓度为 。为尽可能多地提取 ,
可提高月桂酸钠的加入量,但应确保“过滤2”前的溶液中 低于_______ (保留两位有
效数字)。
(4)①“加热搅拌”有利于加快 溶出、提高产率,其原因是_______。
②“操作X”的过程为:先_______,再固液分离。
(5)该工艺中,可再生循环利用的物质有_______(写化学式)。
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂 。
①还原 和 熔融盐制备 时,生成1mol 转移_______ 电子。
② 用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化 的还原,发生的电极反应为
_______。
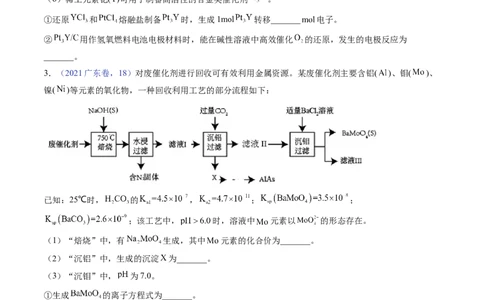
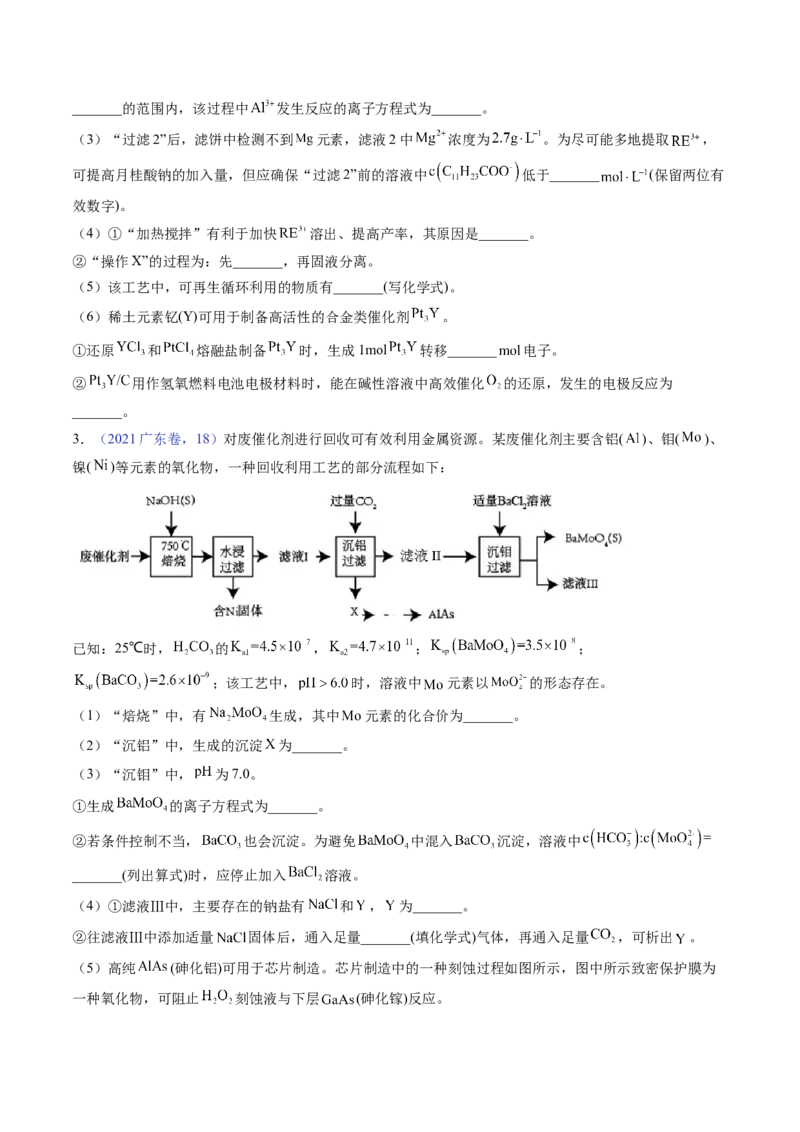
3.(2021广东卷,18)对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝( )、钼( )、
镍( )等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25℃时, 的 , ; ;
;该工艺中, 时,溶液中 元素以 的形态存在。
(1)“焙烧”中,有 生成,其中 元素的化合价为_______。
(2)“沉铝”中,生成的沉淀 为_______。
(3)“沉钼”中, 为7.0。
①生成 的离子方程式为_______。
②若条件控制不当, 也会沉淀。为避免 中混入 沉淀,溶液中
_______(列出算式)时,应停止加入 溶液。
(4)①滤液Ⅲ中,主要存在的钠盐有 和 , 为_______。
②往滤液Ⅲ中添加适量 固体后,通入足量_______(填化学式)气体,再通入足量 ,可析出 。
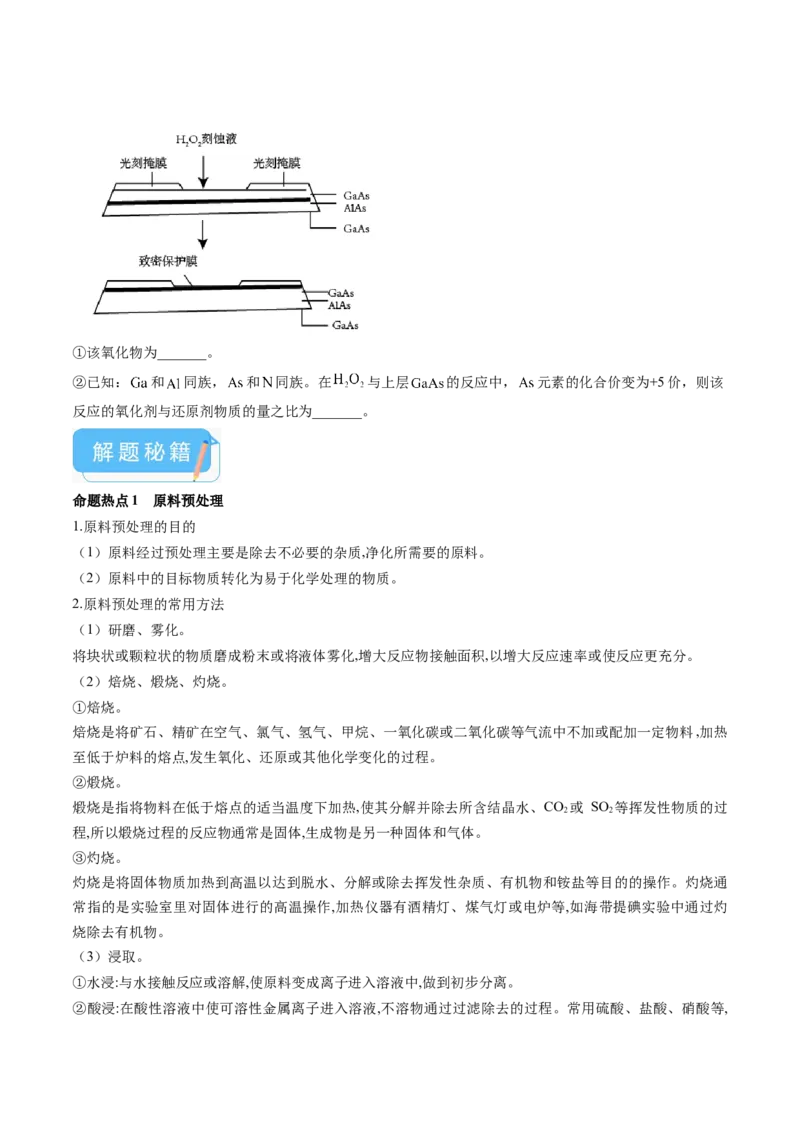
(5)高纯 (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为
一种氧化物,可阻止 刻蚀液与下层 (砷化镓)反应。①该氧化物为_______。
②已知: 和 同族, 和 同族。在 与上层 的反应中, 元素的化合价变为+5价,则该
反应的氧化剂与还原剂物质的量之比为_______。
命题热点1 原料预处理
1.原料预处理的目的
(1)原料经过预处理主要是除去不必要的杂质,净化所需要的原料。
(2)原料中的目标物质转化为易于化学处理的物质。
2.原料预处理的常用方法
(1)研磨、雾化。
将块状或颗粒状的物质磨成粉末或将液体雾化,增大反应物接触面积,以增大反应速率或使反应更充分。
(2)焙烧、煅烧、灼烧。
①焙烧。
焙烧是将矿石、精矿在空气、氯气、氢气、甲烷、一氧化碳或二氧化碳等气流中不加或配加一定物料,加热
至低于炉料的熔点,发生氧化、还原或其他化学变化的过程。
②煅烧。
煅烧是指将物料在低于熔点的适当温度下加热,使其分解并除去所含结晶水、CO 或 SO 等挥发性物质的过
2 2
程,所以煅烧过程的反应物通常是固体,生成物是另一种固体和气体。
③灼烧。
灼烧是将固体物质加热到高温以达到脱水、分解或除去挥发性杂质、有机物和铵盐等目的的操作。灼烧通
常指的是实验室里对固体进行的高温操作,加热仪器有酒精灯、煤气灯或电炉等,如海带提碘实验中通过灼
烧除去有机物。
(3)浸取。
①水浸:与水接触反应或溶解,使原料变成离子进入溶液中,做到初步分离。
②酸浸:在酸性溶液中使可溶性金属离子进入溶液,不溶物通过过滤除去的过程。常用硫酸、盐酸、硝酸等,用盐酸、硝酸酸溶时要注意控温,用硫酸酸溶时要关注Pb2+ 、Ca2+ 、Ag+会生成PbSO 、 CaSO 、Ag SO
4 4 2 4
在滤渣中出现。
③碱浸:常用NaOH溶液、氨水、NaCO 溶液等,与碱接触反应或溶解,NaOH溶液使酸性氧化物和两性氧化
2 3
物以含氧酸根离子(如Si、Al、Zn、Cr等元素),或与NH 形成配离子进入溶液。
3
④盐浸:用铵盐溶液、FeCl 溶液等。
3
⑤醇浸:提取有机物,常采用有机溶剂(乙醚、二氯甲烷等)浸取的方法提取有机物。
命题热点2 反应条件的控制
一、反应条件的控制方法
通过控制一定的反应条件来达到提高物质转化率或除去杂质的目的。
1.控制溶液的pH
(1)增强物质的氧化性、还原性(H+能增强MnO- 、NO-
的氧化性),调节离子的水解程度。
4 3
(2)通过控制溶液的pH可以除去某些金属离子。
如要除去溶液中含有的Fe3+、Al3+,可调节溶液的pH使之转变为Fe(OH) 、Al(OH) 沉淀。
3 3
2.控制温度(常用水浴、冰水浴等)
(1)控制反应速率(升温增大反应速率)、使催化剂达到最大活性、防止副反应的发生。
(2)使化学平衡移动,控制化学反应进行的方向。
(3)升温:使溶液中的气体逸出,使易挥发物质挥发,使易分解的物质分解。
(4)煮沸:使气体逸出;促进水解,聚沉后利于过滤分离。
(5)控制固体的溶解与结晶。
趁热过滤:减少因降温而析出的溶质的量。
蒸发浓缩:蒸发除去部分溶剂,提高溶液的浓度。
蒸发结晶:蒸发溶剂,使溶液由不饱和变为饱和,继续蒸发,过剩的溶质就会呈晶体析出。
3.使用保护气
(1)隔绝空气(主要是O、HO)。
2 2
(2)抑制弱离子的水解(如HCl氛围)。
二、陌生图像中反应条件的选择
[例1] 浸出过程中时间和液固比对锰浸出率的影响分别如图甲、图乙所示。
则适宜的浸出时间和液固比分别为60 min、3。
[例2] “酸浸”实验中,镁的浸出率结果如图所示。由图可知,当镁的浸出率为80%时,所采用的实验条件为
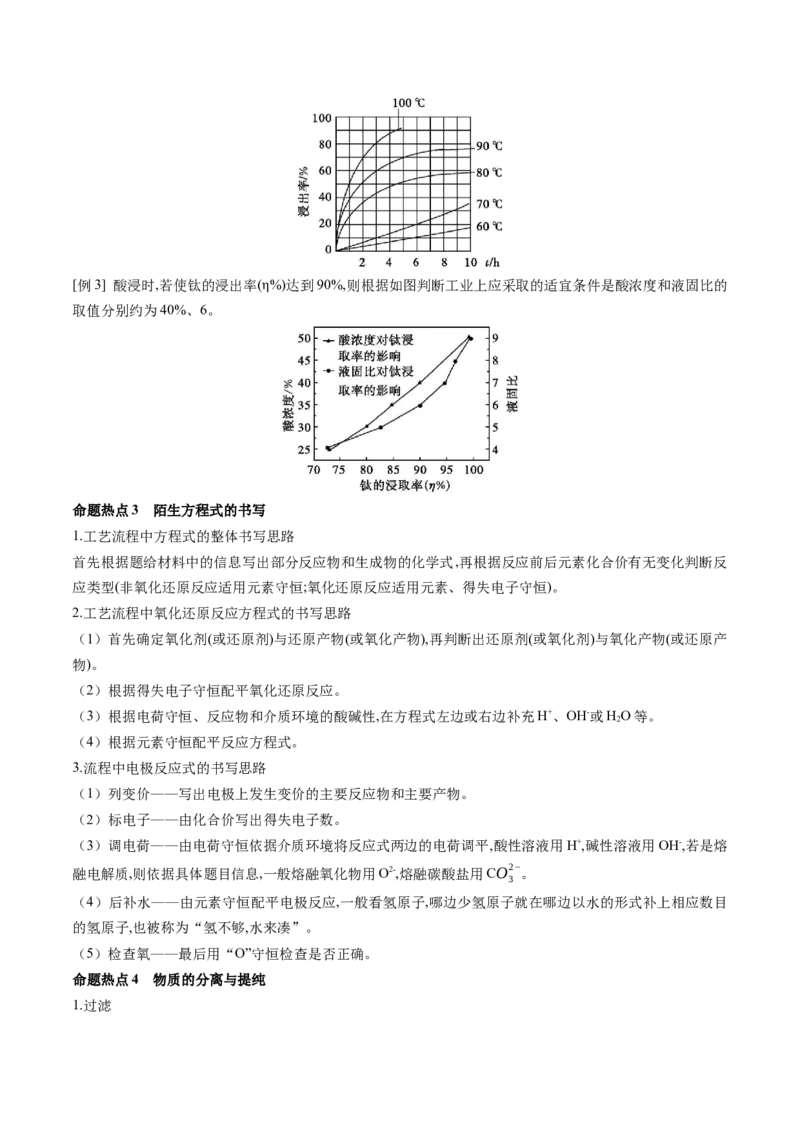
100 ℃、3 h左右。[例3] 酸浸时,若使钛的浸出率(η%)达到90%,则根据如图判断工业上应采取的适宜条件是酸浓度和液固比的
取值分别约为40%、6。
命题热点3 陌生方程式的书写
1.工艺流程中方程式的整体书写思路
首先根据题给材料中的信息写出部分反应物和生成物的化学式,再根据反应前后元素化合价有无变化判断反
应类型(非氧化还原反应适用元素守恒;氧化还原反应适用元素、得失电子守恒)。
2.工艺流程中氧化还原反应方程式的书写思路
(1)首先确定氧化剂(或还原剂)与还原产物(或氧化产物),再判断出还原剂(或氧化剂)与氧化产物(或还原产
物)。
(2)根据得失电子守恒配平氧化还原反应。
(3)根据电荷守恒、反应物和介质环境的酸碱性,在方程式左边或右边补充H+、OH-或HO等。
2
(4)根据元素守恒配平反应方程式。
3.流程中电极反应式的书写思路
(1)列变价——写出电极上发生变价的主要反应物和主要产物。
(2)标电子——由化合价写出得失电子数。
(3)调电荷——由电荷守恒依据介质环境将反应式两边的电荷调平,酸性溶液用H+,碱性溶液用OH-,若是熔
融电解质,则依据具体题目信息,一般熔融氧化物用O2-,熔融碳酸盐用CO2−
。
3
(4)后补水——由元素守恒配平电极反应,一般看氢原子,哪边少氢原子就在哪边以水的形式补上相应数目
的氢原子,也被称为“氢不够,水来凑”。
(5)检查氧——最后用“O”守恒检查是否正确。
命题热点4 物质的分离与提纯
1.过滤固液分离的一种方法,主要有常压过滤、减压过滤、热过滤。
(1)常压过滤:滤液靠自身的重力透过滤纸流下,实现分离,过滤时需要分析产品的需求及生产目的,准确判
断经过过滤后产生的滤液、滤渣的主要成分,准确判断是留下滤液还是滤渣。
(2)减压过滤(抽滤):过滤在减低的压力下进行,滤液在内外压强差作用下透过滤纸或砂芯流下,实现分离。
相比普通过滤,抽滤加快了过滤的速度。抽滤的优点是快速过滤,有时还可以过滤掉气体,并能达到快速干燥
产品的作用。
(3)趁热过滤:将温度较高的固液混合物直接使用常规过滤操作进行过滤,由于常规过滤操作往往耗时较长,
这样会导致在过滤过程中因混合物温度降低而使溶质析出,影响分离效果。可使用热过滤仪器将固液混合物
的温度保持在一定范围内进行过滤,所以又称为热过滤。
2.蒸发结晶
(1)适用范围:提取溶解度随温度变化不大的溶质,如:NaCl。
(2)蒸发结晶的标志:当有大量晶体出现时,停止加热,利用余热蒸干。
3.冷却结晶
(1)适用范围:提取溶解度随温度变化较大的物质(如KNO)、易水解的物质(如FeCl )或结晶水合物(如
3 3
CuSO ·5H O)。
4 2
(2)冷却结晶的标志:当有少量晶体(晶膜)出现时。
4.沉淀洗涤时洗涤剂的选择
洗涤试剂 适用范围 目的
溶解度随温度升高而升高,且 除去固体表面吸附着的××杂质,减少固体
蒸 冷水
变化较大 因为洗涤液温度高造成溶解损失
馏
除去固体表面吸附着的××杂质,减少固体
水 热水 溶解度随温度升高而降低
因为洗涤液温度低造成溶解损失
固体易溶于水、难溶于有机 减少固体溶解损失;利用有机溶剂的挥发
有机溶剂(酒精、丙酮等)
溶剂 性除去固体表面的水分,增大干燥速率
饱和溶液 对纯度要求不高的产品 减少固体溶解
除去固体表面吸附着的可溶于酸、碱的杂
酸、碱溶液 产物不溶于酸、碱
质;减少固体溶解
洗涤沉淀的方法:向过滤器中加入蒸馏水至浸没沉淀,待水自然流下后,重复以上操作2~3次
检验沉淀是否洗涤干净的方法:取少量最后一次的洗涤液于试管中,向其中滴入某试剂,若未出现特征反应
现象,则沉淀洗涤干净
5.重结晶
将结晶得到的晶体溶于溶剂制得饱和溶液,又重新从溶液结晶的过程。
6.萃取与反萃取
利用溶质在互不相溶的两种溶剂里的溶解度不同,用一种溶剂(萃取剂)把溶质从它与另一种溶剂组
萃取
成的溶液里提取出来的过程,萃取后需要分液。如:用CCl 萃取溴水中的Br
4 2
反萃
在溶剂萃取分离过程中,当完成萃取操作后,为进一步纯化目标产物或便于下一步分离操作的实施,
取将目标产物从有机相转入水相的萃取操作称为反萃取,为萃取的逆过程
7.蒸馏
蒸馏是利用液体混合物中各组分的沸点不同,给液体混合物加热,使其中的某一组分变成蒸气再冷凝成液体,
跟其他组分分离的过程。
8.冷却法
利用气体易液化的特点分离气体,如合成氨工业采用冷却法分离氨与氮气、氢气。
命题热点5 电离常数、溶度积常数的有关计算
1.水溶液中平衡常数之间的关系
(1)平衡常数都只与温度有关,温度不变,平衡常数不变,升高温度,K、K、K 、K 均增大。
a b w h
K K
w w
(2)K、K、K 三者的关系式为K= ;K 、K、K 三者的关系式为K= 。
a h w h K b h w h K
a b
(3)二元酸的K 、K 与相应酸根离子的K 、K 的关系式为K ·K =K ,K ·K =K 。
a1 a2 h1 h2 a1 h2 w a2 h1 w
K (CdS)
sp
(4)反应CdS(s)+2H+(aq) Cd2+(aq)+H S(aq)的平衡常数为K,则K= 。
2 K (H S)·K (H S)
a1 2 a2 2
2.溶度积(K )的常见计算类型
sp
(1)已知溶度积求溶液中的某种离子的浓度,如K =a的饱和AgCl溶液中 c(Ag+)=√a mol/L。
sp
(2)已知溶度积、溶液中某离子的浓度,求溶液中另一种离子的浓度,如某温度下AgCl的K =a,在0.1 mol/L
sp
的NaCl溶液中加入过量的AgCl固体,达到平衡后c(Ag+)=10a mol/L。
c(Mn2+)
(3)计算沉淀转化的平衡常数,如 Cu2+(aq)+MnS(s) CuS(s)+Mn2+(aq),平衡常数 K= =
c(Cu2+)
c(Mn2+)·c(S2−) K (MnS)
sp
= 。
c(Cu2+)·c(S2−) K (CuS)
sp
考点一 物质制备类
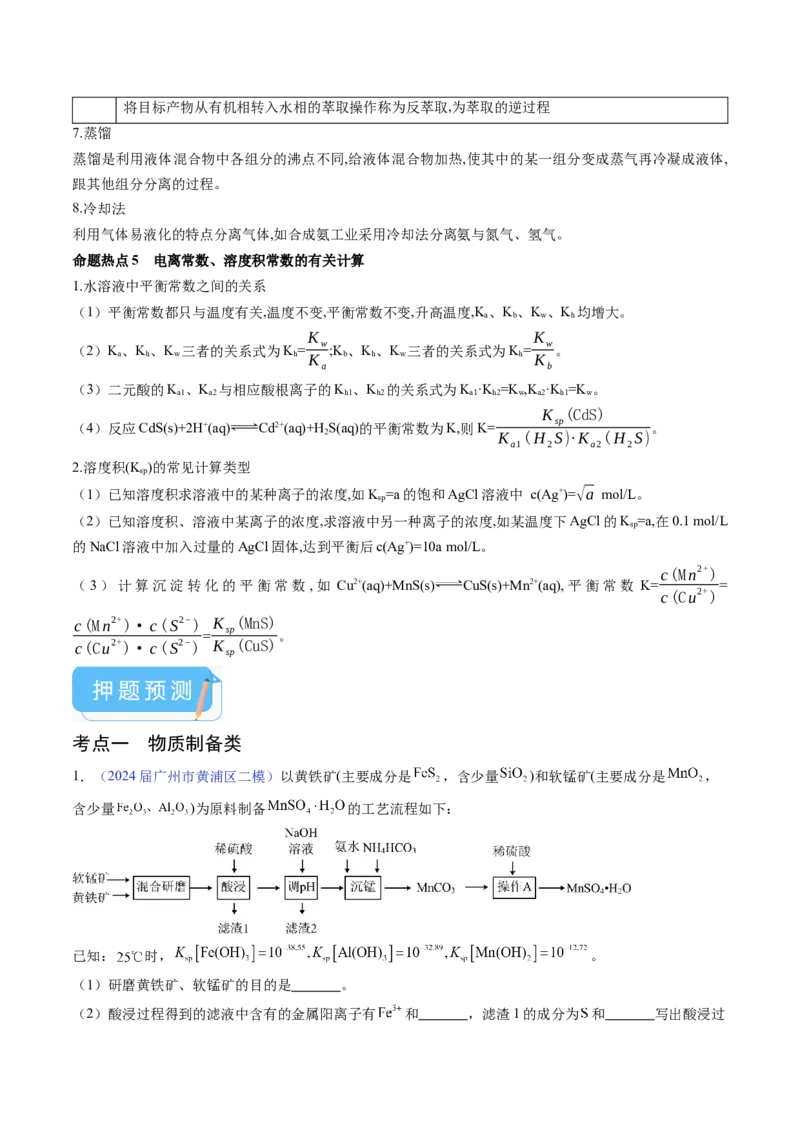
1.(2024届广州市黄浦区二模)以黄铁矿(主要成分是 ,含少量 )和软锰矿(主要成分是 ,
含少量 )为原料制备 的工艺流程如下:
已知: 时, 。
(1)研磨黄铁矿、软锰矿的目的是 。
(2)酸浸过程得到的滤液中含有的金属阳离子有 和 ,滤渣1的成分为 和 写出酸浸过程中主要反应的离子方程式 。
(3)调 时,若溶液中 ,为得到尽可能多且纯净的产品,应控制 的范围是
。
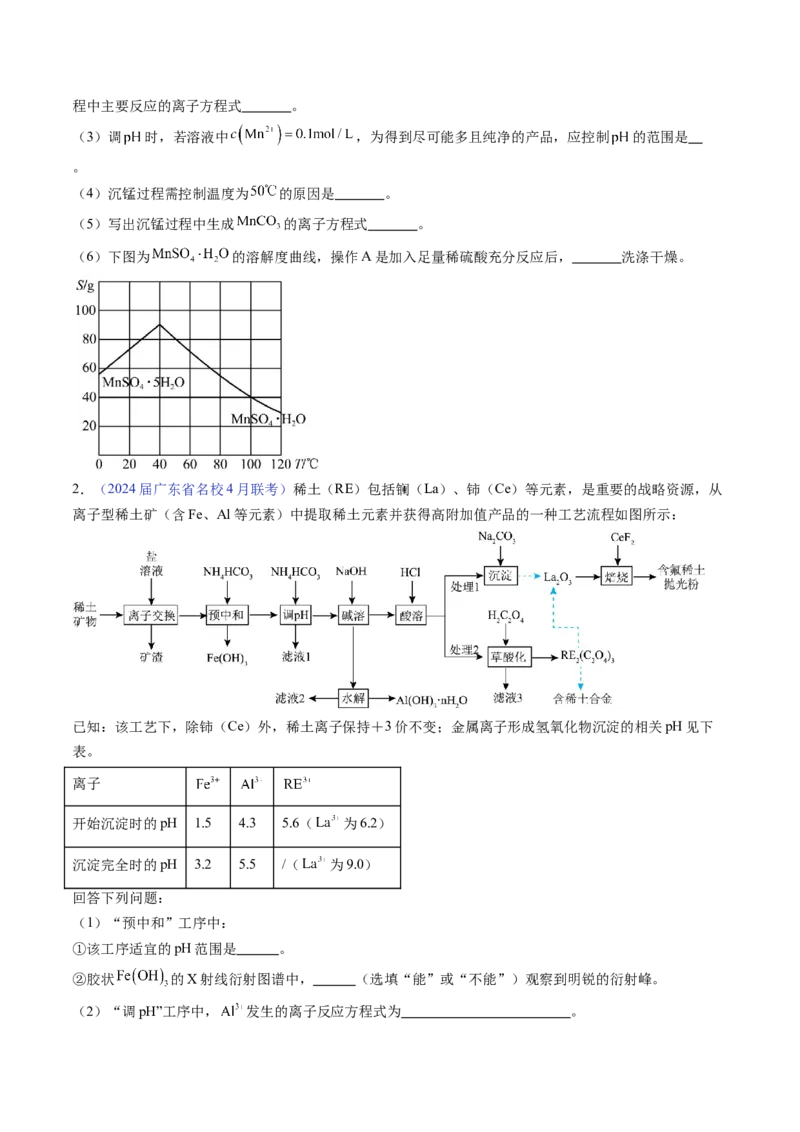
(4)沉锰过程需控制温度为 的原因是 。
(5)写出沉锰过程中生成 的离子方程式 。
(6)下图为 的溶解度曲线,操作A是加入足量稀硫酸充分反应后, 洗涤干燥。
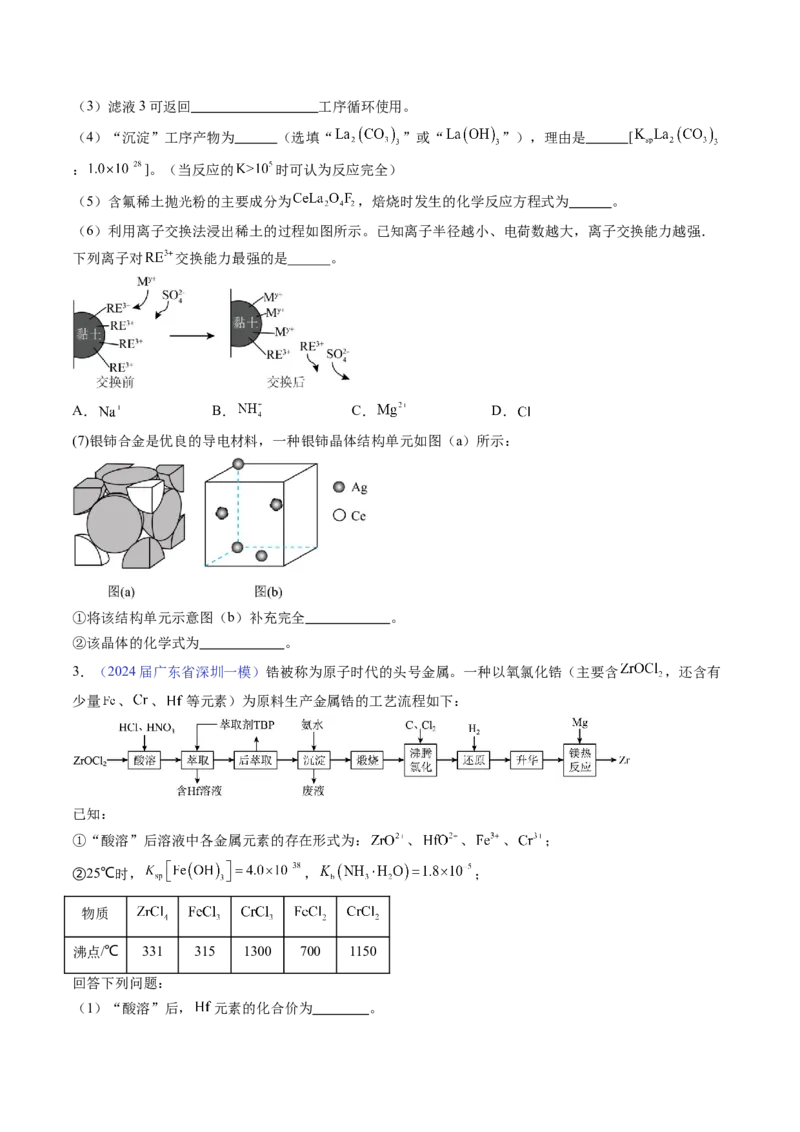
2.(2024届广东省名校4月联考)稀土(RE)包括镧(La)、铈(Ce)等元素,是重要的战略资源,从
离子型稀土矿(含Fe、Al等元素)中提取稀土元素并获得高附加值产品的一种工艺流程如图所示:
已知:该工艺下,除铈(Ce)外,稀土离子保持+3价不变;金属离子形成氢氧化物沉淀的相关pH见下
表。
离子
开始沉淀时的pH 1.5 4.3 5.6( 为6.2)
沉淀完全时的pH 3.2 5.5 /( 为9.0)
回答下列问题:
(1)“预中和”工序中:
①该工序适宜的pH范围是 。
②胶状 的X射线衍射图谱中, (选填“能”或“不能”)观察到明锐的衍射峰。
(2)“调pH”工序中, 发生的离子反应方程式为 。(3)滤液3可返回 工序循环使用。
(4)“沉淀”工序产物为 (选填“ ”或“ ”),理由是 [
: ]。(当反应的 时可认为反应完全)
(5)含氟稀土抛光粉的主要成分为 ,焙烧时发生的化学反应方程式为 。
(6)利用离子交换法浸出稀土的过程如图所示。已知离子半径越小、电荷数越大,离子交换能力越强.
下列离子对 交换能力最强的是______。
A. B. C. D.
(7)银铈合金是优良的导电材料,一种银铈晶体结构单元如图(a)所示:
①将该结构单元示意图(b)补充完全 。
②该晶体的化学式为 。
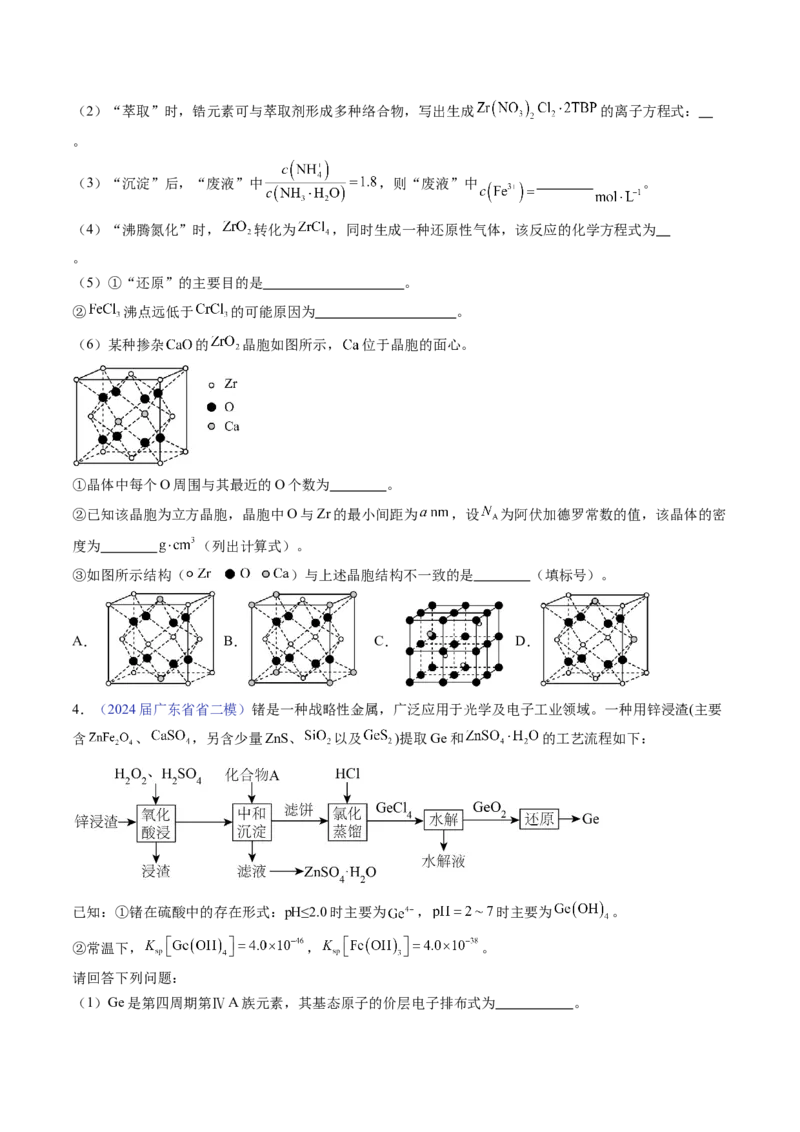
3.(2024届广东省深圳一模)锆被称为原子时代的头号金属。一种以氧氯化锆(主要含 ,还含有
少量 、 、 等元素)为原料生产金属锆的工艺流程如下:
已知:
①“酸溶”后溶液中各金属元素的存在形式为: 、 、 、 ;
②25℃时, , ;
物质
沸点/℃ 331 315 1300 700 1150
回答下列问题:
(1)“酸溶”后, 元素的化合价为 。(2)“萃取”时,锆元素可与萃取剂形成多种络合物,写出生成 的离子方程式:
。
(3)“沉淀”后,“废液”中 ,则“废液”中 。
(4)“沸腾氮化”时, 转化为 ,同时生成一种还原性气体,该反应的化学方程式为
。
(5)①“还原”的主要目的是 。
② 沸点远低于 的可能原因为 。
(6)某种掺杂 的 晶胞如图所示, 位于晶胞的面心。
①晶体中每个O周围与其最近的O个数为 。
②已知该晶胞为立方晶胞,晶胞中O与Zr的最小间距为 ,设 为阿伏加德罗常数的值,该晶体的密
度为 (列出计算式)。
③如图所示结构( )与上述晶胞结构不一致的是 (填标号)。
A. B. C. D.
4.(2024届广东省省二模)锗是一种战略性金属,广泛应用于光学及电子工业领域。一种用锌浸渣(主要
含 、 ,另含少量ZnS、 以及 )提取Ge和 的工艺流程如下:
已知:①锗在硫酸中的存在形式:pH≤2.0时主要为 , 时主要为 。
②常温下, , 。
请回答下列问题:
(1)Ge是第四周期第ⅣA族元素,其基态原子的价层电子排布式为 。(2)“氧化酸浸”工序中,溶液 ,浸渣的主要成分为 、S和 (填化学式);
被双氧水氧化的离子方程式为 。
(3)“中和沉淀”工序中,所加化合物A为 (填一种物质的化学式);调节溶液 ,Ge
和Fe共沉淀,此时滤液中 。
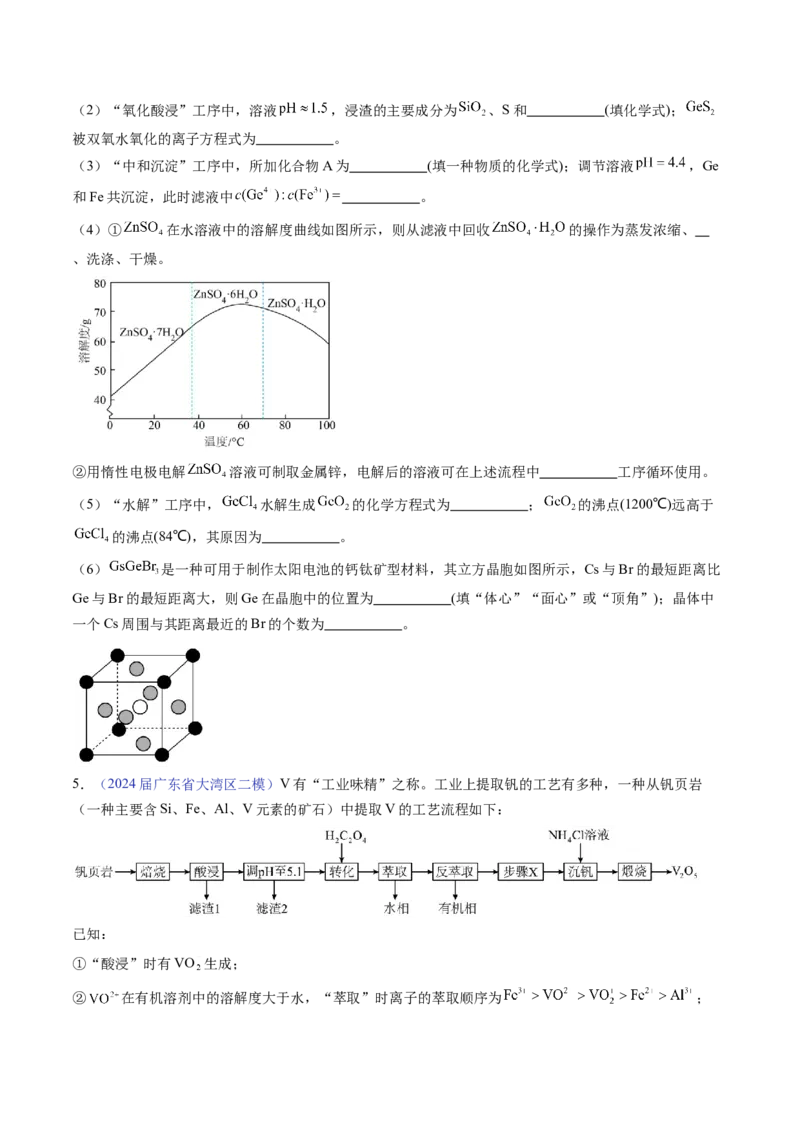
(4)① 在水溶液中的溶解度曲线如图所示,则从滤液中回收 的操作为蒸发浓缩、
、洗涤、干燥。
②用惰性电极电解 溶液可制取金属锌,电解后的溶液可在上述流程中 工序循环使用。
(5)“水解”工序中, 水解生成 的化学方程式为 ; 的沸点(1200℃)远高于
的沸点(84℃),其原因为 。
(6) 是一种可用于制作太阳电池的钙钛矿型材料,其立方晶胞如图所示,Cs与Br的最短距离比
Ge与Br的最短距离大,则Ge在晶胞中的位置为 (填“体心”“面心”或“顶角”);晶体中
一个Cs周围与其距离最近的Br的个数为 。
5.(2024届广东省大湾区二模)V有“工业味精”之称。工业上提取钒的工艺有多种,一种从钒页岩
(一种主要含Si、Fe、Al、V元素的矿石)中提取V的工艺流程如下:
已知:
①“酸浸”时有VO 生成;
② 在有机溶剂中的溶解度大于水,“萃取”时离子的萃取顺序为 ;③VO 和 可以相互转化。
回答下列问题:
(1)“焙烧”时可添加适量“盐对”NaCl- 与钒页岩形成混合物,这样做的目的是
。
(2)“滤渣1”除掉的主要杂质元素是 (填元素符号)。
(3) 作用是将VO 转化为 ,转化的目的是 ,发生的离子反应方程式为
。
(4)①“沉钒”时,生成 沉淀,“步骤X”应该加入 (填“氧化剂”或“还原剂”),
写出“沉钒”时的离子反应方程式 。
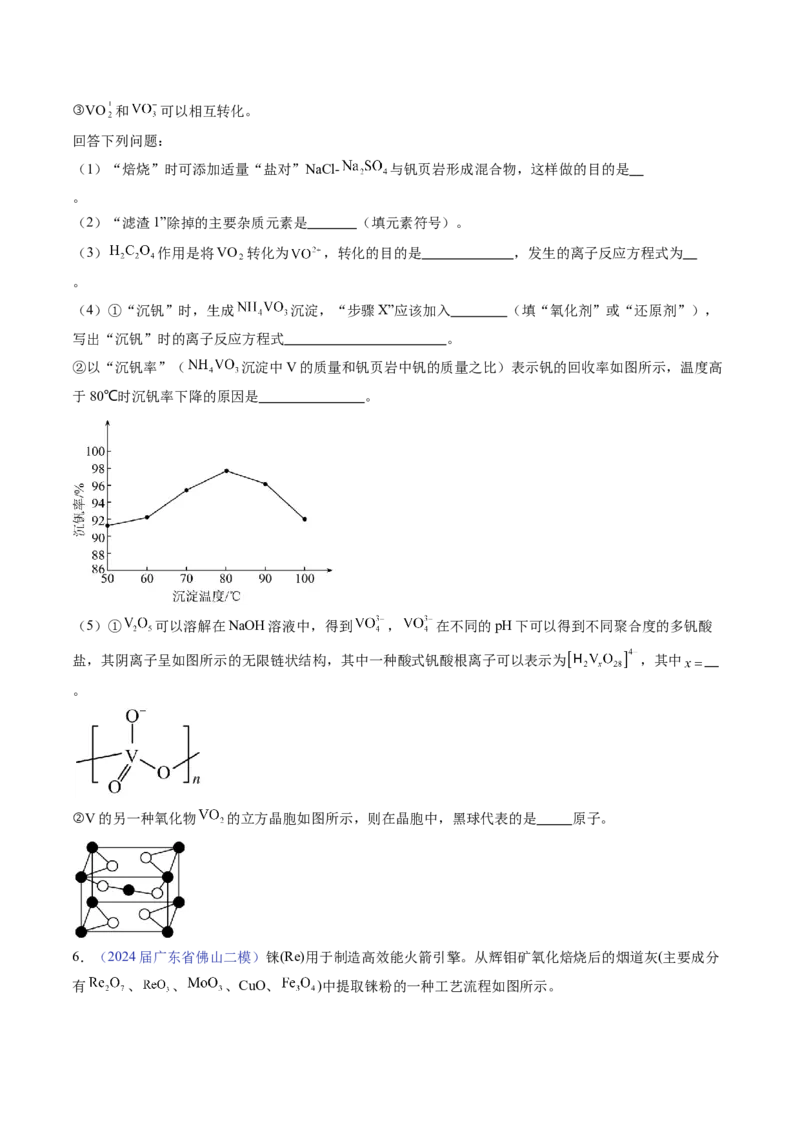
②以“沉钒率”( 沉淀中V的质量和钒页岩中钒的质量之比)表示钒的回收率如图所示,温度高
于80℃时沉钒率下降的原因是 。
(5)① 可以溶解在NaOH溶液中,得到 , 在不同的pH下可以得到不同聚合度的多钒酸
盐,其阴离子呈如图所示的无限链状结构,其中一种酸式钒酸根离子可以表示为 ,其中
。
②V的另一种氧化物 的立方晶胞如图所示,则在晶胞中,黑球代表的是 原子。
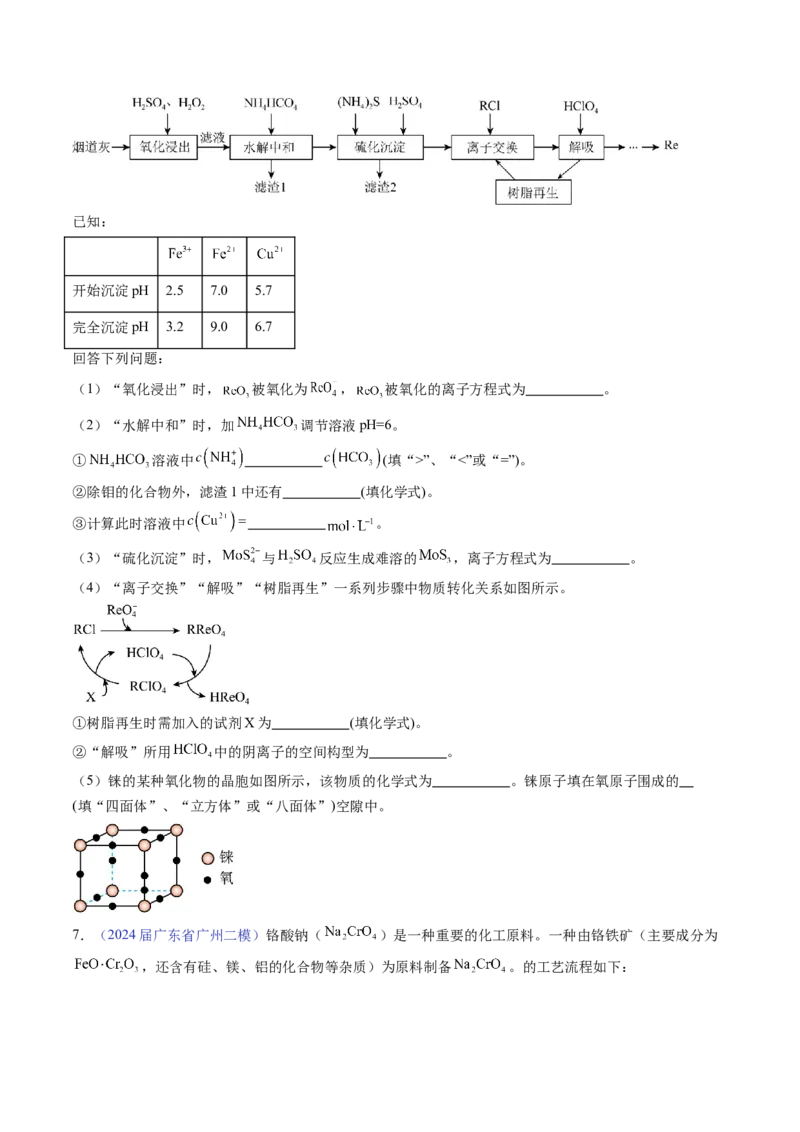
6.(2024届广东省佛山二模)铼(Re)用于制造高效能火箭引擎。从辉钼矿氧化焙烧后的烟道灰(主要成分
有 、 、 、CuO、 )中提取铼粉的一种工艺流程如图所示。已知:
开始沉淀pH 2.5 7.0 5.7
完全沉淀pH 3.2 9.0 6.7
回答下列问题:
(1)“氧化浸出”时, 被氧化为 , 被氧化的离子方程式为 。
(2)“水解中和”时,加 调节溶液pH=6。
① 溶液中 (填“>”、“<”或“=”)。
②除钼的化合物外,滤渣1中还有 (填化学式)。
③计算此时溶液中 。
(3)“硫化沉淀”时, 与 反应生成难溶的 ,离子方程式为 。
(4)“离子交换”“解吸”“树脂再生”一系列步骤中物质转化关系如图所示。
①树脂再生时需加入的试剂X为 (填化学式)。
②“解吸”所用 中的阴离子的空间构型为 。
(5)铼的某种氧化物的晶胞如图所示,该物质的化学式为 。铼原子填在氧原子围成的
(填“四面体”、“立方体”或“八面体”)空隙中。
7.(2024届广东省广州二模)铬酸钠( )是一种重要的化工原料。一种由铬铁矿(主要成分为
,还含有硅、镁、铝的化合物等杂质)为原料制备 。的工艺流程如下:已知:25℃时, , , ,
。
回答下列问题:
(1)基态Cr3+的价层电子排布式为 。
(2)“碱浸氧化”时, 转化为 和 ,该反应中氧化剂和还原剂的物质的量之比为
。
(3)“除铝”时, 转化为 沉淀,该反应的离子方程式为 。
(4)“沉铬”中,常温下,往“除铝”所得滤液中加入过量 固体,充分搅拌,当溶液中
沉淀完全( )时,滤液1中 为 ,滤液1经浓缩后可循环至
工序重复使用。(已知: )
(5)“酸溶还原”所得溶液中的溶质除HCl外,还含有 (填化学式)。
(6)“碱溶氧化”中,生成 ,反应的化学方程式为 。
(7) 的一种晶胞如图1,沿z轴方向的投影如图2,其中氧原子不在图中标注,Cr位于晶胞面上及
晶胞内。
①每个晶胞中含有 的个数为
②晶胞中位于晶胞顶角及体心的 的距离为 nm(用含a、b、c的式子表示)。
8.(2024届广东省韶关二模)二氧化铈( )是一种典型的金属氧化物,具有较强的氧化性广泛应用
于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含 、
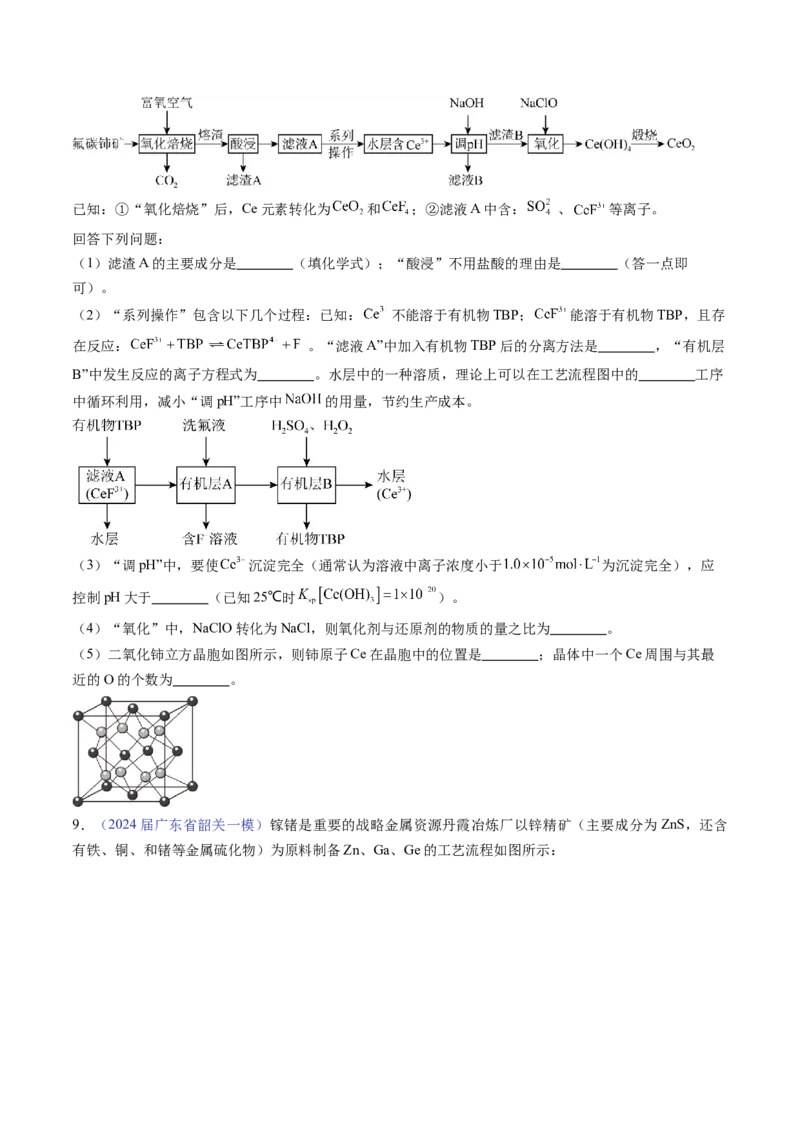
等)为原料制备 的一种工艺流程如下图所示:已知:①“氧化焙烧”后,Ce元素转化为 和 ;②滤液A中含: 、 等离子。
回答下列问题:
(1)滤渣A的主要成分是 (填化学式);“酸浸”不用盐酸的理由是 (答一点即
可)。
(2)“系列操作”包含以下几个过程:已知: 不能溶于有机物TBP; 能溶于有机物TBP,且存
在反应: 。“滤液A”中加入有机物TBP后的分离方法是 ,“有机层
B”中发生反应的离子方程式为 。水层中的一种溶质,理论上可以在工艺流程图中的 工序
中循环利用,减小“调pH”工序中 的用量,节约生产成本。
(3)“调pH”中,要使 沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应
控制pH大于 (已知25℃时 )。
(4)“氧化”中,NaClO转化为NaCl,则氧化剂与还原剂的物质的量之比为 。
(5)二氧化铈立方晶胞如图所示,则铈原子Ce在晶胞中的位置是 ;晶体中一个Ce周围与其最
近的O的个数为 。
9.(2024届广东省韶关一模)镓锗是重要的战略金属资源丹霞冶炼厂以锌精矿(主要成分为ZnS,还含
有铁、铜、和锗等金属硫化物)为原料制备Zn、Ga、Ge的工艺流程如图所示:已知:①该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
金属离子 Fe3+ Ga3+ Cu2+
开始沉淀时的pH 2.5 3.5 5.3
沉淀完全时的pH 3.3 4.6 6.4
②镓与铝同主族,化学性质相似。
(1)基态镓原子的核外电子排布式为 。
(2)“氧压浸出”时,ZnS发生反应的化学方程式是 。
(3)“滤渣I”的主要成分为 (填化学式)。
(4)“萃取”的原理为Mn+(水相)+nHA(有机相) MA (有机相)+nH+(水相)(M为Cu或Ga),则“反萃
n
取”工序中的试剂X宜选用 (填化学式)。
(5)反萃取后的水溶液中含有Ga3+、Cu2+,“沉镓”时应控制溶液的pH范围为 。
(6)写出“碱溶”过程中发生反应的离子方程式 。
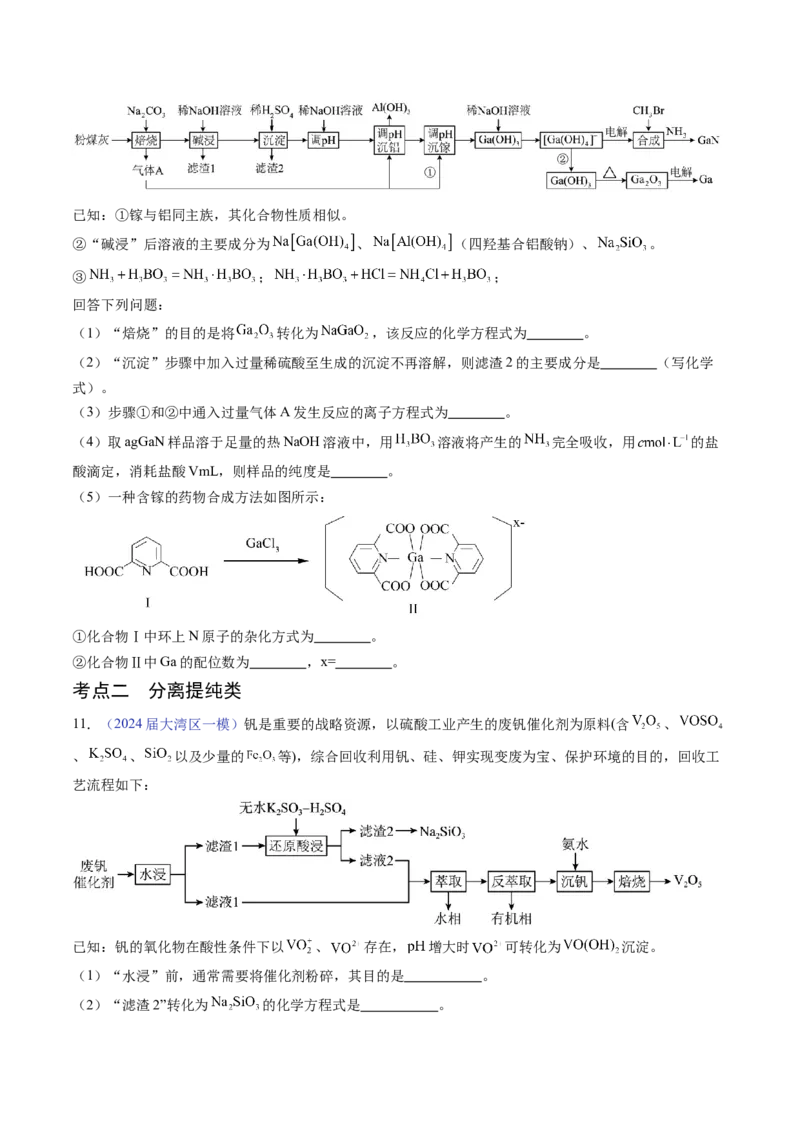
(7)砷化镓GaAs是一种重要的半导体材料,其晶体的立方体晶胞如图所示,设晶胞边长为apm,阿伏加德
罗常数为N ,则晶胞的密度为 g/cm3(写出表达式)。
A
10.(2024届广东省韶关二模)2023年7月3日,商务部与海关总署发布公告,宣布对镓、锗相关物质实
施出口管制。金属镓被称为“电子工业脊梁”,氮化镓是5G技术中广泛应用的新型半导体材料。利用粉
煤灰(主要成分为 、 、 ,还有少量 等杂质)制备镓和氮化镓的流程如下:已知:①镓与铝同主族,其化合物性质相似。
②“碱浸”后溶液的主要成分为 、 (四羟基合铝酸钠)、 。
③ ; ;
回答下列问题:
(1)“焙烧”的目的是将 转化为 ,该反应的化学方程式为 。
(2)“沉淀”步骤中加入过量稀硫酸至生成的沉淀不再溶解,则滤渣2的主要成分是 (写化学
式)。
(3)步骤①和②中通入过量气体A发生反应的离子方程式为 。
(4)取agGaN样品溶于足量的热NaOH溶液中,用 溶液将产生的 完全吸收,用 的盐
酸滴定,消耗盐酸VmL,则样品的纯度是 。
(5)一种含镓的药物合成方法如图所示:
①化合物Ⅰ中环上N原子的杂化方式为 。
②化合物Ⅱ中Ga的配位数为 ,x= 。
考点二 分离提纯类
11.(2024届大湾区一模)钒是重要的战略资源,以硫酸工业产生的废钒催化剂为原料(含 、
、 、 以及少量的 等),综合回收利用钒、硅、钾实现变废为宝、保护环境的目的,回收工
艺流程如下:
已知:钒的氧化物在酸性条件下以 、 存在, 增大时 可转化为 沉淀。
(1)“水浸”前,通常需要将催化剂粉碎,其目的是 。
(2)“滤渣2”转化为 的化学方程式是 。(3)“还原酸浸”时:
①硫酸的用量会影响钒的浸出率, 需保持在1.2以下的原因是 。
②过程中除了有 被还原成 ,还涉及的反应离子方程式为 。
③若以磷酸为介质处理废催化剂,可以提高钒的浸出率。一种钒磷配合物的结构如图所示,形成配位键时
V提供 (选填“孤对电子”或“空轨道”)。
(4)“萃取”时选择有机萃取剂,原理是: (有机层) (有机层),“反萃取”
应选择在 环境中进行(选填“酸性”、“中性”或“碱性”)。
(5)加氨水生成 沉淀,若经焙烧得到 产品,则消耗空气中 。
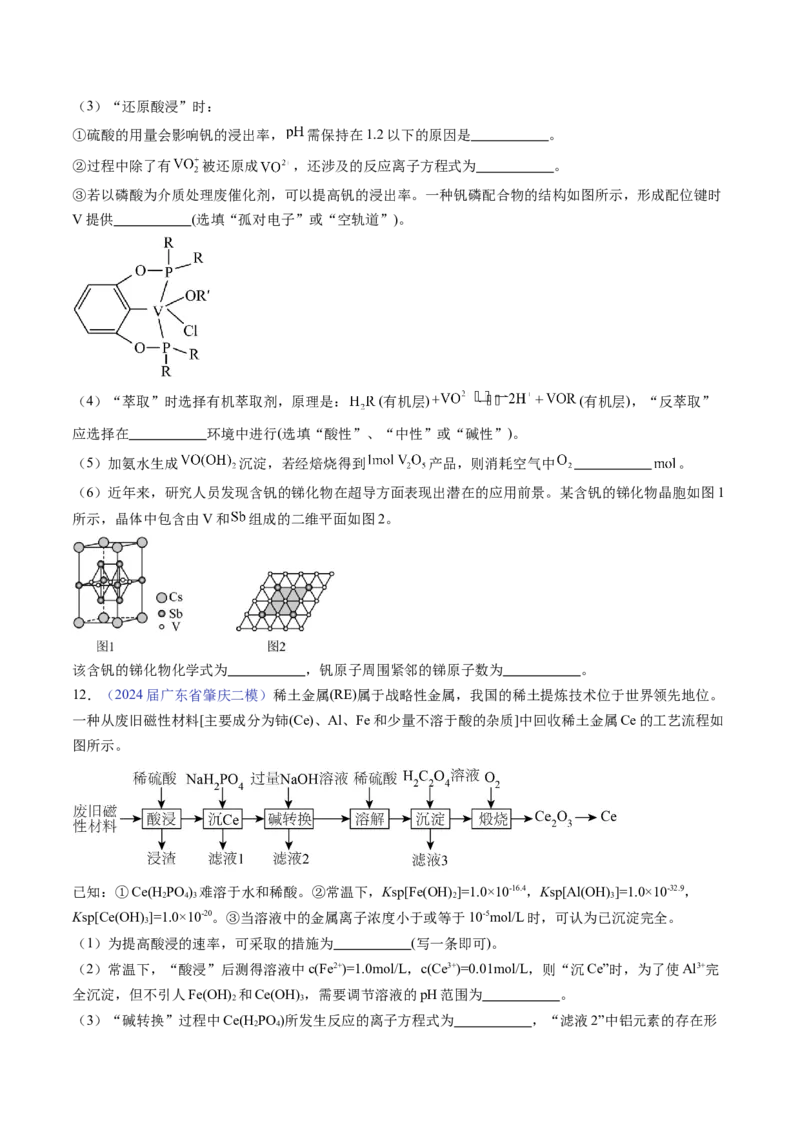
(6)近年来,研究人员发现含钒的锑化物在超导方面表现出潜在的应用前景。某含钒的锑化物晶胞如图1
所示,晶体中包含由V和 组成的二维平面如图2。
该含钒的锑化物化学式为 ,钒原子周围紧邻的锑原子数为 。
12.(2024届广东省肇庆二模)稀土金属(RE)属于战略性金属,我国的稀土提炼技术位于世界领先地位。
一种从废旧磁性材料[主要成分为铈(Ce)、Al、Fe和少量不溶于酸的杂质]中回收稀土金属Ce的工艺流程如
图所示。
已知:①Ce(HPO ) 难溶于水和稀酸。②常温下,Ksp[Fe(OH) ]=1.0×10-16.4,Ksp[Al(OH) ]=1.0×10-32.9,
2 4 3 2 3
Ksp[Ce(OH) ]=1.0×10-20。③当溶液中的金属离子浓度小于或等于10-5mol/L时,可认为已沉淀完全。
3
(1)为提高酸浸的速率,可采取的措施为 (写一条即可)。
(2)常温下,“酸浸”后测得溶液中c(Fe2+)=1.0mol/L,c(Ce3+)=0.01mol/L,则“沉Ce”时,为了使Al3+完
全沉淀,但不引人Fe(OH) 和Ce(OH) ,需要调节溶液的pH范围为 。
2 3
(3)“碱转换”过程中Ce(HPO )所发生反应的离子方程式为 ,“滤液2”中铝元素的存在形
2 4式为 (填化学式)。
(4)“沉淀”后所得的固体为Ce (C O)·10H O,将其煅烧可得Ce O 和一种无毒的气体,发生反应的化
2 2 4 3 2 2 3
学方程式为 。
(5)某稀土金属氧化物的立方晶胞如图所示,则该氧化物的化学式为 ,距离RE原子最近的
O原子有 个。若M(晶胞)=Mg/mol,晶胞边长为anm,N 为阿伏加德罗常数的值,则晶胞的密
A
度为 g/cm3(列出计算式)。
13.(2024届广东省省2月联考)钼具有耐腐耐磨的特性,目前广泛应用于化工、医疗和国防领域。一种
使用先进的碱性氧化焙烧法,从镍钼矿(主要成分是 )中回收钼的流程如图所示:
已知:①“焙烧”后钼元素以 的形式存在, 的化合价不变且以氧化物的形式存在,“焙烧”
过程中未见有含 气态物的生成。
② 。
③一般离子浓度达到 以下视为沉淀完全。
回答下列问题:
(1)写出“焙烧”过程中 发生反应的化学方程式: 。
(2)“滤渣1”的主要成分为 (填化学式)。
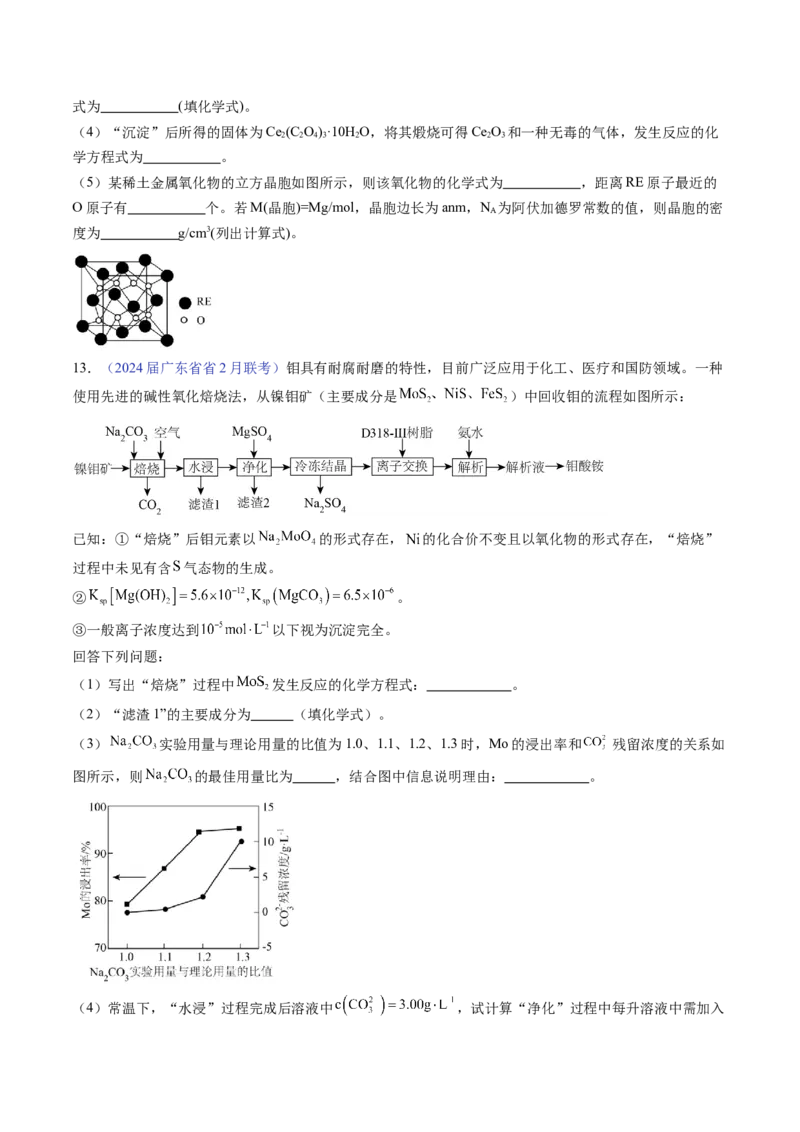
(3) 实验用量与理论用量的比值为1.0、1.1、1.2、1.3时,Mo的浸出率和 残留浓度的关系如
图所示,则 的最佳用量比为 ,结合图中信息说明理由: 。
(4)常温下,“水浸”过程完成后溶液中 ,试计算“净化”过程中每升溶液中需加入(保留两位有效数字) ,若“净化”完成后溶液的 ,则此时溶液中 (填“不存
在”或“存在”) 沉淀。
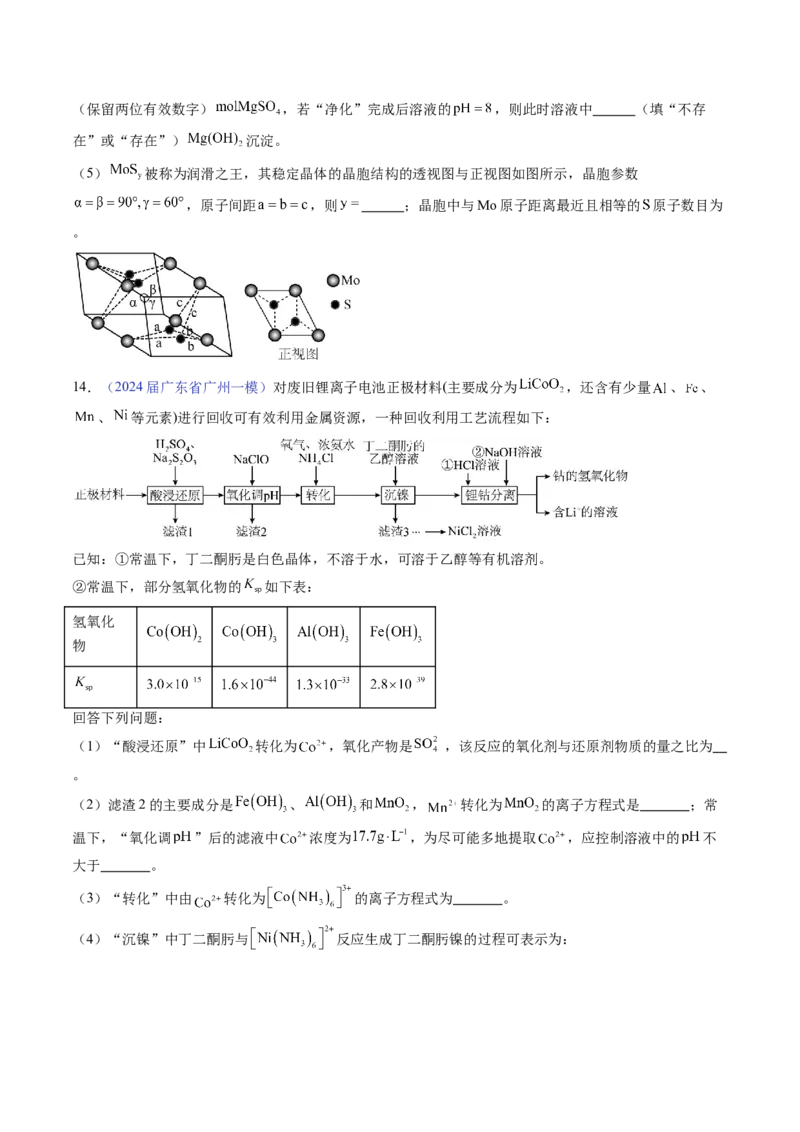
(5) 被称为润滑之王,其稳定晶体的晶胞结构的透视图与正视图如图所示,晶胞参数
,原子间距 ,则 ;晶胞中与Mo原子距离最近且相等的 原子数目为
。
14.(2024届广东省广州一模)对废旧锂离子电池正极材料(主要成分为 ,还含有少量 、 、
、 等元素)进行回收可有效利用金属资源,一种回收利用工艺流程如下:
已知:①常温下,丁二酮肟是白色晶体,不溶于水,可溶于乙醇等有机溶剂。
②常温下,部分氢氧化物的 如下表:
氢氧化
物
回答下列问题:
(1)“酸浸还原”中 转化为 ,氧化产物是 ,该反应的氧化剂与还原剂物质的量之比为
。
(2)滤渣2的主要成分是 、 和 , 转化为 的离子方程式是 ;常
温下,“氧化调 ”后的滤液中 浓度为 ,为尽可能多地提取 ,应控制溶液中的 不
大于 。
(3)“转化”中由 转化为 的离子方程式为 。
(4)“沉镍”中丁二酮肟与 反应生成丁二酮肟镍的过程可表示为:从滤渣3中分离出丁二酮肟固体的方法是 。
(5)“锂钴分离”可产生能重复利用的物质是 。
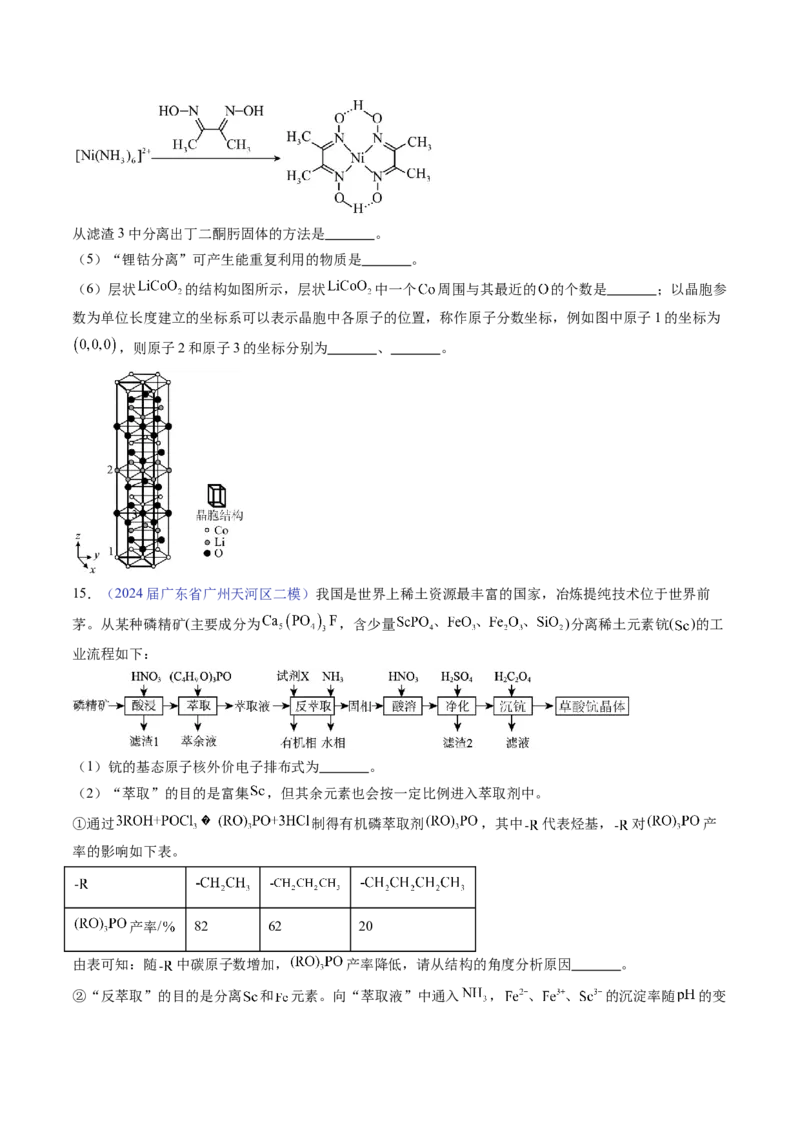
(6)层状 的结构如图所示,层状 中一个 周围与其最近的 的个数是 ;以晶胞参
数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中原子1的坐标为
,则原子2和原子3的坐标分别为 、 。
15.(2024届广东省广州天河区二模)我国是世界上稀土资源最丰富的国家,冶炼提纯技术位于世界前
茅。从某种磷精矿(主要成分为 ,含少量 )分离稀土元素钪( )的工
业流程如下:
(1)钪的基态原子核外价电子排布式为 。
(2)“萃取”的目的是富集 ,但其余元素也会按一定比例进入萃取剂中。
①通过 制得有机磷萃取剂 ,其中 代表烃基, 对 产
率的影响如下表。
产率/ 82 62 20
由表可知:随 中碳原子数增加, 产率降低,请从结构的角度分析原因 。
②“反萃取”的目的是分离 和 元素。向“萃取液”中通入 , 的沉淀率随 的变化如图。试剂X为 (填“ ”或“ ”),应调节 为 。
③反萃取时,通入 得到 沉淀的过程为:
i.
ii. (写出该过程的化学方程式)。
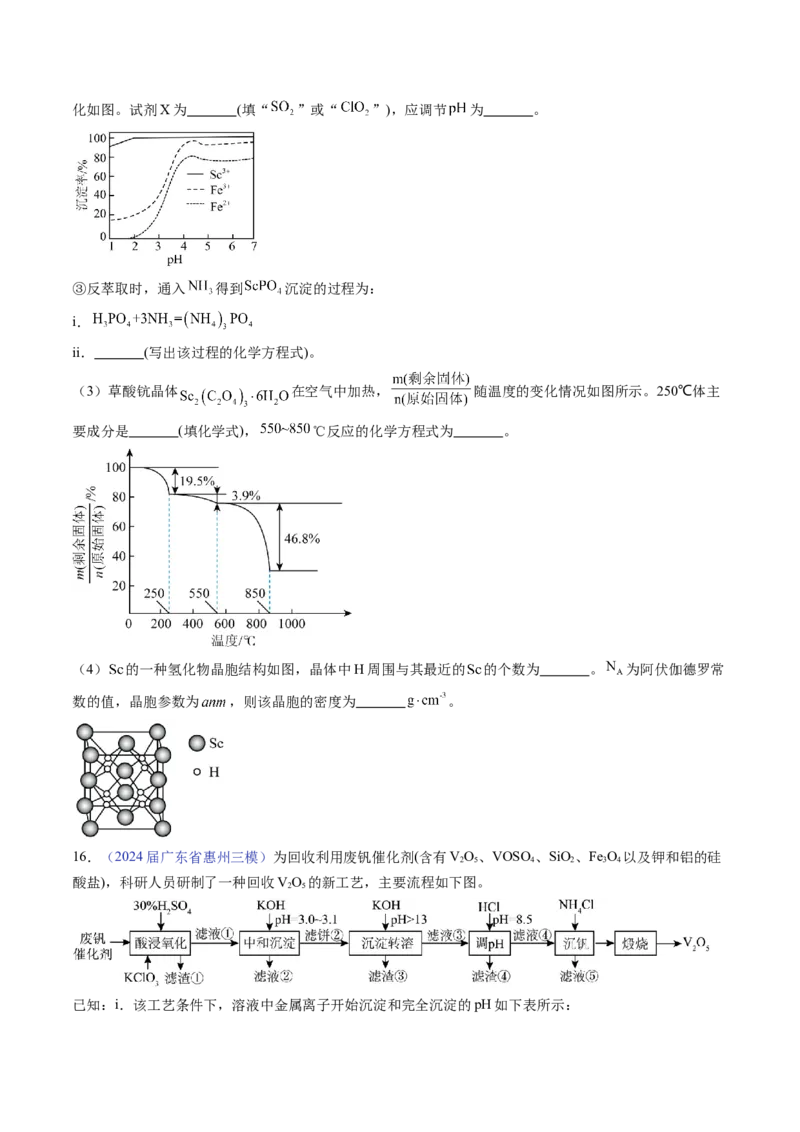
(3)草酸钪晶体 在空气中加热, 随温度的变化情况如图所示。250℃体主
要成分是 (填化学式), ℃反应的化学方程式为 。
(4) 的一种氢化物晶胞结构如图,晶体中H周围与其最近的 的个数为 。 为阿伏伽德罗常
数的值,晶胞参数为 ,则该晶胞的密度为 。
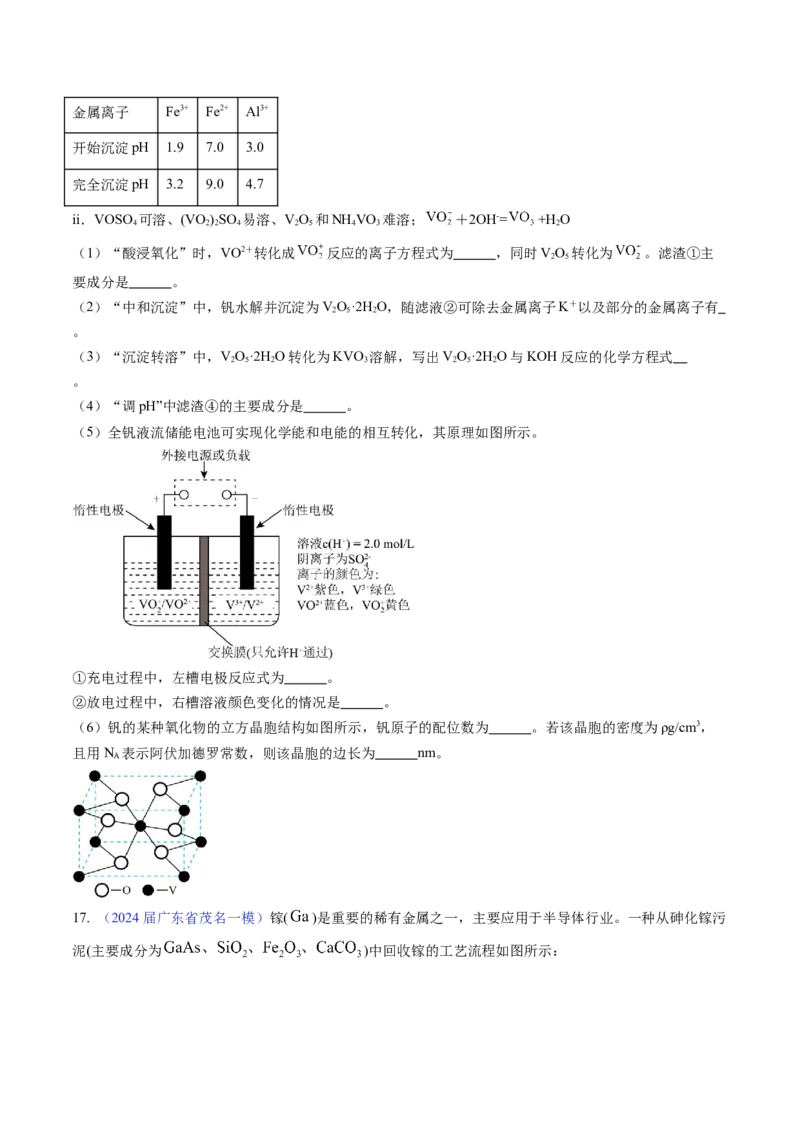
16.(2024届广东省惠州三模)为回收利用废钒催化剂(含有VO、VOSO、SiO、Fe O 以及钾和铝的硅
2 5 4 2 3 4
酸盐),科研人员研制了一种回收VO 的新工艺,主要流程如下图。
2 5
已知:i.该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:金属离子 Fe3+ Fe2+ Al3+
开始沉淀pH 1.9 7.0 3.0
完全沉淀pH 3.2 9.0 4.7
ii.VOSO 可溶、(VO )SO 易溶、VO 和NH VO 难溶; +2OH-= +H O
4 2 2 4 2 5 4 3 2
(1)“酸浸氧化”时,VO2+转化成 反应的离子方程式为 ,同时VO 转化为 。滤渣①主
2 5
要成分是 。
(2)“中和沉淀”中,钒水解并沉淀为VO·2H O,随滤液②可除去金属离子K+以及部分的金属离子有
2 5 2
。
(3)“沉淀转溶”中,VO·2H O转化为KVO 溶解,写出VO·2H O与KOH反应的化学方程式
2 5 2 3 2 5 2
。
(4)“调pH”中滤渣④的主要成分是 。
(5)全钒液流储能电池可实现化学能和电能的相互转化,其原理如图所示。
①充电过程中,左槽电极反应式为 。
②放电过程中,右槽溶液颜色变化的情况是 。
(6)钒的某种氧化物的立方晶胞结构如图所示,钒原子的配位数为 。若该晶胞的密度为ρg/cm3,
且用N 表示阿伏加德罗常数,则该晶胞的边长为 nm。
A
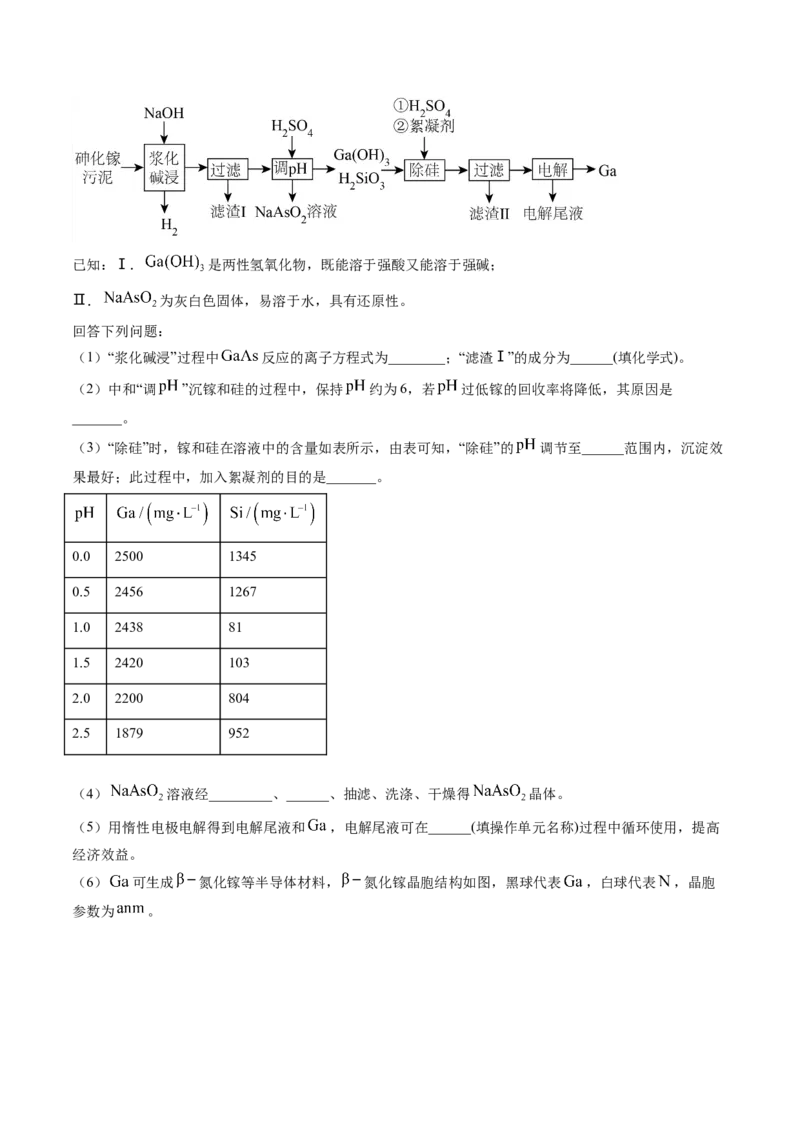
17. (2024届广东省茂名一模)镓( )是重要的稀有金属之一,主要应用于半导体行业。一种从砷化镓污
泥(主要成分为 )中回收镓的工艺流程如图所示:已知:Ⅰ. 是两性氢氧化物,既能溶于强酸又能溶于强碱;
Ⅱ. 为灰白色固体,易溶于水,具有还原性。
回答下列问题:
(1)“浆化碱浸”过程中 反应的离子方程式为________;“滤渣Ⅰ”的成分为______(填化学式)。
(2)中和“调 ”沉镓和硅的过程中,保持 约为6,若 过低镓的回收率将降低,其原因是
_______。
(3)“除硅”时,镓和硅在溶液中的含量如表所示,由表可知,“除硅”的 调节至______范围内,沉淀效
果最好;此过程中,加入絮凝剂的目的是_______。
0.0 2500 1345
0.5 2456 1267
1.0 2438 81
1.5 2420 103
2.0 2200 804
2.5 1879 952
(4) 溶液经_________、______、抽滤、洗涤、干燥得 晶体。
(5)用惰性电极电解得到电解尾液和 ,电解尾液可在______(填操作单元名称)过程中循环使用,提高
经济效益。
(6) 可生成 氮化镓等半导体材料, 氮化镓晶胞结构如图,黑球代表 ,白球代表 ,晶胞
参数为 。① 氮化镓晶体中每个 原子周围最近的 原子的个数为_____。
②距离最近的两个 原子之间的距离为_______ (用含 的代数式表示)。
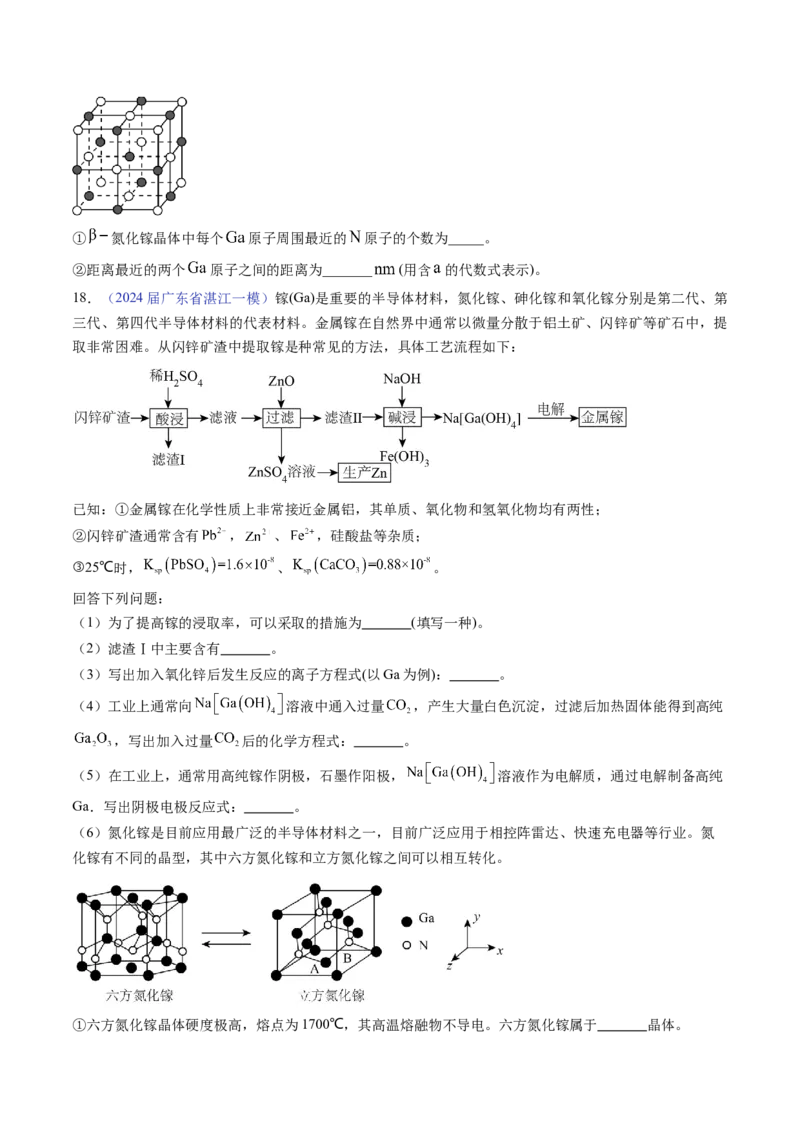
18.(2024届广东省湛江一模)镓(Ga)是重要的半导体材料,氮化镓、砷化镓和氧化镓分别是第二代、第
三代、第四代半导体材料的代表材料。金属镓在自然界中通常以微量分散于铝土矿、闪锌矿等矿石中,提
取非常困难。从闪锌矿渣中提取镓是种常见的方法,具体工艺流程如下:
已知:①金属镓在化学性质上非常接近金属铝,其单质、氧化物和氢氧化物均有两性;
②闪锌矿渣通常含有 , 、 ,硅酸盐等杂质;
③25℃时, 、 。
回答下列问题:
(1)为了提高镓的浸取率,可以采取的措施为 (填写一种)。
(2)滤渣Ⅰ中主要含有 。
(3)写出加入氧化锌后发生反应的离子方程式(以Ga为例): 。
(4)工业上通常向 溶液中通入过量 ,产生大量白色沉淀,过滤后加热固体能得到高纯
,写出加入过量 后的化学方程式: 。
(5)在工业上,通常用高纯镓作阴极,石墨作阳极, 溶液作为电解质,通过电解制备高纯
Ga.写出阴极电极反应式: 。
(6)氮化镓是目前应用最广泛的半导体材料之一,目前广泛应用于相控阵雷达、快速充电器等行业。氮
化镓有不同的晶型,其中六方氮化镓和立方氮化镓之间可以相互转化。
①六方氮化镓晶体硬度极高,熔点为1700℃,其高温熔融物不导电。六方氮化镓属于 晶体。②写出六方氮化镓晶胞的组成: 。
(7)①已知 的坐标为 ,请写出 的坐标 。
②若立方氮化镓的边长为a nm,则其密度为 (列出计算式)。
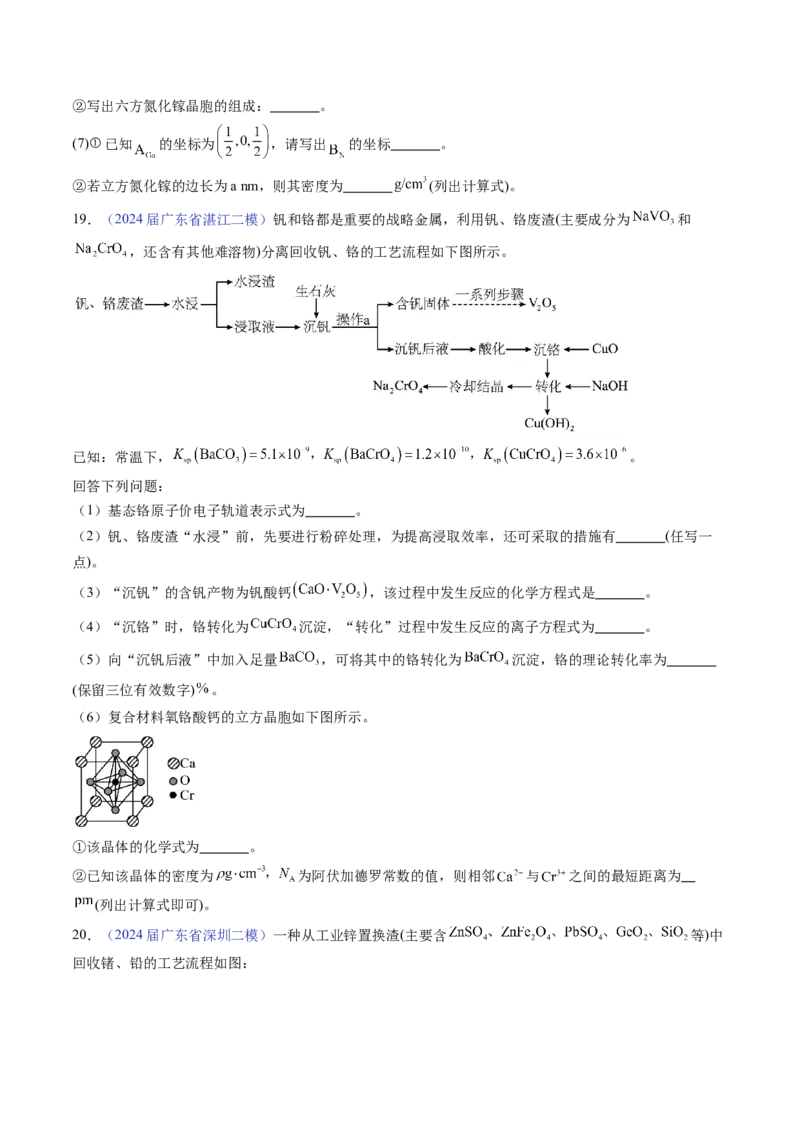
19.(2024届广东省湛江二模)钒和铬都是重要的战略金属,利用钒、铬废渣(主要成分为 和
,还含有其他难溶物)分离回收钒、铬的工艺流程如下图所示。
已知:常温下, 。
回答下列问题:
(1)基态铬原子价电子轨道表示式为 。
(2)钒、铬废渣“水浸”前,先要进行粉碎处理,为提高浸取效率,还可采取的措施有 (任写一
点)。
(3)“沉钒”的含钒产物为钒酸钙 ,该过程中发生反应的化学方程式是 。
(4)“沉铬”时,铬转化为 沉淀,“转化”过程中发生反应的离子方程式为 。
(5)向“沉钒后液”中加入足量 ,可将其中的铬转化为 沉淀,铬的理论转化率为
(保留三位有效数字) 。
(6)复合材料氧铬酸钙的立方晶胞如下图所示。
①该晶体的化学式为 。
②已知该晶体的密度为 为阿伏加德罗常数的值,则相邻 与 之间的最短距离为
(列出计算式即可)。
20.(2024届广东省深圳二模)一种从工业锌置换渣(主要含 等)中
回收锗、铅的工艺流程如图:已知: 能溶于强酸的浓溶液或强碱溶液; 可溶于热盐酸中: ;常温下,
。
(1)“还原浸出”时, 的存在可促进 浸出。
① 的空间结构为 。
②该反应中氧化剂与还原剂的物质的量之比为 。
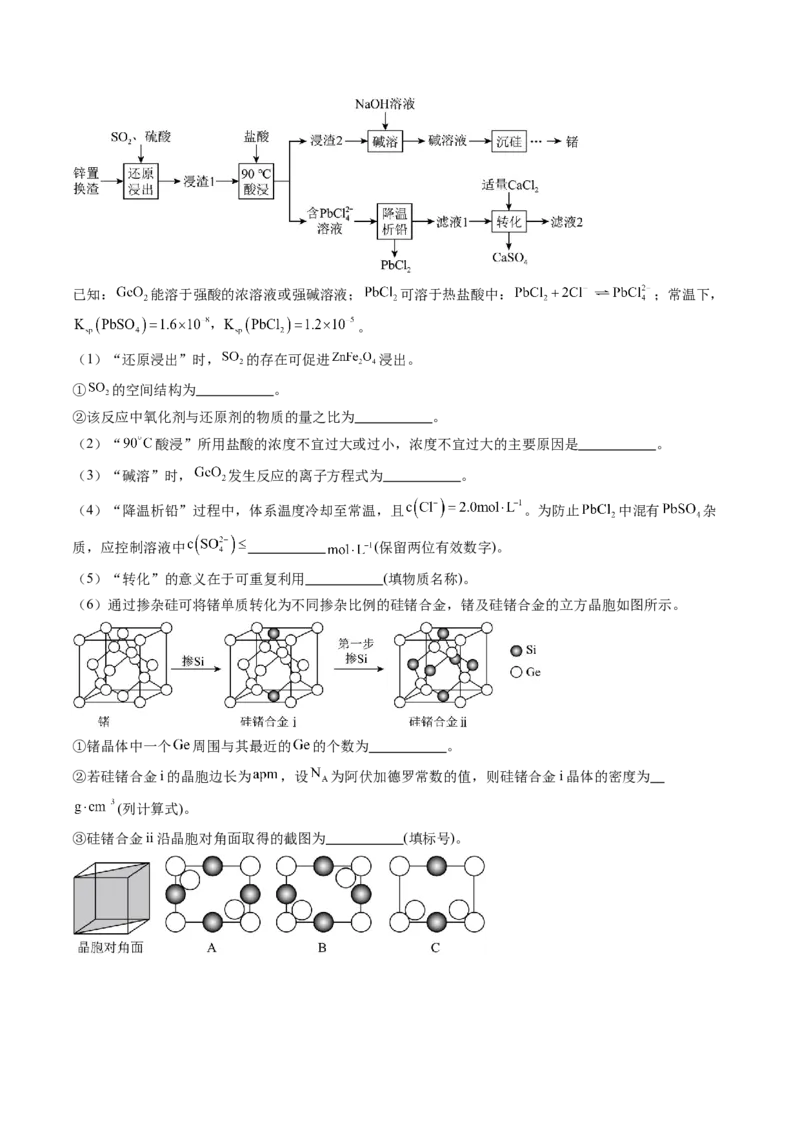
(2)“ 酸浸”所用盐酸的浓度不宜过大或过小,浓度不宜过大的主要原因是 。
(3)“碱溶”时, 发生反应的离子方程式为 。
(4)“降温析铅”过程中,体系温度冷却至常温,且 。为防止 中混有 杂
质,应控制溶液中 (保留两位有效数字)。
(5)“转化”的意义在于可重复利用 (填物质名称)。
(6)通过掺杂硅可将锗单质转化为不同掺杂比例的硅锗合金,锗及硅锗合金的立方晶胞如图所示。
①锗晶体中一个 周围与其最近的 的个数为 。
②若硅锗合金i的晶胞边长为 ,设 为阿伏加德罗常数的值,则硅锗合金i晶体的密度为
(列计算式)。
③硅锗合金ii沿晶胞对角面取得的截图为 (填标号)。