文档内容
易错专题 11 电化学基础
聚焦易错点:
►易错点一 化学电源
►易错点二 电解原理的应用
典例精讲
易错点一 化学电源
【易错典例】
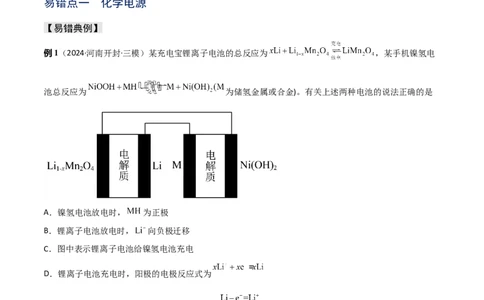
例1(2024·河南开封·三模)某充电宝锂离子电池的总反应为 ,某手机镍氢电
池总反应为 为储氢金属或合金)。有关上述两种电池的说法正确的是
A.镍氢电池放电时, 为正极
B.锂离子电池放电时, 向负极迁移
C.图中表示锂离子电池给镍氢电池充电
D.锂离子电池充电时,阳极的电极反应式为
C【分析】锂离子电池放电时负极电极反应式为 ,正极电极反应式为
,充电时,阳极电极反应式为 ,阴极电
极反应式为 ;镍氢电池放电时负极电极反应式为 ,正极电极反应式为
,充电时阳极的电极反应式为 ,阴极的电极反应式为。A.镍氢电池放电时, 为负极,A错误;B.锂离子电池放电时, 向正极迁移,
参与正极反应,B错误;C.图中表示锂离子电池给镍氢电池充电,C正确;D.锂离子电池充电时,阳极
的电极反应式为 ,D错误。
【解题必备】
1.化学电源
(1)放电是原电池反应,充电是电解池反应。
(2)判断电池放电时电极极性和材料,可先标出放电(原电池)总反应式电子转移的方向和数目,失去
电子的一极为负极,该物质即为负极材料;得到电子的一极为正极,该物质即为正极材料。若判断电池充
电时电极极性和材料,方法同前,失去电子的一极为阳极,该物质即为阳极材料;得到电子的一极为阴极,
该物质即为阴极材料。
(3) 放电时,阴离子移向负极,阳离子移向正极;充电时,阴离子移向阳极,阳离子移向阴极。
(4) 可充电电池用完后充电时,原电池的负极与外电源的负极相连,原电池的正极与外电源的正极相连。
(5)放电(原电池)的负极及充电(电解池)的阳极均失去电子,发生了氧化反应,其变价元素被氧化;
放电(原电池)的正极及充电(电解池)的阴极均得到电子,发生了还原反应,其变价元素被还原。
(6)书写可充电电池电极反应式,一般都是先书写放电的电极反应式。书写放电的电极反应式时,一般
要遵守三步:先标出原电池总反应式电子转移的方向和数目,指出参与负极和正极反应的物质;写出一个
比较容易书写的电极反应式(书写时一定要注意电极产物是否与电解质溶液共存);在电子守恒的基础上,
总反应式减去写出的电极反应式即得另一电极反应式。充电的电极反应与放电的电极反应过程相反,充电
的阳极反应为放电正极反应的逆过程,充电的阴极反应为放电负极反应的逆过程。
2.燃料电池
(1)燃料电池就是将燃料(如氢气、甲烷、乙醇等)氧化时,化学能直接转变为电能的装置。它由燃料、
氧化剂、电极、电解质组成。在结构上具有正负极,且正负极被电解质分隔。所有燃料电池的基本形式为:
将燃料和氧气(或空气)分别充入负极和正极,两者在电极的催化下发生化学反应,从而产生电流。
(2)燃料电池在放电时发生的总反应和燃料燃烧的总反应一样。一般是氧气做氧化剂,可燃物为还原剂。
据电池的基本原理,负极发生氧化反应,正极发生还原反应,所以可燃物为负极反应物,氧气为正极反应
物。
(3)根据燃烧反应的方程式书写电极反应式应遵循原子守恒、电子守恒及电荷守恒 ,注意电解质溶液参
与电极反应,若电解质溶液为碱溶液,则正极反应式为:O+2HO+4e - =4OH-;若电解质溶液为酸溶液,则
2 2
正极反应式为O+4H++4e-=2HO;若电解质为熔融碳酸盐,则正极反应式为O+4e- +2CO=2CO2-。
2 2 2 2 33.新型电池的电极反应式
总反应:AgO+Zn+HO 2Ag+Zn(OH)
2 2 2
锌银电池 正极:AgO+HO+2e-===2Ag+2OH-
2 2
负极:Zn+2OH--2e-===Zn(OH)
2
总反应:NiO+Fe+2HO Fe(OH)+Ni(OH)
2 2 2 2
镍铁电池
正极:NiO+2e-+2HO===Ni(OH)+2OH-
2 2 2
负极:Fe-2e-+2OH-===Fe(OH)
2
总反应:3Zn+2KFeO+8HO 3Zn(OH)+2Fe(OH)+4KOH
2 4 2 2 3
高铁电池
正极:FeO+3e-+4HO===Fe(OH)+5OH-
2 3
负极:Zn-2e-+2OH-===Zn(OH)
2
总反应:Cd+2NiOOH+2HO Cd(OH)+2Ni(OH)
2 2 2
镍镉电池
正极:NiOOH+HO+e-===Ni(OH)+OH-
2 2
负极:Cd-2e-+2OH-===Cd(OH)
2
总反应:HO+2H++Mg===Mg2++2HO
2 2 2
MgHO 电池 正极:HO+2H++2e-===2HO
2 2 2 2 2
负极:Mg-2e-===Mg2+
总反应:Mg+2AgCl===2Ag+MgCl
2
MgAgCl电池 正极:2AgCl+2e-===2Ag+2Cl-
负极:Mg-2e-===Mg2+
总反应:2Na+xS===NaS
2 x
钠硫电池 正极:xS+2e-===S
负极:2Na-2e-===2Na+
总反应:VO+2H++V2+ V3++VO2++HO
2
全钒液流电池
正极:VO+2H++e-===VO2++HO
2
负极:V2+-e-===V3+
总反应:2Li+CuO+HO===2Cu+2Li++2OH-
2 2
锂铜电池 正极:CuO+HO+2e-===2Cu+2OH-
2 2
负极:Li-e-===Li+总反应:Li CoO+LiC LiCoO+C(x<1)
1-x 2 x 6 2 6
锂离子电池
正极:Li CoO+xe-+xLi+===LiCoO
1-x 2 2
负极:LiC-xe-===xLi++C
x 6 6
【变式突破】
1.(2024·黑龙江大庆·模拟预测)某实验小组用这种电极构建全碱性肼-硝酸根燃料电池(结构如图所示)。
已知:双极膜由阴、阳离子膜组成,双极膜中水电离出 和 ,在电场力作用下向两极迁移。
下列叙述错误的是
A.电极a为负极,电极b为正极
B.电极b上的电极反应式为
C.转移nmol电子时,负极区质量减少7ng
D.电极a上生成 时,有 向电极b迁移
C【分析】由题干原电池装置图可知,电极a为由N H 转化为N ,发生氧化反应,故a为负极,电极反应
2 4 2
为:N H -4e-+4OH-=N +4H O,则b为正极,电极反应为: +6H O+8e-=NH +9OH-。A.由分析可知,电极
2 4 2 2 2 3
a为负极,电极b为正极,A正确;B.由分析可知,电极b上的电极反应式为
,B正确;C.由分析可知,转移nmol电子时,负极区逸出7ng的N ,同时
2
流入17ng的OH-,故质量增重10ng,C错误;D.由分析可知,a为负极,电极反应为:N H -4e-+4OH-
2 4
=N +4H O,则电极a上生成 时电路上通过的电子的物质的量为: =0.8mol,根据电荷守恒
2 2可知有 向电极b迁移,D正确。
2.(2024·宁夏银川·二模)我国科学家设计一种以ZnI 水溶液作为锌离子电池介质的Zn-BiOI电池,通过
2
Bi/Bi3+与I-/I 转化反应之间的协同作用实现优异的电化学性能,原理如图所示。碘离子作为氧化还原媒介体,
可以加快动力学转化过程,促进更快的电荷转移。下列说法错误的是
A.充电时,主要发生的电池反应为2Bi+2Bi O +3ZnI =6BiOI+3Zn
2 3 2
B.放电时,部分I-在Zn电极转化为I
C.充电时,每生成1molBiOI,转移电子数为3mol
D.电池工作时,I-与I 之间转化反应能够提供额外的电化学容量
C【分析】该电池为二次电池,放电时锌作负极,BiOI作正极,放电时电池的总反应为:
6BiOI+3Zn=2Bi+2Bi O +3ZnI ;充电时的总反应为:2Bi+2Bi O +3ZnI =6BiOI+3Zn。A.由分析可知,充电时,
2 3 2 2 3 2
主要发生的电池反应为2Bi+2Bi O +3ZnI =6BiOI+3Zn,A正确;B.由分析可知,放电时,部分I-在Zn电极失
2 3 2
去电子转化为I ,然后I 与I-反应转化为I ,B正确;C.由总反应可知,每生成6molBiOI时有2molBi参与
2 2
反应,转移6mol电子,即生成1molBiOI,转移1mole-,C错误;D.由B项分析可知,电池工作时,I-与I
之间转化反应能够提供额外的电化学容量,D正确。
3.(2024·江西萍乡·二模)锂离子电池及其迭代产品依然是目前世界上主流的手机电池。科学家近期研发
的一种新型的Ca—LiFePO 可充电电池的原理示意图如图,电池反应为:
4,下列说法正确的是
A.放电时,钙电极为负极,发生还原反应
B.充电时, / 电极的电极反应式为
C.锂离子导体膜的作用是允许Li+和水分子通过,同时保证Li+定向移动以形成电流
D.充电时,当转移0.2mol电子时,理论上阴极室中电解质的质量减轻4.0g
B【分析】放电时,Ca失电子转化为Ca2+,则钙电极为负极, / 电极为正极;充电时,钙
电极为阴极, / 电极为阳极。A.由分析可知,放电时,钙电极为负极,失电子发生氧化
反应,A不正确;B.充电时, / 电极为阳极, 失电子转化为 和Li+,
电极反应式为 ,B正确;C.Ca的金属性强,能与水发生剧烈反应,所以
LiPF -LiAsF 为非水电解质,锂离子导体膜不允许水分子通过,锂离子导体膜允许Li+通过,其主要作用是允
6 6
许Li+定向移动,构成闭合回路,从而形成电流,C不正确;D.充电时,当转移0.2mol电子时,理论上阴
极室电解质中0.1mol Ca2+得电子生成0.1mol Ca,同时迁移入Li+0.2mol,质量减
轻0.1mol×40g/mol-0.2mol×7g/mol=2.6g,D不正确。
易错点二 电解原理的应用
【易错典例】
例2(2024·云南曲靖·二模)我国科学家设计了一种基于时间解耦氨分解的新型可充电 电池,以实
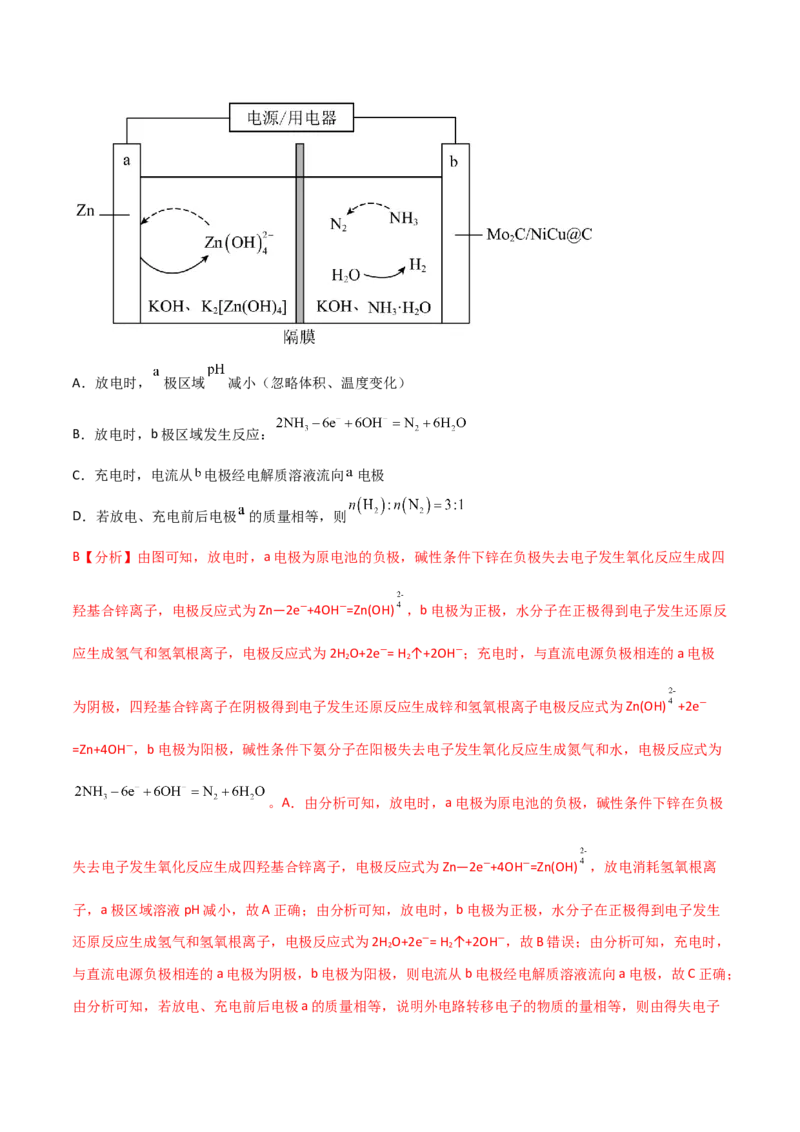
现 到 的高效转化,其原理如下图所示,下列说法错误的是A.放电时, 极区域 减小(忽略体积、温度变化)
B.放电时,b极区域发生反应:
C.充电时,电流从 电极经电解质溶液流向 电极
D.若放电、充电前后电极 的质量相等,则
B【分析】由图可知,放电时,a电极为原电池的负极,碱性条件下锌在负极失去电子发生氧化反应生成四
羟基合锌离子,电极反应式为Zn—2e—+4OH—=Zn(OH) ,b电极为正极,水分子在正极得到电子发生还原反
应生成氢气和氢氧根离子,电极反应式为2H O+2e—= H ↑+2OH—;充电时,与直流电源负极相连的a电极
2 2
为阴极,四羟基合锌离子在阴极得到电子发生还原反应生成锌和氢氧根离子电极反应式为Zn(OH) +2e—
=Zn+4OH—,b电极为阳极,碱性条件下氨分子在阳极失去电子发生氧化反应生成氮气和水,电极反应式为
。A.由分析可知,放电时,a电极为原电池的负极,碱性条件下锌在负极
失去电子发生氧化反应生成四羟基合锌离子,电极反应式为Zn—2e—+4OH—=Zn(OH) ,放电消耗氢氧根离
子,a极区域溶液pH减小,故A正确;由分析可知,放电时,b电极为正极,水分子在正极得到电子发生
还原反应生成氢气和氢氧根离子,电极反应式为2H O+2e—= H ↑+2OH—,故B错误;由分析可知,充电时,
2 2
与直流电源负极相连的a电极为阴极,b电极为阳极,则电流从b电极经电解质溶液流向a电极,故C正确;
由分析可知,若放电、充电前后电极a的质量相等,说明外电路转移电子的物质的量相等,则由得失电子数目守恒可知,放电时生成氢气和充电时生成氨气的物质的量比为3:1,故D正确。
【解题必备】
1.“三池”的判断:电化学知识包括原电池和电解池,首先要确定装置是原电池还是电解池。若无外接电
源,可能是原电池,然后依据原电池的形成条件分析判定;若有外接电源,两极插入电解质溶液中,则可
能是电解池或电镀池,当阳极金属与电解质溶液中的金属阳离子相同则为电镀池,其他情况为电解池。
2.常见考点归纳
负极:元素化合价升高或发生氧化反应的物质
电极判断 正极:元素化合价降低或发生还原反应的物质
阴极:“放电”时的负极在“充电”时为阴极
阳极:“放电”时的正极在“充电”时为阳极
电子流向 原电池:负极→正极
电解池:电源负极→阴极,阳极→电源正极
离子流向 原电池:阳离子移向正极,阴离子移向负极
电解池:阳离子移向阴极,阴离子移向阳极
“放电”时依据条件,指出参与负极和正极反应的物质,根据化合价的
变化,判断转移电子的数目;根据守恒书写负极(或正极)反应式,特别应
电极反应式
注意电极产物是否与电解质溶液共存
充电时的电极反应与放电时的电极反应过程相反,充电的阳极反应为放
电时正极反应的逆过程,充电的阴极反应为放电时负极反应的逆过程
离子交换膜 离子交换膜是一种选择性透过膜,离子交换膜的作用是允许相应离子通
过,离子迁移方向遵循原电池或电解池中离子迁移方向
3.金属腐蚀与保护
(1)析氢腐蚀和吸氧腐蚀
类型 析氢腐蚀 吸氧腐蚀
条件 水膜呈酸性 水膜呈弱酸性或中性
正极反应 2H++2e-===H↑ O+2HO+4e-===4OH-
2 2 2
负极反应 Fe-2e-===Fe2+
Fe2++2OH-===Fe(OH) ↓
2
其他反应 4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
Fe(OH) 失去部分水转化为铁锈
3
(2)金属腐蚀的防护方法
①加防护层:如在金属表面加上油漆、搪瓷、沥青、塑料、橡胶等耐腐蚀的非金属材料;采用电镀或表面
钝化等方法在金属表面镀上一层不易被腐蚀的金属或生成一层致密的薄膜。
②电化学防护法:牺牲阳极的阴极保护法——原电池原理:正极为被保护的金属,负极为比被保护的金属
活泼的金属;外加电流的阴极保护法——电解原理:阴极为被保护的金属,阳极为惰性电极。
【变式突破】
4.(2024·湖北·三模)一种新型原电池的工作原理如图所示,其中电极材料均为石墨,阴离子交换膜只允许 通过,工作时两极室均无气体生成。下列说法错误的是
A.电极a为负极 B.工作时乙室溶液pH减小
C.该电池的总反应为 D.每转移 时甲室质量增加48g
B【详解】A.根据 移动方向可知a极为负极,A正确;B.b极为正极,发生反应
,电池工作时乙室溶液pH增大,B错误;C.该电池的总反应为 ,
C正确;D.甲室发生反应 ,电池工作时每转移 甲室迁移进入 ,质量
增加48g,D正确。
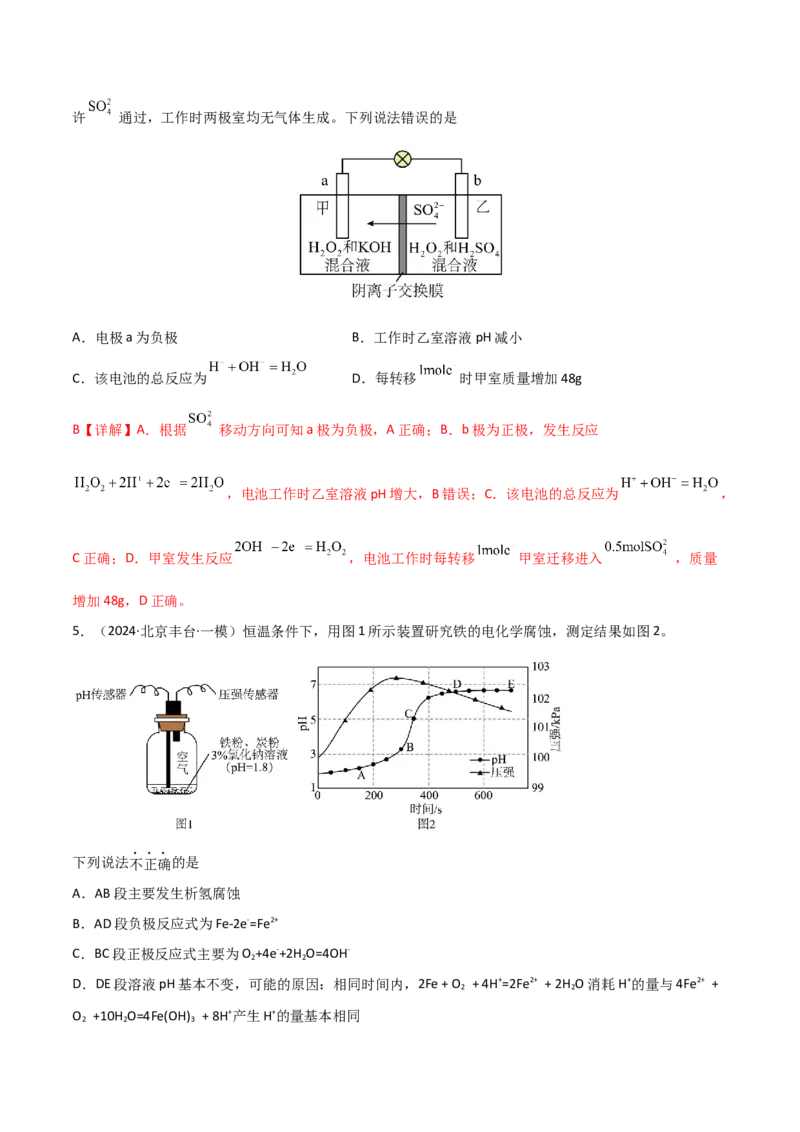
5.(2024·北京丰台·一模)恒温条件下,用图1所示装置研究铁的电化学腐蚀,测定结果如图2。
下列说法不正确的是
A.AB段主要发生析氢腐蚀
B.AD段负极反应式为Fe-2e-=Fe2+
C.BC段正极反应式主要为O +4e-+2H O=4OH-
2 2
D.DE段溶液pH基本不变,可能的原因:相同时间内,2Fe + O + 4H+=2Fe2+ + 2H O消耗H+的量与4Fe2+ +
2 2
O +10H O=4Fe(OH) + 8H+产生H+的量基本相同
2 2 3C【分析】图1中构成原电池,铁作负极,开始时pH=1.8,AB段溶液pH值增大,体系压强增大,铁主要发
生析氢腐蚀;BD段溶液的pH值增加,体系压强减小,正极反应式为:O +4e-+4H+=2H O;DE段溶液pH基
2 2
本不变,但压强减小,产生的Fe2+被O 氧化,pH基本不变可能的原因:相同时间内,2Fe + O + 4H+=2Fe2+
2 2
+ 2H O消耗H+的量与4Fe2+ + O +10H O=4Fe(OH) + 8H+产生H+的量基本相同。A.由图可知,AB段体系的
2 2 2 3
压强增大,说明产生了氢气,故AB段主要发生析氢腐蚀,A正确;AD段内发生的都是铁的电化学腐蚀,
铁在负极的电极式为:Fe-2e-=Fe2+,B正确;由图可知BC段的pH为3-5,正极不能产生氢氧根,电极反应
式为:O +4e-+4H+=2H O,C错误。
2 2
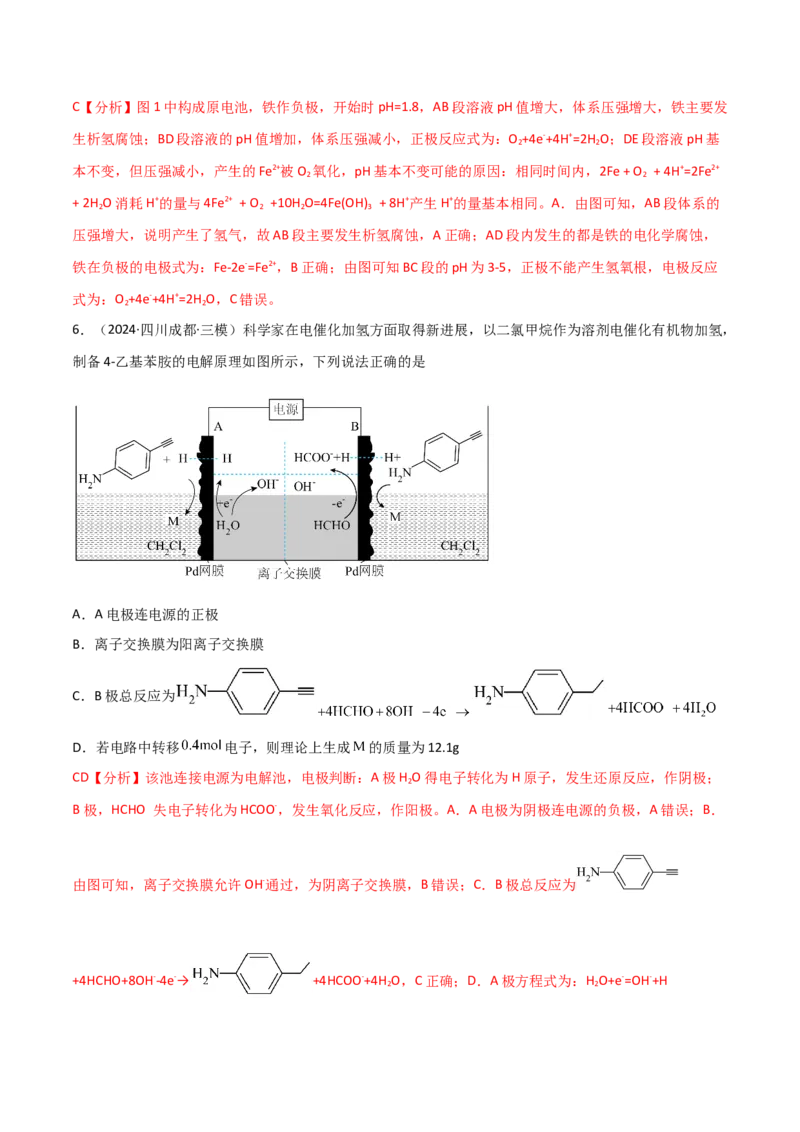
6.(2024·四川成都·三模)科学家在电催化加氢方面取得新进展,以二氯甲烷作为溶剂电催化有机物加氢,
制备4-乙基苯胺的电解原理如图所示,下列说法正确的是
A.A电极连电源的正极
B.离子交换膜为阳离子交换膜
C.B极总反应为
D.若电路中转移 电子,则理论上生成 的质量为12.1g
CD【分析】该池连接电源为电解池,电极判断:A极H O得电子转化为H原子,发生还原反应,作阴极;
2
B极,HCHO 失电子转化为HCOO-,发生氧化反应,作阳极。A.A电极为阴极连电源的负极,A错误;B.
由图可知,离子交换膜允许OH-通过,为阴离子交换膜,B错误;C.B极总反应为
+4HCHO+8OH--4e-→ +4HCOO-+4H O,C正确;D.A极方程式为:H O+e-=OH-+H
2 2+4H→ ,M的摩尔质量为121g/mol,若电路中转移0.4mol电子,则
理论上生成0.1molM的质量为12.1g,D正确。
考点精练
1.(2024·广东·二模)一种基于原电池原理的氧气传感器可用于测定样气中氧气的含量,其装置如图所示。
下列说法正确的是
A.铅电极为正极
B.银电极上发生的反应为
C.电子由铅电极经过KOH溶液流向银电极
D.工作过程中,传感器的质量不变
2.(2024·陕西西安·二模)我国科研人员研究出了通过电耦合直接将空气转化为硝酸的方法,其反应原理
如图所示( 表示自由基,具有强氧化性),下列说法不正确的是
A.与a相连的电极上发生的反应为:
B.离子交換膜是阴离子交换膜
C.反应②为:D.每生成 ,阳极产生 (标准状况下)
3.(2024·陕西榆林·一模)含 的废水在废水处理过程中与臭氧发生反应会产生 。模拟在
上电催化处理 的示意图如图所示,下列说法正确的是
A.电子流向: 导线 电解质溶液
B.该装置工作时,阳极区溶液酸性减弱
C.P极上的电极反应式为
D.每处理 ,理论上可生成
4.(2024·海南·一模)一种采用天燃气为原料气、固体氧化锆为电解质的装置,其结构如图。下列有关说
法正确的是A.电池工作时, 从 极区移向 极区
B. 极上的电极反应式为
C.两极物质消耗的比例:
D.电池工作一段时间后,电解质物质的量理论上保持不变
5.(2024·河北邢台·二模)中国科学院物理研究所发明了一种以对苯二甲酸二钠复合材料和硬碳(多孔形态,
化学式为C)为电极材料的有机钠离子电池,其内部结构如下图所示,放电时,a电极发生如下变化:
下列说法错误的是
A.放电时,a电极电势高于b电极
B.充电时, 向b电极移动
C.放电时,b电极的电极反应式为
D.用该电池为一个60200mAh的充电宝充满电,a电极质量增加51.75g( ,一个电子的电量
, 为 )
6.(2024·内蒙古呼和浩特·二模)用电解法(图1)通过翻转电极可同时处理含 和 的生活污水,联
合脱除过程中,测得溶液pH变化如图2所示。0~20分钟除去 的原理如图3所示,20~40分钟除
的方法是将其转化为 沉淀。下列说法不正确的是
A.在 时内,a为电源的负极
B.除 时,阳极的电极反应式为:
C.除 过程中,溶液pH变小
D.除 的总反应离子方程式为:
7.(2024·山西运城·二模)近日,美国威斯康星大学麦迪逊分校课题组使用锰一四苯基卟啉催化剂将电化
学氧还原和水氧化进行配对,在两个电极上生成活性锰一氧物种,从而将 转化为 。
下列叙述正确的是
A.a极电势高于 极
B. 极反应:
C.电路上转移 电子理论上生成
D.“ 和 ”总量几乎不变8.(2024·河北·二模)一种催化重整利用PET废塑料水解产物乙二醇耦合二氧化碳高效生成甲酸的工作原
理如图所示。下列说法错误的是
A.a极为直流电源的负极
B. 电极反应为
C.该离子交换膜为阴离子交换膜
D.当外电路中转移 电子时,阴极区溶液质量增重
9.(2024·广东惠州·一模)将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池(如图所示),
该电池可将可乐 中的葡萄糖转化成葡萄糖内酯,下列说法正确的是
A.葡萄糖发生还原反应
B.MnO 在正极失电子
2
C.H+由a极移向b极
D.当电路中转移0.1N 个电子时,生成0.1mol葡萄糖内酯
A
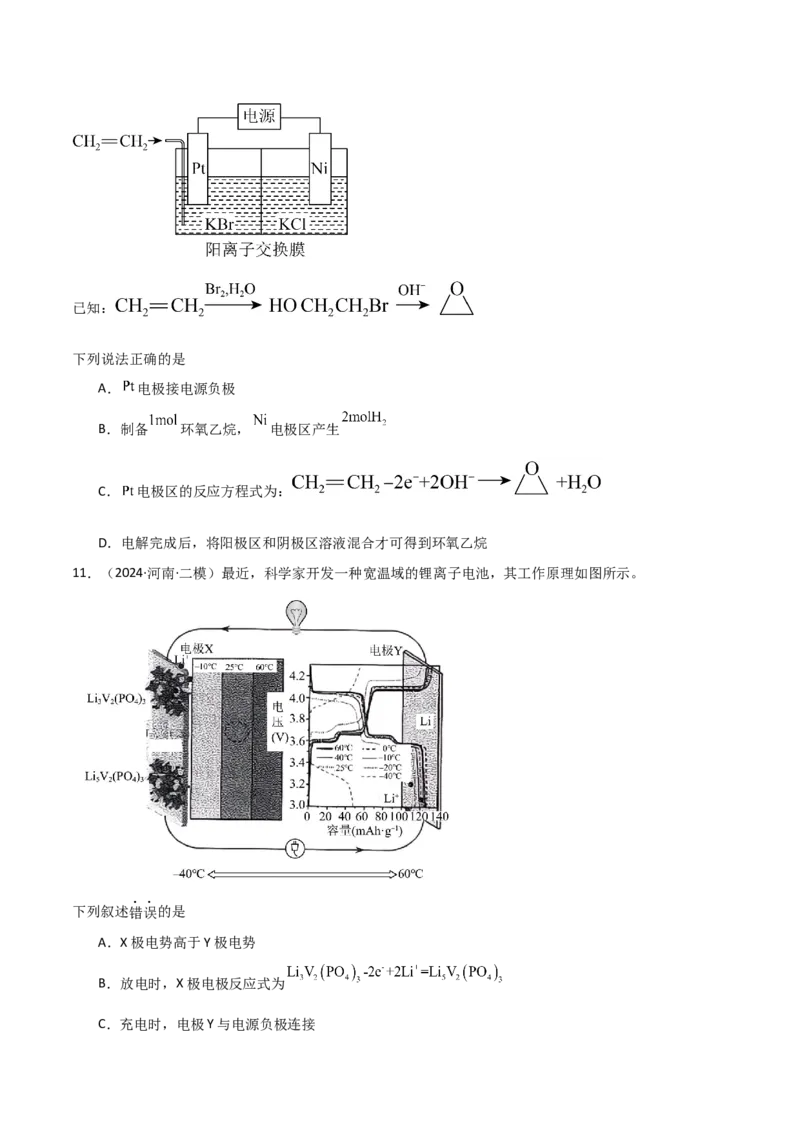
10.(2024·广东惠州·一模)环氧乙烷( )可用于生产乙二醇。电化学合成环氧乙烷( )的装置如图
所示:已知:
下列说法正确的是
A. 电极接电源负极
B.制备 环氧乙烷, 电极区产生
C. 电极区的反应方程式为:
D.电解完成后,将阳极区和阴极区溶液混合才可得到环氧乙烷
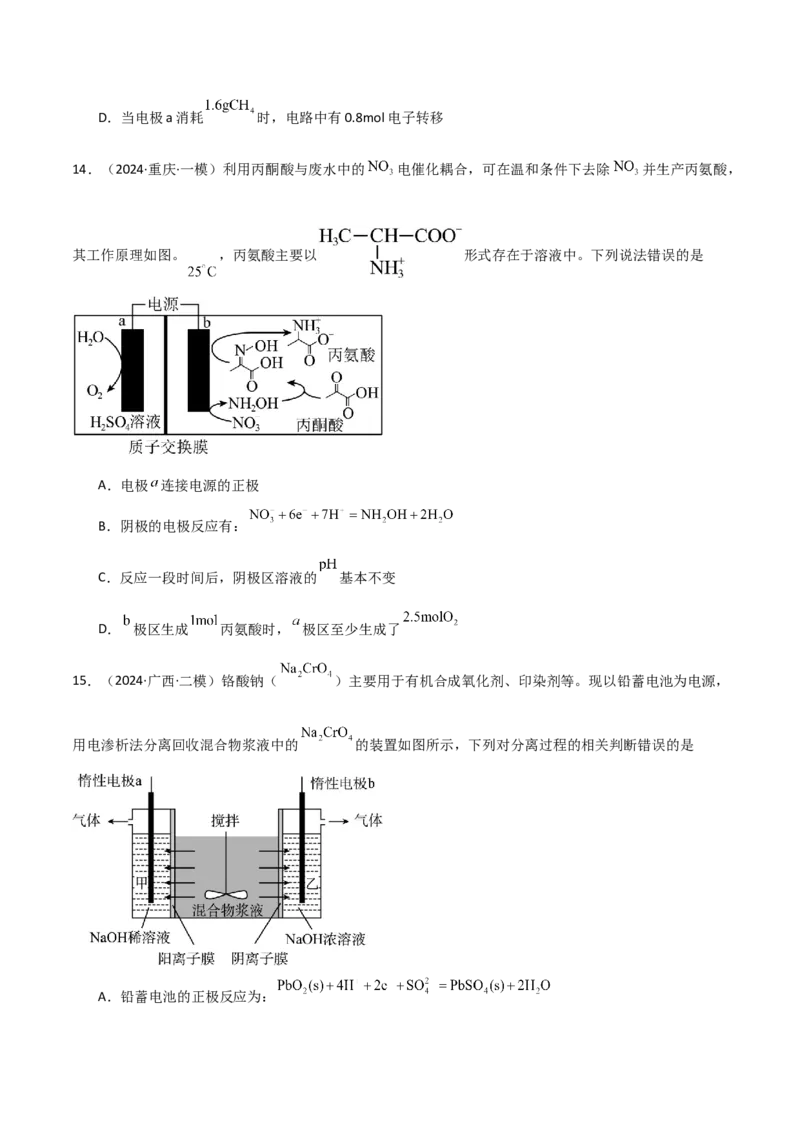
11.(2024·河南·二模)最近,科学家开发一种宽温域的锂离子电池,其工作原理如图所示。
下列叙述错误的是
A.X极电势高于Y极电势
B.放电时,X极电极反应式为
C.充电时,电极Y与电源负极连接D.充电时,每生成1.4 g Li时理论上转移电子数约为
12.(2024·山西晋中·二模)我国科学家设计可同时实现 制备和海水淡化的新型电池,其工作原理如图
所示。下列说法正确的是
A.电极上的电势
B.d是阳离子交换膜
C.电极 上的电极反应式为
D.工作过程中,正极区溶液的 减小
13.(2024·四川眉山·二模)图1是一种居家天然气报警器成品装置,其工作原理如图2所示,其中 可
以在固体电解质ZnO —Na O中移动。当空间内甲烷达到一定浓度时,传感器随之产生电信号并联动报警。
2 2
当报警器触发工作时,下列说法不正确的是
A.电极a的电势比电极b高
B. 在电解质中向电极a移动
C.电极a上发生的电极反应为:D.当电极a消耗 时,电路中有0.8mol电子转移
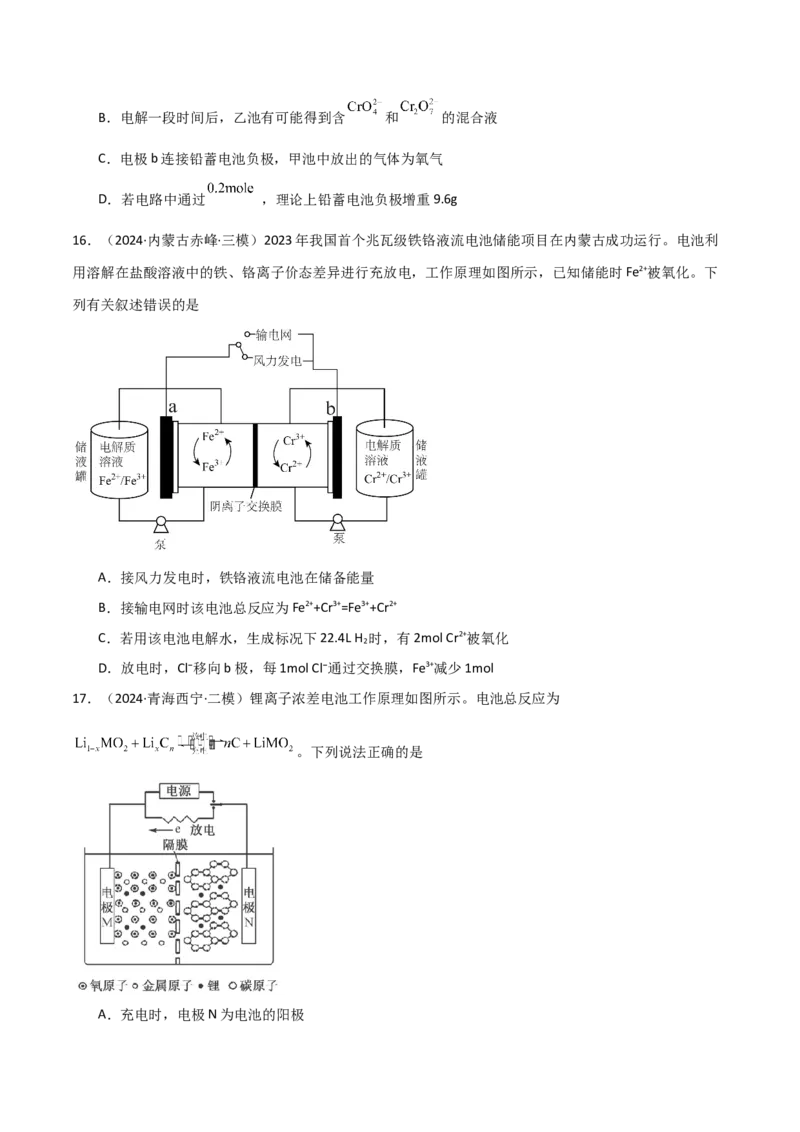
14.(2024·重庆·一模)利用丙酮酸与废水中的 电催化耦合,可在温和条件下去除 并生产丙氨酸,
其工作原理如图。 ,丙氨酸主要以 形式存在于溶液中。下列说法错误的是
A.电极 连接电源的正极
B.阴极的电极反应有:
C.反应一段时间后,阴极区溶液的 基本不变
D. 极区生成 丙氨酸时, 极区至少生成了
15.(2024·广西·二模)铬酸钠( )主要用于有机合成氧化剂、印染剂等。现以铅蓄电池为电源,
用电渗析法分离回收混合物浆液中的 的装置如图所示,下列对分离过程的相关判断错误的是
A.铅蓄电池的正极反应为:B.电解一段时间后,乙池有可能得到含 和 的混合液
C.电极b连接铅蓄电池负极,甲池中放出的气体为氧气
D.若电路中通过 ,理论上铅蓄电池负极增重9.6g
16.(2024·内蒙古赤峰·三模)2023年我国首个兆瓦级铁铬液流电池储能项目在内蒙古成功运行。电池利
用溶解在盐酸溶液中的铁、铬离子价态差异进行充放电,工作原理如图所示,已知储能时Fe2+被氧化。下
列有关叙述错误的是
A.接风力发电时,铁铬液流电池在储备能量
B.接输电网时该电池总反应为Fe2++Cr3+=Fe3++Cr2+
C.若用该电池电解水,生成标况下22.4L H 时,有2mol Cr2+被氧化
2
D.放电时,Cl⁻移向b极,每1mol Cl⁻通过交换膜,Fe3+减少1mol
17.(2024·青海西宁·二模)锂离子浓差电池工作原理如图所示。电池总反应为
。下列说法正确的是
A.充电时,电极N为电池的阳极B.该电池隔膜为阴离子交换膜
C.放电时,负极电极反应式为
D.放电时,若导线有4 电子通过,则正极质量增加14g
18.(2024·广西·二模)海水电池在海洋能源领域应用广泛,铁、镁、钠、锂都可以作为海水电池的电极
材料,其工作原理如图所示。下列说法错误的是
A.该装置不能将化学能完全转化为电能
B.海水中盐分大,可作为电解质溶液
C.钠、锂等活泼金属作B极,要防止其与海水直接接触
D.若铁为B极材料,则正极反应式一定为
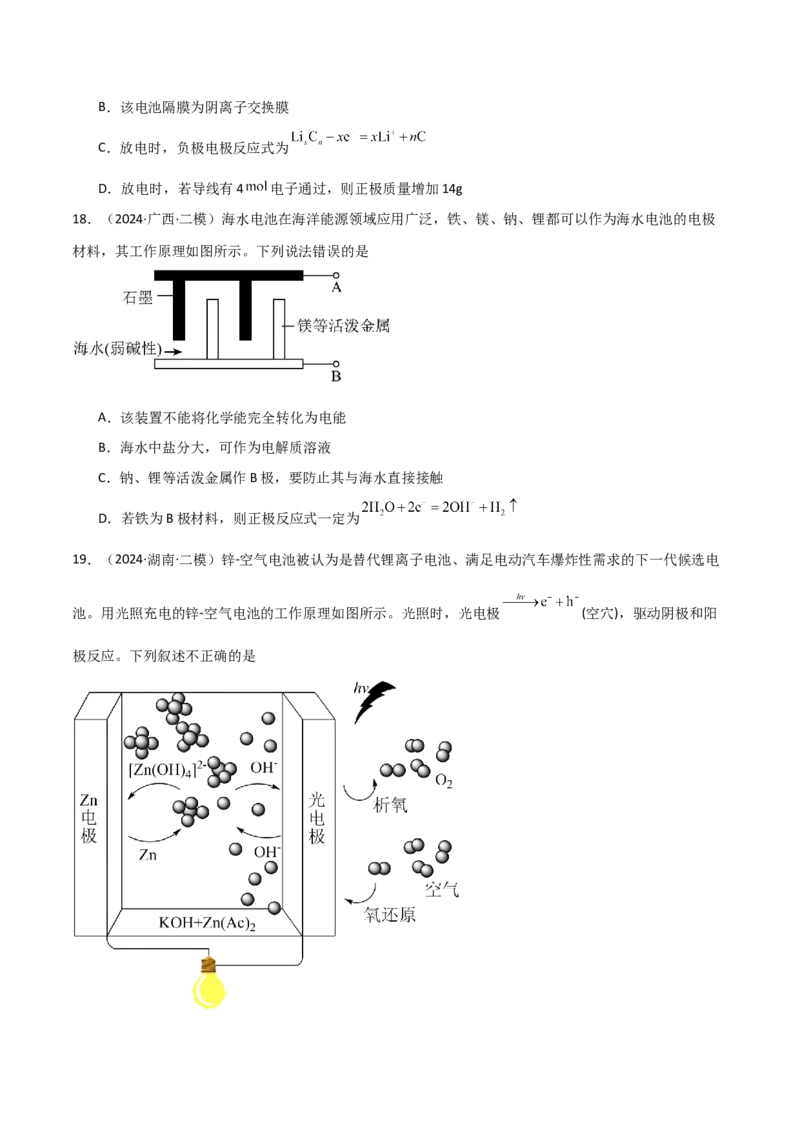
19.(2024·湖南·二模)锌-空气电池被认为是替代锂离子电池、满足电动汽车爆炸性需求的下一代候选电
池。用光照充电的锌-空气电池的工作原理如图所示。光照时,光电极 (空穴),驱动阴极和阳
极反应。下列叙述不正确的是A.放电时, 向光电极迁移 B.充电时的阳极反应为
C.放电时,光电子经电解液向 极移动D. 是配离子,配位数是4
20.(2024·青海海东·二模)某大学研究团队推出一种新型Zn-NO 电池。该电池能有效地捕获NO ,将其
2 2
转化为 ,再将产生的 电解制氨,过程如图所示。下列说法正确的是
A.d电极的电势比c电极的电势高
B.Zn极为原电池正极
C.c极的电极反应为 -6e-+7H+=NH +2H O
3 2
D.电路中转移0.2mole-时,理论上能得到1.12LO
2
21.(2024·四川成都·二模)自由基因为化学性质不稳定往往不能稳定存在,羟基自由基(·OH)有极强的氧
化性,其氧化性仅次于氟单质。我国科学家设计的一种能将苯酚(C H O)氧化为CO 和H O的原电池—电解
6 6 2 2
池组合装置如图所示,该装置能实现发电、环保二位一体。下列说法错误的是
A.该装置工作时,电流方向为电极b→Ⅲ室→Ⅱ室→Ⅰ室→电极a→电极b
B.当电极a上有1molCr(OH) 生成时,c极区溶液仍为中性
3
C.电极d的电极反应为H O–e-=H++·OH
2
D.当电极b上有0.3molCO 生成时,电极c、d两极共产生气体11.2L(标准状况)
222.(2024·山东济南·一模)我国科学家发现,利用如下装置可以将邻苯二醌类物质转化为邻苯二酚类物
质,已知双极膜(膜a、膜b)中间层中的H O可解离为H+和OH-。下列说法错误的是
2
A.电极电势:M