文档内容
易错点 14 元素周期表和元素周期律
易错题【01】元素周期表的结构
①基态原子最外层电子排布相同的原子对应元素不一定处于同主族,如He、Be的最外层
均有2个电子,前者处于0族,后者处于第IIA族。
②第IA族和0族不是含元素种类最多的族,应是第ⅢB族,共有32种元素。
③第VIII族属于副族,但表示时仍表示“VIII族”;过渡元素包括8个副族,全部是金属
元素,原子最外层电子数不超过2个。
易错题【02】周期表的分区
分区 价层电子排布
s区 ns1~2
p区 ns2np1~6(除He外)
d区 (n-1)d1~9ns1~2(除钯外)
ds区 (n-1)d10ns1~2
f区 (n-2)f0~14(n-1)d0~2ns2
易错题【03】电离能和电负性
(1)电离能:同周期从左到右,第一电离能呈增大的趋势,稀有气体的第一电离能最大,
碱金属的第一电离能最小;同主族从上到下,第一电离能逐渐减小。
①判断元素金属性的强弱:第一电离能越小,金属越容易失去电子,金属性越强;反之越
弱。
②判断元素的化合价(I、I……表示各级电离能):如果某元素的I I,则该元素的常见
1 2 n+1 n
化合价为+n。例如,钠元素的I I,故钠元素的化合价为+1。
2 1 ≫
③判断核外电子的分层排布情况:多电子原子中,元素的各级电离能逐级增大,有一定的
≫
规律性。当电离能的变化出现突变时,电子层数就可能发生变化。
④第二、三、四周期中,第IIA族、第VA族元素的第一电离能比相邻主族元素都大。
(2)电负性:一般来说,同周期元素从左至右,元素的电负性逐渐变大;同族元素从上至
下,元素的电负性逐渐变小。金属元素的电负性一般小于1.8,非金属元素的电负性一般大
于1.8,而位于非金属三角区边界的“类金属”(如锗、锑等)的电负性则在1.8左右,它们
既有金属性又有非金属性。
易错题【04】元素金属性(非金属性)相对强弱的判断规律
元素的性质 本质 判断的一般依据
元素的原子失电子的能 与水或酸(非氧化性)反应置换出氢的难易力(与失电子的数目无 最高价氧化物对应水化物的碱性强弱
关),原子越容易失去
水溶液中单质间的置换反应
电子,元素金属性越
强;反之则弱 原电池中的正负极(Mg—Al---NaOH溶液例
元素金属性
外)
阳离子在电解池中阴极上的放电顺序
元素的原子得电子的能 与氢气化合的难易
力(与得电子的数目无
气态氢化物的稳定性
关),原子越容易得到
电子,元素非金属性越 最高价氧化物对应水化物的酸性强弱
元素的非金属性
强;反之则弱。
水溶液中单质间的置换反应(单质作氧化
剂)
阴离子的还原性
易错题【05】微粒半径大小比较中的规律
同周期 随原子序数递增,原子半径减小。如:r(Na)>r( Mg)>r(Al)>r
M
(Si)>r(P)>r(S)>r(Cl)
随原子序数递增,原子或离子半径减小。如:r(Li)<r(Na)<r(k)<r
(Rb)<r(Cs),r(Li+)<r(Na+)<r(k+)<r(Rb+)<r(Cs+),r(F
同主族
—)<r(Cl—)<r(Br—)<r(I—)
同电子层 核电荷数越大,离子半径越小。如:r(O2—)>r(F—)>r(Na+)>r
(Mg2+)>r(Al3+)
同元素 阴离子大于原子,原子大于阳离子,低价阳离子大于高价阳离子。如:r(Cl-)
>r(Cl),r(Fe)>r(Fe2+)>r(Fe3+)
易错题【06】元素周期表中“位-构-性”的关系
典例分析
例题1、元素X、Y、Z、Q、R的原子序数依次增大且小于20,其原子半径和最外层电子
数之间的关系如图所示。下列判断正确的是( )A. X的电负性比Q的大
B. Q的简单离子半径比R的大
C. Z的简单气态氢化物的热稳定性比Q的强
D. Y的最高价氧化物对应的水化物的碱性比R的强
B【解析】X、Y、Z、Q、R的原子序数依次增大且小于20,由图像中最外层电子数和原
子半径的关系可知,X为C、Y为Na、Z为S、Q为Cl、R为K。C的电负性比Cl的小,A
错误;核外电子数相同时质子数越大半径越小,故Q的简单离子半径比R的大,B正确;
同周期元素的原子序数越大,元素的非金属性越强,则简单氢化物更稳定,则Z的简单气
态氢化物的热稳定性比Q的弱,C错误;同主族元素的原子序数越大,金属性越强,则最
高价氧化物对应水化物的碱性越强,则Y的最高价氧化物对应的水化物的碱性比R的弱,
D错误。
例题2、四种短周期元素在周期表中的相对位置如下表所示,其中Y的简单氢化物的水溶
液呈碱性,下列说法正确的是( )
A.元素W位于第三周期第ⅤA族 X Y
B.非金属性:X>Y Z W
C.最高价氧化物对应水化物的酸性:Z>W
D.Z的最高化合价为+5价
D 【解析】由四种元素的相对位置可知,X、Y处于第二周期,Z、W处于第三周期。Y的
简单氢化物的水溶液呈碱性,该溶液是氨水,Y是N,结合四种元素在周期表中的相对位
置关系推知,X、Z、W分别为C、P、S元素。W(S)位于第三周期第VIA族,A错误;
同周期主族元素,从左到右元素的非金属性逐渐增强,则非金属性:C<N,B错误;元素
的非金属性:P<S,则最高价氧化物对应水化物的酸性:HPO <HSO ,C错误;Z是P
3 4 2 4
元素,处于第VA族,最高化合价为+5,D正确。
例题3、一种麻醉剂的分子结构式如图所示。其中,X的原子核只有1个质子;元素Y、
Z、W原子序数依次增大,且均位于X的下一周期;元素E的原子比W原子多8个电子。下列说法不正确的是( )
A. XEZ 是一种强酸 B. 非金属性:W>Z>Y
4
C. 原子半径:Y>W>E D. ZW 中,Z的化合价为+2价
2
C【解析】X的原子核只有1个质子,则X为H元素;题给化合物结构中X、W、E均形成
1个共价键、Y形成4个共价键、Z形成2个共价键。元素Y、Z、W原子序数依次增大,
且均位于X的下一周期,即第二周期元素,则Y为C元素,Z为O元素,W为F元素;元
素E的原子比W原子多8个电子,则E为Cl元素。氯元素非金属性较强,其最高价氧化
物的水化物HClO 是一种强酸,A正确;同一周期元素从左到右非金属性逐渐增强,则非
4
金属性:F>O>C,B正确; 同一周期从左到右原子半径逐渐减小,同一主族从上到下原子
半径逐渐增大,电子层越多半径越大,则原子半径:Cl>C>F,C错误; OF 中,F为-1
2
价,则O的化合价为+2价,D正确。
例题4、以下是A、B、C、D、E五种短周期元素的某些性质:下列判断正确的是
序号 A B C D E
最低负化合价 -4 -2 -1 -2 -1
电负性 2.5 2.5 3.0 3.5 4.0
A.C、D、E的气态氢化物的稳定性顺序为
B.元素A的最高能级轨道中无自旋方向相同的电子
C.与元素B处于同周期且在该周期中第一电离能最小的元素的单质能与 发生置换反
应
D.元素A、C不可能形成化合物
C【解析】由最低化合价知,B和D为第ⅥA族元素,C和E为第VⅡA族元素,同主族元
素,由上到下,电负性逐渐减小,故B是硫元素,D是氧元素;故C是氯元素,E是氟元
素;A为第ⅣA族元素,同周期元素,从左到右,电负性逐渐增大,故A不是硅、而是碳
元素。A.非金属性: 所以三者简单氢化物的稳定性: ,A项错
误;
B.碳原子最高能级轨道即2p轨道中有2个自旋状态相同的电子,B项错误;
C. 与元素S同周期且在该周期中第一电离能最小的元素的单质为Na,它能与HO发生
2
置换反应,C项正确;
D. 元素C、Cl之间可以形成化合物,如CCl 等,D项错误。
4
1.(2022·江苏·高考真题)工业上电解熔融 和冰晶石 的混合物可制得铝。
下列说法正确的是
A.半径大小: B.电负性大小:
C.电离能大小: D.碱性强弱:
2.(2022·海南·高考真题)短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同
周期并相邻,Y是组成水的元素之一,Z在同周期主族元素中金属性最强,W原子在同周
期主族元素中原子半径最小,下列判断正确的是
A. 是非极性分子
B.简单氢化物沸点:
C.Y与Z形成的化合物是离子化合物
D.X、Y、Z三种元素组成的化合物水溶液呈酸性
3.(2022·辽宁·高考真题)下列类比或推理合理的是
已知 方法 结论
A 沸点: 类比 沸点:
B 酸性: 类比 酸性:
C 金属性: 推理 氧化性:
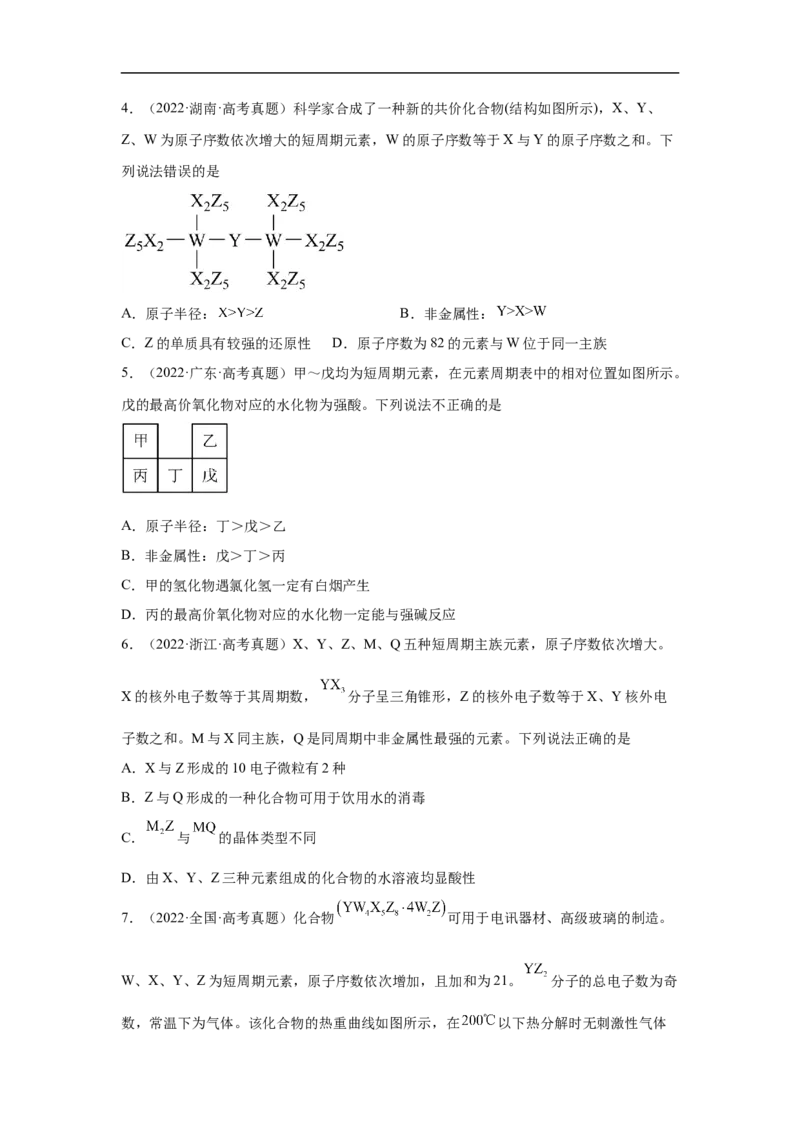
D : 推理 溶解度:4.(2022·湖南·高考真题)科学家合成了一种新的共价化合物(结构如图所示),X、Y、
Z、W为原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和。下
列说法错误的是
A.原子半径: B.非金属性:
C.Z的单质具有较强的还原性 D.原子序数为82的元素与W位于同一主族
5.(2022·广东·高考真题)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。
戊的最高价氧化物对应的水化物为强酸。下列说法不正确的是
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
6.(2022·浙江·高考真题)X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。
X的核外电子数等于其周期数, 分子呈三角锥形,Z的核外电子数等于X、Y核外电
子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是
A.X与Z形成的10电子微粒有2种
B.Z与Q形成的一种化合物可用于饮用水的消毒
C. 与 的晶体类型不同
D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性
7.(2022·全国·高考真题)化合物 可用于电讯器材、高级玻璃的制造。
W、X、Y、Z为短周期元素,原子序数依次增加,且加和为21。 分子的总电子数为奇
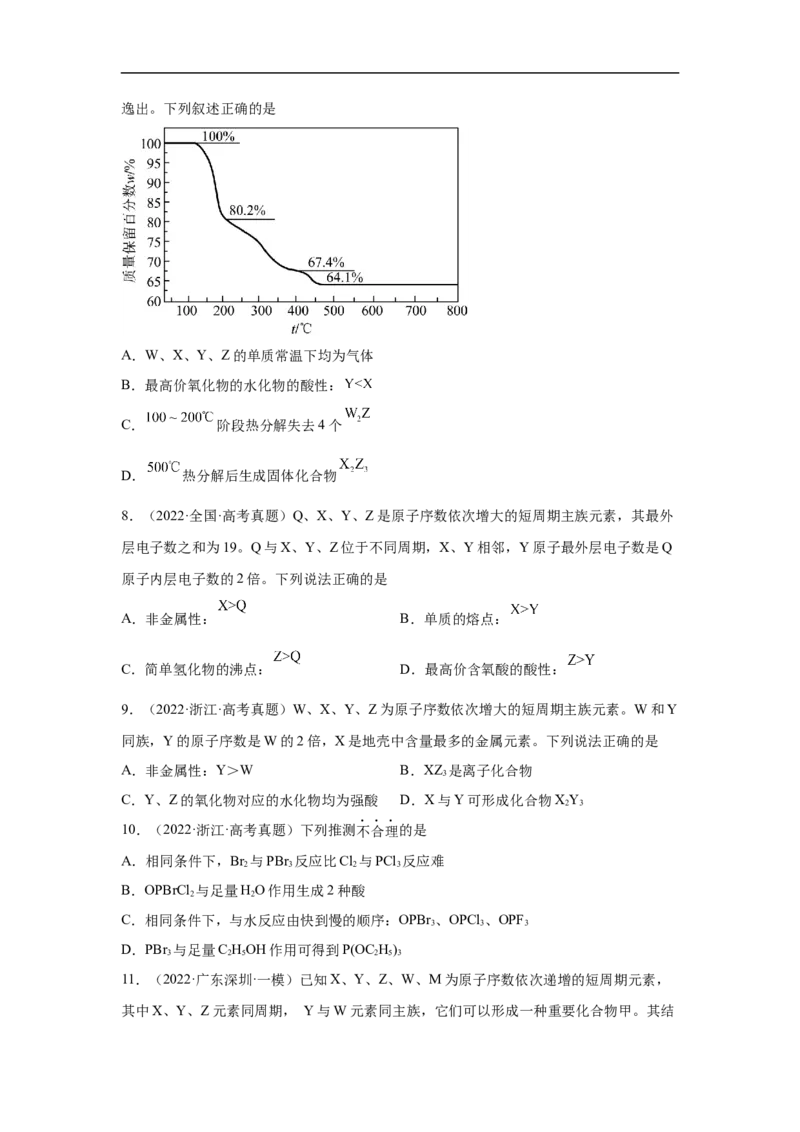
数,常温下为气体。该化合物的热重曲线如图所示,在 以下热分解时无刺激性气体逸出。下列叙述正确的是
A.W、X、Y、Z的单质常温下均为气体
B.最高价氧化物的水化物的酸性:
C. 阶段热分解失去4个
D. 热分解后生成固体化合物
8.(2022·全国·高考真题)Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外
层电子数之和为19。Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q
原子内层电子数的2倍。下列说法正确的是
A.非金属性: B.单质的熔点:
C.简单氢化物的沸点: D.最高价含氧酸的酸性:
9.(2022·浙江·高考真题)W、X、Y、Z为原子序数依次增大的短周期主族元素。W和Y
同族,Y的原子序数是W的2倍,X是地壳中含量最多的金属元素。下列说法正确的是
A.非金属性:Y>W B.XZ 是离子化合物
3
C.Y、Z的氧化物对应的水化物均为强酸 D.X与Y可形成化合物XY
2 3
10.(2022·浙江·高考真题)下列推测不合理的是
A.相同条件下,Br 与PBr 反应比Cl 与PCl 反应难
2 3 2 3
B.OPBrCl 与足量HO作用生成2种酸
2 2
C.相同条件下,与水反应由快到慢的顺序:OPBr 、OPCl 、OPF
3 3 3
D.PBr 与足量C HOH作用可得到P(OC H)
3 2 5 2 5 3
11.(2022·广东深圳·一模)已知X、Y、Z、W、M为原子序数依次递增的短周期元素,
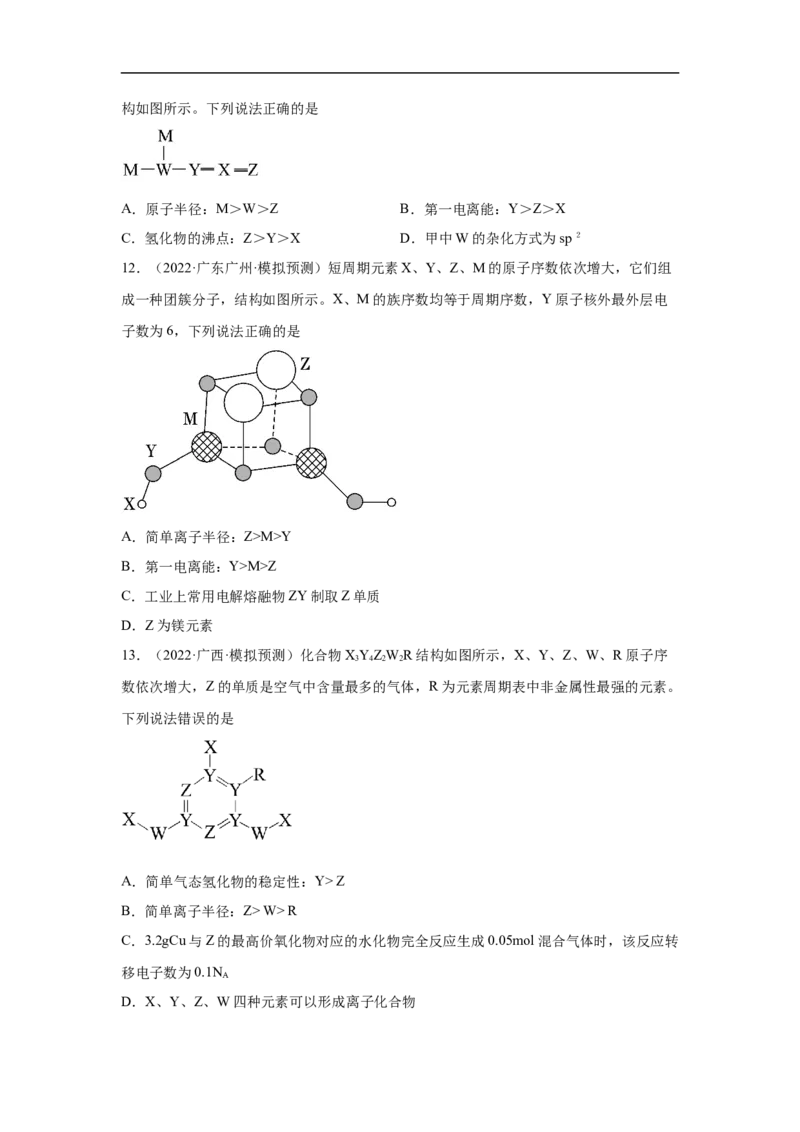
其中X、Y、Z元素同周期, Y与W元素同主族,它们可以形成一种重要化合物甲。其结构如图所示。下列说法正确的是
A.原子半径:M>W>Z B.第一电离能:Y>Z>X
C.氢化物的沸点:Z>Y>X D.甲中W的杂化方式为sp2
12.(2022·广东广州·模拟预测)短周期元素X、Y、Z、M的原子序数依次增大,它们组
成一种团簇分子,结构如图所示。X、M的族序数均等于周期序数,Y原子核外最外层电
子数为6,下列说法正确的是
A.简单离子半径:Z>M>Y
B.第一电离能:Y>M>Z
C.工业上常用电解熔融物ZY制取Z单质
D.Z为镁元素
13.(2022·广西·模拟预测)化合物XYZWR结构如图所示,X、Y、Z、W、R原子序
3 4 2 2
数依次增大,Z的单质是空气中含量最多的气体,R为元素周期表中非金属性最强的元素。
下列说法错误的是
A.简单气态氢化物的稳定性:Y> Z
B.简单离子半径:Z> W> R
C.3.2gCu与Z的最高价氧化物对应的水化物完全反应生成0.05mol混合气体时,该反应转
移电子数为0.1N
A
D.X、Y、Z、W四种元素可以形成离子化合物14.(2022·湖北·襄阳五中模拟预测)在通常条件下,下列各组物质的性质排列错误的是
A.密度:
B.沸点:
C.熔点:
D.水溶性:
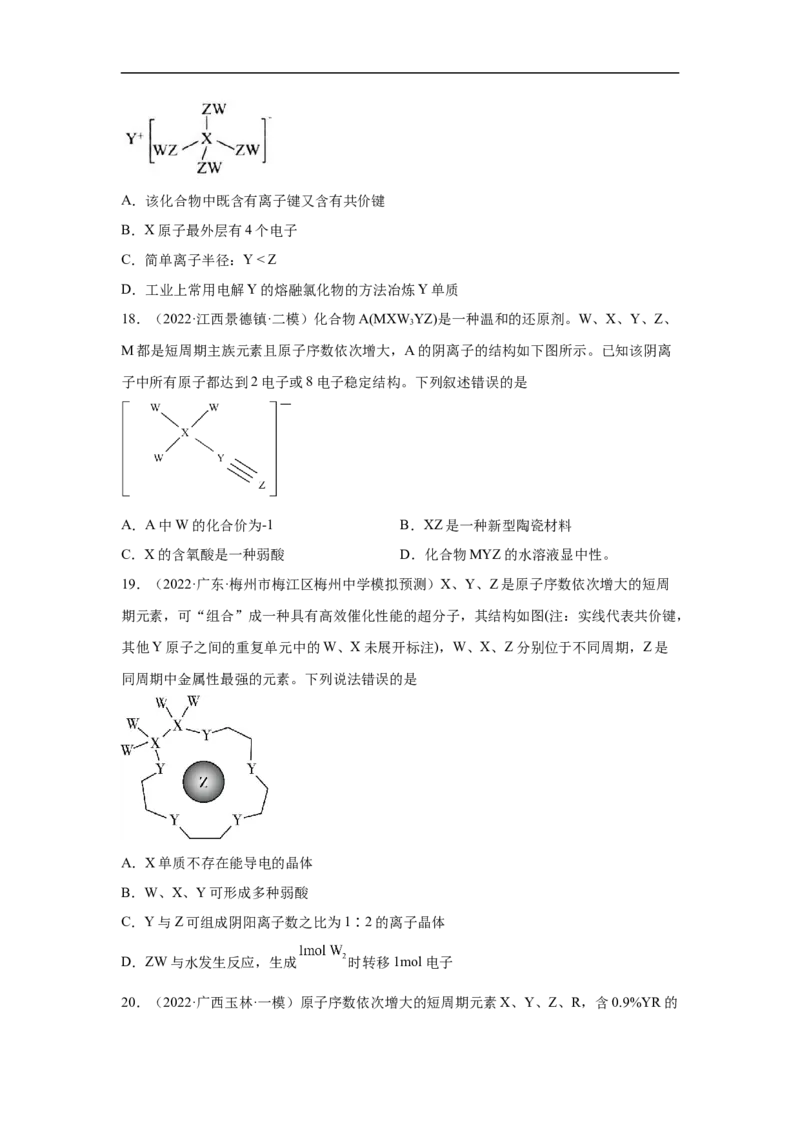
15.(2022·内蒙古包头·一模)如图所示的两种化合物可应用于阻燃材料和生物材料的合
成。其中W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y的原子序数
为W原子价电子数的3倍。下列说法错误的是
A.四种元素中,Y原子半径最大,X原子半径最小
B.W、Z和氢三种元素可形成含有共价键的离子化合物
C.W、X、Z氢化物沸点一定是:X>W>Z
D.Y、Z形成的一种二元化合物与水反应生成两种酸
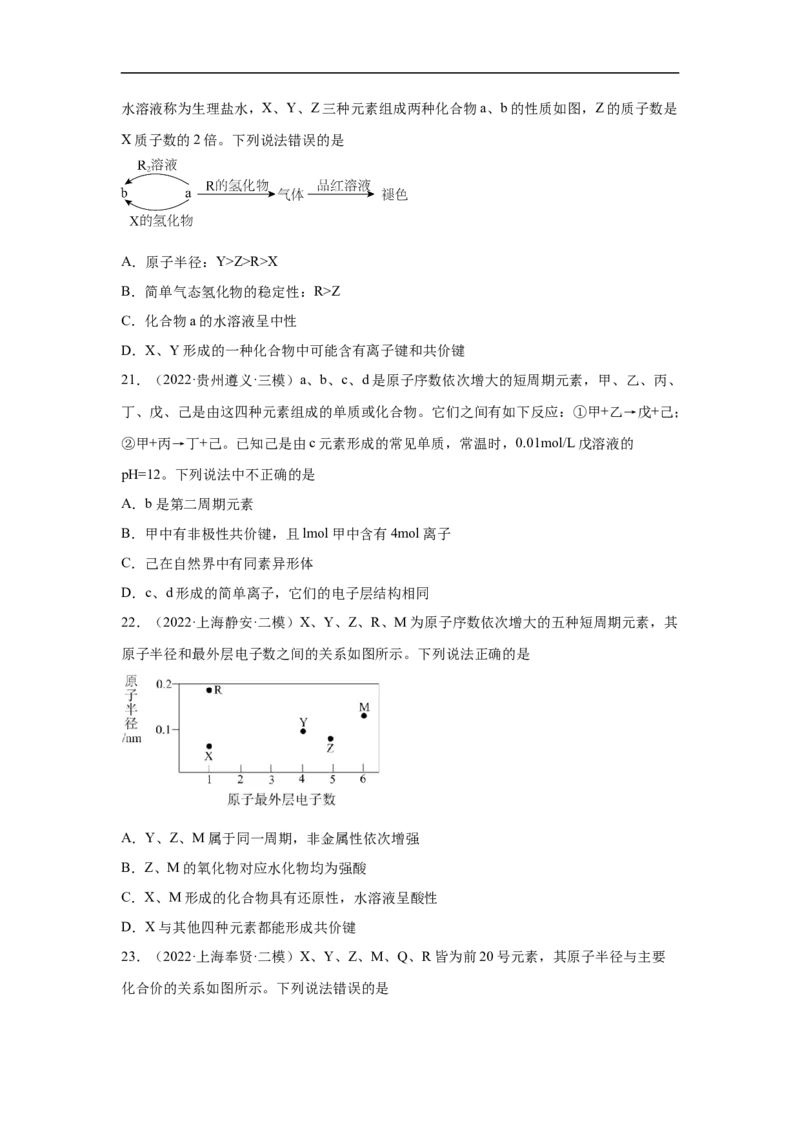
16.(2022·四川乐山·一模)X、Y、Z、W四种短周期元素在周期表中的位置如图所示,
元素Z的核电荷数是元素Y的两倍,下列有关说法不正确的是
X Y
Z W
A.原子半径:X> Y
B.简单阴离子还原性:Z> W
C.元素X、Y的单质在放电条件下生成红棕色气体
D.四种元素的简单氢化物中,Y的氢化物沸点最高
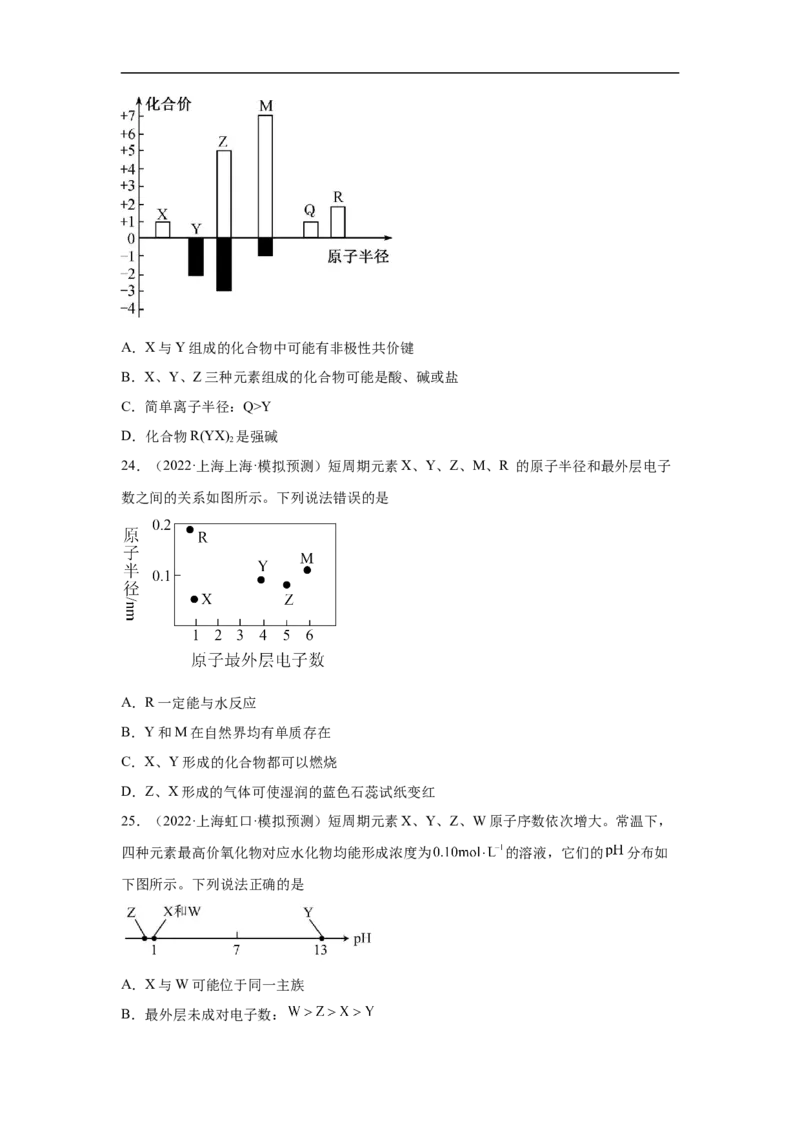
17.(2022·内蒙古·海拉尔第二中学模拟预测)W、X、Y、Z为原子序数依次增大的四种
短周期主族元素,由上述四种元素组成的某种化合物的结构简式如图所示。下列说法错误
的是A.该化合物中既含有离子键又含有共价键
B.X原子最外层有4个电子
C.简单离子半径:Y < Z
D.工业上常用电解Y的熔融氯化物的方法冶炼Y单质
18.(2022·江西景德镇·二模)化合物A(MXW YZ)是一种温和的还原剂。W、X、Y、Z、
3
M都是短周期主族元素且原子序数依次增大,A的阴离子的结构如下图所示。已知该阴离
子中所有原子都达到2电子或8电子稳定结构。下列叙述错误的是
A.A中W的化合价为-1 B.XZ是一种新型陶瓷材料
C.X的含氧酸是一种弱酸 D.化合物MYZ的水溶液显中性。
19.(2022·广东·梅州市梅江区梅州中学模拟预测)X、Y、Z是原子序数依次增大的短周
期元素,可“组合”成一种具有高效催化性能的超分子,其结构如图(注:实线代表共价键,
其他Y原子之间的重复单元中的W、X未展开标注),W、X、Z分别位于不同周期,Z是
同周期中金属性最强的元素。下列说法错误的是
A.X单质不存在能导电的晶体
B.W、X、Y可形成多种弱酸
C.Y与Z可组成阴阳离子数之比为1∶2的离子晶体
D.ZW与水发生反应,生成 时转移1mol电子
20.(2022·广西玉林·一模)原子序数依次增大的短周期元素X、Y、Z、R,含0.9%YR的水溶液称为生理盐水,X、Y、Z三种元素组成两种化合物a、b的性质如图,Z的质子数是
X质子数的2倍。下列说法错误的是
A.原子半径:Y>Z>R>X
B.简单气态氢化物的稳定性:R>Z
C.化合物a的水溶液呈中性
D.X、Y形成的一种化合物中可能含有离子键和共价键
21.(2022·贵州遵义·三模)a、b、c、d是原子序数依次增大的短周期元素,甲、乙、丙、
丁、戊、己是由这四种元素组成的单质或化合物。它们之间有如下反应:①甲+乙→戊+己;
②甲+丙→丁+己。已知己是由c元素形成的常见单质,常温时,0.01mol/L戊溶液的
pH=12。下列说法中不正确的是
A.b是第二周期元素
B.甲中有非极性共价键,且lmol甲中含有4mol离子
C.己在自然界中有同素异形体
D.c、d形成的简单离子,它们的电子层结构相同
22.(2022·上海静安·二模)X、Y、Z、R、M为原子序数依次增大的五种短周期元素,其
原子半径和最外层电子数之间的关系如图所示。下列说法正确的是
A.Y、Z、M属于同一周期,非金属性依次增强
B.Z、M的氧化物对应水化物均为强酸
C.X、M形成的化合物具有还原性,水溶液呈酸性
D.X与其他四种元素都能形成共价键
23.(2022·上海奉贤·二模)X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要
化合价的关系如图所示。下列说法错误的是A.X与Y组成的化合物中可能有非极性共价键
B.X、Y、Z三种元素组成的化合物可能是酸、碱或盐
C.简单离子半径:Q>Y
D.化合物R(YX) 是强碱
2
24.(2022·上海上海·模拟预测)短周期元素X、Y、Z、M、R 的原子半径和最外层电子
数之间的关系如图所示。下列说法错误的是
A.R一定能与水反应
B.Y和M在自然界均有单质存在
C.X、Y形成的化合物都可以燃烧
D.Z、X形成的气体可使湿润的蓝色石蕊试纸变红
25.(2022·上海虹口·模拟预测)短周期元素X、Y、Z、W原子序数依次增大。常温下,
四种元素最高价氧化物对应水化物均能形成浓度为 的溶液,它们的 分布如
下图所示。下列说法正确的是
A.X与W可能位于同一主族
B.最外层未成对电子数:C.四种元素的简单离子中Y的半径最小
D.四种元素的最高价氧化物对应水化物中Z的酸性最强
参考答案
1.A【详解】A.核外电子数相同时,核电荷数越大半径越小,故半径大小为
,故A正确;
B.同周期元素核电荷数越大电负性越大,故 ,故B错误;
C.同周期从左往右第一电离能呈增大趋势,同主族从上往下第一电离能呈减小趋势,故
电离能大小为 ,故C错误;
D.元素金属性越强,其最高价氧化物对应水化物的碱性越强,故碱性强弱为
,故D错误;
故选A。
2.C【详解】X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y同周期并相邻,
且Y是组成水的元素之一,则Y为O元素,X为N元素,Z在同周期主族元素中金属性最
强,则Z为Na元素,W原子在同周期主族元素中原子半径最小,则W为Cl元素,据此分
析解答。
A.由分析,X为N元素,W为Cl元素,NCl 分子的空间构型为三角锥形,其正负电荷的
3
中心不重合,属于极性分子,A错误;
B.HO和NH 均含有氢键,但HO分子形成的氢键更多,故沸点HO>NH ,B错误;
2 3 2 2 3
C.Y为O元素,Z为Na元素,两者形成的化合物为NaO、NaO 均为离子化合物,C正
2 2 2
确;
D.N、O、Na三种元素组成的化合物NaNO 呈中性、NaNO 呈碱性,D错误;
3 2
答案选C。
3.A【详解】A. 、 、 的相对分子质量逐渐增大,沸点逐渐升高,可推知分子晶
体的相对分子质量越大,分子间作用力越大,沸点越高,由于相对分子质量:,所以沸点: ,故A正确;
B.非金属元素最高价含氧酸的酸性与非金属性有关,元素的非金属性越强,最高价含氧
酸的酸性越强,所以酸性: ,酸性: ,故B错误;
C.由金属性: ,可推出氧化性 ;由离子方程式 可
得,氧化性: ,故C错误;
D. 和 的阴、阳离子个数比不相同,不能通过 大小来比较二者在水中的
溶解度,故D错误;
选A。
4.C【详解】由共价化合物的结构可知,X、W形成4个共价键,Y形成2个共价键,Z
形成1个共价键,X、Y、Z、W是原子序数依次增大的短周期元素,W的原子序数等于X
与Y的原子序数之和,则X为C元素、Y为O元素、Z为F元素、W为Si元素。
A.同周期元素,从左到右原子半径依次减小,则C、O、F的原子半径大小顺序为C>O
>F,故A正确;
B.同周期元素,从左到右元素的非金属性依次增强,同主族元素,从上到下元素的非金
属性依次减弱,则C、O、Si的非金属性强弱顺序为O>C>Si,故B正确;
C.位于元素周期表右上角的氟元素的非金属性最强,单质具有很强的氧化性,故C错误;
D.原子序数为82的元素为铅元素,与硅元素都位于元素周期表ⅣA族,故D正确;
故选C。
5.C【详解】甲~戊是短周期元素,戊中的最高价氧化物对应水化物为强酸,则可能是硫
酸或高氯酸,若是高氯酸,则戊为Cl,甲为N、乙为F、丙为P、丁为S,若是硫酸,则戊
为S,甲为C、乙为O、丙为Si、丁为P。
A.根据层多径大,同电子层结构核多径小原则,则原子半径:丁>戊>乙,故A正确;
B.根据同周期从左到右非金属性逐渐增强,则非金属性:戊>丁>丙,故B正确;
C.甲的氢化物可能为氨气,可能为甲烷、乙烷等,若是氨气,则遇氯化氢一定有白烟产
生;若是甲烷、乙烷等,则遇氯化氢不反应,没有白烟生成,故C错误;
D.丙的最高价氧化物对应的水化物可能是硅酸、也可能是磷酸,都一定能与强碱反应,
故D正确。综上所述,答案为C。
6.B【详解】X的核外电子数等于其周期数,X为H,YX 分子呈三角锥形,Y为N,Z的
3
核外电子数等于X、Y核外电子数之和,则Z为O,M与X同主族,则M为Na,Q是同周
期中非金属性最强的元素,则Q为Cl,综合分析,X为H,Y为N,Z为O,M为Na,Q
为Cl,以此解题。
A.由分析可知X为H,Z为O,则其形成的10电子微粒有HO、OH-、HO+,A错误;
2 3
B.由分析可知Z为O,Q为Cl,可形成ClO ,有氧化性,可用于自来水消毒,B正确;
2
C.由分析可知Z为O,M为Na,Q为Cl,则MZ为NaO,为离子晶体,MQ为NaCl,
2 2
为离子晶体,晶体类型相同,C错误;
D.由分析可知X为H,Y为N,Z为O,这三种元素可以形成NH₃·H₂O,其溶液显碱性,
D错误;
故选B。
7.D【详解】化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z
4 5 8 2
为短周期元素,原子序数依次增加,且加和为21。该化合物的热重曲线如图所示,在
200℃以下热分解时无刺激性气体逸出,则说明失去的是水,即W为H,Z为O,YZ 分子
2
的总电子数为奇数,常温下为气体,则Y为N,原子序数依次增加,且加和为21,则X为
B。
【详解】A.X(B)的单质常温下为固体,故A错误;
B.根据非金属性越强,其最高价氧化物的水化物酸性越强,则最高价氧化物的水化物酸
性:X(H BO)<Y(HNO ),故B错误;
3 3 3
C.根据前面已知200℃以下热分解时无刺激性气体逸出,则说明失去的是水,若100~
200℃阶段热分解失去4个HO,则质量分数 ,
2
则说明不是失去4个HO,故C错误;
2
D.化合物(NH B O·4H O)在500℃热分解后若生成固体化合物XZ(B O),根据硼元素守
4 5 8 2 2 3 2 3
恒,则得到关系式2NH B O·4H O~5B O,则固体化合物B O 质量分数为
4 5 8 2 2 3 2 3
,说明假设正确,故D正确。
综上所述,答案为D。8.D【详解】Q、X、Y、Z为原子序数依次增大的短周期主族元素,Q与X、Y、Z不在同
一周期,Y原子最外层电子数为Q原子内层电子数的2倍,则Q应为第二周期元素,X、
Y、Z位于第三周期,Y的最外层电子数为4,则Y为Si元素,X、Y相邻,且X的原子序
数小于Y,则X为Al元素,Q、X、Y、Z的最外层电子数之和为19,则Q、Z的最外层电
子数之和为19-3-4=12,主族元素的最外层电子数最多为7,若Q的最外层电子数为7,为
F元素,Z的最外层电子数为5,为P元素,若Q的最外层电子数为6,为O元素,则Z的
最外层电子数为6,为S元素,若Q的最外层电子数为5,为N元素,Z的最外层电子数为
7,为Cl元素;综上所述,Q为N或O或F,X为Al,Y为Si,Z为Cl或S或P,据此分
析解题。
A.X为Al,Q为N或O或F,同一周期从左往右元素非金属性依次增强,同一主族从上
往下依次减弱,故非金属性:Q>X,A错误;
B.由分析可知,X为Al属于金属晶体,Y为Si属于原子晶体或共价晶体,故单质熔点
Si>Al,即Y>X,B错误;
C.含有氢键的物质沸点升高,由分析可知Q为N或O或F,其简单氢化物为HO或NH
2 3
或HF,Z为Cl或S或P,其简单氢化物为HCl或HS或PH ,由于前者物质中存在分子间
2 3
氢键,而后者物质中不存在,故沸点Q>Z,C错误;
D.元素的非金属性越强,其最高价含氧酸的酸性越强,P、S、Cl的非金属性均强于Si,
因此最高价含氧酸酸性:Z>Y,D正确;
故答案为:D。
9.D【详解】X是地壳中含量最多的金属元素,X为Al元素,W和Y同族,Y的原子序
数是W的2倍,W为O元素,Y为S元素,Z为Cl元素,据此分析解题。
A.非金属性同主族从上至下逐渐减弱:Y<W,A错误;
B.氯化铝是共价化合物,B错误;
C.Y、Z的最高价氧化物对应的水化物分别硫酸和高氯酸,两者均为强酸,次氯酸也是氯
的氧化物对应的水化合物,但次氯酸为弱酸,C错误;
D.根据化合物的化合价代数和为0可知,铝与硫元素形成的化合物化学式为Al S,D正
2 3
确;
答案选D。
10.B【详解】A.氯原子半径较小,氯气更容易靠近三氯化磷中的磷原子发生反应生成五
氯化磷,A正确;B.OPBrCl 与HO反应的方程式为:OPBrCl +3H O=HPO +2HCl+HBr,一共生成3种酸,
2 2 2 2 3 4
B错误;
C.从P—Br键到P—F键,键的稳定性逐渐增强,在和水反应时越难断裂,反应速率越慢,
C正确;
D.PBr 与C HOH反应的时候,Br乙醇羟基上的氢原子结合,乙醇的其余部分和磷结合
3 2 5
生成P(OC H),D正确;
2 5 3
故选B。
11.B【详解】已知X、Y、Z、W、M为原子序数依次递增的短周期元素,其中X、Y、Z
元素同周期,X形成四个共价键,则X特征最外层有4个电子,X是C元素;Y形成3个
共价键,Y 原子最外层有5个电子,Y是N元素;Z形成2个共价键,则Z最外层有6个
电子,Y与W元素同主族,则W是P元素,M原子序数比P大,可形成1个共价键,则
M 最外层有7个电子,M是Cl元素,然后根据元素周期律及物质的性质分析解答。
根据上述分析可知:X是C,Y是N,Z是O,W是P,M是Cl元素。
A.同一周期主族元素从左到右原子半径逐渐减小,所以原子半径P>Cl,不同周期元素,
原子核外电子层数越多,原子半径越大,则原子半径大小关系为: W(P)>M(Cl)>Z(O),
A错误;
B.一般情况下同一周期元素的第一电离能随原子序数的增大而增强,但当元素处于第
ⅡA|diⅤA时,原子核外电子处于全满、半满的稳定状态,其第一电离能大于同一周期相
邻元素,由于N的2p轨道处于半满状态,较稳定,所以第一电离能:N>O>C,B正确;
C.碳的氢化物种类较多,物质分子中含有的C原子数目多少不同,物质沸点高低不同,
因此无法确定X、Y、Z三种元素的氢化物熔沸点高低,C错误;
D.W是P,P原子价层电子对数是3+ =4,元素甲中W的杂化方式为sp3杂化,D错
误;
故合理选项是B。
12.D【详解】短周期元素X、Y、Z、M的原子序数依次增大,X、M的族序数均等于周
期序数,Y原子核外最外层电子数为6,则X是H,M是Al,Y是O,根据团簇分子结构
发现Z的原子半径大于M,大于Y,所以Z元素应该和M同周期,再结合团簇分子发现,
H原子2个,O原子6个,Al原子2个,Z原子2个,根据化合物化合价总和推断出Z元素
是Mg。
A.电子层结构相同时,核电荷数越大半径越小,则简单离子半径:Y>Z>M,A错误;B.非金属元素第一电离能通常大于金属元素第一电离能,Mg最外层电子排布式为3s2全
满而稳定,第一电离能比Al大,即第一电离能Y>Z>M,B错误;
C.MgCl 熔点远低于MgO,为节约能耗用电解熔融MgCl 制取Mg单质,C错误;
2 2
D.据分析知,Z为镁元素,D正确;
故选D。
13.A【详解】R 为周期表中电负性最大的元素,则R为F元素;根据XYZWR 结构图
3 4 2 2
可知,X可形成1个共价键,Y可形成4个共价键,Z可形成3个共价键,W可形成2个共
价键,又因为X、Y、Z、W、R 原子序数依次增大,所以X为H元素,Y为C元素,Z为
N元素,W为O元素。
A.Y为C元素,Z为N元素,N的非金属性强于C,因此简单气态氢化物热稳定性:
Y O2-> F-,即Z>
W> R,选项B正确;
C.3.2gCu与Z的最高价氧化物对应的水化物HNO 完全反应生成0.05mol混合气体时,每
3
个铜原子失去2个电子,故该反应转移电子数为0.1N ,选项C正确;
A
D.X、Y、Z、W四种元素可以形成离子化合物NH NO 等,选项D正确;
4 3
答案选A。
14.B【详解】A. 钾的密度比钠的密度小,故A正确;
B. 的分子间氢键比氨气的分子间氢键多,故沸点: ,故B错误;
C. 饱和一卤代烃的熔沸点随着碳原子数的增多而增大,因此熔点大小顺序CHCHCHCl
3 2 2
>CHCHCl,故C正确;
3 2
D. 饱和一元醇的水溶性随着碳原子数的增多而减小,故水溶性是CHCHOH>
3 2
CHCHCHCHOH,故D正确;
3 2 2 2
答案选B。
15.C【详解】W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,XZ均形
成1个共价键,X、Z分别为氟、氯元素;W形成3个共价键,则为氮;Y的原子序数为W
原子价电子数的3倍,Y原子序数为15,是磷。
A.电子层数越多半径越大,电子层数相同时,核电荷数越大,半径越小;四种元素中,Y
原子半径最大,X原子半径最小,A正确;
B.W、Z和氢三种元素可形成含有共价键的离子化合物氯化铵,氯化铵为离子化合物且铵根离子中含有共价键,B正确;
C.W、X、Z氢化物中N可以形成NH 或NH,NH 沸点高于HF,C错误;
3 2 4 2 4
D.Y、Z形成的一种二元化合物PCl ,PCl 与水反应生成磷酸和盐酸两种酸,D正确;
3 3
故选C。
16.C【详解】由题干信息结合四种元素在周期表中的位置可知,元素Z的核电荷数是元
素Y的两倍,则Y是O,Z为S,X为N,W为Cl,据此分析解答。
A.X为N,Y是O,原子半径:N>O,故A错误;
B.Z的简单阴离子:S2-、W的简单阴离子:Cl-还原性:S2-> Cl-,故B正确;
C.元素X、Y的单质即氮气和氧气,在放电条件下生成一氧化氮,为无色气体,故C错
误;
D.四种元素的简单氢化物分别为:NH 、HO、HS、HCl,其中HO中存在氢键,沸点最
3 2 2 2
高,故D正确;
故答案选C。
17.B【详解】W、X、Y、Z为原子序数依次增大的四种短周期主族元素,由上述四种元
素组成的某种化合物的结构简式,结合元素的价键可推出W为H,X为B,Y为Na,Z为
S。
A.该化合物中既含有钠离子与[B(SH) ]-之间形成的离子键,又含有O与S之间形成的共价
4
键等,选项A正确;
B.X为B,原子最外层有3个电子,选项B错误;
C.简单离子半径:Na+ S>Cl>O,A正确;
B.Cl非金属性强于S,因此简单气态氢化物稳定性R>Z,B正确;
C.a为亚硫酸钠,其水解呈碱性,C错误;
D.O和Na可以形成NaO,其中含有离子键和共价键,D正确;
2 2
故答案选C。
21.B【详解】常温下,0.01mol/L戊溶液的pH=12说明戊为一元强碱,短周期中只有Na
可形成一元强碱,故戊为NaOH,甲能与乙、丙分别反应生成单质己,可推断甲为NaO,
2 2
乙为HO,丙为CO,丁为NaCO,则a、b、c、d分别为H、C、O、Na四种元素,据此
2 2 2 3
可分析解答。
A.碳元素是6号元素,位于第二周期IVA族,A选项正确;
B.NaO 中含有O-O非极性键,1mol Na O 中含有2molNa+和1molO 共3mol离子,B选
2 2 2 2
项错误;
C.O 在自然界中有同素异形体O,C选项正确;
2 3D.O、Na形成的简单离子核外电子数均为10,电子层结构相同,D选项正确;
答案选B。
22.C【详解】根据半径大小及最外层电子数可推断,X为H,Y为C,Z为N,R为Na,
M为S;
A.同周期元素随原子序数递增,原子半径递减(除去0族元素),M原子半径大于Z,说明
不是同周期元素,A错误;
B.Z为氮元素,其氧化物多种,且水化物也存在HNO 这类的弱酸,M为硫元素,其氧化
2
物有SO 、SO ,SO 的水化物HSO 是弱酸,B错误;
2 3 2 2 3
C.HS有强还原性,溶于水具有酸性,溶液称为氢硫酸,C正确;
2
D.H元素与Na元素的原子之间无法形成共价键,D错误;
综上,本题选C。
23.C【详解】X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系
如图所示,X为+1价,其原子半径最小,则X为H元素;Y只有-2价,则Y为O元素;M
存在-1和+7价,则M为Cl元素;Z存在+5和-3价,其原子半径大于O小于Cl,则Z为N
元素;Q化合价为+1,其原子半径大于Cl小于R,则Q为Na元素;R的化合价为+2,其
原子半径大于Na,则R为Ca元素,以此分析解答。
X为H元素、Y为O元素、Z为N元素,M为Cl元素,Q为Na元素,R为Ca元素。
A.H、O组成的过氧化氢分子中含有O-O非极性共价键,故A正确;
B.H、O、N形成的化合物有硝酸、硝酸铵、一水合氨等,组成的化合物可能是酸、碱或
盐,故B正确;
C.钠离子和氧离子的核外电子层结构相同,核电荷数越大离子半径越小,则简单离子半
径:Q<Y,故C错误;
D.R(YX) 为Ca(OH) ,Ca(OH) 属于强碱,故D正确;
2 2 2
故选:C。
24.D【详解】X、R原子最外层电子数都为1,X、R位于第IA族,X的原子半径最小,
X为H元素;Y、Z、M的最外层电子数依次为4、5、6,Y、Z、M依次位于第IVA族、
第VA族、第VIA族,原子半径R>M>Y>Z,则R为Na元素、Y为C元素、Z为N元素、
M为S元素。
A.R为Na,Na与HO反应生成NaOH和H,A项正确;
2 2
B.Y为C元素, C元素在自然界中有单质存在如石墨等,M为S元素,游离态的硫常存
在于火山口附近或地壳的岩石中,B项正确;C.X为H,Y为C,H、C形成的化合物为烃,烃都可以燃烧,C项正确;
D.Z为N、X为H,N与H形成的气体NH 可使湿润的红色石蕊试纸变蓝,D项错误;
3
答案选D。
25.C【详解】短周期元素X、Y、Z、W原子序数依次增大,常温下,四种元素最高价氧
化物对应水化物均能形成浓度为0.1mol/L的溶液,根据它们的pH分布可知,X、W的
pH=1,应该为硝酸和高氯酸,则X为N,W为Cl,Z的pH小于1,应该为硫酸,Z为S,
Y的pH=13,应该为氢氧化钠,则Y为Na,据此作答。
A.X、W分别位于ⅤA族和ⅦA族,二者不同主族,A错误;
B.N、Na、S、Cl的最外层未成对电子数分别为3、1、2、1,则最外层未成对电子数
X>Z>W=Y,B错误;
C.电子层数越多,离子半径越大,电子层结构相同,核电荷数越大离子半径越小,则简
单离子半径Z>W>X>Y,C正确;
D.非金属性Cl>N>S,则最高价氧化物对应水化物的酸性W>X>Z,即四种元素的最高价
氧化物对应水化物的酸性W最强,D错误;
故答案选C。