文档内容
模板 04 有机物的综合推断
本节导航
识·题型解读 考情分析+命题预测/技巧解读
明·模板构建 答题模板 + 技巧点拨
技法01 有机合成推断的方法和流程 技法02 有机物推断常用“突破口”
通·模板运用 真题示例+模板答题+变式训练
练 ·模板演练 最新模拟、预测考向
有机综合推断题常以框图或变相框图的形式呈现一系列物质的衍变关系,经常是在一系列衍变关
系中有部分产物已知或衍变条件已知,因而解答此类问题的关键是熟悉烃及各种衍生物之间的转化关
系及转化条件。
第一步:确定目标产物 根据题目所给合成线路找到合成的目标产物的结构特点特别是
官能团。
第二步:对比+类比推断有机合 ①对比合成线路中分子式、结构变化;②类比根据合成线路中
成线路中的未知物质 或已知信息中反应条件、结构变化;
确定结构:找出未知物质的分子式和结构的差异,最终确定该
物质的结构简式、分子式。
技法01 有机合成推断的方法和流程
1.有机合成的主要任务
|—构建碳骨架
实现目标化合物—
—引入官能团
2.有机合成遵循的原则①起始原料要廉价、易得、低毒性、低污染。
②应尽量选择步骤较少的合成路线。
③原子经济性高,具有较高的产率。
④有机合成反应要操作简单、条件温和、能耗低、易于实现。
3.有机合成的分析方法
①正向合成分析法的过程:
②逆向合成分析法的过程:
4.有机物的推断流程
技法02 有机物推断常用“突破口”
1.根据反应条件推断反应物或生成物所含的官能团
(1)“浓HSO 、加热”为R—OH的消去或酯化反应
2 4
⃗浓硫酸
醇的消去反应
CHCHOH 170°C CH==CH↑+HO
3 2 2 2 2
O O
酯化反应 浓硫酸
CH 3 C OH+HO C 2 H 5 CH 3 C O C 2 H 5 +H 2 O
(2)“HNO 、浓HSO 、加热”为苯环上的硝化反应
3 2 4
NO2
苯环的硝化反应 +HO—NO 浓硫酸 +H 2 O
2 50°C~60°C
(3)“稀硫酸、加热”为酯水解、二糖、多糖等水解
O O
酯的水解 稀H 2 SO 4
CH 3 C O C 2 H 5+ H OH CH 3 C OH+C 2 H 5 OH
淀粉的水解 (C H O)+nHO ⃗稀硫酸或酶 nC H O(葡萄糖)
6 10 5 n 2 6 12 6
(4)“稀硫酸(H+)”为羧酸盐、苯酚钠酸化
羧酸盐的酸化 CHCOONH+HCl―→CHCOOH+NH Cl
3 4 3 4
ONa OH
苯酚钠的酸化
+HCl +NaCl
(5)“NaOH水溶液、加热”为R—X的水解反应,或酯( )的水解反应⃗
卤代烃的水解(成醇) 水
CHCH—Br+NaOH Δ CHCH—OH+NaBr
3 2 3 2
O O
酯的水解
CH 3 C O C 2 H 5+NaOH CH 3 C ONa+C 2 H 5 OH
(6)“NaOH醇溶液、加热”为R—X的消去反应
⃗乙醇
卤代烃的消去反应
CHCHBr+NaOH Δ CH==CH↑+NaBr+HO
3 2 2 2 2
(7)“溴水或溴的CCl 溶液”为碳碳双键、碳碳三键的加成
4
碳碳双键的加成 CH 2 ==CH 2 +Br 2 ⃗CCl 4 CH 2 Br—CH 2 Br
碳碳三键的加成 HC≡CH+Br CHBr==CHBr,CHBr==CHBr+Br CHBr —CHBr
2 2 2 2
(8)“浓溴水”为酚取代、醛氧化
OH OH
Br Br
苯酚(酚类)取代 +3Br +3HBr
2
Br
醛氧化 CHCHO+Br +HO CHCOOH+2HBr
3 2 2 3
(9)“氯气(Br)、光照”为烷烃取代、苯的同系物侧链上的取代
2
烷烃与氯气的光照取代 CHCH+Cl ⃗光照 HCl+CHCHCl (还有其他的卤代烃)
3 3 2 3 2
光照
甲苯与氯气的光照取代 CH 3+ Cl
2
CH 2 Cl + HCl
(10)“液溴、FeBr (Fe)”为苯或苯的同系物发生苯环上的取代
3
FeBr
苯与液溴反应 +Br
2
3 Br +HBr
CH CH
3 FeCl 3
3
+ Cl + HCl
2
甲苯与液氯的取代 Cl
FeCl
CH 3+ Cl 2 3 Cl CH 3 + HCl
(11)“氧气、Cu或Ag作催化剂、加热”为某些醇氧化
正丙醇催化氧化
⃗Cu/Ag
2CHCHCHOH+O Δ 2CHCHCHO+2HO
3 2 2 2 3 2 2
OH O
异丙醇催化氧化
Cu
2CH
3
—CH—CH
3
+O
2 r
2CH
3
—C—CH
3
+2H
2
O
(12)“氢气、Ni作催化剂、加热”为碳碳双键、碳碳三键、苯、醛、酮加成
⃗催化剂
碳碳双键与氢气的加成
CH==CH+H Δ CH—CH
2 2 2 3 3
⃗催化剂 ⃗催化剂
碳碳三键与氢气的加成 HC≡CH+H Δ CH==CH ;CH==CH +H Δ
2 2 2 2 2 2
CH—CH
3 3
催化剂
苯环与氢气的加成 +3H
2O
醛与氢气的加成
催化剂
CH
3
C H+ H
2
CH
3
CH
2
OH
O OH
酮与氢气的加成
催化剂
CH 3 C CH 3 + H 2 CH 3 CH CH 3
(13)“Ag(NH)OH/ ”或“新制的Cu(OH) / ”为醛的氧化反应
3 2 2
乙醛与银氨溶液△反应 CHCHO+2△Ag(NH)OH 2Ag↓+CHCOONH+3NH +HO
3 3 2 3 4 3 2
(14)“能与NaHCO 溶液反应”为R—COOH
3
乙酸与NaHCO 反应 CHCOOH+NaHCO CHCOONa+CO↑+HO
3 3 3 3 2 2
2.根据特征现象进行推断
(1)溴水褪色:一般含碳碳双键、碳碳三键或醛基(—CHO)
(2)酸性高锰酸钾溶液褪色:含碳碳双键、碳碳三键、醛基或为苯的同系物(与苯环相连的碳原子上连
有氢原子)
(3)遇FeCl 溶液显紫色:含酚羟基
3
(4)加入溴水产生白色沉淀:含酚羟基
(5)加入新制的Cu(OH) 悬浊液(或银氨溶液),加热后出现砖红色沉淀(或银镜):含醛基
2
(6)加入Na,产生H:含羟基或羧基
2
(7)加入NaHCO 溶液,产生气体:含羧基(—COOH)
3
3.根据特征产物推断碳骨架结构和官能团的位置
(1)由消去反应的产物可确定—OH或—X的大致位置
(2)由取代产物的种类可确定碳骨架结构
CHOH
(3)若醇能被氧化为醛或羧酸:含CHOH结构;若醇能被氧化为酮:含 结构;若醇不能被催化
2
氧化:含 C OH结构
(4)由加氢或加溴后的碳骨架结构可确定 或—C≡C—的位置
(5)由有机物发生酯化反应能生成环酯或高聚酯,可确定该有机物中含—OH和—COOH,并根据酯环
的大小,确定—OH与—COOH的相对位置
4.根据特殊的转化关系推断有机物的类型
(1)A
⃗氧化
B
⃗氧化
C,此转化关系一般代表A、B、C分别为醇、醛、羧酸
B
无机酸或碱
(2)A(C n H 2n O 2 ) ,符合此转化关系的有机物A为酯
C
(3)有机三角 ,由此转化关系可推知三种有机物分别是烯烃、卤代烃和醇
5.根据化学计量关系推断有机物中官能团的数目
[Ag(NH ) ]+
32
2Ag
(1) CHO
新制的Cu(OH) 2 悬浊液, r
Cu O (砖红色)
2
(2)2—OH(醇、酚、羧酸)
N⃗a
H
2⃗CO ⃗HCO
(3)2—COOH 3 2— CO 2 ,—COOH 3 — CO 2
⃗CH COOH
3
(4)RCHOH浓硫酸,ΔCHCOOCH R
2 3 2
M M+42
r r
⃗CH CH OH
3 2
(5)RCOOH 浓硫酸,Δ RCOOC H
2 5
M M+28
r r
6.根据题给“已知”中的信息反应进行推断
以信息反应为突破口进行推断,其实是一个拓宽视野和“模仿”的过程,解题时首先确定合成路线中
哪一步反应是以信息反应为模型的,可通过对比特殊的反应条件进行确定,也可通过对比信息反应及合成
路线中反应物和生成物的特殊官能团进行确定;然后分析信息反应中旧键的断裂和新键的形成,以及由此
引起的官能团转化,将其迁移应用到合成路线中,即可推出物质的结构。
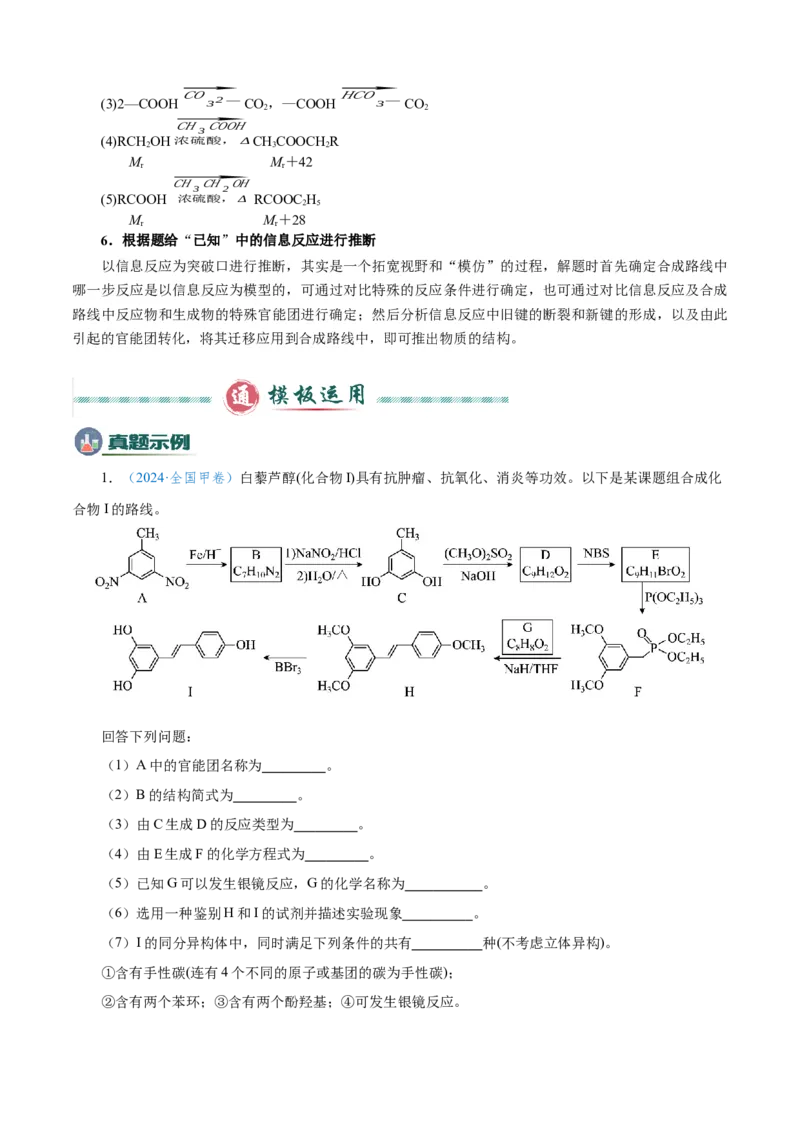
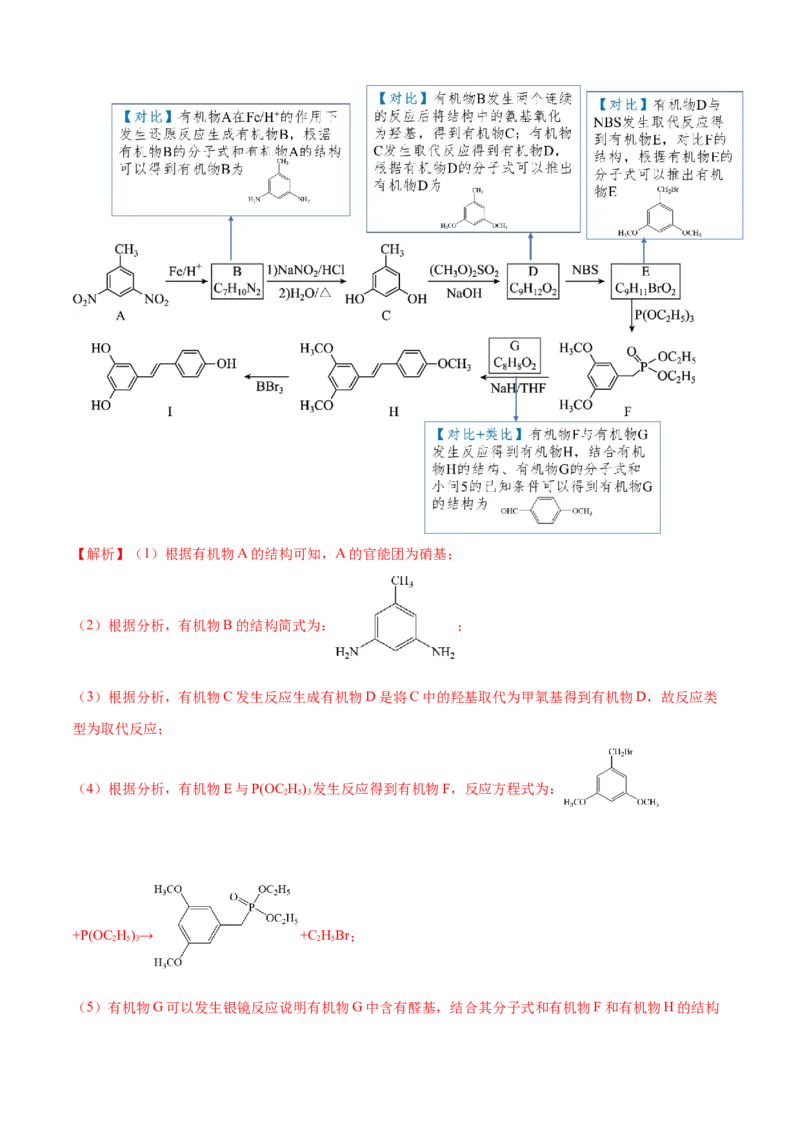
1.(2024·全国甲卷)白藜芦醇(化合物I)具有抗肿瘤、抗氧化、消炎等功效。以下是某课题组合成化
合物I的路线。
回答下列问题:
(1)A中的官能团名称为 。
(2)B的结构简式为 。
(3)由C生成D的反应类型为 。
(4)由E生成F的化学方程式为 。
(5)已知G可以发生银镜反应,G的化学名称为 。
(6)选用一种鉴别H和I的试剂并描述实验现象 。
(7)I的同分异构体中,同时满足下列条件的共有 种(不考虑立体异构)。
①含有手性碳(连有4个不同的原子或基团的碳为手性碳);
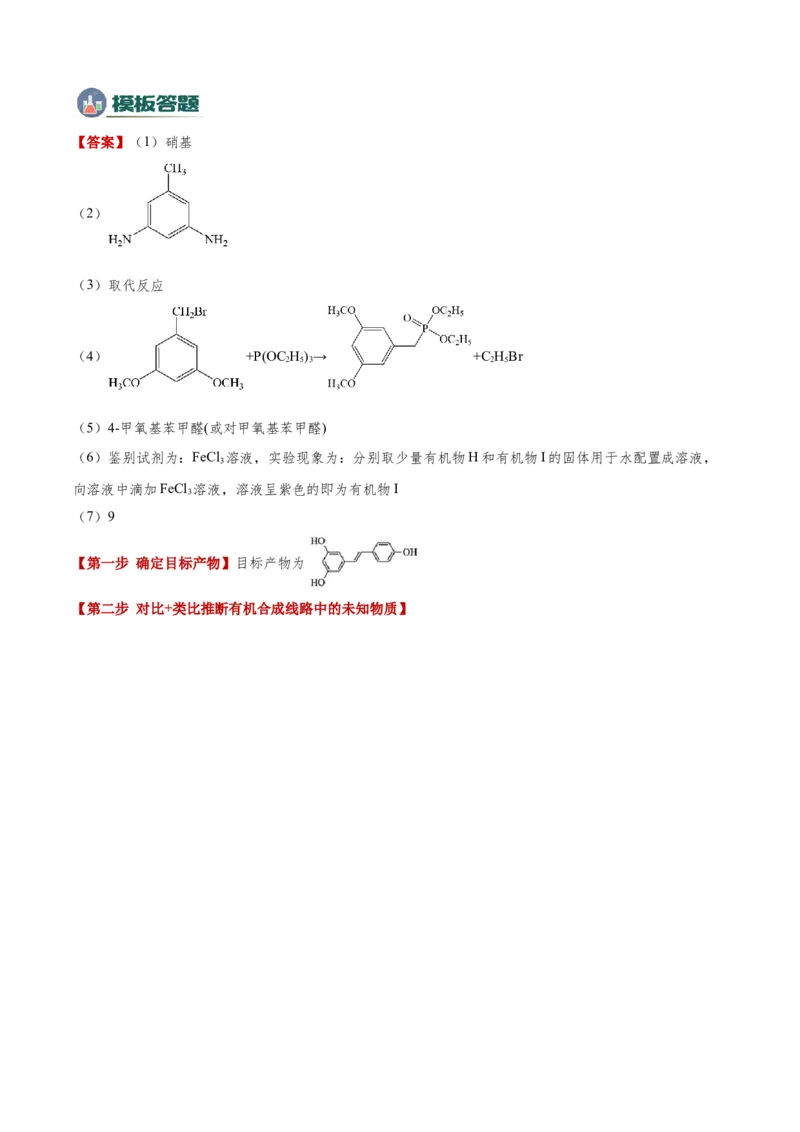
②含有两个苯环;③含有两个酚羟基;④可发生银镜反应。【答案】(1)硝基
(2)
(3)取代反应
(4) +P(OC H)→ +C HBr
2 5 3 2 5
(5)4-甲氧基苯甲醛(或对甲氧基苯甲醛)
(6)鉴别试剂为:FeCl 溶液,实验现象为:分别取少量有机物H和有机物I的固体用于水配置成溶液,
3
向溶液中滴加FeCl 溶液,溶液呈紫色的即为有机物I
3
(7)9
【第一步 确定目标产物】目标产物为
【第二步 对比+类比推断有机合成线路中的未知物质】【解析】(1)根据有机物A的结构可知,A的官能团为硝基;
(2)根据分析,有机物B的结构简式为: ;
(3)根据分析,有机物C发生反应生成有机物D是将C中的羟基取代为甲氧基得到有机物D,故反应类
型为取代反应;
(4)根据分析,有机物E与P(OC H) 发生反应得到有机物F,反应方程式为:
2 5 3
+P(OC H)→ +C HBr;
2 5 3 2 5
(5)有机物G可以发生银镜反应说明有机物G中含有醛基,结合其分子式和有机物F和有机物H的结构可以得到有机物G的结构为 ,其化学名称为:4-甲氧基苯甲醛(或对甲氧基苯甲醛);
(6)对比有机物H和有机物I的结构可以看出,有机物I中含有酚羟基,可以由此进行鉴别,鉴别试剂为
FeCl 溶液,实验现象为分别取少量有机物H和有机物I的固体用于水配置成溶液,向溶液中滴加FeCl 溶
3 3
液,溶液呈紫色的即为有机物I;
(7)对于有机物I的同分异构体,可以发生银镜反应说明含有醛基;含有手性碳原子,说明有饱和碳原子,
可以得到其主体结构为 ,因其含有两个酚羟基和手性碳原子,则满足条件的同分异构
体有9种,分别为: 、 、 、
、 、 、 、
、 。
1.(2024·山东卷)心血管药物缬沙坦中间体(F)的两条合成路线如下:
已知:
I.
Ⅱ.R CHO———————→ R CHNHR
1 1 2 2
回答下列问题:
(1)A结构简式为 ;B→C反应类型为 。
(2)C+D→F化学方程式为 。
(3)E中含氧官能团名称为 ;F中手性碳原子有 个。(4)D的一种同分异构体含硝基和3种不同化学环境的氢原子(个数此为 ),其结构简式为
。
(5)C→E的合成路线设计如下:
试剂X为 (填化学式);试剂Y不能选用 ,原因是 。
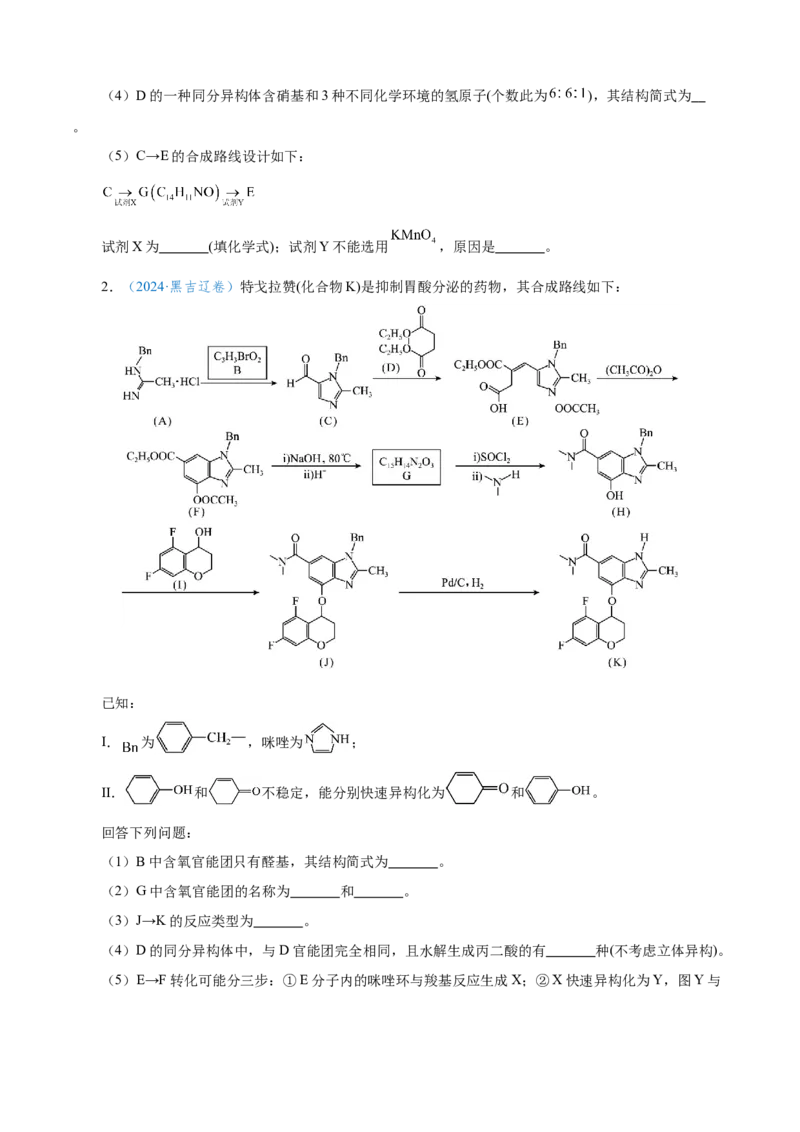
2.(2024·黑吉辽卷)特戈拉赞(化合物K)是抑制胃酸分泌的药物,其合成路线如下:
已知:
I. 为 ,咪唑为 ;
II. 和 不稳定,能分别快速异构化为 和 。
回答下列问题:
(1)B中含氧官能团只有醛基,其结构简式为 。
(2)G中含氧官能团的名称为 和 。
(3)J→K的反应类型为 。
(4)D的同分异构体中,与D官能团完全相同,且水解生成丙二酸的有 种(不考虑立体异构)。
(5)E→F转化可能分三步:①E分子内的咪唑环与羧基反应生成X;②X快速异构化为Y,图Y与反应生成F。第③步化学方程式为 。
(6)苯环具有与咪唑环类似的性质。参考B→X的转化,设计化合物I的合成路线如下(部分反应条件
己略去)。其中M和N的结构简式为 和 。
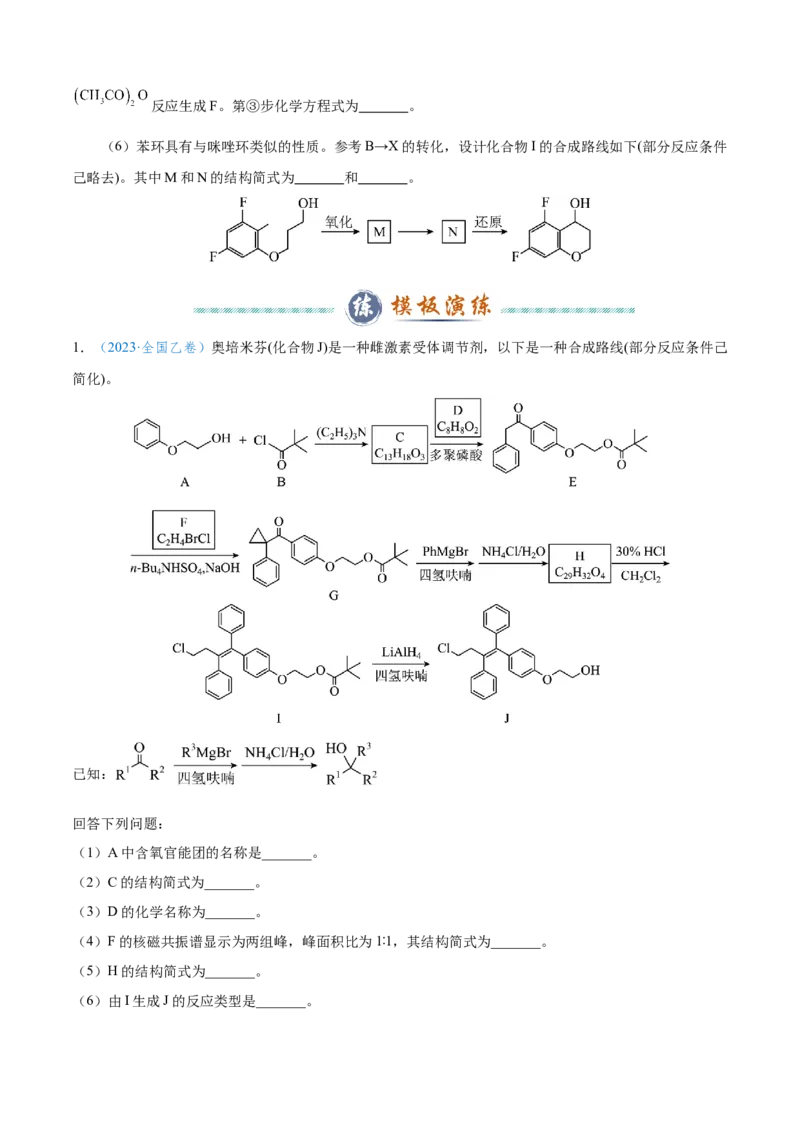
1.(2023·全国乙卷)奥培米芬(化合物J)是一种雌激素受体调节剂,以下是一种合成路线(部分反应条件己
简化)。
已知:
回答下列问题:
(1)A中含氧官能团的名称是_______。
(2)C的结构简式为_______。
(3)D的化学名称为_______。
(4)F的核磁共振谱显示为两组峰,峰面积比为1∶1,其结构简式为_______。
(5)H的结构简式为_______。
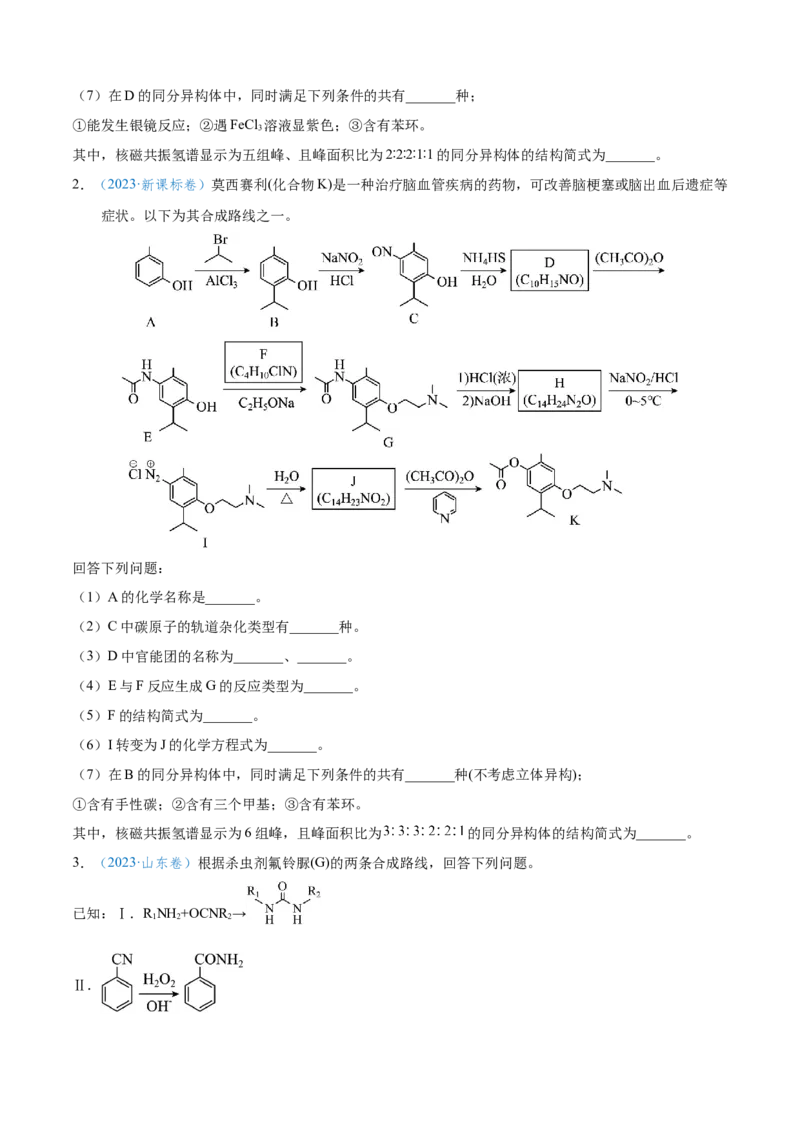
(6)由I生成J的反应类型是_______。(7)在D的同分异构体中,同时满足下列条件的共有_______种;
①能发生银镜反应;②遇FeCl 溶液显紫色;③含有苯环。
3
其中,核磁共振氢谱显示为五组峰、且峰面积比为2∶2∶2∶1∶1的同分异构体的结构简式为_______。
2.(2023·新课标卷)莫西赛利(化合物K)是一种治疗脑血管疾病的药物,可改善脑梗塞或脑出血后遗症等
症状。以下为其合成路线之一。
回答下列问题:
(1)A的化学名称是_______。
(2)C中碳原子的轨道杂化类型有_______种。
(3)D中官能团的名称为_______、_______。
(4)E与F反应生成G的反应类型为_______。
(5)F的结构简式为_______。
(6)I转变为J的化学方程式为_______。
(7)在B的同分异构体中,同时满足下列条件的共有_______种(不考虑立体异构);
①含有手性碳;②含有三个甲基;③含有苯环。
其中,核磁共振氢谱显示为6组峰,且峰面积比为 的同分异构体的结构简式为_______。
3.(2023·山东卷)根据杀虫剂氟铃脲(G)的两条合成路线,回答下列问题。
已知:Ⅰ.R NH +OCNR →
1 2 2
Ⅱ.路线:
(1)A的化学名称为_____(用系统命名法命名); 的化学方程式为_____;D中含氧官能团的名称为
_____;E的结构简式为_____。
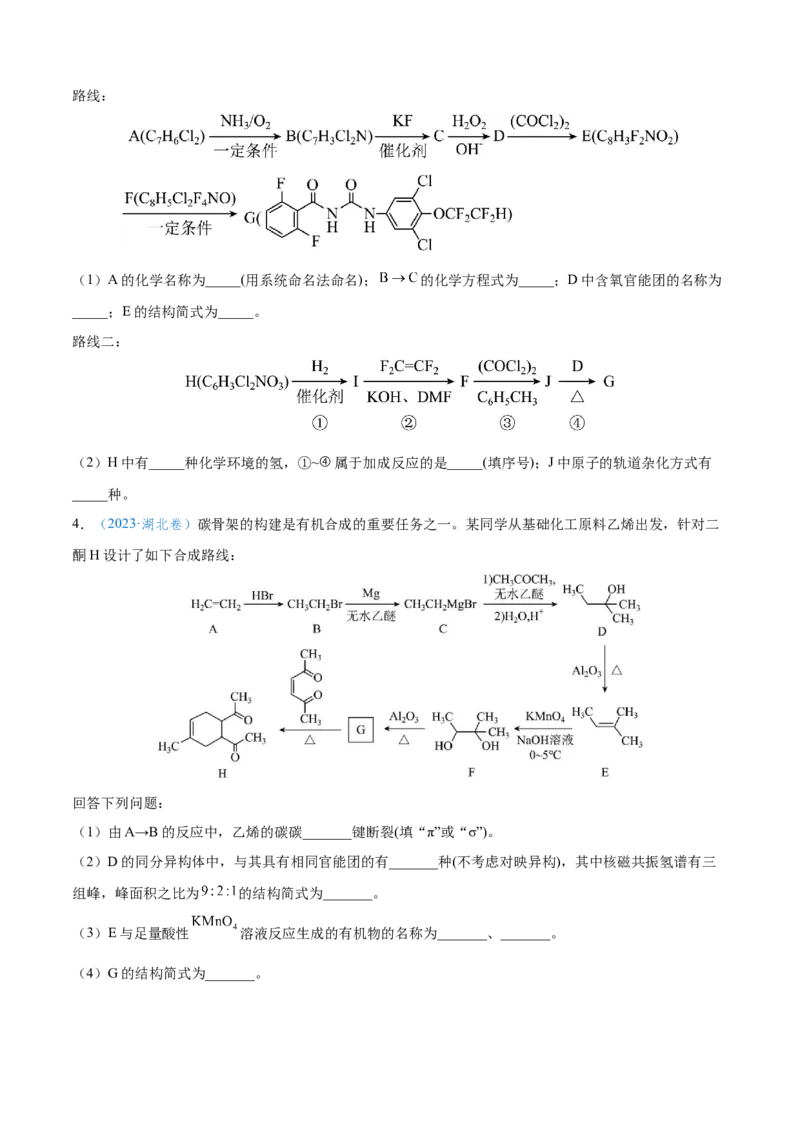
路线二:
(2)H中有_____种化学环境的氢,①~④属于加成反应的是_____(填序号);J中原子的轨道杂化方式有
_____种。
4.(2023·湖北卷)碳骨架的构建是有机合成的重要任务之一。某同学从基础化工原料乙烯出发,针对二
酮H设计了如下合成路线:
回答下列问题:
(1)由A→B的反应中,乙烯的碳碳_______键断裂(填“π”或“σ”)。
(2)D的同分异构体中,与其具有相同官能团的有_______种(不考虑对映异构),其中核磁共振氢谱有三
组峰,峰面积之比为 的结构简式为_______。
(3)E与足量酸性 溶液反应生成的有机物的名称为_______、_______。
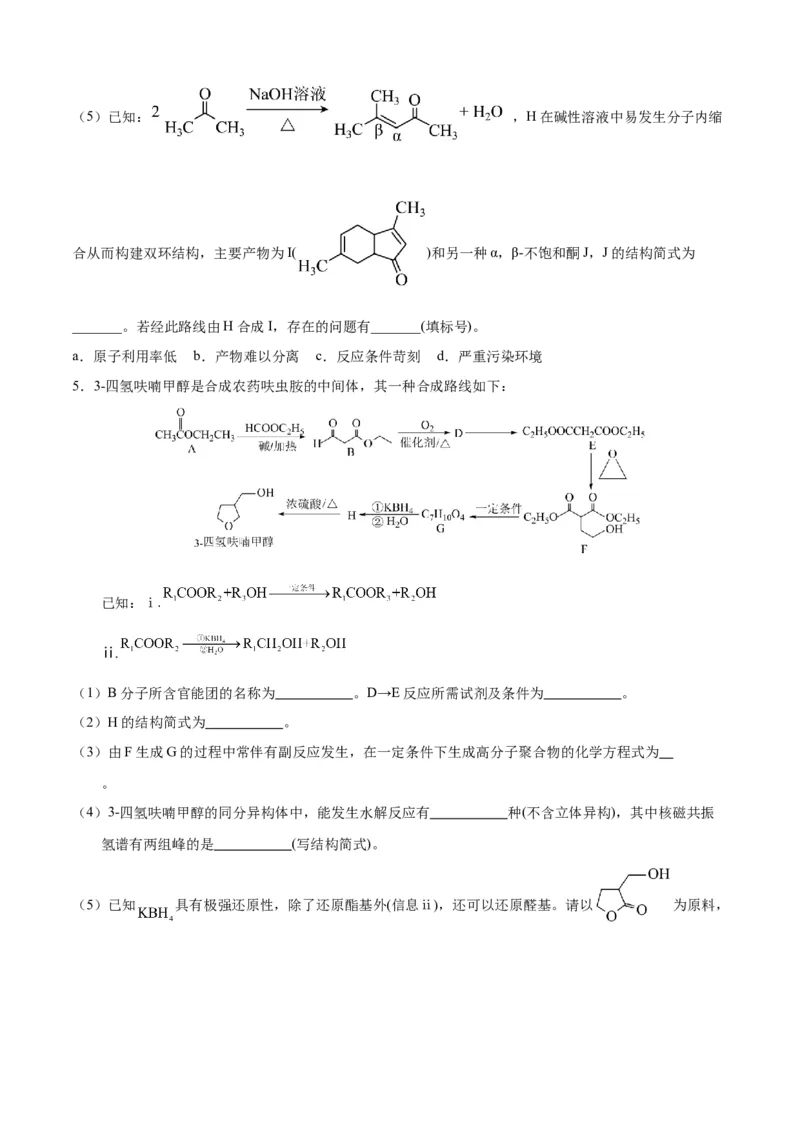
(4)G的结构简式为_______。(5)已知: ,H在碱性溶液中易发生分子内缩
合从而构建双环结构,主要产物为I( )和另一种α,β-不饱和酮J,J的结构简式为
_______。若经此路线由H合成I,存在的问题有_______(填标号)。
a.原子利用率低 b.产物难以分离 c.反应条件苛刻 d.严重污染环境
5.3-四氢呋喃甲醇是合成农药呋虫胺的中间体,其一种合成路线如下:
已知:ⅰ.
ⅱ.
(1)B分子所含官能团的名称为 。D→E反应所需试剂及条件为 。
(2)H的结构简式为 。
(3)由F生成G的过程中常伴有副反应发生,在一定条件下生成高分子聚合物的化学方程式为
。
(4)3-四氢呋喃甲醇的同分异构体中,能发生水解反应有 种(不含立体异构),其中核磁共振
氢谱有两组峰的是 (写结构简式)。
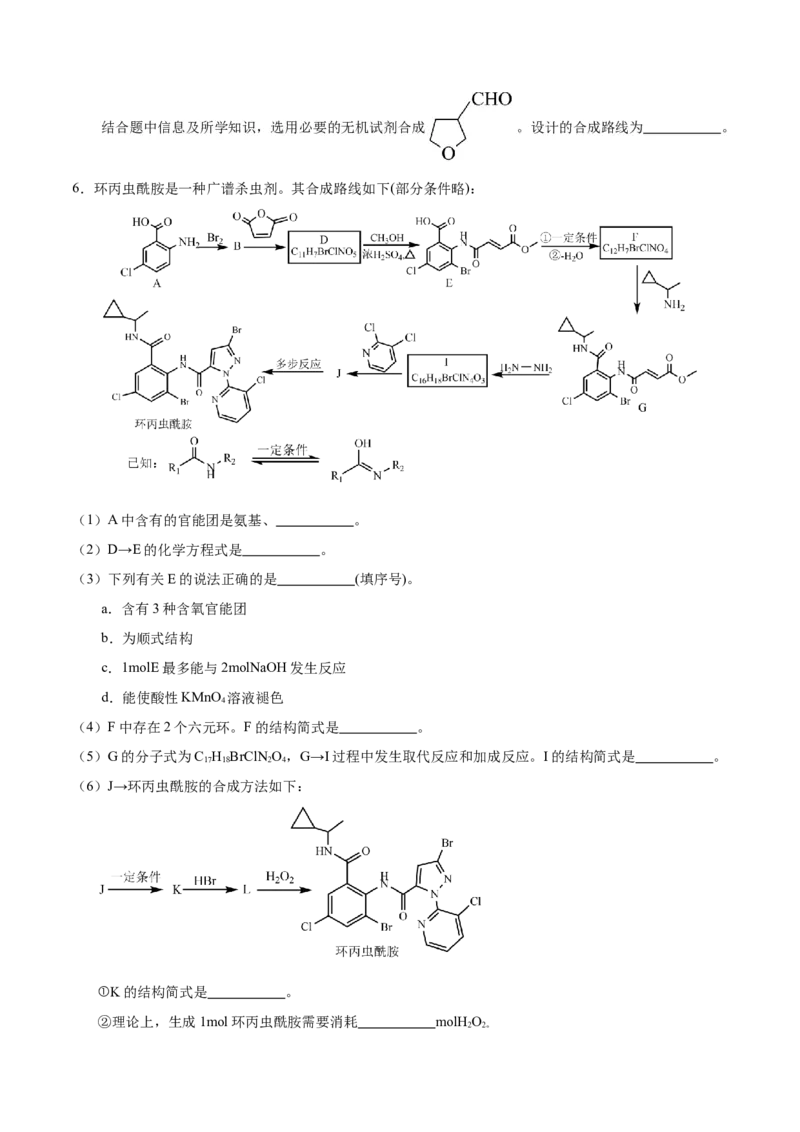
(5)已知 具有极强还原性,除了还原酯基外(信息ⅱ),还可以还原醛基。请以 为原料,结合题中信息及所学知识,选用必要的无机试剂合成 。设计的合成路线为 。
6.环丙虫酰胺是一种广谱杀虫剂。其合成路线如下(部分条件略):
(1)A中含有的官能团是氨基、 。
(2)D→E的化学方程式是 。
(3)下列有关E的说法正确的是 (填序号)。
a.含有3种含氧官能团
b.为顺式结构
c.1molE最多能与2molNaOH发生反应
d.能使酸性KMnO 溶液褪色
4
(4)F中存在2个六元环。F的结构简式是 。
(5)G的分子式为C H BrClN O,G→I过程中发生取代反应和加成反应。I的结构简式是 。
17 18 2 4
(6)J→环丙虫酰胺的合成方法如下:
①K的结构简式是 。
②理论上,生成1mol环丙虫酰胺需要消耗 molH O
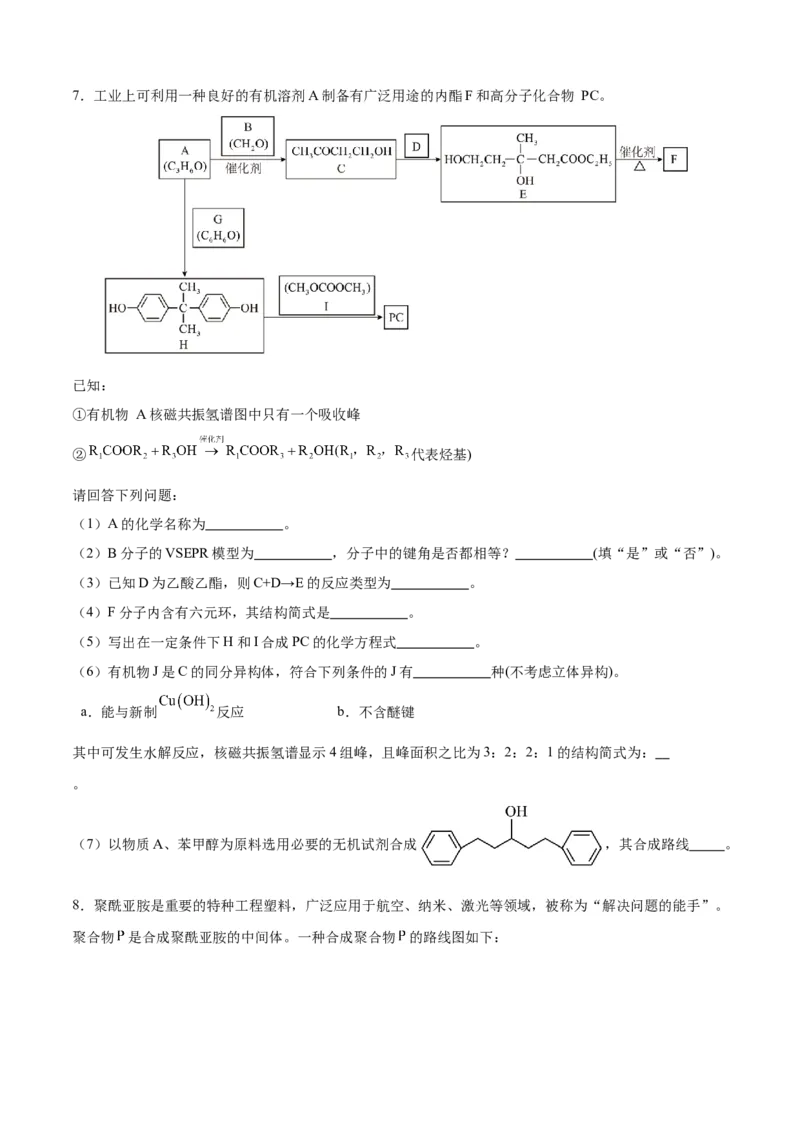
2 2。7.工业上可利用一种良好的有机溶剂A制备有广泛用途的内酯F和高分子化合物 PC。
已知:
①有机物 A核磁共振氢谱图中只有一个吸收峰
② 代表烃基)
请回答下列问题:
(1)A的化学名称为 。
(2)B分子的VSEPR模型为 ,分子中的键角是否都相等? (填“是”或“否”)。
(3)已知D为乙酸乙酯,则C+D→E的反应类型为 。
(4)F分子内含有六元环,其结构简式是 。
(5)写出在一定条件下H和I合成PC的化学方程式 。
(6)有机物J是C的同分异构体,符合下列条件的J有 种(不考虑立体异构)。
a.能与新制 反应 b.不含醚键
其中可发生水解反应,核磁共振氢谱显示4组峰,且峰面积之比为3:2:2:1的结构简式为:
。
(7)以物质A、苯甲醇为原料选用必要的无机试剂合成 ,其合成路线 。
8.聚酰亚胺是重要的特种工程塑料,广泛应用于航空、纳米、激光等领域,被称为“解决问题的能手”。
聚合物 是合成聚酰亚胺的中间体。一种合成聚合物 的路线图如下:已知:
ⅰ.
ⅱ. (R代表烃基)
回答下列问题:
(1) 中官能团的名称是 , 的反应类型是 。
(2) 苯环上的一氯代物有2种,则 的化学方程式是
(3)下列有关说法正确的是 (填字母)。
a.A中所有原子可能共平面
b.B生成C所需试剂是浓硝酸,反应条件是浓硫酸和加热
c.能够用酸性 溶液鉴别 、
d. 中所有碳原子的杂化方式均为 杂化
(4) 的结构简式为 。
(5)同时符合下列条件的B的同分异构体有 种。
①含有苯环;②能与 溶液反应生成 ;
(6)参照上述合成路线,设计由 、 和 制备
的合成路线: (用流程图表示,无机试剂任选)。
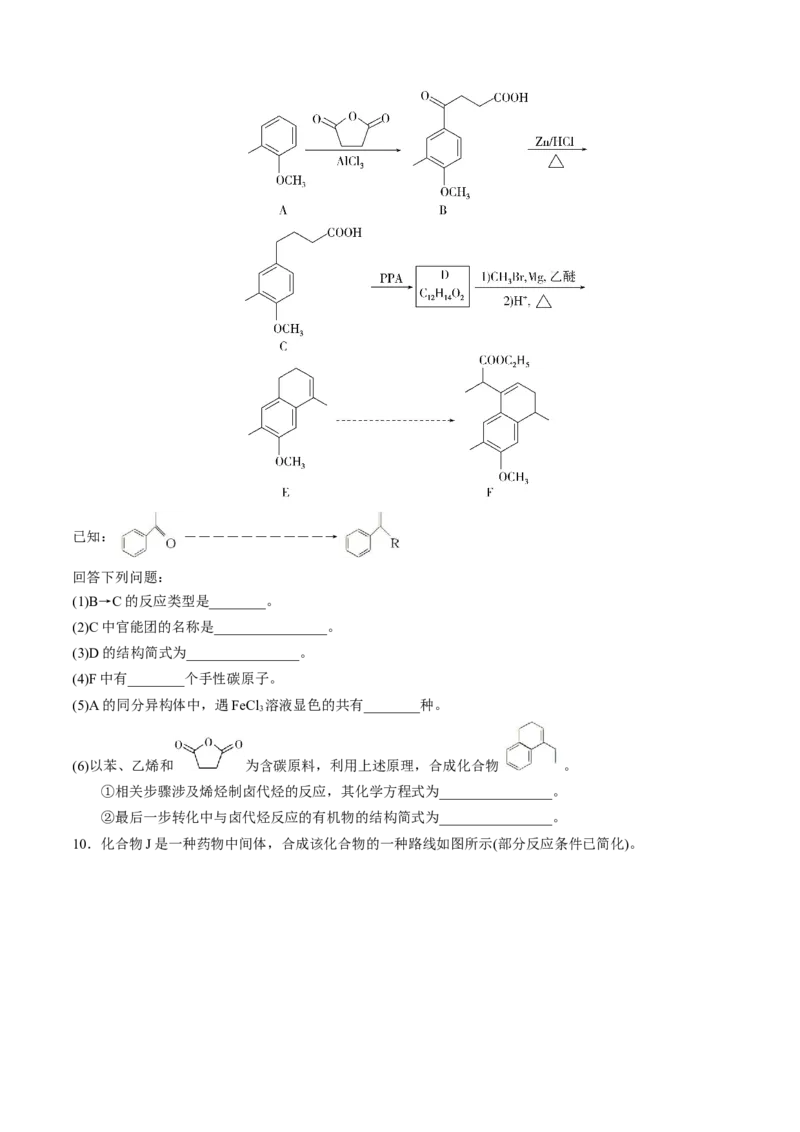
9.化合物F是合成药物的重要中间体,其合成路线如图所示。已知: ――――――――――→
回答下列问题:
(1)B→C的反应类型是________。
(2)C中官能团的名称是________________。
(3)D的结构简式为________________。
(4)F中有________个手性碳原子。
(5)A的同分异构体中,遇FeCl 溶液显色的共有________种。
3
(6)以苯、乙烯和 为含碳原料,利用上述原理,合成化合物 。
①相关步骤涉及烯烃制卤代烃的反应,其化学方程式为________________。
②最后一步转化中与卤代烃反应的有机物的结构简式为________________。
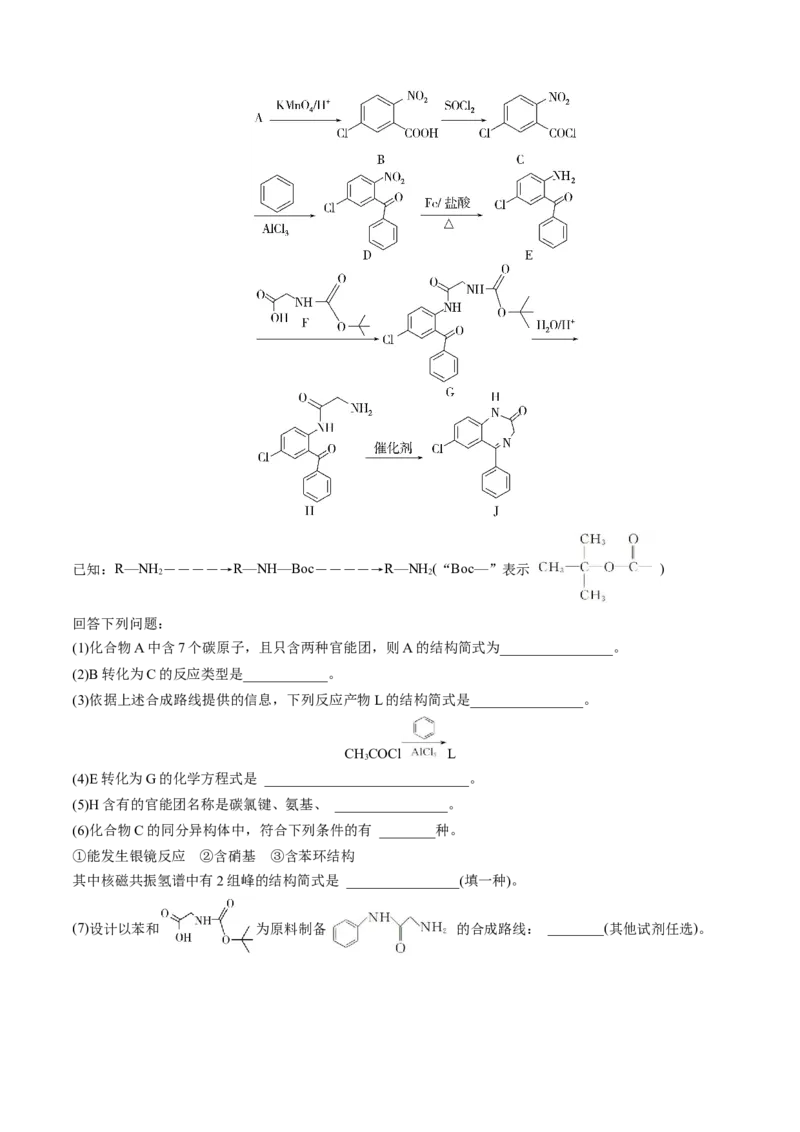
10.化合物J是一种药物中间体,合成该化合物的一种路线如图所示(部分反应条件已简化)。已知:R—NH ――――→R—NH—Boc――――→R—NH (“Boc—”表示 )
2 2
回答下列问题:
(1)化合物A中含7个碳原子,且只含两种官能团,则A的结构简式为________________。
(2)B转化为C的反应类型是____________。
(3)依据上述合成路线提供的信息,下列反应产物L的结构简式是________________。
CHCOCl L
3
(4)E转化为G的化学方程式是 _____________________________。
(5)H含有的官能团名称是碳氯键、氨基、 ________________。
(6)化合物C的同分异构体中,符合下列条件的有 ________种。
①能发生银镜反应 ②含硝基 ③含苯环结构
其中核磁共振氢谱中有2组峰的结构简式是 ________________(填一种)。
(7)设计以苯和 为原料制备 的合成路线: ________(其他试剂任选)。