文档内容
2020 级高三下学期开学考试
化学试卷
一、单项选择题(每小题只有一个正确选项,每小题3分,共14题.)
1.下列物质用途的描述正确的是( )。
A.明矾溶液用作铜绿去除剂,利用了其水解显酸性
B.淀粉溶液用作碘量法滴定的指示剂,利用了其不饱和性
C.FeS用作除去含Cu2废水的沉淀剂,利用了其还原性
D.SO 用作海水提溴的吸收剂,利用了其漂白性
2
2.下列有关说法正确的是( )。
A.N H 的结构式为 B.中子数为8的氮原子可表示为8 N
2 4 7
C.SO 的VSEPR 模型: D.NaCl的电子式为
3
3.N 为阿伏加德罗常数的值,下列说法正确的是( )。
A
A.1mol金刚烷 中含有键数为12N
A
B.14.4g28Si 15N 中含有质子数为7N
3 4 A
C.标准状况下,11.2L二氯甲烷中含有氯原子数为1N
A
D.0.1mol碘蒸气与足量氢气加热,得到HI的分子数为0.2N
A
4.能正确表示下列反应的离子方程式为( )。
A.硫化钠溶液和硝酸混合:S2 2H H S
2
B.明矾溶液与过量氨水混合:Al3 4NH H O AlO 4NH
3 2 2 4
C.1L 1mol L FeBr 溶液与一定量氯气反应转移的电子数为26.021023时,反应的离子方程式为:
2
2Fe2 2Br 2Cl Br 4Cl
2 2
D.向NaClO溶液中通入少量SO :ClO SO H O SO2 Cl 2H
2 2 2 45.ClO 与Na O 在碱性溶液中可以发生反应:2ClO Na O 2NaClO O ,下列有关说法错
2 2 2 2 2 2 2 2
误的是( )。
A.ClO 与Na O 均可用作杀菌剂、漂白剂
2 2 2
B.Na O 与NaClO 晶体中阴阳离子个数比值不同
2 2 2
C.Na、Cl、O2离子半径:r
Cl
r
Na
r
O2
D.反应中有离子键的断裂与形成
6.含S元素的某钠盐a能发生如图转化。下列说法错误的是( )。
A.a可能为正盐,也可能为酸式盐
B.c为不溶于盐酸的白色沉淀
C.d分子中心原子杂化轨道类型为sp3杂化
D.反应②中还可能生成淡黄色沉淀
7.下列各粒子组在溶液中能否大量共存的判断和分析均正确的是( )。
选项 粒子组 判断和分析
Na、Al3、Cl、 不能大量共存,因发生反应:
A
NH H O Al3 4NH H O AlO 4NH 2H O
3 2 3 2 2 4 2
OH 、Ca2、SO2、
4
B
不能大量共存,因HCO发生水解
3
HCO
3
C
K、Ba2、I、MnO 不能大量共存,因MnO和I发生氧化还原反应
4 4
D Na、Fe3、SO2、H O 不能大量共存,因发生反应:Fe3 H O Fe2 O H O
4 2 2 2 2 2 2
8.连花清瘟因含连翘、金银花而得名,其有效成分绿原酸的结构简式如下图,下列有关绿原酸的说法中正
确的是( )A.绿原酸的分子式为C H O B.1个绿原酸分子中含有3个手性碳原子
16 18 9
C.1mol绿原酸可消耗3mol NaOH D.绿原酸含氧官能团有羟基、酯基、羧基、醚键
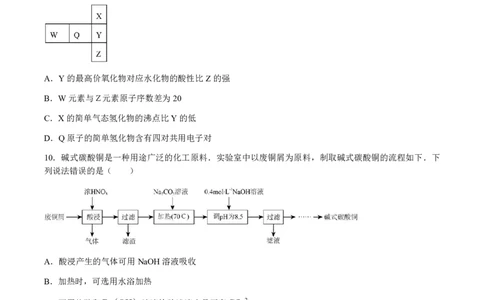
9.下图是元素周期表的一部分,五种元素属于前四周期主族元素,其中只有W为金属元素.下列说法不
正确的是( )
A.Y的最高价氧化物对应水化物的酸性比Z的强
B.W元素与Z元素原子序数差为20
C.X的简单气态氢化物的沸点比Y的低
D.Q原子的简单氢化物含有四对共用电子对
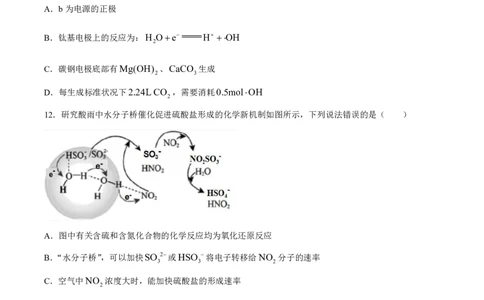
10.碱式碳酸铜是一种用途广泛的化工原料.实验室中以废铜屑为原料,制取碱式碳酸铜的流程如下.下
列说法错误的是( )
A.酸浸产生的气体可用NaOH溶液吸收
B.加热时,可选用水浴加热
C.可用盐酸和Ba OH 溶液检验滤液中是否有CO 2
2 3
D.温度和pH是影响产品纯度的主要因素
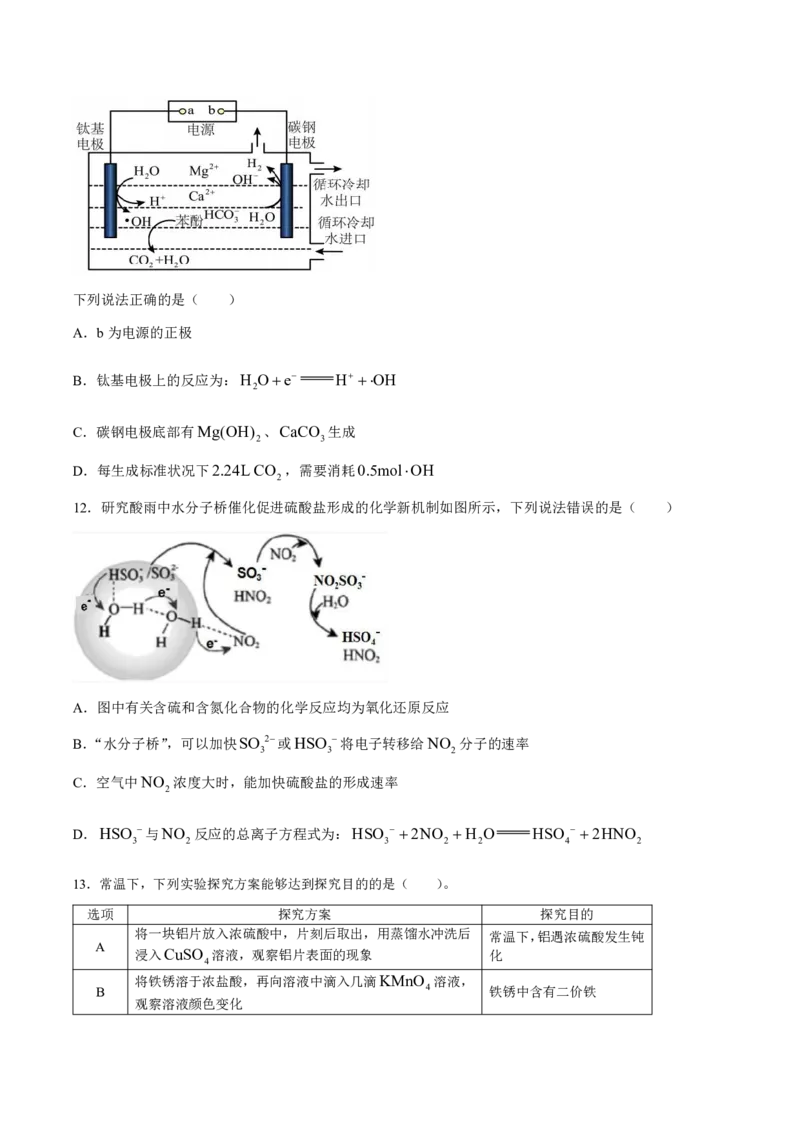
11.用电化学方法可以去除循环冷却水(含有Ca2、Mg2、HCO 、苯酚等)中的有机污染物,同时经
3
处理过的冷却水还能减少结垢,其工作原理如下图所示.下列说法正确的是( )
A.b为电源的正极
B.钛基电极上的反应为:H Oe H OH
2
C.碳钢电极底部有Mg(OH) 、CaCO 生成
2 3
D.每生成标准状况下2.24L CO ,需要消耗0.5molOH
2
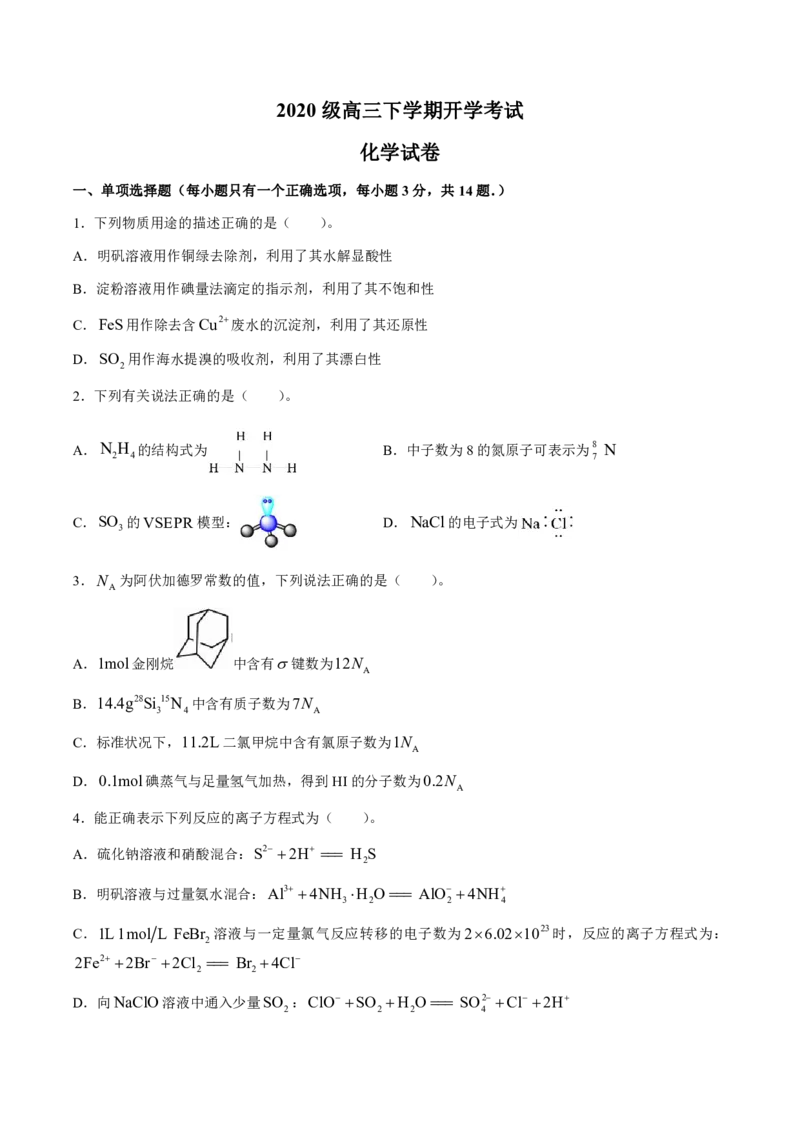
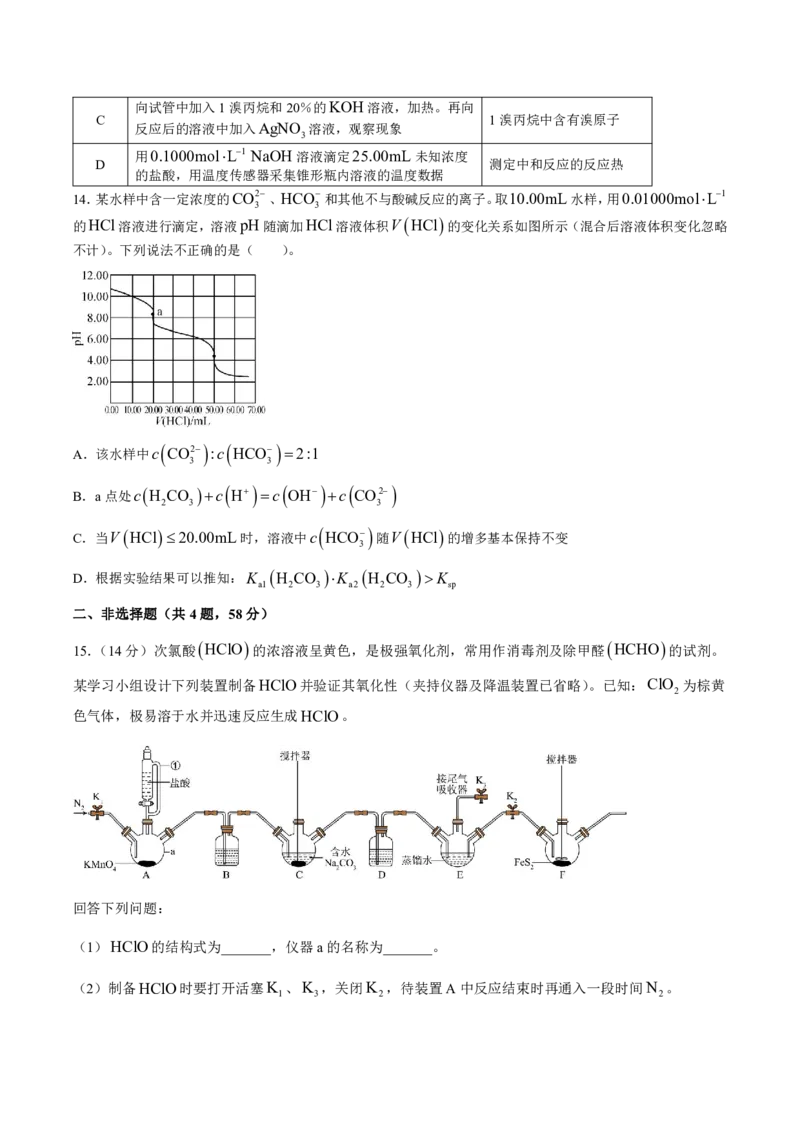
12.研究酸雨中水分子桥催化促进硫酸盐形成的化学新机制如图所示,下列说法错误的是( )
A.图中有关含硫和含氮化合物的化学反应均为氧化还原反应
B.“水分子桥”,可以加快SO 2或HSO 将电子转移给NO 分子的速率
3 3 2
C.空气中NO 浓度大时,能加快硫酸盐的形成速率
2
D.HSO 与NO 反应的总离子方程式为:HSO 2NO H O HSO 2HNO
3 2 3 2 2 4 2
13.常温下,下列实验探究方案能够达到探究目的的是( )。
选项 探究方案 探究目的
将一块铝片放入浓硫酸中,片刻后取出,用蒸馏水冲洗后 常温下,铝遇浓硫酸发生钝
A
浸入CuSO 溶液,观察铝片表面的现象 化
4
将铁锈溶于浓盐酸,再向溶液中滴入几滴KMnO 溶液,
B 4 铁锈中含有二价铁
观察溶液颜色变化向试管中加入1溴丙烷和20%的KOH溶液,加热。再向
C 1溴丙烷中含有溴原子
反应后的溶液中加入AgNO 溶液,观察现象
3
用0.1000molL1 NaOH溶液滴定25.00mL未知浓度
D 测定中和反应的反应热
的盐酸,用温度传感器采集锥形瓶内溶液的温度数据
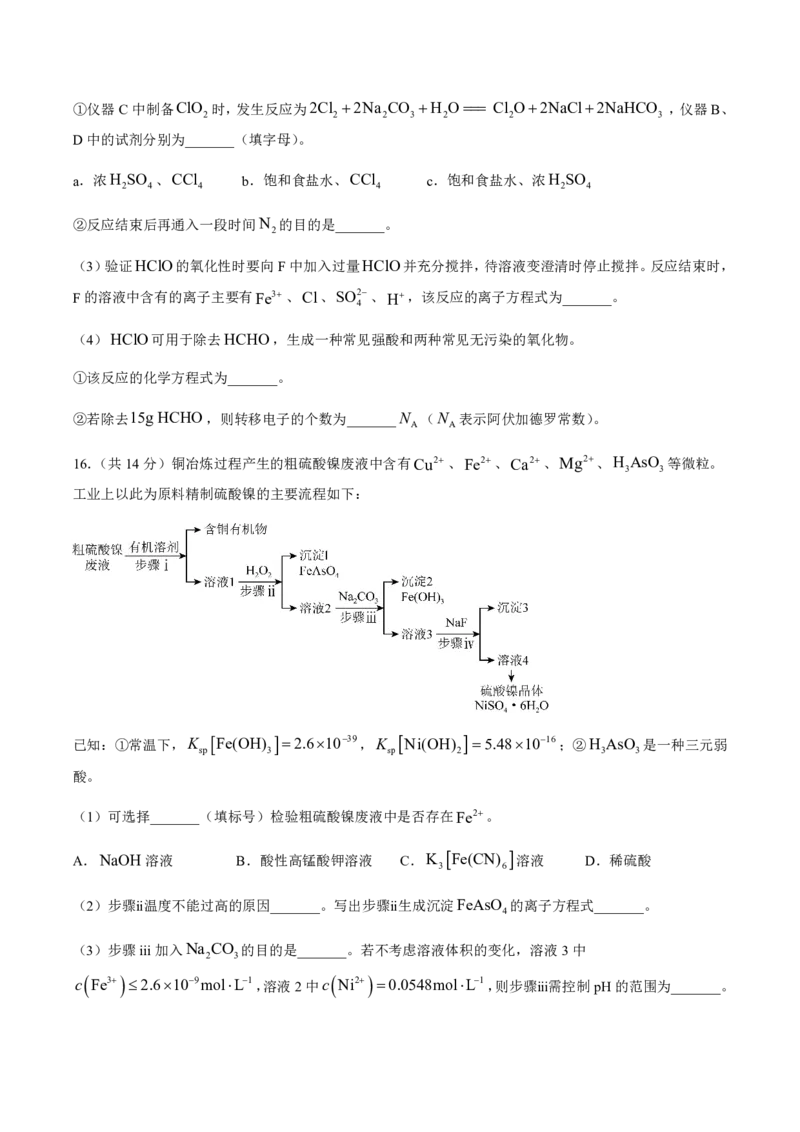
14.某水样中含一定浓度的CO2、HCO和其他不与酸碱反应的离子。取10.00mL水样,用0.01000molL1
3 3
的HCl溶液进行滴定,溶液pH随滴加HCl溶液体积V HCl 的变化关系如图所示(混合后溶液体积变化忽略
不计)。下列说法不正确的是( )。
A.该水样中c
CO2
:c
HCO
2:1
3 3
B.a点处c H CO c H c OH c CO2
2 3 3
C.当V HCl 20.00mL时,溶液中c HCO 随V HCl 的增多基本保持不变
3
D.根据实验结果可以推知:K H CO K H CO K
a1 2 3 a2 2 3 sp
二、非选择题(共4题,58分)
15.(14分)次氯酸
HClO
的浓溶液呈黄色,是极强氧化剂,常用作消毒剂及除甲醛
HCHO
的试剂。
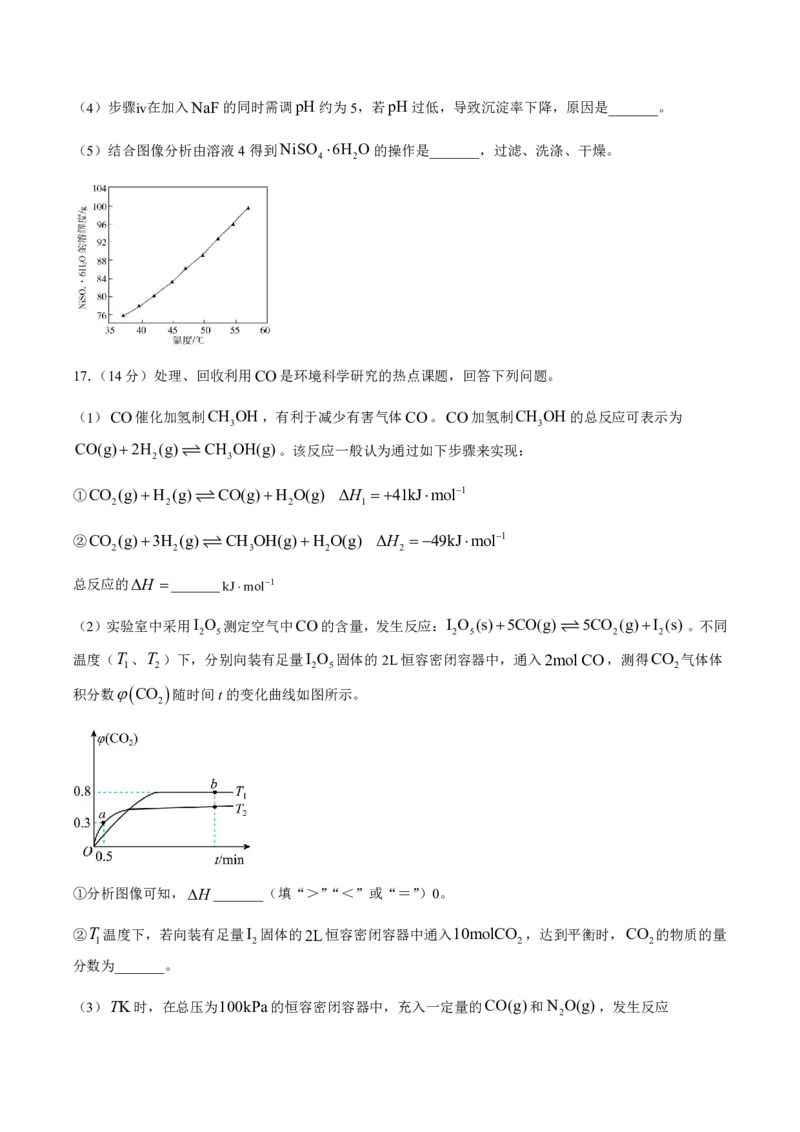
某学习小组设计下列装置制备HClO并验证其氧化性(夹持仪器及降温装置已省略)。已知:ClO 为棕黄
2
色气体,极易溶于水并迅速反应生成HClO。
回答下列问题:
(1)HClO的结构式为_______,仪器a的名称为_______。
(2)制备HClO时要打开活塞K 、K ,关闭K ,待装置A中反应结束时再通入一段时间N 。
1 3 2 2①仪器C中制备ClO 时,发生反应为2Cl 2Na CO H O Cl O2NaCl2NaHCO ,仪器B、
2 2 2 3 2 2 3
D中的试剂分别为_______(填字母)。
a.浓H SO 、CCl b.饱和食盐水、CCl c.饱和食盐水、浓H SO
2 4 4 4 2 4
②反应结束后再通入一段时间N 的目的是_______。
2
(3)验证HClO的氧化性时要向F中加入过量HClO并充分搅拌,待溶液变澄清时停止搅拌。反应结束时,
F的溶液中含有的离子主要有Fe3、Cl、SO2、H,该反应的离子方程式为_______。
4
(4)HClO可用于除去HCHO,生成一种常见强酸和两种常见无污染的氧化物。
①该反应的化学方程式为_______。
②若除去15g HCHO,则转移电子的个数为_______N (N 表示阿伏加德罗常数)。
A A
16.(共14分)铜冶炼过程产生的粗硫酸镍废液中含有Cu2、Fe2、Ca2、Mg2、H AsO 等微粒。
3 3
工业上以此为原料精制硫酸镍的主要流程如下:
已知:①常温下,K
Fe(OH)
2.61039,K
Ni(OH)
5.481016;②H
AsO 是一种三元弱
sp 3 sp 2 3 3
酸。
(1)可选择_______(填标号)检验粗硫酸镍废液中是否存在Fe2。
A.NaOH溶液 B.酸性高锰酸钾溶液 C.K Fe(CN) 溶液 D.稀硫酸
3 6
(2)步骤ⅱ温度不能过高的原因_______。写出步骤ⅱ生成沉淀FeAsO 的离子方程式_______。
4
(3)步骤iii加入Na CO 的目的是_______。若不考虑溶液体积的变化,溶液3中
2 3
c Fe3 2.6109molL1,溶液2中c Ni2 0.0548molL1,则步骤ⅲ需控制pH的范围为_______。(4)步骤ⅳ在加入NaF的同时需调pH约为5,若pH过低,导致沉淀率下降,原因是_______。
(5)结合图像分析由溶液4得到NiSO 6H O的操作是_______,过滤、洗涤、干燥。
4 2
17.(14分)处理、回收利用CO是环境科学研究的热点课题,回答下列问题。
(1)CO催化加氢制CH OH,有利于减少有害气体CO。CO加氢制CH OH的总反应可表示为
3 3
CO(g)2H (g)CH OH(g)。该反应一般认为通过如下步骤来实现:
2 3
①CO (g)H (g)CO(g)H O(g) ΔH 41kJmol1
2 2 2 1
②CO (g)3H (g)CH OH(g)H O(g) ΔH 49kJmol1
2 2 3 2 2
总反应的ΔH _______kJmol1
(2)实验室中采用I O 测定空气中CO的含量,发生反应:I O (s)5CO(g) 5CO (g)I (s) 。不同
2 5 2 5 2 2
温度(T 、T )下,分别向装有足量I O 固体的2L恒容密闭容器中,通入2mol CO,测得CO 气体体
1 2 2 5 2
积分数
CO
随时间t的变化曲线如图所示。
2
①分析图像可知,H _______(填“>”“<”或“=”)0。
②T 温度下,若向装有足量I 固体的2L恒容密闭容器中通入10molCO ,达到平衡时,CO 的物质的量
1 2 2 2
分数为_______。
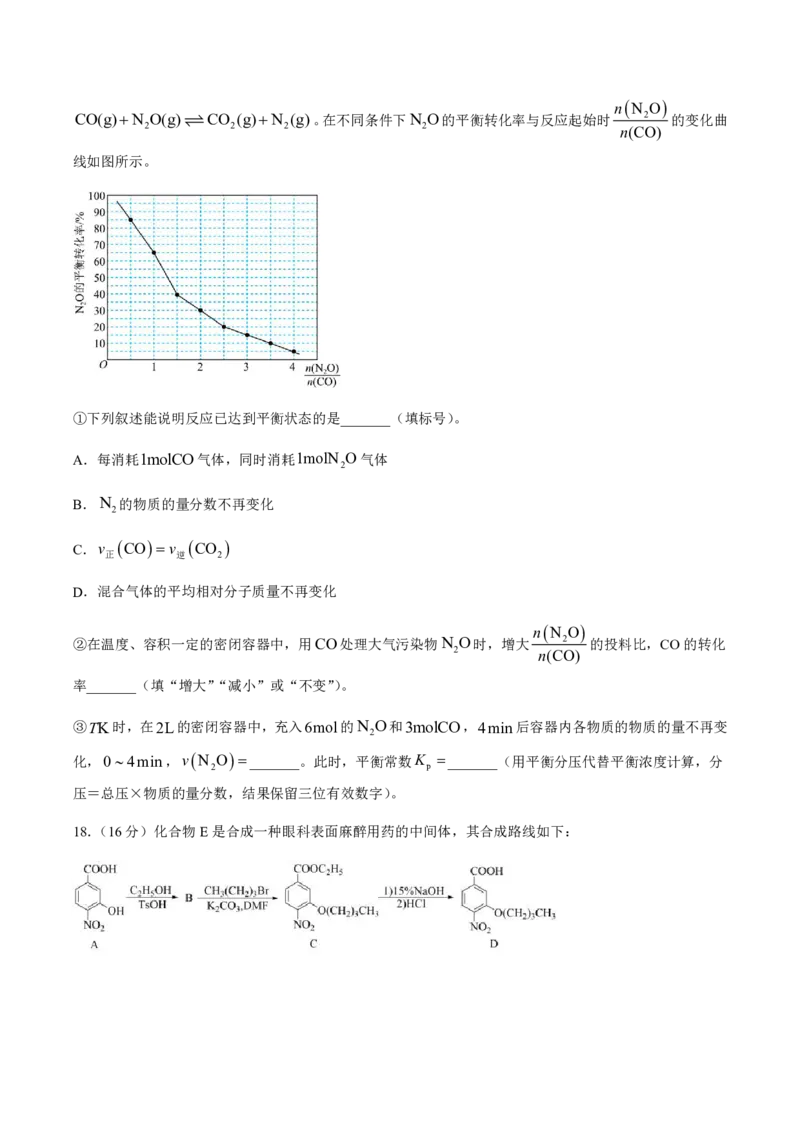
(3)TK时,在总压为100kPa的恒容密闭容器中,充入一定量的CO(g)和N O(g),发生反应
2
n N O
CO(g)N O(g)CO (g)N (g)。在不同条件下N O的平衡转化率与反应起始时 2 的变化曲
2 2 2 2
n(CO)
线如图所示。
①下列叙述能说明反应已达到平衡状态的是_______(填标号)。
A.每消耗1molCO气体,同时消耗1molN O气体
2
B.N 的物质的量分数不再变化
2
C.v CO v CO
正 逆 2
D.混合气体的平均相对分子质量不再变化
n N O
②在温度、容积一定的密闭容器中,用CO处理大气污染物N O时,增大 2 的投料比,CO的转化
2
n(CO)
率_______(填“增大”“减小”或“不变”)。
③TK时,在2L的密闭容器中,充入6mol的N O和3molCO,4min后容器内各物质的物质的量不再变
2
化,04min,v N O _______。此时,平衡常数K _______(用平衡分压代替平衡浓度计算,分
2 p
压=总压×物质的量分数,结果保留三位有效数字)。
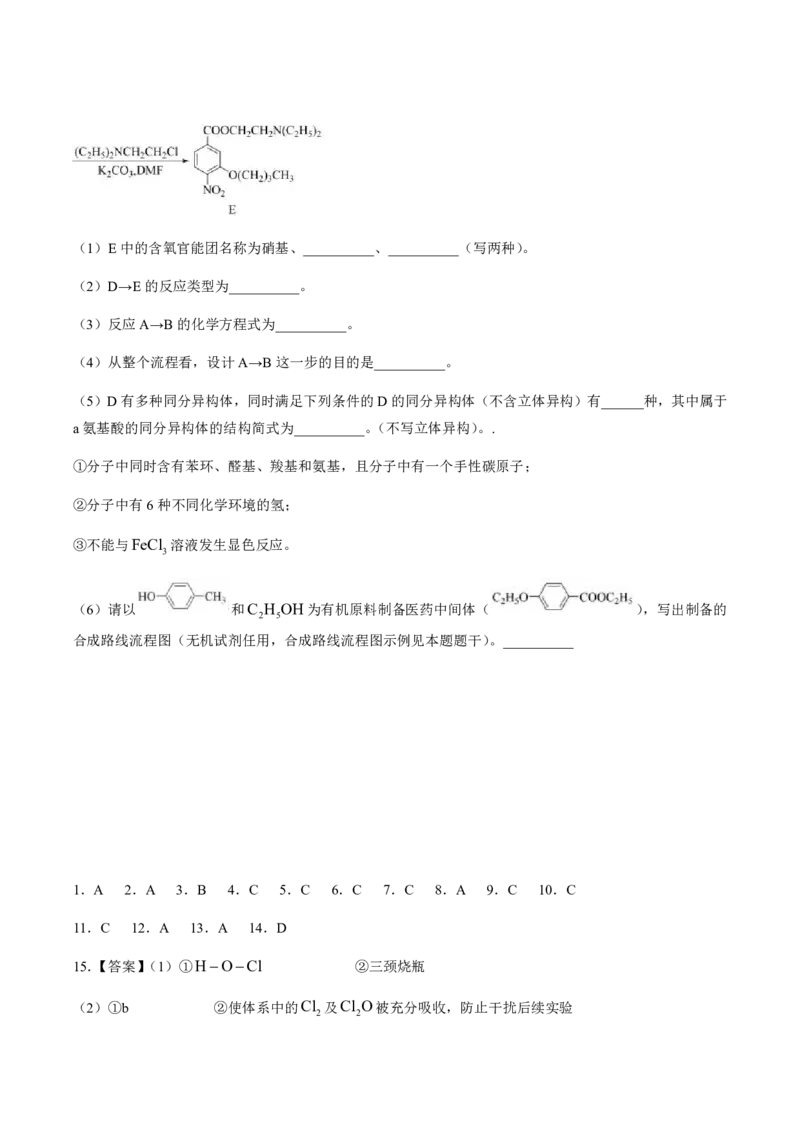
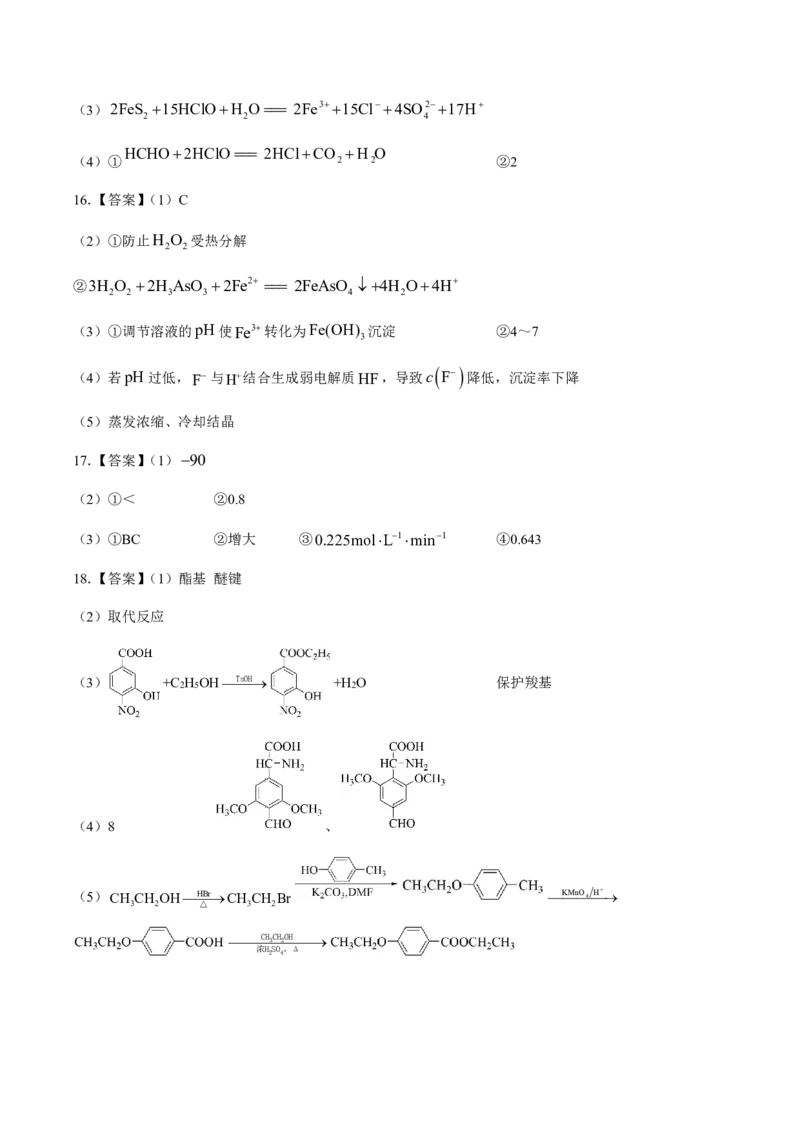
18.(16分)化合物E是合成一种眼科表面麻醉用药的中间体,其合成路线如下:(1)E中的含氧官能团名称为硝基、__________、__________(写两种)。
(2)D→E的反应类型为__________。
(3)反应A→B的化学方程式为__________。
(4)从整个流程看,设计A→B这一步的目的是__________。
(5)D有多种同分异构体,同时满足下列条件的D的同分异构体(不含立体异构)有______种,其中属于
a氨基酸的同分异构体的结构简式为__________。(不写立体异构)。.
①分子中同时含有苯环、醛基、羧基和氨基,且分子中有一个手性碳原子;
②分子中有6种不同化学环境的氢;
③不能与FeCl 溶液发生显色反应。
3
(6)请以 和C H OH为有机原料制备医药中间体( ),写出制备的
2 5
合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。__________
1.A 2.A 3.B 4.C 5.C 6.C 7.C 8.A 9.C 10.C
11.C 12.A 13.A 14.D
15.【答案】(1)①HOCl ②三颈烧瓶
(2)①b ②使体系中的Cl 及Cl O被充分吸收,防止干扰后续实验
2 2(3)2FeS 15HClOH O 2Fe315Cl4SO217H
2 2 4
HCHO2HClO 2HClCO H O
(4)① 2 2 ②2
16.【答案】(1)C
(2)①防止H O 受热分解
2 2
②3H O 2H AsO 2Fe2 2FeAsO 4H O4H
2 2 3 3 4 2
(3)①调节溶液的pH使Fe3转化为Fe(OH) 沉淀 ②4~7
3
(4)若pH过低,F与H结合生成弱电解质HF,导致c
F
降低,沉淀率下降
(5)蒸发浓缩、冷却结晶
17.【答案】(1)90
(2)①< ②0.8
(3)①BC ②增大 ③0.225molL1min1 ④0.643
18.【答案】(1)酯基 醚键
(2)取代反应
(3) +C H OHTsOH +H O 保护羧基
2 5 2
(4)8 、
(5)CH CH OHHBrCH CH Br KMnO4H+
3 2 △ 3 2
CH 3 CH 2 OH
浓HSO,Δ
2 4