文档内容
热点 04 化学微型实验
►命题趋势►解题策略►真题回眸►限时检测
考向一 无机物制备类实验
化学微型实验 考向二 有机物制备类实验
考向三 性质探究型实验
实验原理、实验技能和实验仪器是实验的三要素,在高考中常将“ 三要素”进行组合,形成综合性
强、能力层次要求高的实验题。综合性化学实验题(选择题)考查内容全面,从定性分析到定量分析、从
化学原理到实际操作、从无机物到有机物都有涉及,主要考查物质的检验、物质的制备、性质的验证、化
学性质递变规律与化学反应规律的研究、化学常见仪器的使用、物质的分离除杂提纯过程中的方法、试剂
的选择与操作、实验方案的设计与评价等内容。
预计2024年高考综合实验选择题,将结合文字叙述、图表数据、实验装置,探究内容上主要取材于教
材实验、日常生活和社会热点问题等,考察物质的制备、检验、鉴别等。
【策略1】熟悉以气体制备为主线的综合实验
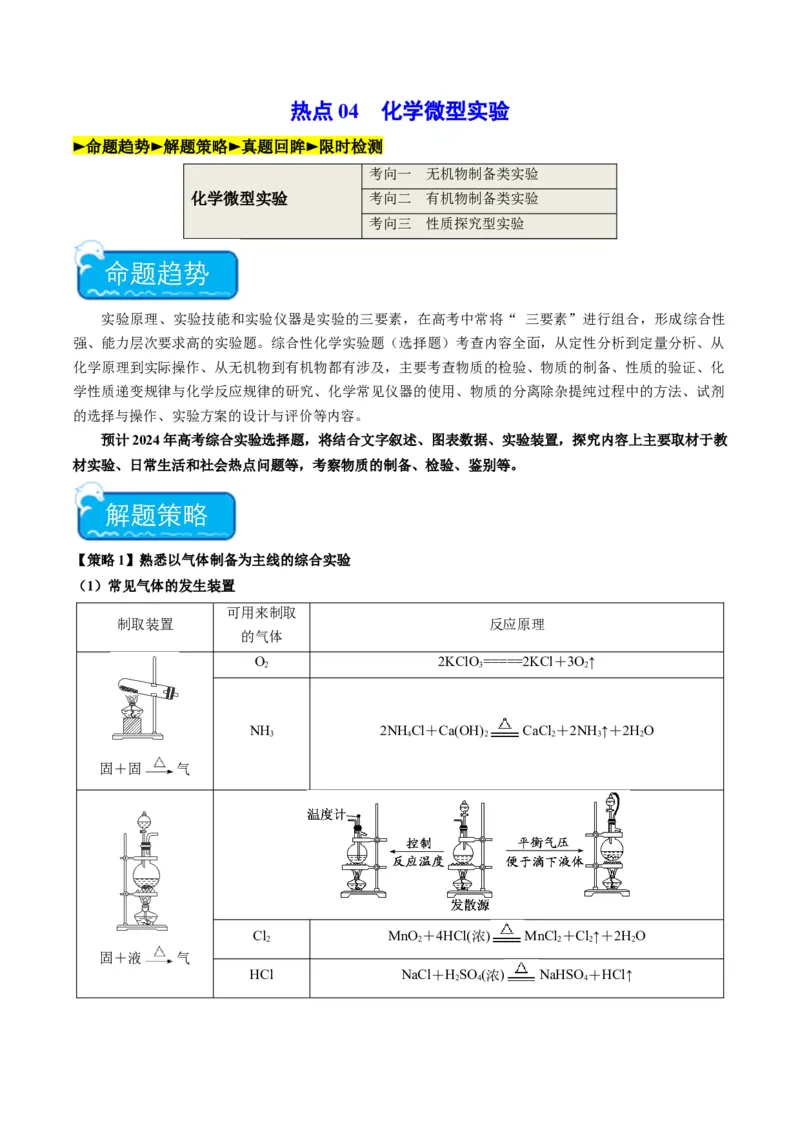
(1)常见气体的发生装置
可用来制取
制取装置 反应原理
的气体
O 2KClO=====2KCl+3O↑
2 3 2
NH 2NH Cl+Ca(OH) CaCl +2NH ↑+2HO
3 4 2 2 3 2
固+固 气
Cl MnO +4HCl(浓) MnCl +Cl↑+2HO
2 2 2 2 2
固+液 气
HCl NaCl+HSO (浓) NaHSO+HCl↑
2 4 4H 2H++Zn===H ↑+Zn2+
2 2
CO CaCO +2HCl===CaCl +CO↑+HO
2 3 2 2 2
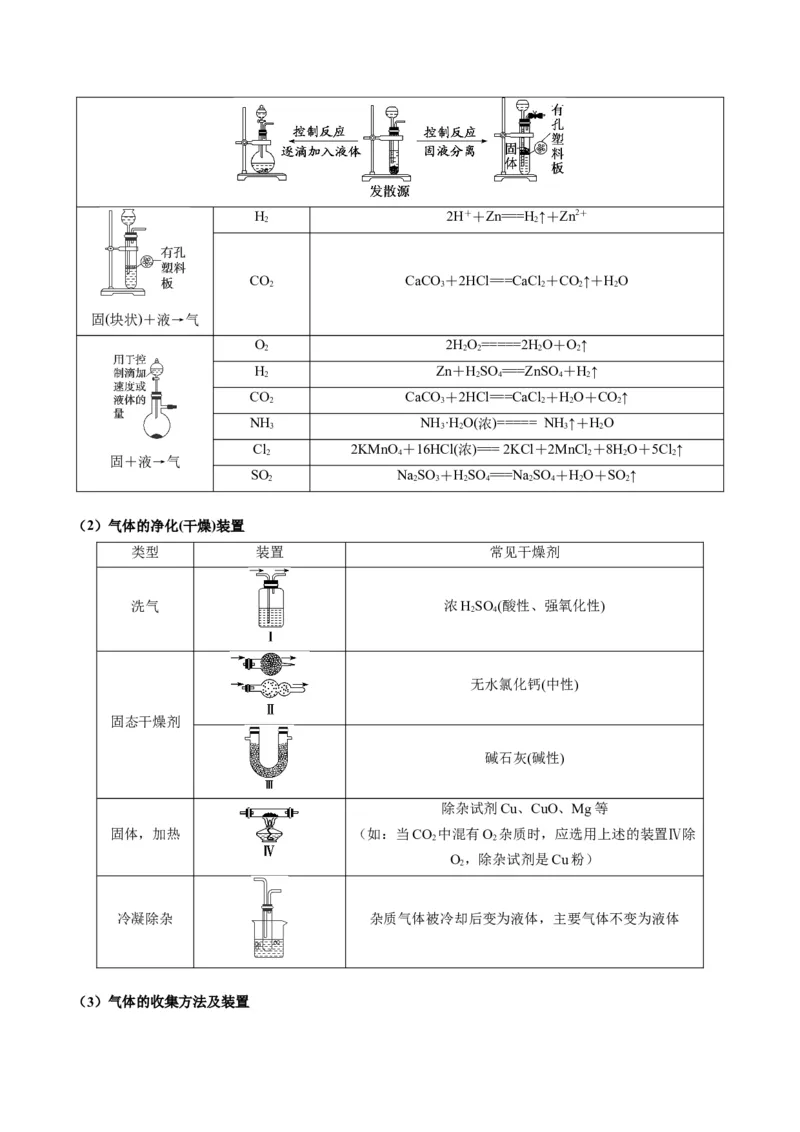
固(块状)+液→气
O 2HO=====2HO+O↑
2 2 2 2 2
H Zn+HSO ===ZnSO +H↑
2 2 4 4 2
CO CaCO +2HCl===CaCl +HO+CO↑
2 3 2 2 2
NH NH ·H O(浓)===== NH ↑+HO
3 3 2 3 2
Cl 2KMnO +16HCl(浓)=== 2KCl+2MnCl +8HO+5Cl↑
2 4 2 2 2
固+液→气
SO NaSO +HSO ===Na SO +HO+SO ↑
2 2 3 2 4 2 4 2 2
(2)气体的净化(干燥)装置
类型 装置 常见干燥剂
洗气 浓HSO (酸性、强氧化性)
2 4
无水氯化钙(中性)
固态干燥剂
碱石灰(碱性)
除杂试剂Cu、CuO、Mg等
固体,加热 (如:当CO 中混有O 杂质时,应选用上述的装置Ⅳ除
2 2
O,除杂试剂是Cu粉)
2
冷凝除杂 杂质气体被冷却后变为液体,主要气体不变为液体
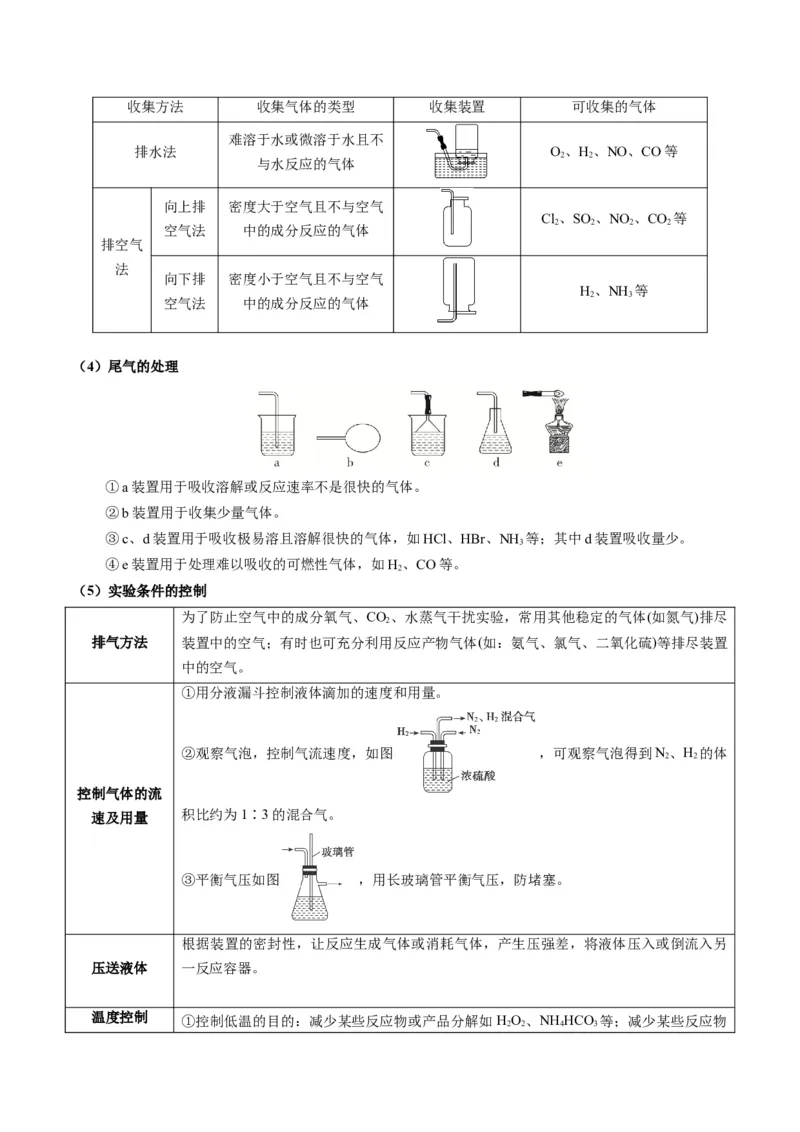
(3)气体的收集方法及装置收集方法 收集气体的类型 收集装置 可收集的气体
难溶于水或微溶于水且不
排水法 O、H、NO、CO等
2 2
与水反应的气体
向上排 密度大于空气且不与空气
Cl、SO 、NO 、CO 等
2 2 2 2
空气法 中的成分反应的气体
排空气
法
向下排 密度小于空气且不与空气
H、NH 等
2 3
空气法 中的成分反应的气体
(4)尾气的处理
①a装置用于吸收溶解或反应速率不是很快的气体。
②b装置用于收集少量气体。
③c、d装置用于吸收极易溶且溶解很快的气体,如HCl、HBr、NH 等;其中d装置吸收量少。
3
④e装置用于处理难以吸收的可燃性气体,如H、CO等。
2
(5)实验条件的控制
为了防止空气中的成分氧气、CO 、水蒸气干扰实验,常用其他稳定的气体(如氮气)排尽
2
排气方法 装置中的空气;有时也可充分利用反应产物气体(如:氨气、氯气、二氧化硫)等排尽装置
中的空气。
①用分液漏斗控制液体滴加的速度和用量。
②观察气泡,控制气流速度,如图 ,可观察气泡得到N 、H 的体
2 2
控制气体的流
速及用量 积比约为1∶3的混合气。
③平衡气压如图 ,用长玻璃管平衡气压,防堵塞。
根据装置的密封性,让反应生成气体或消耗气体,产生压强差,将液体压入或倒流入另
压送液体 一反应容器。
温度控制 ①控制低温的目的:减少某些反应物或产品分解如 HO 、NH HCO 等;减少某些反应物
2 2 4 3或产品挥发,如盐酸、氨水等;防止某物质水解,避免副反应发生等。
②采取加热的目的:加快反应速率或使平衡移动,加速溶解等。
③常考温度控制方式:
a.水浴加热:均匀加热,反应温度100 ℃以下。
b.油浴加热:均匀加热,反应温度100~260 ℃。
c.冰水冷却:使某物质液化、降低产物的溶解度;减少其他副反应,提高产品纯度
等。
d.保温:如中和反应反应热测定时,两烧杯之间填泡沫,真空双层玻璃容器等。
(6)有关沉淀的洗涤操作与规范解答
(1)若滤渣是所需的物质,洗涤的目的是除去其表面的可溶性杂质,得到更纯净的
沉淀物。
洗涤沉淀的目的
(2)若滤液是所需的物质,洗涤的目的是洗涤过滤所得到的滤渣,把有用的物质如
目标产物尽可能洗出来。
(1)蒸馏水:主要适用于除去沉淀吸附的可溶性杂质。
(2)冷水:除去沉淀表面的可溶性杂质,降低沉淀在水中的溶解度而减少沉淀损
失。
常用洗涤剂
(3)沉淀的饱和溶液:减小沉淀的溶解。
(4)有机溶剂(酒精、乙醚等):适用于易溶于水的固体,既减少了固体溶解,又利
用有机溶剂的挥发性,除去固体表面的水分,产品易干燥。
(1)检验沉淀是否完全的答题模板:
静置,取上层清液→加沉淀剂→有无沉淀→结论
(2)沉淀洗涤的答题模板:
注洗涤液(沿玻璃棒向漏斗中注入洗涤液)→标准(使洗涤液完全浸没沉淀或晶
三套答题模板
体)→重复(待洗涤液流尽后,重复操作2~3次)
(3)检验沉淀是否洗净的答题模板:
取样(取少量最后一次洗涤液于一洁净的试管中)→加试剂[加入××试剂(必要时加
热,如检验NH)]→现象(不产生××沉淀、溶液不变××色或不产生××气体)→结论(说明
沉淀已经洗涤干净)
【策略2】掌握有机物制备的实验装置和提纯方法
(1)熟悉常用仪器(2)熟悉常用装置
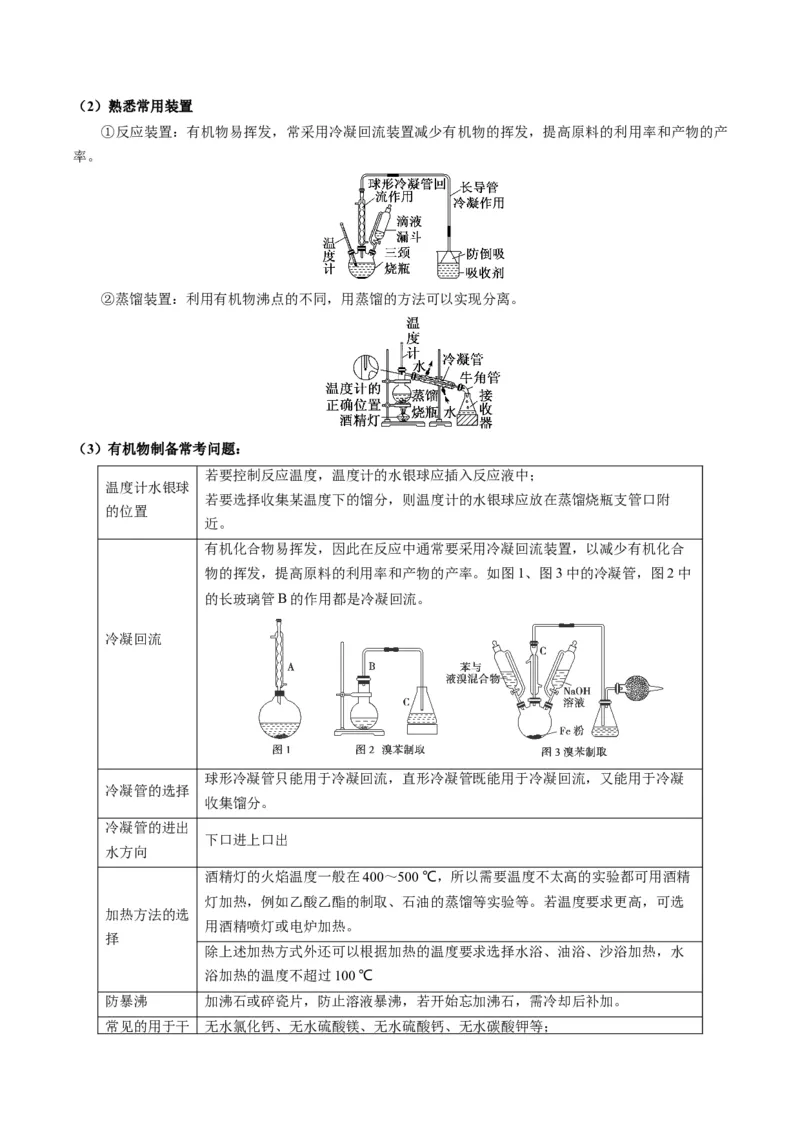
①反应装置:有机物易挥发,常采用冷凝回流装置减少有机物的挥发,提高原料的利用率和产物的产
率。
②蒸馏装置:利用有机物沸点的不同,用蒸馏的方法可以实现分离。
(3)有机物制备常考问题:
若要控制反应温度,温度计的水银球应插入反应液中;
温度计水银球
若要选择收集某温度下的馏分,则温度计的水银球应放在蒸馏烧瓶支管口附
的位置
近。
有机化合物易挥发,因此在反应中通常要采用冷凝回流装置,以减少有机化合
物的挥发,提高原料的利用率和产物的产率。如图1、图3中的冷凝管,图2中
的长玻璃管B的作用都是冷凝回流。
冷凝回流
球形冷凝管只能用于冷凝回流,直形冷凝管既能用于冷凝回流,又能用于冷凝
冷凝管的选择
收集馏分。
冷凝管的进出
下口进上口出
水方向
酒精灯的火焰温度一般在400~500 ℃,所以需要温度不太高的实验都可用酒精
灯加热,例如乙酸乙酯的制取、石油的蒸馏等实验等。若温度要求更高,可选
加热方法的选
用酒精喷灯或电炉加热。
择
除上述加热方式外还可以根据加热的温度要求选择水浴、油浴、沙浴加热,水
浴加热的温度不超过100 ℃
防暴沸 加沸石或碎瓷片,防止溶液暴沸,若开始忘加沸石,需冷却后补加。
常见的用于干 无水氯化钙、无水硫酸镁、无水硫酸钙、无水碳酸钾等;燥有机物的药
品
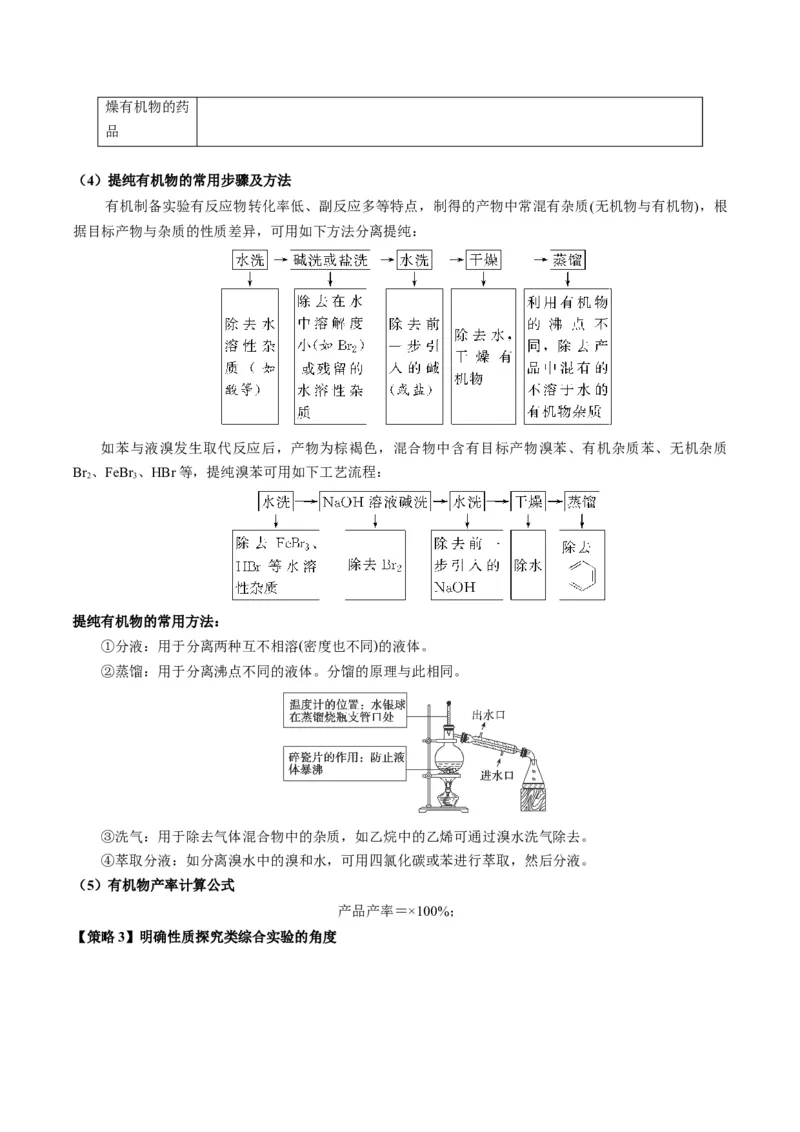
(4)提纯有机物的常用步骤及方法
有机制备实验有反应物转化率低、副反应多等特点,制得的产物中常混有杂质(无机物与有机物),根
据目标产物与杂质的性质差异,可用如下方法分离提纯:
如苯与液溴发生取代反应后,产物为棕褐色,混合物中含有目标产物溴苯、有机杂质苯、无机杂质
Br 、FeBr 、HBr等,提纯溴苯可用如下工艺流程:
2 3
提纯有机物的常用方法:
①分液:用于分离两种互不相溶(密度也不同)的液体。
②蒸馏:用于分离沸点不同的液体。分馏的原理与此相同。
③洗气:用于除去气体混合物中的杂质,如乙烷中的乙烯可通过溴水洗气除去。
④萃取分液:如分离溴水中的溴和水,可用四氯化碳或苯进行萃取,然后分液。
(5)有机物产率计算公式
产品产率=×100%;
【策略3】明确性质探究类综合实验的角度(1)物质氧化性、还原性及其强弱的判断。
如探究SO 具有还原性的方法是将气体通入酸性KMnO 溶液中,通过观察酸性KMnO 溶液是否褪色
2 4 4
来说明;如探究Fe3+的氧化性强于I 时,可利用FeCl 与淀粉KI溶液反应,通过溶液变蓝色来说明Fe3+的
2 3
氧化性强于I。
2
(2)验证同周期、同主族元素性质的递变规律.
一般通过设计比较元素金属性、非金属性强弱的实验来完成。如通过比较Mg、Al与同浓度盐酸反应
产生H 的快慢来说明Mg、Al的活泼性顺序。
2
(3)电解质强弱的判断。
如探究化合物HA是弱电解质的方法是常温下配制NaA溶液,测pH,若pH>7,则说明HA为弱电解
质。
(4)物质酸性强弱的判断。
如探究碳酸和硅酸的酸性强弱,可利用相对强的酸制备相对弱的酸的反应原理,将 CO 气体通入
2
NaSiO 溶液,看是否有白色沉淀生成来判断。
2 3
(5)钢铁发生电化学腐蚀的规律探究。
可以通过控制钢铁是否与空气接触、所接触的电解质溶液的酸碱度、钢铁在腐蚀过程中体系内的气压
变化等设计实验,找出规律。
(6)热分解产物的性质探究、判断。
①难溶性碳酸盐 氧化物+CO;
2
②碳酸的酸式盐 碳酸的正盐+CO+HO;
2 2
③铵盐(NH NO 除外) NH +相应的酸(或酸性氧化物+HO);
4 3 3 2
④硝酸盐 金属(或金属氧化物、亚硝酸盐)+氮氧化物(NO或NO )+O;
2 2
⑤草酸晶体 CO+CO+HO。
2 2
考向一 无机物制备类综合实验
1.(2023·湖北·统考高考真题)利用如图所示的装置(夹持及加热装置略)制备高纯白磷的流程如下:下列操作错误的是
A.红磷使用前洗涤以除去表面杂质
B.将红磷转入装置,抽真空后加热外管以去除水和氧气
C.从a口通入冷凝水,升温使红磷转化
D.冷凝管外壁出现白磷,冷却后在氮气氛围下收集
考向二 有机物制备类综合实验
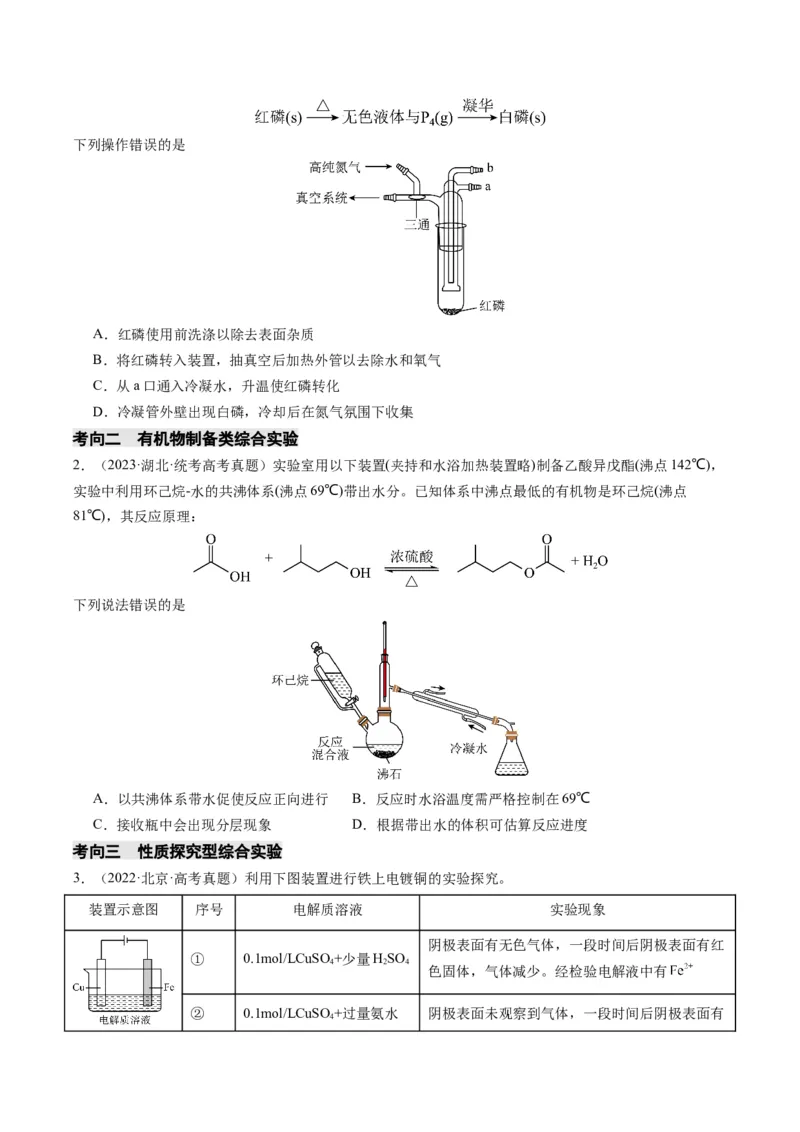
2.(2023·湖北·统考高考真题)实验室用以下装置(夹持和水浴加热装置略)制备乙酸异戊酯(沸点142℃),
实验中利用环己烷-水的共沸体系(沸点69℃)带出水分。已知体系中沸点最低的有机物是环己烷(沸点
81℃),其反应原理:
下列说法错误的是
A.以共沸体系带水促使反应正向进行 B.反应时水浴温度需严格控制在69℃
C.接收瓶中会出现分层现象 D.根据带出水的体积可估算反应进度
考向三 性质探究型综合实验
3.(2022·北京·高考真题)利用下图装置进行铁上电镀铜的实验探究。
装置示意图 序号 电解质溶液 实验现象
阴极表面有无色气体,一段时间后阴极表面有红
① 0.1mol/LCuSO +少量HSO
4 2 4
色固体,气体减少。经检验电解液中有
② 0.1mol/LCuSO +过量氨水 阴极表面未观察到气体,一段时间后阴极表面有
4致密红色固体。经检验电解液中无 元素
下列说法不正确的是
A.①中气体减少,推测是由于溶液中 减少,且 覆盖铁电极,阻碍 与铁接触
B.①中检测到 ,推测可能发生反应:
C.随阴极析出 ,推测②中溶液 减少, 平衡逆移
D.②中 生成 ,使得 比①中溶液的小, 缓慢析出,镀层更致密
4.(2022·湖南·高考真题)为探究 的性质,进行了如下实验( 和 溶液浓度均为
)。
实
操作与现象
验
① 在 水中滴加2滴 溶液,呈棕黄色;煮沸,溶液变红褐色。
在 溶液中滴加2滴 溶液,变红褐色;
②
再滴加 溶液,产生蓝色沉淀。
在 溶液中滴加2滴 溶液,变红褐色;
③
将上述混合液分成两份,一份滴加 溶液,无蓝色沉淀生成;
另一份煮沸,产生红褐色沉淀。
依据上述实验现象,结论不合理的是
A.实验①说明加热促进 水解反应
B.实验②说明 既发生了水解反应,又发生了还原反应
C.实验③说明 发生了水解反应,但没有发生还原反应
D.整个实验说明 对 的水解反应无影响,但对还原反应有影响
(建议用时:35分钟)
1.(2023·湖南株洲·统考一模)化学是一门以实验为基础的学科,某同学为探究FeCl 溶液的性质进行如
3
下实验,操作如图所示,根据实验现象,下列分析不正确的是A.①~④的变化中,有2处涉及氧化还原反应
B.向②后试管加入足量稀盐酸,沉淀部分溶解
C.若将FeCl 溶液滴加到NaS溶液中,产生的现象与图中①、②现象不相同
3 2
D.④中的现象与胶体的聚沉有关
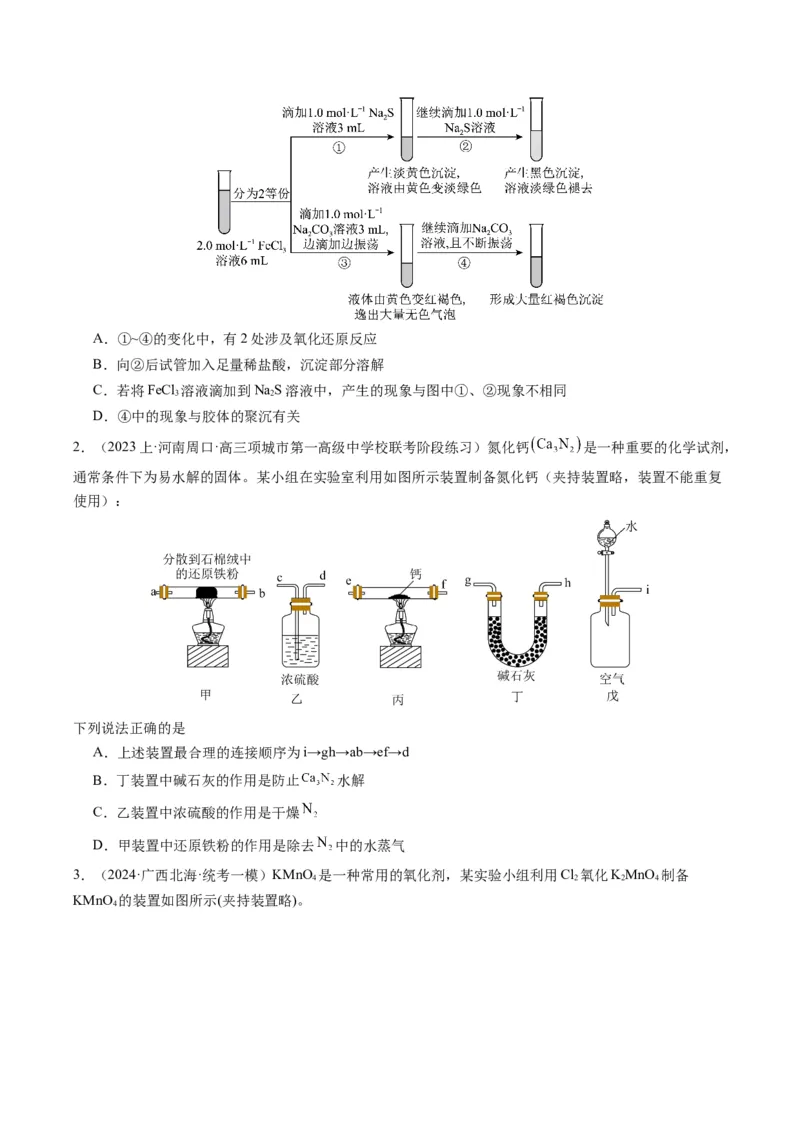
2.(2023上·河南周口·高三项城市第一高级中学校联考阶段练习)氮化钙 是一种重要的化学试剂,
通常条件下为易水解的固体。某小组在实验室利用如图所示装置制备氮化钙(夹持装置略,装置不能重复
使用):
下列说法正确的是
A.上述装置最合理的连接顺序为i→gh→ab→ef→d
B.丁装置中碱石灰的作用是防止 水解
C.乙装置中浓硫酸的作用是干燥
D.甲装置中还原铁粉的作用是除去 中的水蒸气
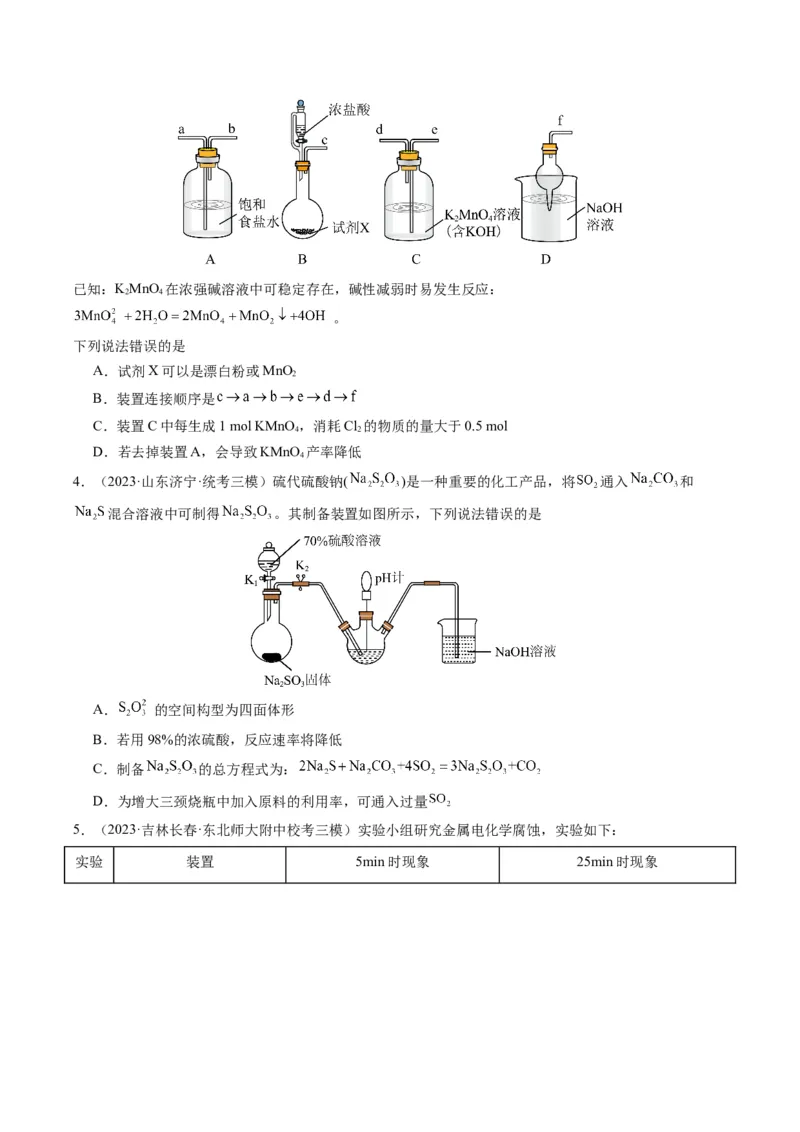
3.(2024·广西北海·统考一模)KMnO 是一种常用的氧化剂,某实验小组利用Cl 氧化KMnO 制备
4 2 2 4
KMnO 的装置如图所示(夹持装置略)。
4已知:KMnO 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
2 4
。
下列说法错误的是
A.试剂X可以是漂白粉或MnO
2
B.装置连接顺序是
C.装置C中每生成1 mol KMnO,消耗Cl 的物质的量大于0.5 mol
4 2
D.若去掉装置A,会导致KMnO 产率降低
4
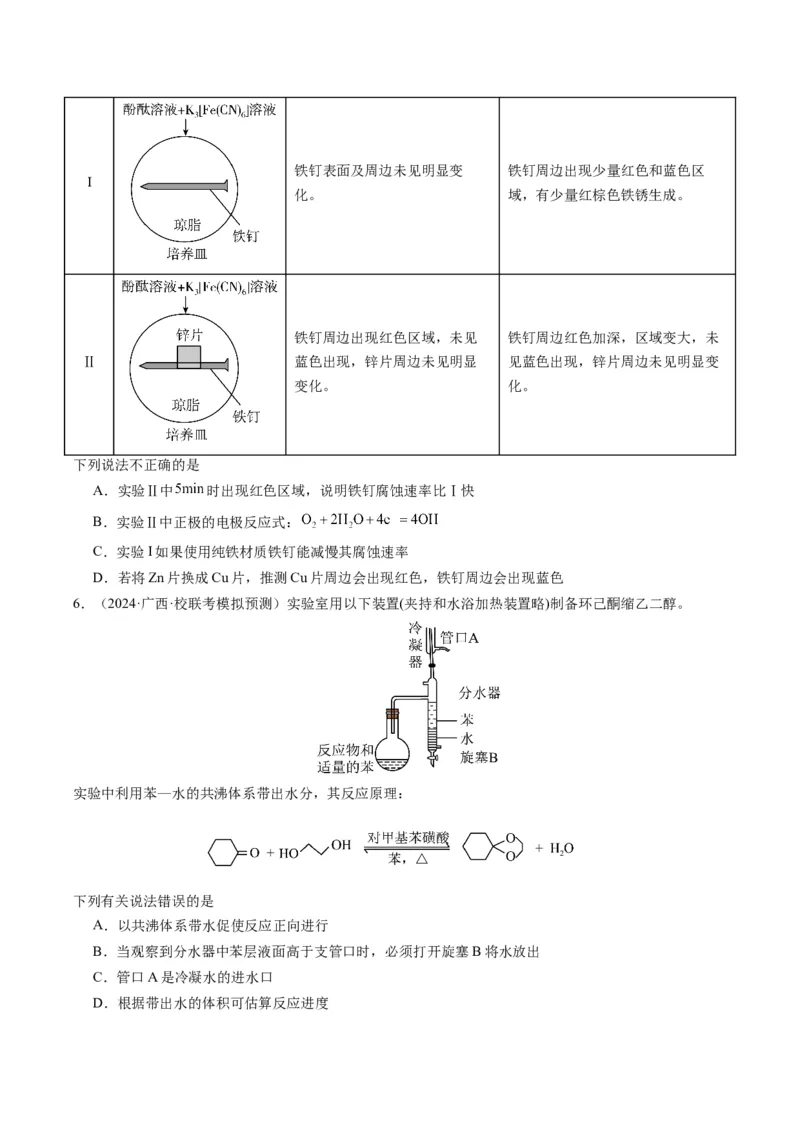
4.(2023·山东济宁·统考三模)硫代硫酸钠( )是一种重要的化工产品,将 通入 和
混合溶液中可制得 。其制备装置如图所示,下列说法错误的是
A. 的空间构型为四面体形
B.若用98%的浓硫酸,反应速率将降低
C.制备 的总方程式为:
D.为增大三颈烧瓶中加入原料的利用率,可通入过量
5.(2023·吉林长春·东北师大附中校考三模)实验小组研究金属电化学腐蚀,实验如下:
实验 装置 5min时现象 25min时现象铁钉表面及周边未见明显变 铁钉周边出现少量红色和蓝色区
I
化。 域,有少量红棕色铁锈生成。
铁钉周边出现红色区域,未见 铁钉周边红色加深,区域变大,未
Ⅱ 蓝色出现,锌片周边未见明显 见蓝色出现,锌片周边未见明显变
变化。 化。
下列说法不正确的是
A.实验Ⅱ中 时出现红色区域,说明铁钉腐蚀速率比Ⅰ快
B.实验Ⅱ中正极的电极反应式:
C.实验I如果使用纯铁材质铁钉能减慢其腐蚀速率
D.若将Zn片换成Cu片,推测Cu片周边会出现红色,铁钉周边会出现蓝色
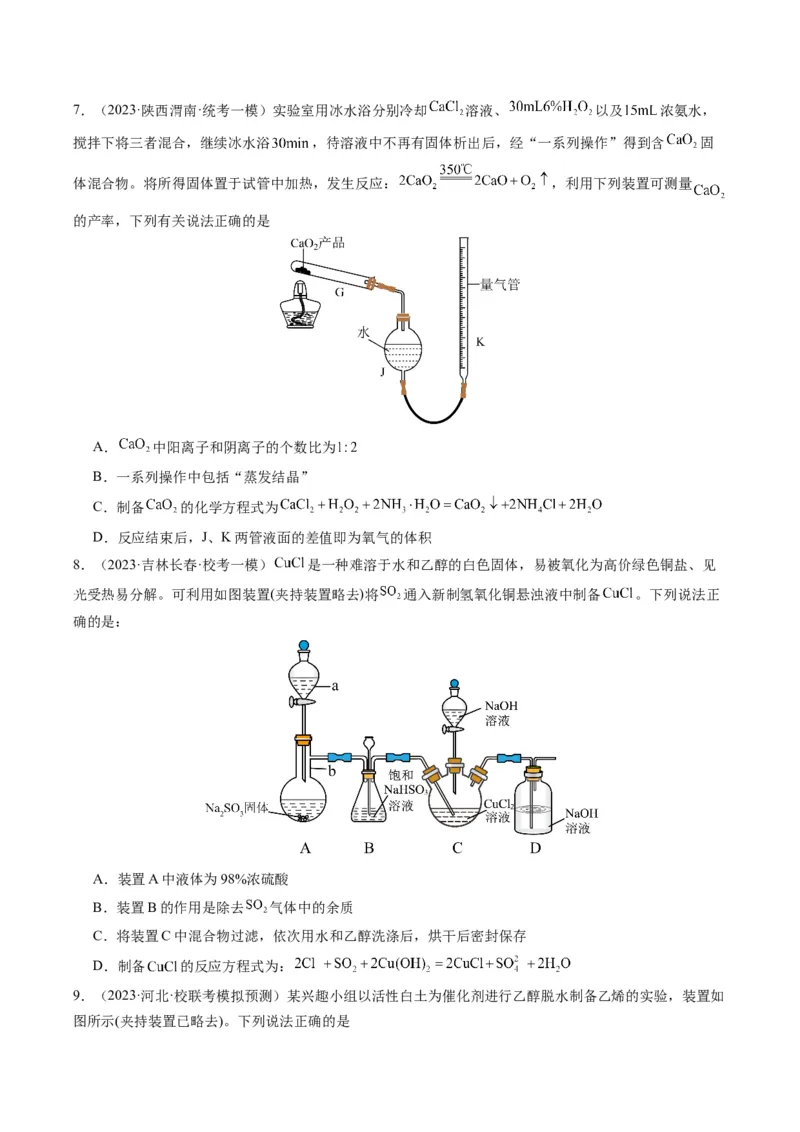
6.(2024·广西·校联考模拟预测)实验室用以下装置(夹持和水浴加热装置略)制备环己酮缩乙二醇。
实验中利用苯—水的共沸体系带出水分,其反应原理:
下列有关说法错误的是
A.以共沸体系带水促使反应正向进行
B.当观察到分水器中苯层液面高于支管口时,必须打开旋塞B将水放出
C.管口A是冷凝水的进水口
D.根据带出水的体积可估算反应进度7.(2023·陕西渭南·统考一模)实验室用冰水浴分别冷却 溶液、 以及 浓氨水,
搅拌下将三者混合,继续冰水浴 ,待溶液中不再有固体析出后,经“一系列操作”得到含 固
体混合物。将所得固体置于试管中加热,发生反应: ,利用下列装置可测量
的产率,下列有关说法正确的是
A. 中阳离子和阴离子的个数比为
B.一系列操作中包括“蒸发结晶”
C.制备 的化学方程式为
D.反应结束后,J、K两管液面的差值即为氧气的体积
8.(2023·吉林长春·校考一模) 是一种难溶于水和乙醇的白色固体,易被氧化为高价绿色铜盐、见
光受热易分解。可利用如图装置(夹持装置略去)将 通入新制氢氧化铜悬浊液中制备 。下列说法正
确的是:
A.装置A中液体为98%浓硫酸
B.装置B的作用是除去 气体中的余质
C.将装置C中混合物过滤,依次用水和乙醇洗涤后,烘干后密封保存
D.制备 的反应方程式为:
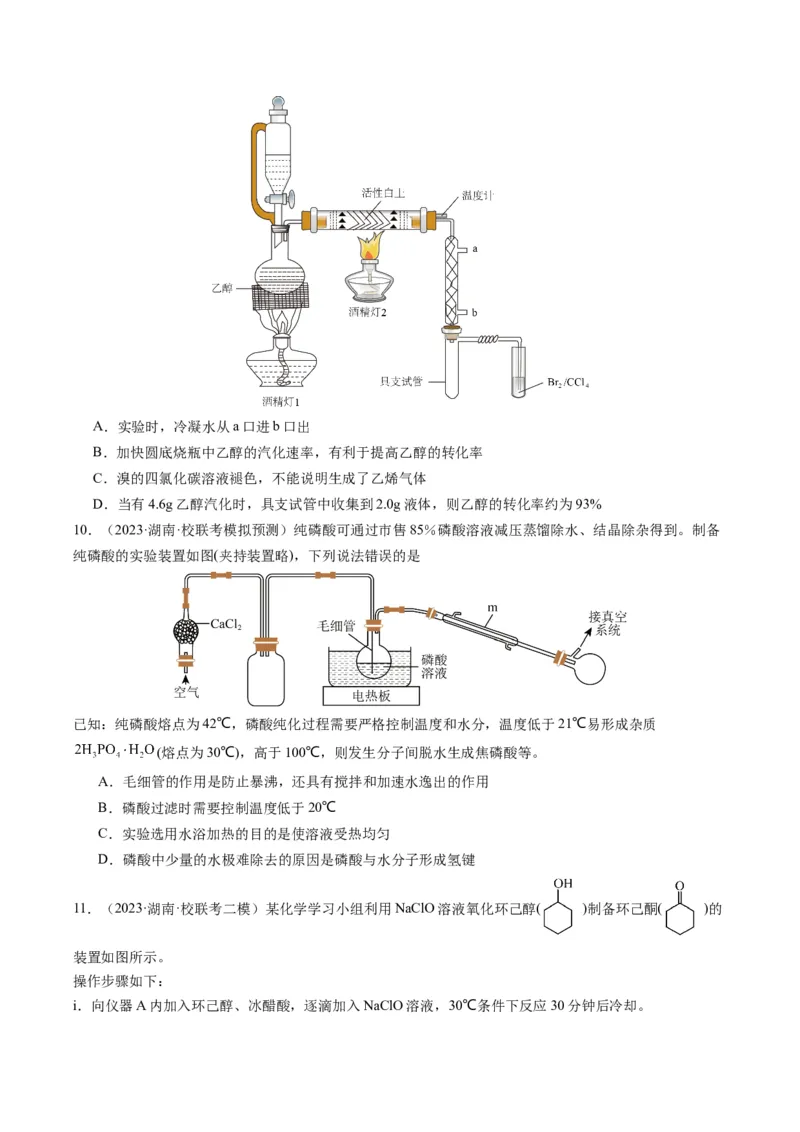
9.(2023·河北·校联考模拟预测)某兴趣小组以活性白土为催化剂进行乙醇脱水制备乙烯的实验,装置如
图所示(夹持装置已略去)。下列说法正确的是A.实验时,冷凝水从a口进b口出
B.加快圆底烧瓶中乙醇的汽化速率,有利于提高乙醇的转化率
C.溴的四氯化碳溶液褪色,不能说明生成了乙烯气体
D.当有4.6g乙醇汽化时,具支试管中收集到2.0g液体,则乙醇的转化率约为93%
10.(2023·湖南·校联考模拟预测)纯磷酸可通过市售85%磷酸溶液减压蒸馏除水、结晶除杂得到。制备
纯磷酸的实验装置如图(夹持装置略),下列说法错误的是
已知:纯磷酸熔点为42℃,磷酸纯化过程需要严格控制温度和水分,温度低于21℃易形成杂质
(熔点为30℃),高于100℃,则发生分子间脱水生成焦磷酸等。
A.毛细管的作用是防止暴沸,还具有搅拌和加速水逸出的作用
B.磷酸过滤时需要控制温度低于20℃
C.实验选用水浴加热的目的是使溶液受热均匀
D.磷酸中少量的水极难除去的原因是磷酸与水分子形成氢键
11.(2023·湖南·校联考二模)某化学学习小组利用NaClO溶液氧化环己醇( )制备环己酮( )的
装置如图所示。
操作步骤如下:
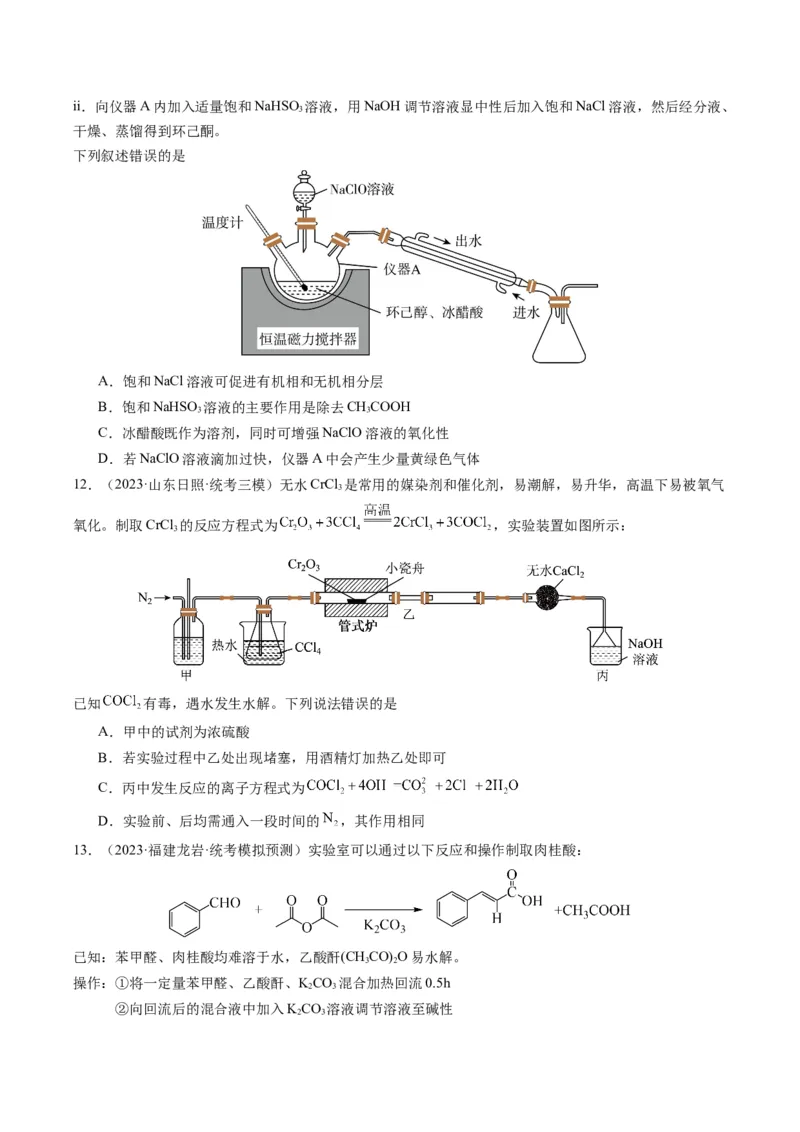
i.向仪器A内加入环己醇、冰醋酸,逐滴加入NaClO溶液,30℃条件下反应30分钟后冷却。ii.向仪器A内加入适量饱和NaHSO 溶液,用NaOH调节溶液显中性后加入饱和NaCl溶液,然后经分液、
3
干燥、蒸馏得到环己酮。
下列叙述错误的是
A.饱和NaCl溶液可促进有机相和无机相分层
B.饱和NaHSO 溶液的主要作用是除去CHCOOH
3 3
C.冰醋酸既作为溶剂,同时可增强NaClO溶液的氧化性
D.若NaClO溶液滴加过快,仪器A中会产生少量黄绿色气体
12.(2023·山东日照·统考三模)无水CrCl 是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气
3
氧化。制取CrCl 的反应方程式为 ,实验装置如图所示:
3
已知 有毒,遇水发生水解。下列说法错误的是
A.甲中的试剂为浓硫酸
B.若实验过程中乙处出现堵塞,用酒精灯加热乙处即可
C.丙中发生反应的离子方程式为
D.实验前、后均需通入一段时间的 ,其作用相同
13.(2023·福建龙岩·统考模拟预测)实验室可以通过以下反应和操作制取肉桂酸:
已知:苯甲醛、肉桂酸均难溶于水,乙酸酐(CHCO) O易水解。
3 2
操作:①将一定量苯甲醛、乙酸酐、KCO 混合加热回流0.5h
2 3
②向回流后的混合液中加入KCO 溶液调节溶液至碱性
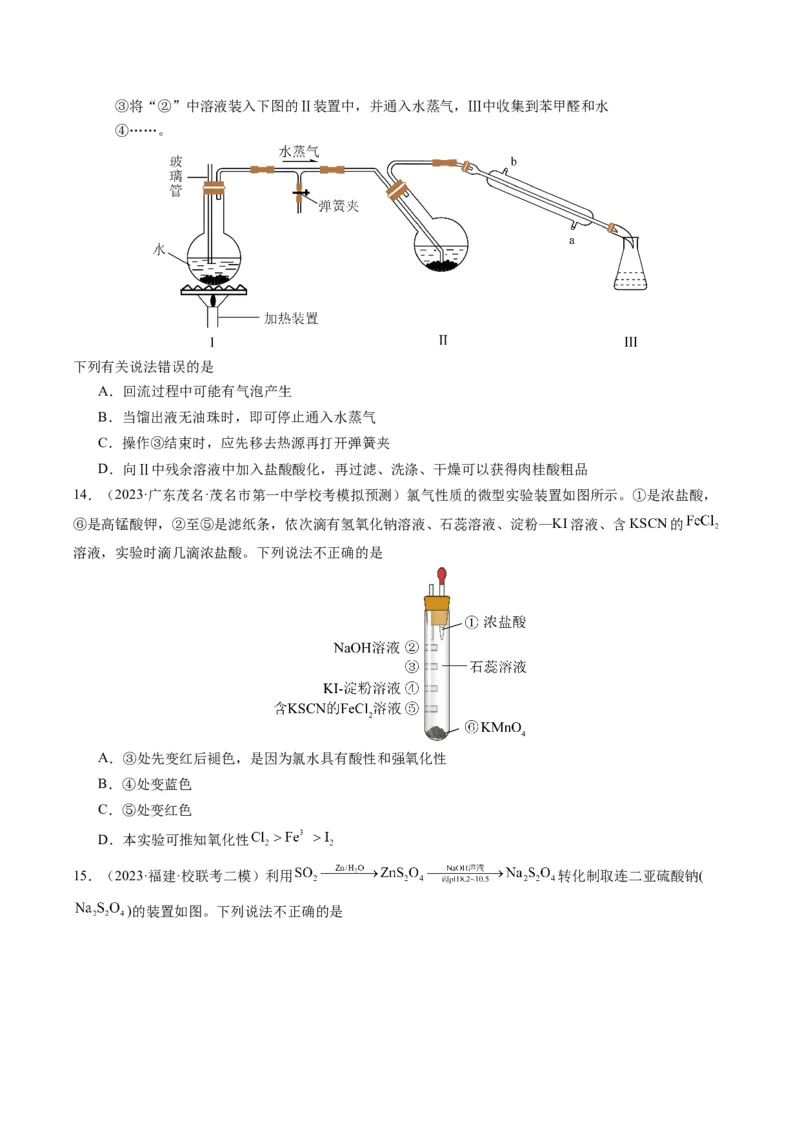
2 3③将“②”中溶液装入下图的Ⅱ装置中,并通入水蒸气,Ⅲ中收集到苯甲醛和水
④……。
下列有关说法错误的是
A.回流过程中可能有气泡产生
B.当馏出液无油珠时,即可停止通入水蒸气
C.操作③结束时,应先移去热源再打开弹簧夹
D.向Ⅱ中残余溶液中加入盐酸酸化,再过滤、洗涤、干燥可以获得肉桂酸粗品
14.(2023·广东茂名·茂名市第一中学校考模拟预测)氯气性质的微型实验装置如图所示。①是浓盐酸,
⑥是高锰酸钾,②至⑤是滤纸条,依次滴有氢氧化钠溶液、石蕊溶液、淀粉—KI溶液、含KSCN的
溶液,实验时滴几滴浓盐酸。下列说法不正确的是
A.③处先变红后褪色,是因为氯水具有酸性和强氧化性
B.④处变蓝色
C.⑤处变红色
D.本实验可推知氧化性
15.(2023·福建·校联考二模)利用 转化制取连二亚硫酸钠(
)的装置如图。下列说法不正确的是A.单向阀的作用是防倒吸
B.先通入 至悬浊液变澄清,再打开滴液漏斗旋塞
C.NaOH溶液不宜加入过多的原因是防止 水解
D.上述反应液经过滤,在冷却搅拌下加入一定量NaCl的作用是提高产率