文档内容
热点 04 无机化工微流程
(建议用时:35分钟)
【真题再现】
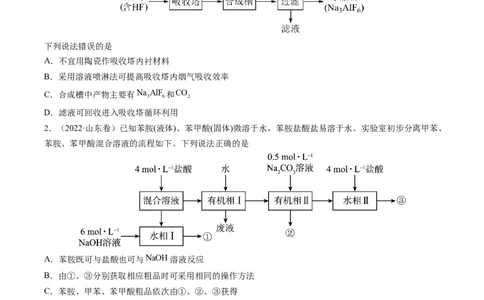
1.(2022·湖南卷)铝电解厂烟气净化的一种简单流程如下:
下列说法错误的是
A.不宜用陶瓷作吸收塔内衬材料
B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有Na AlF 和CO
3 6 2
D.滤液可回收进入吸收塔循环利用
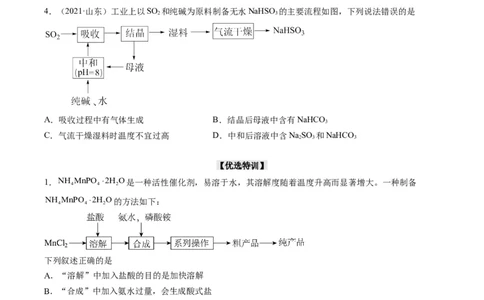
2.(2022·山东卷)已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步分离甲苯、
苯胺、苯甲酸混合溶液的流程如下。下列说法正确的是
A.苯胺既可与盐酸也可与NaOH溶液反应
B.由①、③分别获取相应粗品时可采用相同的操作方法
C.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
D.①、②、③均为两相混合体系
3.(2022·山东卷)高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂质)为主
要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。Fe(OH) Cu(OH) Zn(OH)
3 2 2
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是A.固体X主要成分是Fe(OH) 和S;金属M为Zn
3
B.浸取时,增大O 压强可促进金属离子浸出
2
C.中和调pH的范围为3.2~4.2
D.还原时,增大溶液酸度有利于Cu的生成
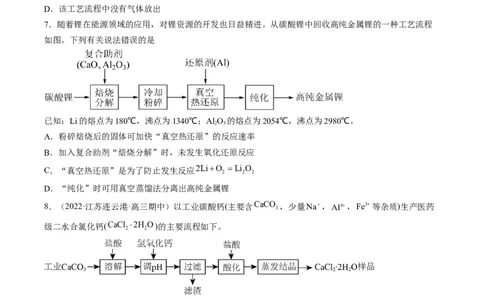
4.(2021·山东)工业上以SO 和纯碱为原料制备无水NaHSO 的主要流程如图,下列说法错误的是
2 3
A.吸收过程中有气体生成 B.结晶后母液中含有NaHCO
3
C.气流干燥湿料时温度不宜过高 D.中和后溶液中含NaSO 和NaHCO
2 3 3
【优选特训】
1.NH MnPO 2H O是一种活性催化剂,易溶于水,其溶解度随着温度升高而显著增大。一种制备
4 4 2
NH MnPO 2H O的方法如下:
4 4 2
下列叙述正确的是
A.“溶解”中加入盐酸的目的是加快溶解
B.“合成”中加入氨水过量,会生成酸式盐
C.“系列操作”需要酒精灯、蒸馏烧瓶等仪器
D.采用“重结晶”可提纯产品
2.溴化钙可用作镇静剂、食物保存剂等。通过下列实验流程可制备少量CaBr 6H O。下列说法不正确的
2 2
是
A.空气吹出法是海水提溴最成熟的工业方法B.步骤①可用热水浴加热
C.步骤②中尿素作氧化剂 D.步骤④中活性炭作脱色剂3.(2022·山东日照·模拟预测)过氧化钙
CaO
是一种白色固体,能潮解,难溶于水,不溶于醇类,常
2
用作杀菌消毒剂。一种工业生产过氧化钙
CaO
过程如下图所示。
2
下列说法错误的是
A.“冷水浴反应”中H O 的作用是氧化剂
2 2
B.母液经处理后可返回“冷水浴反应”循环利用
C.操作2需要用到坩埚、酒精灯、玻璃棒
D.“洗涤”产品需依次用蒸馏水、无水乙醇洗涤,其中乙醇洗涤的目的是为了除去表面的水分
4.(2022·北京·北师大实验中学高三期中)工业废铁的综合利用,是节约资源的重要组成部分。下图是以
废铁块生产净水剂聚合氯化铁和高铁酸钠的流程。
下列说法不正确的是
A.①过程可以用盐酸
B.②氧化的目的是将Fe2+转化为Fe3+
C.为使③中Fe3+的水解程度增大,可将溶液加热
D.④中阳极的电极反应式为Fe-6e-+4H O=FeO2+8H+
2 4
5.(2022·福建·莆田一中高三阶段练习)徐竞等科研人员以永安洪田镇的银精矿(主要成分是Ag和Ag S)
2
为原料,采用浮选-氰化浸出工艺路线提取银,其部分工艺流程如图所示。
下列说法错误的是
A.反应①中的O 主要是氧化矿浆中的Ag
2
B.反应①和②充分反应后均要进行过滤
C.反应②的离子方程式为:2AgZn2AgZn2
D.电解精炼时粗银应当做阳极
6.(2022·湖北·宜城市第一中学高三期中)碳酸锰 (MnCO )是制造电信器材软磁铁氧体,合成二氧化锰和
3
制造其他锰盐的原料。利用软锰矿(主要成分是MnO ,含有少量的Fe O、Al O、SiO 等)制备碳酸锰的工艺
2 2 3 2 3 2流程如下。下列说法错误的是
A.“浸取”时发生反应的离子方程式为MnO +2Fe2++4H+ Mn2++2Fe3++2H O
2 2
B.“转化”的主要目的是将滤液中的Fe2+氧化为Fe3+,以便后续操作除去
C.滤渣2的主要成分为Fe(OH)、Al(OH)
3 3
D.该工艺流程中没有气体放出
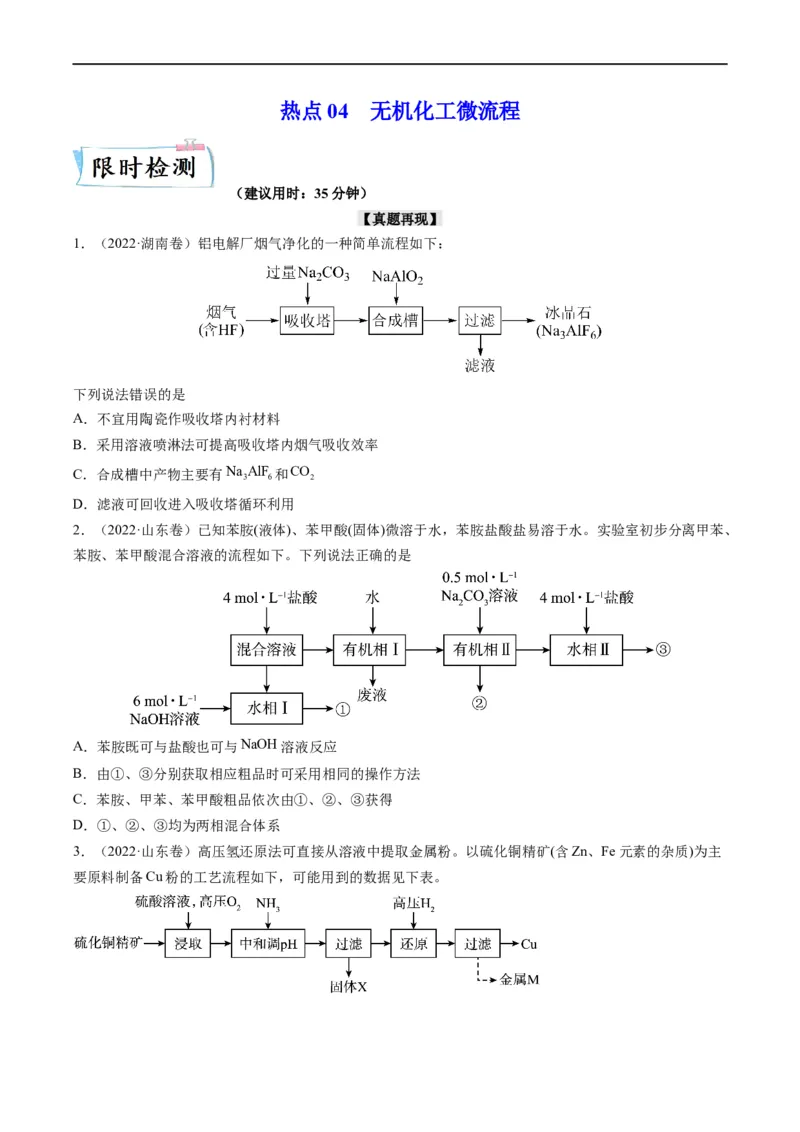
7.随着锂在能源领域的应用,对锂资源的开发也日益精进。从碳酸锂中回收高纯金属锂的一种工艺流程
如图。下列有关说法错误的是
已知:Li的熔点为180℃,沸点为1340℃;Al O 的熔点为2054℃,沸点为2980℃。
2 3
A.粉碎焙烧后的固体可加快“真空热还原”的反应速率
B.加入复合助剂“焙烧分解”时,未发生氧化还原反应
C.“真空热还原”是为了防止发生反应2LiO Li O
2 2 2
D.“纯化”时可用真空蒸馏法分离出高纯金属锂
8.(2022·江苏连云港·高三期中)以工业碳酸钙(主要含CaCO
3
,少量Na,Al3,Fe3等杂质)生产医药
级二水合氯化钙(CaCl 2H O)的主要流程如下。
2 2
下列说法不正确的是
A.“溶解”时将CaCO 粉碎并不断搅拌,有利于加快反应速率
3
B.“过滤”后所得到的滤渣,其主要成分是CaOH 、FeOH
2 3
C.“酸化”时加盐酸可以除去溶液中少量CaOH 和防止吸收空气中CO
2 2
D.制得CaCl 2H O样品中n
Ca2+
:n
Cl-
<1:2
2 2
9.(2022·山东烟台·高三期中)一种利用玻璃窑炉替换下的锆废砖(主要成分ZrO、YO、CaO等)提纯成
2 2 3
分ZrO 和YO 的工艺流程如下。下列说法错误的是
2 2 3A.“酸化”过程中加入的硫酸、硫酸铵可用硝酸、硝酸铵代替
B.滤渣1主要成分为CaSO
4
C.“中和1”调节pH范围在4~5.5目的是沉淀锆离子
D.整个工艺过程中,硫酸铵可以实现循环利用
10.锑(Sb)可用作阻燃剂、电极材料、催化剂等物质的原材料。一种以灰锑矿(主要成分为Sb S ,还有
2 3
FeO,Al O ,MgO等)为原料提取锑的工艺如下:
2 3 2 3
下列说法不正确的是:
A.“水解”时可加入Na CO 粉末以促进水解
2 3
B.“还原”的目的是防止Fe3+在后续水解生成FeOH
,影响产品纯度
3
C.“滤液”中含有的主要金属阳离子有:Fe2+、Al3+、Mg2+
D.“溶浸”时Sb S 转化为SbCl ,发生反应的离子方程式为:Sb S Fe3+6Cl=2SbCl Fe2+3S
2 3 3 2 3 3
11.碳酸锂是制备高纯锂化合物和锂合金的主要原料,在玻璃和陶瓷制造、医药、有色金属冶炼、锂电池
电极材料等领域具有广阔的应用前景。某化学小组在实验室用含锂废渣(主要含LiO,还含有少量其他能
2
溶于盐酸的金属氧化物及少量碳单质)制备碳酸锂的流程如图所示:
下列说法错误的是
A.“浸渣”的主要成分是碳单质
B.“萃取”和“反萃取”均应在烧杯中进行
C.“蒸发浓缩”的目的之一是除去过量的HCl
D.“沉锂”后所得母液中含有NaCl
12.精炼铜工业中阳极泥的综合利用具有重要意义。从阳极泥中回收多种金属的流程如下。已知:分金液中含 AuCl ;分金渣的主要成分为AgCl;N H H O在反应中被氧化为N 。
4 2 4 2 2
下列说法不正确的是
A.“分铜”时加入NaCl的目的是降低银的浸出率
B.得到分金液的反应为:2AuClO7Cl 6H 2AuCl 3H O
3 4 2
C.得到分银液的反应为:AgCl2NH
3
AgNH
3
2
Cl
D.“滤液2”中含有大量的氨,可直接循环利用
13.实验室模拟以磷石膏(含CaSO 2H O及杂质Al O 、Fe O 等)为原料制取轻质CaCO ,流程如下:
4 2 2 3 2 3 3
下列说法错误的是
A.“浸取1”时,加快搅拌速率、不断升高温度均可提高CaSO 的转化率
4
B.“浸取1”时,应先通NH 再通CO ,滤液1中浓度最大的阴离子为SO2
3 2 4
C.“浸取2”时,发生反应的离子方程式为CaO2NH+H O=Ca22NH H O
4 2 3 2
D.“浸取2”时,所得滤渣2的主要成分为Al O 、Fe O
2 3 2 3
14.(2022·山东烟台·高三期中)氧化钪(Sc O )广泛用于航天、激光和导弹等尖端科学领域。一种从钛白
2 3
酸性废水(含H、Sc3、Ti4、Fe2、SO2
4
)中富集钪并制备Sc
2
O
3
的工艺流程如下。可能用到的数据见下
表。
金属离子 Ti4 Fe2 Fe3 Sc3
开始沉淀pH 1.3 6.8 1.9 4.0
沉淀完全pH 2.3 9.0 3.2 5.0
已知:“有机相”中主要含有Ti4、Fe2、Sc3。下列说法正确的是A.加H
2
O
2
的目的是将Fe2氧化为Fe3
B.操作Ⅰ用到的玻璃仪器有玻璃棒、烧杯和分液漏斗
C.加10%盐酸调pH的范围为3.2~4.0
D.草酸钪焙烧生成Sc O 是非氧化还原反应
2 3
15.(2022·安徽省阜阳第一中学高三阶段练习)电解法制备锰会有大量的阳极泥(主要含MnO ,杂质
2
PbSO 、CaSO 等)产生,煅烧氧化法将电解锰阳极泥回收制备二氧化锰的流程如图所示。下列说法正确的
4 4
是
已知:2Na MnO HCHO2MnO Na CO 2NaOH
2 4 2 2 3
A.将阳极泥煅烧氧化的原因是将MnO 转化为可溶性盐Na MnO
2 2 4
B.滤渣的主要成分为Pb、CaSO
4
C.制备流程中甲醛作氧化剂
D.理论上每产生43.5g的二氧化锰,需要消耗质量分数为30%的甲醛50g