文档内容
高考热点专项 溶液中粒子浓度大小比较
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.单一溶液中粒子浓度的关系.............................................................................................................................
2.混合溶液(缓冲溶液)中粒子浓度的关系判断..................................................................................................
3.混合溶液中离子浓度的比较.............................................................................................................................
【命题预测】...........................................................................................................................................................
考向1溶液混合型粒子浓度关系...........................................................................................................................
考向2 化工流程中粒子浓度关系..........................................................................................................................
考点要求 考题统计 考情分析
2024· 重庆卷,11,3分;2024·江
苏卷,12,3分;2024·安徽卷, 溶液中离子浓度的大小比较是主流试题,
文字陈述 13,3分;2023•浙江省6月选考, 难度在选择题中最大,往往是压轴题。此
15,3分;2022•重庆卷,11,3 类试题信息量大,且都隐藏于题目或图象
分;2022·浙江省6月卷,23,2分 中,主要通过酸碱中和滴定、电离平衡、
水解平衡和沉淀溶解平衡的情境,利用三
大守恒进行离子浓度大小比较、离子浓
2024·湖南卷,13,3分;2023•湖
度、电离平衡常数、水解平衡常数和溶度
南卷,12,3分;2023•江苏卷,
图象分析 积常数的计算等。预计2025年此类题仍活
12,3分;2022•福建卷,10;
跃在卷面上。
2022•江苏卷,12,3分;1.(2024· 重庆卷,11,3分)某兴趣小组探究[Cu(NH )](NO ) 的生成过程。若向
3 4 3 2
3mL0.1mol·L-1Cu(NO ) 溶液中逐滴加入 氨水,则下列说法正确的是( )
3 2
A.产生少量沉淀时(pH =4.8),溶液中c(NH +)c(NO -)
4 3
C.沉淀部分溶解时,溶液中c(Cu2+) < c(NH +)
4
D.沉淀完全溶解时,溶液中2c([Cu(NH )]2+) >c(NO -)
3 4 3
【答案】C
【解析】在 Cu(NO ) 溶液中逐滴加入氨水的反应方程式为:① Cu(NO ) + 2NH •H O=
3 2 3 2 3 2
Cu(OH) ↓+2NHNO ; ② Cu(OH) + 4NH •H O=[Cu(NH )](OH) +4H O , ③ 总 反 应
2 4 3 2 3 2 3 4 2 2
Cu(NO )+4NH •H O=[Cu(NH)](NO )+4H O。】A项,产生少量沉淀时(pH = 4.8),按照反应①处理,溶液
3 2 3 2 3 4 3 2 2
中的溶质为Cu(NO )、NH NO ,NH NO 在水溶液中完全电离,溶液呈酸性,溶液中c(OH―)很小,则溶液
3 2 4 3 4 3
中 c(NH +)> c(OH―),A 错误;B 项,产生大量沉淀时(pH= 6.0),按照反应①处理,溶液中的溶质为
4
Cu(NO ) 、NH NO ,Cu(NO ) 、NH NO 都电离出c(NO -),只有NH NO 电离出c(NH +),所以c(NH +) <
3 2 4 3 3 2 4 3 3 4 3 4 4
c(NO -),B错误;C项,沉淀部分溶解时,按照反应②③处理,溶液中的溶质为 NH NO 、[Cu(NH )]
3 4 3 3 4
(NO ) ,NH NO 完全电离出 c(NH +),Cu(OH) 、[Cu(NH )](NO ) 电离出的 c(Cu2+)很小,所以溶液中
3 2 4 3 4 2 3 4 3 2
c(Cu2+) < c(NH +), C 正确;D 项,沉淀完全溶解时,按照反应③处理,溶液中的溶质为[Cu(NH )]
4 3 4(NO ),[Cu(NH )]2+ 部分水解,NO -不水解,所以溶液中2c([Cu(NH )]2+) < c(NO -),D错误;故选C。
3 2 3 4 3 3 4 3
2.(2024·江苏卷,12,3分)室温下,通过下列实验探究SO 的性质。已知K (H SO )=1.3×10-2,
2 a1 2 3
K (H SO )=6.2×10-8.。
a2 2 3
实验1:将SO 气体通入水中,测得溶液pH=3。
2
实验2:将SO 气体通入0.1mol·L-1NaOH溶液中,当溶液pH=4时停止通气。
2
实验3:将SO 气体通入0.1mol·L-1酸性KMnO 溶液中,当溶液恰好褪色时停止通气。
2 4
下列说法正确的是( )
A.实验1所得溶液中:cSO 2-+cHSO ->c(H+)
3 3
B.实验2所得溶液中:cSO 2->cHSO -
3 3
C.实验2所得溶液经蒸干、灼烧制得NaHSO 固体
3
D.实验3所得溶液中:cSO 2->cMn2+
4
【答案】D
【解析】实验1得到HSO 溶液,实验2溶液的pH为4,实验2为NaHSO 溶液,实验3中SO 和酸
2 3 3 2
性KMnO 溶液反应的离子方程式为:5SO +2MnO- +2H O= 5SO 2-+2Mn2++4H+。A项, 实验1得到HSO
4 2 4 2 4 2 3
溶液,其质子守恒关系式为:2cSO 2-+cHSO -+ cOH-=c(H+),则 cSO 2-+cHSO -<c(H+),A错误;
3 3 3 3
B项,实验2为pH为4,依据 ,则 = ,溶液,则cSO 2-<
3
cHSO -,B错误;C项,NaHSO 溶液蒸干、灼烧制得NaHSO 固体,C错误;D项,实验3依据发生的反
3 3 4
应:5SO +2MnO- +2H O= 5SO 2-+2Mn2++4H+,则恰好完全反应后cSO 2->cMn2+,D正确;故选D。
2 4 2 4 4
3.(2024·安徽卷,13,3分)环境保护工程师研究利用NaS、FeS和HS处理水样中的Cd2+。已知
2 2
时,HS饱和溶液浓度约为0.1mol·L-1,K (H S)=10-6.97,K (H S)=10-12.90,K (FeS)=10-17.20,K (CdS)=10-
2 a1 2 a2 2 sp sp
26.10。下列说法错误的是( )
A.NaS溶液中:cNa++cH+=cOH-+cHS-+2cS2-
2
B.0.01mol·L-1NaS溶液中:cNa+>cS2->cOH->cHS-
2
C.向cCd2+=0.01mol·L-1的溶液中加入FeS,可使
D.向cCd2+=0.01mol·L-1的溶液中通入HS气体至饱和,所得溶液中:cH+>cCd2+
2
【答案】B
【解析】A项,NaS溶液中只有5种离子,分别是H+、Na+、OH-、HS-、cS2-,溶液是电中性的,
2
存在电荷守恒,可表示为cNa++cH+=cOH-+cHS-+2cS2-,A正确;B项,0.01mol·L-1NaS溶液
2中,S2-水解使溶液呈碱性,其水解常数为 ,根据硫元素守
恒可知 ,所以 ,则cOH->cS2-,B不正确;C项,K (FeS)远远大
sp
于K (CdS),向 的溶液中加入FeS时,可以发生沉淀的转化,该反应的平衡常数为
sp
, 因 此 该 反 应 可 以 完 全 进 行 , CdS 的 饱 和 溶 液 中
,若加入足量FeS时可使 ,C正确;D
项 , Cd2++HS CdS+2H+ 的 平 衡 常 数
2
,该反应可以完全进行,因此,当向
cCd2+=0.01mol·L-1的溶液中通入HS气体至饱和,Cd2+可以完全沉淀,所得溶液中cH+>cCd2+,D正确;
2
故选B。
4.(2024·湖南卷,13,3分)常温下K(HCOOH)=1.8×10-4,向20mL0.10mol·L-1NaOH溶液中缓慢滴入
a
相同浓度的HCOOH溶液,混合溶液中某两种离子的浓度随加入HCOOH溶液体积的变化关系如图所示,
下列说法错误的是( )
A. 水的电离程度:M<N
B. M点:cNa++cH+=2cOH-
C. 当V(HCOOH)=10mL时,cOH-=cH++cHCOO-+2cHCOOH
D. N点:cNa+>cHCOO->c(OH―)>c(H+)>cHCOOH【答案】D
【解析】结合起点和终点,向20mL0.10mol·L-1NaOH溶液中滴入相同浓度的HCOOH溶液,发生浓度
改变的微粒是OH-和HCOO-,当V(HCOOH)=0mL,溶液中存在的微粒是OH-,可知随着甲酸的加入,OH-
被消耗,逐渐下降,即经过M点在下降的曲线表示的是OH-浓度的改变,经过M点、N点的在上升的曲线
表示的是HCOO-浓度的改变。A项,M点时,V(HCOOH)=10mL,溶液中的溶质为cHCOOH:cHCOO-
=1:1,仍剩余有未反应的甲酸,对水的电离是抑制的,N点HCOOH溶液与NaOH溶液恰好反应生成
HCOONa,此时仅存在 HCOONa 的水解,此时水的电离程度最大,故 A 正确;B 项,M 点时,
V(HCOOH)=10mL,溶液中的溶质为cHCOOH:cHCOO-=1:1,根据电荷守恒有cNa++cH+=cOH
-+cHCOO-,M点为交点可知cOH-=cHCOO-,联合可得cNa++cH+=2cOH-,故B正确;C项,
当V(HCOOH)=10mL时,溶液中的溶质为cHCOOH:cHCOONa=1:1,根据电荷守恒有cNa++cH+
=cOH-+cHCOO-,根据物料守恒 cNa+=2cHCOOH+2cHCOO-,联合可得 cOH-=cH++
cHCOO-+2cHCOOH,故C正确;D项,N点HCOOH溶液与NaOH溶液恰好反应生成HCOONa,甲酸
根发生水解,因此cNa+>cHCOOH及c(OH―)>c(H+)观察图中N点可知, ,
根据 ,可知cHCOOH>cH+,故D错误;故选D。
5.(2023•湖南卷,12)常温下,用浓度为0.0200mol·L-1的NaOH标准溶液滴定浓度均为0.0200mol·L-1
的HCl和CHCOOH的混合溶液,滴定过程中溶液的 随 ( )的变化曲线如图所示。下
3
列说法错误的是( )
A.K(CHCOOH)约为10-4.76
a 3B.点a:c(Na+)=c(Cl-)=c(CH COOH)+c(CH COO-)
3 3
C.点b:c(CHCOOH)d,故D错误;故选D。
6.(2023•浙江省6月选考,15)草酸(H C O)是二元弱酸。某小组做如下两组实验:
2 2 4
实验I:往20mL0.1mol·L-1NaHC O 溶液中滴加0.1mol·L-1NaOH溶液。
2 4
实验Ⅱ:往20mL0.1mol·L-1NaHC O 溶液中滴加0.1mol·L-1 CaCl 溶液。
2 4 2
[已知:HC O 的电离常数K =5.4×10-2,K =5.4×10-5,K (CaC O)= 2.4×10-9,溶液混合后体积变化忽
2 2 4 a1 a2 sp 2 4
略不计],下列说法正确的是
A.实验I可选用甲基橙作指示剂,指示反应终点
B.实验I中V(NaOH)=10mL时,存在c(C O2-)<c(HC O-)
2 4 2 4
C.实验Ⅱ中发生反应Ca2++ HC O- =CaC O↓+H+
2 4 2 4
D.实验Ⅱ中V(CaCl)=80mL时,溶液中c(C O2-)=4.0×10-8mol·L-1
2 2 4
【答案】D
【解析】A项,NaHC O 溶液被氢氧化钠溶液滴定到终点时生成显碱性的草酸钠溶液,为了减小实验
2 4
误差要选用变色范围在碱性范围的指示剂,因此,实验I可选用酚酞作指示剂,指示反应终点,故A错误;
B项,实验I中V(NaOH)=10mL时,溶质是NaHC O、NaC O 且两者物质的量浓度相等,
2 4 2 2 4
,,则草酸氢根的电离程度大于草酸根的水解程度,因此存在c(C O2-)>
2 4c(HC O-),故B错误;C项,实验Ⅱ中,由于开始滴加的氯化钙量较少而NaHC O 过量,因此该反应在初
2 4 2 4
始阶段发生的是Ca2++ 2HC O- =CaC O↓+H C O,该反应的平衡常数为
2 4 2 4 2 2 4
,因为平衡常数很大,说明反应能够完全进行,
当NaHC O 完全消耗后,HC O 再和CaCl 发生反应,故C错误;D项,实验Ⅱ中V(CaCl)=80mL时,溶
2 4 2 2 4 2 2
液中的钙离子浓度为 ,溶液中
,故D正确。故选D。
7.(2023•江苏卷,12,3分)室温下,用含少量Mg2+的MnSO 溶液制备MnCO 的过程如题图所示。已
4 3
知K (MgF)=5.2×10-11,K(HF)=6.3×10-4。下列说法正确的是( )
sp 2 a
A.0.1mol·L-1NaF溶液中:c(F-)= c(Na+)+c(H+)
B.“除镁”得到的上层清液中:
C.0.1mol·L-1NaHCO 溶液中:c(CO2―)=c(H+)+c(H CO)-c(OH―)
3 3 2 3
D.“沉锰”后的滤液中:(Na+)+c(H+)= c(OH―)+c(HCO -)+2c(CO2―)
3 3
【答案】C
【解析】A项,0.1mol·L-1NaF溶液中存在电荷守恒:c(OH―)+c(F-)= c(Na+)+c(H+),A错误;
B项,“除镁”得到的上层清液中为MgF 的饱和溶液,有K (MgF)=c(Mg2+)·c2(F―),故
2 sp 2
,B错误;C项,0.1mol·L-1NaHCO 溶液中存在质子守恒:c(CO2―)+c(OH―)=c(H
3 3
+)+c(H CO),故c(CO2―)=c(H+)+c(H CO)-c(OH―),C正确;D项,“沉锰”后的滤液中还存在F-、SO 2-
2 3 3 2 3 4等离子,故电荷守恒中应增加其他离子使等式成立,D错误。 故选C。
分析溶液中微粒浓度关系的思维模型
1 .单一溶液中粒子浓度的关系
(1)电荷守恒:电解质溶液中,无论存在多少种离子,溶液都是呈电中性,即电解质溶液中阳离子所带
的电荷总数与阴离子所带的电荷总数相等
实
例 以NaCO 溶液为例
2 3
分析思路
NaCO===2Na++CO2-
2 3 3
①写出NaCO 溶液中电离和水 CO2-+HO HCO -+OH-
2 3 3 2 3
解过程 HCO -+HO HCO+OH-
3 2 2 3
HO H++OH-
2
②分析溶液中所有的阴、阳离
Na+、H+、CO2-、HCO -、OH-
3 3
子
** 错误的表达式 **阴、阳离
1×c(Na+)+1×c(H+)=2×c(CO2-)+1×c(HCO -)+1×c(OH-)
3 3
子浓度乘以自身所带的电荷
化简得:c(Na+)+c(H+)=2c(CO2-)+c(HCO -)+c(OH-)
3 3
数建立等式
(2)元素质量守恒(也叫物料守恒):在电解质溶液中,由于某些离子发生水解或电离,离子的存在形式发生了变化,变成了其它离子或分子,使离子的种类增多,但却不能使离子或分子中某种特定元素的原子
的数目发生变化,其质量在反应前后是守恒的,始终遵循原子守恒
实例
以NaCO 溶液为例
2 3
分析思路
n(Na+):n(CO2-)=2:1,即n(Na+)=2n(CO2
3 3
①分析溶质中的特定元素的原子或原子团间
-),CO2-在水中部分会水解成 HCO -、
3 3
的定量关系(特定元素除H、O元素外)
HCO,共三种含碳元素的存在形式
2 3
②找出特征元素在水溶液中的所有存在形式 c(Na+)=2c(CO2-)+2c(HCO -)+2c(H CO)
3 3 2 3
(3)质子守恒——以NaCO 溶液为例
2 3
①方法一:可以由电荷守恒与物料守恒推导出来,将两个守恒中不水解的Na+消掉
电荷守恒:c(Na+)+c(H+)=2c(CO2-)+c(HCO -)+c(OH-)
3 3
元素质量守恒:c(Na+)=2c(CO2-)+2c(HCO -)+2c(H CO)
3 3 2 3
将Na+消掉得:c(H+)+2c(H CO)+c(HCO -)=c(OH-),即为质子守恒
2 3 3
②方法二:质子守恒是依据水的电离平衡:HO H++OH-,水电离产生的H+和OH-的物质的量
2
总是相等的,无论在溶液中由水电离出的H+和OH-以什么形式存在。可用下列图示进行快速书写
NaCO 水溶液中的质子转移作用图 质子守恒
2 3
c(H O+)+2c(H CO)+c(HCO -)=c(OH-)
3 2 3 3
或c(H+)+2c(H CO)+c(HCO -)=c(OH-)
2 3 3
微点拨 得、失几个质子,微粒前面系数就是几个
(4)离子(粒子)浓度比较——以NaCO 溶液为例
2 3
分析思路
抓住电离和水解都是微弱的,分清主次关系
存在的平衡过程
NaCO===2Na++CO2-
2 3 3
CO2-+HO HCO -+OH- (主) 粒子浓度顺序:c(Na+)>c(CO2-)>c(OH-)>
3 2 3 3
HCO -+HO HCO+OH- (次) c(HCO -)>c(H CO)>c(H+)
3 2 2 3 3 2 3
HO H++OH-
2
2 .混合溶液 ( 缓冲溶液 ) 中粒子浓度的关系判断
以“常温下,浓度均为0.1 mol·L-1CHCOOH(弱酸)溶液和CHCOONa溶液等体积混合,溶液呈酸性”
3 3
为例:
实例 常温下,0.1 mol·L-1CHCOOH溶液和CHCOONa溶液等体积混
3 3
分析思路 合,溶液呈酸性
CHCOONa===Na++CHCOO-
3 3
写出混合溶液中存在的平
①呈酸性,以HA电离为主
衡过程
CHCOOH自身电离:CHCOOH H++CHCOO-
3 3 3②水解呈碱性,次要
CHCOO-中水解:CHCOO-+HO CHCOOH+OH-
3 3 2 3
** 错误的表达式 **水的电离:HO H++OH-
2
①电荷守恒 c(Na+)+c(H+)=c(CHCOO-)+c(OH-)
3
②元素质量守恒 2c(Na+)=c(CHCOO-)+c(CHCOOH)
3 3
** 错误的表达式 **质子
将Na+消掉得:c(CHCOOH)+2c(H+)=c(CHCOO-)+2c(OH-)
3 3
守恒
分析:在没有电离和水解之前 c(Na+)、c(CHCOO-)、
3
c(CHCOOH)均为0.1 mol·L-1,
3
但由于溶液呈酸性,以HA的电离为主,即电离程度大于水解程
** 错误的表达式 **离子 度
(粒子)浓度比较 c(CH 3 COOH)=0.1-电离消耗+水解生成<0.1
c(CHCOO-)=0.1+电离生成-水解消耗>0.1
3
c(Na+)=0.1,H+是由HA电离出来的,电离程度很微弱,故浓度
大小为:c(CHCOO-)>c(Na+)>c(CHCOOH)>c(H+)>c(OH-)
3 3
3 . 混合溶液中离子浓度的比较
(1)判断反应产物:判断两种溶液混合时生成了什么物质,是否有物质过量,再确定反应后溶液的组成。
(2)明确溶液中存在的所有平衡:根据溶液的组成,写出溶液中存在的所有平衡(水解平衡、电离平衡)。
(3)确定溶液的酸碱性:根据题给信息,确定溶液的酸碱性,判断是以电离为主还是以水解为主。
(4)比大小:比较离子大小,在比较中,要充分运用电荷守恒、物料守恒关系。
【名师提醒】
考向 1 溶液混合型粒子浓度关系
1.天门冬氨酸( ,记为HY)是一种天然氨基酸,水溶液显酸性,溶液中存在HY
2 2
H++HY-,HY- H++Y2-,与足量NaOH反应生成NaY ,与盐酸反应生成YH Cl。下列说法正确的是(
2 3
)
A.常温下,0.05 mol·L-1的HY溶液的pH=1
2B.pH=2.97的HY溶液稀释100倍,所得溶液pH=4.97
2
C.YH Cl水溶液中:c(H+)+c(YH-)= c(OH-)+ c(Cl-)+c(HY-)
3 3
D.NaY溶液中:c(OH-)=c(H+)+c(HY-)+ 2c(HY)+3c(YH -)
2 2 3
【答案】D
【解析】A项,HY部分电离,常温下,0.05 mol·L-1的HY溶液的pH>1,A错误;B项,稀释过程中
2 2
电离程度增大,pH=2.97的HY溶液稀释100倍,所得溶液pH<4.97,B错误;C项,根据电荷守恒知,
2
YH Cl水溶液中:c(H+)+c(YH-)= c(OH-)+ c(Cl-)+c(HY-)+ 2c(Y2-),C错误;D项,根据电荷守恒和物料守恒
3 3
知,NaY溶液中:c(OH-)=c(H+)+c(HY-)+ 2c(HY)+3c(YH -),D正确;故选D。
2 2 3
2.室温下用0.1mol•L-1NaOH溶液吸收SO ,若通入SO 所引起的溶液体积变化和HO挥发可忽略,
2 2 2
溶液中含硫物种的浓度c =c(H SO )+c(HSO -)+c(SO 2-)。HSO 电离常数分别为K =1.54×10-2、K =1.00×10-
总 2 3 3 3 2 3 a1 a2
7。下列说法正确的是( )
A.NaOH溶液吸收SO 所得到的溶液中:c(SO 2-)>c(HSO -)>c(H SO )
2 3 3 2 3
B.NaOH完全转化为NaHSO 时,溶液中:c(H+)+c(SO 2-)=c(OH—)+c(H SO )
3 3 2 3
C.NaOH完全转化为NaSO 时,溶液中:c(Na+)>c(SO 2-)>c(OH—)>c(HSO -)
2 3 3 3
D.NaOH溶液吸收SO ,c =0.1mol•L-1溶液中:c(H SO )>c(SO 2-)
2 总 2 3 3
【答案】C
【解析】由电离常数可知,亚硫酸氢根离子的水解常数K = = <K ,说明亚硫酸氢根离
h a2
子在溶液中的电离程度大于水解程度,亚硫酸氢钠溶液呈酸性。A项,氢氧化钠溶液吸收二氧化硫可能得
到亚硫酸氢钠溶液,由分析可知,亚硫酸氢根离子在溶液中的电离程度大于水解程度,溶液中c(HSO -)>
3
c(SO 2-) > c(H SO ),故A错误;B项,亚硫酸氢钠溶液中存在质子守恒关系c(H+)+ c(H SO ) =c(OH—)+
3 2 3 2 3
c(SO 2-),故B错误;C项,亚硫酸钠是强碱弱酸盐,亚硫酸根离子在溶液中分步水解,以一级水解为主,
3
则溶液中离子浓度的大小顺序为c(Na+)>c(SO 2-)>c(OH—)>c(HSO -),故C正确;D项,c =0.1mol•L-1溶液
3 3 总
为亚硫酸氢钠溶液,由分析可知,亚硫酸氢根离子在溶液中的电离程度大于水解程度,溶液中c(SO 2-) >
3
c(H SO ),故D错误;故选C。
2 3
3.室温下,通过下列实验探究NaHSO、NaSO 溶液的性质。
3 2 3
实验1:用pH试纸测量0.1mol·L-1NaHSO 溶液的pH,测得pH约为5
3
实验2:0.1mol·L-1NaHSO 溶液中加入等体积0.1mol·L-1NaOH溶液,没有明显现象
3
实验3:0.1mol·L-1NaSO 溶液中滴加新制饱和氯水,氯水颜色褪去
2 3
实验4:将0.1mol·L-1NaSO 溶液与0.1mol·L-1CaCl 溶液等体积混合,产白色沉淀
2 3 2
下列说法正确的是( )
A.由实验1可得出: >K (H SO )
a2 2 3B.实验2所得的溶液中c(HSO -)>c(SO 2-)
3 3
C.实验3中发生反应的离子方程式为HO+Cl + SO 2-=SO2-+2H++2Cl-
2 2 3 4
D.实验4中两溶液混合时有:c(Ca2+)·c(SO 2-)<K (CaSO)
3 sp 3
【答案】C
【解析】A项,溶液显酸性,说明溶液中亚硫酸氢根离子的电离程度大于其水解程度,第二步电离常
数大于水解常数,即K (H SO )> ,A错误;B项,0.1mol·L-1NaHSO 溶液中加入等体积
a2 2 3 3
0.1mol·L-1NaOH溶液,所得溶液为NaSO 溶液,溶液中c(SO 2-)>c(HSO -),B错误;C项,新制饱和氯水
2 3 3 3
中有氯气,氯气具有强氧化性,亚硫酸根离子具有还原性,两者发生氧化还原反应,其离子方程式为:
HO+Cl +SO2-=SO2-+2H++2Cl-,C正确;D项,两溶液混合若产生白色沉淀,说明溶液中
2 2 3 4
c(Ca2+)·c(SO 2-)>K (CaSO),D错误;故选C。
3 sp 3
4.(2025· 江浙皖高中发展共同体高三联考)草酸钠(Na C O)可用作抗凝血剂。室温下,通过下列实验
2 2 4
探究NaC O 溶液的性质。
2 2 4
实验 实验操作和现象
1 测得0.1mol·L-1NaC O 溶液的pH=8.4
2 2 4
2 向0.2mol·L-1NaC O 溶液中加入等体积 盐酸,测得混合后溶液的pH=5.5
2 2 4
3 向0.1mol·L-1NaC O 溶液中滴加几滴酸性KMnO 溶液,振荡,溶液仍为无色
2 2 4 4
4 向0.1mol·L-1NaC O 溶液中加入等体积0.1mol·L-1CaCl 溶液,产生白色沉淀
2 2 4 2
下列有关说法正确的是( )
A.0.1mol·L-1NaC O 溶液中存在:cNa++cH+=cOH-+cHC O-+cC O2-
2 2 4 2 4 2 4
B.实验2得到的溶液中:c(Cl-)>cHC O>cC O2-
2 2 4 2 4
C.实验3中 被还原成 ,则反应的离子方程式:C O2-+2MnO-+16H+=10CO ↑+Mn2++8H O
2 4 4 2 2
D.依据实验4可得:K (CaC O) >2.5×10-3
sp 2 4
【答案】C
【解析】实验1草酸钠溶液显碱性,说明草酸钠为强碱弱酸盐,故草酸为弱酸;实验2溶液混合后发
生反应:NaC O+HCl= NaCl+NaHC O,氯离子浓度为0.1mol/L,溶液的pH=5.5,说明草酸氢根的电离程
2 2 4 2 4
度大于其水解程度,故草酸根浓度大于草酸浓度,即>cHC O;实验3中草酸根与酸性高锰酸钾溶液发
2 2 4
生氧化还原反应,酸性高锰酸钾溶液褪色;实验4中生成白色沉淀,说明溶液中 。A项,
0.1mol·L-1NaC O 溶液中存在电荷守恒:cNa++cH+=cOH-+cHC O-+2cC O2-,A错误;B项,
2 2 4 2 4 2 4实验2中:c(Cl-)>cC O2->cHC O,B错误;C项,若实验3中MnO -被还原成Mn2+,草酸根具有还
2 4 2 2 4 4
原性,能与酸性高锰酸钾溶液发生氧化还原反应,根据得失电子守恒和原子守恒,离子方程式为:5C O2-
2 4
+2MnO-+16H+=10CO ↑+Mn2++8H O,C正确;D项,实验4中产生白色沉淀,则
4 2 2
,即:K (CaC O)<2.5×10-3,D错误;故选C。
sp 2 4
5.(2022·江苏省百校大联考高三第二次考试)室温下,通过下列实验探究亚硫酸盐的性质。已知:
K (H SO )=1.54×10-2、K (H SO )=1.02×10-7
a1 2 3 a2 2 3
实验 实验操作和现象
1 向10mL0.10mol·L-1NaOH溶液通入11.2mL(标准状况)SO ,测得pH约为9
2
2 向10mL0.10mol·L-1NaOH溶液通入SO 至溶液pH=7
2
3 向10mL0.1mol·L-1NaOH溶液通入22.4mL(标准状况)SO ,测得pH约为3
2
4 取实验3所得溶液1mL,加入1mL0.01mol·L-1Ba(OH) 溶液,产生白色沉淀
2
下列说法正确的是( )
A.实验1得到的溶液中有:c(SO 2-)+c(HSO -)+c(H+)c(OH-),故A错误;B项,Ka(H SO )= =1.02×10-7,实验2得到的溶
3 3 2 2 3
液pH=7,即c(H+)=1.0×10-7,即 =1.02,有c(SO 2-)>c(HSO -),故B错误;C项,22.4mL(标准状
3 3
况)SO 的物质的量为 =0.001mol,故实验 3 得到 NaHSO 溶液,其浓度为 0.1mol/L,c(H+)
2 3+c(Na+)=c(HSO -)+2c(SO2-)+c(OH-) , 由 K(HS )= = c(OH-),且c(SO 2-)>c(H SO ),可知:c(H+)+c(Na+)>c(HSO -)+2c(H SO )+c(OH-)>c(HSO -)+2c(H SO ),
3 2 3 3 2 3 3 2 3
故C错误;D项,实验4中发生的反应为亚硫酸氢钠溶液与少量氢氧化钡溶液反应生成亚硫酸钡沉淀、亚
硫酸钠和水,反应的离子方程式为2 HSO -+2OH-+Ba2+=BaSO ↓+ SO 2-+2H O,实验4中亚硫酸氢钠浓度为
3 3 3 2
0.1mol/L,Ba(OH) 溶液0.01mol/L,等体积混合,则氢氧化钡少量,c(SO 2-)=
2 3
,c(Ba2+)= ,Q(BaSO )=0.01×0.005=5×10-5>Ksp(BaSO ),故有沉淀,故D正确;故选D。
3 3
6.室温下: 、 、 、 实验室进行多组
实验测定某些酸、碱、盐性质,相关实验记录如下:
实验 实验操作和现象
1 测定0.10mol•L-1NaHCO 溶液的pH约为8
3
2 测定0.10mol•L-1HCN与0.05mol•L-1NaOH溶液等体积混合,测得混合溶液的pH>7
3 向NaClO溶液中通入少量的CO,测得pH降低
2
4 向0.01mol•L-1NaCO 溶液中加入等体积0.02mol•L-1CaCl 溶液,产生白色沉淀
2 3 2
下列所得结论正确的是( )
A.实验1溶液中存在:c(Na+)+c(H+)= c(OH-)+c(CO 2-)+c(HCO-)
3 3
B.由实验2可得
C.实验3反应的离子方程式:CO+H O+2 = CO2-+2HClO
2 2 3
D.实验4所得上层清液中的
【答案】D
【解析】由电离常数可知,弱酸和酸式根离子在溶液中的电离程度为HCO >HClO>HCO -;由实验
2 3 3
1可知,碳酸氢根离子在溶液中的水解趋势大于电离趋势,使溶液呈碱性;由实验2可知,0.10mol•L-1氢
氰酸与0.05mol•L-1氢氧化钠溶液等体积混合后反应得到等浓度的氢氰酸和氰酸钠的混合溶液,氢氰酸的电
离程度小于氰酸根离子的水解程度,使溶液呈碱性。A项,碳酸氢钠溶液中存在的电荷守恒关系为c(Na+)+c(H+)= c(OH-)+2c(CO 2-)+c(HCO-),故A错误;B项,实验2中0.10mol•L-1氢氰酸与0.05mol•L-1氢氧化钠
3 3
溶液等体积混合后反应得到等浓度的氢氰酸和氰酸钠的混合溶液,氢氰酸的电离程度小于氰酸根离子的水
解程度,使溶液呈碱性,则氢氰酸的电离常数K(HCN)小于水解常数 ,故B错误;C.
a
项,弱酸和酸式根离子在溶液中的电离程度为HCO >HClO>HCO -,则次氯酸钠溶液与少量二氧化碳反
2 3 3
应生成碳酸氢钠和次氯酸,反应的离子方程式为CO+H O+ClO-= HCO -+HClO,故C错误;D项,由题意
2 2 3
可知,VL0.01mol/L碳酸钠溶液和VL0.02mol/L氯化钙溶液等体积混合反应后溶液中过量的钙离子浓度为
=0.005mol/L,由碳酸钙的溶度积可知溶液中碳酸根离子浓度为 =
=2×10—6.55mol/L,故D正确;故选D。
7.常温下,向新制氯水中滴加 溶液,溶液中水电离出的OH-浓度与 溶液体积之间的关系
如图所示。下列推断正确的是( )
A.E、H点溶液的 分别为3和7
B.F点对应的溶液中:c(Na+)=c(Cl-)+c(ClO-)
C.G点对应的溶液中:c(Na+)>c(ClO-)>c(Cl-)>c(OH-)>c(H+)
D.E~H点对应的溶液中,c(Cl-)+c(ClO-)+c(HClO)+c(Cl )为定值
2
【答案】B
【解析】通过图象分析,E点位新制的氯水,溶液为盐酸和次氯酸的混合溶液,对水的电离有抑制作
用,F点溶液为中性,G点促进水的电离,为氯化钠、次氯酸钠的混合溶液,次氯酸钠水解,使溶液呈碱
性,H点溶液呈碱性。A项,E点新制氯水溶液,溶液显酸性,由水电离出的 ,溶液中OH−完全是由水电离出来的,所以c(OH−)= ,则溶液中 ,
则溶液pH=3;H点NaOH过量,溶液为碱性溶液,溶质为NaCl、NaClO和NaOH,pH>7,A错误;B项,
F 溶液为中性,c(OH-)=c(H+),根据溶液呈电中性,c(Na+) +c(H+)=c(Cl-)+c(ClO-)+c(OH-),可得 c(Na+)=
c(Cl-)+c(ClO-),B正确;C项,G点促进水的电离,为氯化钠、次氯酸钠的混合溶液,且物质的量相等,次
氯酸钠水解,使溶液呈碱性,溶液中的次氯酸根离子浓度减小,则 c(Na+)>c(Cl-)>c(ClO-)>c(OH-)>
c(H+),C错误;D项,根据Cl元素守恒,E~H点对应的溶液中,c(Cl-)+c(ClO-)+c(HClO)+2c(Cl )为定值,
2
D错误;故选B。
考向 2 化工流程中粒子浓度关系
8.(2024·江苏省苏锡常镇四市高三下教学情况调研一模)室温下,通过矿物中PbSO 获得Pb(NO ) 的
4 3 2
过程如下:
已知: , 。下列说法正确的是( )
A.NaCO 溶液中:cOH-<cH++cHCO -+2cHCO
2 3 3 2 3
B.反应PbSO (s)+CO2-(aq) PbCO (s))+SO 2-(aq)正向进行,需满足
4 3 3 4
C.“脱硫”后上层清液中:cNa++cH+=cOH-+2cSO 2-
4
D.PbCO 悬浊液加入HNO “溶解”过程中,溶液中CO2-浓度逐渐减小
3 3 3
【答案】D
【解析】PbSO 中加入NaCO 溶液脱硫,PbSO 与NaCO 反应转化为PbCO 沉淀,再加入HNO 溶解
4 2 3 4 2 3 3 3
得到Pb(NO )。A项,由质子守恒关系得:cOH-=cH++cHCO -+2cHCO,故A错误;B项,
3 2 3 2 3
PbSO (s)+CO2-(aq) PbCO (s))+SO 2-(aq)该反应的平衡常数
4 3 3 4
,当浓度商
时,平衡正向移动,故B错误;C项,“脱硫”后上层清液主要是NaSO 溶液,
2 4
还含有未反应完的NaCO 溶液,守恒关系还应考虑CO2,故C错误;D项,PbCO 悬浊液加入HNO“溶
2 3 3 3 3
解”过程中,由于CO2会和H+反应生成CO,所以溶液中CO2浓度逐渐减小,故D正确;故选D。
3 2 39.(2024· 江苏省南通市高三第二次调研测试)实验室通过下列过程制取草酸亚铁晶体。
已知: 、
下列说法不正确的是( )
A.pH=2的HC O 溶液中:cHC O<cH C O-
2 2 4 2 2 4 2 4
B.“酸化”后的溶液中:cNH ++2c Fe2+<2cSO 2-
4 4
C.可以用酸性KMnO 溶液检验“沉淀”后的上层清液中是否含有Fe2+
4
D.水洗后,再用乙醇洗涤有利于晶体快速干燥
【答案】C
【解析】A项,pH=2的HC O 溶液中c(H+)= 10-2mol·L-1,
2 2 4
, ,即cHC O<cH C O-,A正确;B项,根据电荷守恒:
2 2 4 2 4
,溶液显酸性,cH+>cOH-,cNH ++2c Fe2+<
4
2cSO 2-,B正确;C项,酸性KMnO 除了可以氧化Fe2+,也可以氧化HC O 等,溶液褪色不能证明是否
4 4 2 2 4
含Fe2+,C错误;D项,乙醇与水互溶,用乙醇洗可带走水分,利于干燥,D正确;故选C。
10.[真题改编](2023•江苏卷,12)室温下,用含少量Mg2+的MnSO 溶液制备MnCO 的过程如题图所
4 3
示:
已知:K (MgF )=5.2×10-11,K (MnCO )=8.0×10-11,K [Mn(OH) ]=1.9×10-13;K (H CO)=4.5×10-7,
sp 2 sp 3 sp 2 a1 2 3
K (H CO)=4.7×10-11。下列说法正确的是( )
a2 2 3
A.MgF 饱和溶液中:cF-+cHF=2cMg2+
2
B.为提高MnCO 的产率,使用NaCO 溶液“沉锰”效果更好
3 2 3
C.0.1mol·L-1NaHCO 溶液中,cNa+>cHCO ->cCO2->cHCO
3 3 3 2 3
D.反应Mn2++2HCO-=MnCO↓+HCO 的平衡常数为
3 3 2 3【答案】D
【解析】由题给流程可知,向硫酸锰溶液中加入氟化钠溶液,将溶液中的镁离子转化为氟化镁沉淀,
过滤得到氟化镁和滤液;向滤液中加入碳酸氢钠溶液,将溶液中的锰离子转化为碳酸锰沉淀,过滤得到碳
酸锰。A项,氟化镁饱和溶液中存在如下物料守恒cF-+cHF=2cMg2++2c[Mg(OH) ],故A错误;B项,
2
由电离常数可知,碳酸钠溶液的碱性强于碳酸氢钠,使用碳酸钠溶液“沉锰”时,可能使锰离子转化为氢
氧化锰沉淀导致碳酸锰的产率降低,故B错误;C项,由电离常数可知,碳酸氢根离子在溶液中的水解常
数为K = = ≈2.2×10—8>K ,则碳酸氢根离子在溶液中的水解程度大于电离程度,溶液中碳酸
h a2
浓度大于碳酸根离子浓度,故C错误;D项,由方程式可知,反应的平衡常数K= =
= = ≈1.3×106,故D正确;故选D。
11.(2024· 江苏省南通市海门高三第一次调研考试)室温下,用 溶液吸收SO
2
的过程如图所示。已知 , ,下列说法正确的是( )
A. 溶液中:
B. 溶液中:
C.吸收烟气后的溶液中:
D.“沉淀”得到的上层清液中:
【答案】C【解析】A项,由 可知, , 的电离能力
大于水解能力,所以 ,A错误; B项, 溶液中:
,B错误;C项,吸收烟气后的溶液为 和 的混合
溶液,则 ,C正确;D项,有沉淀产生,因此上层清液为饱和
溶液,则 ,D错误;故选C。
12.(2024· 江苏省南通市如皋市高三下适应性考试)室温下,用含少量ZnSO 杂质的1mol·L-1 MnSO
4 4
溶液制备MnCO 的过程如下图所示。下列说法正确的是( )
3
已知:
A.“除锌”后所得上层清液中, 一定小于
B.0.1mol·L-1NH HCO 溶液中存在:
4 3
C.氨水、NH HCO 溶液中存在:
4 3
D.“沉锰”后的滤液中存在:
【答案】A
【解析】“除锌”步骤中,由于 ,因此当加入过量MnS时,
产生ZnS沉淀,过滤后除掉过量的MnS和产生的ZnS沉淀,再用NH HCO 将Mn2+沉淀为MnCO 。A项,
4 3 3MnS过量,“除锌”步骤完成沉淀生成ZnS,则上层清液 一定小于 ,A正确;B项,
NH HCO 溶液中由电荷守恒 ,由物料守恒
4 3
,联立两式可得
,B错误;C项,由电荷守恒
,pH>7,说明 ,则
,C错误;D项,沉锰后滤液成分是(NH )SO 、NH ·H O、NH HCO ,则
4 2 4 3 2 4 3
,D错误;故选A。
13.(2024·江苏省盐城市高三一模考试)室温下,用含少量 的FeSO 溶液制备FeCO 的过程如图所
4 3
示。已知: 。下
列说法正确的是( )
A. 溶液中:
B.“除钙”得到的上层清液中:
C. 的氨水−NH HCO 溶液:
4 3
D.“沉铁”反应的离子方程式:
【答案】C
【解析】含少量Ca2+的FeSO 溶液中,加入NH F溶液将Ca2+转化为CaF 沉淀除去,所得滤液主要含
4 4 2
有Fe2+、SO 2-和NH +,再加入氨水−NH HCO 溶液“沉铁”得到FeCO 沉淀。A项,因F−、NH +均能水解
4 4 4 3 3 4生成HF、NH ·H O,则0.1mol⋅L−1NH F溶液中,由物料守恒得: ,
3 2 4
A错误;B项,“除钙”得到的上层清液为CaF 的饱和溶液,则 ,B错误;C项,
2
pH=10的氨水−NH HCO 溶液中,因 ,则
4 3
,C正确;D项,Fe2+与HCO -反应生成FeCO 沉淀,HCO -电离出的H+与NH ·H O结
3 3 3 3 2
合生成NH +和HO,则“沉铁”反应的离子方程式为: ,
4 2
D错误; 故选C。
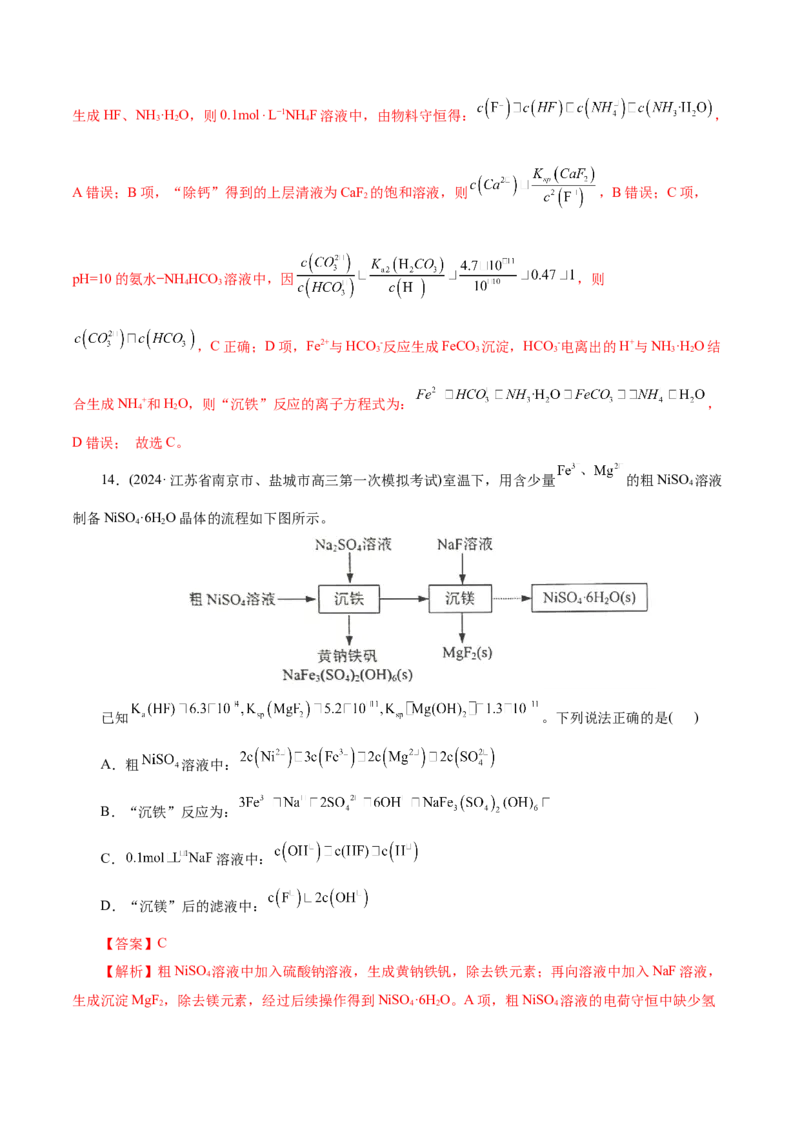
14.(2024·江苏省南京市、盐城市高三第一次模拟考试)室温下,用含少量 的粗NiSO 溶液
4
制备NiSO·6H O晶体的流程如下图所示。
4 2
已知 。下列说法正确的是( )
A.粗 溶液中:
B.“沉铁”反应为:
C. 溶液中:
D.“沉镁”后的滤液中:
【答案】C
【解析】粗NiSO 溶液中加入硫酸钠溶液,生成黄钠铁钒,除去铁元素;再向溶液中加入NaF溶液,
4
生成沉淀MgF ,除去镁元素,经过后续操作得到NiSO ·6H O。A项,粗NiSO 溶液的电荷守恒中缺少氢
2 4 2 4离子和氢氧根离子浓度,A错误;B项,溶液呈弱酸性,“沉铁”反应为:3Fe3++Na++2SO2-
4
+6H O=NaFe (SO )(OH) ↓+6H+,B错误;C项,氟化氢为弱酸, 溶液中根据质子守恒:
2 3 4 2 6
cHF+cH+=cOH-,C正确;D项,沉镁过程形成MgF 沉淀,根据沉淀溶解平衡,
2
,
,此时 ,该溶液中,
镁离子浓度相同,形成的是MgF 沉淀,没有形成Mg(OH) 沉淀,则溶液中 ,故
2 2
得出沉镁后 ,D错误;故选C。
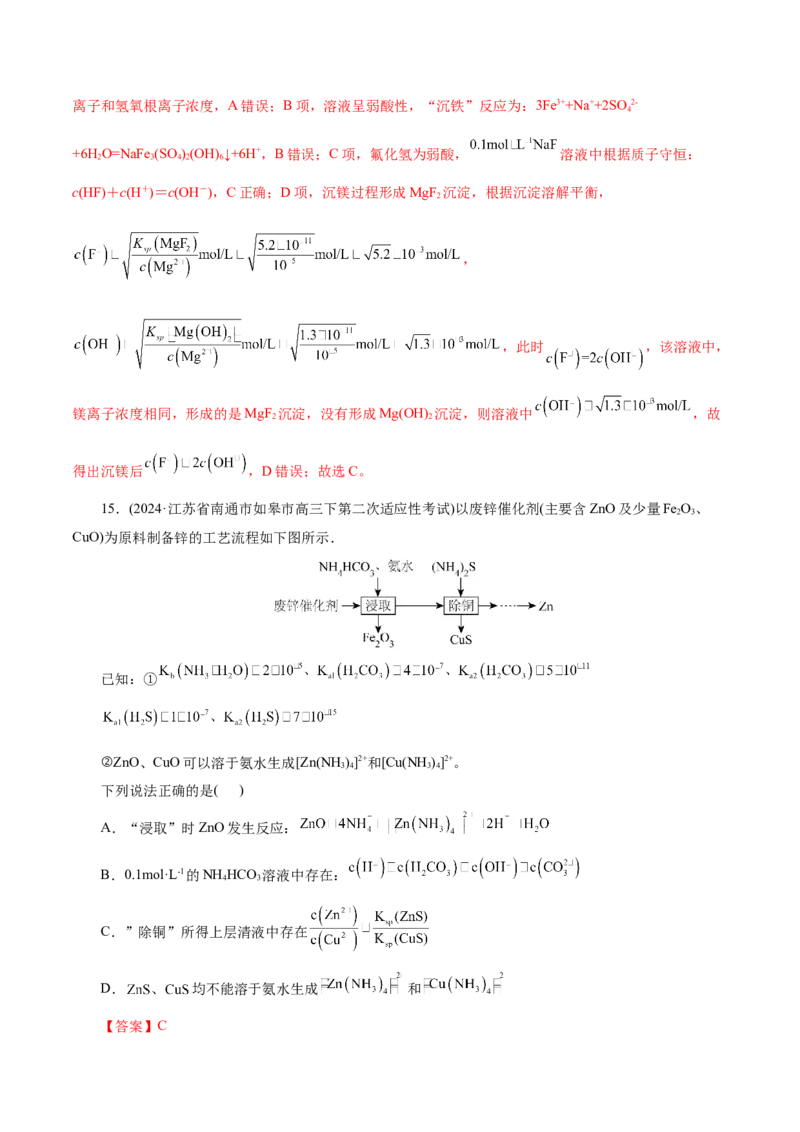
15.(2024·江苏省南通市如皋市高三下第二次适应性考试)以废锌催化剂(主要含ZnO及少量Fe O、
2 3
CuO)为原料制备锌的工艺流程如下图所示.
已知:①
②ZnO、CuO可以溶于氨水生成[Zn(NH )]2+和[Cu(NH )]2+。
3 4 3 4
下列说法正确的是( )
A.“浸取”时ZnO发生反应:
B.0.1mol·L-1的NH HCO 溶液中存在:
4 3
C.”除铜”所得上层清液中存在
D. 均不能溶于氨水生成 和
【答案】C【解析】A项,根据已知②,“浸取”时ZnO发生反应:
,A错误;B项,0.1mol·L-1的NH HCO 溶液中存在质子
4 3
守恒: ,B错误;C项,”除铜”所得上层清液中锌
离子没有沉淀,溶液中存在 , ,故存在
,C正确;D项,ZnS能溶于氨水生成[Zn(NH )]2+,D错误;故选C。
3 4
16.(2024· 江苏省南京航空航天大学苏州附属中学高三适应性测试)某实验室回收废水中苯酚的过程如
下图所示。已知:苯酚的电离常数K=1.0×10-10,HCO 的电离常数K =4.5×10-7,K =4.7×10-11。
a 2 3 a1 a2
下列有关说法不正确的是( )
A.操作1、操作2 均为分液
B. NaHCO 溶液中存在:c(HCO)+c(H+)=c(OH-)+c(CO 2-)
3 2 3 3
C.若反应1后溶液中存在c(Na+)=2 c(C HO-)+2 c(C HOH),此时c(C HO-)>c(HCO-)
6 5 6 5 6 5 3
D.反应2 中通入CO 至溶液 pH=10时, 此时溶液中存在: c(C HO-)= c(C HOH)
2 6 5 6 5
【答案】C
【解析】据流程图可知,将苯酚废水用有机溶剂苯先进行萃取分液,得到苯酚的苯溶液,接着加入碳
酸钠溶液,使苯酚转化成苯酚钠进入水溶液中,再通过分液分离有机层苯,随后往苯酚钠溶液中通入二氧
化碳,苯酚在水中溶解度小,析出后过滤即可得到苯酚。A项,结合流程分析,操作1、操作2均溶液分
层,采取分液的方法进行分离,A正确;B项, NaHCO 溶液中存在质子守恒:
3
c(HCO)+c(H+)=c(OH-)+c(CO 2-),B正确;C项,苯酚酸性小于碳酸,因此反应1苯酚与碳酸钠溶液混合
2 3 3
生成碳酸氢钠和苯酚钠,根据电离常数可知,苯酚钠的水解能力大于碳酸氢钠,故c(C HO-)<c(HCO -),
6 5 3
C错误;D项,反应2 中通入 CO 至溶液 pH=10时,此时溶液中存在:
2,故 c (C HO-)=c (C HOH),D正确; 故选C。
6 5 6 5
17.(2024·江苏省连云港市高三第一次调研考试)室温下,用含少量Co2+和Ni2+的FeSO 溶液制备
4
FeC O·2H O的过程如下。
2 4 2
已知: , ; ,
下列说法正确的是( )
A.0.01mol·L-1NaS溶液中:c(HS―)>c(S2-)
2
B.“除钴镍”后得到的上层清液中c(Co2+)为6.0×10-2mol·L-1,则c(Ni2+)为1.0×10-6mol·L-1
C.0.1mol·L-1NaHC O 溶液中:cOH-=cH++ c C O2-+cHC O
2 4 2 4 2 2 4
D.“沉铁”后的滤液中:cNa++ cH+=cOH-+2c C O2-+cH C O-
2 4 2 4
【答案】A
【解析】该工艺流程的原料为含少量Co2+和Ni2+的FeSO 溶液,产品为FeC O·2H O,加入NaS溶液,
4 2 4 2 2
使Co2+和Ni2+转化为CoS、NiS沉淀过滤除去,滤液中加入NaHC O 溶液,与Fe2+反应生成FeC O·2H O。
2 4 2 4 2
A项,NaS溶液中,S2-发生水解S2-+H O HS-+OH-、HS-+H O HS+OH-,水解程度
2 2 2 2
较大, ,以第一步水解
为主,设发生水解的S2-为xmol/L,
则 ,解得 ,故 c(HS―)>c(S2-),A 正确;B 项,“除钴
镍 ” 后 得 到 的 上 层 清 液 中 c(Ni2+) 为 ,, 则
,B 错误;C 项,NaHC O 溶液存在电荷守恒
2 4
cNa++ cH+=cOH-+2c C O2-+cH C O-及物料守恒cNa+=c C O2-+cH C O-+cHC O,则
2 4 2 4 2 4 2 4 2 2 4
质子守恒为cOH-+ c C O2-=cH++cHC O,C错误;D项,除去Co2+和Ni2+的FeSO 溶液,加入
2 4 2 2 4 4
NaHC O 溶液 “沉铁”后,滤液中含有NaSO 、少量HC O 及可能过量的NaHC O ,故电荷守恒,因为
2 4 2 4 2 2 4 2 4
阴离子种类不全,cNa++ cH+≠ cOH-+2c C O2-+cH C O-,D错误;故选A。
2 4 2 4
18.燃煤烟气脱硫的一种方法如图所示。室温下以150mL 0.2 氨水吸收 ,若通入 所引
起的溶液体积变化和 、 挥发可忽略,溶液中含硫物种的浓度 。
的电离平衡常数分别为: , ; 的电离平衡常数为:
。下列说法正确的是( )
A.NH ·H O吸收 所得到的溶液中:
3 2
B.NH ·H O吸收 , 溶液:
3 2
C.NH ·H O吸收标况下0.448L ,所得溶液中:
3 2
D.题图所示“吸收”“氧化”后的溶液pH增大
【答案】A
【解析】A项,“吸收”过程中,NH ·H O和SO 反应生成(NH )SO ,若NH +和SO 2-都不发生水解,
3 2 2 4 2 3 4 3
则 ,但NH +和SO 2-都发生水解,K(NH +)=
4 3 h 4
,则SO 2-的水解程度大于NH +,溶液中:
3 4
,故A正确;B项,NH ·H O吸收SO 反应生成(NH )SO ,
3 2 2 4 2 3
=0.1mol/L,则c(NH +)+c(NH·H O)=2c =0.2mol/L,再结合电荷守恒:
4 3 2 总
,可得 - c(NH·H O),
3 2
故B错误;C项,标况下0.448L SO 的物质的量为 ,150mL 0.2 氨水中
2n(NH ·H O)=0.15L×0.2mol/L=0.03mol,得到物料守恒:2(NH +)+2c(NH·H O)=
3 2 4 3 2
,故C错误;D项,由图可知,“吸收”“氧化”后溶质由
NH ·H O转化为(NH )SO ,故溶液的pH减小,故D错误;故选A。
3 2 4 2 3