文档内容
专项训练 盐溶液中离子浓度大小的比较(解析版)
1.常温下,下列说法不正确的是
A.0.02mol•L-1的NaOH溶液与0.04mol•L-1的NaHC O 溶液等体积混合:2c(OH-)
2 4
+c(C O )=c(HC O )+2c(H+)
2 2
B.pH为2的醋酸和pH为2的盐酸等体积混合后溶液的pH=2
C.叠氮酸(HN )与醋酸酸性相近,0.1mol•L-1NaN 水溶液中离子浓度大小顺序为
3 3
c(Na+)>c(N )>c(OH-)>c(H+)
D.向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中c(NH )=c(Cl-)
【答案】A
【详解】A.混合后得到等物质的量浓度的NaHC O 和NaC O 混合溶液,根据电荷守
2 4 2 2 4
恒可知: ,根据物料守恒可知:
,消去Na+可得:
,A错误;
B.混合前后H+的浓度没有发生改变,所以溶液的pH还是为2,B正确;
C.叠氮酸是弱酸,则N 水解,溶液显碱性,所以会有c(Na+)>c(N )>c(OH-)>
c(H+),C正确;
D.pH=7时,溶液中 ,根据电荷守恒可知c(NH )=c(Cl-),D正确;
故选A。
2.常温下,在不同试剂中加入酸或碱后体系pH的变化如表所示。下列说法错误的是
pH
试剂 通入 加入
初
0.01molHCl气 0.01molNaOH固
始
体 体
①1LH O 7 a 12
2
②0.10molCH COOH,
3 4.76 4.67 4.85
0.10molCHCOONa配制成1L的溶液
3
1
学科网(北京)股份有限公司已知:缓冲作用是维持溶液自身pH值的相对稳定。
A.表中a的数值等于2(忽略通入HCl气体前后体系的体积变化)
B.试剂①如表所示通入HCl和加入NaOH相比,水的电离程度相同
C.试剂②中c(CHCOOH)>c(Na+)>c(CH COO-)
3 3
D.NH ·H O—NHCl溶液具有与试剂②相似的缓冲作用
3 2 4
【答案】C
【分析】0.10molCHCOOH,0.10molCHCOONa配制成1L的溶液是缓冲溶液,开始
3 3
时pH=4.76,通入0.01molHCl后,pH变成4.67,变化不大,加入0.01molNaOH后pH
变为4.85,也变化不大,有缓冲酸碱的作用。
【详解】A.0.01molHCl气体通入1L水中,忽略体积变化,浓度是0.01mol/L,由于
盐酸是强酸完全电离,H+浓度为0.01mol/L,a=2,故A正确;
B.0.01molHCl气体通入1L水中与0.01molNaOH加入水中,二者的浓度相同,都是一
元强酸碱,都抑制水的电离,抑制的程度一样,因此水电离程度一样,故B正确;
C.试剂②是0.10molCHCOOH,0.10molCHCOONa配制成1L的溶液,溶液呈酸性,
3 3
说明CHCOOH的电离大于CHCOO-的水解,因此CHCOO-的浓度大于CHCOOH的
3 3 3 3
浓度,故C错误;
D.NH ·H O—NHCl溶液同样具有与试剂②相似的缓冲作用,故D正确;
3 2 4
答案选C。
3.下列离子浓度的关系正确的是
A.0.1mol·L-1KS溶液中:c(H+)+c(HS-)+2c(H S)=c(OH-)
2 2
B.0.1mol·L-1NaHCO 溶液中:c( )+2c( )+c(H CO)=c(Na+)
3 2 3
C.等物质的量的CHCOONa和盐酸的混合溶液中:c(Na+)+c(H+)=c(CH COO-)
3 3
+c(OH-)
D.物质的量浓度相等的NH Cl溶液、CHCOONH 溶液和NH HSO 溶液中c( )
4 3 4 4 4
依次增大
【答案】A
【详解】A.根据质子守恒可知,0.1mol·L-1KS溶液中:c(H+)+c(HS-)
2
+2c(H S)=c(OH-),A正确;
2
B.0.1mol·L-1NaHCO 溶液中:c(HCO )+c(CO )+c(H CO)=c(Na+),B错误;
3 2 3
C.等物质的量的CHCOONa和盐酸的混合溶液中:c(Na+)+c(H+)=c(CH COO-)+c(OH-)
3 3
+c(Cl-),C错误;
资料收集整理【淘宝店铺:向阳百分百】 第2页,共20页D.物质的量浓度相等的NH Cl溶液、CHCOONH 溶液和NH HSO 溶液中c(NH +)最
4 3 4 4 4 4
大的是NH HSO ,NH Cl溶液次之,CHCOONH 溶液最小,D错误;
4 4 4 3 4
故选A。
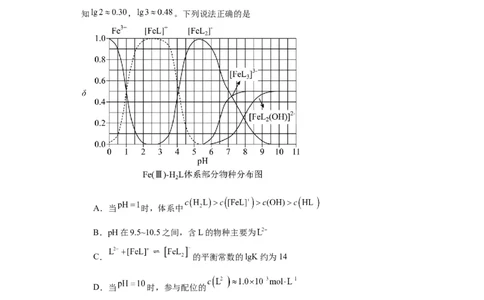
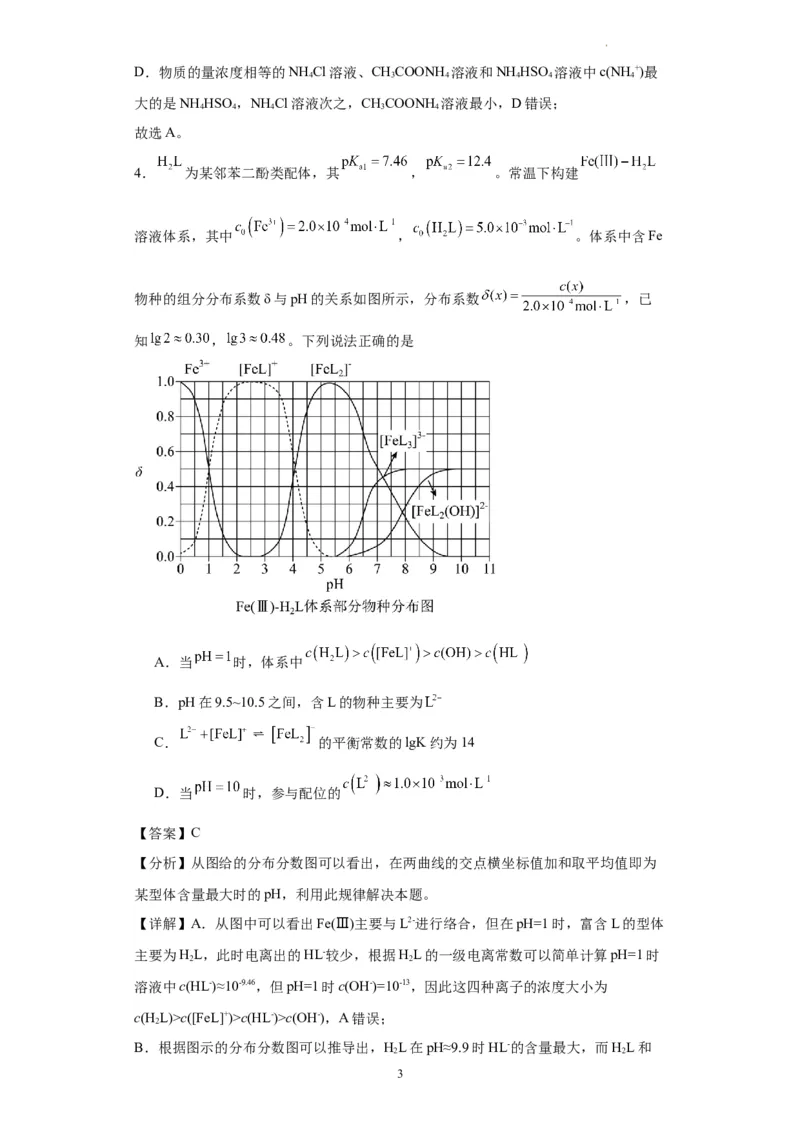
4. 为某邻苯二酚类配体,其 , 。常温下构建
溶液体系,其中 , 。体系中含Fe
物种的组分分布系数δ与pH的关系如图所示,分布系数 ,已
知 , 。下列说法正确的是
A.当 时,体系中
B.pH在9.5~10.5之间,含L的物种主要为
C. 的平衡常数的lgK约为14
D.当 时,参与配位的
【答案】C
【分析】从图给的分布分数图可以看出,在两曲线的交点横坐标值加和取平均值即为
某型体含量最大时的pH,利用此规律解决本题。
【详解】A.从图中可以看出Fe(Ⅲ)主要与L2-进行络合,但在pH=1时,富含L的型体
主要为HL,此时电离出的HL-较少,根据HL的一级电离常数可以简单计算pH=1时
2 2
溶液中c(HL-)≈10-9.46,但pH=1时c(OH-)=10-13,因此这四种离子的浓度大小为
c(H L)>c([FeL]+)>c(HL-)>c(OH-),A错误;
2
B.根据图示的分布分数图可以推导出,HL在pH≈9.9时HL-的含量最大,而HL和
2 2
3
学科网(北京)股份有限公司L2-的含量最少,因此当pH在9.5~10.5之间时,含L的物种主要为HL-,B错误;
C.该反应的平衡常数K= ,当[FeL ]-与[FeL]+分布分数相等时,可以将
2
K简化为K= ,此时体系的pH=4,在pH=4时可以计算溶液中c(L2-)=5.0×10-14.86,
则该络合反应的平衡常数K≈10-14.16,即lg K≈14,C正确;
D.根据图像,pH=10时溶液中主要的型体为[FeL ]3-和[FeL (OH)]2-,其分布分数均为
3 2
0.5,因此可以得到c([FeL ]3-)=c([FeL (OH)]2-)=1×10-4mol·L-1,此时形成[FeL ]3-消耗了
3 2 3
3×10-4mol·L-1的L2-,形成[FeL (OH)]2-消耗了2×10-4mol·L-1的L2-,共消耗了5×10-
2
4mol·L-1的L2-,即参与配位的c(L2-)≈5×10-4,D错误;
故答案选C。
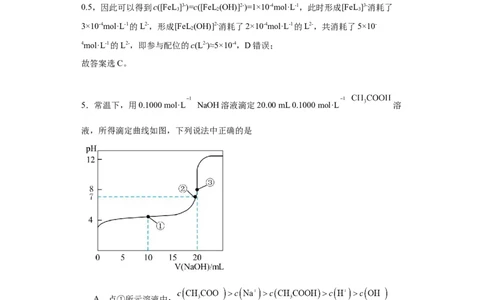
5.常温下,用0.1000 mol·L NaOH溶液滴定20.00 mL 0.1000 mol·L 溶
液,所得滴定曲线如图,下列说法中正确的是
A.点①所示溶液中:
B.点②所示溶液中:
C.点③所示溶液中:
D.点②所示的溶液中:
【答案】A
【分析】点①是加入了10ml的NaOH,此时溶液中有CHCOONa和CHCOOH共存,
3 3
资料收集整理【淘宝店铺:向阳百分百】 第4页,共20页物质的量之比为1:1,点②是pH=7的点,此时溶液显中性,但醋酸没有完全反应,
点③是加入NaOH溶液20ml,正好完全反应生成醋酸钠正盐,溶液显碱性。
【详解】A.点①是CHCOONa和CHCOOH物质的量之比为1:1,存在电荷守恒和
3 3
物料守恒,c(CHCOO-)+c(OH-)=c(Na+)+c(OH-)、2c(Na+)= c(CHCOO-)+c(CH COOH),
3 3 3
由于此时溶液显酸性,c(H+)>c(OH-),得出
,故A正确;
B.点②溶液呈中性,但是醋酸过量, ,故B错
误;
C.点③溶液是醋酸钠溶液,醋酸根离子水解显碱性,但氢离子和氢氧根离子都是少量
离子,正确的离子关系是 ,故C错误;
D.点②溶液呈中性,离子关系是 ,故D错
误;
答案选A。
6.已知: 。室温下,向0.10mol/LHX溶液中滴加0.10mol/
LNaOH溶液,溶液pH随 变化关系如图所示。下列说法错误的是
A.溶液中水的电离程度:a<b<c
B.b点溶液中:
C.c点溶液中:
5
学科网(北京)股份有限公司D.室温下NaX的水解平衡常数为
【答案】C
【分析】电离平衡常数只受温度的影响,因此用a或c点进行判断,用a点进行分析,
,c(H+)=10-3.75mol·L-1,HX的电离平衡常数的表达式
,代入数值,Ka=10-4.75,由于a、b、c均为酸性溶液,因此溶质均
为HX和NaX,不可能是NaX或NaX和NaOH,pH<7说明HX的电离程度大于X-的
水解程度,即只考虑HX电离产生H+对水的抑制作用,然后进行分析;
【详解】A.根据图示可知,a、b、c均为酸性溶液,则溶质为HX和NaX,pH<7的
溶液中,HX的电离程度大于X-的水解程度,可只考虑H+对水的电离的抑制,溶液pH
越大氢离子浓度越小,水的电离程度越大,则溶液中水的电离程度:a c(OH-),则c(Na+)<10c(HX),C错误;
D.HX在溶液中存在电离平衡:HX H++X-,Ka= ,则pH=pKa+p[
⇌
],带入c点坐标(1,5.75)可知,pKa=4.75,则Ka=10-4.75,则室温下室温下NaX
的水解平衡常数K = =10-9.25,D正确;
h
故合理选项是C。
7.下列关于电解质溶液的叙述正确的是
资料收集整理【淘宝店铺:向阳百分百】 第6页,共20页A.常温下,pH=7的NH Cl与氨水的混合溶液中离子浓度大小顺序为c(Cl-)>c(NH
4
)>c(H+)>c(OH-)
B.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同
D.常温下,同浓度的NaS与NaHS溶液相比,NaS溶液的pH大
2 2
【答案】D
【详解】A.常温下,溶液的pH=7,c(H+)=c(OH-),再结合电荷守恒得溶液中c
(Cl-)=c(NH +),溶液中离子浓度大小顺序为c(Cl-)=c(NH+)>c(H+)=c(OH-),选
4 4
项A错误;
B.醋酸在稀释的过程中,c(H+)减小,水的离子积常数K 不变,c(OH-)升高,选
W
项B错误;
C.醋酸是弱电解质,氯化氢是强电解质,pH相等的醋酸和盐酸,c(CHCOOH)大
3
于c(HCl),等体积等pH的两种酸,醋酸的物质的量大于盐酸,所以醋酸消耗的氢
氧化钠多,选项C错误;
D.常温下, NaS的水解程度比NaHS大,同浓度的NaS溶液碱性强于NaHS溶液,
2 2
所以NaS溶液的pH大,选项D正确;
2
答案选D。
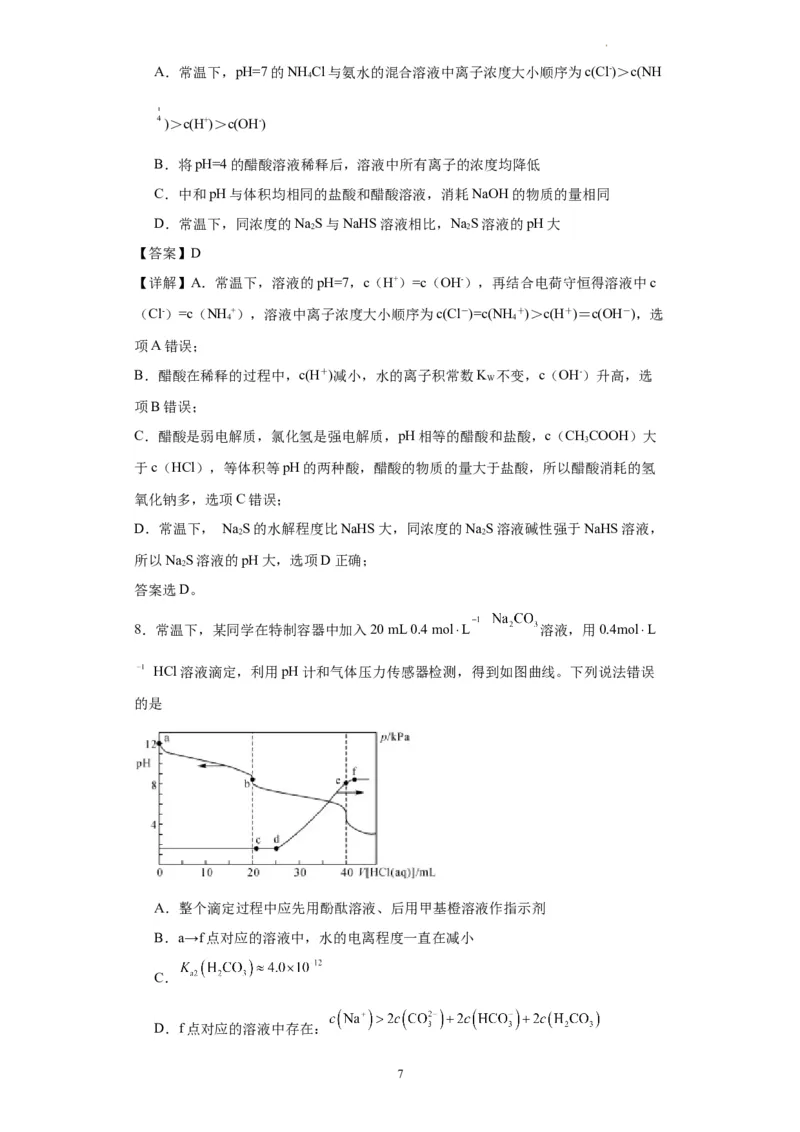
8.常温下,某同学在特制容器中加入20 mL 0.4 mol⋅L 溶液,用0.4mol⋅L
HCl溶液滴定,利用pH计和气体压力传感器检测,得到如图曲线。下列说法错误
的是
A.整个滴定过程中应先用酚酞溶液、后用甲基橙溶液作指示剂
B.a→f点对应的溶液中,水的电离程度一直在减小
C.
D.f点对应的溶液中存在:
7
学科网(北京)股份有限公司【答案】C
【详解】A.酚酞的pH变色范围是8.2~10,甲基橙的pH变色范围是3.1~4.4。
溶液与逐滴滴入的HCl溶液分两步发生反应:第一步反应是
;第二步反应是
。整个滴定过程中应先用酚酞溶液、后用甲基橙
溶液作指示剂,A正确;
B.盐水解促进水电离,水解程度越大水电离程度越大,酸溶液抑制水电离,a点对应
溶液的溶质为 ,b点对应溶液的溶质为( 、NaCl,e点对应溶液的溶
质主要为NaCl、 ,f点对应溶液的溶质主要为NaCl、HCl,因此水的电离程度
一直在减小,B正确;
C.根据图像可知,当 mL时,为0.4 mol·L 溶液,此时溶
液 , mol⋅L ,则常温下此时溶液中 mol⋅L ,则
水解平衡常数 ,因为
,故 ,C错误;
D.由于反应产生了大量的 气体,因此根据物料守恒可知f点对应的溶液中存在:
,D正确;
故选C。
9.下列判断不正确的是
资料收集整理【淘宝店铺:向阳百分百】 第8页,共20页A.在 的 溶液中
B. 溶液和 溶液中所含微粒种类相同
C.氨水和 溶液混合,形成 的溶液中
D. 的 溶液中
【答案】A
【详解】A.根据碳元素守恒可知, ,A错
误;
B.NaCO 与NaHCO 溶液中均含有HO、Na+、HCO、HCO 、CO 、H+、OH-,故
2 3 3 2 2 3
所含微粒种类相同,B正确;
C.氨水和NH Cl溶液混合,形成pH=19的溶液,则 ,根据电荷守恒
4
c(Cl-)+c(OH-)=c(NH )+c(H+),则 ,故 ,
C正确;
D.根据电荷守恒可知, ,D正确;
故选A。
10.常温下,二元酸HA的K (H A)= 1.0 ×10-2。 在某体系中,H+与A2-离子不能穿过
2 a2 2
隔膜,HA-可自由穿过该膜(如图所示)。溶液中c (H A)=c(HA-)+c(A2-),当达到平衡时,
总 2
下列叙述正确的是
A.溶液I中: c(H+)-c(OH-)=c (H A)
总 2
B.溶液II中: c (H A) >c(H+)>c(HA-) >c(OH-)
2
9
学科网(北京)股份有限公司C.溶液I和II中的c (H A)不相等
总 2
D.溶液I和II中的c(A2-)之比为105
【答案】C
【分析】由c (H A)=c(HA-)+c(A2-)可知溶液中不存在HA分子,说明HA的第一步电
总 2 2 2
离是完全电离,由H+与A2-离子不能穿过隔膜,HA-可自由穿过该膜可知溶液I和溶液
II中HA-的浓度相同。
【详解】A.溶液I中pH=7.0,c(H+)=c(OH-),A错误;
B.HA的第一步电离是完全电离,所以溶液中不存在HA分子,B错误;
2 2
C.结合K (H A)=1.0 ×10-2可计算出c(A2-)= ,又因溶液I
a2 2
和溶液II中HA-的浓度相同而H+浓度不同,因此c(A2-)的浓度不同,又因c (H A)
总 2
=c(HA-)+c(A2-),故溶液I和II中的c (H A)不相等,C正确;
总 2
D.由c(A2-)= 可计算出二者c(A2-)的比值为10-1:10-7=106,
D错误;
故选C。
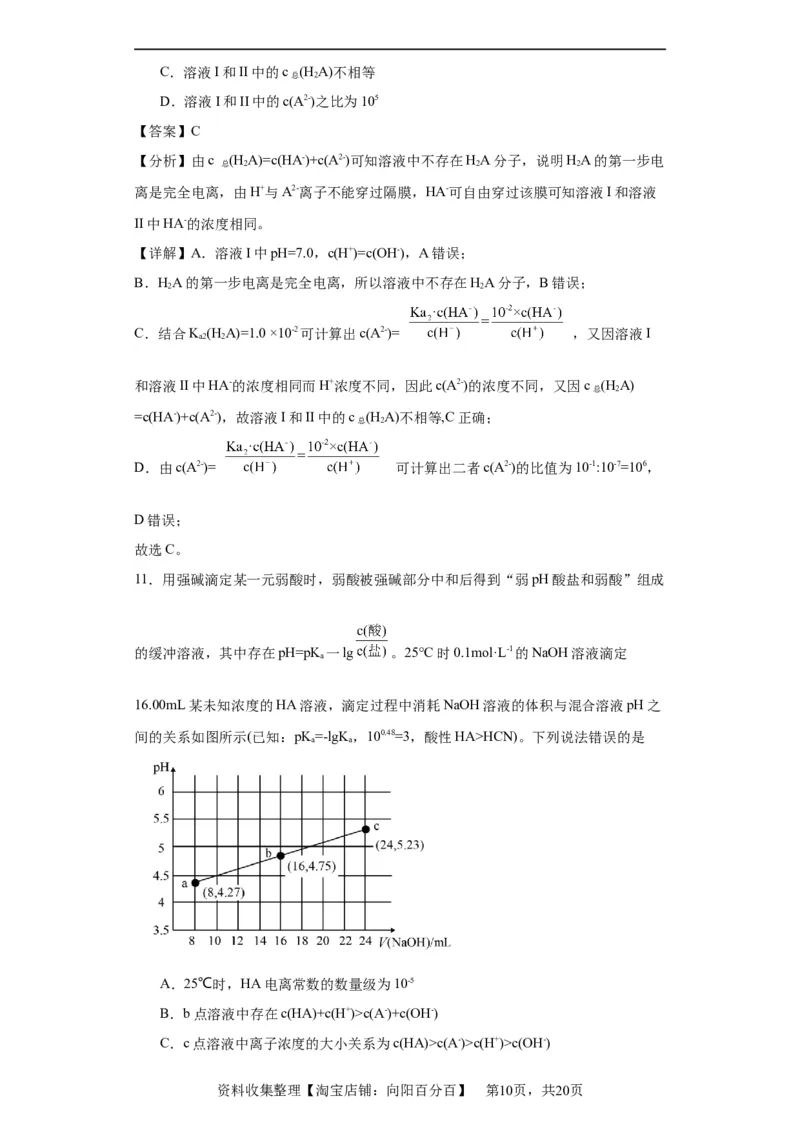
11.用强碱滴定某一元弱酸时,弱酸被强碱部分中和后得到“弱pH酸盐和弱酸”组成
的缓冲溶液,其中存在pH=pK 一lg 。25°C时0.1mol·L-1的NaOH溶液滴定
a
16.00mL某未知浓度的HA溶液,滴定过程中消耗NaOH溶液的体积与混合溶液pH之
间的关系如图所示(已知:pK=-lgK,100.48=3,酸性HA>HCN)。下列说法错误的是
a a
A.25℃时,HA电离常数的数量级为10-5
B.b点溶液中存在c(HA)+c(H+)>c(A-)+c(OH-)
C.c点溶液中离子浓度的大小关系为c(HA)>c(A-)>c(H+)>c(OH-)
资料收集整理【淘宝店铺:向阳百分百】 第10页,共20页D.若将HA改为等体积、等浓度的HCN,则pH随NaOH溶液体积的变化曲线竖
直上移
【答案】C
【分析】温度不变,酸的电离常数不变,设酸的浓度为 ,由 ,
可得 ,a点 、pH=4.27,b点 、溶液
的pH=4.75,存在 ,化简得 ,解得
c=0.2,以此解答。
【详解】A. 即 ,HA电离常数的数量级为 ,
故A正确;
B.由分析可知 ,b点时 ,故 ,
此时溶液显酸性, ,故 ,故B正确;
C.由B项分析可知b点时,故 ,则随氢氧化钠溶液体积增大,c点时溶
液 ,由图可知溶液呈酸性 ,酸电离程度较小,所以离子浓
度的大小关系为: ,故C错误;
D.由HA的酸性强于HCN可知,HA的电离常数大于HCN,由 可知,
当 相等时,酸的电离常数越大,溶液$pH$越小,则若将HA改为等体积等浓度
的HCN,则pH随NaOH溶液体积的变化曲线竖直上移,故D正确;
故选C。
12.食用级NaHSO 产品用作防腐剂、抗氧化剂等。根据常温时下列实验得到的粒子
3
浓度关系正确的是
11
学科网(北京)股份有限公司实
实验操作和现象 粒子浓度的关系
验
向蓝色石蕊试纸上滴入2滴0.1 mol c(Na+) >c( ) >c( )
①
·L-1NaHSO 溶液,试纸变红
3 >c(H SO )
2 3
向10 mL0.1 mol ·L-1NaHSO 溶液中加入等体 c(Na+)-c( ) -c( )
② 3
积等浓度的NaOH溶液 -c(HSO ) =0.05 mol ·L-1
2 3
向0.1 mol ·L-1NaHSO 溶液中加入等浓度的
③ 3 c( ) +c( )=c(Na+)
NaOH溶液至pH=7
A.①③ B.②③ C.①② D.①②③
【答案】C
【详解】NaHSO 溶液中存在 电离平衡 和水解平衡过程, 、
3
、 ;向蓝色石蕊试纸上滴入2滴0.1 mol
·L-1NaHSO 溶液,试纸变红,证明0.1 mol ·L-1NaHSO 溶液呈酸性, ,
3 3
溶液中 电离大于水解,故c(Na+) > c( ) >c( ) >c(HSO ),①正确;
2 3
向10 mL0.1 mol ·L-1NaHSO 溶液中加入等体积等浓度的NaOH溶液,两溶液等体积混
3
合,混合后溶液中钠离子浓度降为原来的一半,则c(Na+)=0.1 mol ·L-1,c(OH-)=0.05
mol ·L-1,根据题意c( ) +c( ) +c(HSO )=c(OH-),故c(Na+)-c( ) -c( )
2 3
-c(HSO ) =0.05 mol ·L-1,②正确;
2 3
向0.1 mol ·L-1NaHSO 溶液中加入等浓度的NaOH溶液至pH=7,溶液中存在电荷守恒
3
,溶液pH=7,即 ,则
,故③错误。
故选C。
13.25°C时,向20mL 0.10mol·L-1的一元酸HA (K =1.0×10-2) 中逐滴加入0.10mol·L-
a
1NaOH溶液,溶液pH随加入NaOH溶液体积的变化关系如图所示,下列说法正确的
是
资料收集整理【淘宝店铺:向阳百分百】 第12页,共20页A.a点时,c (H+) +0.1=c (HA) +c (OH-)
B.b点时水电离出的c (OH -) =10-2mol·L-1
C.滴加NaOH溶液过程中,不存在c (H+) >c (A-) >c (Na+) >c (OH-)
D.c点时,c (Na+) =c (A-) =c (H+) =c (OH-)
【答案】C
【分析】由图可知,a点溶液pH为2,由HA的电离常数K = =1.0×10—2可
a
知,溶液中A—离子浓度与HA的浓度相等,则反应所得溶液为NaA和HA的混合溶液;
由电离常数K = 可知,NaA的水解常数为K = = =
a h
=1.0×10-12,由图可知,b点溶液pH为12,则溶液中A—离子浓度是HA的
浓度的1010倍,反应所得溶液为NaA和NaOH的混合溶液。
【详解】A.由分析可知,a点为A—离子浓度与HA的浓度相等的NaA和HA的混合
溶液,溶液中存在电荷守恒关系c(Na+)+ c(H+)=c(A—)+ c(OH—),溶液中钠离子浓度为
≠0.1mol/L,则溶液中c (H+) +0.1≠c (HA) +c (OH-),故A错误;
B.由分析可知,b点为NaA和NaOH的混合溶液,则溶液中水电离出的氢氧根离子浓
度小于10-2 mol/L,故B错误;
C.若溶液中离子浓度的关系为c (H+) >c (A-) >c (Na+) >c (OH-),溶液中阳离子的电
荷总数大于阴离子电荷总数,不符合电荷守恒的原则,所以滴加氢氧化钠溶液过程中,
溶液中不存在c (H+) >c (A-) >c (Na+) >c (OH-),故C正确;
13
学科网(北京)股份有限公司D.由图可知,c点时溶液pH为7,溶液中氢离子浓度与氢氧根离子浓度相等,则由
电荷守恒关系c(Na+)+ c(H+)=c(A—)+ c(OH—)可知,溶液中离子浓度的关系为c (Na+)
=c (A-) >c (H+) =c (OH-),故D错误;
故选C。
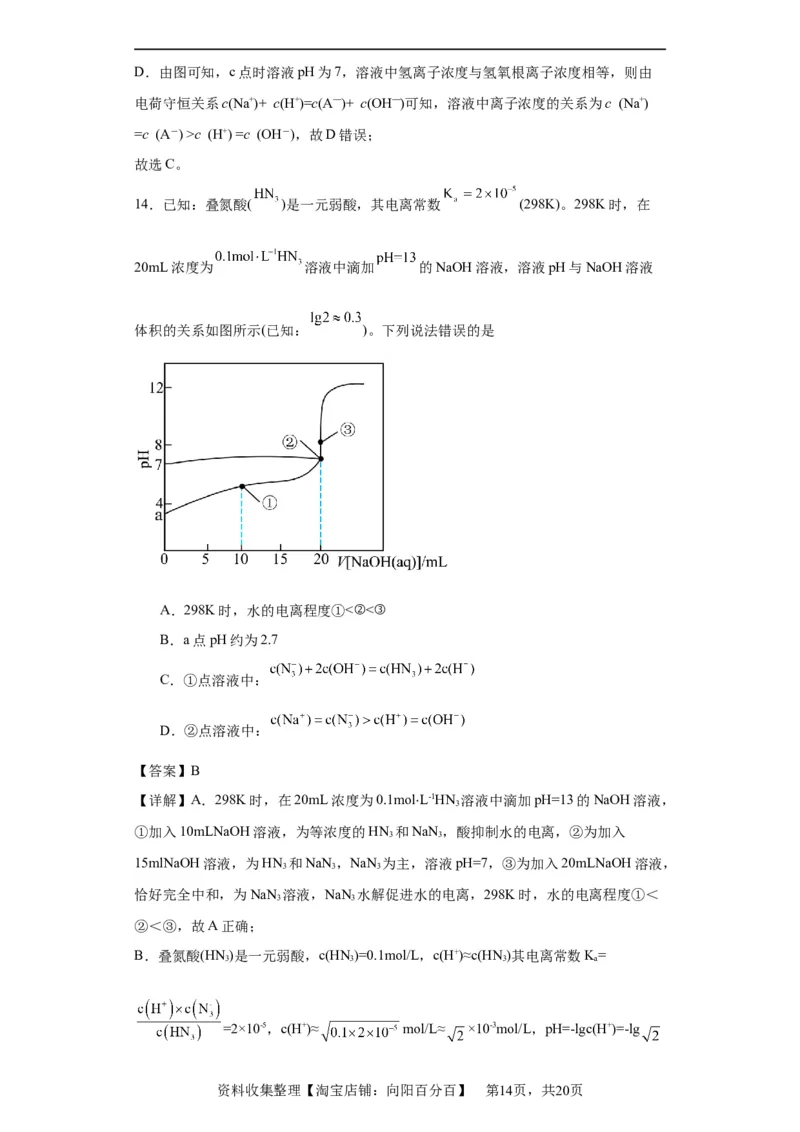
14.已知:叠氮酸( )是一元弱酸,其电离常数 (298K)。298K时,在
20mL浓度为 溶液中滴加 的NaOH溶液,溶液pH与NaOH溶液
体积的关系如图所示(已知: )。下列说法错误的是
A.298K时,水的电离程度①<②<③
B.a点pH约为2.7
C.①点溶液中:
D.②点溶液中:
【答案】B
【详解】A.298K时,在20mL浓度为0.1molL-1HN 溶液中滴加pH=13的NaOH溶液,
3
①加入10mLNaOH溶液,为等浓度的HN 和N⋅aN ,酸抑制水的电离,②为加入
3 3
15mlNaOH溶液,为HN 和NaN ,NaN 为主,溶液pH=7,③为加入20mLNaOH溶液,
3 3 3
恰好完全中和,为NaN 溶液,NaN 水解促进水的电离,298K时,水的电离程度①<
3 3
②<③,故A正确;
B.叠氮酸(HN )是一元弱酸,c(HN )=0.1mol/L,c(H+)≈c(HN )其电离常数K=
3 3 3 a
=2×10-5,c(H+)≈ mol/L≈ ×10-3mol/L,pH=-lgc(H+)=-lg
资料收集整理【淘宝店铺:向阳百分百】 第14页,共20页×10-3=3- lg2≈2.85,故B错误;
C.①点溶液中存在电荷守恒:c(H+)+c(Na+)=c(OH-)+c( ),物料守恒为:2c(Na+)=c(
)+c(HN),整理得到:c( )+2c(OH-)=c(HN)+2c(H+),故C正确;
3 3
D.②点溶液pH=7,溶液显中性,液中存在电荷守恒:c(H+)+c(Na+)=c(OH-)+c( ),
得到c(Na+)=c( )>c(H+)=c(OH-),故D正确;
故选:B。
15.向两个相同的容器中分别加入20mL 溶液和40mL
溶液,然后分别滴加 盐酸,滴加过程中溶液的pH、容器中气体压力
随盐酸的体积的变化如图所示。下列说法正确的是
A.曲线甲表示向 溶液中滴加盐酸,曲线乙表示向 溶液中滴加盐
酸
B.当滴加盐酸的体积为 mL时(b点),溶液中:
C.滴定时,a点可用酚酞、c点可用甲基橙作指示剂指示滴定终点
D.向40mL 溶液容器中滴加盐酸体积为20mL时,溶液中:
15
学科网(北京)股份有限公司【答案】C
【详解】A.碳酸钠的水解程度大于碳酸氢钠,故碳酸钠的碱性强于碳酸氢钠,碳酸
钠与盐酸反应先生成碳酸氢钠,再产生二氧化碳气体,故图中甲曲线表示向NaCO 溶
2 3
液中滴加盐酸,乙曲线表示向NaHCO 溶液中滴加盐酸,故A错误;
3
B.当滴加盐酸的体积为 mL时(b点),溶液中溶质是碳酸氢钠、氯化钠,溶液显碱性,
根据电荷守恒溶液中存在: ,
物料守恒 ,因此有
,故B错误;
C.滴定时,a点消耗盐酸20mL,碳酸钠恰好转化为碳酸氢钠,c点碳酸氢钠恰好转化
为二氧化碳,a点的pH在9左右,符合酚酞的指示范围,故可用酚酞作指示剂;c点
的pH在4左右,符合甲基橙的指示范围,故可用甲基橙作指示剂指示滴定终点,因此
滴定时,a点可用酚酞、c点可用甲基橙作指示剂指示滴定终点,故C正确;
D.向40mL 溶液容器中滴加盐酸体积为20mL时,碳酸氢钠恰好转
化为二氧化碳,二氧化碳在水中的溶解度不大,所以溶液中:
,故D错误;
故选C。
16.谷氨酸( ,用 表示)在生物体内的蛋白质代谢过程中占重要地位,
在水溶液中有4种分布形式( 、 、 和 )。常温下,用
溶液滴定 溶液。下列叙述正确的是
A. 溶液中,
B.当 时 , 时 ,则 的
资料收集整理【淘宝店铺:向阳百分百】 第16页,共20页C.当 时,
D.当 时,
【答案】C
【详解】A. 溶液中由电荷守恒可知,
,A错误;
B.当 时 , ; 时
,则 ,则 的 ,B错误;
C.当 时,溶质为等浓度的 、 、NaCl,由电荷守恒可知:
① ,由物料守恒可知:
② ;①-②得:
,C正确;
D.当 时,根据A、Cl元素守恒可知,
,D错误;
故选C。
17.室温下,向某浓度的二元碱X(OH) 水溶液中逐滴加入一定浓度的盐酸,所得溶液
2
中相关组分的物质的量分数随溶液pH变化的曲线如图所示。下列说法错误的是
17
学科网(北京)股份有限公司A.X(OH) 的K =10-4.8
2 b1
B.X(OH)Cl的水溶液显碱性
C.pH=7时,c[X(OH)]c(ClO- )
D.25 °C时,pH=7的NaClO和HClO混合溶液中存在:
资料收集整理【淘宝店铺:向阳百分百】 第18页,共20页c(HClO)c(ClO- ),故C正确;
D.25 °C时, ,则水解平衡常数 ,则水解强于电
离;由电荷守恒 ,pH=7, ,则
,由水解强于电离可知, ,故D错误;
答案选C。
19.常温下,向新制氯水中滴加NaOH溶液,溶液中水电离出的 与NaOH溶
液体积的关系如图所示。下列说法正确的是
A.用pH试纸测得E点对应的溶液pH=3
19
学科网(北京)股份有限公司B.F点对应的溶液中存在
C.G点对应的溶液中:
D.H点对应的溶液呈中性
【答案】C
【分析】由图可知,E点时,氯水中的盐酸和次氯酸电离出的氢离子抑制水的电离,
水的电离程度最小;G点时,水的电离程度最大,说明氯水中盐酸和次氯酸与氢氧化
钠溶液恰好反应生成等浓度的氯化钠和次氯酸钠,次氯酸钠在溶液中水解促进水的电
离;F点时,氢氧化钠溶液与氯水反应得到氯化钠、次氯酸钠和次氯酸的混合溶液,
溶液呈中性;H点时,氢氧化钠溶液过量,加入氢氧化钠溶液得到的是氯化钠、次氯
酸钠和氢氧化钠的混合溶液,溶液呈碱性。
【详解】A.由分析可知,E点为未加入氢氧化钠溶液的氯水,氯水中含有的次氯酸具
有强氧化性,会使有机色质漂白褪色,则用pH试纸无法测得E点氯水的pH值,故A
错误;
B.由分析可知,F点为氯化钠、次氯酸钠和次氯酸的混合溶液,溶液中电荷守恒关系
为c(Na+)+c(H+)= c(Cl-)+c(ClO-)+c(OH-),中性溶液中c(OH-)=c(H+),则溶液中
c(Na+)=c(Cl-)+c(ClO-),故B错误;
C.由分析可知,G点等浓度的氯化钠和次氯酸钠,次氯酸钠在溶液中水解使溶液呈碱
性,则溶液中离子浓度的大小关系为c(Na+)>c(Cl-)>c(ClO-)>c(OH-)>c(H+),故C正确;
D.由分析可知,H点为氯化钠、次氯酸钠和氢氧化钠的混合溶液,溶液呈碱性,故D
错误;
故选C。
20.25℃时,向一定浓度的NaC O 溶液中逐滴加入HCl,以X表示 或
2 2 4
。已知pX=-lgX,混合溶液pX与pH的关系如图所示。下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】 第20页,共20页A.曲线II表示p[ ]与pH的关系
B.HC O 第二步电离常数的数量级为10-6
2 2 4
C.pH=2.71时,c(HC O )>c(C O )>c(HC O)
2 2 2 2 4
D.pH=1.23时,c(H+)+3c(H C O)=c(OH-)+c(Cl-)
2 2 4
【答案】D
【分析】草酸属于二元弱酸,其电离方程式为HC O HC O +H+,HC O C O
2 2 4 2 2 2
+H+,K = ,K = ,K >K ,pX=-lgX,pX越大,X越
1 2 1 2
小,因此推出曲线Ⅰ代表p[ ]与pH关系,曲线Ⅱ代表 与pH关系,
据此分析;
【详解】A.根据上述分析,曲线Ⅰ代表p[ ]与pH关系,曲线Ⅱ代表
与pH关系,故A错误;
B.草酸的二级电离K = ,取(3.19,1)代入上述表达式,K =
2 2
=10-4.19,数量级约为10-5,故B错误;
C.由图可知,pH=2.71时, >0,则c(HC O )>c(C O );
2 2
21
学科网(北京)股份有限公司, ;
,此时pH=2.71,则 ,
得c(C O )=c(H C O),故C错误;
2 2 2 4
D.由电荷守恒可知, ;由物料守
恒可知, ;两式联立可得:
; ,pH=1.23
时, ,则有 ,故D正确;
答案为D。
资料收集整理【淘宝店铺:向阳百分百】 第22页,共20页