文档内容
知识清单 01 物质的分类及转化
知识点01 物质的分类 知识点02 纯净物和混合物
知识点03 分散系和胶体 知识点04 物质间关系
知识点05 物质的变化 知识点06 物质的转化知识点 01 物质的分类
1.元素、物质及微粒
(1)元素的存在形态:
①游离态:元素以 形式存在的状态。
②化合态:元素以 形式存在的状态。
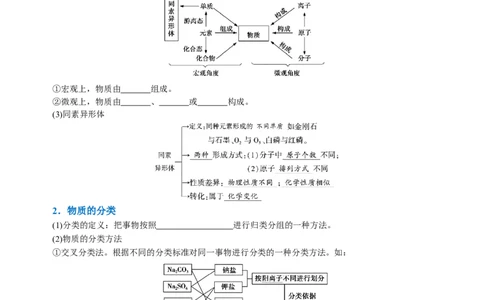
(2)元素、微粒及物质间的关系图
①宏观上,物质由 组成。
②微观上,物质由 、 或 构成。
(3)同素异形体
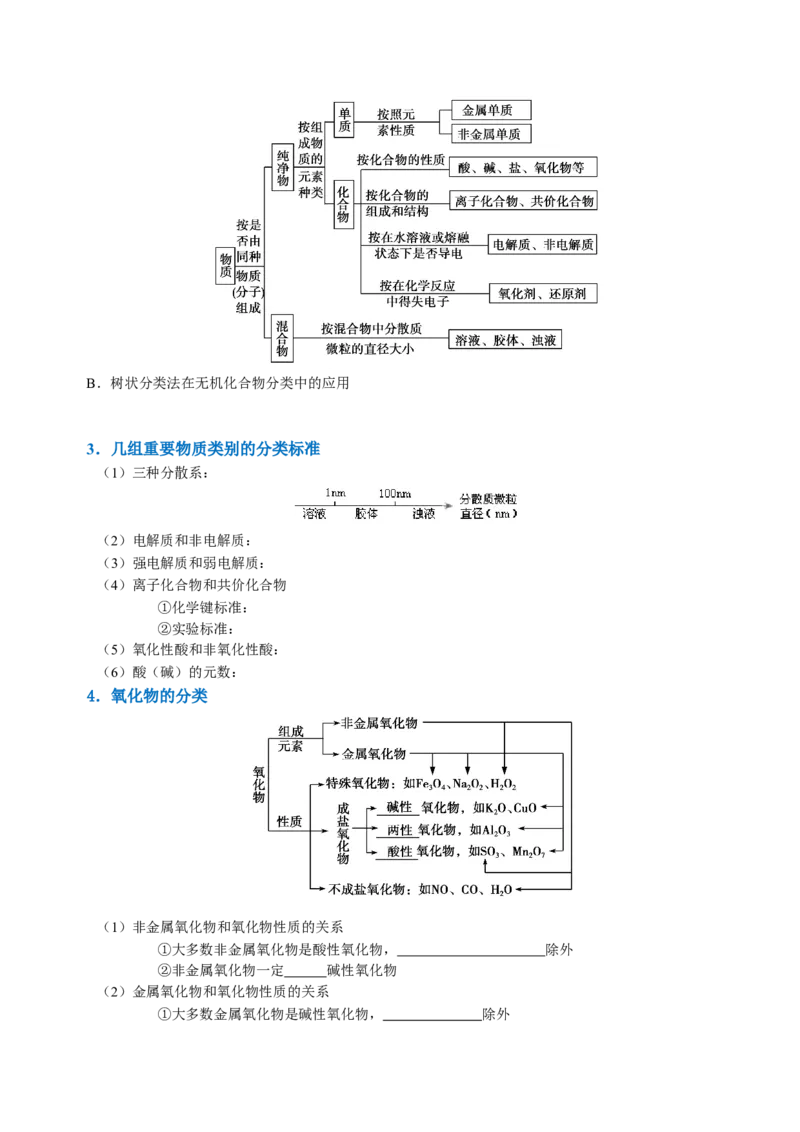
2.物质的分类
(1)分类的定义:把事物按照 进行归类分组的一种方法。
(2)物质的分类方法
①交叉分类法。根据不同的分类标准对同一事物进行分类的一种分类方法。如:
②树状分类法
简单地说,是将被分类对象按照从属关系逐级进行(不同层次)分类的一种分类方法,其陈列式的形状像
树。
A.明确分类标准是对物质正确树状分类的关键B.树状分类法在无机化合物分类中的应用
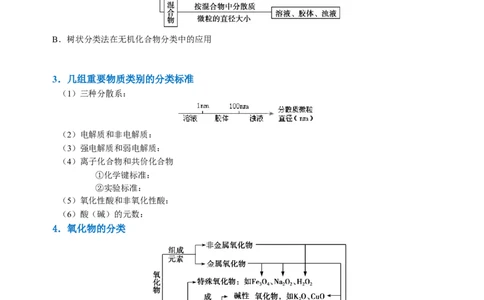
3.几组重要物质类别的分类标准
(1)三种分散系:
(2)电解质和非电解质:
(3)强电解质和弱电解质:
(4)离子化合物和共价化合物
①化学键标准:
②实验标准:
(5)氧化性酸和非氧化性酸:
(6)酸(碱)的元数:
4.氧化物的分类
(1)非金属氧化物和氧化物性质的关系
①大多数非金属氧化物是酸性氧化物, 除外
②非金属氧化物一定 碱性氧化物
(2)金属氧化物和氧化物性质的关系
①大多数金属氧化物是碱性氧化物, 除外②少数金属氧化物是酸性氧化物:如 (HMnO 的酸酐)
4
③少数金属氧化物是两性氧化物,如
④碱性氧化物 是金属氧化物
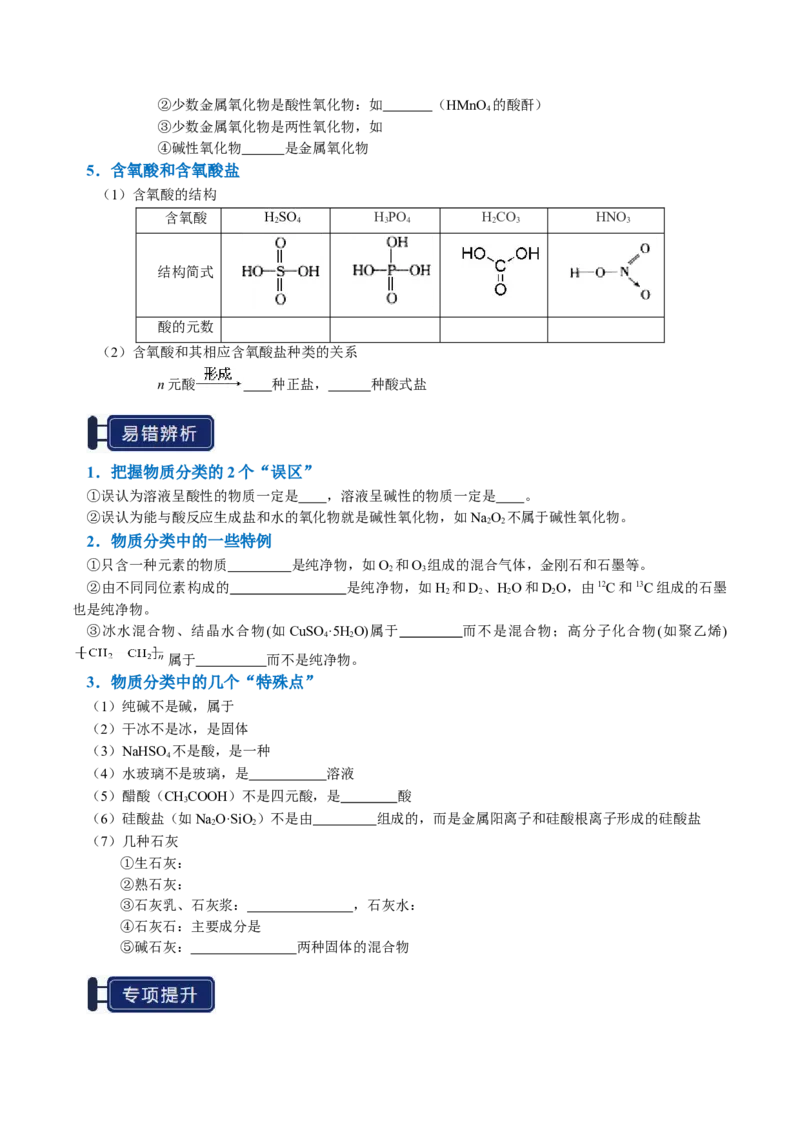
5.含氧酸和含氧酸盐
(1)含氧酸的结构
含氧酸 HSO HPO HCO HNO
2 4 3 4 2 3 3
结构简式
酸的元数
(2)含氧酸和其相应含氧酸盐种类的关系
n元酸 种正盐, 种酸式盐
1.把握物质分类的2个“误区”
①误认为溶液呈酸性的物质一定是 ,溶液呈碱性的物质一定是 。
②误认为能与酸反应生成盐和水的氧化物就是碱性氧化物,如NaO 不属于碱性氧化物。
2 2
2.物质分类中的一些特例
①只含一种元素的物质 是纯净物,如O 和O 组成的混合气体,金刚石和石墨等。
2 3
②由不同同位素构成的 是纯净物,如H 和D 、HO和DO,由12C和13C组成的石墨
2 2 2 2
也是纯净物。
③冰水混合物、结晶水合物(如CuSO ·5H O)属于 而不是混合物;高分子化合物(如聚乙烯)
4 2
属于 而不是纯净物。
3.物质分类中的几个“特殊点”
(1)纯碱不是碱,属于
(2)干冰不是冰,是固体
(3)NaHSO 不是酸,是一种
4
(4)水玻璃不是玻璃,是 溶液
(5)醋酸(CHCOOH)不是四元酸,是 酸
3
(6)硅酸盐(如NaO·SiO)不是由 组成的,而是金属阳离子和硅酸根离子形成的硅酸盐
2 2
(7)几种石灰
①生石灰:
②熟石灰:
③石灰乳、石灰浆: ,石灰水:
④石灰石:主要成分是
⑤碱石灰: 两种固体的混合物1.下列各组物质分类正确的是
混合
选项 纯净物 酸 碱 盐 酸性氧化物 碱性氧化物
物
碱石
A 液氯 HPO 纯碱 NaHSO CO NaO
3 4 4 2
灰
B 石墨 盐酸 HNO 烧碱 NaHCO SO CuO
3 3 2
C 大理石 碘酒 CHCOOH 苛性钾 NaCl MnO Al O
3 2 7 2 3
漂白
D 空气 HS 熟石灰 KClO SiO CaO
2 3 2
粉
2.下列物质分类正确的有几项
①混合物:铝热剂、氯水、水玻璃、漂白粉
②胶体:饱和氯化铁溶液、淀粉溶液、牛奶
③酸性氧化物: 、 、 、NO
2
④同素异形体: 、 、金刚石、石墨
⑤电解质: 、 、NaOH、冰醋酸
⑥硅酸盐产品:水晶、水泥、陶瓷
⑦碱:苛性钠、纯碱、熟石灰
⑧盐:胆矾、小苏打、铜绿
⑨放热反应:盐酸与氢氧化钠、碳与二氧化碳高温化合成一氧化碳、甲烷燃烧
A.2 B.3 C.4 D.5
知识点 02 纯净物和混合物
1.本质区别:是否由一种 组成
(1)由同种元素组成的物质 是纯净物,如氧气和臭氧的混合物
(2)由同种分子组成的物质 是纯净物
(3)由不种分子组成的物质 是混合物,如HD和HT是不同的氢气分子,一般认为是纯净物
(4)分子式相同的物质 是纯净物,如同分异构体
(5)相对分子质量相同的物质 是纯净物,如乙烯、一氧化碳、氮气
(6)某金属元素的阳离子和某非金属元素的阴离子构成的物质 是纯净物,如氧化钠和过氧化
钠都是由钠元素的阳离子和氧元素的阴离子构成的
2.“名不符实”的物质
(1) 冰水混合物 冰和水是同一物质的 状态
(2) 纯净的盐酸 盐酸是氯化氢气体的水溶液,属于(3) 纯净的矿泉水 矿泉水中含有少量的矿物质杂质,属于
(4) 纯净的二氧化氮 存在双聚平衡:2NO NO,NO 中一定含
2 2 4 2
(5) 高分子化合物 聚合度n值不同,所有的高聚物都是
(6) 化合物HD 是一种氢气分子,属于
3.常见的混合物
(1) 分散系 、 、
天然高分子化合
、 、 、
(2) 高分子化合物 物:
合成高分子化合物 、 、
(3) 三大化石燃料 、 、
石油分馏产品 、 、 、 、 、
石油及其加工
(4) 石油裂化产品 裂化汽油:含烷烃和烯烃
产品
石油裂解产品 石油裂解气( 、 、 )
水煤气 和
煤及其加工产
(5) 焦炉气: H、CH、C H、CO
品 2 4 2 4
煤焦油 粗苯、粗氨水、酚类、萘和沥青
(6) 油脂 和
氨水 的水溶液
氯水 的水溶液
水玻璃 溶液
(7 水银
几种“水”
) 重水
超重水
王水 浓盐酸和浓硝酸按照体积比 组成的混合物
铁水 液态铁
碱石灰
(8 常见的无机混 铝热剂
) 合物 合金 金属和金属或非金属组成的
漂白粉
4.常见的纯净物
(1)氯仿: 的俗名
(2)酒精: 的俗名
(3)冰醋酸: 的俗名
(4)甘油:结构简式为 ,属于 物质
(5)结晶水合物:如CuSO ·5HO
4 2(1)纯净物 有固定的熔、沸点,有固定熔、沸点的物质一定是纯净物。
(2)某物质经科学测定只含有一种元素,可以断定该物质 是一种单质。
(3)由同种元素组成的物质 是纯净物,如氧气和臭氧的混合物
(4)由同种分子组成的物质 是纯净物
(5)由不种分子组成的物质 是混合物,如HD和HT是不同的氢气分子,一般认为是纯净物
(6)分子式相同的物质 是纯净物,如同分异构体
(7)相对分子质量相同的物质 是纯净物,如乙烯、一氧化碳、氮气
(8)某金属元素的阳离子和某非金属元素的阴离子构成的物质 是纯净物,如氧化钠和过氧化
钠都是由钠元素的阳离子和氧元素的阴离子构成的
3.科学家制得一种新型分子 。关于 和 的下列说法不正确的是
A. 和 互为同位素 B. 和 均属于纯净物
C.都属于单质 D. 和 的化学性质不相同
4.某种物质经检测,只含有一种元素,则该物质
A.一定是纯净物 B.一定是单质 C.一定不是化合物 D.一定是混合物
5.下列说法正确的是
①由一种元素组成的物质一定是纯净物②冰水混合物是纯净物③金属氧化物一定是碱性氧化物④非金属氧
化物不一定是酸性氧化物⑤ 是混合物
A.①② B.②④ C.②⑤ D.全部
知识点 03 分散系和胶体
1.分散系
定义 把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系
分散质 分散系中 的物质
组成
分散剂 分散系中 的物质
分散质
分类
按分散质、分散剂的状态分类
分为9种分散系:
(1)分散系中至少含有两种物质,都属于混合物,蒸馏水 一种分散系
(2)三种分散系之间的转化为 变化(3)透明不代表无色,如CuSO 溶液为蓝色溶液,Fe(OH) 胶体为红褐色液体。
4 3
(4)胶体不一定都呈液体,胶体除了液溶胶还有气溶胶和固溶胶。
2.胶体的性质
(1
外观
)
(2
通透性 透过滤纸, 透过半透膜
)
(3
电学特性 胶体 电荷
)
3.常见胶体
(1) 气溶胶 云、烟、雾
(2) 液溶胶 豆浆、氢氧化铝胶体、Fe(OH) 胶体、硅酸胶体
3
(3) 固溶胶 果冻、宝石、烟水晶、有色玻璃
(4) 三种有机胶体 、 、
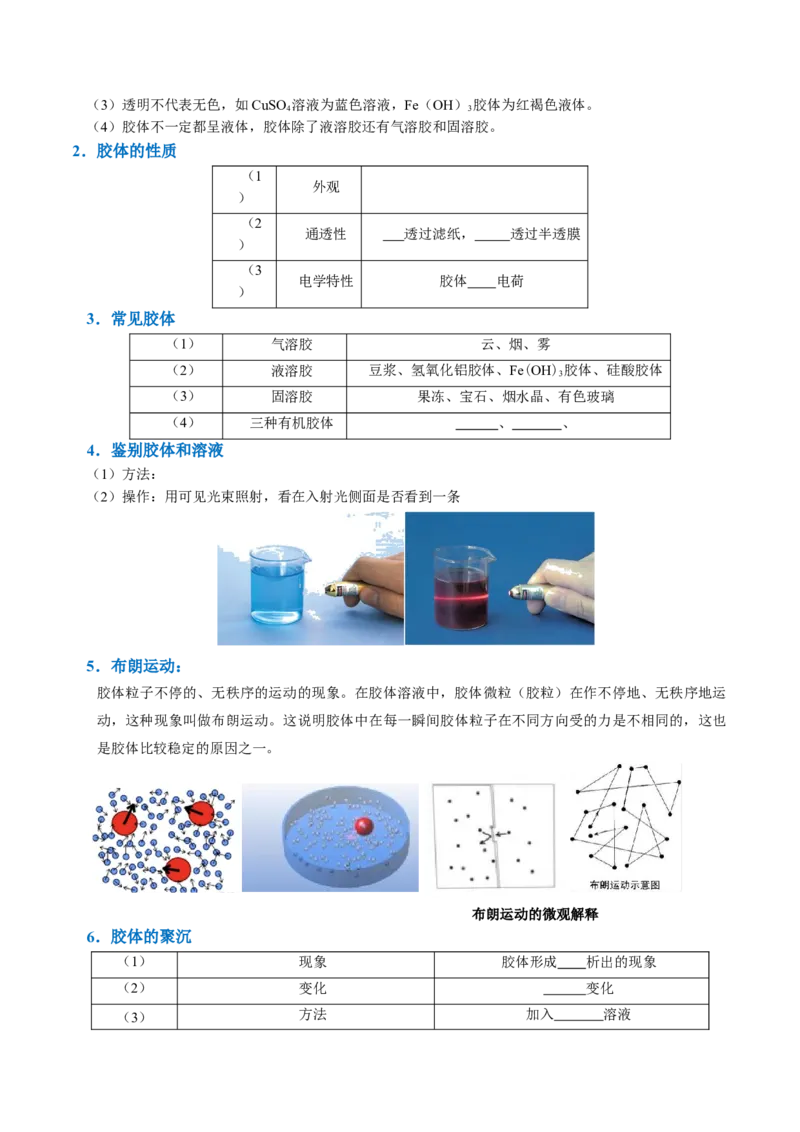
4.鉴别胶体和溶液
(1)方法:
(2)操作:用可见光束照射,看在入射光侧面是否看到一条
5.布朗运动:
胶体粒子不停的、无秩序的运动的现象。在胶体溶液中,胶体微粒(胶粒)在作不停地、无秩序地运
动,这种现象叫做布朗运动。这说明胶体中在每一瞬间胶体粒子在不同方向受的力是不相同的,这也
是胶体比较稳定的原因之一。
布朗运动的微观解释
6.胶体的聚沉
(1) 现象 胶体形成 析出的现象
(2) 变化 变化
(3) 方法 加入 溶液加入带 电荷胶粒的胶体
或
(4) Fe(OH) 胶体-----------------------→ ,
3
7.胶体的吸附性:胶体的 大,吸附能力强
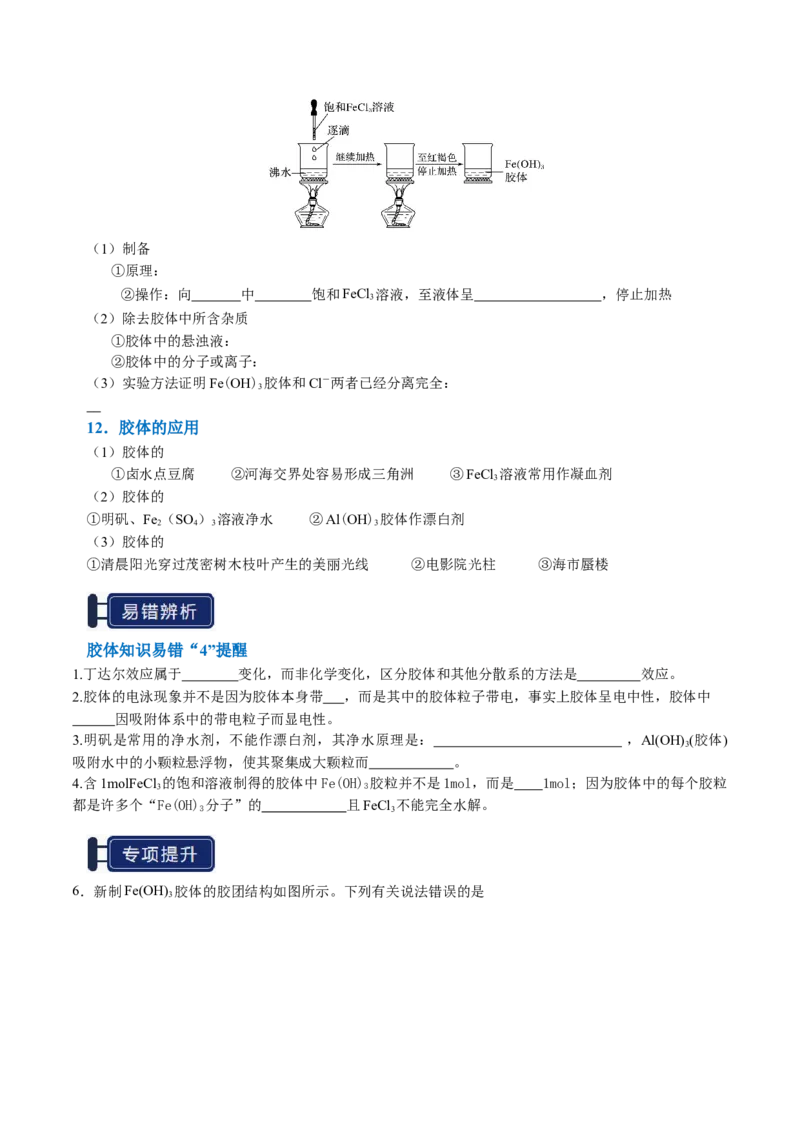
8.胶体的电泳
(1)概念:在外电场的作用下胶体微粒发生 移动
(2)原因:胶体微粒 , 能力强,吸附了带电离子而带电荷
(3)规律:带正电荷的胶粒向 极移动,带负电荷的胶粒向 极移动
(4)变化:发生 变化(电解反应)
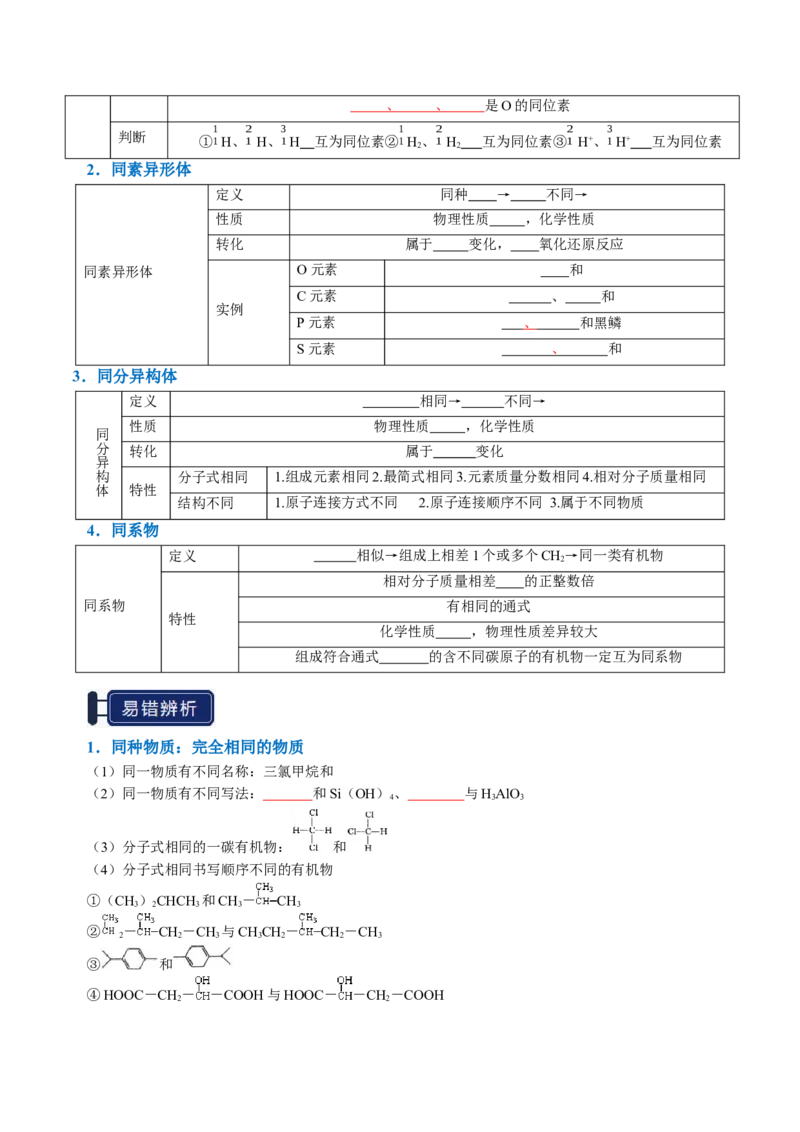
9.渗析
利用 (如羊皮纸、膀胱膜等)使胶体和其中所含的可溶性杂质分离的过程称为 ,又称透
析。半透膜的细孔能让可溶性杂质的分子或离子通过,但不能让较大的 通过,因而可以达到分
离的目的。渗析是一种物理分离方法。
10.胶体的形成
(1)形成过程:将纳米颗粒分散到适当的 中形成的一种分散系
(2)结构特点:胶粒是 聚合体
①胶体中所含胶粒的个数
②胶粒所带的电荷数
(3)胶体的介稳性:胶体的稳定性介于溶液和浊液之间,在一定条件下能稳定存在,属于 。
胶体具有介稳性的两个原因:原因一 胶体粒子可以通过吸附而带有电荷,同种胶粒带同种电荷,
而同种电荷会相互排斥(要使胶体聚沉,就要克服排斥力,消除胶粒所带电荷 )。
原因二 胶体粒子在不停地做布朗运动,与重力作用相同时便形成沉降平衡的状态。
(4)淀粉胶体的特殊性
①结构特征:淀粉胶体为 胶体,胶粒
②性质特性:加入电解质溶液 发生聚沉,通电后 发生电泳
11.Fe(OH) 胶体的制备和分离提纯
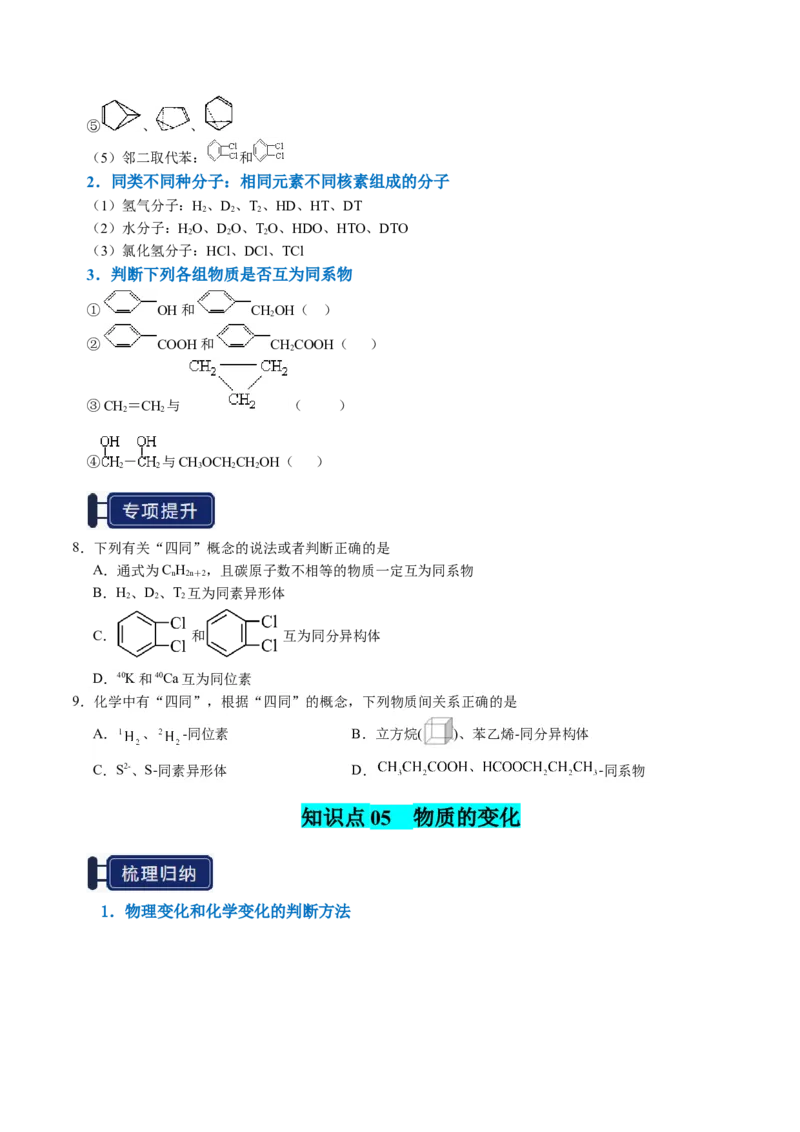
3(1)制备
①原理:
②操作:向 中 饱和FeCl 溶液,至液体呈 ,停止加热
3
(2)除去胶体中所含杂质
①胶体中的悬浊液:
②胶体中的分子或离子:
(3)实验方法证明Fe(OH) 胶体和Cl-两者已经分离完全:
3
12.胶体的应用
(1)胶体的
①卤水点豆腐 ②河海交界处容易形成三角洲 ③FeCl 溶液常用作凝血剂
3
(2)胶体的
①明矾、Fe (SO ) 溶液净水 ②Al(OH) 胶体作漂白剂
2 4 3 3
(3)胶体的
①清晨阳光穿过茂密树木枝叶产生的美丽光线 ②电影院光柱 ③海市蜃楼
胶体知识易错“4”提醒
1.丁达尔效应属于 变化,而非化学变化,区分胶体和其他分散系的方法是 效应。
2.胶体的电泳现象并不是因为胶体本身带 ,而是其中的胶体粒子带电,事实上胶体呈电中性,胶体中
因吸附体系中的带电粒子而显电性。
3.明矾是常用的净水剂,不能作漂白剂,其净水原理是: ,Al(OH) (胶体)
3
吸附水中的小颗粒悬浮物,使其聚集成大颗粒而 。
4.含1molFeCl 的饱和溶液制得的胶体中Fe(OH) 胶粒并不是1mol,而是 1mol;因为胶体中的每个胶粒
3 3
都是许多个“Fe(OH) 分子”的 且FeCl 不能完全水解。
3 3
6.新制Fe(OH) 胶体的胶团结构如图所示。下列有关说法错误的是
3A.Fe(OH) 胶体显电中性
3
B.Fe(OH) 胶团结构可表示为:{[Fe(OH) ] ·nFeO+·(n-x)Cl-}x+·xCl-
3 3 m
C.Fe(OH) 胶体中加入过量盐酸,先产生红褐色沉淀后沉淀溶解
3
D.Fe(OH) 胶团第一层和第二层共同构成胶体粒子,带正电,在外加直流电源下向阳极移动
3
7.判断正误:
(1)胶体、溶液和浊液这三种分散系的根本区别是分散质粒子直径的大小
(2)利用丁达尔效应可以区别溶液与胶体
(3)溶液是电中性的,胶体是带电的
(4)雾是气溶胶,在阳光下可观察到丁达尔效应
(5)“钴酞菁”的分子(直径为1.3×10-9m)在水中形成的分散系能产生丁达尔效应
(6)Fe(OH) 胶体无色、透明、能产生丁达尔效应
3
(7)胶体与溶液都可以通过滤纸、半透膜和分子筛
(8)用激光笔照射鸡蛋清溶液,侧面可观察到明显的光路
(9)明矾与水反应生成的Al(OH) 胶体能吸附水中悬浮物,可用于水的净化
3
(10)水泥厂、冶金厂用高压电作用于气溶胶以除去烟尘,是利用了电泳原理
(11)将“纳米材料”分散到某液体中,用滤纸过滤的方法可以从此分散系中分离得到该“纳米材料”
(12)碳纳米管属于胶体分散系,该材料具有超强的吸附能力
(13)胶体微粒可用于制备纳米材料
(14)浓氨水中滴加FeCl 饱和溶液可制得Fe(OH) 胶体
3 3
知识点 04 物质间关系
1.同位素
定义 相同→ 不同→ 元素→
性质 物理性质 ,化学性质
同 结构 同位素的核外电子排布
位
、 、 是H的同位素
素
实例
C、 C、 C是C的同位素、 、 是O的同位素
1 2 3 1 2 2 3
判断
①1H、1 H、1H 互为同位素②1H、1 H 互为同位素③1 H+、1H+ 互为同位素
2 2
2.同素异形体
定义 同种 → 不同→
性质 物理性质 ,化学性质
转化 属于 变化, 氧化还原反应
同素异形体 O元素 和
C元素 、 和
实例
P元素 、 和黑鳞
S元素 、 和
3.同分异构体
定义 相同→ 不同→
性质 物理性质 ,化学性质
同
分 转化 属于 变化
异
构 分子式相同 1.组成元素相同2.最简式相同3.元素质量分数相同4.相对分子质量相同
体 特性
结构不同 1.原子连接方式不同 2.原子连接顺序不同 3.属于不同物质
4.同系物
定义 相似→组成上相差1个或多个CH→同一类有机物
2
相对分子质量相差 的正整数倍
同系物 有相同的通式
特性
化学性质 ,物理性质差异较大
组成符合通式 的含不同碳原子的有机物一定互为同系物
1.同种物质:完全相同的物质
(1)同一物质有不同名称:三氯甲烷和
(2)同一物质有不同写法: 和Si(OH)、 与HAlO
4 3 3
(3)分子式相同的一碳有机物: 和
(4)分子式相同书写顺序不同的有机物
①(CH)CHCH 和CH- CH
3 2 3 3 3
② - CH-CH 与CHCH- CH-CH
2 2 3 3 2 2 3
③ 和
④HOOC-CH- -COOH与HOOC- -CH-COOH
2 2⑤ 、 、
(5)邻二取代苯: 和
2.同类不同种分子:相同元素不同核素组成的分子
(1)氢气分子:H、D、T、HD、HT、DT
2 2 2
(2)水分子:HO、DO、TO、HDO、HTO、DTO
2 2 2
(3)氯化氢分子:HCl、DCl、TCl
3.判断下列各组物质是否互为同系物
① OH和 CHOH( )
2
② COOH和 CHCOOH( )
2
③CH=CH 与 ( )
2 2
④ - 与CHOCH CHOH( )
2 2 3 2 2
8.下列有关“四同”概念的说法或者判断正确的是
A.通式为C H ,且碳原子数不相等的物质一定互为同系物
n 2n+2
B.H、D、T 互为同素异形体
2 2 2
C. 和 互为同分异构体
D.40K和40Ca互为同位素
9.化学中有“四同”,根据“四同”的概念,下列物质间关系正确的是
A. 、 -同位素 B.立方烷( )、苯乙烯-同分异构体
C.S2-、S-同素异形体 D. -同系物
知识点 05 物质的变化
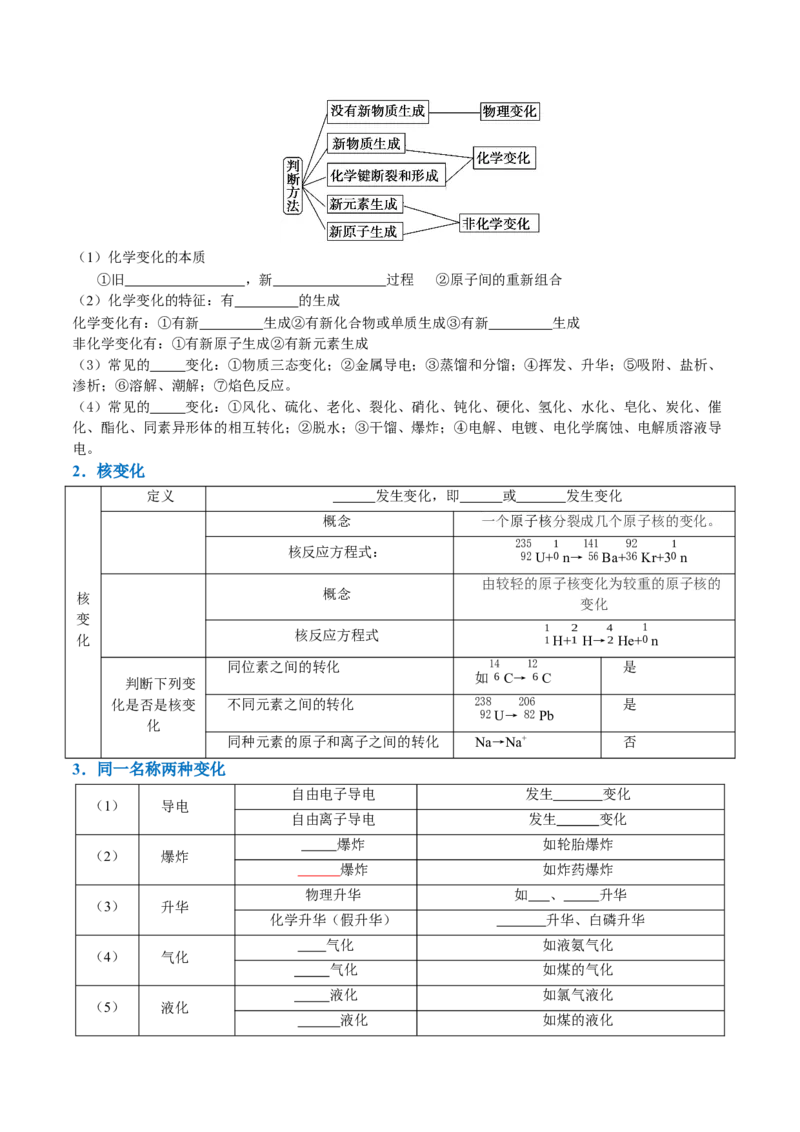
1.物理变化和化学变化的判断方法(1)化学变化的本质
①旧 ,新 过程 ②原子间的重新组合
(2)化学变化的特征:有 的生成
化学变化有:①有新 生成②有新化合物或单质生成③有新 生成
非化学变化有:①有新原子生成②有新元素生成
(3)常见的 变化:①物质三态变化;②金属导电;③蒸馏和分馏;④挥发、升华;⑤吸附、盐析、
渗析;⑥溶解、潮解;⑦焰色反应。
(4)常见的 变化:①风化、硫化、老化、裂化、硝化、钝化、硬化、氢化、水化、皂化、炭化、催
化、酯化、同素异形体的相互转化;②脱水;③干馏、爆炸;④电解、电镀、电化学腐蚀、电解质溶液导
电。
2.核变化
定义 发生变化,即 或 发生变化
概念 一个原子核分裂成几个原子核的变化。
235 1 141 92 1
核反应方程式:
92U+0n→ 56Ba+36Kr+30n
由较轻的原子核变化为较重的原子核的
概念
核
变化
变
1 2 4 1
核反应方程式
化 1H+1 H→2 He+0n
同位素之间的转化 14 12 是
如 6C→ 6C
判断下列变
化是否是核变 不同元素之间的转化 238 206 是
92U→ 82Pb
化
同种元素的原子和离子之间的转化 Na→Na+ 否
3.同一名称两种变化
自由电子导电 发生 变化
(1) 导电
自由离子导电 发生 变化
爆炸 如轮胎爆炸
(2) 爆炸
爆炸 如炸药爆炸
物理升华 如 、 升华
(3) 升华
化学升华(假升华) 升华、白磷升华
气化 如液氨气化
(4) 气化
气化 如煤的气化
液化 如氯气液化
(5) 液化
液化 如煤的液化易错点:物质变化的辨析
(1)同素异形体之间的转化为 ,如O 与O 间的转化。
3 2
(2)不同原子间的转化不属于 变化,其对应的反应也不属于 反应,如U―→Th+He。
(3)化学变化中一定存在化学键的 和 ,但存在化学键断裂的变化 是化学变化,如金
属熔化、HCl溶于水、NaCl熔化均属于物理变化。
(4)化学变化不仅有 的变化,同时还伴随有 的变化。
(5)化学变化中一定伴随 变化,物理变化中一定没有 变化。
(6)非化学变化
(7)煤的 、 属于化学变化。
煤的气化是将其转化为可燃性气体的过程,主要反应是碳与水蒸气反应生成 等。
煤的液化是将其直接或间接转化为 等液体燃料。
(8)结晶水合物失去结晶水的过程属于 变化。
(9)浓硫酸的 性属于物理性质, 性属于化学性质。
(10)煤的干馏、煤的气化以及煤的液化都属于 变化,石油的分馏属于物理变化,石油的裂化和裂解
都属于化学变化。
(11)金属导电、吸附、胶体聚沉等属于 变化。
10.我国古书《天工开物》中记载了以竹子制造竹纸的方法,其步骤大致有以下几步:①斩竹漂塘(杀青)
②煮楻足火 ③春臼 ④荡料入帘 ⑤覆帘压纸 ⑥透火焙干。其中未涉及化学变化的是
A.③④⑤ B.②③④ C.①②③ D.②⑤⑥
11.下列成语中,没有涉及化学变化的是
A.严冬冱寒,滴水成冰 B.水滴石穿,绳锯木断
C.趁热打铁,百炼成钢 D.星星之火,可以燎原
12.下列变化一定属于化学变化的是
①金属导电
②爆炸
③二氧化氮经加压冷却凝结称无色液体
④氯气使品红溶液褪色
⑤无水硫酸铜由白变蓝
⑥工业制氧气
⑦十水碳酸钠风化
⑧久置浓硝酸变黄
⑨ 和 间的相互转化
⑩煤的干馏和石油的分馏
A.③④⑤⑦⑧ B.②④⑦⑧⑨ C.①②⑤⑥⑩ D.①③⑥⑨⑩
知识点 06 物质的转化1.化学反应的分类
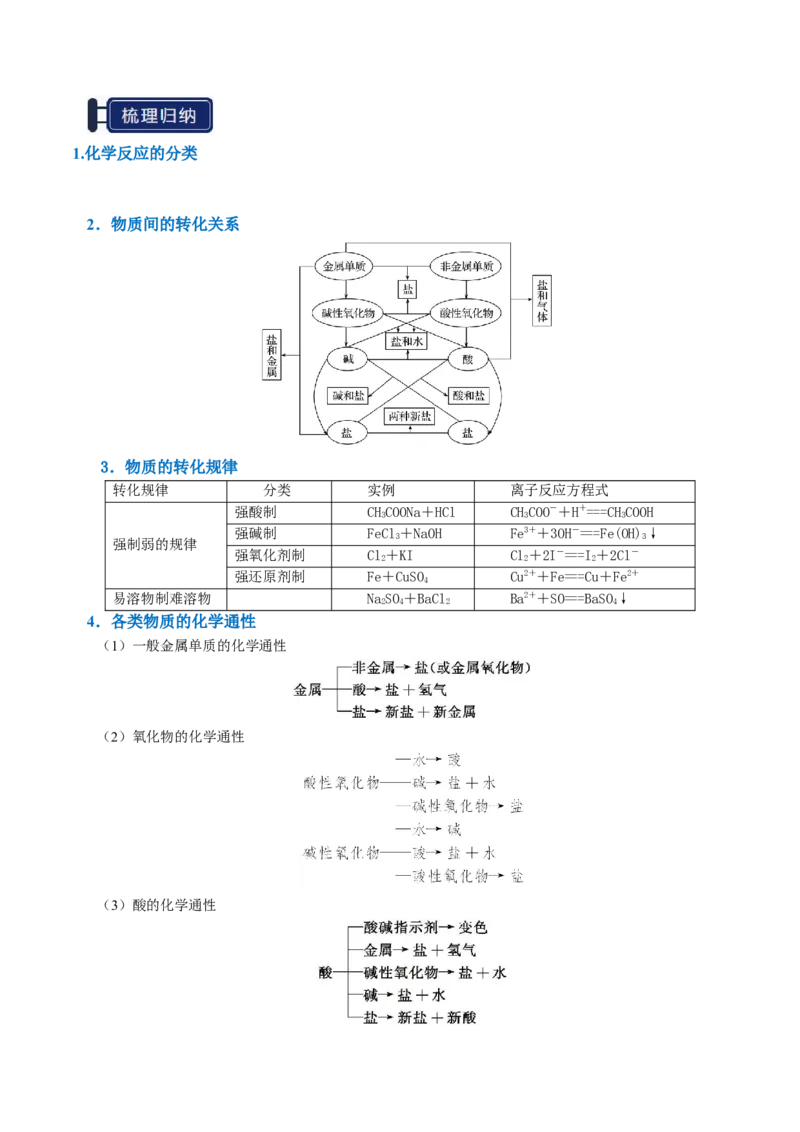
2.物质间的转化关系
3.物质的转化规律
转化规律 分类 实例 离子反应方程式
强酸制 CHCOONa+HCl CHCOO-+H+===CHCOOH
3 3 3
强碱制 FeCl+NaOH Fe3++3OH-===Fe(OH)↓
3 3
强制弱的规律
强氧化剂制 Cl+KI Cl+2I-===I+2Cl-
2 2 2
强还原剂制 Fe+CuSO Cu2++Fe===Cu+Fe2+
4
易溶物制难溶物 NaSO+BaCl Ba2++SO===BaSO↓
2 4 2 4
4.各类物质的化学通性
(1)一般金属单质的化学通性
(2)氧化物的化学通性
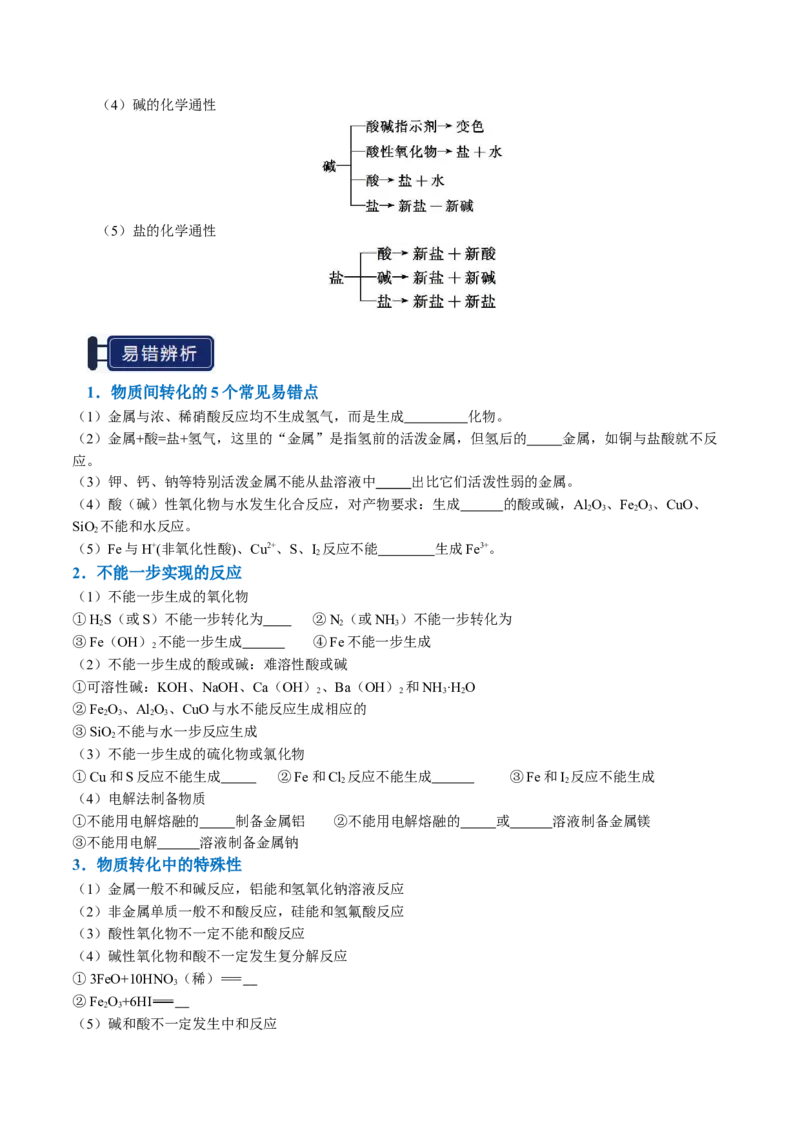
(3)酸的化学通性(4)碱的化学通性
(5)盐的化学通性
1.物质间转化的5个常见易错点
(1)金属与浓、稀硝酸反应均不生成氢气,而是生成 化物。
(2)金属+酸=盐+氢气,这里的“金属”是指氢前的活泼金属,但氢后的 金属,如铜与盐酸就不反
应。
(3)钾、钙、钠等特别活泼金属不能从盐溶液中 出比它们活泼性弱的金属。
(4)酸(碱)性氧化物与水发生化合反应,对产物要求:生成 的酸或碱,Al O、Fe O、CuO、
2 3 2 3
SiO 不能和水反应。
2
(5)Fe与H+(非氧化性酸)、Cu2+、S、I 反应不能 生成Fe3+。
2
2.不能一步实现的反应
(1)不能一步生成的氧化物
①HS(或S)不能一步转化为 ②N(或NH )不能一步转化为
2 2 3
③Fe(OH) 不能一步生成 ④Fe不能一步生成
2
(2)不能一步生成的酸或碱:难溶性酸或碱
①可溶性碱:KOH、NaOH、Ca(OH)、Ba(OH) 和NH ·H O
2 2 3 2
②Fe O、Al O、CuO与水不能反应生成相应的
2 3 2 3
③SiO 不能与水一步反应生成
2
(3)不能一步生成的硫化物或氯化物
①Cu和S反应不能生成 ②Fe和Cl 反应不能生成 ③Fe和I 反应不能生成
2 2
(4)电解法制备物质
①不能用电解熔融的 制备金属铝 ②不能用电解熔融的 或 溶液制备金属镁
③不能用电解 溶液制备金属钠
3.物质转化中的特殊性
(1)金属一般不和碱反应,铝能和氢氧化钠溶液反应
(2)非金属单质一般不和酸反应,硅能和氢氟酸反应
(3)酸性氧化物不一定不能和酸反应
(4)碱性氧化物和酸不一定发生复分解反应
①3FeO+10HNO(稀)
3
②Fe O+6HI
2 3
(5)碱和酸不一定发生中和反应①3Fe(OH)+10HNO(稀)
2 3
②Fe O+6HI
2 3
13.金属及其化合物转化关系是化学学习的重要内容之一,下列各组物质的转化关系不能全部通过一步反
应完成的是
A.Na→NaOH→Na CO→NaCl B.Fe→FeCl →Fe(OH) →Fe O
2 3 3 3 2 3
C.Al→Al O→Al(OH) →AlCl D.Mg→MgCl →Mg(OH) →MgSO
2 3 3 3 2 2 4
14.下列关于物质转化的关系不正确的是
A.金属单质+氯气→高价金属氯化物
B.酸性氧化物+碱性氧化物→盐+水
C.难溶性碱→碱性氧化物+水
D.盐+酸→新盐+新酸
15.化学是研究物质及其变化的科学。通常条件下,下列各组物质按右图所示转化关系每一步都能一步实
现的是
选
甲 乙 丙 丁
项
A
B Si
C NO
D Cu CuO
16.一定条件下,碳酸钙可以发生一系列转化(如图所示),下列每步转化反应与选项中的反应类型匹配的
是
石灰石 生石灰 熟石灰 碳酸钙 氯化钙
A.分解反应、化合反应、复分解反应、复分解反应
B.分解反应、复分解反应、化合反应、复分解反应
C.分解反应、化合反应、复分解反应、置换反应
D.复分解反应、化合反应、复分解反应、分解反应