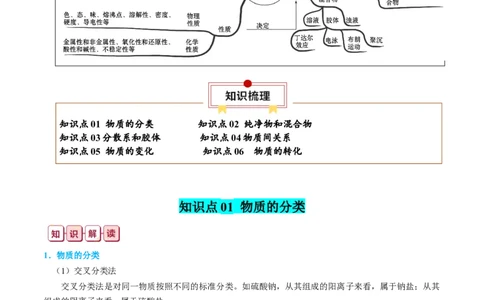
文档内容
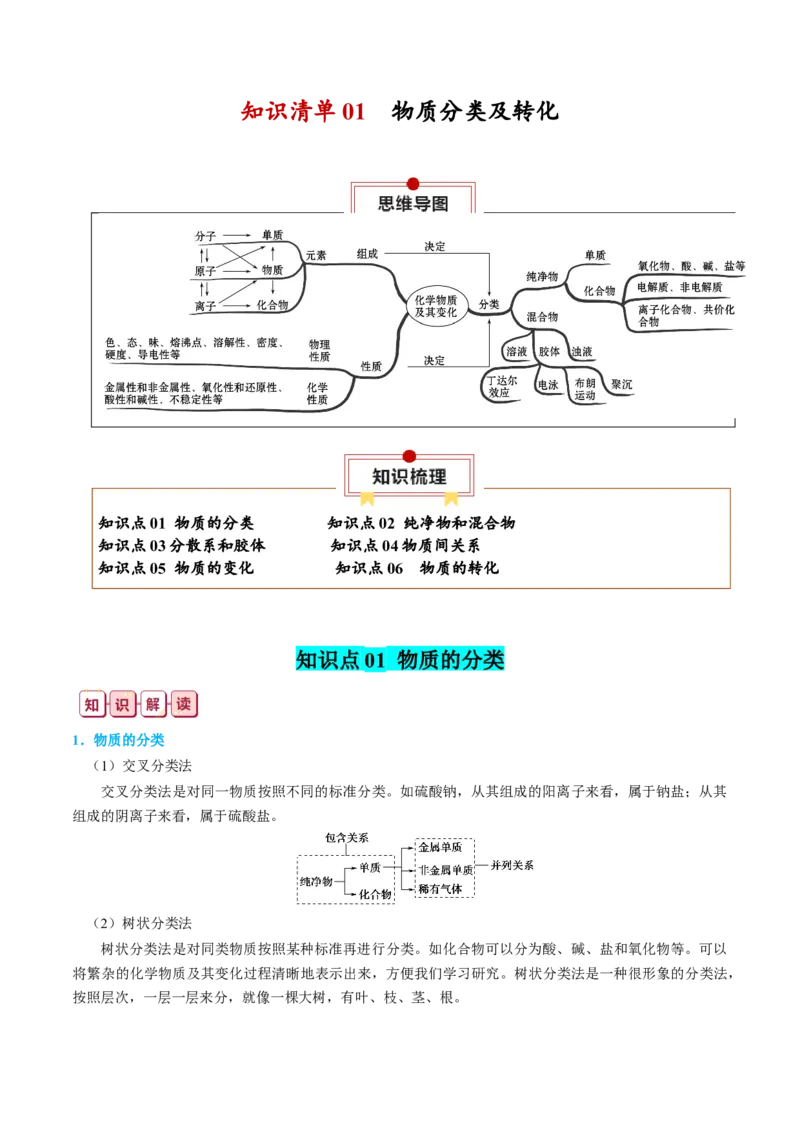
知识清单 01 物质分类及转化
知识点01 物质的分类 知识点02 纯净物和混合物
知识点03分散系和胶体 知识点04物质间关系
知识点05 物质的变化 知识点06 物质的转化
知识点 01 物质的分类
1.物质的分类
(1)交叉分类法
交叉分类法是对同一物质按照不同的标准分类。如硫酸钠,从其组成的阳离子来看,属于钠盐;从其
组成的阴离子来看,属于硫酸盐。
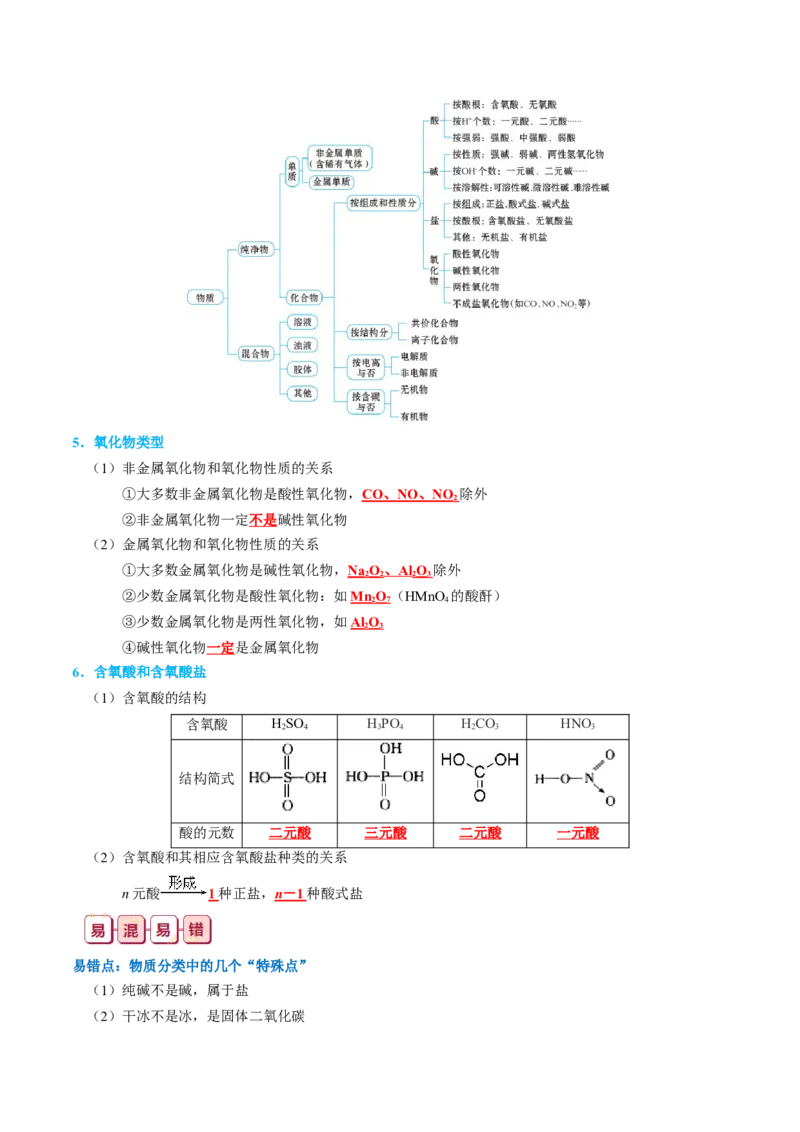
(2)树状分类法
树状分类法是对同类物质按照某种标准再进行分类。如化合物可以分为酸、碱、盐和氧化物等。可以
将繁杂的化学物质及其变化过程清晰地表示出来,方便我们学习研究。树状分类法是一种很形象的分类法,
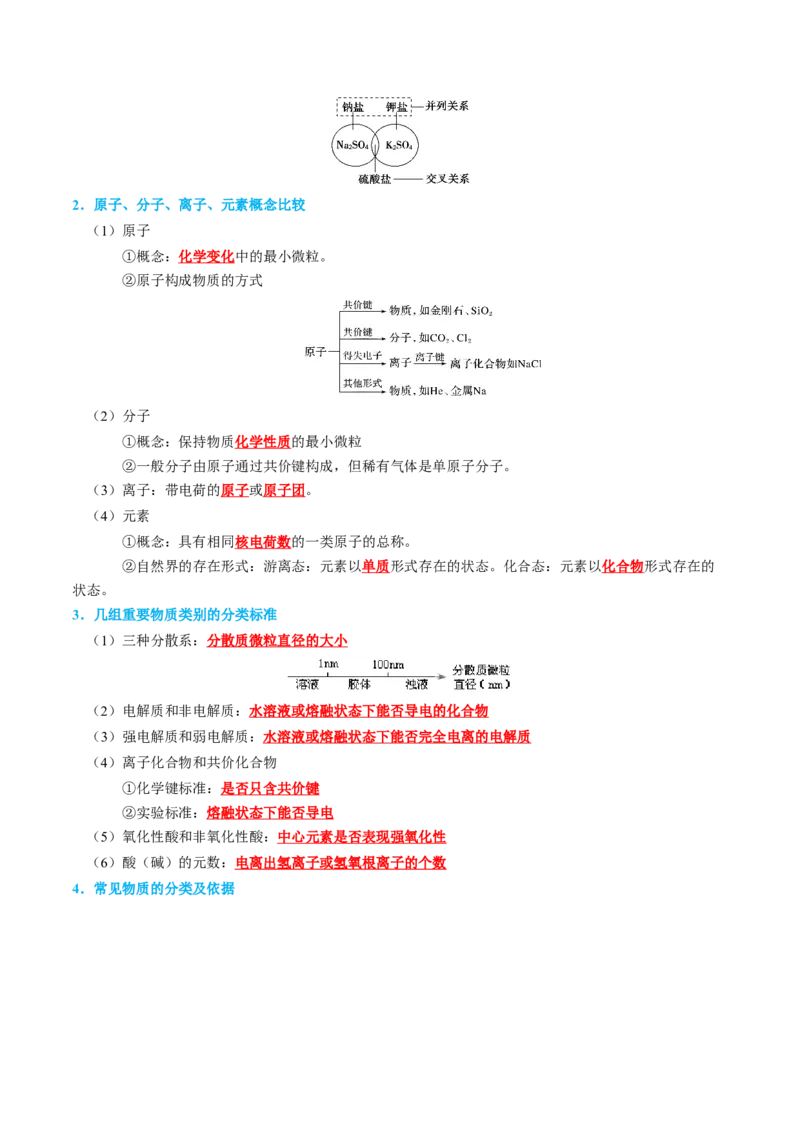
按照层次,一层一层来分,就像一棵大树,有叶、枝、茎、根。2.原子、分子、离子、元素概念比较
(1)原子
①概念:化学变化中的最小微粒。
②原子构成物质的方式
(2)分子
①概念:保持物质化学性质的最小微粒
②一般分子由原子通过共价键构成,但稀有气体是单原子分子。
(3)离子:带电荷的原子或原子团。
(4)元素
①概念:具有相同核电荷数的一类原子的总称。
②自然界的存在形式:游离态:元素以单质形式存在的状态。化合态:元素以化合物形式存在的
状态。
3.几组重要物质类别的分类标准
(1)三种分散系:分散质微粒直径的大小
(2)电解质和非电解质:水溶液或熔融状态下能否导电的化合物
(3)强电解质和弱电解质:水溶液或熔融状态下能否完全电离的电解质
(4)离子化合物和共价化合物
①化学键标准:是否只含共价键
②实验标准:熔融状态下能否导电
(5)氧化性酸和非氧化性酸:中心元素是否表现强氧化性
(6)酸(碱)的元数:电离出氢离子或氢氧根离子的个数
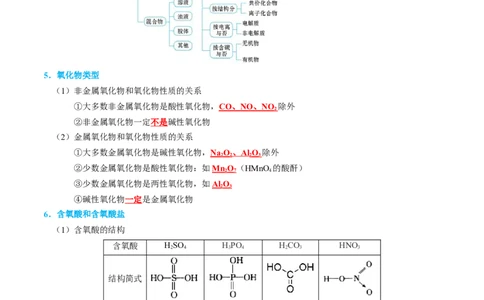
4.常见物质的分类及依据5.氧化物类型
(1)非金属氧化物和氧化物性质的关系
①大多数非金属氧化物是酸性氧化物, CO 、 NO 、 NO 除外
2
②非金属氧化物一定不是碱性氧化物
(2)金属氧化物和氧化物性质的关系
①大多数金属氧化物是碱性氧化物,Na O 、 A l O 除外
2 2 2 3
②少数金属氧化物是酸性氧化物:如Mn O(HMnO 的酸酐)
2 7 4
③少数金属氧化物是两性氧化物,如Al O
2 3
④碱性氧化物一定是金属氧化物
6.含氧酸和含氧酸盐
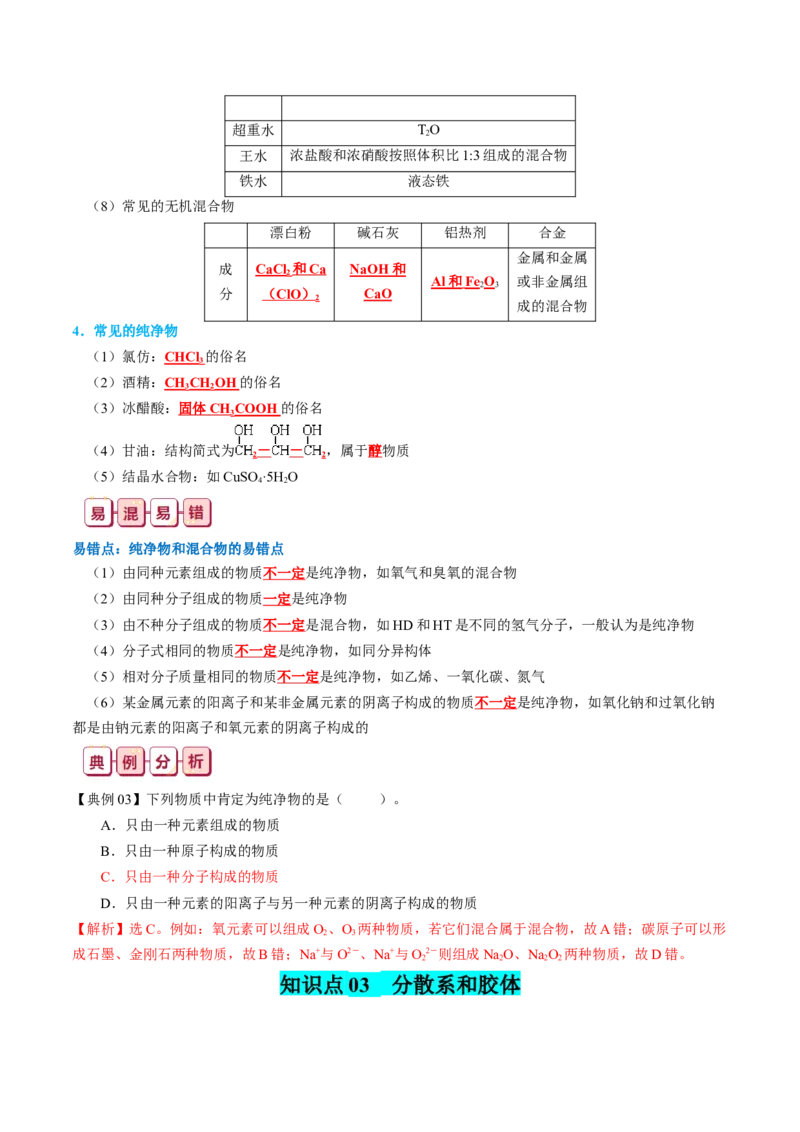
(1)含氧酸的结构
含氧酸 HSO HPO HCO HNO
2 4 3 4 2 3 3
结构简式
酸的元数 二元酸 三元酸 二元酸 一元酸
(2)含氧酸和其相应含氧酸盐种类的关系
n元酸 1 种正盐, n - 1 种酸式盐
易错点:物质分类中的几个“特殊点”
(1)纯碱不是碱,属于盐
(2)干冰不是冰,是固体二氧化碳(3)NaHSO 不是酸,是一种酸式盐
4
(4)水玻璃不是玻璃,是硅酸钠溶液
(5)醋酸(CHCOOH)不是四元酸,是一元酸
3
(6)硅酸盐(如NaO·SiO)不是由氧化物组成的,而是金属阳离子和硅酸根离子形成的硅酸盐
2 2
(7)几种石灰
①生石灰:CaO
②熟石灰:Ca(OH)
2
③石灰乳、石灰浆:Ca(OH) 悬浊液,石灰水:Ca(OH) 溶液
2 2
④石灰石:主要成分是CaCO
3
⑤碱石灰:NaOH和CaO两种固体的混合物
【典例01】(2023·辽宁省实验中学一模)物质的分类多种多样,下列说法及物质的分类均正确的是(
)。
A.金属氧化物一般为碱性氧化物,Na、Mg、Al、Fe、Mn的最高价氧化物均为碱性氧化物
B.非金属氧化物一般为酸性氧化物,C、N、S、P、Cl、Si的最高价氧化物均为酸性氧化物
C.在水溶液中能导电的物质一般是电解质,HCl、HO、CHCOOH、AgCl、NH 、NaOH均为电解质
2 3 3
D.高分子化合物在人类生活中必不可少,淀粉、纤维素、蛋白质、油脂、橡胶、塑料均为高分子化
合物
【解析】选B。A项,能和酸反应生成盐和水的氧化物属于碱性氧化物,大多数金属氧化物是碱性氧化物
金属氧化物不一定是碱性氧化物,而Al的最高价氧化物Al O 为两性氧化物,Mn的最高价氧化物MnO
2 3 2 7
为酸性氧化物,故A错误;B项,酸性氧化物是指能和碱反应生成盐和水的氧化物,CO 、NO 、SO 、
2 2 5 3
PO 、ClO 、SiO 均能与碱反应生成盐和水,是酸性氧化物,故B正确;C项,在水溶液中或熔化状态下
2 5 2 7 2
能导电的化合物称为电解质,NH 在水中形成的NH ·H O是电解质,而NH 是非电解质,故C错误;D项,
3 3 2 3
高分子化合物一般是指相对分子质量大于一万的化合物,油脂不是高分子化合物,故D错误。
【典例02】(广东梅州2022~2023学年度高三3月模拟)下图是磷酸、亚磷酸、次磷酸的结构式,其中磷
酸为三元中强酸,亚磷酸为二元弱酸,则下列说法正确的是( )。
A.磷酸(HPO )的电离方程式为:HPO 3H++PO 3-
3 4 3 4 4
B.亚磷酸(HPO )与足量NaOH溶液反应生成NaPO
3 3 3 3
C.NaH PO 溶液呈酸性,是因为HPO 2-的水解程度比电离程度大
2 4 4
D.NaH PO 溶液呈碱性
2 2
【解析】选D。磷酸为三元中强酸,应分步电离,且可逆,电离方程式为HPO H++HPO -,HPO -
3 4 2 4 2 4
H++HPO 2-,HPO 2- H++PO 3-,故A错误;亚磷酸为二元弱酸,只能电离出两个氢离子,所以
4 4 4与足量NaOH溶液反应生成NaHPO ,故B错误;如果NaH PO 溶液呈酸性,说明HPO 2-电离程度大于水
2 3 2 4 4
解程度,故C错误;磷酸含有三个羟基氢为三元酸,亚磷酸含有两个羟基氢为二元酸,而次磷酸只含一个
羟基氢,所以应为一元酸,所以NaH PO 为正盐,且为强碱弱酸盐,溶液中存在次磷酸根的水解,使溶液
2 2
显碱性,故D正确。
知识点 02 纯净物和混合物
1.本质区别:是否由一种物质组成
2.有欺骗性名称或符号的物质
(1)冰水混合物:冰和水是同一物质的不同状态
(2)纯净的盐酸:盐酸是氯化氢气体的水溶液,属于混合物
(3)纯净的矿泉水:矿泉水中含有少量的矿物质杂质,属于混合物
(4)纯净的二氧化氮:存在双聚平衡:2NO NO,NO 中一定含NO
2 2 4 2 2 4
(5)高分子化合物:聚合度n值不同,所有的高聚物都是混合物
(6)化合物HD:是一种氢气分子,属于单质
3.常见的混合物
(1)分散系:溶液、浊液、胶体
(2)高分子化合物
①天然高分子化合物:淀粉、纤维素、天然橡胶、蛋白质
②合成高分子化合物:塑料、合成纤维、合成橡胶
(3)三大化石燃料:煤、石油、天然气
(4)石油及其加工产品
①石油分馏产品:石油气、汽油、煤油、柴油、石蜡油、润滑油、沥青
②石油裂化产品:裂化汽油:含烷烃和烯烃
③石油裂解产品:石油裂解气(乙烯、丙烯、丁二烯)
(5)煤及其加工产品
①水煤气:CO和H
2
②焦炉气:H、CH、C H、CO
2 4 2 4
③煤焦油:粗苯、粗氨水、酚类、萘和沥青
(6)油脂:动物油和植物油
(7)几种“水”
成分
氨水 氨气的水溶液
氯水 氯气的水溶液
水玻璃 硅酸钠溶液
水银 Hg
重水 DO
2超重水 TO
2
王水 浓盐酸和浓硝酸按照体积比1:3组成的混合物
铁水 液态铁
(8)常见的无机混合物
漂白粉 碱石灰 铝热剂 合金
金属和金属
成 CaCl 和 C a NaOH 和
2
Al 和 Fe O 或非金属组
2 3
分 ( ClO ) Ca O
2
成的混合物
4.常见的纯净物
(1)氯仿:CHCl 的俗名
3
(2)酒精:CH CH OH 的俗名
3 2
(3)冰醋酸: 固体 CH COOH 的俗名
3
(4)甘油:结构简式为 - - ,属于醇物质
2 2
(5)结晶水合物:如CuSO ·5HO
4 2
易错点:纯净物和混合物的易错点
(1)由同种元素组成的物质不一定是纯净物,如氧气和臭氧的混合物
(2)由同种分子组成的物质一定是纯净物
(3)由不种分子组成的物质不一定是混合物,如HD和HT是不同的氢气分子,一般认为是纯净物
(4)分子式相同的物质不一定是纯净物,如同分异构体
(5)相对分子质量相同的物质不一定是纯净物,如乙烯、一氧化碳、氮气
(6)某金属元素的阳离子和某非金属元素的阴离子构成的物质不一定是纯净物,如氧化钠和过氧化钠
都是由钠元素的阳离子和氧元素的阴离子构成的
【典例03】下列物质中肯定为纯净物的是( )。
A.只由一种元素组成的物质
B.只由一种原子构成的物质
C.只由一种分子构成的物质
D.只由一种元素的阳离子与另一种元素的阴离子构成的物质
【解析】选C。例如:氧元素可以组成O、O 两种物质,若它们混合属于混合物,故A错;碳原子可以形
2 3
成石墨、金刚石两种物质,故B错;Na+与O2-、Na+与O2-则组成NaO、NaO 两种物质,故D错。
2 2 2 2
知识点 03 分散系和胶体1.分散系
(1)分散系中至少含有两种物质,都属于混合物,蒸馏水不是一种分散系
(2)三种分散系之间的转化为物理变化
(3)透明不代表无色,如CuSO 溶液为蓝色溶液,Fe(OH) 胶体为红褐色液体。
4 3
(4)胶体不一定都呈液体,胶体除了液溶胶还有气溶胶和固溶胶。
2.胶体的性质
(1)外观: 较均一、较透明、 较稳定
(2)通透性:能透过滤纸,不能透过半透膜
(3)电学特性:胶不带电荷
3.常见胶体
(1)气溶胶:云、烟、雾
(2)液溶胶:豆浆、氢氧化铝胶体、Fe(OH) 胶体、硅酸胶体
3
(3)固溶胶:果冻、宝石、烟水晶、有色玻璃
(4)三种有机胶体:淀粉溶液、肥皂溶液、蛋白质溶液
4.鉴别胶体和溶液
(1)方法:丁达尔效应
(2)操作:用可见光束照射,看在入射光侧面是否看到一条光亮的“通路”
5.胶体的聚沉
(1)现象:胶体形成沉淀析出的现象
(2)变化:物理变化
(3)方法
①加入电解质溶液
②加入带相反电荷胶粒的胶体
③加热或搅拌
(4)Fe(OH) 胶体-----------------------→先产生红褐色沉淀,后沉淀全部溶解
3
6.胶体的吸附性:胶体的比表面积大,吸附能力强
7.胶体的电泳(1)概念:在外电场的作用下胶体微粒发生定向移动
(2)原因:胶体微粒比表面积大,吸附能力强,吸附了带电离子而带电荷
(3)规律:带正电荷的胶粒向阴极移动,带负电荷的胶粒向阳极移动
(4)变化:发生化学变化(电解反应)
8.胶体的形成
(1)形成过程:将纳米颗粒分散到适当的分散剂中形成的一种分散系
(2)结构特点:胶粒是高分子或多分子聚合体
①胶体中所含胶粒的个数不确定
②胶粒所带的电荷数不确定
(3)淀粉胶体的特殊性
①结构特征:淀粉胶体为分子胶体,胶粒不带电荷
②性质特性:加入电解质溶液不能发生聚沉,通电后不能发生电泳
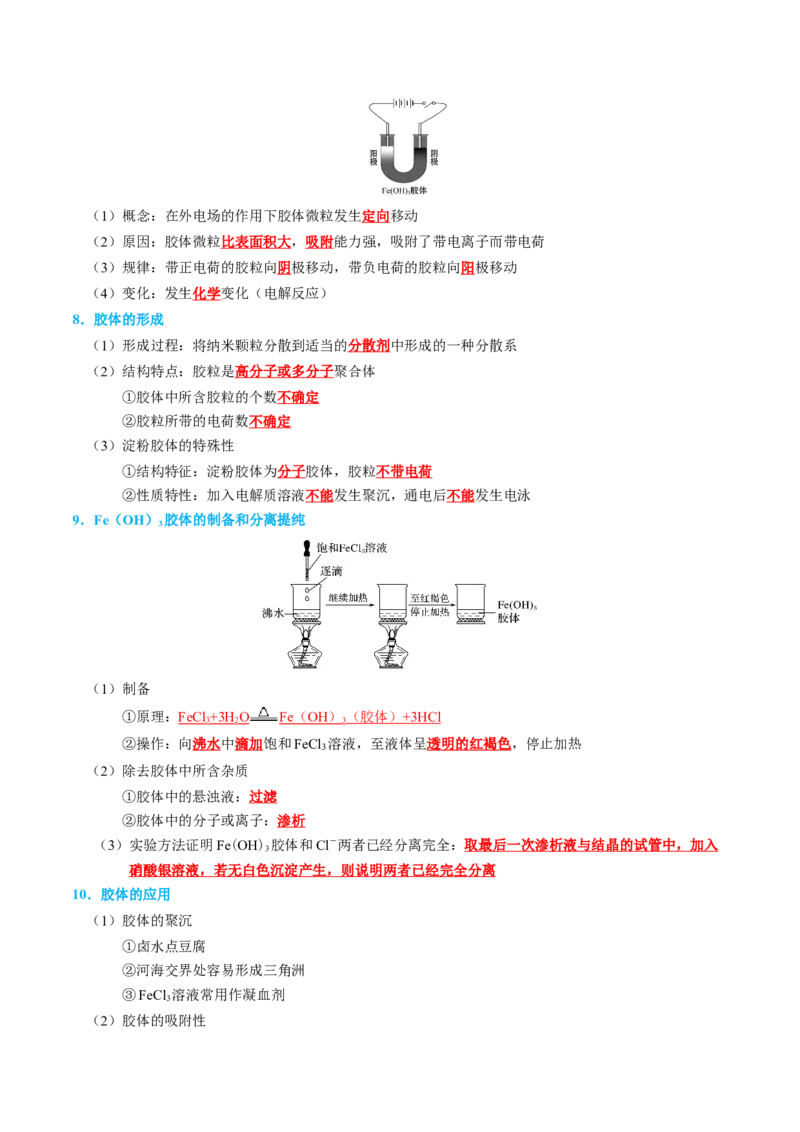
9.Fe(OH) 胶体的制备和分离提纯
3
(1)制备
①原理:FeCl +3H O Fe ( OH ) (胶体) +3HC l
3 2 3
②操作:向沸水中滴加饱和FeCl 溶液,至液体呈透明的红褐色,停止加热
3
(2)除去胶体中所含杂质
①胶体中的悬浊液:过滤
②胶体中的分子或离子:渗析
(3)实验方法证明Fe(OH) 胶体和Cl-两者已经分离完全:取最后一次渗析液与结晶的试管中,加入
3
硝酸银溶液,若无白色沉淀产生,则说明两者已经完全分离
10.胶体的应用
(1)胶体的聚沉
①卤水点豆腐
②河海交界处容易形成三角洲
③FeCl 溶液常用作凝血剂
3
(2)胶体的吸附性①明矾、Fe (SO ) 溶液净水
2 4 3
②Al(OH) 胶体作漂白剂
3
(3)胶体的丁达尔现象
①清晨阳光穿过茂密树木枝叶产生的美丽光线
②电影院光柱
③海市蜃楼
易错点:胶体的易错点
(1)丁达尔效应是物理变化而不是化学变化。
(2)明矾作净水剂是利用明矾溶于水生成Al(OH) 胶体,胶体具有吸附性;但胶体没有杀菌消毒的
3
作用。
(3)胶体呈电中性,不带电荷。而胶粒可能带正电荷或负电荷或不带电荷。
【典例04】(2022·山西太原高三上学期期中)FeCl 与HO制得胶体的胶团结构为{[Fe(OH)]
3 2 3
·nFeO+(n-x)Cl-}x+·xCl-(如图)。下列说法正确的是( )。
m
A.Fe(OH) 胶体带正电
3
B.胶体粒子的直径介于1~100 nm之间
C.16.25g FeCl 水解形成的Fe(OH) 胶体粒子数为6.02×1022
3 3
D.在U形管中注入Fe(OH) 胶体,插入石墨电极通电,阳极周围颜色加深
3
【解析】选B。胶体是由分散质(胶粒)和分散剂构成的,Fe(OH) 胶体的分散质是{[Fe(OH)]
3 3
·nFeO+(n-x)Cl-}x+,带正电荷,而胶体的胶团(胶体)结构为{[Fe(OH)] ·nFeO+(n-x)Cl
m 3 m
-}x+·xCl-,正负电荷数相同,所以Fe(OH) 胶体不带电荷,A选项错误;胶体是分散质粒子直径介于1
3
~100 nm之间的分散系,B选项正确;Fe(OH) 胶体粒子是由无数个Fe(OH) 分子构成的,所以不能
3 3
确定胶体粒子数为多少,C选项错误;Fe(OH) 胶粒带正电荷,电泳时向电解池的阴极移动,即阴极附
3
近红褐色变深,D选项错误。
知识点 04 物质间的关系1.同位素:质子数相同→中子数不同→同种元素→原子(核素)
(1)性质:物理性质不同,化学性质相似
(2)结构:同位素的核外电子排布相同
(3)判断
① H、 H、 H是互为同位素
② H、 H 不是互为同位素
2 2
③ H+、 H+不是互为同位素
2.同素异形体:同种元素→结构不同→单质
(1)性质:物理性质不同,化学性质相似
(2)转化:属于化学变化,非氧化还原反应
(3)实例
①氧元素:氧气和臭氧
②碳元素:金刚石、石墨和碳六十
③磷元素:红磷、白磷(黄磷)和黑鳞
④硫元素:单斜硫、斜方硫和正交硫
3.同分异构体:分子式相同→结构不同→化合物
(1)性质:物理性质不同,化学性质不同或相似
(2)转化:属于化学变化
4.同系物:组成相似→组成上相差1个或多个CH→同一类有机物
2
(1)同系物的相对分子质量相差14 的正整数倍
(2)同系物有相同的通式
(3)组成符合通式C H 的含不同碳原子的有机物一定互为同系物
n 2n+2
(4)同系物的化学性质相似,物理性质差异较大
(5)判断下列各组物质是否互为同系物
① OH和 CHOH(×)
2
② COOH和 CHCOOH(√)
2
③CH=CH 与 (×)
2 2④ - 与CHOCH CHOH(×)
2 2 3 2 2
5.同类不同种分子:相同元素不同核素组成的分子
(1)氢气分子:H、D、T、HD、HT、DT
2 2 2
(2)水分子:HO、DO、TO、HDO、HTO、DTO
2 2 2
(3)氯化氢分子:HCl、DCl、TCl
易错点:常见的同种物质
(1)同一物质有不同名称:三氯甲烷和氯仿
(2)同一物质有不同写法:HSiO 和Si(OH)、Al(OH) 与HAlO
4 4 4 3 3 3
(3)分子式相同的一碳有机物: 和
(4)分子式相同书写顺序不同的有机物
①(CH)CHCH 和CH- CH
3 2 3 3 3
② - CH-CH 与CHCH- CH-CH
2 2 3 3 2 2 3
③ 和
④HOOC-CH- -COOH与HOOC- -CH-COOH
2 2
⑤ 、 、
(5)邻二取代苯: 和
【典例05】正确掌握化学用语和化学基本概念是学好化学的基础。下列有关表述中正确的一组是
( )。
A.过氧乙酸(CHCOOOH)与羟基乙酸(HOCH COOH)所含官能团相同;两者互为同分异构体
3 2
B.16O与18O互为同位素;H16O、D16O、H18O、D18O互为同素异形体
2 2 2 2
C. 和 互为同分异构体
D.醋酸CHCOOH和硬脂酸C H COOH互为同系物
3 17 35
【解析】选D。过氧乙酸的结构是CH- -O-OH,而羟基乙酸的结构是HO-CH- -OH,显然两者
3 2
的官能团不一样,但是二者的分子式相同,互为同分异构体,A 选项错误;16O与18O不是质子数相同,中
子数不同的两种氧原子,二者互为同位素,H16O、D16O、H18O、D18O是四种不同的水分子,都是化合物,
2 2 2 2
不是同种元素组成的不同单质,不是同素异形体,B选项错误;由于甲烷是正四面体结构,所以二溴甲烷分子中的两个溴原子都是邻边关系,所以 和 是同一种物质,C选项错误;醋酸
CHCOOH和硬脂酸C H COOH都是饱和一元羧酸,结构相似,组成上差16个CH,二者互为同系物,
3 17 35 2
D选项正确。
知识点 05 物质的变化
1.化学变化的本质
(1)旧化学键的断裂,新化学键的形成过程
(2)原子间的重新组合
2.化学变化的特征:有新物质的生成
(1)有新分子生成(√)
(2)有新原子生成(×)
(3)有新化学键生成(√)
(4)有新化合物或单质生成(√)
3.核变化:原子核发生变化,即质子数或中子数发生变化
(1)核裂变
①概念:一个原子核分裂成几个原子核的变化。
②核反应方程式: U+ n→ Ba+ Kr+3 n
(2)核聚变
①概念:由较轻的原子核变化为较重的原子核的变化
②核反应方程式: H+ H→ He+ n
(3)判断下列变化是否是核变化
①同位素之间的转化(如 C→ C)(√)
②不同元素之间的转化(如 U→ Pb)(√)
③同种元素的原子和离子之间的转化(如Na→Na+)(×)
4.同一名称两种变化
(1)导电
①自由电子导电:发生物理变化
②自由离子导电:发生化学变化
(2)爆炸
①物理爆炸:如轮胎爆炸
②化学爆炸:如炸药爆炸
(3)升华①物理升华:如碘、干冰升华
②化学升华(假升华):氯化铵升华、白磷升华
(4)气化
①物理气化:如液氨气化
②化学气化:如煤的气化
(5)液化
①物理液化:如氯气液化
②化学液化:如煤的液化
易错点:物质变化判断的易错点
(1)同位素原子间的相互转化不属于化学变化,因为化学变化中原子核不发生变化。
(2)同素异形体间相互转化属于化学变化,因为有新物质生成。
(3)存在化学键断裂的变化不一定是化学变化,如HCl溶于水,熔融氯化钠的电离等是物理变化。
(4)金属导电、吸附、胶体聚沉等属于物理变化。
(5)同素异形体之间的相互转化、煤的气化(液化)等属于化学变化。
【典例06】(2021年高三八省联考广东卷)“古诗文经典已融入中华民族的血脉”。下列诗文中隐含化学
变化的是( )。
A.月落乌啼霜满天,江枫渔火对愁眠
B.掬月水在手,弄花香满衣
C.飞流直下三千尺,疑是银河落九天
D.举头望明月,低头思故乡
【解析】选A。渔火为物质燃烧发的光,燃烧属于化学变化,A符合题意;捧起清澄明澈的泉水,泉水照
见月影,好像那一轮明月在自己的手里一般;摆弄山花,馥郁之气溢满衣衫,为物理变化,B与题意不符;
飞流直下三千尺,为水的自由落体运动,为物理变化,C与题意不符;举头望明月,月光为反射的太阳光,
为物理变化,D与题意不符。
知识点 06 物质的转化
1.化学反应的分类2.物质间的转化关系
3.各类物质的化学通性
(1)一般金属单质的化学通性
(2)氧化物的化学通性
(3)酸的化学通性
(4)碱的化学通性(5)盐的化学通性
易错点01:物质转化间关系的特殊性
(1)金属+酸盐+氢气,这里的“金属”是指氢前的活泼金属,但氢前的不活泼金属,如铜与盐酸就不
反应。
(2)钾、钙、钠等特别活泼金属不能盐溶液中置换出比它们活泼性弱的金属。
(3)酸(碱)性氧化物与水发生化合反应,对产物要求:生成可溶性的酸或碱,Al O、Fe O、CuO、
2 3 2 3
SiO 不能和水反应。
2
易错点02:不能一步实现的反应
(1)不能一步生成的氧化物
①HS(或S)不能一步转化为SO
2 3
②N(或NH )不能一步转化为NO
2 3 2
③Fe(OH) 不能一步生成Fe O
2 2 3
④Fe不能一步生成Fe O
2 3
(2)不能一步生成的酸或碱:难溶性酸或碱
①可溶性碱:KOH、NaOH、Ca(OH)、Ba(OH) 和NH ·H O
2 2 3 2
②Fe O、Al O、CuO与水不能反应生成相应的碱
2 3 2 3
③SiO 不能与水一步反应生成HSiO
2 2 3
(3)不能一步生成的硫化物或氯化物
①Cu和S反应不能生成CuS
②Fe和Cl 反应不能生成FeCl
2 2
(4)电解法制备物质
①不能用电解熔融的AlCl 制备金属铝
3
②不能用电解熔融的MgO或MgCl 溶液制备金属镁
2
③不能用电解NaCl溶液制备金属钠
易错点03:物质转化中的特殊点
(1)酸性氧化物不一定不能和酸反应
SiO+4HF SiF↑+2HO
2 4 2
(2)碱性氧化物和酸不一定发生复分解反应①3FeO+10HNO(稀) 3Fe(NO )+NO↑+5H O
3 3 3 2
②Fe O+6HI 2FeI+I ↓+3H O
2 3 2 2 2
(3)碱和酸不一定发生中和反应
①3Fe(OH)+10HNO(稀) 3Fe(NO )+NO↑+8H O
2 3 3 3 2
②Fe O+6HI 2FeI+I ↓+3H O
2 3 2 2 2
【典例07】(黑龙江省牡丹江市2022届高三上学期期末)下列各组物质中,物质之间通过一步反应就能
实现如图所示转化的是( )。
选项 X Y Z R
A Al AlCl Al(OH) NaAlO
3 3 2
B Na NaO NaO NaOH
2 2 2
C HS S SO SO
2 2 3
D Fe FeCl FeCl Fe(OH)
2 3 3
【解析】选B。Al可以分别与盐酸、NaOH一步转化成AlCl 、NaAlO ,但Al无法一步转化成Al(OH)
3 2 3
沉淀,故A不符合题意;Na与O 不加热时生成NaO,加热时生成NaO,与水反应生成NaOH,NaO与
2 2 2 2 2
氧气反应能够生成NaO,NaO、NaO 与水反应都能生成NaOH,都可一步实现图示转化,故B符合题意;
2 2 2 2 2
S无法通过一步反应转化成SO ,故C不符合题意;铁与氯气反应生成氯化铁,与盐酸反应生成FeCl ,但
3 2
铁无法一步转化成Fe(OH) 沉淀,故D不符合题意。
3