文档内容
知识清单 24 烃
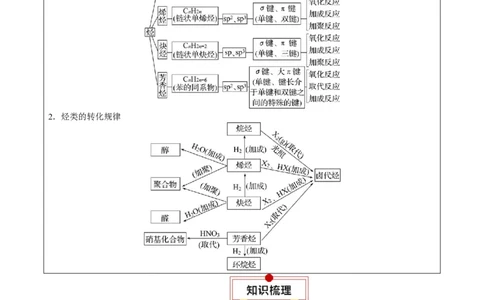
1.烃类的组成、结构与性质
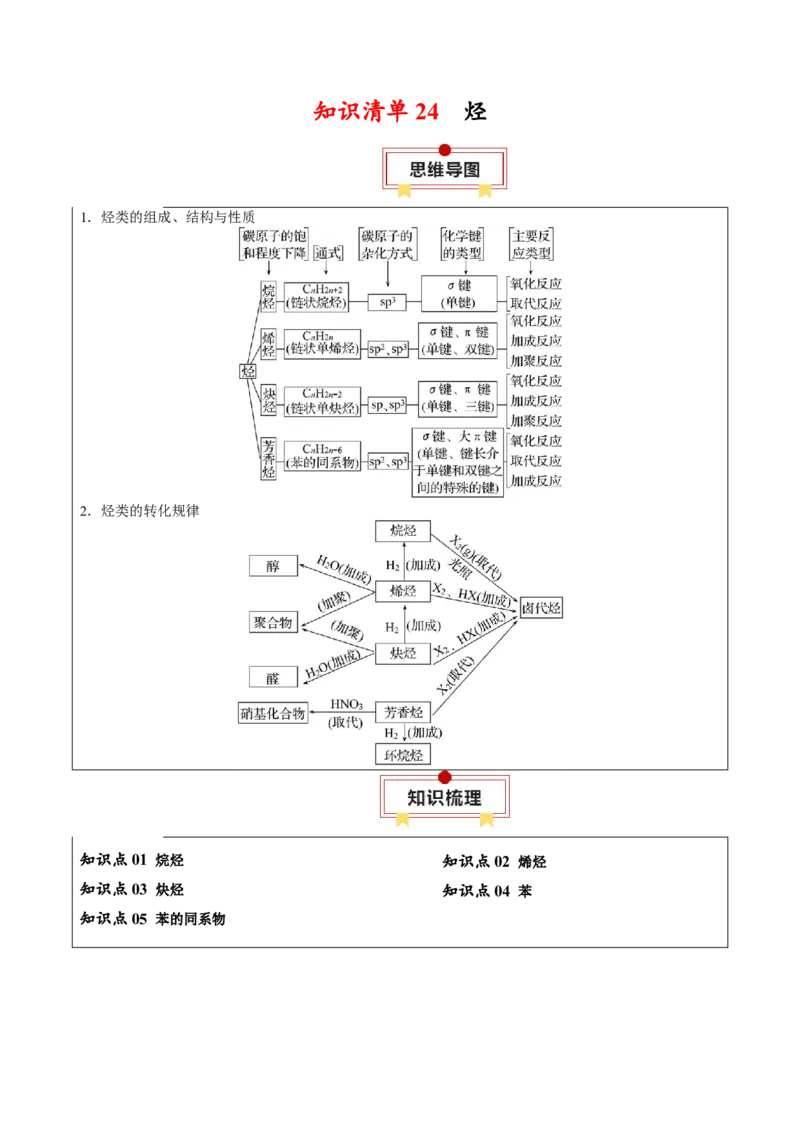
2.烃类的转化规律
知识点01 烷烃 知识点02 烯烃
知识点03 炔烃 知识点04 苯
知识点05 苯的同系物知识点 01 烷烃
一、烷烃的结构和物理性质
1.烷烃的结构
2.烷烃的物理性质
(1)状态:当碳原子数小于或等于4 时,烷烃在常温下呈气态
(2)溶解性:不溶于水,易溶于苯、乙醚等有机溶剂
(3)熔、沸点
①碳原子数不同:碳原子数的越多,熔、沸点越高;
CHCHCHCHCHCH>CH- CHCH
3 2 2 2 2 3 3 2 3
②碳原子数相同:支链越多,熔、沸点越低
CHCH- CHCH>CH- CH
3 2 2 3 3 3
③碳原子数和支链数都相同:结构越对称,熔、沸点越低
CH- CHCH>
3 2 3
(4)密度:随碳原子数的增加,密度逐渐增大,但比水的小
二、烷烃的化学性质
1.稳定性:常温下烷烃很不活泼,与强酸、强碱、强氧化剂和还原剂都不发生反应。
(1)性质
(2)烷烃不能使酸性高锰酸钾溶液褪色
2.氧化反应
3n+1
(1)可燃性:C H + 2 O n CO + ( n +1 ) H O
n 2n+2 2 2 2
(2)KMnO (H+):不褪色
4
3.分解反应:烷烃受热时会分解产生含碳原子数较少的烷烃和烯烃
C H CH +C H
16 34 8 16 8 18
4.取代反应
(1)反应举例:CHCH+Cl CH CH Cl+HCl(一氯取代)
3 3 2 3 2
(2)反应条件:光照和纯净的气态卤素单质
①在光照条件下烷烃能够使溴蒸汽褪色
②在光照条件下烷烃不能使溴水褪色。
③在光照条件下烷烃不能使溴的四氯化碳溶液褪色。
④液态烷烃能够和溴水发生萃取,液体分层,上层颜色深,下层颜色浅。
(3)化学键变化:断裂C-H键和X-X键;形成C-X键和H-X键
(4)取代特点:分子中的氢原子被卤素原子逐步取代,往往是各步反应同时发生
(5)产物种类:多种卤代烷烃的混合物,HX 的物质的量最多
(6)产物的量
①根据碳元素守恒,烷烃的物质的量等于所有卤代烷烃的物质的量之和
②根据取代反应的特点,有机物中卤素的物质的量等于HX的物质的量等于反应了的X 的物质的
2
量,即反应了的n(X)=n(一卤代物)+2n(二卤代物)+3n(三卤代物)+……=n(HX)=n(C-
2X)
【典例01】下列有关烷烃的说法中正确的是
A.链状烷烃的分子组成都满足C H (n≥1),彼此都是同系物
n 2n+2
B.烷烃的沸点高低仅取决于碳原子数的多少
C.戊烷(C H )有三种同分异构体
5 12
D.正丁烷的四个碳原子可以在同一条直线上
【答案】C
【详解】A.链状烷烃的C原子之间彼此一单键结合,剩余价电子全部与H原子结合,因此其分子组成都
满足C H (n≥1),但是若分子中C原子相同时,彼此不都是同系物,如分子式是C H 的物质有正丁烷和
n 2n+2 4 10
异丁烷,两种物质互为同分异构体,A错误;
B.烷烃都是由分子构成的物质,物质分子内C原子数越多,分子间作用力就越大,物质的熔沸点就越高;
当两种不同物质分子中C原子数相同时,分子内支链越多,分子间作用力就越小,物质的熔沸点就越低,
所以烷烃的沸点高低不仅取决于碳原子数的多少,也与物质分子内支链多少有关,B错误;
C.戊烷(C H )有正戊烷、异戊烷和新戊烷三种不同结构,这三种物质互为同分异构体,C正确;
5 12
D.烷烃分子中C原子采用sp3杂化,与该C原子连接的四个原子形成的是四面体结构,因此当物质分子中
有多个碳原子时,碳原子之间形成的碳链呈锯齿形连接,并不是碳原子在一条直线上,D错误;
故合理选项是C。
【典例02】汽油中异辛烷( )的含量越高,抗爆性能越好,下列有关异辛烷的说法
正确的是
A.常温常压下为气体 B.一氯代物有4种
C.可由炔烃或二烯烃加氢制得 D.系统命名为2,4,4-三甲基戊烷
【答案】B
【详解】A.异辛烷分子中碳原子数大于4,常温常压下为液体,故A错误;
B. 中有4中等效氢,一氯代物有4种,故B正确;
C. 可由单烯烃 、 加氢制得,不能由
炔烃或二烯烃加氢制得,故C错误;
D.根据烷烃的系统命名原则,系统命名为2,2,4-三甲基戊烷,故D错误;选B。
知识点 02 烯烃
一、烯烃的结构和物理性质
1.结构特点
(1)烯烃的官能团是碳碳双键( )。乙烯是最简单的烯烃。
(2)乙烯的结构特点:分子中所有原子都处于同一平面内。
2.通式:单烯烃的通式为C H (n≥2)
n 2n
3.物理性质
(1)常温常压下的状态:碳原子数≤4的烯烃为气态,其他为液态或固态。
(2)熔、沸点:碳原子越多,烯烃的熔、沸点越高;相同碳原子数时,支链越多,熔沸点越低。
(3)密度:相对密度逐渐增大,但相对密度均小于1。
(4)溶解性:都难溶于水,易溶于有机溶剂。
二、烯烃的化学性质
1.氧化反应
(1)可燃性
3n
①反应:C H + 2 O nCO+nH O
n 2n 2 2 2
②现象:产生明亮火焰,冒黑烟
(2)KMnO (H+)
4
①反应:CH=CH CO+H O
2 2 2 2
②现象:酸性高锰酸钾溶液褪色(区分烷烃与烯烃)
2.加成反应
(1)与Br 反应:CHCH=CH+Br CH - - CH Br
2 3 2 2 3 2
(2)与H 反应:CHCH=CH+H CH CH CH
2 3 2 2 3 2 3
(3)与HCl反应:CHCH=CH+HCl CH - - CH 或CH CH CHCl
3 2 3 3 3 2
(4)与HO反应:CHCH=CH+H O CH - - CH 或CH CH CHOH
2 3 2 2 3 3 3 2
3.加聚反应
(1)乙烯:n CH=CH CH - CH
2 2 2 2 n
(2)丙烯:nCH-CH=CH CH -
3 2 2 n
4.二烯烃的化学性质
(1)加成反应(2)加聚反应:发生1,4-加聚
①1,3-丁二烯:nCH=CH-CH=CH CH - CH = CH - CH
2 2 2 2 n
②2-甲基-1,3-丁二烯:nCH=CH- CH CH - CH - CH
2 2 2 2 n
【典例03】煤油的主要成分癸烷( C H ),丙烯可以由癸烷裂解制得:C H →2C H+X,下列说法错误的
10 22 10 22 3 6
是v
A.癸烷是难溶于水的液体
B.丙烯通过加聚反应生产聚丙烯用于制备口罩材料
C.丙烯和X均可以使溴水褪色
D.X的同分异构体可以用“正”、“异”进行区分
【答案】C
【分析】根据元素守恒可知X的化学式为C H 。
4 10
【详解】A.石油脑分子中含有10个碳原子,沸点较高,常温下为液体,难溶于水,选项A正确;
B.丙烯中含有碳碳双键,可以发生加聚反应生成聚丙烯,选项B正确;
C.X为丁烷,不含碳碳双键,不能使溴水褪色,选项C错误;
D.X为丁烷,有正丁烷(CHCHCHCH)、异丁烷[HC(CH )]两种同分异构体,选项D正确;
3 2 2 3 3 3
答案选B。
【典例04】丙烯可发生如下转化,下列说法不正确的是
A.丙烯分子中最多7个原子共平面
B.X的结构简式为CHCHBrCHBr
3 2 2
C.Y与足量KOH醇溶液共热可生成丙炔D.聚合物Z的链节为
【答案】B
【分析】由有机物的转化关系可知,光照条件下丙烯与溴发生取代反应生成BrCHCH=CH,则X为
2 2
BrCHCH=CH;丙烯与溴的四氯化碳溶液发生加成反应生成 ,则Y为
2 2
;催化剂作用下丙烯发生加聚反应生成 ,则Z为
。
【详解】A.丙烯分子中碳碳双键为平面结构,由三点成面可知,分子中最多有7个原子共平面,故A正
确;
B.由分析可知,X的结构简式为BrCHCH=CH,故B错误;
2 2
C.由分析可知,Y的结构简式为 , 在氢氧化钾醇溶液中共热
发生消去反应生成丙炔,故C正确;
D.由分析可知,Z的结构简式为 ,高聚物的链节为 ,故D正
确;
故选B。
知识点 03 炔烃
一、炔烃的结构和性质
1.乙炔
(1)结构特点
分子式 电子式 结构式 结构简式
CH H - C≡C - H CH≡CH
2 2
C-H键成
碳原子杂化方式 C≡C键成分 相邻两个键之间的键角 分子空间结构
分
1 个 σ 键和 2 个
sp 杂化 σ 键 180° 直线形结构
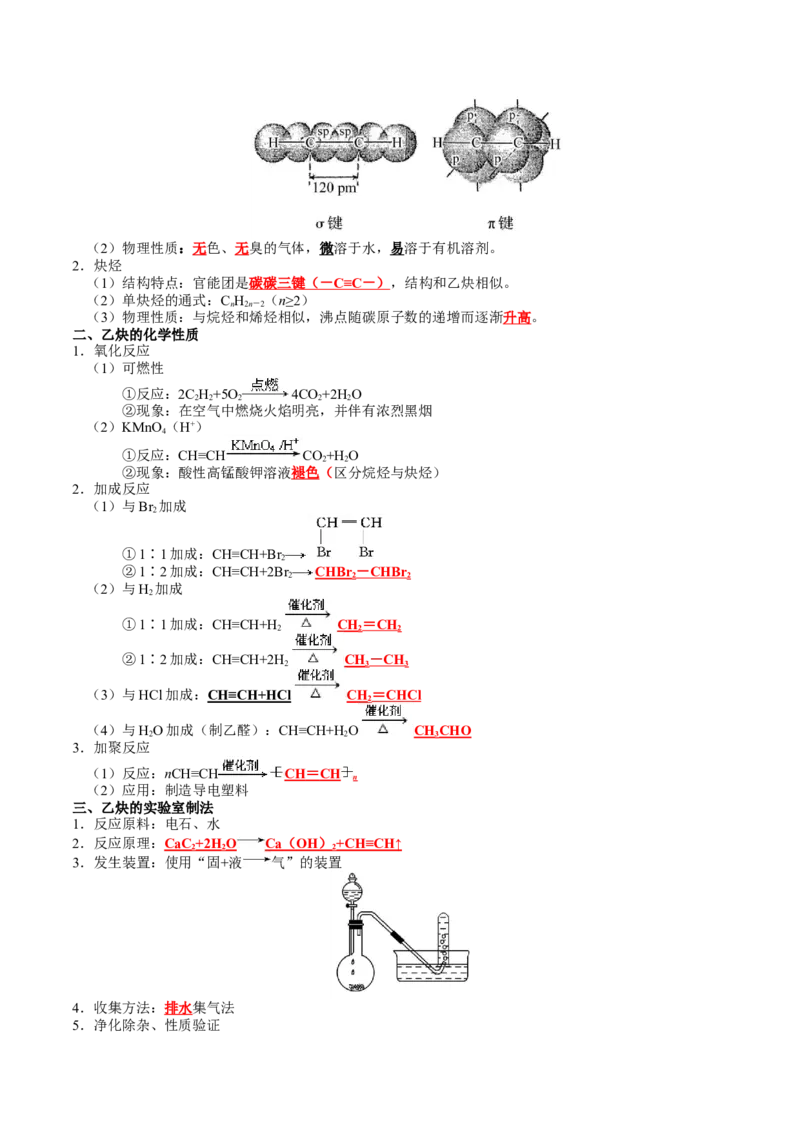
π 键(2)物理性质:无色、无臭的气体,微溶于水,易溶于有机溶剂。
2.炔烃
(1)结构特点:官能团是 碳碳三键(- C≡C -) ,结构和乙炔相似。
(2)单炔烃的通式:C H (n≥2)
n 2n-2
(3)物理性质:与烷烃和烯烃相似,沸点随碳原子数的递增而逐渐升高。
二、乙炔的化学性质
1.氧化反应
(1)可燃性
①反应:2C H+5O 4CO+2H O
2 2 2 2 2
②现象:在空气中燃烧火焰明亮,并伴有浓烈黑烟
(2)KMnO (H+)
4
①反应:CH≡CH CO+H O
2 2
②现象:酸性高锰酸钾溶液褪色(区分烷烃与炔烃)
2.加成反应
(1)与Br 加成
2
①1∶1加成:CH≡CH+Br
2
②1∶2加成:CH≡CH+2Br CHBr - CHB r
2 2 2
(2)与H 加成
2
①1∶1加成:CH≡CH+H CH = CH
2 2 2
②1∶2加成:CH≡CH+2H CH - CH
2 3 3
(3)与HCl加成:CH≡CH+HCl CH = CHC l
2
(4)与HO加成(制乙醛):CH≡CH+HO CH CHO
2 2 3
3.加聚反应
(1)反应:nCH≡CH CH = CH
n
(2)应用:制造导电塑料
三、乙炔的实验室制法
1.反应原料:电石、水
2.反应原理:CaC +2H O Ca ( OH ) +CH≡CH↑
2 2 2
3.发生装置:使用“固+液 气”的装置
4.收集方法:排水集气法
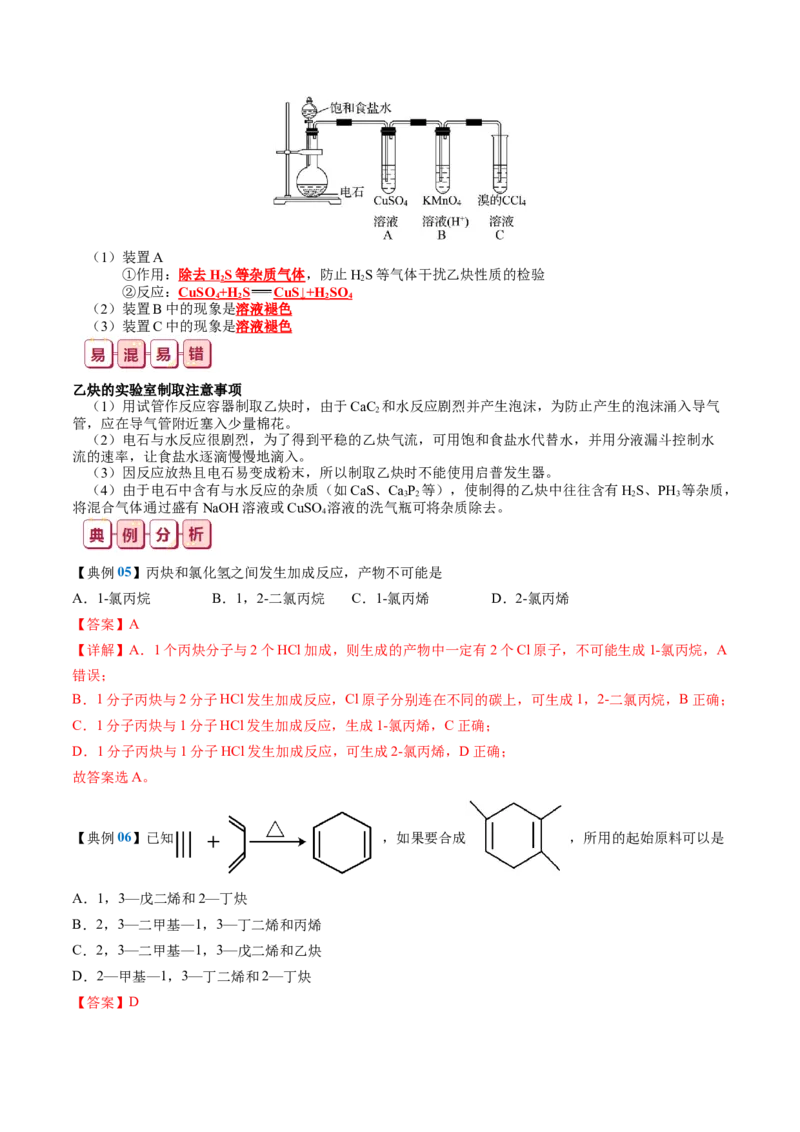
5.净化除杂、性质验证(1)装置A
①作用: 除去 H S 等杂质气体 ,防止HS等气体干扰乙炔性质的检验
2 2
②反应:CuSO +H S CuS↓+H SO
4 2 2 4
(2)装置B中的现象是溶液褪色
(3)装置C中的现象是溶液褪色
乙炔的实验室制取注意事项
(1)用试管作反应容器制取乙炔时,由于CaC 和水反应剧烈并产生泡沫,为防止产生的泡沫涌入导气
2
管,应在导气管附近塞入少量棉花。
(2)电石与水反应很剧烈,为了得到平稳的乙炔气流,可用饱和食盐水代替水,并用分液漏斗控制水
流的速率,让食盐水逐滴慢慢地滴入。
(3)因反应放热且电石易变成粉末,所以制取乙炔时不能使用启普发生器。
(4)由于电石中含有与水反应的杂质(如CaS、Ca P 等),使制得的乙炔中往往含有HS、PH 等杂质,
3 2 2 3
将混合气体通过盛有NaOH溶液或CuSO 溶液的洗气瓶可将杂质除去。
4
【典例05】丙炔和氯化氢之间发生加成反应,产物不可能是
A.1-氯丙烷 B.1,2-二氯丙烷 C.1-氯丙烯 D.2-氯丙烯
【答案】A
【详解】A.1个丙炔分子与2个HCl加成,则生成的产物中一定有2个Cl原子,不可能生成1-氯丙烷,A
错误;
B.1分子丙炔与2分子HCl发生加成反应,Cl原子分别连在不同的碳上,可生成1,2-二氯丙烷,B正确;
C.1分子丙炔与1分子HCl发生加成反应,生成1-氯丙烯,C正确;
D.1分子丙炔与1分子HCl发生加成反应,可生成2-氯丙烯,D正确;
故答案选A。
【典例06】已知 ,如果要合成 ,所用的起始原料可以是
A.1,3—戊二烯和2—丁炔
B.2,3—二甲基—1,3—丁二烯和丙烯
C.2,3—二甲基—1,3—戊二烯和乙炔
D.2—甲基—1,3—丁二烯和2—丁炔
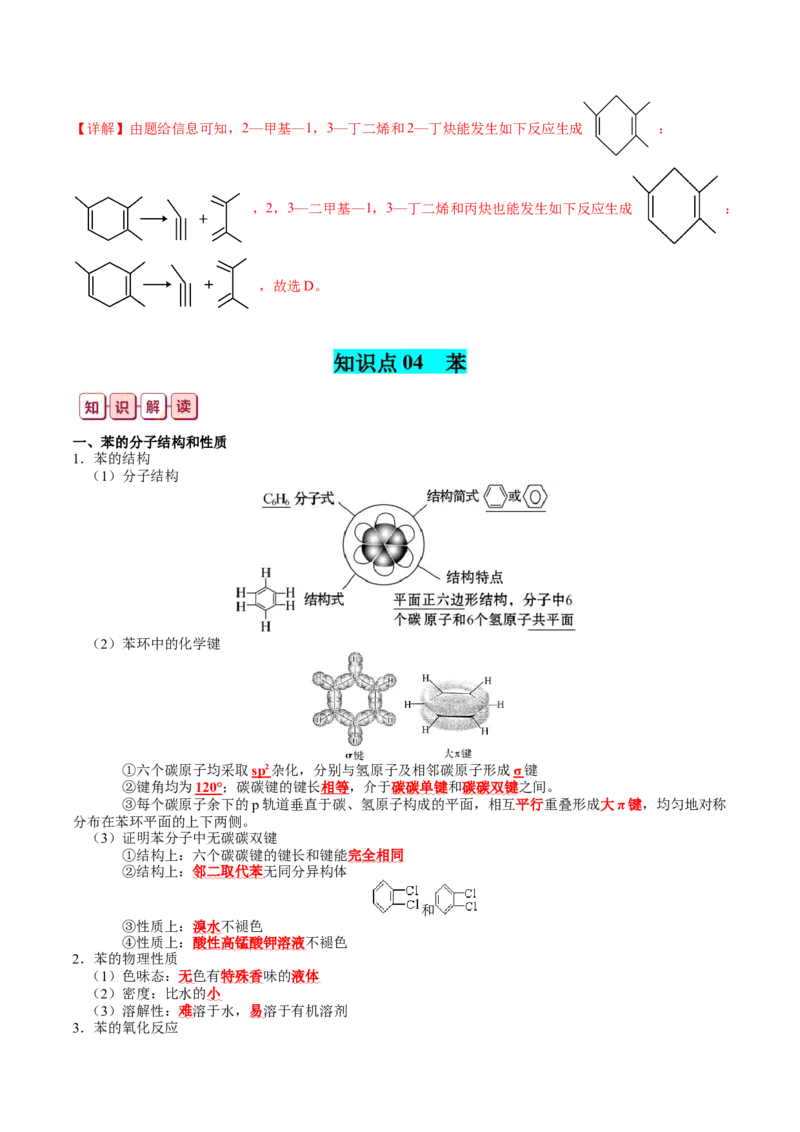
【答案】D【详解】由题给信息可知,2—甲基—1,3—丁二烯和2—丁炔能发生如下反应生成 :
,2,3—二甲基—1,3—丁二烯和丙炔也能发生如下反应生成 :
,故选D。
知识点 04 苯
一、苯的分子结构和性质
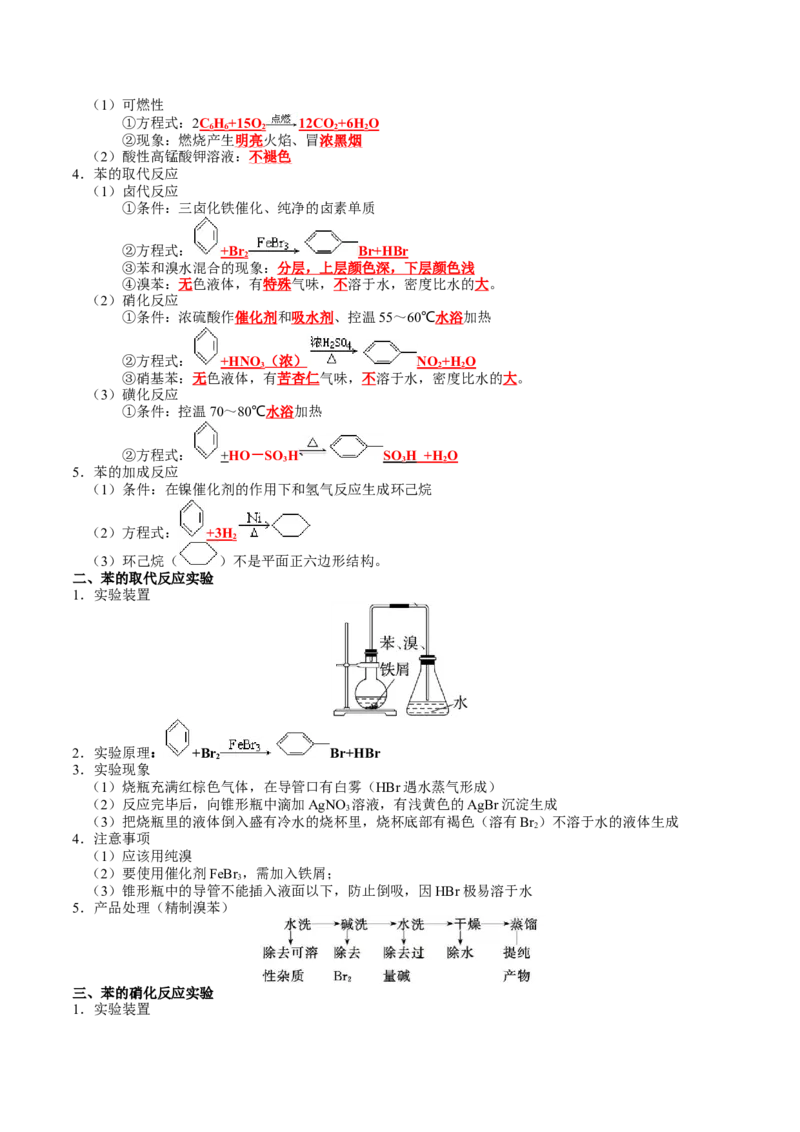
1.苯的结构
(1)分子结构
(2)苯环中的化学键
①六个碳原子均采取 sp 2 杂化,分别与氢原子及相邻碳原子形成σ 键
②键角均为120°;碳碳键的键长相等,介于碳碳单键和碳碳双键之间。
③每个碳原子余下的p轨道垂直于碳、氢原子构成的平面,相互平行重叠形成大π键,均匀地对称
分布在苯环平面的上下两侧。
(3)证明苯分子中无碳碳双键
①结构上:六个碳碳键的键长和键能完全相同
②结构上:邻二取代苯无同分异构体
和
③性质上:溴水不褪色
④性质上:酸性高锰酸钾溶液不褪色
2.苯的物理性质
(1)色味态:无色有特殊香味的液体
(2)密度:比水的小
(3)溶解性:难溶于水,易溶于有机溶剂
3.苯的氧化反应(1)可燃性
①方程式:2CH+15O 12 CO + 6 H O
6 6 2 2 2
②现象:燃烧产生明亮火焰、冒浓黑烟
(2)酸性高锰酸钾溶液:不褪色
4.苯的取代反应
(1)卤代反应
①条件:三卤化铁催化、纯净的卤素单质
②方程式: +Br Br+HBr
2
③苯和溴水混合的现象:分层,上层颜色深,下层颜色浅
④溴苯:无色液体,有特殊气味,不溶于水,密度比水的大。
(2)硝化反应
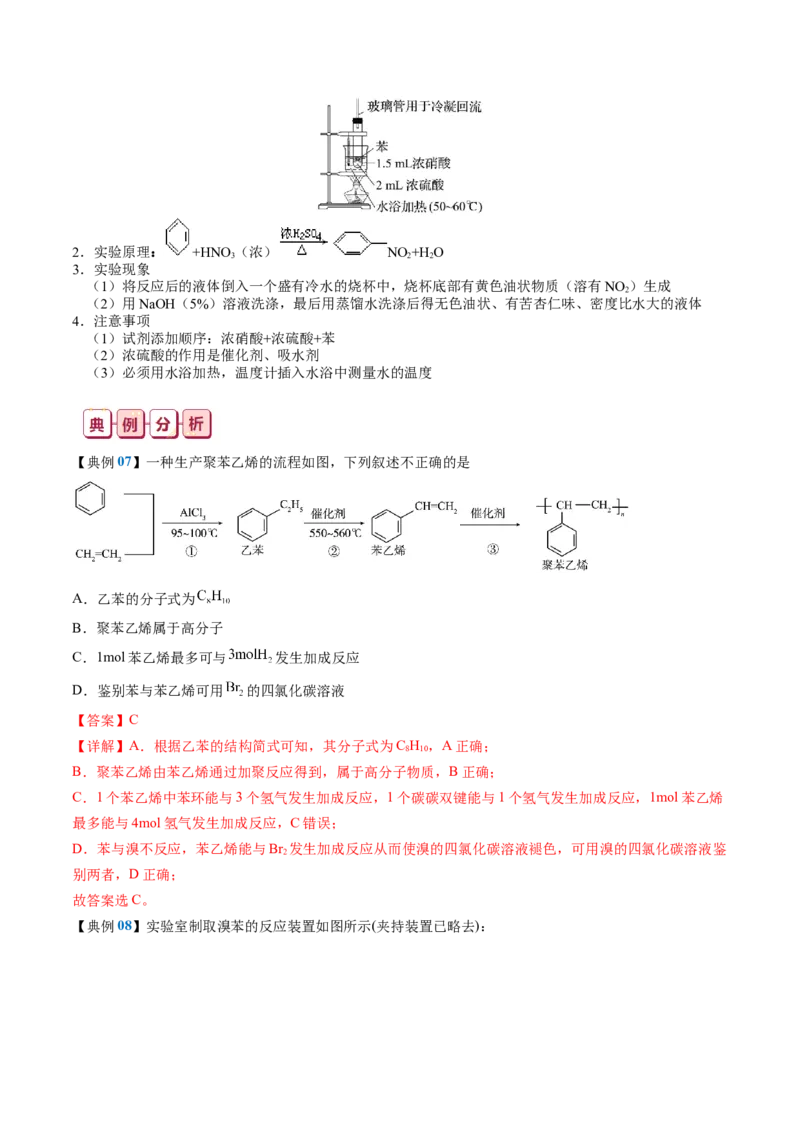
①条件:浓硫酸作催化剂和吸水剂、控温55~60℃水浴加热
②方程式: +HNO (浓) NO +H O
3 2 2
③硝基苯:无色液体,有苦杏仁气味,不溶于水,密度比水的大。
(3)磺化反应
①条件:控温70~80℃水浴加热
②方程式: +HO-SO H SO H +H O
3 3 2
5.苯的加成反应
(1)条件:在镍催化剂的作用下和氢气反应生成环己烷
(2)方程式: + 3H
2
(3)环己烷( )不是平面正六边形结构。
二、苯的取代反应实验
1.实验装置
2.实验原理: +Br Br+HBr
2
3.实验现象
(1)烧瓶充满红棕色气体,在导管口有白雾(HBr遇水蒸气形成)
(2)反应完毕后,向锥形瓶中滴加AgNO 溶液,有浅黄色的AgBr沉淀生成
3
(3)把烧瓶里的液体倒入盛有冷水的烧杯里,烧杯底部有褐色(溶有Br )不溶于水的液体生成
2
4.注意事项
(1)应该用纯溴
(2)要使用催化剂FeBr ,需加入铁屑;
3
(3)锥形瓶中的导管不能插入液面以下,防止倒吸,因HBr极易溶于水
5.产品处理(精制溴苯)
三、苯的硝化反应实验
1.实验装置2.实验原理: +HNO (浓) NO +H O
3 2 2
3.实验现象
(1)将反应后的液体倒入一个盛有冷水的烧杯中,烧杯底部有黄色油状物质(溶有NO )生成
2
(2)用NaOH(5%)溶液洗涤,最后用蒸馏水洗涤后得无色油状、有苦杏仁味、密度比水大的液体
4.注意事项
(1)试剂添加顺序:浓硝酸+浓硫酸+苯
(2)浓硫酸的作用是催化剂、吸水剂
(3)必须用水浴加热,温度计插入水浴中测量水的温度
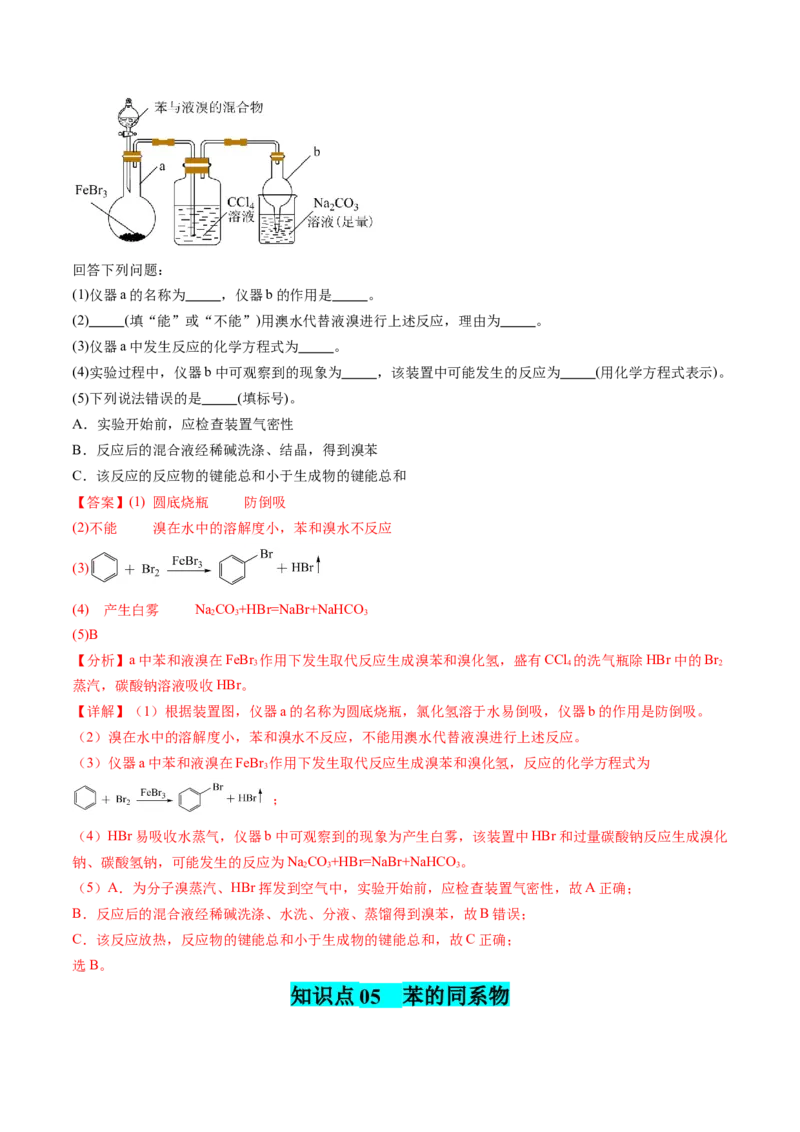
【典例07】一种生产聚苯乙烯的流程如图,下列叙述不正确的是
A.乙苯的分子式为
B.聚苯乙烯属于高分子
C.1mol苯乙烯最多可与 发生加成反应
D.鉴别苯与苯乙烯可用 的四氯化碳溶液
【答案】C
【详解】A.根据乙苯的结构简式可知,其分子式为C H ,A正确;
8 10
B.聚苯乙烯由苯乙烯通过加聚反应得到,属于高分子物质,B正确;
C.1个苯乙烯中苯环能与3个氢气发生加成反应,1个碳碳双键能与1个氢气发生加成反应,1mol苯乙烯
最多能与4mol氢气发生加成反应,C错误;
D.苯与溴不反应,苯乙烯能与Br 发生加成反应从而使溴的四氯化碳溶液褪色,可用溴的四氯化碳溶液鉴
2
别两者,D正确;
故答案选C。
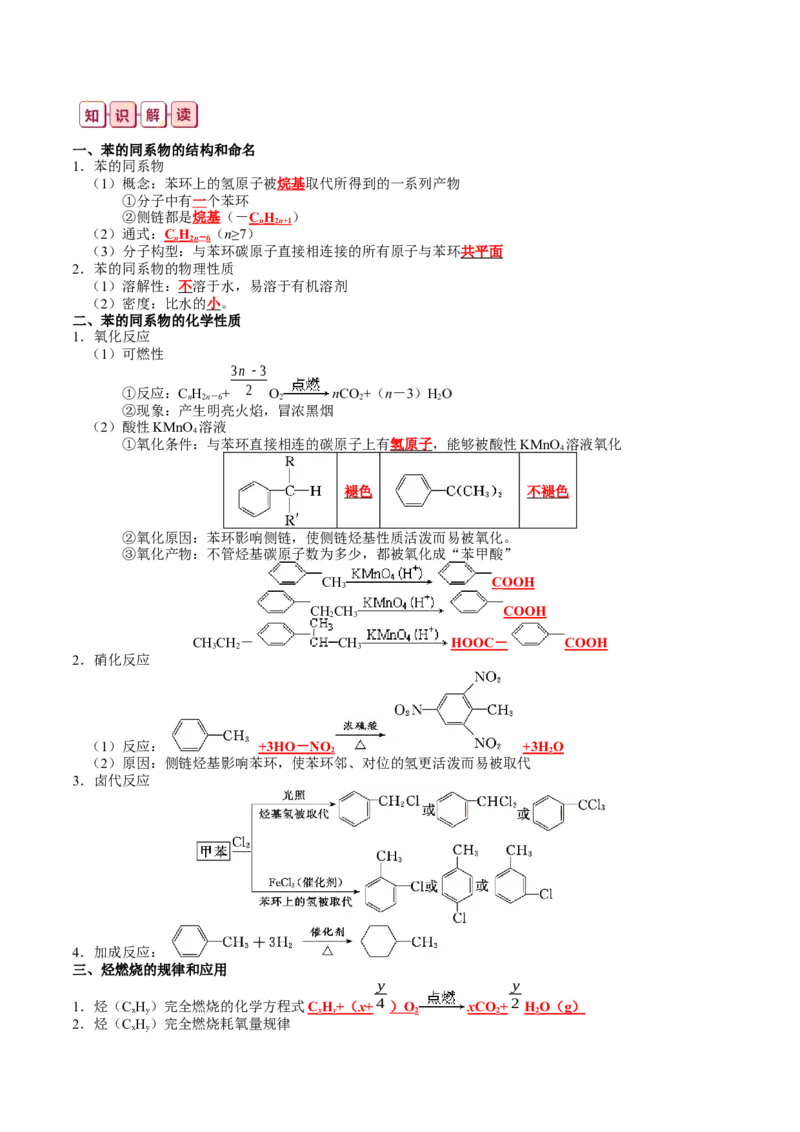
【典例08】实验室制取溴苯的反应装置如图所示(夹持装置已略去):回答下列问题:
(1)仪器a的名称为 ,仪器b的作用是 。
(2) (填“能”或“不能”)用澳水代替液溴进行上述反应,理由为 。
(3)仪器a中发生反应的化学方程式为 。
(4)实验过程中,仪器b中可观察到的现象为 ,该装置中可能发生的反应为 (用化学方程式表示)。
(5)下列说法错误的是 (填标号)。
A.实验开始前,应检查装置气密性
B.反应后的混合液经稀碱洗涤、结晶,得到溴苯
C.该反应的反应物的键能总和小于生成物的键能总和
【答案】(1) 圆底烧瓶 防倒吸
(2)不能 溴在水中的溶解度小,苯和溴水不反应
(3)
(4) 产生白雾 NaCO+HBr=NaBr+NaHCO
2 3 3
(5)B
【分析】a中苯和液溴在FeBr 作用下发生取代反应生成溴苯和溴化氢,盛有CCl 的洗气瓶除HBr中的Br
3 4 2
蒸汽,碳酸钠溶液吸收HBr。
【详解】(1)根据装置图,仪器a的名称为圆底烧瓶,氯化氢溶于水易倒吸,仪器b的作用是防倒吸。
(2)溴在水中的溶解度小,苯和溴水不反应,不能用澳水代替液溴进行上述反应。
(3)仪器a中苯和液溴在FeBr 作用下发生取代反应生成溴苯和溴化氢,反应的化学方程式为
3
;
(4)HBr易吸收水蒸气,仪器b中可观察到的现象为产生白雾,该装置中HBr和过量碳酸钠反应生成溴化
钠、碳酸氢钠,可能发生的反应为NaCO+HBr=NaBr+NaHCO 。
2 3 3
(5)A.为分子溴蒸汽、HBr挥发到空气中,实验开始前,应检查装置气密性,故A正确;
B.反应后的混合液经稀碱洗涤、水洗、分液、蒸馏得到溴苯,故B错误;
C.该反应放热,反应物的键能总和小于生成物的键能总和,故C正确;
选B。
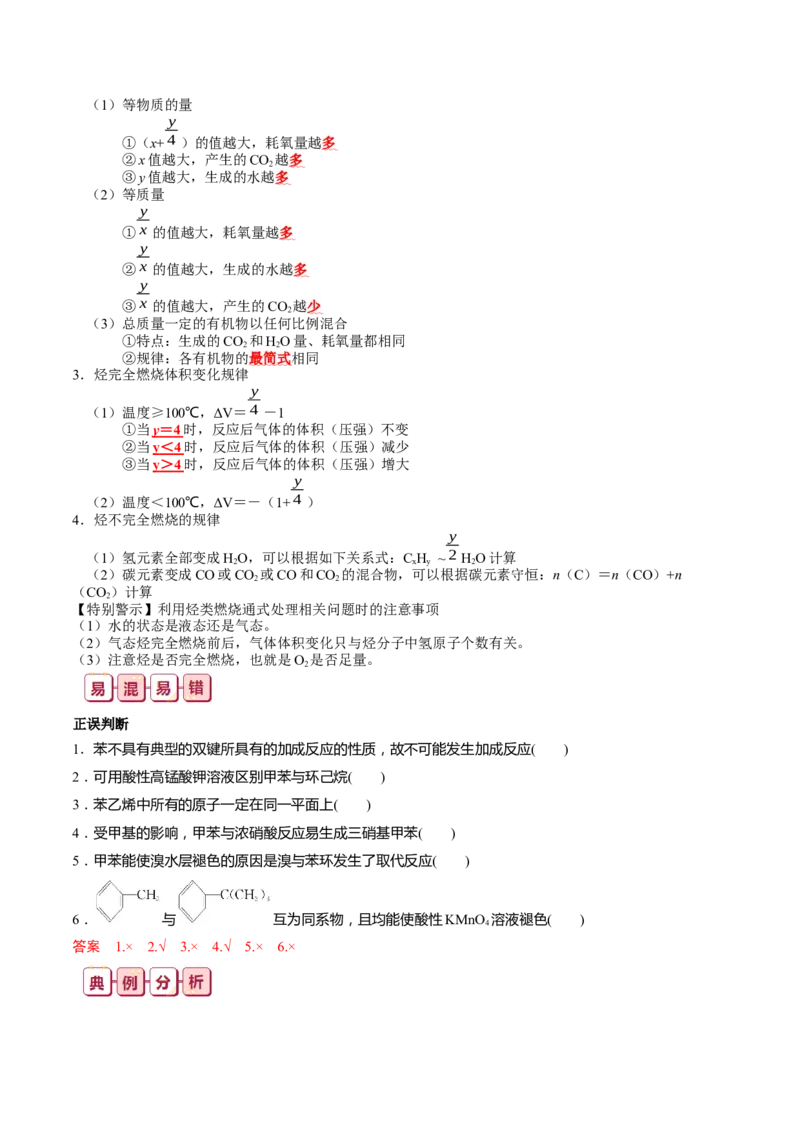
知识点 05 苯的同系物一、苯的同系物的结构和命名
1.苯的同系物
(1)概念:苯环上的氢原子被烷基取代所得到的一系列产物
①分子中有一个苯环
②侧链都是烷基(-C H )
n 2n+1
(2)通式:C H (n≥7)
n 2n-6
(3)分子构型:与苯环碳原子直接相连接的所有原子与苯环共平面
2.苯的同系物的物理性质
(1)溶解性:不溶于水,易溶于有机溶剂
(2)密度:比水的小。
二、苯的同系物的化学性质
1.氧化反应
(1)可燃性
3n-3
①反应:C H + 2 O nCO+(n-3)HO
n 2n-6 2 2 2
②现象:产生明亮火焰,冒浓黑烟
(2)酸性KMnO 溶液
4
①氧化条件:与苯环直接相连的碳原子上有氢原子,能够被酸性KMnO 溶液氧化
4
褪色 不褪色
②氧化原因:苯环影响侧链,使侧链烃基性质活泼而易被氧化。
③氧化产物:不管烃基碳原子数为多少,都被氧化成“苯甲酸”
CH COOH
3
CHCH COOH
2 3
CHCH- CH HOOC - COOH
3 2 3
2.硝化反应
(1)反应: +3HO - NO +3H O
2 2
(2)原因:侧链烃基影响苯环,使苯环邻、对位的氢更活泼而易被取代
3.卤代反应
4.加成反应:
三、烃燃烧的规律和应用
y y
1.烃(C H)完全燃烧的化学方程式CH + ( x + 4 ) O x CO +2 H O ( g )
x y x y 2 2 2
2.烃(C H)完全燃烧耗氧量规律
x y(1)等物质的量
y
①(x+4 )的值越大,耗氧量越多
②x值越大,产生的CO 越多
2
③y值越大,生成的水越多
(2)等质量
y
①x 的值越大,耗氧量越多
y
②x 的值越大,生成的水越多
y
③x 的值越大,产生的CO 越少
2
(3)总质量一定的有机物以任何比例混合
①特点:生成的CO 和HO量、耗氧量都相同
2 2
②规律:各有机物的最简式相同
3.烃完全燃烧体积变化规律
y
(1)温度≥100℃,ΔV=4 -1
①当 y = 4 时,反应后气体的体积(压强)不变
②当 y < 4 时,反应后气体的体积(压强)减少
③当 y > 4 时,反应后气体的体积(压强)增大
y
(2)温度<100℃,ΔV=-(1+4 )
4.烃不完全燃烧的规律
y
(1)氢元素全部变成HO,可以根据如下关系式:C H ~2 HO计算
2 x y 2
(2)碳元素变成CO或CO 或CO和CO 的混合物,可以根据碳元素守恒:n(C)=n(CO)+n
2 2
(CO)计算
2
【特别警示】利用烃类燃烧通式处理相关问题时的注意事项
(1)水的状态是液态还是气态。
(2)气态烃完全燃烧前后,气体体积变化只与烃分子中氢原子个数有关。
(3)注意烃是否完全燃烧,也就是O 是否足量。
2
正误判断
1.苯不具有典型的双键所具有的加成反应的性质,故不可能发生加成反应( )
2.可用酸性高锰酸钾溶液区别甲苯与环己烷( )
3.苯乙烯中所有的原子一定在同一平面上( )
4.受甲基的影响,甲苯与浓硝酸反应易生成三硝基甲苯( )
5.甲苯能使溴水层褪色的原因是溴与苯环发生了取代反应( )
6. 与 互为同系物,且均能使酸性KMnO 溶液褪色( )
4
答案 1.× 2.√ 3.× 4.√ 5.× 6.×【典例09】关于 的说法正确的是
A.分子中有3种杂化轨道类型的碳原子
B.分子中共平面的原子数目最多为14
C.分子的核磁共振氢谢图中共有5组峰
D.与 发生取代反应生成两种产物
【答案】A
【详解】A.sp3杂化的为甲基-CH 中的碳原子,sp2杂化的是苯环中的碳原子,直线结构的乙炔基的碳原子
3
为sp杂化;共有3种杂化类型,故A正确;
B.苯为平面结构,6个C原子和6个H原子共平面,乙炔基为直线结构,乙炔基的直线在苯的对角线上,
CH 为正四面体结构,最多3个原子共平面,甲基-CH 中的3个H原子最多有一个在苯的平面上,分子中
4 3
共平面的原子数目最多为12+1+2=15,故B错误;
C. 含有6种氢原子,故核磁共振氢谱图中共有6组峰,故C错误;
D.与氯气发生一氯取代时,产物有5种,但还有可能发生二氯、三氯等取代,所以取代产物远多于5种,
故D错误;
故选:A。
【典例10】下列对以下A、B、C、D四种有机化合物的论述,正确的是
A.这四种物质结构相似,且互为同分异构体
B.通过C−C单键的旋转,A、B、D三种物质均可分别实现所有原子共平面
C.若不考虑立体异构,C和D两种物质的一氯代物种数相同
D.若将等物的量的四种物质分别与足量Br /CCl 溶液反应,A和B消耗Br 的物质的量相同
2 4 2
【答案】C
【详解】A.根据它们结构简式,四种有机物的分子式分别为C H、C H、C H 、C H ,A和B互为同分
8 8 8 8 8 10 8 10
异构体,C和D互为同分异构体,故A错误;
B.D中含有两个甲基,根据甲烷的空间构型为正四面体,因此D中所有原子不可能共面,故B错误;
C.若不考虑立体异构,C中3种氢原子,一氯代物有3种,D中有3种氢原子,其一氯代物也是3种,故
C正确;
D.A中含有1个碳碳双键,B中含有4个碳碳双键,则等物质的量的A和B消耗溴单质物质的量不相同,
故D错误;答案为C。