文档内容
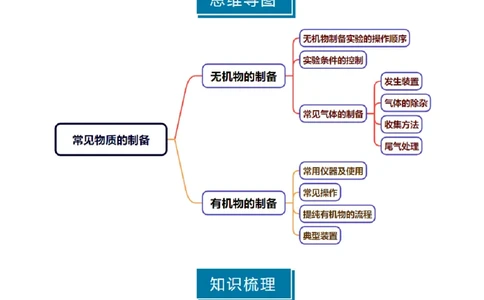
知识清单 32 常见物质的制备
知识点01无机物的制备 知识点02有机物的制备
知识点 01 无机物的制备
(1)实验操作顺序
(2)加热操作先后顺序的选择若气体制备实验需加热,应先加热气体发生装置,待产生的气体排尽装置中的空气后,再给实验中
其他需要加热的装置加热。
其目的:①防止爆炸(如氢气还原氧化铜);②保证产品纯度,防止反应物或生成物与空气中的物质
反应。
完成实验后,熄灭酒精灯的顺序则相反。
(3)防止实验中反应物或产物变质或损失
①实验中反应物或产物若易吸水潮解、水解等,要采取措施防止吸水;
②易挥发的液体产物要及时冷却;
③易挥发的液体反应物,需在反应装置中加装冷凝回流装置(如长导管、竖直的干燥管、冷凝管等);
④注意防止倒吸的问题。
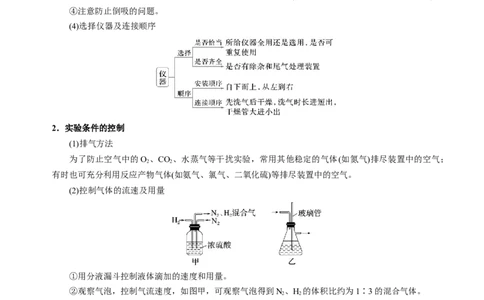
(4)选择仪器及连接顺序
2.实验条件的控制
(1)排气方法
为了防止空气中的O 、CO 、水蒸气等干扰实验,常用其他稳定的气体(如氮气)排尽装置中的空气;
2 2
有时也可充分利用反应产物气体(如氨气、氯气、二氧化硫)等排尽装置中的空气。
(2)控制气体的流速及用量
①用分液漏斗控制液体滴加的速度和用量。
②观察气泡,控制气流速度,如图甲,可观察气泡得到N、H 的体积比约为1∶3的混合气体。
2 2
③平衡气压,如图乙,用长玻璃管平衡气压,防堵塞。
(3)压送液体
根据装置的密封性,让反应生成气体或消耗气体,产生压强差,将液体压入或倒流入另一反应容器。
(4)温度控制
①控制低温的目的:减少某些反应物或产物分解,如HO、NH HCO 等;减少某些反应物或产物挥
2 2 4 3
发,如盐酸、氨水等;防止某些物质水解,避免副反应发生等。
②采取加热的目的:加快反应速率或使平衡移动,加速溶解等。
③常考的温度控制方式
a.水浴加热:均匀加热,反应温度在100 ℃以下。
b.油浴加热:均匀加热,反应温度在100~260 ℃之间。c.冰水冷却:使某物质液化、降低产物的溶解度;减少其他副反应,提高产品纯度等。
d.保温:如真空双层玻璃容器等。
3.常见气体的制备
(1)气体制备实验的基本思路
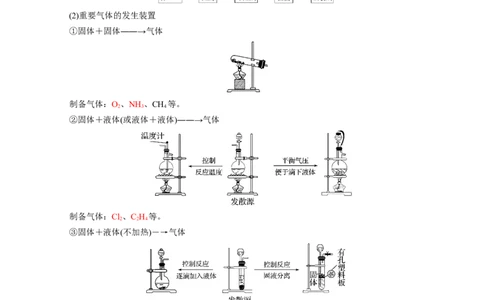
(2)重要气体的发生装置
①固体+固体――→气体
制备气体:O、NH 、CH 等。
2 3 4
②固体+液体(或液体+液体)――→气体
制备气体:Cl、C H 等。
2 2 4
③固体+液体(不加热)―→气体
制备气体:选择合适的药品和装置能制取中学化学中常见的气体。
(3)常见气体典型制备:
①Cl 的实验室制备
2②SO 的实验室制备
2
③NH 的实验室制备
3
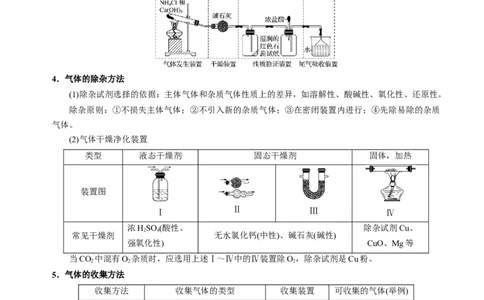
4.气体的除杂方法
(1)除杂试剂选择的依据:主体气体和杂质气体性质上的差异,如溶解性、酸碱性、氧化性、还原性。
除杂原则:①不损失主体气体;②不引入新的杂质气体;③在密闭装置内进行;④先除易除的杂质
气体。
(2)气体干燥净化装置
类型 液态干燥剂 固态干燥剂 固体,加热
装置图
Ⅰ Ⅱ Ⅲ Ⅳ
浓HSO (酸性、 除杂试剂Cu、
2 4
常见干燥剂 无水氯化钙(中性)、碱石灰(碱性)
强氧化性) CuO、Mg等
当CO 中混有O 杂质时,应选用上述Ⅰ~Ⅳ中的Ⅳ装置除O,除杂试剂是Cu粉。
2 2 2
5.气体的收集方法
收集方法 收集气体的类型 收集装置 可收集的气体(举例)
难溶于水或微溶于水,且不与 O、H、NO、CO
2 2
排水法
水反应的气体 等
向上排 密度大于空气且不与空气中的 Cl、SO 、NO 、
2 2 2
空气法 成分反应 CO
2
排空
气法
向下排 密度小于空气且不与空气中的
H、NH
2 3
空气法 成分反应
6.尾气处理的方法及装置(1)原因:有些气体有毒或有可燃性,任其逸散到空气中,会污染空气或者引发火灾、爆炸等灾害。
(2)处理方法:一般根据气体的相关性质,使其转化为非气态物质或无毒物质,如酸性有毒气体用碱
溶液吸收,可燃性气体用点燃等措施。
(3)尾气处理装置(见下图a、b、c)
①实验室制取Cl 时,尾气的处理可采用b装置。
2
②制取CO时,尾气处理可采用a、c装置。
③制取H 时,尾气处理可采用a、c装置。
2
7.防倒吸装置
肚容式 分液式
(1)用铁片和稀HSO 反应制取H 时,为加快产生H 的速率可改用浓HSO ( × )
2 4 2 2 2 4
错因:浓硫酸使铁钝化,不能生成H。
2
(2)用KMnO 固体和用KClO 固体制备O 的装置完全相同( √ )
4 3 2
(3)用向上排空气法收集铜粉和稀硝酸反应产生的NO( × )
错因:NO和氧气反应,应用排水法收集。
(4)浓盐酸与MnO 反应制备纯净Cl:气体产物先通过浓硫酸,后通过饱和食盐水( × )
2 2
错因:先干燥后通过饱和食盐水时会混入水蒸气,应后干燥。
(5)吸收NH 可用如下图装置,或将有机溶剂CCl 换成苯( × )
3 4
错因:NH 极易溶于水,如图所示装置可以防倒吸,苯的密度小于水,不能有效防倒吸。
3
(6)可利用如图装置收集H( × )
2
错因:排水法收集气体时进气管短,出水管要深入广口瓶底部。(7)SO 是还原性气体,不能用浓硫酸干燥( × )
2
错因:SO 与浓硫酸不反应,可以用浓硫酸干燥。
2
(8)使用MnO 作催化剂制备氧气,不一定需要加热( √ )
2
错因:若用MnO 催化氯酸钾分解需要加热,而催化过氧化氢分解不需加热。
2
(9)实验室中可利用二氧化锰或高锰酸钾与浓盐酸反应制取氯气,两制备方法中氯气的发生装置完全相同(
× )
错因:二氧化锰与浓盐酸反应需要加热,高锰酸钾与浓盐酸反应不需要加热,二者制备氯气的装置不同。
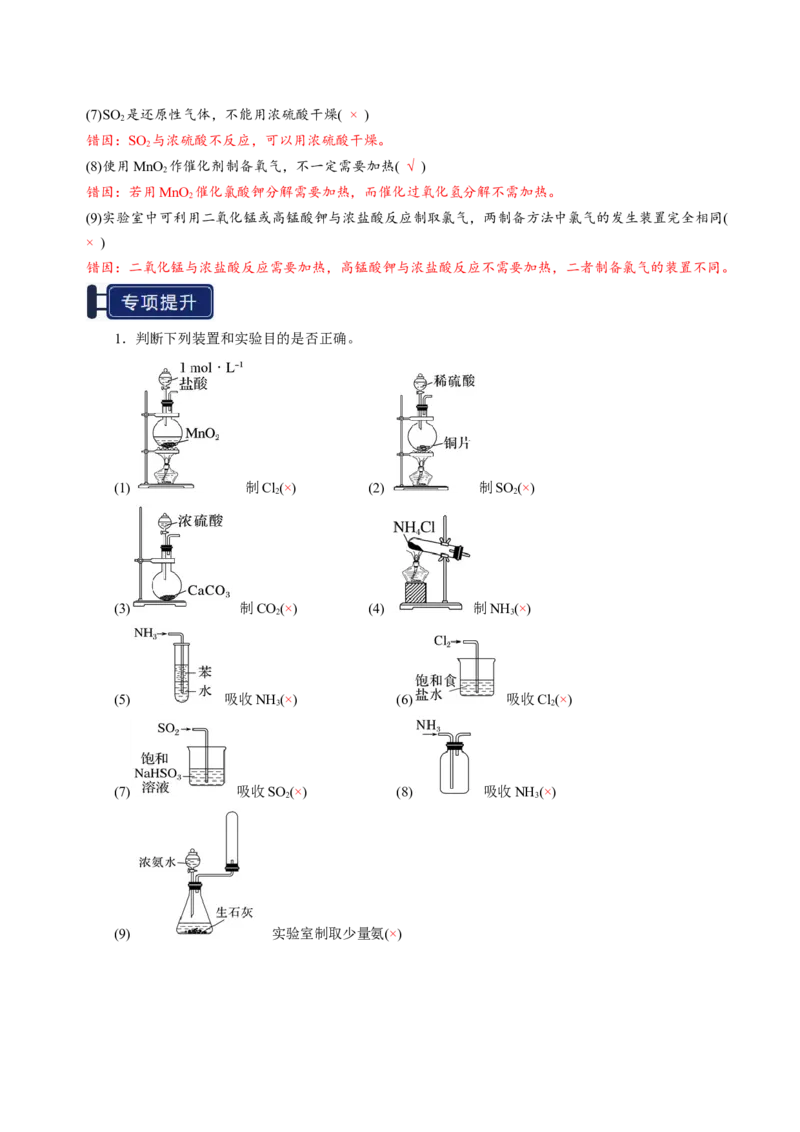
1.判断下列装置和实验目的是否正确。
(1) 制Cl(×) (2) 制SO (×)
2 2
(3) 制CO(×) (4) 制NH (×)
2 3
(5) 吸收NH (×) (6) 吸收Cl(×)
3 2
(7) 吸收SO (×) (8) 吸收NH (×)
2 3
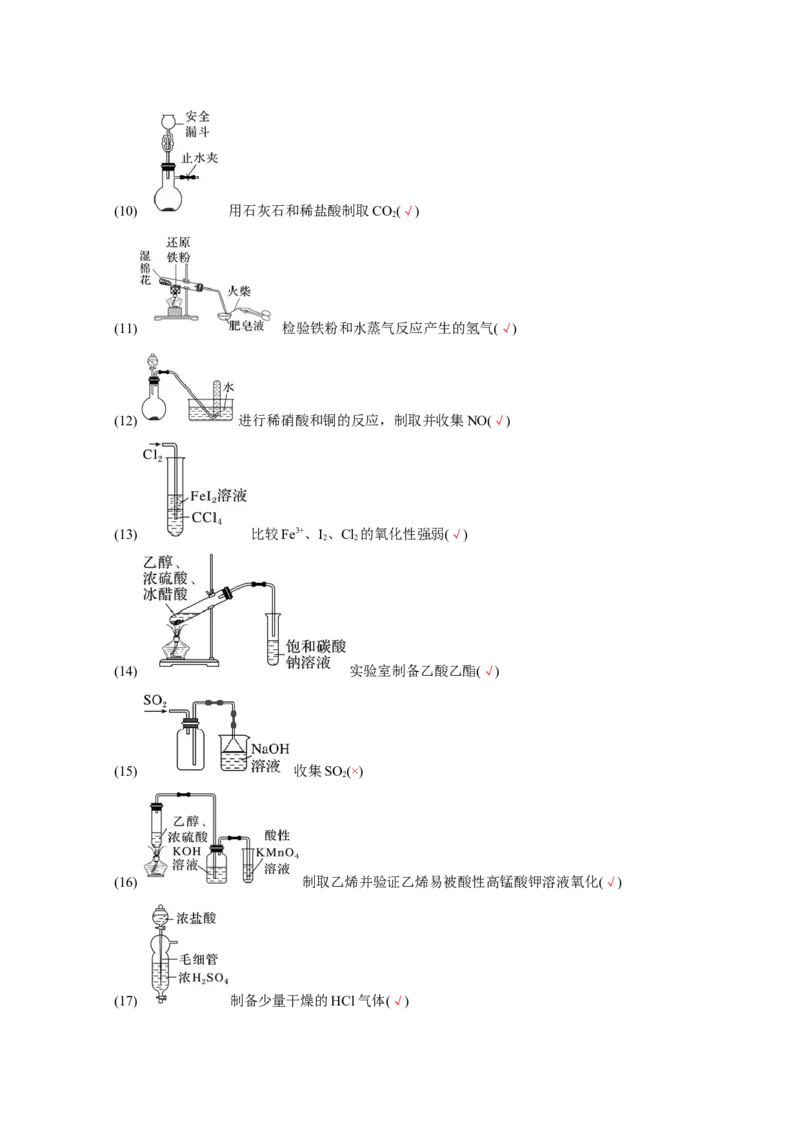
(9) 实验室制取少量氨(×)(10) 用石灰石和稀盐酸制取CO(√)
2
(11) 检验铁粉和水蒸气反应产生的氢气(√)
(12) 进行稀硝酸和铜的反应,制取并收集NO(√)
(13) 比较Fe3+、I、Cl 的氧化性强弱(√)
2 2
(14) 实验室制备乙酸乙酯(√)
(15) 收集SO (×)
2
(16) 制取乙烯并验证乙烯易被酸性高锰酸钾溶液氧化(√)
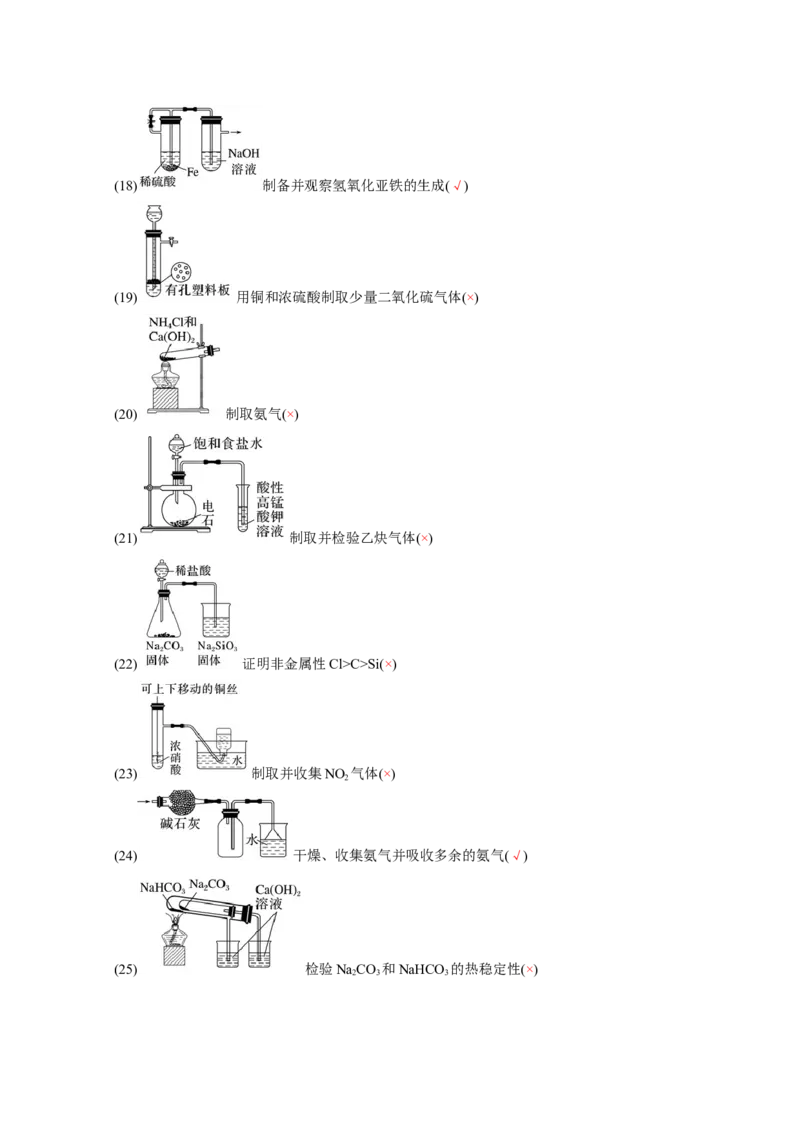
(17) 制备少量干燥的HCl气体(√)(18) 制备并观察氢氧化亚铁的生成(√)
(19) 用铜和浓硫酸制取少量二氧化硫气体(×)
(20) 制取氨气(×)
(21) 制取并检验乙炔气体(×)
(22) 证明非金属性Cl>C>Si(×)
(23) 制取并收集NO 气体(×)
2
(24) 干燥、收集氨气并吸收多余的氨气(√)
(25) 检验NaCO 和NaHCO 的热稳定性(×)
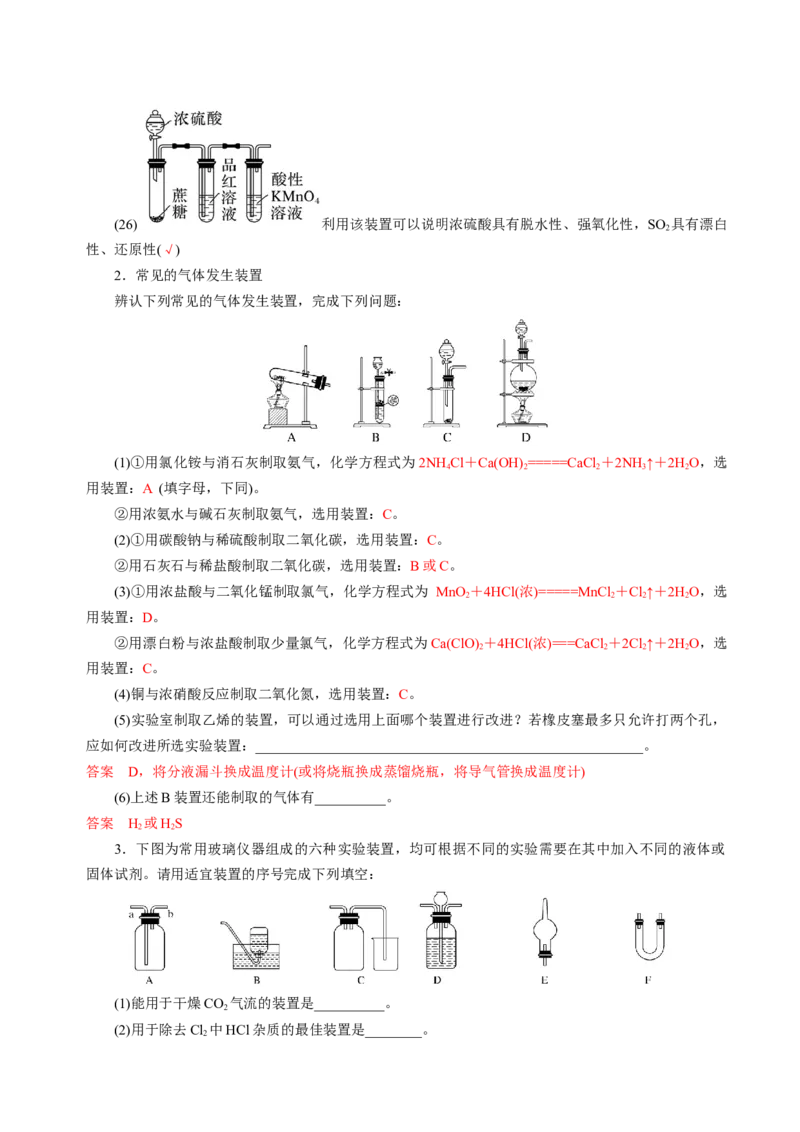
2 3 3(26) 利用该装置可以说明浓硫酸具有脱水性、强氧化性,SO 具有漂白
2
性、还原性(√)
2.常见的气体发生装置
辨认下列常见的气体发生装置,完成下列问题:
(1)①用氯化铵与消石灰制取氨气,化学方程式为2NH Cl+Ca(OH) =====CaCl +2NH ↑+2HO,选
4 2 2 3 2
用装置:A (填字母,下同)。
②用浓氨水与碱石灰制取氨气,选用装置:C。
(2)①用碳酸钠与稀硫酸制取二氧化碳,选用装置:C。
②用石灰石与稀盐酸制取二氧化碳,选用装置:B或C。
(3)①用浓盐酸与二氧化锰制取氯气,化学方程式为 MnO +4HCl(浓)=====MnCl +Cl↑+2HO,选
2 2 2 2
用装置:D。
②用漂白粉与浓盐酸制取少量氯气,化学方程式为Ca(ClO) +4HCl(浓)===CaCl +2Cl↑+2HO,选
2 2 2 2
用装置:C。
(4)铜与浓硝酸反应制取二氧化氮,选用装置:C。
(5)实验室制取乙烯的装置,可以通过选用上面哪个装置进行改进?若橡皮塞最多只允许打两个孔,
应如何改进所选实验装置:_______________________________________________________。
答案 D,将分液漏斗换成温度计(或将烧瓶换成蒸馏烧瓶,将导气管换成温度计)
(6)上述B装置还能制取的气体有__________。
答案 H 或HS
2 2
3.下图为常用玻璃仪器组成的六种实验装置,均可根据不同的实验需要在其中加入不同的液体或
固体试剂。请用适宜装置的序号完成下列填空:
(1)能用于干燥CO 气流的装置是__________。
2
(2)用于除去Cl 中HCl杂质的最佳装置是________。
2(3)用于尾气吸收并能防止液体倒吸到反应装置中的是________。
(4)接在气体制备的连续实验装置中间,用于控制气流平稳的装置是________。
(5)利用装置A收集CO 气体,应从______口进气。A中装满水,用排水法测量生成H 的体积,应
2 2
从______口进气。
答案 (1)AEF (2)A (3)CE (4)D (5)a b
4.一套装置可以用于制备多种气体,根据如图“套装”回答下列问题。
(1)若使用如图所示装置制备干燥的SO 气体:
2
①A中盛液体的玻璃仪器名称是______________________,实验开始后A中反应的化学方程式为
_____________________________________________。
②B装置的作用是_______________________;C装置的作用是____________________。
③E装置中固体试剂为________。
(2)若使用如图所示装置制备干燥的Cl:
2
①A中反应的化学方程式为______________________________。
②B装置的作用为除去Cl 中混有的HCl,则B装置中盛装的试剂为________,如何改进装置?
2
________________________;C装置的作用是_____________________________。
答案 (1)①分液漏斗 NaSO +HSO (浓)===Na SO +SO ↑+HO ②防倒吸 干燥SO 气体
2 3 2 4 2 4 2 2 2
③碱石灰 (2)①2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO[或KClO +6HCl(浓)===KCl+
4 2 2 2 3
3Cl↑+3HO] ②饱和食盐水 导管“长进短出” 干燥Cl
2 2 2
5.如图是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已
略去)。请根据下列要求回答问题。
(1)若烧瓶中盛装锌片,分液漏斗中盛装稀硫酸,则:
①当仪器连接顺序为A→C→B→B→D时,两次使用B装置,其中所盛的药品依次是CuO、无水
CuSO 粉末。此实验的目的是 ,D装置的作用是 。
4
②为了使B装置中CuO反应充分,在不改变现有药品的条件下,可采取的方法有________________
________________(写一种)。
③加热前必须进行的操作是 。
(2)若烧瓶中盛装NaO 固体,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞,则:
2 2
①烧瓶内产生的气体主要有 (写化学式)。②用产生的气体做氨的催化氧化实验,各装置按气流方向从左到右的连接顺序是 (填
字母)→E。
③B装置中反应的化学方程式为 。
答案:(1)①验证H 的还原性并检验其氧化产物 防止空气中的水蒸气进入B装置,干扰H 氧化产物
2 2
的检验
②控制分液漏斗的活塞,使稀HSO 缓慢滴下(或向烧瓶中加水或将烧瓶放入冰水中或用冰毛巾捂着烧
2 4
瓶等,其他答案合理即可)
③检验装置中空气是否排尽(或检验氢气是否纯净)
(2)①O、NH ②A→D→B
2 3
催化剂
③4NH +5O 4NO+6HO
3 2 △ 2
解析:(1)①A装置中锌片与稀硫酸反应产生H ,用C装置对H 进行干燥,然后依次通过分别盛有
2 2
CuO、无水CuSO 粉末的B装置;通过盛有CuO的B装置时,氢气与CuO反应生成Cu和HO;通过盛
4 2
有无水CuSO 粉末的B装置时,可以检验生成的水,故实验目的是验证H 的还原性并检验其氧化产物;
4 2
D装置的作用是防止空气中的水蒸气进入B装置,干扰产物HO的检验。②使B装置中CuO反应充分,
2
在不改变现有药品的条件下,可以减缓A装置中产生氢气的速率,如控制稀硫酸的滴入速率、控制烧瓶
的温度等。③加热前必须检验装置中空气是否排尽或检验氢气是否纯净。(2)①滴入浓氨水,则NaO
2 2
与HO反应生成O ,放热使氨水挥发,氨气逸出。②做氨的催化氧化实验时,A装置为O 、NH 的发生
2 2 2 3
装置,由于产生的O、NH 中含有水蒸气,需要先通过D装置干燥后再进入B装置发生催化氧化反应。
2 3
知识点 02 有机物的制备
1.有机物制备实验的常用仪器
2.常见操作
(1)加热:酒精灯的火焰温度一般在400~500 ℃,乙酸乙酯的制取、石油的蒸馏等实验选用酒精灯加
热,若温度要求更高,可选用酒精喷灯或电炉加热。除上述加热方式外还可以根据加热的温度要求选择
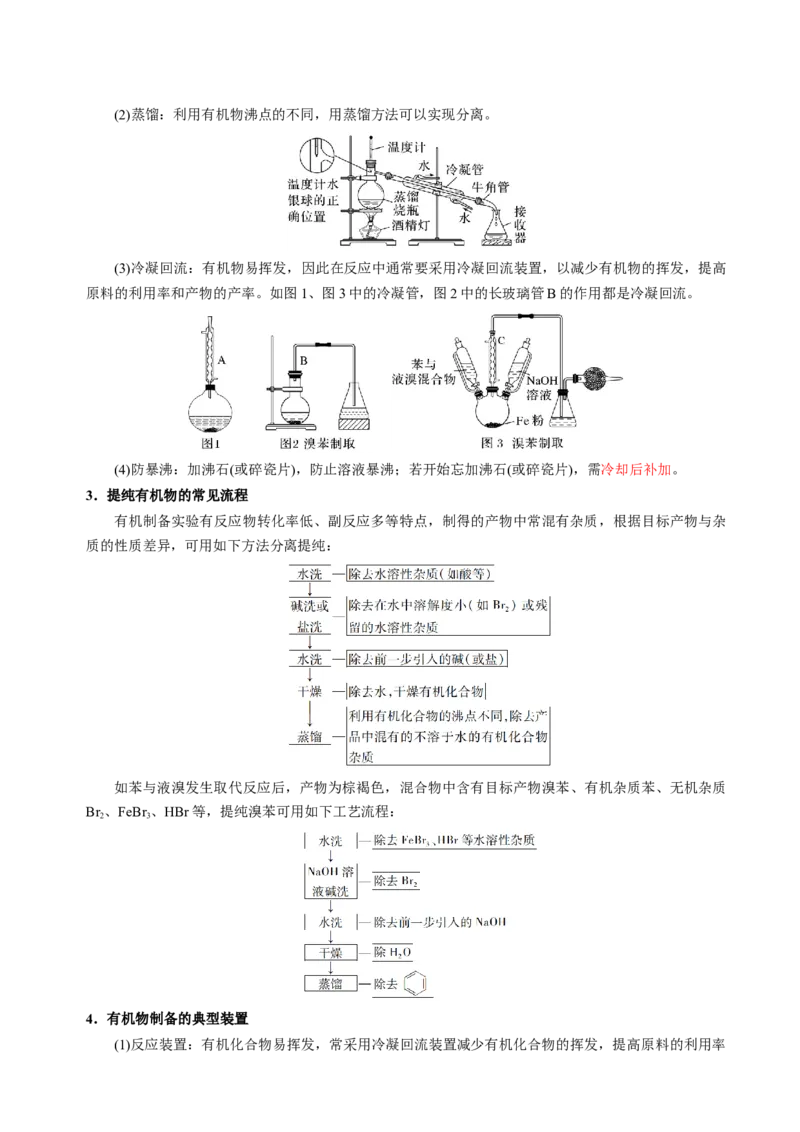
水浴、油浴、沙浴加热。(2)蒸馏:利用有机物沸点的不同,用蒸馏方法可以实现分离。
(3)冷凝回流:有机物易挥发,因此在反应中通常要采用冷凝回流装置,以减少有机物的挥发,提高
原料的利用率和产物的产率。如图1、图3中的冷凝管,图2中的长玻璃管B的作用都是冷凝回流。
(4)防暴沸:加沸石(或碎瓷片),防止溶液暴沸;若开始忘加沸石(或碎瓷片),需冷却后补加。
3.提纯有机物的常见流程
有机制备实验有反应物转化率低、副反应多等特点,制得的产物中常混有杂质,根据目标产物与杂
质的性质差异,可用如下方法分离提纯:
如苯与液溴发生取代反应后,产物为棕褐色,混合物中含有目标产物溴苯、有机杂质苯、无机杂质
Br 、FeBr 、HBr等,提纯溴苯可用如下工艺流程:
2 3
4.有机物制备的典型装置
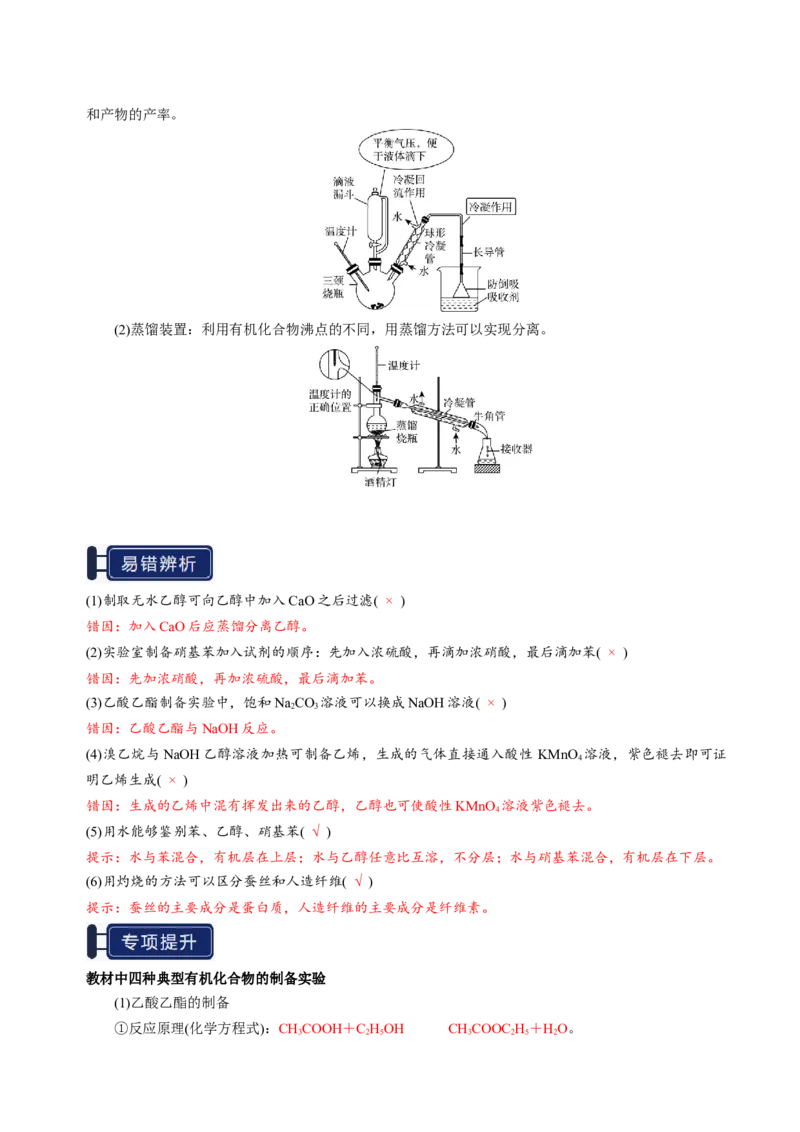
(1)反应装置:有机化合物易挥发,常采用冷凝回流装置减少有机化合物的挥发,提高原料的利用率和产物的产率。
(2)蒸馏装置:利用有机化合物沸点的不同,用蒸馏方法可以实现分离。
(1)制取无水乙醇可向乙醇中加入CaO之后过滤( × )
错因:加入CaO后应蒸馏分离乙醇。
(2)实验室制备硝基苯加入试剂的顺序:先加入浓硫酸,再滴加浓硝酸,最后滴加苯( × )
错因:先加浓硝酸,再加浓硫酸,最后滴加苯。
(3)乙酸乙酯制备实验中,饱和NaCO 溶液可以换成NaOH溶液( × )
2 3
错因:乙酸乙酯与NaOH反应。
(4)溴乙烷与NaOH乙醇溶液加热可制备乙烯,生成的气体直接通入酸性 KMnO 溶液,紫色褪去即可证
4
明乙烯生成( × )
错因:生成的乙烯中混有挥发出来的乙醇,乙醇也可使酸性KMnO 溶液紫色褪去。
4
(5)用水能够鉴别苯、乙醇、硝基苯( √ )
提示:水与苯混合,有机层在上层;水与乙醇任意比互溶,不分层;水与硝基苯混合,有机层在下层。
(6)用灼烧的方法可以区分蚕丝和人造纤维( √ )
提示:蚕丝的主要成分是蛋白质,人造纤维的主要成分是纤维素。
教材中四种典型有机化合物的制备实验
(1)乙酸乙酯的制备
①反应原理(化学方程式):CHCOOH+C HOHCHCOOC H+HO。
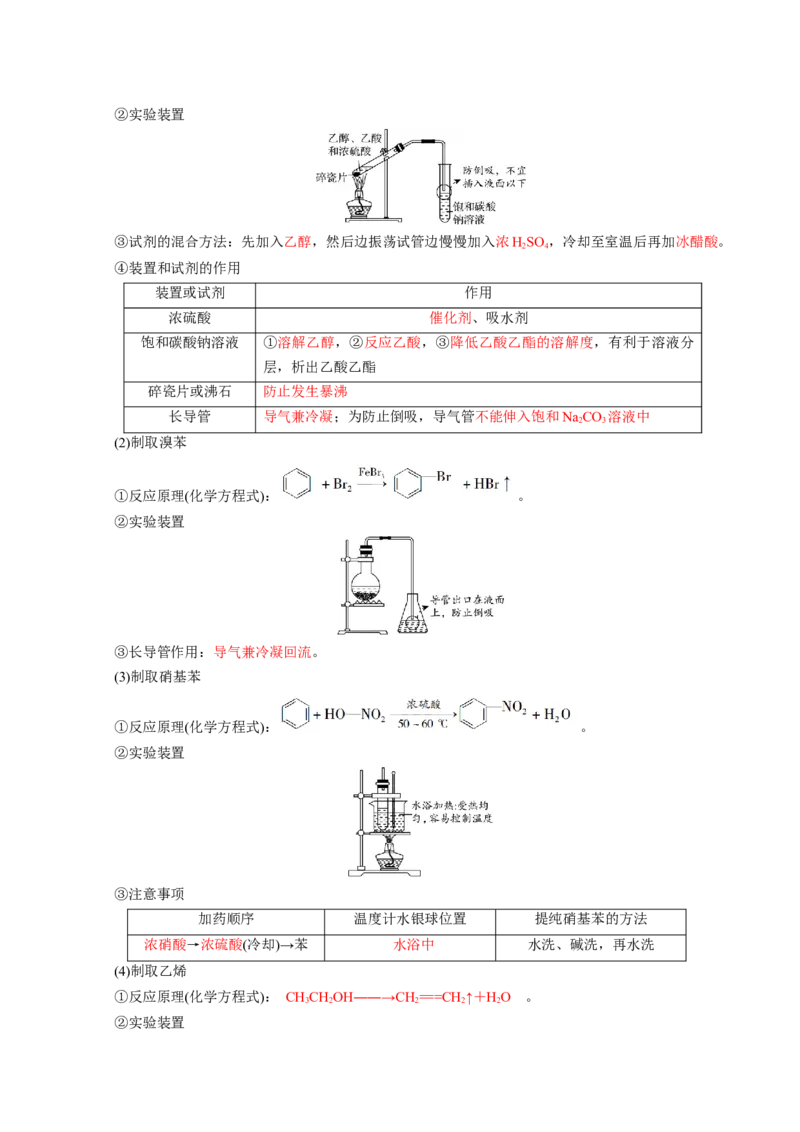
3 2 5 3 2 5 2②实验装置
③试剂的混合方法:先加入乙醇,然后边振荡试管边慢慢加入浓HSO ,冷却至室温后再加冰醋酸。
2 4
④装置和试剂的作用
装置或试剂 作用
浓硫酸 催化剂、吸水剂
饱和碳酸钠溶液 ①溶解乙醇,②反应乙酸,③降低乙酸乙酯的溶解度,有利于溶液分
层,析出乙酸乙酯
碎瓷片或沸石 防止发生暴沸
长导管 导气兼冷凝;为防止倒吸,导气管不能伸入饱和NaCO 溶液中
2 3
(2)制取溴苯
①反应原理(化学方程式): 。
②实验装置
③长导管作用:导气兼冷凝回流。
(3)制取硝基苯
①反应原理(化学方程式): 。
②实验装置
③注意事项
加药顺序 温度计水银球位置 提纯硝基苯的方法
浓硝酸→浓硫酸(冷却)→苯 水浴中 水洗、碱洗,再水洗
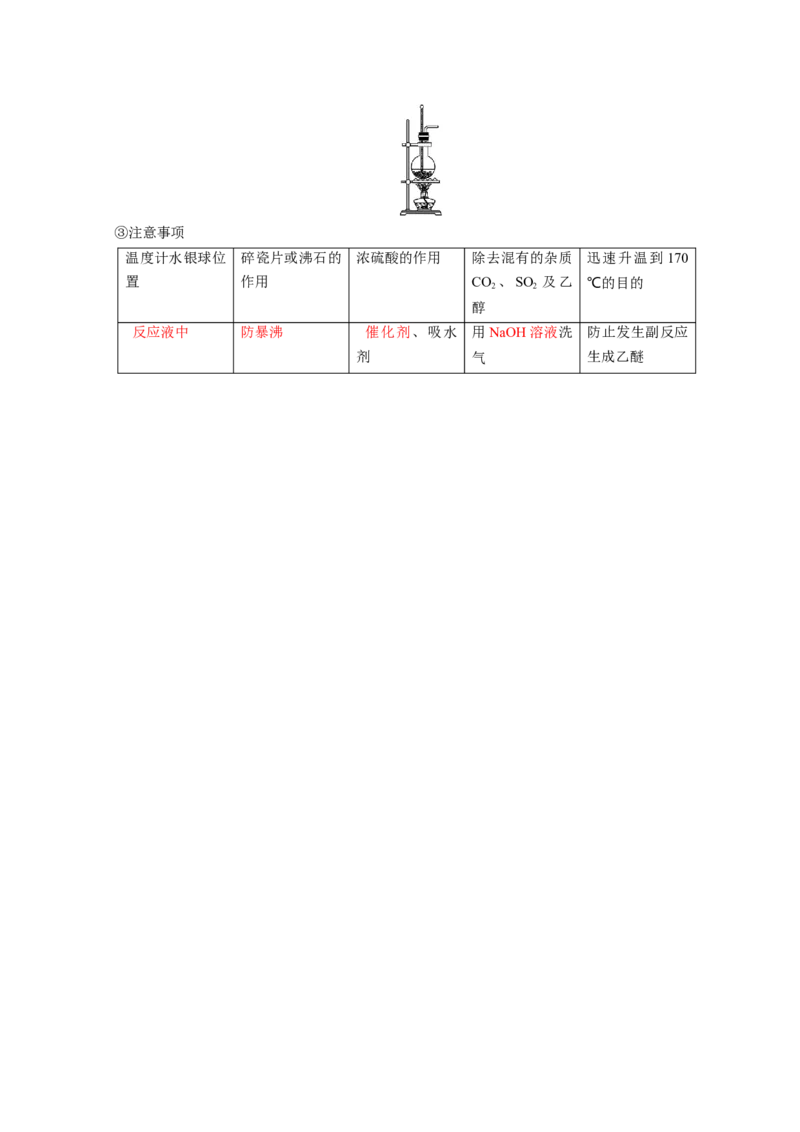
(4)制取乙烯
①反应原理(化学方程式): CHCHOH――→CH===CH ↑+HO 。
3 2 2 2 2
②实验装置③注意事项
温度计水银球位 碎瓷片或沸石的 浓硫酸的作用 除去混有的杂质 迅速升温到 170
置 作用 CO 、SO 及乙 ℃的目的
2 2
醇
反应液中 防暴沸 催化剂、吸水 用NaOH溶液洗 防止发生副反应
剂 气 生成乙醚