文档内容
福宁古五校教学联合体 2023 届高三毕业班三月质量检测
化学试题
(考试时间:75分钟 满分:100分)
注意事项:1.答卷前,考生务必将班级、姓名、座号填写清楚。
2.每小题选出答案后,填入答案卷中。
3.考试结束,考生只将答案卷交回,试卷自己保留。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Fe-56 Co-59
第Ⅰ卷(选择题,共 40分)
选择题(10小题,每小题4分,共40分。每小题只有一个选项符合题意)
1. 化学和生产生活紧密相关,下列叙述错误的是
A. 硝酸铵是一种高效氮肥,但受热或经撞击易发生爆炸,因此必须作改性处理才能施用
B. 加工馒头、面包和饼干等产品时,加入一些膨松剂(如碳酸氢铵、碳酸氢钠),可中和
酸和受热分解
C. 糖类、油脂、蛋白质是人体基本营养物质,均属于高分子化合物
D. 免洗洗手消毒液的成分——活性银离子、乙醇均能使蛋白质变性
2.N 为阿伏加德罗常数的值,关于反应O +2KI+H O=2KOH+I +O 的说法正确的是
A 3 2 2 2
A.标准状况下5.6LI 含碘原子数目为0.5N
2 A
B.常温常压下16gO 完全反应得到电子数目为2N
3 A
C.0.1mol/LKI溶液中含钾离子数目为0.1N
A
D.4.8gO 和O 的混合气体含氧原子数目为0.3N
2 3 A
3.蟾蜍是捕食害虫的田园卫士,还能向人类提供治病良药。蟾蜍的药用成分之一华蟾毒
精醇的结构如图。下列说法正确的是
A.该物质属于芳香族化合物
B.该物质可发生加成反应、取代反应、氧化反应
C.1mol该物质能消耗4molNaOH
D.该物质可以使酸性高锰酸钾溶液和溴水褪色,且原理相同
4.常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 小苏打溶液中:K+、Na+、Br—、AlO —
2
B.c(OH— )/c(H+)=1012的溶液中:[Ag(NH ) ]+、K+、Cl—、NO —
3 2 3
C.pH=7的溶液中:NH +、Fe3+、Cl—、SO 2—
4 4
D. 水电离的c(OH—)=1×10—13mol·L—1的溶液中:K+、Cl—、CH COO—、Cu2+
3
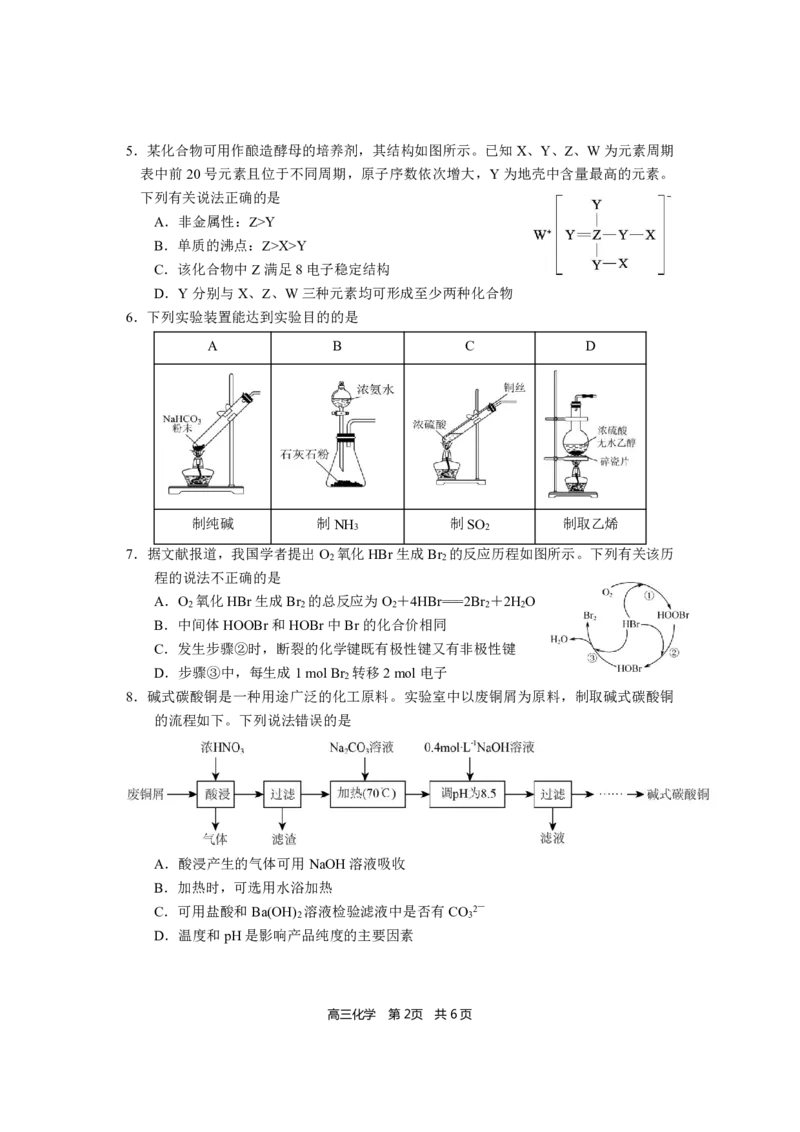
高三化学 第1页 共6页5.某化合物可用作酿造酵母的培养剂,其结构如图所示。已知X、Y、Z、W为元素周期
表中前20号元素且位于不同周期,原子序数依次增大,Y为地壳中含量最高的元素。
下列有关说法正确的是
A.非金属性:Z>Y
B.单质的沸点:Z>X>Y
C.该化合物中Z满足8电子稳定结构
D.Y分别与X、Z、W三种元素均可形成至少两种化合物
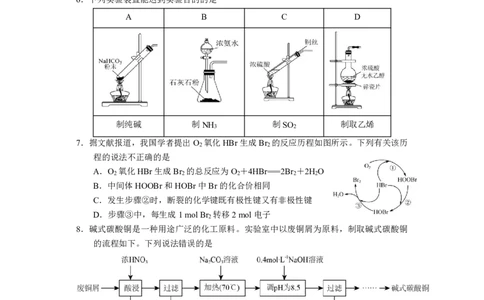
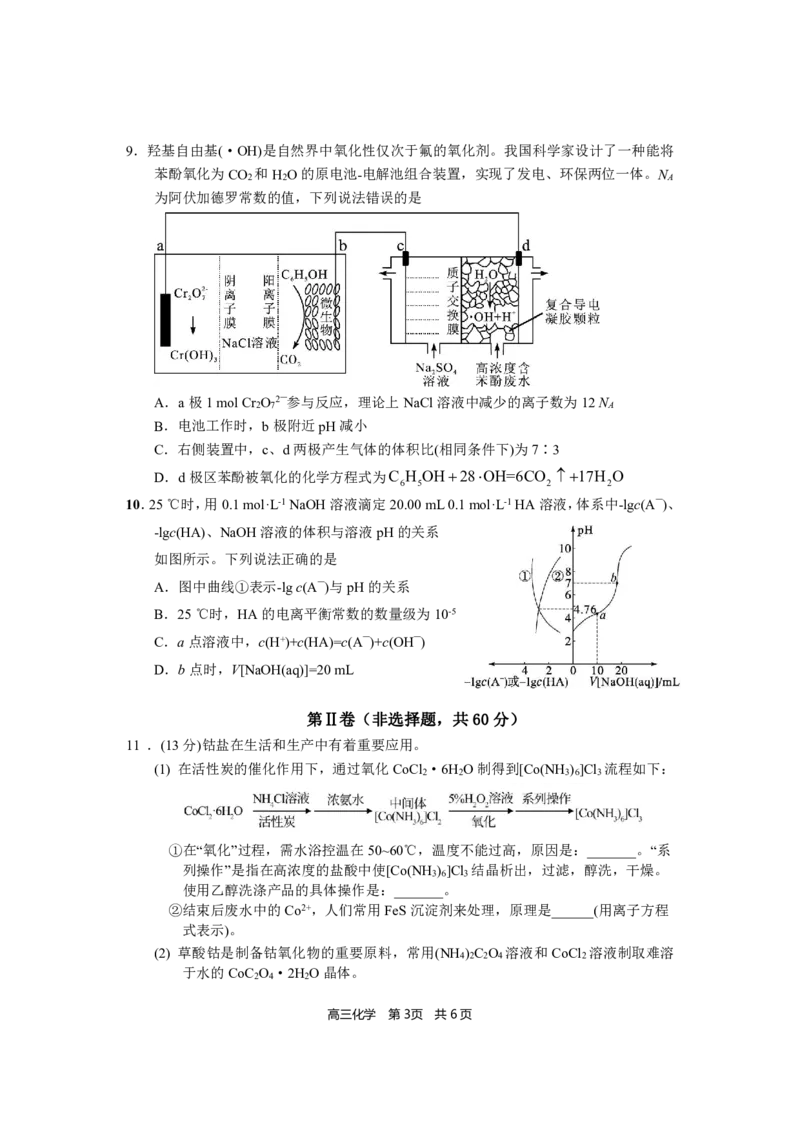
6.下列实验装置能达到实验目的的是
A B C D
制纯碱 制NH 制SO 制取乙烯
3 2
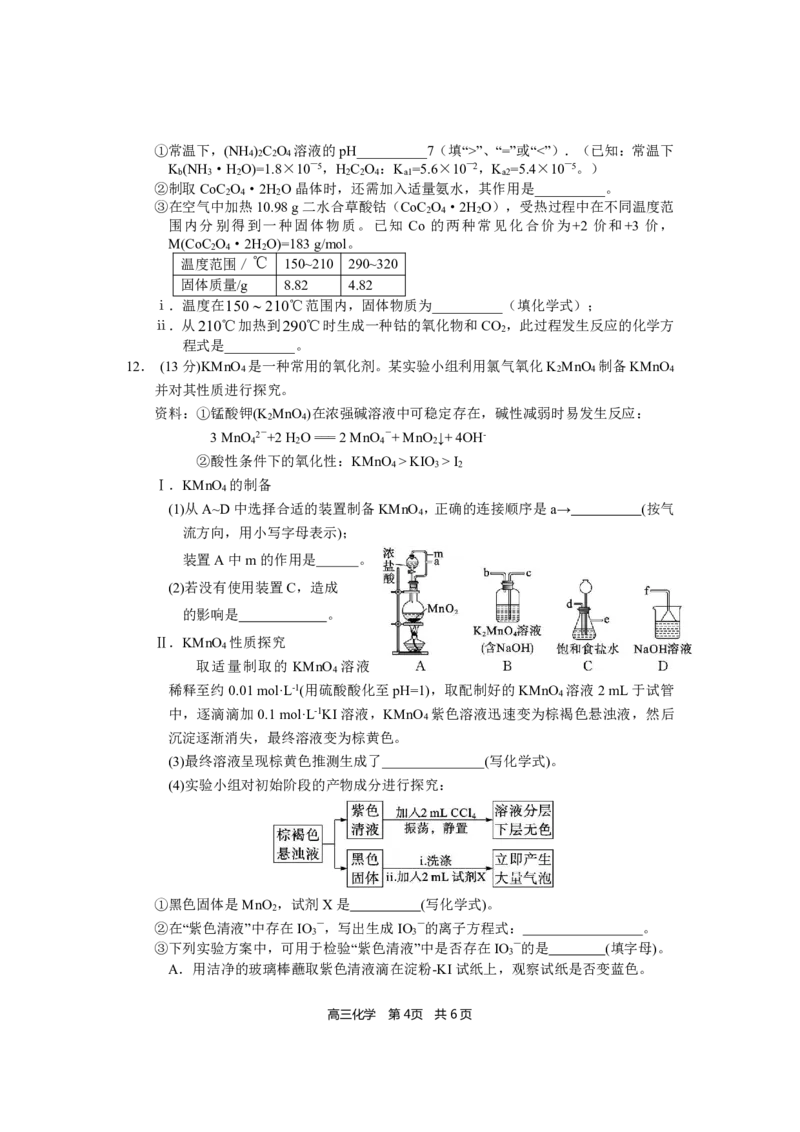
7.据文献报道,我国学者提出O 氧化HBr生成Br 的反应历程如图所示。下列有关该历
2 2
程的说法不正确的是
A.O 氧化HBr生成Br 的总反应为O +4HBr===2Br +2H O
2 2 2 2 2
B.中间体HOOBr和HOBr中Br的化合价相同
C.发生步骤②时,断裂的化学键既有极性键又有非极性键
D.步骤③中,每生成1molBr 转移2mol电子
2
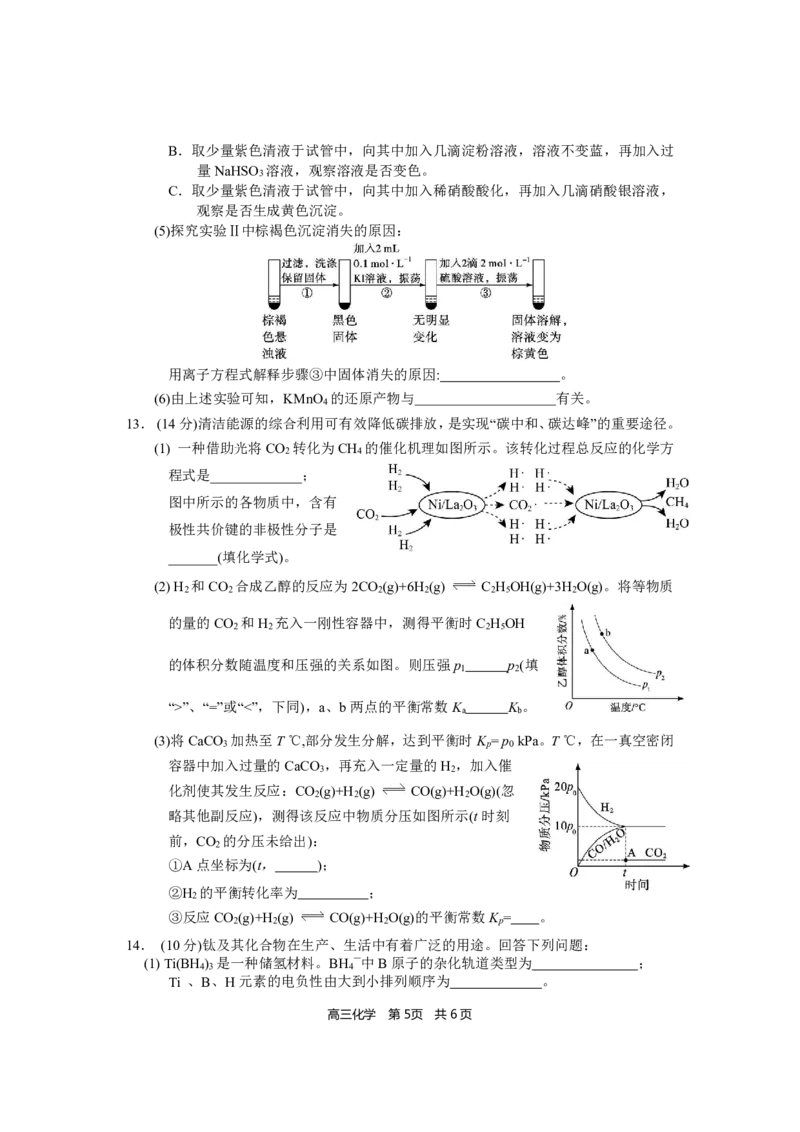
8.碱式碳酸铜是一种用途广泛的化工原料。实验室中以废铜屑为原料,制取碱式碳酸铜
的流程如下。下列说法错误的是
A.酸浸产生的气体可用NaOH溶液吸收
B.加热时,可选用水浴加热
C.可用盐酸和Ba(OH) 溶液检验滤液中是否有CO 2—
2 3
D.温度和pH是影响产品纯度的主要因素
高三化学 第2页 共6页9.羟基自由基(·OH)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将
苯酚氧化为CO 和H O的原电池-电解池组合装置,实现了发电、环保两位一体。N
2 2 A
为阿伏加德罗常数的值,下列说法错误的是
A.a极1molCr O 2—参与反应,理论上NaCl溶液中减少的离子数为12N
2 7 A
B.电池工作时,b极附近pH减小
C.右侧装置中,c、d两极产生气体的体积比(相同条件下)为7∶3
D.d极区苯酚被氧化的化学方程式为C H OH28OH=6CO 17H O
6 5 2 2
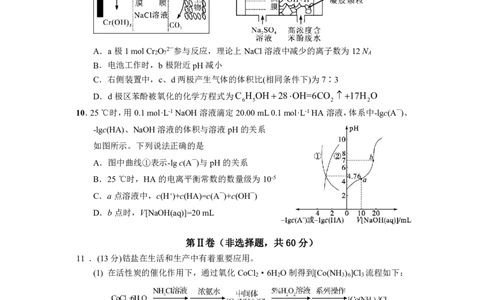
10.25℃时,用0.1mol·L-1NaOH溶液滴定20.00mL0.1mol·L-1HA溶液,体系中-lgc(A—)、
-lgc(HA)、NaOH溶液的体积与溶液pH的关系
如图所示。下列说法正确的是
A.图中曲线①表示-lgc(A—)与pH的关系
B.25℃时,HA的电离平衡常数的数量级为10-5
C.a点溶液中,c(H+)+c(HA)=c(A—)+c(OH—)
D.b点时,V[NaOH(aq)]=20mL
第Ⅱ卷(非选择题,共 60 分)
11 .(13分)钴盐在生活和生产中有着重要应用。
(1) 在活性炭的催化作用下,通过氧化CoCl ·6H O制得到[Co(NH ) ]Cl 流程如下:
2 2 3 6 3
①在“氧化”过程,需水浴控温在50~60℃,温度不能过高,原因是:_______。“系
列操作”是指在高浓度的盐酸中使[Co(NH ) ]Cl 结晶析出,过滤,醇洗,干燥。
3 6 3
使用乙醇洗涤产品的具体操作是:_______。
②结束后废水中的Co2+,人们常用FeS沉淀剂来处理,原理是______(用离子方程
式表示)。
(2) 草酸钴是制备钴氧化物的重要原料,常用(NH ) C O 溶液和CoCl 溶液制取难溶
4 2 2 4 2
于水的CoC O ·2H O晶体。
2 4 2
高三化学 第3页 共6页①常温下,(NH ) C O 溶液的pH__________7(填“>”、“=”或“<”).(已知:常温下
4 2 2 4
K (NH ·H O)=1.8×10—5,H C O :K =5.6×10—2,K =5.4×10—5。)
b 3 2 2 2 4 a1 a2
②制取CoC O ·2H O晶体时,还需加入适量氨水,其作用是__________。
2 4 2
③在空气中加热10.98g二水合草酸钴(CoC O ·2H O),受热过程中在不同温度范
2 4 2
围内分别得到一种固体物质。已知 Co 的两种常见化合价为+2 价和+3 价,
M(CoC O ·2H O)=183g/mol。
2 4 2
温度范围/℃
150~210 290~320
固体质量/g 8.82 4.82
ⅰ.温度在150210℃范围内,固体物质为__________(填化学式);
ⅱ.从210℃加热到290℃时生成一种钴的氧化物和CO ,此过程发生反应的化学方
2
程式是__________。
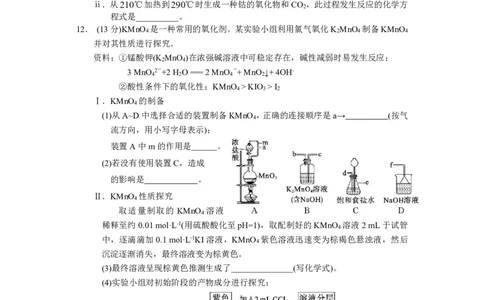
12. (13分)KMnO 是一种常用的氧化剂。某实验小组利用氯气氧化K MnO 制备KMnO
4 2 4 4
并对其性质进行探究。
资料:①锰酸钾(K MnO )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
2 4
3MnO 2-+2H O===2MnO -+MnO ↓+4OH-
4 2 4 2
②酸性条件下的氧化性:KMnO >KIO >I
4 3 2
Ⅰ.KMnO 的制备
4
(1)从A~D中选择合适的装置制备KMnO ,正确的连接顺序是a→ (按气
4
流方向,用小写字母表示);
装置A中m的作用是 。
(2)若没有使用装置C,造成
的影响是 。
Ⅱ.KMnO 性质探究
4
取适量制取的 KMnO 溶液
4
稀释至约0.01mol·L-1(用硫酸酸化至pH=1),取配制好的KMnO 溶液2mL于试管
4
中,逐滴滴加0.1mol·L-1KI溶液,KMnO 紫色溶液迅速变为棕褐色悬浊液,然后
4
沉淀逐渐消失,最终溶液变为棕黄色。
(3)最终溶液呈现棕黄色推测生成了 (写化学式)。
(4)实验小组对初始阶段的产物成分进行探究:
①黑色固体是MnO ,试剂X是 (写化学式)。
2
②在“紫色清液”中存在IO —,写出生成IO —的离子方程式: 。
3 3
③下列实验方案中,可用于检验“紫色清液”中是否存在IO —的是 (填字母)。
3
A.用洁净的玻璃棒蘸取紫色清液滴在淀粉-KI试纸上,观察试纸是否变蓝色。
高三化学 第4页 共6页B.取少量紫色清液于试管中,向其中加入几滴淀粉溶液,溶液不变蓝,再加入过
量NaHSO 溶液,观察溶液是否变色。
3
C.取少量紫色清液于试管中,向其中加入稀硝酸酸化,再加入几滴硝酸银溶液,
观察是否生成黄色沉淀。
(5)探究实验Ⅱ中棕褐色沉淀消失的原因:
用离子方程式解释步骤③中固体消失的原因: 。
(6)由上述实验可知,KMnO 的还原产物与 有关。
4
13.(14分)清洁能源的综合利用可有效降低碳排放,是实现“碳中和、碳达峰”的重要途径。
(1) 一种借助光将CO 转化为CH 的催化机理如图所示。该转化过程总反应的化学方
2 4
程式是_____________;
图中所示的各物质中,含有
极性共价键的非极性分子是
_______(填化学式)。
(2)H 和CO 合成乙醇的反应为2CO (g)+6H (g) C H OH(g)+3H O(g)。将等物质
2 2 2 2 2 5 2
的量的CO 和H 充入一刚性容器中,测得平衡时C H OH
2 2 2 5
的体积分数随温度和压强的关系如图。则压强p p (填
1 2
“>”、“=”或“<”,下同),a、b两点的平衡常数K K 。
a b
(3)将CaCO 加热至T℃,部分发生分解,达到平衡时K =p kPa。T℃,在一真空密闭
3 p 0
容器中加入过量的CaCO ,再充入一定量的H ,加入催
3 2
化剂使其发生反应:CO (g)+H (g) CO(g)+H O(g)(忽
2 2 2
略其他副反应),测得该反应中物质分压如图所示(t时刻
前,CO 的分压未给出):
2
①A点坐标为(t, );
②H 的平衡转化率为 ;
2
③反应CO (g)+H (g) CO(g)+H O(g)的平衡常数K = 。
2 2 2 p
14. (10分)钛及其化合物在生产、生活中有着广泛的用途。回答下列问题:
(1)Ti(BH ) 是一种储氢材料。BH —中B原子的杂化轨道类型为 ;
4 3 4
Ti 、B、H元素的电负性由大到小排列顺序为 。
高三化学 第5页 共6页(2) 已知Ti3+易形成多种配合物,[TiCl(H O) ]Cl ·H O是其中的一种。
2 5 2 2
①1mol该配合物中含有 molσ键。
②Ti3+具有较强还原性的原因是 。
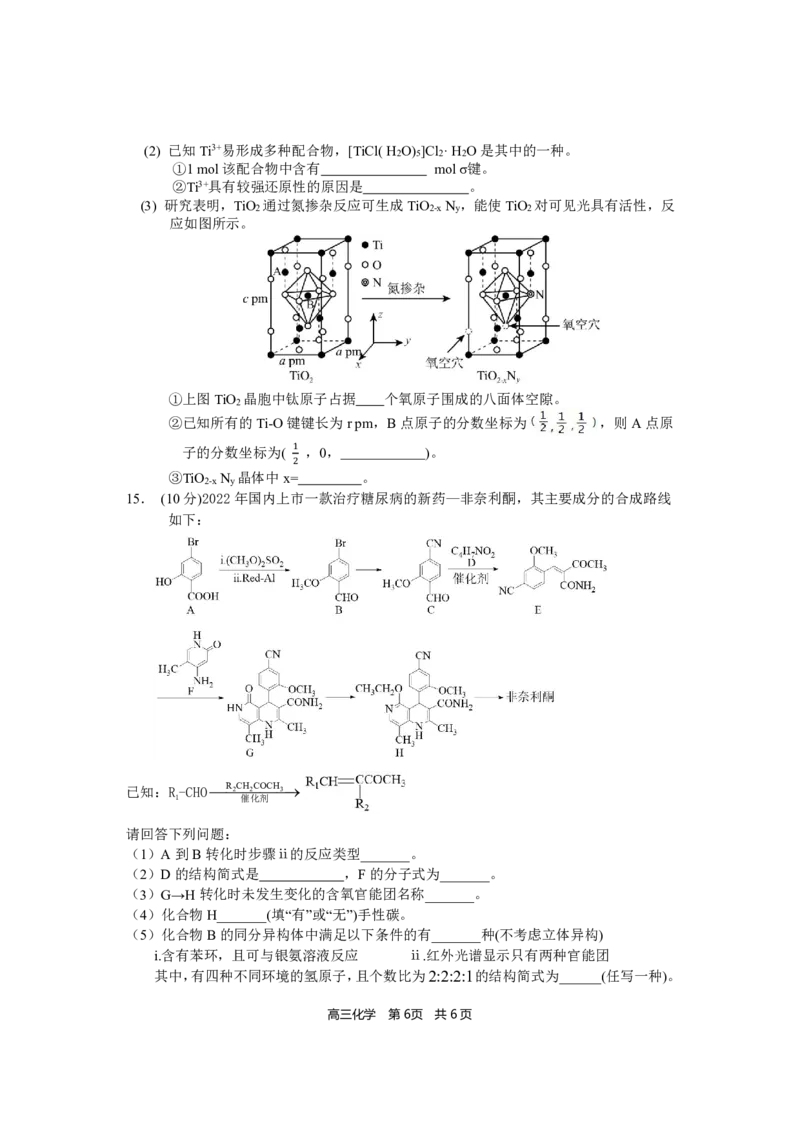
(3) 研究表明,TiO 通过氮掺杂反应可生成TiO N ,能使TiO 对可见光具有活性,反
2 2-x y 2
应如图所示。
①上图TiO 晶胞中钛原子占据 个氧原子围成的八面体空隙。
2
②已知所有的Ti-O键键长为rpm,B点原子的分数坐标为 ,则A点原
子的分数坐标为( ,0, )。
1
③TiO N 晶体中x= 。
2-x y 2
15. (10分)2022年国内上市一款治疗糖尿病的新药—非奈利酮,其主要成分的合成路线
如下:
已知:R-CHOR2 CH2 COCH3
1 催化剂
请回答下列问题:
(1)A到B转化时步骤ⅱ的反应类型_______。
(2)D的结构简式是 ,F的分子式为_______。
(3)G→H转化时未发生变化的含氧官能团名称_______。
(4)化合物H_______(填“有”或“无”)手性碳。
(5)化合物B的同分异构体中满足以下条件的有_______种(不考虑立体异构)
i.含有苯环,且可与银氨溶液反应 ⅱ.红外光谱显示只有两种官能团
其中,有四种不同环境的氢原子,且个数比为2:2:2:1的结构简式为______(任写一种)。
高三化学 第6页 共6页