文档内容
第 01 讲 物质的量 气体摩尔体积
目录
01
考情透视·目标导航 2
02 知识导图·思维引航.........................................................................................................................3
03 考点突破·考法探究.........................................................................................................................4
考点一 物质的量 阿伏加德罗常数.............................................................................................4
知识点1 物质的量 阿伏加德罗常数......................................................................................4
知识点2 摩尔质量......................................................................................................................4
考向1 考查有关“物质的量”概念理解与辨析......................................................................5
考向2 物质的量、质量、微粒数之间的关系..........................................................................6
考点二 气体摩尔体积 阿伏加德罗定律.....................................................................................6
知识点1 影响物质体积大小的因素..........................................................................................6
知识点2 气体摩尔体积..............................................................................................................6
知识点3 阿伏加德罗定律及其推论..........................................................................................8
考向1 气体摩尔体积..................................................................................................................8
考向2 阿伏加德罗定律及应用..................................................................................................9
考向3 气体摩尔质量计算的常用方法....................................................................................10
04真题练习·命题洞见........................................................................................................................11考点要求 考题统计 考情分析
2024浙江卷第1次4题,2分
2023全国甲卷10题,6分
本讲为高考命题热点,题型以选择题为主,
2023辽宁卷5题,3分
试题以物质的组成和结构、弱电解质电离、可逆
2023重庆卷4题,3分 反应、氧化还原反应为载体,综合考查基本概
阿伏加德罗常数
2023福建卷4题,4分 念、基本理论、化学计算。可能会从考查气体摩
2023河北卷4题,3分 尔体积的使用条件、物质结构、弱电解质电离、
2022全国甲卷11题,6分 可逆反应、氧化还原反应中电子转移等相关内容
命题,解题时注意题设中的陷阱,构建好解题模
2022浙江卷第1次12题,3分
型。
2021山东卷6题,3分
阿伏加德罗定律
2020北京卷5题,3分
复习目标:
1.了解物质的量(n)及其单位摩尔(mol)、摩尔质量(M)、气体摩尔体积(V )、阿伏加德罗常数(N )的含
m A
义。
2.能根据粒子(原子、分子、离子等)数目、物质的量、气体体积(标准状况下)之间的相互关系进行有关
计算。考点一 物质的量 阿伏加德罗常数
知识点1 物质的量 阿伏加德罗常数
1.物质的量(n)
表示含有一定数目粒子的集合体的物理量,单位为___________。
2.物质的量的规范表示方法:
3.阿伏加德罗常数(N )
A
1 mol任何粒子的粒子数叫做阿伏加德罗常数,其数值约为___________,单位为___________。
说明:(1)N 的基准是12g12C中的原子个数
A
(2)12C不仅是摩尔的基准对象,而且还是相对原子质量的基准
(3)N 是一个实验值,现阶段常取6.02×1023作计算
A
(4)要注意N 与6.02×1023的区别
A
4.物质的量(n)、阿伏加德罗常数(N )与粒子数(N)之间关系公式:N =___________。
A A
【易错提醒】(1)物质的量只能衡量微观粒子,必须指明具体粒子的种类或化学式,故摩尔后面应为确
切的微粒名称;如1 mol氢(不确切)和1 mol大米(宏观物质)皆为错误说法。(2)物质的量是物理量,摩尔是物质的量的单位,不是物理量。
(3)6.02×1023是个纯数值,没有任何物理意义,而阿伏加德罗常数(N )是指1 mol任何微粒所含的粒子
A
数,它与0.012 kg12C所含的碳原子数相同,数值约为6.02×1023。
知识点2 摩尔质量
1.定义:______________________的物质所具有的质量。
2.常用单位:___________。
3.物质的量(n)、质量(m)和摩尔质量(M)之间关系公式:M=___________。
4.数值:以__________为单位时,任何粒子的摩尔质量在数值上都__________该粒子的相对分子(原子)质
量。
说明:(1)使用范围:A.任何一种微观粒子 B.无论是否纯净 C.无论物质的状态
(2)注意与式量的比较
(3)注意与1mol物质的质量的比较
(4)将物质的质量换算成物质的量,换算成粒子数,将气体物质质量换算成体积(标准状况),都要通
过摩尔质量这一桥梁进行。
【易错提醒】(1)摩尔质量、相对原子(或分子)质量的含义不同,不是同一个物理量。二者单位也不同,
摩尔质量的单位是g·mol-1或kg·mol-1,相对原子(或分子)质量的单位为1,当摩尔质量以g·mol-1为单位
时,二者在数值上相等。
(2)对具体的物质,其摩尔质量是确定的,不随物质的量的多少而变化,也不随物质的聚集状态而变
化。
考向1 考查有关“物质的量”概念理解与辨析
例1 下列关于物质的量的正确说法是
A.可以理解为物质的质量 B.就是物质的粒子数目
C.表示一定数目微粒集合体的物理量 D.符号 ,单位n
【名师点睛】本题考查的是物质中含有的各种粒子或微观结构的问题,一般来说先计算物质基本微粒中含
有多少个需要计算的粒子或微观结构,再乘以该物质的物质的量,就可以计算出相应结果,稀有气体分子
都是单原子分子。
【变式训练1】下列对于“摩尔”的理解正确的是
A.摩尔是国际科学界建议采用的一种物理量
B.摩尔可以把物质的宏观数量与微观粒子的数量联系起来
C.摩尔是物质的量的单位,简称摩,符号为mol
D.国际上规定0.012kg碳中所含有的碳原子数目约为6.02×1023
【变式训练2】下列叙述错误的是
①摩尔是国际单位制中七个基本物理量之一物质的量的单位;
② 任何物质都含有约 个原子;③ 就是阿伏加德罗常数;
④氢原子的摩尔质量是 ;
⑤ 的摩尔质量不同于 分子的质量;
⑥ 中含有 个碳原子和 个氧原子;
⑦当 水吸收 (标准状况)氨气时所得氨水的浓度是 .
A.①②③⑦ B.②③④⑦ C.②③④⑥ D.全部
考向2 物质的量、质量、微粒数之间的关系
例2 下列关于物质的量的叙述中,正确的是
A.1mol任何物质都含有6.02×1023个分子
B.0.012kg12C中含有约6.02×1023个碳分子
C.1molNH 中含有1 mol 氮和3 mol氢
3
D.1mol Na+中含有6.02×1024个电子
【思维建模】由已知物理量求物质所含的粒子数目的思维模型:记住特殊物质中 1 mol物质所含微粒(分
子、原子、电子、质子、中子等)的数目,如Ne、DO、18O、—OH、OH-等。
2 2
【变式训练1】用N 表示阿伏加德罗常数,下列叙述中不正确的是
A
A.23g钠变为氧化钠时失去电子数约为6.02×1023
B.1L 稀硫酸中硫酸根离子总数为
C.常温常压下,8g由 和 组成的混合气体中含有的氧原子数为
D.1molCO 的质量是44g/mol
2
【变式训练2】(1)某氯原子的质量是a g,12C原子的质量是b g,用N 表示阿伏加德罗常数的值。
A
①该氯原子的相对原子质量为________;
②该氯原子的摩尔质量是________;
③m g该氯原子的物质的量为________;
④n g该氯原子所含的电子数为________。
(2)12.4 g Na R含Na+ 0.4 mol,则NaR的摩尔质量为________,R的相对原子质量为________。含R
2 2
的质量为1.6 g的NaR,其物质的量为________。
2
考点二 气体摩尔体积 阿伏加德罗定律
知识点1 影响物质体积大小的因素
1.影响物质体积大小的因素
①粒子的___________(物质的本性);②粒子间的___________(由温度与压强共同决定);
③粒子的___________(物质的量的大小)。
2.固体、液体的体积由①粒子的大小和③粒子的数目的多少决定,忽略②粒子间距不计。
3.气体的体积由②粒子间距和③粒子的数目的大小决定,忽略①粒子的大小不计。
知识点2 气体摩尔体积
1.含义:______________________的气体所占的体积,符号为V ,标准状况下,V 约为___________。
m m
2.常用单位:L/mol(或L·mol-1)。
3.数值:在___________下(指温度为0℃,压强为101 kPa)约为___________。
4.基本关系式:n=___________==
使用范围:只要物质的组成不变,无论是何状态都可以使用。
5.影响因素:气体摩尔体积的数值不是固定不变的,它决定于气体所处的___________和___________。
6.适用对象:单一气体或互不反应的混合___________。
7.标准状况下的气体摩尔体积
(1)标准状况:______________________。
(2)理想气体:A.不计大小但计质量;B.不计分子间的相互作用。
(3)标准状况下的气体摩尔体积:约___________。
8.主要应用
标准状况下1mol气体为22.4 L,即可导出其质量便是该气体的摩尔质量。据此可求出未知化学式的气体摩
尔质量和相对分子质量,也可求出1L气体的质量即气体密度。反之也可由气体密度求摩尔质量。同温同
压下两气体的密度比叫气体的相对密度,可由气体的相对密度求气体的摩尔质量,如某气体对氢气(H )
2
的相对密度为15,则其相对分子质量为30。常见的有:
(1)由标准状况下气体密度求相对分子质量;
(2)由相对密度求气体的相对分子质量;
(3)求混合气体的平均相对分子质量:即混合气体1mol时的质量数值。
已知各组成气体的体积分数及质量分数;
(4)由同温同压下气体反应时的体积比求分子数比,进而推分子式;
(5)直接将气体摩尔体积代入有关化学方程式进行计算;
(6)气体反应物的体积比即分子数比可便于找出过量气体。
【特别提醒】气体摩尔体积(22.4 L·mol-1)应用的“五大误区”
(1)使用“条件”是标准状况,即0 ℃、101 kPa,而不是常温、常压。
(2)使用对象必须是气体物质,可以是单一气体,也可以是混合气体。标准状况下不是气体而又常在题
中出现的物质有:水、苯、SO 、HF、CCl 、己烷、CS、CHCl 、Br 、乙醇等。
3 4 2 3 2
(3)标准状况下的气体摩尔体积约为22.4 L·mol-1,其他条件下Vm一般不是22.4 L·mol-1。
(4)22.4 L气体,在标准状况下的物质的量是1 mol,在非标准状况下,可能是1 mol,也可能不是1
mol。
(5)物质的质量、物质的量一定时,所含微粒数与物质处于何种条件无关。如常温常压下 32 g O 所含的
2原子数目是2N 。注意不要形成定势思维,看到“常温常压”就排除选项。
A
知识点3 阿伏加德罗定律及其推论
1.阿伏加德罗定律:在相同的温度和压强下,相同体积的任何气体,含有___________数目的分子(或气体
的物质的量___________)。
【名师提醒】可总结为:“三同”定“一同”,即同温、同压下,同体积的任何气体具有相同的分子数。
2.阿伏加德罗定律的推论(以下用到的符号:ρ为密度,p为压强,n为物质的量,M为摩尔质量,m为质
量,V为体积,T为热力学温度)
条件 推论公式 语言叙述
T、p相同 = 同温、同压下,气体的体积与其物质的量成正比
T、V相同 = 温度、体积相同的气体,其压强与其物质的量成正比
T、p相同 = 同温、同压下,气体的密度与其摩尔质量(或相对分子质量)成正比
T、p、m相
= 同温同压下,相同质量的任何气体的体积与它们的摩尔质量成反比
同
T、V、m相 同温同体积时,相同质量的任何气体的压强与它们的摩尔质量成反
=
同 比
T、p、V相 同温同压下,同体积的任何气体的质量比等于它们的摩尔质量之
==
同 比,也等于它们的密度之比
提醒:对于同一种气体,当压强相同时,密度与温度成反比例关系。
【方法技巧】
1、记忆方法:三正比、二反比、一连比。
2、应用阿伏加德罗定律推论时可通过pV=nRT及n=、ρ=导出。
考向1 气体摩尔体积
例1 下列叙述正确的是
A.标准状况下,1mol乙醇的体积约为22.4L
B.0℃、101kPa下,任何气体的摩尔体积都约为
C.气体摩尔体积仅指标准状况下1mol气体的体积
D.若1mol 气体体积约为22.4L,则它所处的条件一定是“标准状况”
【变式训练1】下列说法不正确的是
A.标准状况下,22.4L·mol-1就是气体摩尔体积
B.非标准状况下,1mol任何气体的体积不可能为22.4L
C.标准状况下22.4L任何气体都含有约6.02X1023个分子
D.1molH 和O 的混合气体在标准状况下的体积约为22.4L
2 2
【变式训练2】N 表示阿伏加德罗常数的值,下列说法正确的是
AA.标准状况下, 含有的分子数是
B.常温常压下, 气体含有的分子数是
C. 溶液含有的钠离子数为
D.标准状况下, 和 混合气体所含原子总数为
考向2 阿伏加德罗定律及应用
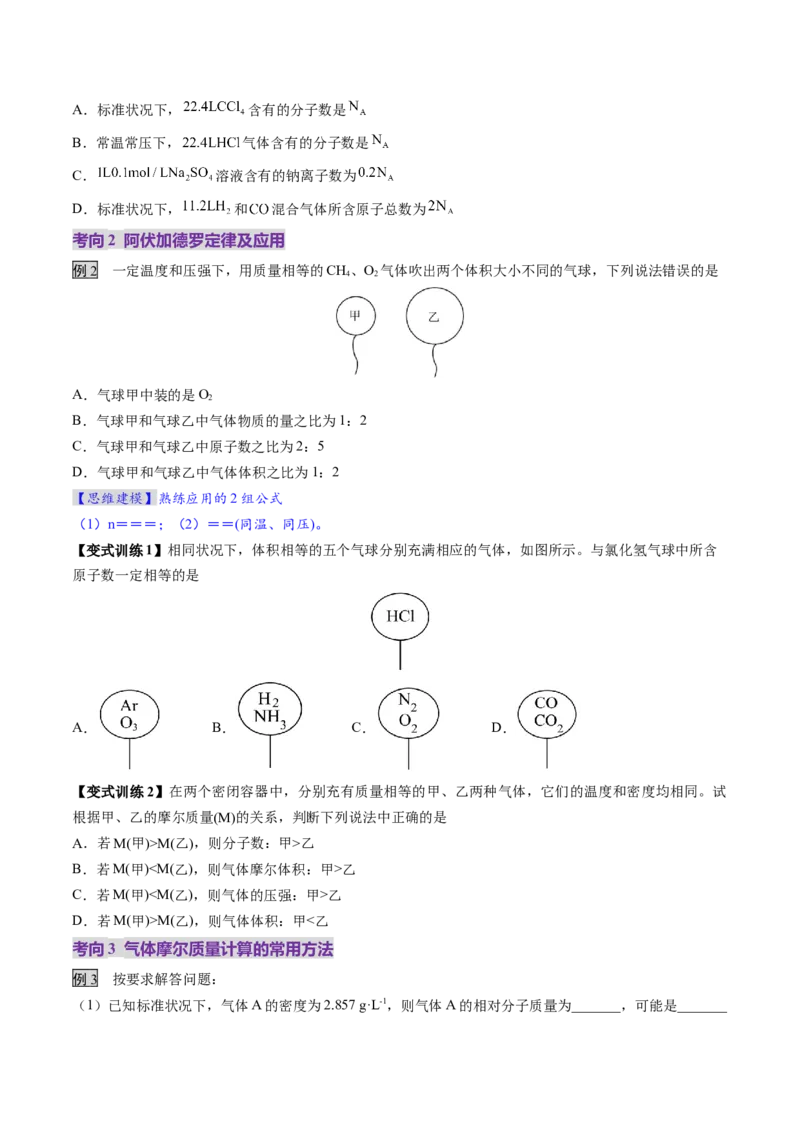
例2 一定温度和压强下,用质量相等的CH、O 气体吹出两个体积大小不同的气球,下列说法错误的是
4 2
A.气球甲中装的是O
2
B.气球甲和气球乙中气体物质的量之比为1:2
C.气球甲和气球乙中原子数之比为2:5
D.气球甲和气球乙中气体体积之比为1:2
【思维建模】熟练应用的2组公式
(1)n===;(2)==(同温、同压)。
【变式训练1】相同状况下,体积相等的五个气球分别充满相应的气体,如图所示。与氯化氢气球中所含
原子数一定相等的是
A. B. C. D.
【变式训练2】在两个密闭容器中,分别充有质量相等的甲、乙两种气体,它们的温度和密度均相同。试
根据甲、乙的摩尔质量(M)的关系,判断下列说法中正确的是
A.若M(甲)>M(乙),则分子数:甲>乙
B.若M(甲)乙
C.若M(甲)乙
D.若M(甲)>M(乙),则气体体积:甲<乙
考向3 气体摩尔质量计算的常用方法
例3 按要求解答问题:
(1)已知标准状况下,气体A的密度为2.857 g·L-1,则气体A的相对分子质量为_______,可能是_______气体。
(2)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为_______。
(3)CO和CO 的混合气体18 g,完全燃烧后测得CO 体积为11.2 L(标准状况),则
2 2
①混合气体在标准状况下的密度是_______g·L-1。
②混合气体的平均摩尔质量是_______ g·mol-1。
【思维建模】求气体摩尔质量M及相对分子质量的常用方法:
(1)根据物质的质量(m)和物质的量(n):M=m/n。
(2)根据一定质量(m)的物质中微粒数目(N)和阿伏加德罗常数(NA):M=NA·m/N。
(3)根据标准状况下气体的密度ρ:M=ρ×22.4 L·mol-1。
(4)根据气体的相对密度(D=ρ/ρ ):M/M =D。
1 2 1 2
(5)对于混合气体,求其平均摩尔质量,上述计算式仍然成立;还可以用下式计算:M=M1×a%+
M2×b%+M3×c%……,a%、b%、c%……指混合物中各成分的物质的量分数(或体积分数)。
【变式训练1】打火机里装有液态的丙烷和丁烷。下列说法错误的是
A.打开打火机开关,分子间距变大
B.摩擦打火石,达到气体着火点
C. 丙烷完全燃烧需要空气约为
D.若n(丙烷):n(丁烷) ,该混合物的摩尔质量为
【变式训练2】某密闭刚性容器由可动活塞隔成甲、乙两室,室温下向甲中充入由H 和O 组成的混合气体
2 2
19g,向乙中充入1mol空气,此时活塞的位置如图所示。下列有关说法正确的是
A.甲室混合气体的分子总数为3N
A
B.甲室H、O 的物质的量之比为1:3
2 2
C.甲室混合气体的密度是同温同压下H 密度的9.5倍
2
D.若将甲室气体点燃引爆并恢复至室温,忽略生成水的体积,活塞最终停留在刻度2处
1.(2023·河北卷) 为阿伏加德罗常数的值,下列说法正确的是
A. 的 溶液中含 个
B.反应 生成 ,转移 个电子
C. 号元素的原子一定含有 个质子、 个中子
D. 组成为 的烃一定含有 个双键2.(2023·福建卷)我国新一代载人飞船使用的绿色推进剂硝酸羟胺 在催化剂作用下可
完全分解为 和 。 为阿伏加德罗常数的值,下列说法正确的是
A. 含有的质子数为
B. 固态硝酸羟胺含有的离子数为
C. 硝酸羟胺含有的 键数为
D.硝酸羟胺分解产生 (已折算为标况)的同时,生成 分子数为
3.(2023·重庆卷)已知反应: , 为阿伏加德罗常数的值,若消耗
(标准状况) ,下列叙述错误的是
A.转移的电子数为 B.生成的 质量为
C.生成的氧化产物分子数为 D.生成的 含有孤电子对数为
4.(2023·海南卷) 代表阿伏加德罗常数的值。下列说法正确的是
A.2.4g镁条在空气中充分燃烧,转移的电子数目为
B.5.6g铁粉与 的HCl的溶液充分反应,产生的气体分子数目为
C.标准状况下, 与 充分反应,生成的 分子数目为
D. 完全溶于 所得溶液, 微粒数目为
5.(2023·广东卷)设 为阿伏加德罗常数的值。侯氏制碱法涉及 和 等物质。下
列叙述正确的是
A. 含有的共价键数目为
B. 完全分解,得到的 分子数目为
C.体积为 的 溶液中, 数目为
D. 和 的混合物中含 ,则混合物中质子数为