文档内容
第 02 讲 物质的量浓度
目录
01 模拟基础练
【题型一】物质的量浓度概念的理解
【题型二】溶液浓度的计算
【题型三】一定物质的量浓度溶液的配制
02 重难创新练
03 真题实战练
题型一 物质的量浓度概念的理解
1.下列操作所得溶液的溶质的物质的量浓度为1 的是( )
A.将9.5g MgCl 溶于蒸馏水,配成100mL溶液
2
B.将4gNaOH固体溶于100mL蒸馏水
C.将50mL2 NaCl溶液与50mL蒸馏水混合
D.将3.36L氯化氢气体溶于水,配成150mL溶液
2.下列说法正确的是( )
A.将44.8 L的HCl气体溶于水配成1 L溶液,溶液的浓度为2 mol/L
B.将40 g NaOH固体溶解在1 L水中,所得溶液的浓度恰好是1 mol/L
C.2 L0.2 mol/L的NaCl溶液与5 L0.4 mol/L的NaCl溶液的Cl-浓度之比为1:2
D.从100 mL硫酸溶液中取出10 mL,则这10 mL硫酸溶液的物质的量浓度是原溶液的
3.某校化学兴趣小组在实验中发现一瓶溶液,标签上标有“CaCl 0.1 mol·L-1”的字样,下面是该小组
2
成员对溶液的叙述,正确的是( )。
A.配制1 L该溶液,可将0.1 mol CaCl 溶于1 L水中
2
B.Ca2+和Cl-的物质的量浓度都是0.1 mol·L-1
C.从试剂瓶中取出该溶液的一半,则所取溶液的物质的量浓度为0.05 mol·L-1
D.将该瓶溶液稀释一倍,所得溶液中c(Cl-)为0.1 mol·L-14.下列溶液Cl-物质的量浓度与200mL1mol·L-1AlCl 溶液中Cl-物质的量浓度相等的是( )
3
A.150mL3mol·L-1NaClO溶液 B.75mL3mol·L-1CaCl 溶液
2
C.150mL3mol·L-1KCl溶液 D.150mL2mol·L-1MgCl 溶液
2
题型二 溶液浓度的计算
5. 一定量的铜和浓硫酸在加热条件下充分反应,向反应后的溶液中逐滴加入含 a mol NaOH的溶液,
恰好使反应后的溶液呈中性,则下列叙述错误的是 ( )
A.溶液中c(Na+)=2c(SO) B. mol>沉淀的物质的量>0
C.沉淀的物质的量= mol D.原浓硫酸中HSO 的物质的量> mol
2 4
6.体积为VmL,密度为的ρg/cm3含有相对分子质量为M的某种物质的溶液,其中溶质为mg,其物
质的量浓度为cmol/L,溶质的质量分数为w%,则下列表示正确的是( )
A. B. C.c= D.
7.现有硫酸钠溶液V mL,其密度是ρ g·mL-1,其中钠离子的质量分数是a%,则有关该溶液的说法
不正确的是( )
A.溶质的质量分数是%
B.溶液的物质的量浓度是 mol·L-1
C.溶质和溶剂的物质的量之比是9a∶(1 000-142a)
D.硫酸根离子的质量分数是%
8.现有硫酸钠溶液V mL,它的密度是ρ g· mL-1,其中钠离子的质量分数是a%,则下列有关该溶液
的说法错误的是( )。
71a
A.溶质的质量分数是 %
23
5ρa
B.溶液的物质的量浓度是 mol·L-1
23
C.溶质和溶剂的物质的量之比是9a∶(2300-71a)
48a
D.硫酸根离子的质量分数是
23
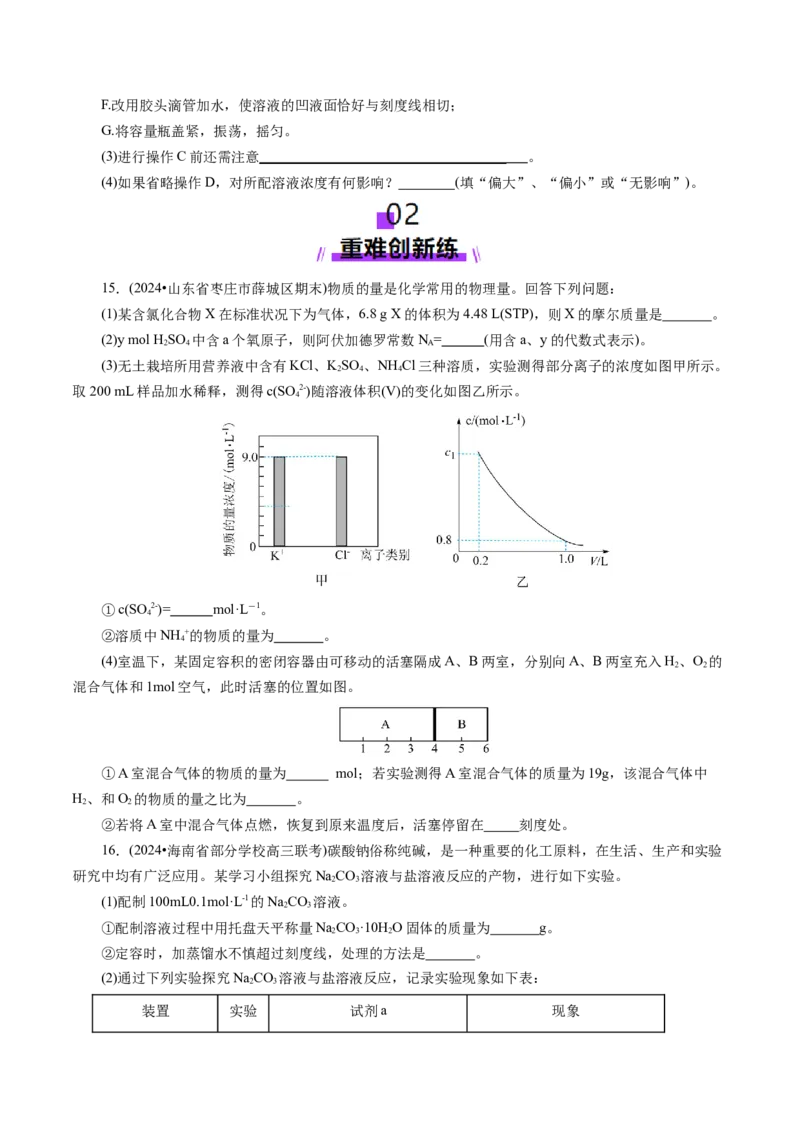
9.已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,
回答下列问题:
溶质的物质的量浓度/mol·L-1 溶液的密度/g·cm-3
硫酸 c ρ
1 1
氨水 c ρ
2 2(1)表中硫酸的质量分数为________(不写单位,用含c、ρ 的代数式表示)。
1 1
(2)物质的量浓度为c mol·L-1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的
1
物质的量浓度为________ mol·L-1。
(3)将物质的量浓度分别为c mol·L-1和c mol·L-1的氨水等质量混合,所得溶液的密度________(填
2 2
“大于”、“小于”或“等于”,下同)ρ g·cm-3,所得溶液的物质的量浓度________c mol·L-1(设混合后
2 2
溶液的体积变化忽略不计)。
题型三 一定物质的量浓度溶液的配制
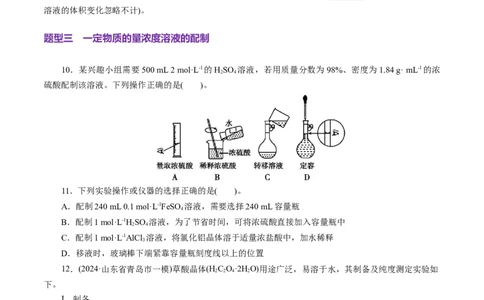
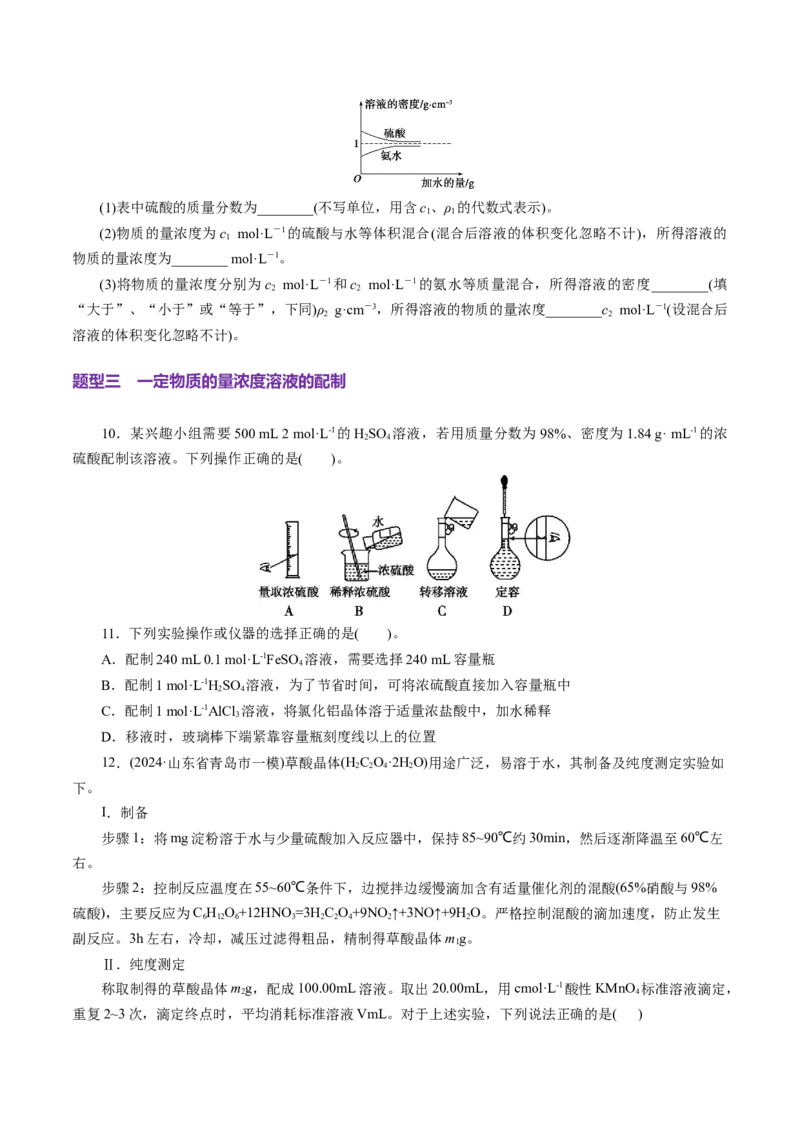
10.某兴趣小组需要500 mL 2 mol·L-1的HSO 溶液,若用质量分数为98%、密度为1.84 g· mL-1的浓
2 4
硫酸配制该溶液。下列操作正确的是( )。
11.下列实验操作或仪器的选择正确的是( )。
A.配制240 mL 0.1 mol·L-1FeSO 溶液,需要选择240 mL容量瓶
4
B.配制1 mol·L-1HSO 溶液,为了节省时间,可将浓硫酸直接加入容量瓶中
2 4
C.配制1 mol·L-1AlCl 溶液,将氯化铝晶体溶于适量浓盐酸中,加水稀释
3
D.移液时,玻璃棒下端紧靠容量瓶刻度线以上的位置
12.(2024·山东省青岛市一模)草酸晶体(H C O·2HO)用途广泛,易溶于水,其制备及纯度测定实验如
2 2 4 2
下。
I.制备
步骤1:将mg淀粉溶于水与少量硫酸加入反应器中,保持85~90℃约30min,然后逐渐降温至60℃左
右。
步骤2:控制反应温度在55~60℃条件下,边搅拌边缓慢滴加含有适量催化剂的混酸(65%硝酸与98%
硫酸),主要反应为C H O+12HNO =3H C O+9NO↑+3NO↑+9HO。严格控制混酸的滴加速度,防止发生
6 12 6 3 2 2 4 2 2
副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体mg。
1
Ⅱ.纯度测定
称取制得的草酸晶体mg,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO 标准溶液滴定,
2 4
重复2~3次,滴定终点时,平均消耗标准溶液VmL。对于上述实验,下列说法正确的是( )A.65%浓硝酸( )的物质的量浓度约为13.6mol·L-1
B.草酸晶体的产率为
C.配制的草酸溶液物质的量浓度为0.025cVmol·L-1
D.草酸晶体的纯度为
13.(2024•山东省烟台市招远二中月考)某“84”消毒液部分标签如下图所示,回答下列问题:
净含量:500mL密度:1.19 g· cm-3
主要成分:25%NaClO(NaClO的摩尔质量74.5
g·molˉ1)
注意事项:密封保存
(1)计算该“84”消毒液的物质的量浓度为 mol·L-1 (保留小数点后一位)。
(2)某实验需用480mL2.0 NaClO的消毒液,现用NaClO固体配制。需要用托盘天平称量NaClO
的固体质量为 g;
(3)在配制过程中,除需要烧杯、玻璃棒外还必需的玻璃仪器有 。
(4)下列操作可能使配制溶液浓度偏低的是(填字母) 。
A.移液时,未洗涤烧杯内壁和玻璃棒
B.溶解后未经冷却就移液
C.移液时,有少量液体溅出
D.定容时,仰视刻度线
E.容量瓶用蒸馏水洗净后,没烘干就直接使用
(5)取该“84”消毒液100mL,再加入28.4克NaSO (Na SO 的摩尔质量142 g·molˉ1)固体,将其溶解并
2 4 2 4
配成500mL溶液,此时溶液中Na+的物质的量浓度为 mol·L-1。
14.(2024•安徽省亳州市涡阳县期末)某学生欲配制1000mL6.0mol·L-1的HSO ,实验室有三种不同浓
2 4
度的硫酸:
①480mL0.5mol·L-1的硫酸;②150mL25%的硫酸(ρ=1.18g·mL-1);③足量的18mol·L-1的硫酸。有三种
规格的容量瓶:250mL、500mL、1000mL。老师要求把①②两种硫酸全部用完,不足的部分由③来补充。
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为 ______ _mol·L-1(保留1位小数)。
(2)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整。
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18mol·L-1的浓硫酸 ______ _mL,沿玻璃棒倒入上述混合液中。并用玻璃
棒搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D.________________________;
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2cm处;F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀。
(3)进行操作C前还需注意___________________________________ 。
(4)如果省略操作D,对所配溶液浓度有何影响? _____ (填“偏大”、“偏小”或“无影响”)。
15.(2024•山东省枣庄市薛城区期末)物质的量是化学常用的物理量。回答下列问题:
(1)某含氯化合物X在标准状况下为气体,6.8 g X的体积为4.48 L(STP),则X的摩尔质量是 。
(2)y mol H SO 中含a个氧原子,则阿伏加德罗常数N = (用含a、y的代数式表示)。
2 4 A
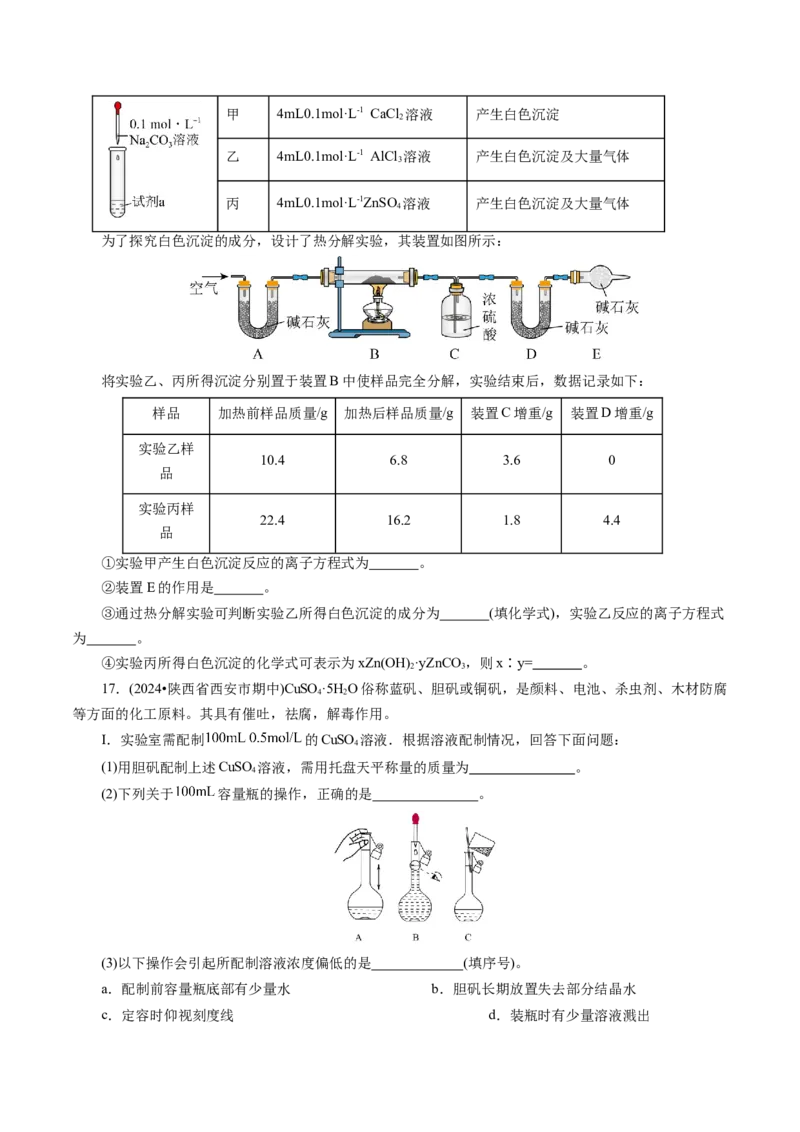
(3)无土栽培所用营养液中含有KCl、KSO 、NH Cl三种溶质,实验测得部分离子的浓度如图甲所示。
2 4 4
取200 mL样品加水稀释,测得c(SO 2-)随溶液体积(V)的变化如图乙所示。
4
①c(SO 2-)= mol·L-1。
4
②溶质中NH +的物质的量为 。
4
(4)室温下,某固定容积的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H、O 的
2 2
混合气体和1mol空气,此时活塞的位置如图。
①A室混合气体的物质的量为 mol;若实验测得A室混合气体的质量为19g,该混合气体中
H、和O 的物质的量之比为 。
2 2
②若将A室中混合气体点燃,恢复到原来温度后,活塞停留在 刻度处。
16.(2024•海南省部分学校高三联考)碳酸钠俗称纯碱,是一种重要的化工原料,在生活、生产和实验
研究中均有广泛应用。某学习小组探究NaCO 溶液与盐溶液反应的产物,进行如下实验。
2 3
(1)配制100mL0.1mol·L-1的NaCO 溶液。
2 3
①配制溶液过程中用托盘天平称量NaCO·10H O固体的质量为 g。
2 3 2
②定容时,加蒸馏水不慎超过刻度线,处理的方法是 。
(2)通过下列实验探究NaCO 溶液与盐溶液反应,记录实验现象如下表:
2 3
装置 实验 试剂a 现象甲 4mL0.1mol·L-1 CaCl 溶液 产生白色沉淀
2
乙 4mL0.1mol·L-1 AlCl 溶液 产生白色沉淀及大量气体
3
丙 4mL0.1mol·L-1ZnSO 溶液 产生白色沉淀及大量气体
4
为了探究白色沉淀的成分,设计了热分解实验,其装置如图所示:
将实验乙、丙所得沉淀分别置于装置B中使样品完全分解,实验结束后,数据记录如下:
样品 加热前样品质量/g 加热后样品质量/g 装置C增重/g 装置D增重/g
实验乙样
10.4 6.8 3.6 0
品
实验丙样
22.4 16.2 1.8 4.4
品
①实验甲产生白色沉淀反应的离子方程式为 。
②装置E的作用是 。
③通过热分解实验可判断实验乙所得白色沉淀的成分为 (填化学式),实验乙反应的离子方程式
为 。
④实验丙所得白色沉淀的化学式可表示为xZn(OH) ·yZnCO,则x∶y= 。
2 3
17.(2024•陕西省西安市期中)CuSO ·5H O俗称蓝矾、胆矾或铜矾,是颜料、电池、杀虫剂、木材防腐
4 2
等方面的化工原料。其具有催吐,祛腐,解毒作用。
I.实验室需配制 的CuSO 溶液.根据溶液配制情况,回答下面问题:
4
(1)用胆矾配制上述CuSO 溶液,需用托盘天平称量的质量为 。
4
(2)下列关于 容量瓶的操作,正确的是 。
(3)以下操作会引起所配制溶液浓度偏低的是 (填序号)。
a.配制前容量瓶底部有少量水 b.胆矾长期放置失去部分结晶水
c.定容时仰视刻度线 d.装瓶时有少量溶液溅出(4)现利用上述CuSO 溶液配制 的CuSO 溶液,需用量筒量取 的
4 4
CuSO 溶液。完成该实验,除用量筒,烧杯,玻璃棒之外,还需使用的玻璃仪器有 。
4
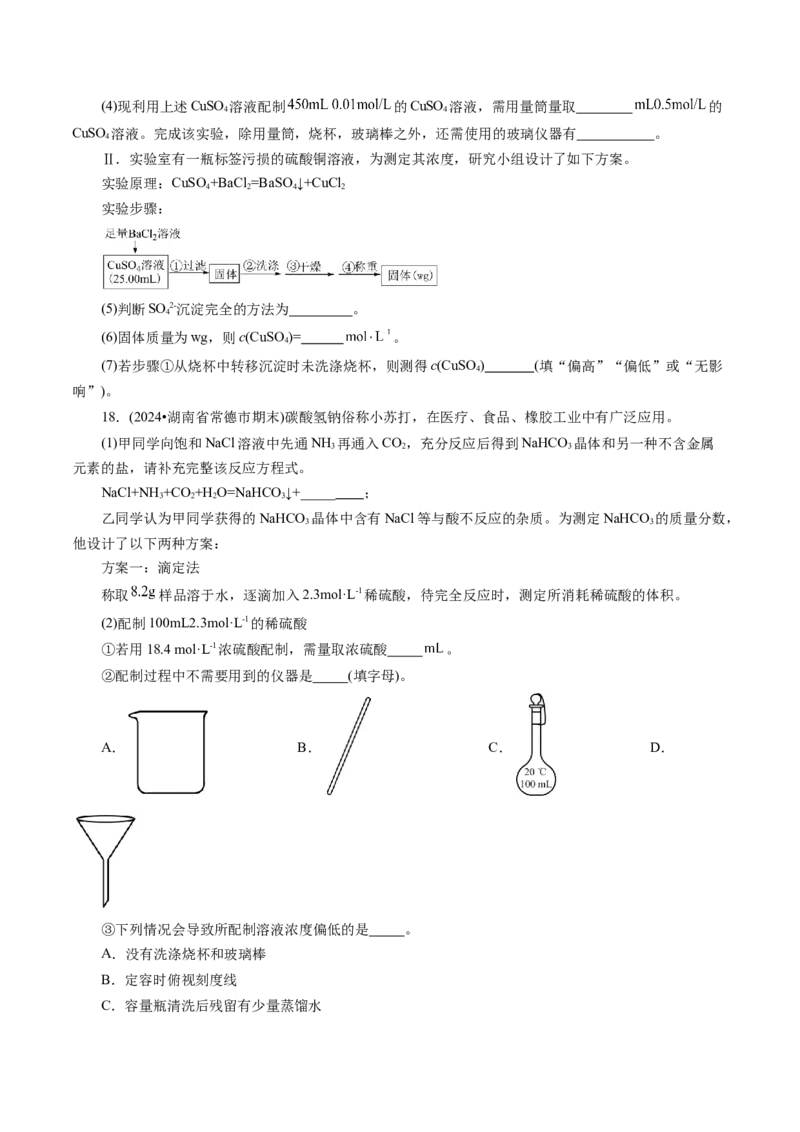
Ⅱ.实验室有一瓶标签污损的硫酸铜溶液,为测定其浓度,研究小组设计了如下方案。
实验原理:CuSO +BaCl =BaSO ↓+CuCl
4 2 4 2
实验步骤:
(5)判断SO 2-沉淀完全的方法为 。
4
(6)固体质量为wg,则c(CuSO )= 。
4
(7)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO ) (填“偏高”“偏低”或“无影
4
响”)。
18.(2024•湖南省常德市期末)碳酸氢钠俗称小苏打,在医疗、食品、橡胶工业中有广泛应用。
(1)甲同学向饱和NaCl溶液中先通NH 再通入CO,充分反应后得到NaHCO 晶体和另一种不含金属
3 2 3
元素的盐,请补充完整该反应方程式。
NaCl+NH +CO +H O=NaHCO ↓+_____ ;
3 2 2 3
乙同学认为甲同学获得的NaHCO 晶体中含有NaCl等与酸不反应的杂质。为测定NaHCO 的质量分数,
3 3
他设计了以下两种方案:
方案一:滴定法
称取 样品溶于水,逐滴加入2.3mol·L-1稀硫酸,待完全反应时,测定所消耗稀硫酸的体积。
(2)配制100mL2.3mol·L-1的稀硫酸
①若用18.4 mol·L-1浓硫酸配制,需量取浓硫酸 。
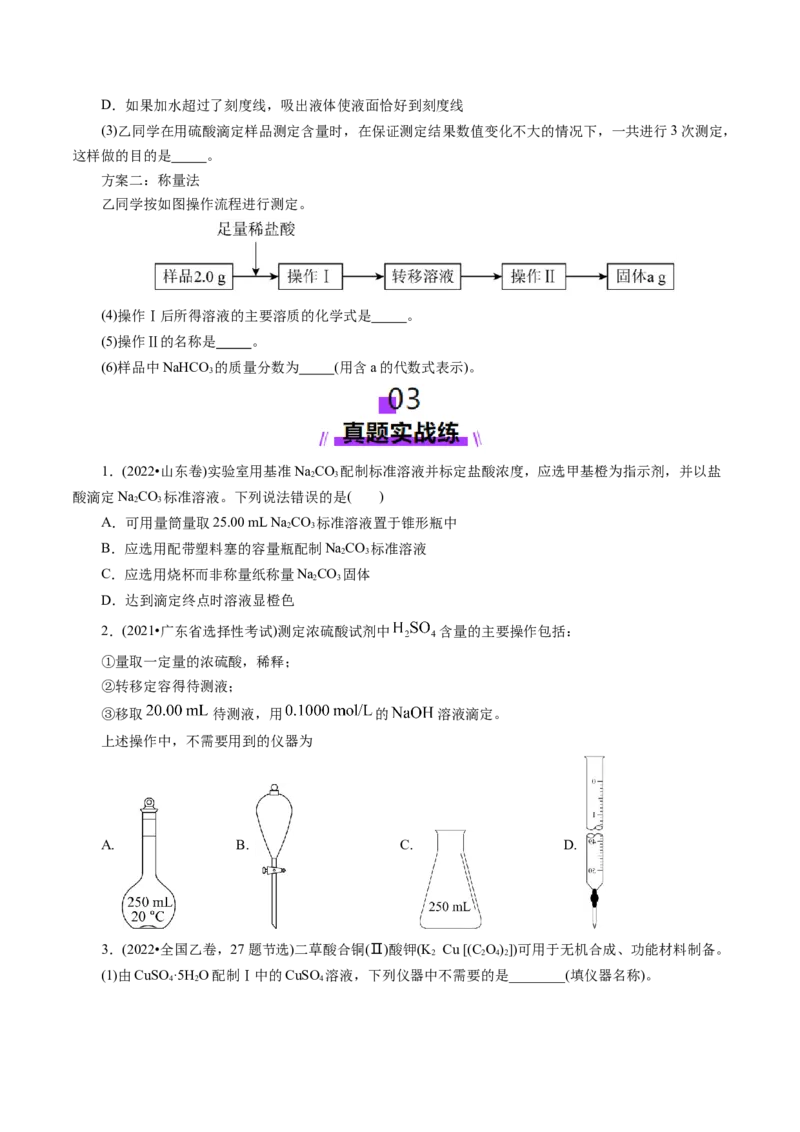
②配制过程中不需要用到的仪器是 (填字母)。
A. B. C. D.
③下列情况会导致所配制溶液浓度偏低的是 。
A.没有洗涤烧杯和玻璃棒
B.定容时俯视刻度线
C.容量瓶清洗后残留有少量蒸馏水D.如果加水超过了刻度线,吸出液体使液面恰好到刻度线
(3)乙同学在用硫酸滴定样品测定含量时,在保证测定结果数值变化不大的情况下,一共进行3次测定,
这样做的目的是 。
方案二:称量法
乙同学按如图操作流程进行测定。
(4)操作Ⅰ后所得溶液的主要溶质的化学式是 。
(5)操作Ⅱ的名称是 。
(6)样品中NaHCO 的质量分数为 (用含a的代数式表示)。
3
1.(2022•山东卷)实验室用基准NaCO 配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐
2 3
酸滴定NaCO 标准溶液。下列说法错误的是( )
2 3
A.可用量筒量取25.00 mL Na CO 标准溶液置于锥形瓶中
2 3
B.应选用配带塑料塞的容量瓶配制NaCO 标准溶液
2 3
C.应选用烧杯而非称量纸称量NaCO 固体
2 3
D.达到滴定终点时溶液显橙色
2.(2021•广东省选择性考试)测定浓硫酸试剂中 含量的主要操作包括:
①量取一定量的浓硫酸,稀释;
②转移定容得待测液;
③移取 待测液,用 的 溶液滴定。
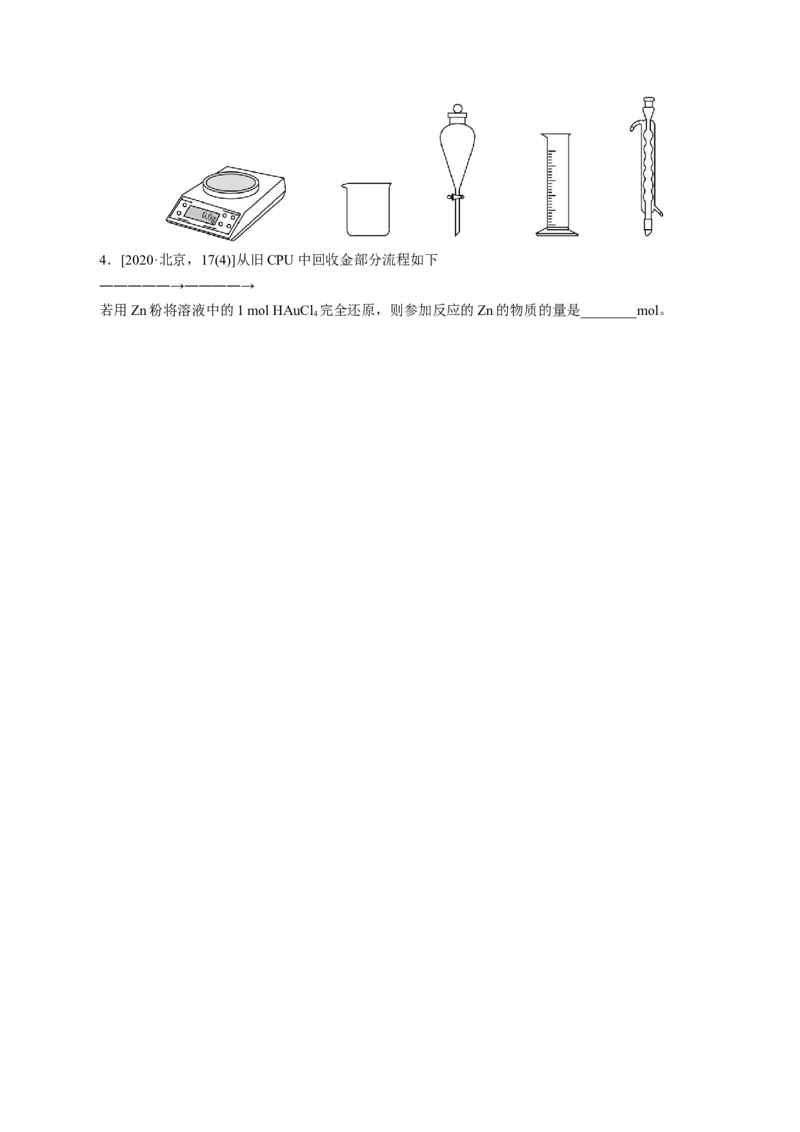
上述操作中,不需要用到的仪器为
A. B. C. D.
3.(2022•全国乙卷,27题节选)二草酸合铜(Ⅱ)酸钾(K Cu [(C O)])可用于无机合成、功能材料制备。
2 2 4 2
(1)由CuSO ·5H O配制Ⅰ中的CuSO 溶液,下列仪器中不需要的是________(填仪器名称)。
4 2 44.[2020·北京,17(4)]从旧CPU中回收金部分流程如下
―――――→――――→
若用Zn粉将溶液中的1 mol HAuCl 完全还原,则参加反应的Zn的物质的量是________mol。
4