文档内容
第 02 讲 物质的量浓度与溶液的配制(练)
第一部分:高考真题感悟
1.(2010·四川·高考真题)标准状况下VL氨气溶解在1L水中(水的密度近似为1g/ml),所得溶液的密
度为ρ g/ml,质量分数为ω,物质的量浓度为c mol/L,则下列关系中不正确的是
A. B.
C. D. =
2.(2009·浙江·高考真题)已知单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点
就越高。则下列溶液沸点最高的是
A.0.01mol· 的蔗糖溶液 B.0.01mol· 的 溶液
C.0.02mol· 的 溶液 D.0.02mol· 的 溶液
3.(2008·广东·高考真题)下列实验能达到预期目的的是
A.向煮沸的1 mol·L-1 NaOH溶液中滴加FeCl 饱和溶液制备Fe(OH) 胶体
2 3
B.向乙酸乙酯中加入饱和NaCO 溶液,振荡,分液分离除去乙酸乙酯中的少量乙酸
2 3
C.称取19.0 g SnCl ,用100 mL蒸馏水溶解,配制1.0 mol·L-1SnCl 溶液
2 2
D.检验葡萄糖,应用氢氧化铜粉末,加热检验。
4.(2020·北京·高考真题)下列说法正确的是
A.同温同压下,O 和CO 的密度相同
2 2
B.质量相同的HO和DO(重水)所含的原子数相同
2 2
C.物质的量相同的CHCHOH和CHOCH 所含共价键数相同
3 2 3 3
D.室温下,pH相同的盐酸和硫酸中,溶质的物质的量浓度相同
5.(2014·上海·高考真题)硫有多种含氧酸,亚硫酸(HSO )、硫酸(HSO )、焦硫酸
2 3 2 4
(HSO ·SO )、硫代硫酸(HSO)等等,其中硫酸最为重要,在工业上有广泛的应用。在实验室,浓硫
2 4 3 2 2 3
酸是常用的干燥剂。完成下列计算:
(1)焦硫酸(HSO ·SO )溶于水,其中的SO 都转化为硫酸。若将445g焦硫酸溶于水配成4.00L硫酸,该
2 4 3 3
硫酸的物质的量浓度为________mol/L。
(2)若以浓硫酸吸水后生成的HSO ·H O计算,250g质量分数为98%的硫酸能吸收_____g水
2 4 2
(3)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化焙烧的化学反应如下:3FeS+8O=Fe O+6SO 4FeS+11 O =2Fe O+8SO
2 2 3 4 2 2 2 2 3 2
若48mol FeS 完全反应耗用氧气2934.4L(标准状况),计算反应产物中Fe O 与Fe O 物质的量之比
2 3 4 2 3
_______。
(4)用硫化氢制取硫酸,既能充分利用资源又能保护环境,是一种很有发展前途的制备硫酸的方法。
硫化氢体积分数为0.84的混合气体(HS、HO、N)在空气中完全燃烧,若空气过量77%,计算产物气
2 2 2
体中SO 体积分数________(水是气体)。(已知空气组成:N 体积分数0.79、O 体积分数0.21)
2 2 2
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·上海·模拟预测)将V L浓度为0.3mol/L的盐酸浓度扩大一倍,采取的措施合理的是
A.将溶液加热浓缩至原来体积的一半
B.通入标准状况下的HCl气体6.72L
C.加入3mol/L的盐酸0.2V L,再稀释至1.5V L
D.加入等体积0.9mol/L的盐酸,混合均匀
2.(2022·浙江·高三)下列说法中正确的是
A.1L水中溶解了58.5gNaCl,该溶液的物质的量浓度为lmol/L
B.从1L2mol/L的HSO 溶液中取出0.5L,该溶液的浓度为lmol/L
2 4
C.配制500mL0.5mol·L-1的CuSO 溶液,需62.5g胆矾(CuSO ·5H O)
4 4 2
D.中和100mL1mol/L的HSO 溶液,需NaOH为4g
2 4
3.(2021·上海静安区·高三二模)将V L浓度为0.3mol/L的盐酸浓度扩大一倍,采取的措施合理的是
A.将溶液加热浓缩至原来体积的一半
B.通入标准状况下的HCl气体6.72L
C.加入3mol/L的盐酸0.2V L,再稀释至1.5V L
D.加入等体积0.9mol/L的盐酸,混合均匀
4.(2021·全国高三)36.5gHCl溶解在1L水中(水的密度近似为1 gmL-1),所得溶液的密度为ρ gmL-1,质
量分数为w,物质的量浓度为c gmL-1,N 表示阿伏加德罗常数,下列说法正确的是
A
A.所得溶液的物质的量浓度:c=1 gmL-1 B.所得溶液中含有N 个HCl分子
A
C.36.5 gHCl气体占有的体积为22.4L D.所得溶液的质量分数: w=
5.(2022·上海·模拟预测)将V L浓度为0.3mol/L的盐酸浓度扩大一倍,采取的措施合理的是
A.将溶液加热浓缩至原来体积的一半B.通入标准状况下的HCl气体6.72L
C.加入3mol/L的盐酸0.2V L,再稀释至1.5V L
D.加入等体积0.9mol/L的盐酸,混合均匀
6.(2021·海南·高三学业考试)钙元素在人体血液中以钙离子的形式存在,正常指标参考值为2.13×10-
3~2.70 ×10-3 mol·L-1。表示该指标的物理量是
A.溶解度 B.体积分数 C.物质的量浓度 D.质量分数
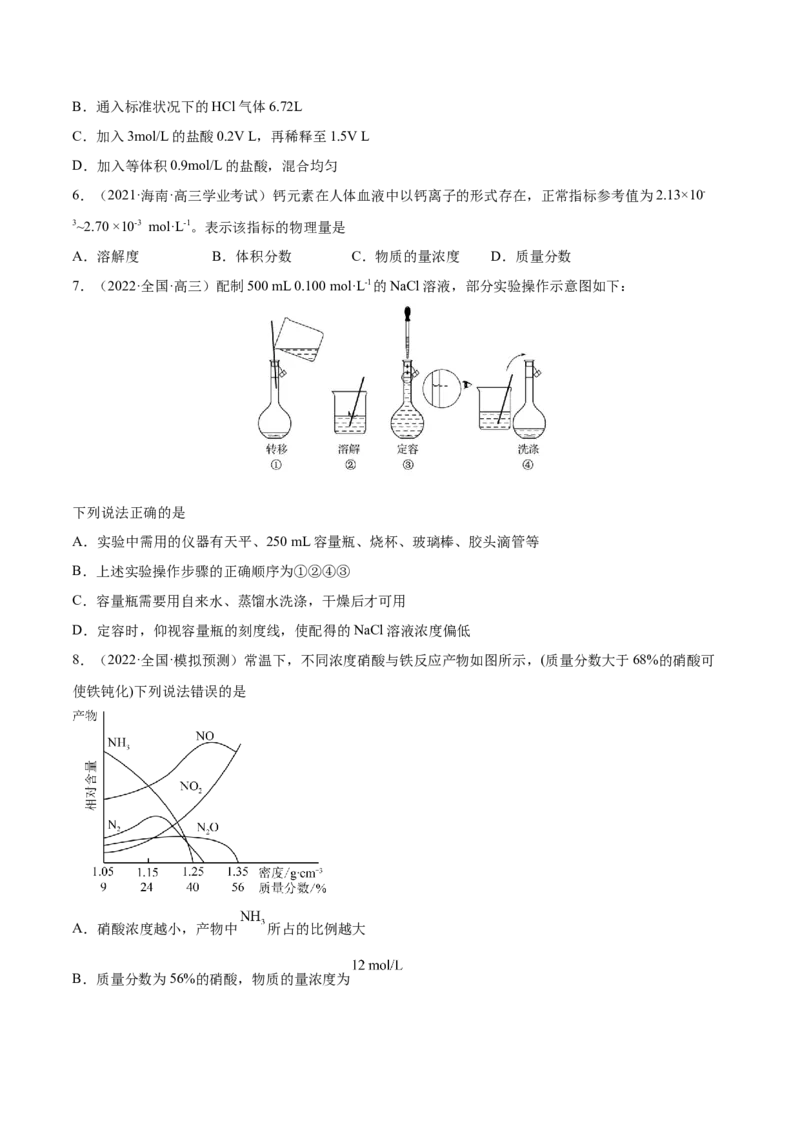
7.(2022·全国·高三)配制500 mL 0.100 mol·L-1的NaCl溶液,部分实验操作示意图如下:
下列说法正确的是
A.实验中需用的仪器有天平、250 mL容量瓶、烧杯、玻璃棒、胶头滴管等
B.上述实验操作步骤的正确顺序为①②④③
C.容量瓶需要用自来水、蒸馏水洗涤,干燥后才可用
D.定容时,仰视容量瓶的刻度线,使配得的NaCl溶液浓度偏低
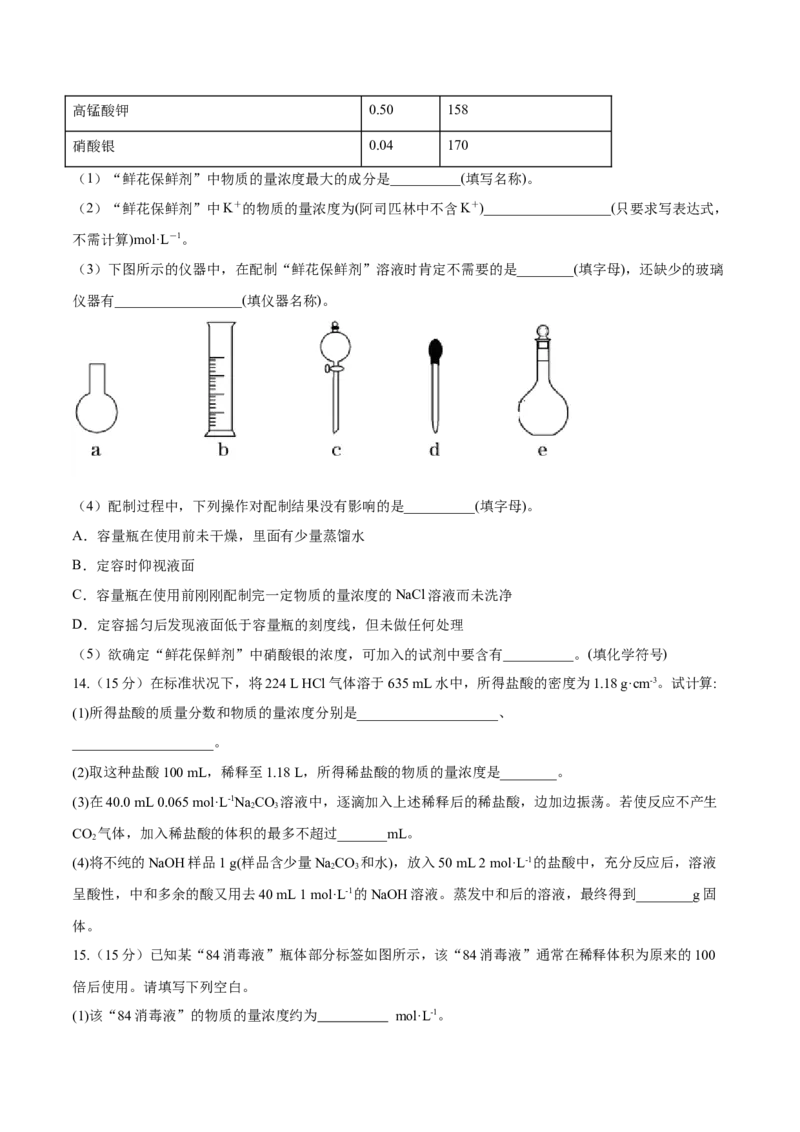
8.(2022·全国·模拟预测)常温下,不同浓度硝酸与铁反应产物如图所示,(质量分数大于68%的硝酸可
使铁钝化)下列说法错误的是
A.硝酸浓度越小,产物中 所占的比例越大
B.质量分数为56%的硝酸,物质的量浓度为C.质量分数为56%~68%的硝酸与少量铁反应时,还原产物仍以 为主
D.若把铁换成铜,硝酸浓度低于24%时,还原产物仍以 为主
9.(2022·全国·高三)下列关于0.1mol·L-1NaCO 溶液的叙述错误的是
2 3
A.0.5L该溶液的钠离子的物质的量浓度为0.2mol·L-1
B.1L该溶液中含有NaCO 的物质的量为0.1mol
2 3
C.从1L该溶液中取出100mL,则取出溶液中NaCO 的物质的量浓度为0.01mol·L-1
2 3
D.取出该溶液10mL,加水稀释至100mL后,NaCO 的物质的量浓度为0.01mol·L-1
2 3
10.(2022·浙江·高三)某温度下,物质XSO 的饱和溶液的密度为ρ g·mL-1,c(X+)=c mol·L-1,溶质的质
2 4
量分数为a%,溶质的摩尔质量为M g·mol-1,溶解度为S g.下列表达式正确的是
A.S= B.c= C.a%= D.S=
11.(2022·浙江·高三)配制一定物质的量浓度的溶液是一个重要的定量实验,下列有关说法正确的是
A.容量瓶用蒸馏水洗净后,可不经干燥直接用于配制溶液
B.配制一定物质的量浓度的稀盐酸时,用量筒量取9.82mL浓盐酸
C.配制1L0.1mol·L—1的NaCl溶液时,用托盘天平称量5.85gNaCl固体
D.定容时,为防止液滴飞溅,胶头滴管紧贴容量瓶内壁
12.(2021·浙江·高三)体积为V(mL)、密度为ρ (g·mL-1)的溶液中,含有摩尔质量为M(g·mol-1)的溶质
m(g),其物质的量浓度为c(mol·L-1),溶质的质量分数为a%。下列有关关系式不正确的是
A.m=V×ρ×a% B.c=1000×ρ·a×M mol·L-1
C.c= ×L-1 D.a%= ×100%
二、主观题(共3小题,共40分)
13.(10分)在花瓶中加入“鲜花保鲜剂”可延长鲜花的寿命。下表是1 L“鲜花保鲜剂”的成分,阅读后
并回答下列问题:
成分 质量/g 摩尔质量/(g·mol-1)
蔗糖 50.00 342
硫酸钾 0.50 174
阿司匹林 0.35 180高锰酸钾 0.50 158
硝酸银 0.04 170
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是__________(填写名称)。
(2)“鲜花保鲜剂”中K+的物质的量浓度为(阿司匹林中不含K+)__________________(只要求写表达式,
不需计算)mol·L-1。
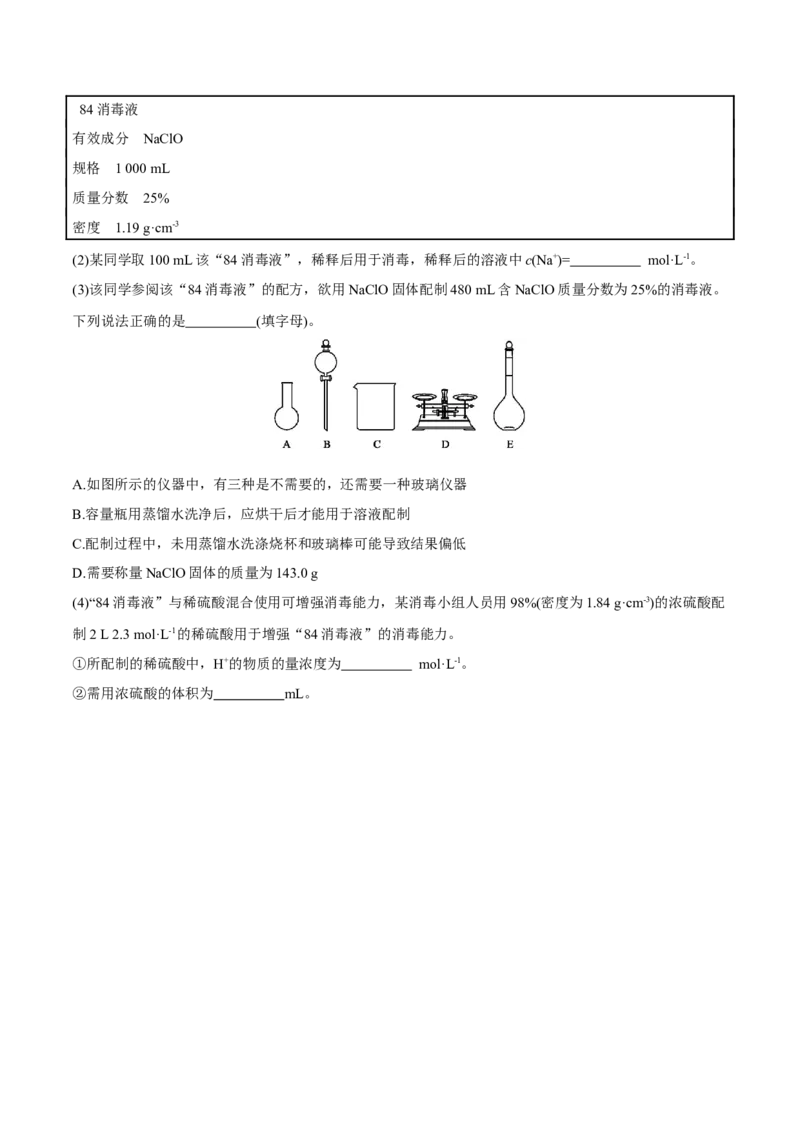
(3)下图所示的仪器中,在配制“鲜花保鲜剂”溶液时肯定不需要的是________(填字母),还缺少的玻璃
仪器有__________________(填仪器名称)。
(4)配制过程中,下列操作对配制结果没有影响的是__________(填字母)。
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视液面
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)欲确定“鲜花保鲜剂”中硝酸银的浓度,可加入的试剂中要含有__________。(填化学符号)
14.(15分)在标准状况下,将224 L HCl气体溶于635 mL水中,所得盐酸的密度为1.18 g·cm-3。试计算:
(1)所得盐酸的质量分数和物质的量浓度分别是____________________、
____________________。
(2)取这种盐酸100 mL,稀释至1.18 L,所得稀盐酸的物质的量浓度是________。
(3)在40.0 mL 0.065 mol·L-1NaCO 溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生
2 3
CO 气体,加入稀盐酸的体积的最多不超过_______mL。
2
(4)将不纯的NaOH样品1 g(样品含少量NaCO 和水),放入50 mL 2 mol·L-1的盐酸中,充分反应后,溶液
2 3
呈酸性,中和多余的酸又用去40 mL 1 mol·L-1的NaOH溶液。蒸发中和后的溶液,最终得到________g固
体。
15.(15分)已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常在稀释体积为原来的100
倍后使用。请填写下列空白。
(1)该“84消毒液”的物质的量浓度约为 mol·L-1。84消毒液
有效成分 NaClO
规格 1 000 mL
质量分数 25%
密度 1.19 g·cm-3
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)= mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。
下列说法正确的是 (填字母)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0 g
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配
制2 L 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为 mol·L-1。
②需用浓硫酸的体积为 mL。