文档内容
第 03 讲 盐类的水解
目录
01 模拟基础练
【题型一】盐类水解规律
【题型二】 盐类水解影响因素
【题型三】盐类水解的应用
【题型四】离子浓度大小比较
【题型五】粒子浓度变化曲线
02 重难创新练
03 真题实战练
题型一 盐类水解规律
1.NH Cl溶于重水(D O)后,产生的一水合氨和水合氢离子为( )
4 2
A.NH D·H O和DO+ B.NH ·D O和HD O+
2 2 3 3 2 2
C.NH ·HDO和DO+ D.NH D·HDO和HDO+
3 3 2 2
2.下列说法及离子方程式正确的是( )
A.NaS水溶液显碱性:S2-+2HO HS+2OH-
2 2 2
B.NH Cl水溶液显酸性:NH Cl===NH+H++Cl-
4 4 3
C.CuSO 水溶液显酸性:Cu2++2HO Cu(OH) ↓+2H+
4 2 2
D.NaHCO 水溶液显碱性:HCO+HO HCO+OH-
3 2 2 3
3.室温下,0.1 mol·L-1的NH CN溶液的pH等于9.32,据此,下列说法错误的是( )
4
A.上述溶液能使甲基橙试剂变黄色
B.室温下,NH ·H O是比HCN更弱的电解质
3 2
C.上述溶液中CN-的水解程度大于NH的水解程度
D.室温下,0.1 mol·L-1 NaCN溶液中,CN-的水解程度小于上述溶液中CN-的水解程度
4.25 ℃时浓度都是1 mol·L-1的四种正盐溶液:AX、BX、AY、BY;AX的溶液pH=7且溶液中
c(X-)=1 mol·L-1,BX的溶液pH=4,BY的溶液pH=6。下列说法正确的是( )
A.电离平衡常数K(BOH)小于K(HY)
B.AY溶液的pH小于BY溶液的pH
C.稀释相同倍数,溶液pH变化BX等于BY
D.将浓度均为1 mol·L-1的HX和HY溶液分别稀释10倍后,HX溶液的pH大于HY5.室温下,有a mol·L-1NaX和b mol·L-1NaY两种盐溶液。下列说法正确的是( )
A.若a=b且c(X-) +c(HX)=c(Y-),则酸性HX>HY
B.若a>b且c(X-)=c(Y-),则酸性HX>HY
C.若 且 ,则酸性HX<HY
D.若a<b且c(X-)<c(Y-),则酸性HX<HY
题型二 盐类水解影响因素
6.在一定条件下,NaCO 溶液存在水解平衡:CO2-+HO HCO -+OH-。下列说法正确的是(
2 3 3 2 3
)
A.稀释溶液,水解平衡向逆反应方向移动,水解程度减小 B.通入CO,平衡向正反应方向移动
2
C.升高温度,c(HCO -)/c(CO2-)减小 D.加入NaOH固体,溶液pH减小
3 3
7.一定条件下,CHCOONa溶液中存在水解平衡:CHCOO-+H O CHCOOH+OH-。下列说法正确
3 3 2 3
的是( )
A.加入少量NaOH固体,c(CHCOO-)增大
3
B.加入少量FeCl 固体,c(CHCOO-)增大
3 3
C.稀释溶液,溶液的pH增大
D.加入适量醋酸得到的酸性混合溶液中:c(Na+)>c(CHCOO-)>c(H+)>c(OH-)
3
8.下列关于FeCl 水解的说法错误的是( )
3
A.在FeCl 稀溶液中,水解达到平衡时,无论加FeCl 饱和溶液还是加水稀释,平衡均向右移动
3 3
B.浓度为5 mol·L-1和0.5 mol·L-1的两种FeCl 溶液,其他条件相同时,前者Fe3+的水解程度小于后者
3
C.其他条件相同时,同浓度的FeCl 溶液在50 ℃和20 ℃时发生水解,50 ℃时Fe3+的水解程度比20
3
℃时的小
D.为抑制Fe3+的水解,更好地保存FeCl 溶液,应加少量盐酸
3
9.常温下,滴有两滴酚酞溶液的 NaCO 溶液中存在CO+HO HCO+OH-平衡,溶液呈红色,
2 3 2
下列说法不正确的是( )
A.稀释溶液, 增大
B.通入CO,或者加入少量氯化铵溶液,溶液pH均减小
2
C.升高温度,红色变深,平衡常数增大
D.加入NaOH固体, 减小
10.某同学探究溶液的酸碱性对FeCl 水解平衡的影响,实验方案如下:配制50 mL 0.001 mol·L-1FeCl
3 3
溶液、50 mL对照组溶液X,向两种溶液中分别滴加1滴1 mol·L-1HCl溶液、1滴1 mol·L-1NaOH溶液,测
得溶液pH随时间变化的曲线如图所示。下列说法不正确的是( )
A.依据M点对应的pH,说明Fe3+发生了水解反应
B.对照组溶液X的组成可能是0.003 mol·L-1KCl溶液
C.依据曲线c和d说明Fe3+水解平衡发生了移动
D.通过仪器检测体系浑浊度的变化,可表征水解平衡移动的方向
题型三 盐类水解的应用
11.下列根据反应原理设计的应用,不正确的是( )
A.CO+HO HCO+OH- 用热的纯碱溶液清洗油污
2
B.Al3++3HO Al(OH) (胶体)+3H+ 明矾净水
2 3
C.TiCl +(x+2)H O(过量) TiO·xHO↓+4HCl 制备TiO 纳米粉
4 2 2 2 2
D.SnCl +HO Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入氢氧化钠
2 2
12. 合理利用某些盐能水解的性质,能解决许多生产、生活中的问题,下列叙述的事实与盐类水解
的性质无关的是( )
A.金属焊接时可用NH Cl溶液做除锈剂
4
B.配制FeSO 溶液时,加入一定量Fe粉
4
C.长期施用铵态氮肥会使土壤酸化
D.向FeCl 溶液中加入CaCO 粉末后有气泡产生
3 3
513.化学在日常生活和生产中有着重要的应用。下列说法不正确的是( )
A.某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为溶液中的SO 2-水解
3
B.明矾水解形成的Al(OH) 胶体能吸附水中悬浮物,可用于水的净化
3
C.将饱和FeCl 溶液滴入沸水中可制备Fe(OH) 胶体,利用的是盐类的水解
3 3
D.配制FeCl 溶液时加入少量的盐酸,抑制Fe3+水解
3
14.下列叙述与盐类水解的性质无关的是( )
A.金属焊接时可用NH Cl溶液作为除锈剂
4
B.配制FeSO 溶液时,加入一定量Fe粉
4
C.长期施用铵态氮肥会使土壤酸化D.向FeCl 溶液中加入CaCO 粉末会有气泡产生
3 3
15.下列关于盐类水解的应用中,说法正确的是( )
A.加热蒸干NaCO 溶液,最后可以得到NaOH和NaCO 的混合固体
2 3 2 3
B.除去MgCl 中的Fe3+,可以加入NaOH固体
2
C.明矾净水的反应:Al3++3HO Al(OH) (胶体)+3H+
2 3
D.加热蒸干KCl溶液,最后得到KOH固体(不考虑CO 的反应)
2
题型四 离子浓度大小比较
16.下列溶液中粒子的物质的量浓度关系正确的是( )
A.0.1 mol·L-1 NaHCO 溶液与0.1 mol·L-1 NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO)>
3
c(HCO)>c(OH-)
B.20 mL 0.1 mol·L-1 CHCOONa溶液与10 mL 0.1 mol·L-1 HCl溶液混合后溶液呈酸性,所得溶液中:
3
c(CHCOO-)>c(Cl-)>c(CHCOOH)>c(H+)
3 3
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH)+c(OH
-)
D.0.1 mol·L-1 CHCOOH溶液与0.1 mol·L-1 NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)
3
+c(CHCOOH)
3
17.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
A.NaHCO 溶液中:c(H+)=c(OH-)+c(HCO)
3 2 3
B.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(NH+)>c(OH-)
4
C.0.1mol/L Na CO 与0.1mol/L NaHCO 溶液等体积混合: 2c(Na+)=3c(CO 2-)+3c(HCO-)+3c(H CO)
2 3 3 3 3 2 3
D.0.1mol/L Na C O 与0.1mol/L 的盐酸等体积混合(H C O 为二元弱酸):2c(C O2-)+c(HC O-)
2 2 4 2 2 4 2 4 2 4
+c(OH-)=c(Na+)+c(H+)
18.常温下,用0.1 mol·L-1氨水滴定10 mL浓度均为0.1 mol·L-1的HCl和CHCOOH的混合液,下列
3
说法不正确的是( )
A.在氨水滴定前,HCl和CHCOOH的混合液中c(Cl-)>c(CHCOO-)
3 3
B.当滴入氨水10
mL时,c(NH+
)+c(NH ·H O)=c(CHCOO-)+c(CHCOOH)
4 3 2 3 3
C.当滴入氨水20 mL时,c(CHCOOH)+c(H+)=c(NH ·H O)+c(OH-)
3 3 2
D.当溶液呈中性时,氨水滴入量大于20
mL,c(NH+
)c(HCOO-)>c(H+)>c(OH-)
B.草酸氢钠溶液中加入甲酸钠溶液至中性:c(Na+)=c(HCO- )+c(CO2-
)+c(HCOO-)
2 4 2 4
C.NaC O
溶液中:c(HCO-
)+2c(H C O)+c(H+)=c(OH-)
2 2 4 2 4 2 2 4
D.足量甲酸与草酸钠溶液反应:2HCOOH+Na C O=H C O+2HCOONa
2 2 4 2 2 4
20.常温下,通过下列实验探究NaHCO 溶液的性质。
3实验1:用 pH计测量0.05mol·L-1 NaHCO 溶液的pH,测得pH为8.3
3
实验2:向 0.05mol·L-1 NaHCO 溶液中逐滴滴加等体积同浓度的NaOH溶液,溶液pH逐渐上升至
3
11.3
实验3:向0.05mol·L-1NaHCO 溶液中逐滴滴加等体积同浓度的盐酸,溶液pH逐渐下降至4.3
3
下列说法正确的是( )
A.由实验1可得出: K <K (H CO) ·K (H CO)
w a1 2 3 a2 2 3
B.实验2过程中,c(OH- )+c(HCO- )+2c(CO 2-- )逐渐增大
3 3
C.实验3过程中,c(Na+)逐渐小于c(HCO - )+c(CO 2-- )+c(H CO)
3 3 2 3
D.实验2和3结束时,用x和y依次表示两份溶液中c(Na+ )+c(H+),则x>y
题型五 粒子浓度变化曲线
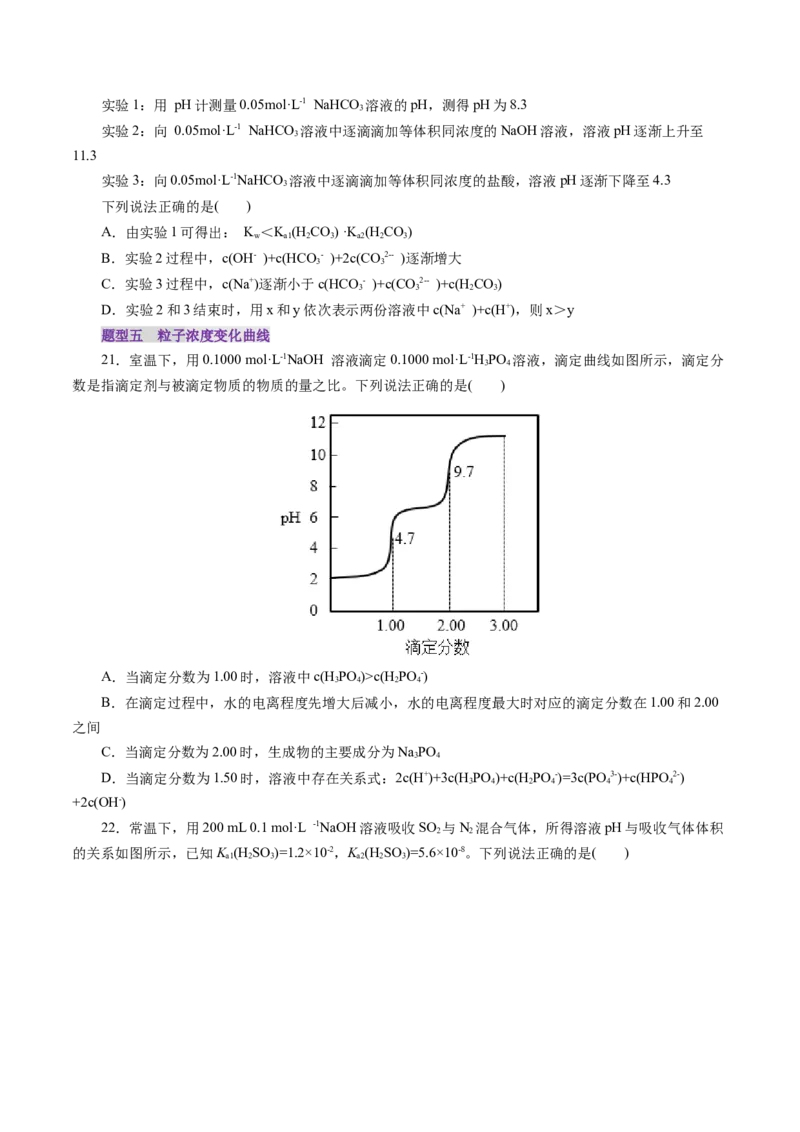
21.室温下,用0.1000 mol·L-1NaOH 溶液滴定0.1000 mol·L-1HPO 溶液,滴定曲线如图所示,滴定分
3 4
数是指滴定剂与被滴定物质的物质的量之比。下列说法正确的是( )
A.当滴定分数为1.00时,溶液中c(HPO )>c(H PO -)
3 4 2 4
B.在滴定过程中,水的电离程度先增大后减小,水的电离程度最大时对应的滴定分数在1.00和2.00
之间
C.当滴定分数为2.00时,生成物的主要成分为NaPO
3 4
D.当滴定分数为1.50时,溶液中存在关系式:2c(H+)+3c(H PO )+c(H PO -)=3c(PO3-)+c(HPO 2-)
3 4 2 4 4 4
+2c(OH-)
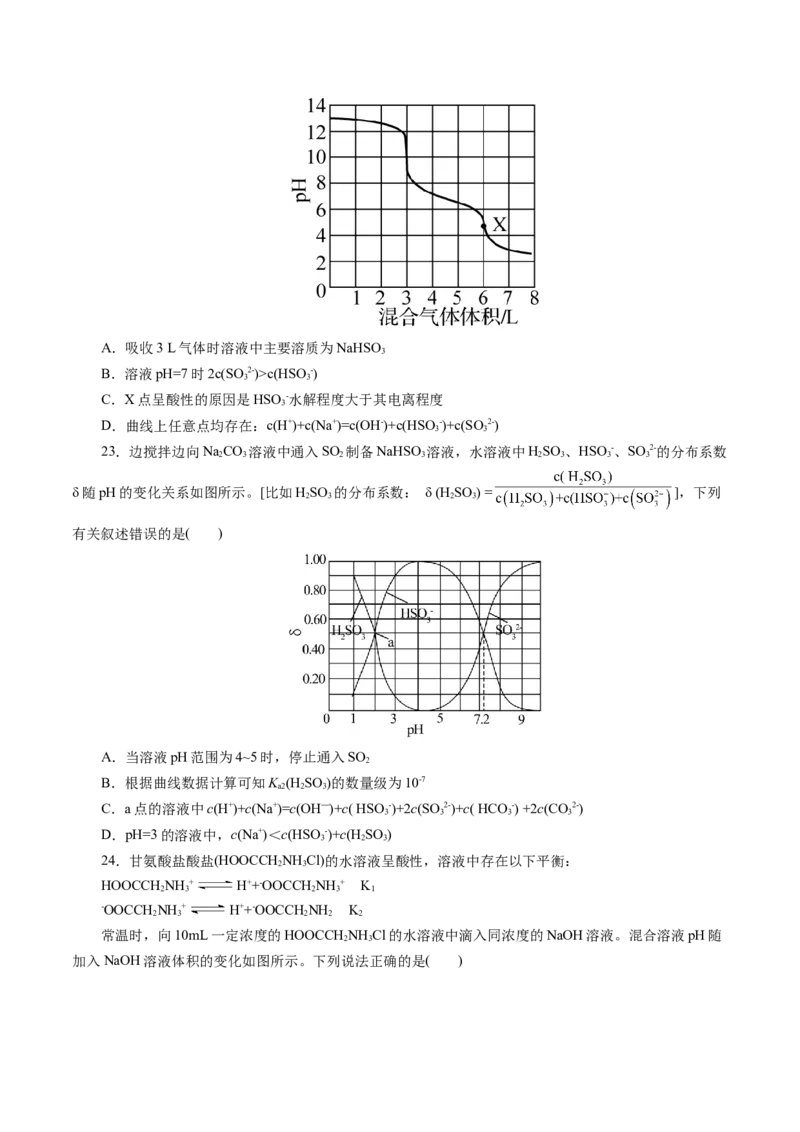
22.常温下,用200 mL 0.1 mol·L -1NaOH溶液吸收SO 与N 混合气体,所得溶液pH与吸收气体体积
2 2
的关系如图所示,已知K (H SO )=1.2×10-2,K (H SO )=5.6×10-8。下列说法正确的是( )
a1 2 3 a2 2 3A.吸收3 L气体时溶液中主要溶质为NaHSO
3
B.溶液pH=7时2c(SO 2-)>c(HSO -)
3 3
C.X点呈酸性的原因是HSO -水解程度大于其电离程度
3
D.曲线上任意点均存在:c(H+)+c(Na+)=c(OH-)+c(HSO -)+c(SO2-)
3 3
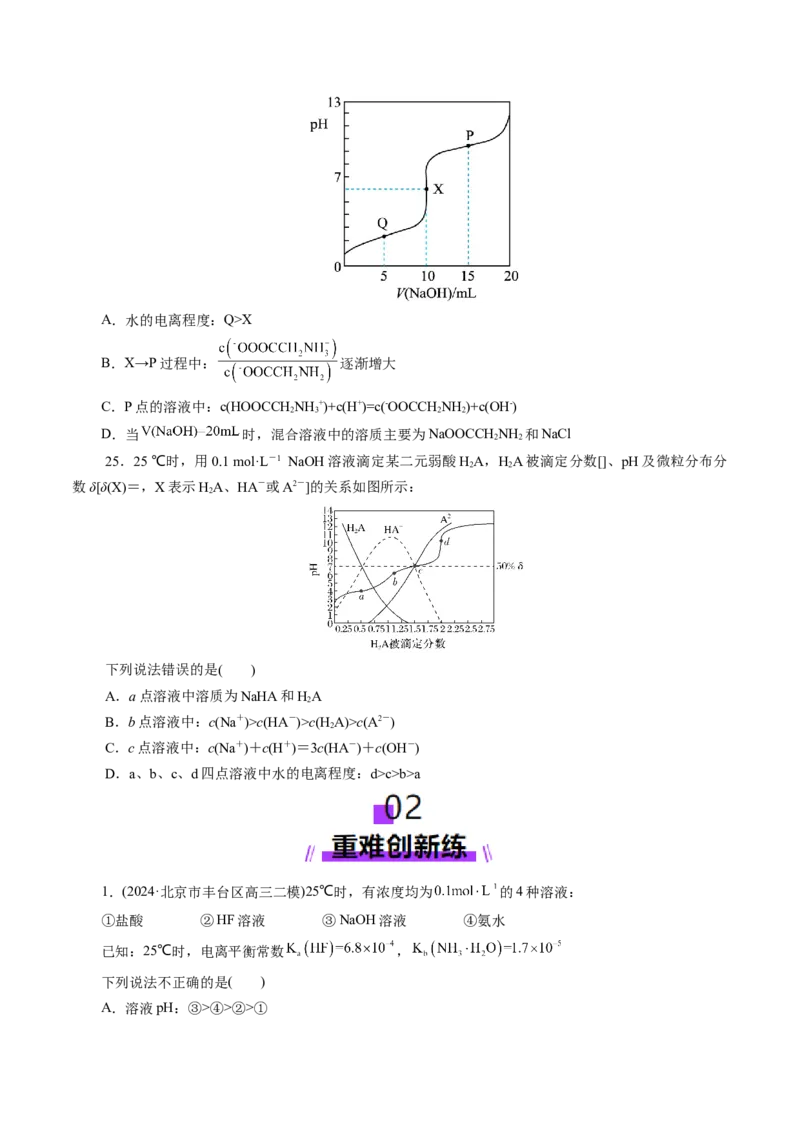
23.边搅拌边向NaCO 溶液中通入SO 制备NaHSO 溶液,水溶液中HSO 、HSO -、SO 2-的分布系数
2 3 2 3 2 3 3 3
δ随pH的变化关系如图所示。[比如HSO 的分布系数: δ (H SO ) = ],下列
2 3 2 3
有关叙述错误的是( )
A.当溶液pH范围为4~5时,停止通入SO
2
B.根据曲线数据计算可知K (H SO )的数量级为10-7
a2 2 3
C.a点的溶液中c(H+)+c(Na+)=c(OH—)+c( HSO -)+2c(SO 2-)+c( HCO-) +2c(CO2-)
3 3 3 3
D.pH=3的溶液中,c(Na+)<c(HSO -)+c(H SO )
3 2 3
24.甘氨酸盐酸盐(HOOCCH NH Cl)的水溶液呈酸性,溶液中存在以下平衡:
2 3
HOOCCH NH + H++-OOCCH NH + K
2 3 2 3 1
-OOCCH NH + H++-OOCCH NH K
2 3 2 2 2
常温时,向10mL一定浓度的HOOCCH NH Cl的水溶液中滴入同浓度的NaOH溶液。混合溶液pH随
2 3
加入NaOH溶液体积的变化如图所示。下列说法正确的是( )A.水的电离程度:Q>X
B.X→P过程中: 逐渐增大
C.P点的溶液中:c(HOOCCH NH +)+c(H+)=c(-OOCCH NH )+c(OH-)
2 3 2 2
D.当 时,混合溶液中的溶质主要为NaOOCCHNH 和NaCl
2 2
25.25 ℃时,用0.1 mol·L-1 NaOH溶液滴定某二元弱酸HA,HA被滴定分数[]、pH及微粒分布分
2 2
数δ[δ(X)=,X表示HA、HA-或A2-]的关系如图所示:
2
下列说法错误的是( )
A.a点溶液中溶质为NaHA和HA
2
B.b点溶液中:c(Na+)>c(HA-)>c(H A)>c(A2-)
2
C.c点溶液中:c(Na+)+c(H+)=3c(HA-)+c(OH-)
D.a、b、c、d四点溶液中水的电离程度:d>c>b>a
1.(2024·北京市丰台区高三二模)25℃时,有浓度均为 的4种溶液:
①盐酸 ②HF溶液 ③NaOH溶液 ④氨水
已知:25℃时,电离平衡常数 ,
下列说法不正确的是( )
A.溶液pH:③>④>②>①B.水电离出的 浓度:①=③<②<④
C.②和④等体积混合后的溶液中:
D. ①和 ③混合后溶液 (溶液体积变化忽略不计),则
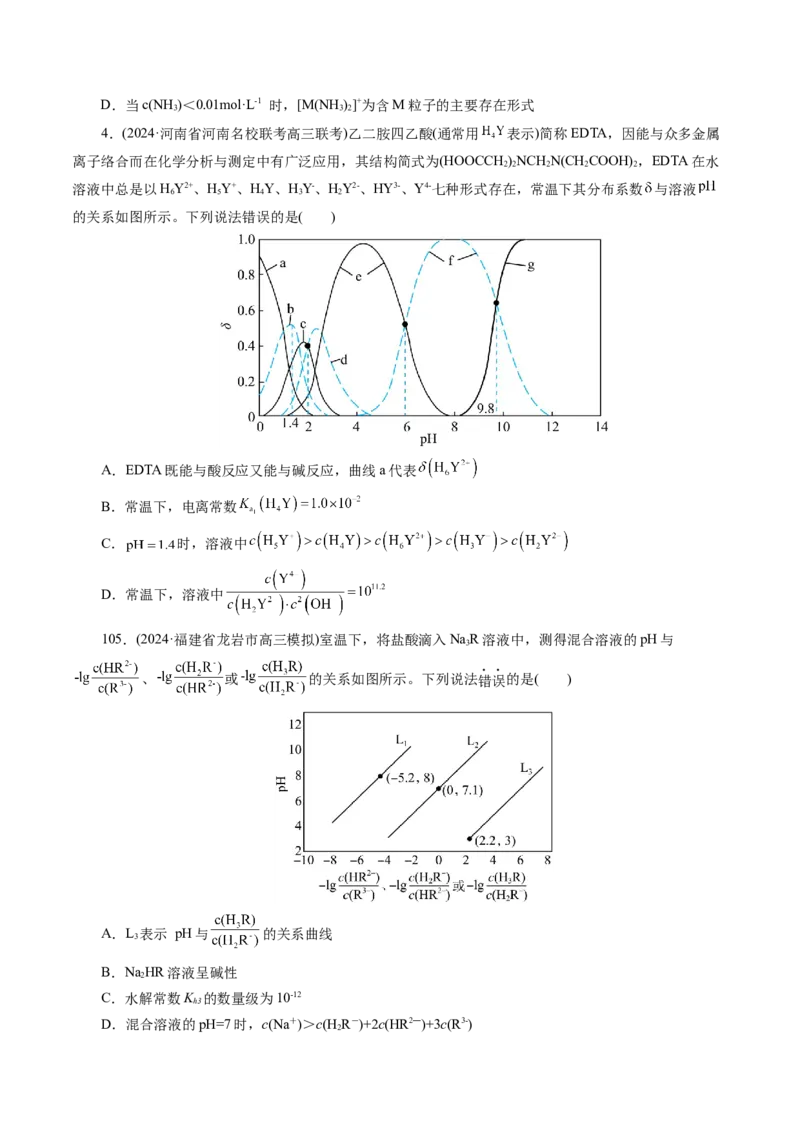
2.(2024·福建省泉州市高三第二次模拟考试)实验室模拟侯氏制碱碳酸化制NaHCO 的过程,将CO 通
3 2
入饱和氨盐水(溶质为NH 、NaCl),实验现象及数据如图1,含碳粒子在水溶液中的物质的量分数(δ)与pH
3
的关系如图2。
下列说法正确的是( )
A.0 min,溶液中c(Na+)+ c(NH +)=c(Cl-)
4
B.0~60 min,发生反应:2CO+3 NH ·H O =CO 2-+HCO-+3NH++H O
2 3 2 3 3 4 2
C.水的电离程度:
D.0~100 min,n(Cl-)、n(Na+)均保持不变
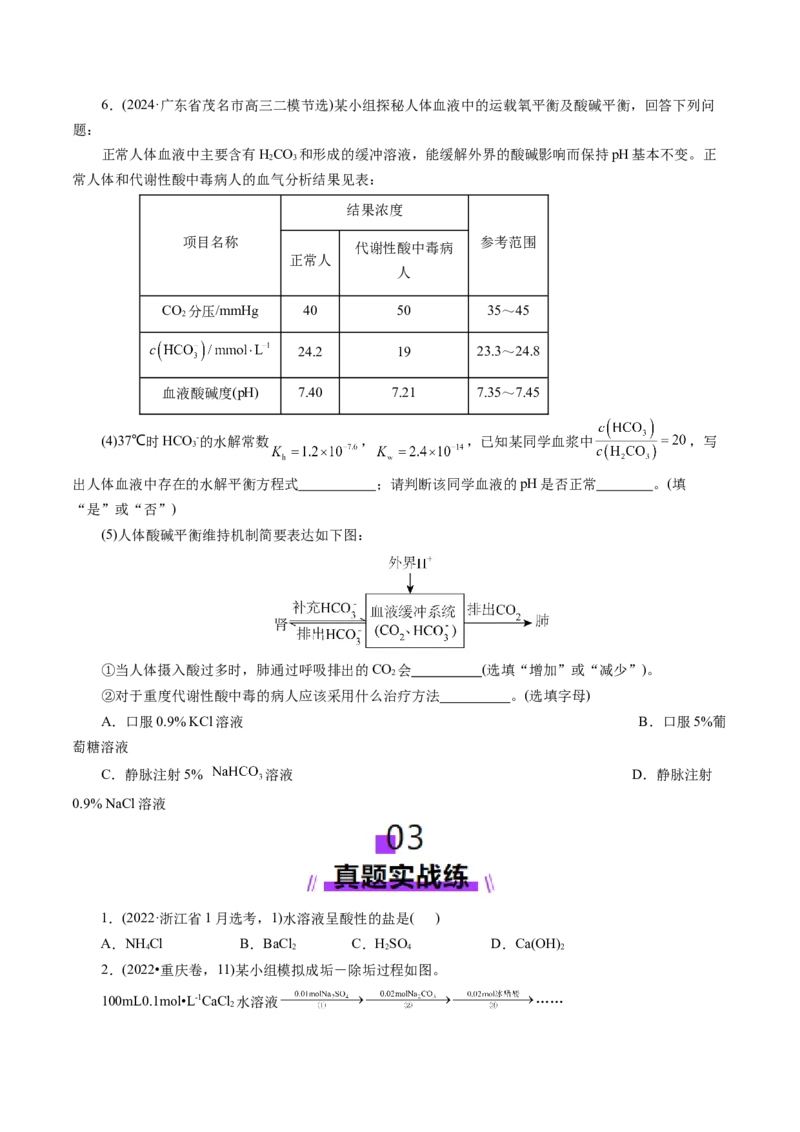
3.(2024·安徽省滁州市高三二模)已知:①M++NH [M(NH)]+ K=103.32
3 3 1
②[M(NH)]+ +NH [M(NH)]+ K
3 2 3 3 2 2
M+、[M(NH)]+、[M(NH)]+ 的分布分数 与 关系如下图所示。下列说法正确的是( )
3 3 2
{分布分数 }
A.K=103.90
2
B.曲线b代表
C.加水稀释,δ(M+)减小D.当c(NH )<0.01mol·L-1 时,[M(NH)]+为含M粒子的主要存在形式
3 3 2
4.(2024·河南省河南名校联考高三联考)乙二胺四乙酸(通常用 表示)简称EDTA,因能与众多金属
离子络合而在化学分析与测定中有广泛应用,其结构简式为(HOOCCH )NCH N(CH COOH),EDTA在水
2 2 2 2 2
溶液中总是以HY2+、HY+、HY、HY-、HY2-、HY3-、Y4-七种形式存在,常温下其分布系数 与溶液
6 5 4 3 2
的关系如图所示。下列说法错误的是( )
A.EDTA既能与酸反应又能与碱反应,曲线a代表
B.常温下,电离常数
C. 时,溶液中
D.常温下,溶液中
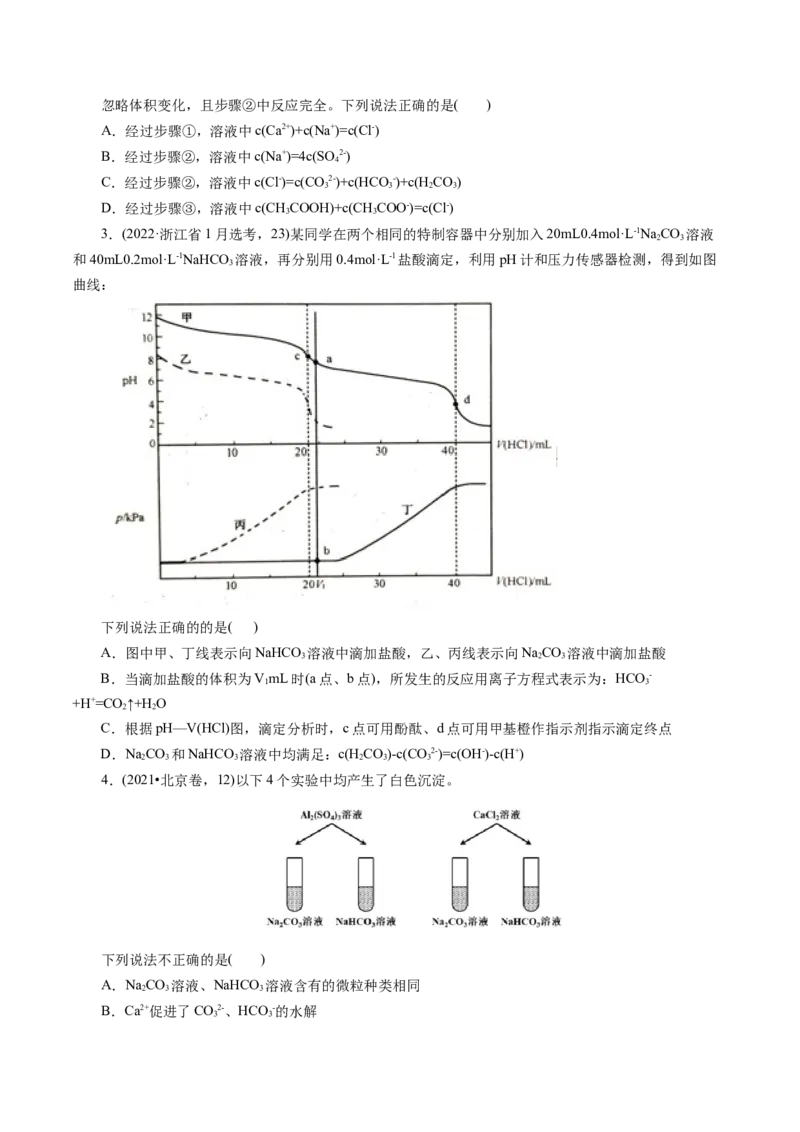
105.(2024·福建省龙岩市高三模拟)室温下,将盐酸滴入NaR溶液中,测得混合溶液的pH与
3
、 或 的关系如图所示。下列说法错误的是( )
A.L 表示 pH与 的关系曲线
3
B.NaHR溶液呈碱性
2
C.水解常数K 的数量级为10-12
h3
D.混合溶液的pH=7时,c(Na+)>c(HR-)+2c(HR2―)+3c(R3-)
26.(2024·广东省茂名市高三二模节选)某小组探秘人体血液中的运载氧平衡及酸碱平衡,回答下列问
题:
正常人体血液中主要含有HCO 和形成的缓冲溶液,能缓解外界的酸碱影响而保持pH基本不变。正
2 3
常人体和代谢性酸中毒病人的血气分析结果见表:
结果浓度
项目名称 参考范围
代谢性酸中毒病
正常人
人
CO 分压/mmHg 40 50 35~45
2
24.2 19 23.3~24.8
血液酸碱度(pH) 7.40 7.21 7.35~7.45
(4)37℃时HCO -的水解常数 , ,已知某同学血浆中 ,写
3
出人体血液中存在的水解平衡方程式 ;请判断该同学血液的pH是否正常 。(填
“是”或“否”)
(5)人体酸碱平衡维持机制简要表达如下图:
①当人体摄入酸过多时,肺通过呼吸排出的CO 会 (选填“增加”或“减少”)。
2
②对于重度代谢性酸中毒的病人应该采用什么治疗方法 。(选填字母)
A.口服0.9% KCl溶液 B.口服5%葡
萄糖溶液
C.静脉注射5% 溶液 D.静脉注射
0.9% NaCl溶液
1.(2022·浙江省1月选考,1)水溶液呈酸性的盐是( )
A.NH Cl B.BaCl C.HSO D.Ca(OH)
4 2 2 4 2
2.(2022•重庆卷,11)某小组模拟成垢-除垢过程如图。
100mL0.1mol•L-1CaCl 水溶液 ……
2忽略体积变化,且步骤②中反应完全。下列说法正确的是( )
A.经过步骤①,溶液中c(Ca2+)+c(Na+)=c(Cl-)
B.经过步骤②,溶液中c(Na+)=4c(SO2-)
4
C.经过步骤②,溶液中c(Cl-)=c(CO 2-)+c(HCO-)+c(H CO)
3 3 2 3
D.经过步骤③,溶液中c(CHCOOH)+c(CH COO-)=c(Cl-)
3 3
3.(2022·浙江省1月选考,23)某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1NaCO 溶液
2 3
和40mL0.2mol·L-1NaHCO 溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图
3
曲线:
下列说法正确的的是( )
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐酸
3 2 3
B.当滴加盐酸的体积为VmL时(a点、b点),所发生的反应用离子方程式表示为:HCO -
1 3
+H+=CO ↑+H O
2 2
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.NaCO 和NaHCO 溶液中均满足:c(HCO)-c(CO2-)=c(OH-)-c(H+)
2 3 3 2 3 3
4.(2021•北京卷,12)以下4个实验中均产生了白色沉淀。
下列说法不正确的是( )
A.NaCO 溶液、NaHCO 溶液含有的微粒种类相同
2 3 3
B.Ca2+促进了CO2-、HCO -的水解
3 3C.Al3+促进了CO2-、HCO -的水解
3 3
D.滴入溶液后,4支试管内溶液的pH都变小
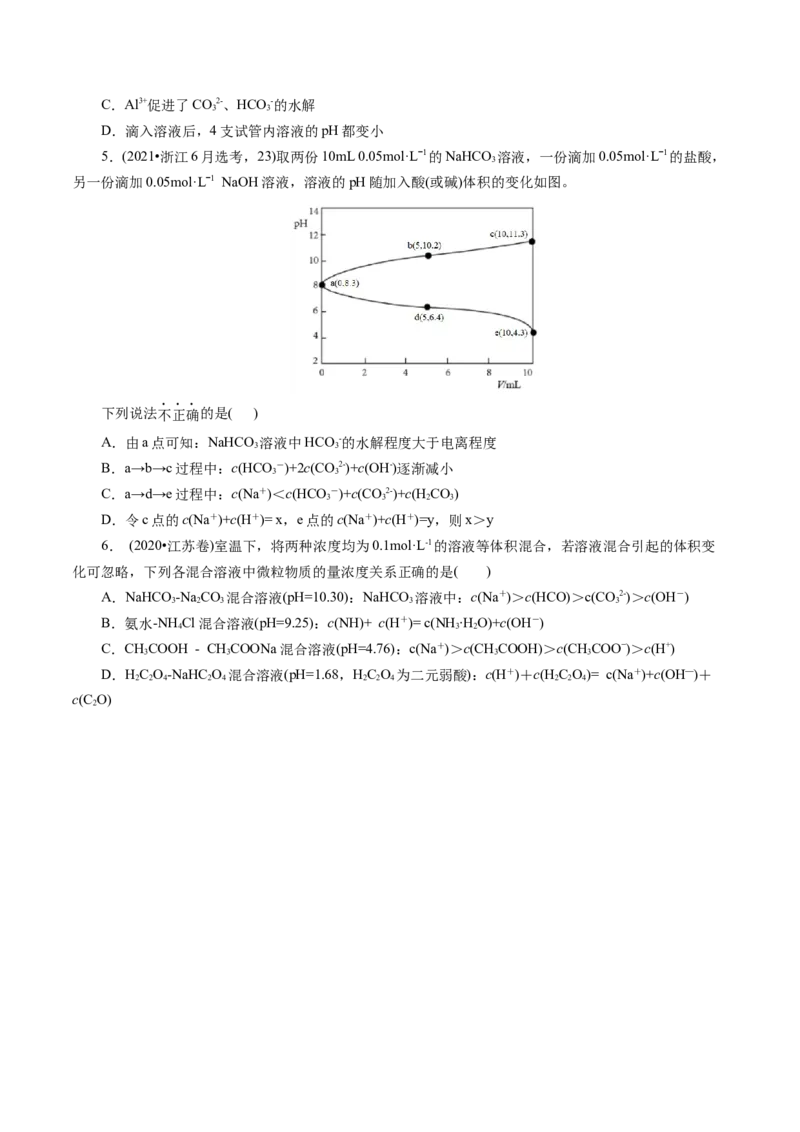
5.(2021•浙江6月选考,23)取两份10mL 0.05mol·Lˉ1的NaHCO 溶液,一份滴加0.05mol·Lˉ1的盐酸,
3
另一份滴加0.05mol·Lˉ1 NaOH溶液,溶液的pH随加入酸(或碱)体积的变化如图。
下列说法不正确的是( )
A.由a点可知:NaHCO 溶液中HCO -的水解程度大于电离程度
3 3
B.a→b→c过程中:c(HCO -)+2c(CO2-)+c(OH-)逐渐减小
3 3
C.a→d→e过程中:c(Na+)<c(HCO -)+c(CO2-)+c(H CO)
3 3 2 3
D.令c点的c(Na+)+c(H+)= x,e点的c(Na+)+c(H+)=y,则x>y
6. (2020•江苏卷)室温下,将两种浓度均为0.1mol·L-1的溶液等体积混合,若溶液混合引起的体积变
化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是( )
A.NaHCO -Na CO 混合溶液(pH=10.30):NaHCO 溶液中:c(Na+)>c(HCO)>c(CO2-)>c(OH-)
3 2 3 3 3
B.氨水-NH Cl混合溶液(pH=9.25):c(NH)+ c(H+)= c(NH ∙HO)+c(OH-)
4 3 2
C.CHCOOH - CHCOONa混合溶液(pH=4.76):c(Na+)>c(CHCOOH)>c(CHCOO−)>c(H+)
3 3 3 3
D.HC O-NaHC O 混合溶液(pH=1.68,HC O 为二元弱酸):c(H+)+c(H C O)= c(Na+)+c(OH—)+
2 2 4 2 4 2 2 4 2 2 4
c(C O)
2