文档内容
第 08 讲 铝、镁及其重要化合物
第一部分:高考真题感悟
1.(2022·浙江·高考真题)下列物质对应的化学式不正确的是
A.氯仿:CHCl B.黄铜矿的主要成分:Cu S
3 2
C.芒硝:NaSO ·10H O D.铝土矿的主要成分:Al O
2 4 2 2 3
2.(2022·浙江·高考真题)下列说法不正确的是
A.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
B.高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明
C.氧化铝熔点高,常用于制造耐高温材料
D.用石灰石-石膏法对燃煤烟气进行脱硫,同时可得到石膏
3.(2021·浙江·高考真题)下列说法不正确的是
A.硅酸钠是一种难溶于水的硅酸盐
B.镁在空气中燃烧可生成氧化镁和氮化镁
C.钠与水反应生成氢氧化钠和氢气
D.常温下,铝遇浓硝酸或浓硫酸时会发生钝化
4.(2022·湖南·高考真题)铝电解厂烟气净化的一种简单流程如下:
下列说法错误的是
A.不宜用陶瓷作吸收塔内衬材料
B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有 和
D.滤液可回收进入吸收塔循环利用
5.(2022·海南·高考真题)依据下列实验,预测的实验现象正确的是
选项 实验内容 预测的实验现象
A 溶液中滴加NaOH溶液至过量 产生白色沉淀后沉淀消失
B 溶液变血红色
溶液中滴加KSCN溶液C AgI悬浊液中滴加NaCl溶液至过量 黄色沉淀全部转化为白色沉淀
D 酸性 溶液中滴加乙醇至过量 溶液紫红色褪去
第二部分:最新模拟精练
完卷时间:50分钟
可能用到的相对原子质量:C 12 Mg 24 Al 27 Br 80
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·上海松江·一模)等量的铝分别与100mL、2mol·L-1的盐酸与NaOH溶液反应产生氢气体积比为
6:7,则反应物的量的关系为
A.均恰好反应 B.酸过量 C.碱过量 D.酸、碱均过量
2.(2022·湖南常德·模拟预测)下列方法正确且涉及氧化还原反应的是
A.工业上电解熔融状态 制备 B.可用 试剂洗涤试管壁上的
C.利用单质 与 溶液制 D.用稀硝酸可除去试管壁上的
3.(2022·江苏·模拟预测)下列有关物质的性质与用途不具有对应关系的是
A.单质铝能导电,可用于制作导线 B. 熔点很高,可用于治炼金属铝
C. 有弱碱性,可用于治疗胃酸过多 D.明矾能水解形成胶体,可用于净水
4.(2021·广东惠州·一模)下列关于物质的制备、生产的说法正确的是
A.用镁粉和空气反应制备
B.工业制取金属铝:电解熔融
C.实验室制取NH :可用浓硫酸干燥
3
D. 溶液与浓 混合制备HI
5.(2022·湖南省桂东县第一中学二模)以混有 的 为原料制备氧化镁的实验流程如图:下列说法错误的是
A.酸浸的离子方程式为
B.浸出渣的成分是
C.母液的主要溶质是
D.固体X是
6.(2021·天津·三模)下列指定反应的离子方程式不正确的是
A.MgCl 溶液中加足量石灰乳:Mg2+(aq)+Ca(OH)(s)=Mg(OH) (s)+Ca2+(aq)
2 2 2
B.0.1mol·L-1CuSO 溶液中加入少量浓氨水:Cu2++2NH·H O=Cu(OH) ↓+2NH
4 3 2 2
C.向NaAlO 溶液中滴入足量Ca(HCO ) 溶液:AlO +HCO +H O=Al(OH) ↓+CO
2 3 2 2 3
D.向铝片中加入氢氧化钠溶液:2A1+2OH-+2H O=2AlO +3H ↑
2 2
7.(2022·河北唐山·三模)化学与生产、生活、社会密切相关。下列有关说法中正确的是
A.可用明矾使海水淡化来解决饮水危机
B.雾是一种气溶胶,能产生丁达尔现象
C.在日常生活中,造成钢铁腐蚀的主要原因是化学腐蚀
D.工业上运输浓硫酸可以使用铝制槽罐车,因为铝与浓硫酸常温下不反应
8.(2022·上海崇明·二模)核潜艇上的核反应堆使用液态铝钠合金作载热介质。有关说法中正确的是
A.该合金的熔点介于钠、铝之间
B.铝钠合金的良好传热性与自由电子有关
C.钠或铝形成的氧化物均为碱性氧化物
D.原子半径钠大于铝,金属键钠强于铝
9.(2022·上海崇明·二模)将足量的CO 不断通入NaOH、Ba(OH) 、NaAlO 的混合溶液中,生成沉淀的
2 2 2
物质的量与通入CO 的体积的关系可表示为
2A. B.
C. D.
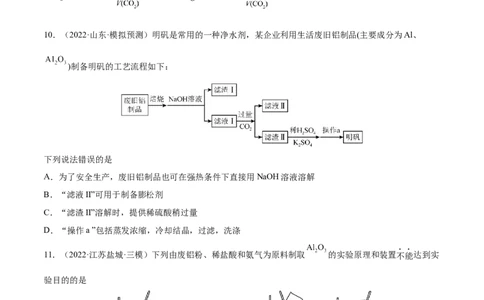
10.(2022·山东·模拟预测)明矾是常用的一种净水剂,某企业利用生活废旧铝制品(主要成分为Al、
)制备明矾的工艺流程如下:
下列说法错误的是
A.为了安全生产,废旧铝制品也可在强热条件下直接用NaOH溶液溶解
B.“滤液II”可用于制备膨松剂
C.“滤渣II”溶解时,提供稀硫酸稍过量
D.“操作a ”包括蒸发浓缩,冷却结晶,过滤,洗涤
11.(2022·江苏盐城·三模)下列由废铝粉、稀盐酸和氨气为原料制取 的实验原理和装置不能达到实
验目的的是
A.用装置甲溶解废铝粉 B.用装置乙制取 固体C.用装置丙过滤得到 固体 D.用装置丁灼烧 固体制得
12.(2022·江苏江苏·二模)反应2Al+Fe O 2Fe+Al O 可用于焊接钢轨。下列有关说法不正确的是
2 3 2 3
A.该反应吸收大量热 B.铝在反应中作还原剂
C.该反应属于置换反应 D.Al O 属于两性氧化物
2 3
二、主观题(共3小题,共40分)
13.(2021·浙江·模拟预测)(12分)某化合物 A 由两种元素组成,可以发生如下的转化。
已知∶标准状况下,气体B的密度是氢气的8倍;固体E既溶于NaOH溶液又可溶于稀硫酸。
请回答∶
(1)B的化学式是______
(2)组成A的元素有______
(3)请写出 A 与 NaOH溶液反应的化学方程式_______
14.(2022·四川德阳·三模)(15分)铝的阳极氧化是一种重要的表面处理技术,其原理是用电化学方法
处理铝件表面,优化氧化膜结构,增强铝件的抗腐蚀性,同时便于表面着色。取铝片模拟该实验,并测定
氧化膜厚度,操作步骤如下:
(1)铝片预处理
铝片表面除去油垢后,用2mol/LNaOH溶液在60~70℃下洗涤,除去铝表面薄氧化膜,离子方程式为:
_______;再用10%(质量分数)的HNO 溶液对铝片表面进行化学抛光。若取一定体积68%(质量分数)的浓
3
硝酸配制该化学抛光液,需要用到的玻璃仪器有_______、_______、玻璃棒和胶头滴管。
(2)电解氧化
取预处理过的铝片和铅做电极,控制电流恒定为0.06A,用直流电源在5~6mol/L硫酸中电解。其中铝片
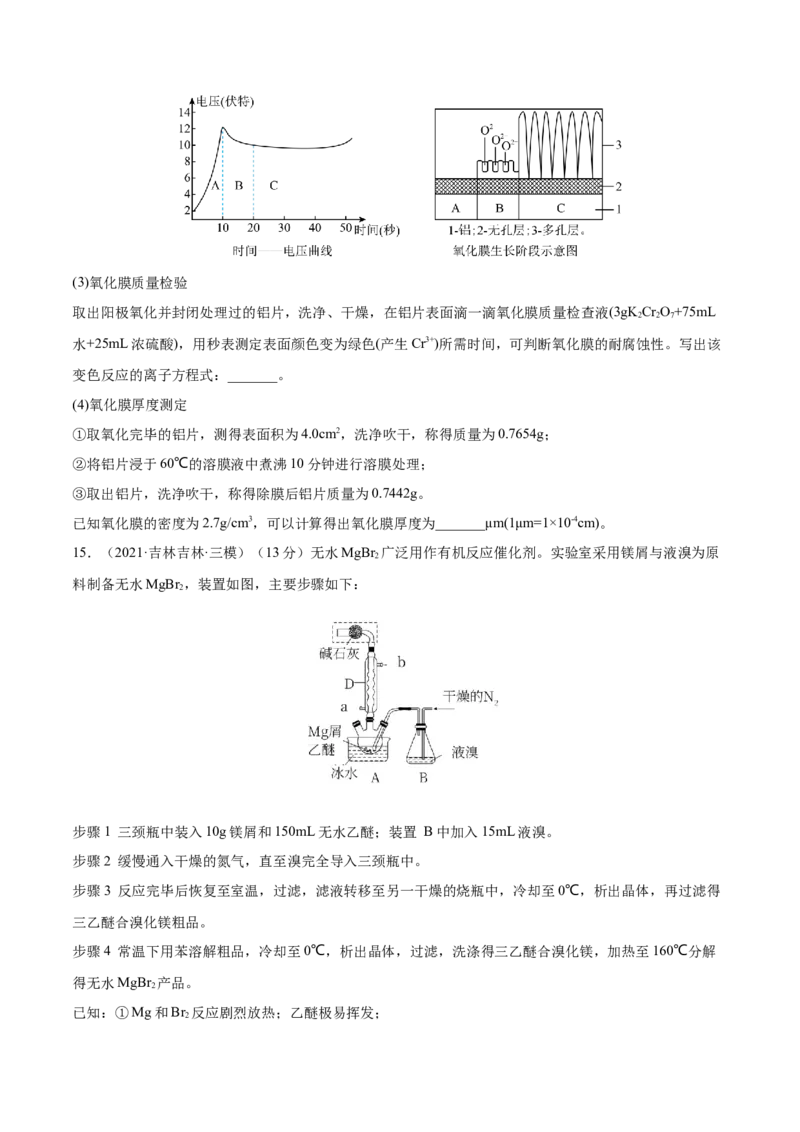
接电源_______极,产生氧化膜的电极反应式为氧化膜的生长过程可大致分为A、B、C三个阶段(如图所
示),C阶段多孔层产生孔隙的离子反应方程式为_____,A阶段电压逐渐增大的原因是_____。(3)氧化膜质量检验
取出阳极氧化并封闭处理过的铝片,洗净、干燥,在铝片表面滴一滴氧化膜质量检查液(3gK Cr O+75mL
2 2 7
水+25mL浓硫酸),用秒表测定表面颜色变为绿色(产生Cr3+)所需时间,可判断氧化膜的耐腐蚀性。写出该
变色反应的离子方程式:_______。
(4)氧化膜厚度测定
①取氧化完毕的铝片,测得表面积为4.0cm2,洗净吹干,称得质量为0.7654g;
②将铝片浸于60℃的溶膜液中煮沸10分钟进行溶膜处理;
③取出铝片,洗净吹干,称得除膜后铝片质量为0.7442g。
已知氧化膜的密度为2.7g/cm3,可以计算得出氧化膜厚度为_______μm(1μm=1×10-4cm)。
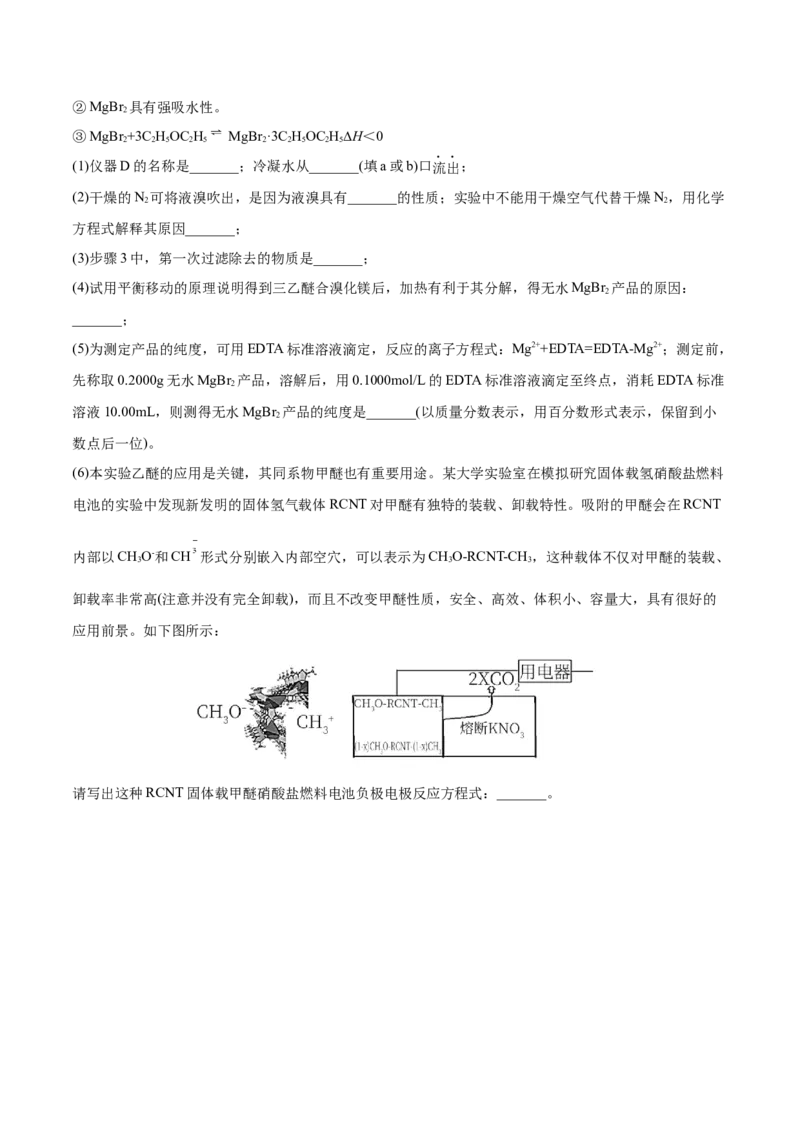
15.(2021·吉林吉林·三模)(13分)无水MgBr 广泛用作有机反应催化剂。实验室采用镁屑与液溴为原
2
料制备无水MgBr ,装置如图,主要步骤如下:
2
步骤1 三颈瓶中装入10g镁屑和150mL无水乙醚;装置 B中加入15mL液溴。
步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3 反应完毕后恢复至室温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得
三乙醚合溴化镁粗品。
步骤4 常温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解
得无水MgBr 产品。
2
已知:①Mg和Br 反应剧烈放热;乙醚极易挥发;
2②MgBr 具有强吸水性。
2
③MgBr +3C HOC H MgBr ·3C HOC H∆H<0
2 2 5 2 5 2 2 5 2 5
(1)仪器D的名称是_______;冷凝水从_______(填a或b)口流出;
(2)干燥的N 可将液溴吹出,是因为液溴具有_______的性质;实验中不能用干燥空气代替干燥N,用化学
2 2
方程式解释其原因_______;
(3)步骤3中,第一次过滤除去的物质是_______;
(4)试用平衡移动的原理说明得到三乙醚合溴化镁后,加热有利于其分解,得无水MgBr 产品的原因:
2
_______;
(5)为测定产品的纯度,可用EDTA标准溶液滴定,反应的离子方程式:Mg2++EDTA=EDTA-Mg2+;测定前,
先称取0.2000g无水MgBr 产品,溶解后,用0.1000mol/L的EDTA标准溶液滴定至终点,消耗EDTA标准
2
溶液10.00mL,则测得无水MgBr 产品的纯度是_______(以质量分数表示,用百分数形式表示,保留到小
2
数点后一位)。
(6)本实验乙醚的应用是关键,其同系物甲醚也有重要用途。某大学实验室在模拟研究固体载氢硝酸盐燃料
电池的实验中发现新发明的固体氢气载体RCNT对甲醚有独特的装载、卸载特性。吸附的甲醚会在RCNT
内部以CHO-和CH 形式分别嵌入内部空穴,可以表示为CHO-RCNT-CH ,这种载体不仅对甲醚的装载、
3 3 3
卸载率非常高(注意并没有完全卸载),而且不改变甲醚性质,安全、高效、体积小、容量大,具有很好的
应用前景。如下图所示:
请写出这种RCNT固体载甲醚硝酸盐燃料电池负极电极反应方程式:_______。