文档内容
第 19 讲 化学平衡
【化学学科素养】
变化观念与平衡思想:知道化学变化需要一定的条件,并遵循一定规律;认识化学变化有一定限度,
是可以调控的。能多角度、动态地分析化学反应,运用化学反应原理解决实际问题。
证据推理与模型认知:建立观点、结论和证据之间的逻辑关系;知道可以通过分析、推理等方法认识
化学平衡的特征及其影响因素,建立模型。能运用模型解释化学现象,揭示现象的本质和规律。
【必备知识解读】
一、化学平衡状态
1.化学平衡研究的对象——可逆反应
2.化学平衡状态
(1)概念
一定条件下的可逆反应,当反应进行到一定程度时,正反应速率和逆反应速率相等,反应物的浓度和
生成物的浓度不再改变,我们称为“化学平衡状态”,简称化学平衡。
(2)建立过程
在一定条件下,把某一可逆反应的反应物加入固定容积的密闭容器中。反应过程如下:
以上过程可用如图表示:
(3)平衡特点二、化学平衡移动
1.化学平衡移动的过程
原化学平衡状态
由上图可推知:
(1)化学反应条件改变,使正、逆反应速率不再相等,化学平衡才会发生移动。
(2)化学平衡发生移动,化学反应速率一定改变。
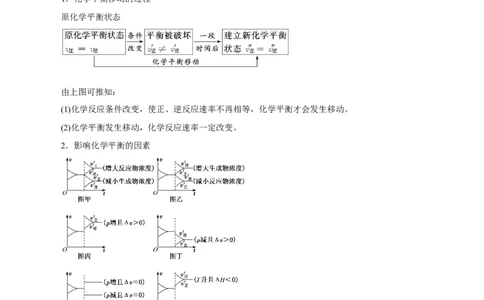
2.影响化学平衡的因素
(1)若其他条件不变,改变下列条件对化学平衡的影响
改变的条件(其他条件不变) 化学平衡移动的方向
浓度 增大反应物浓度或减小 向正反应方向移动,如图甲生成物浓度
减小反应物浓度或增大
向逆反应方向移动,如图乙
生成物浓度
增大压强 向气体分子总数减小的方向移动,如图丙
反应前后气
压强(对有
体体积改变
减小压强 向气体分子总数增大的方向移动,如图丁
气体参加
的反应) 反应前后气
改变压强 平衡不移动,如图戊
体体积不变
温度 升高温度 向吸热反应方向移动,如图己
降低温度 向放热反应方向移动,如图庚
催化剂 同等程度改变v 、v ,平衡不移动,如图辛
正 逆
【特别提醒】
压强对化学平衡的影响主要看改变压强能否引起反应物和生成物的浓度变化,只有引起物质的浓度变
化才会造成平衡移动,否则压强对平衡无影响。
(2)浓度的“决定性”作用
①恒温、恒容条件
原平衡体系――→体系总压强增大―→体系中各组分的浓度不变―→平衡不移动。
②恒温、恒压条件
原平衡体系――→容器容积增大,各反应气体的
3.化学平衡移动与化学反应速率的关系
v >v 平衡向正反应方向移动
正 逆
v =v 反应达到平衡状态,不发生平衡移动
正 逆
v <v 平衡向逆反应方向移动
正 逆
4.勒夏特列原理
如果改变影响化学平衡的条件之一(如温度、压强、以及参加反应的化学物质的浓度),平衡将向着能
够减弱这种改变的方向移动。
【特别提醒】
①由“化学平衡”可知:勒夏特列原理的适用对象是可逆过程。
②由“减弱”可知:只能减弱改变,而不能消除改变。
三、化学图像
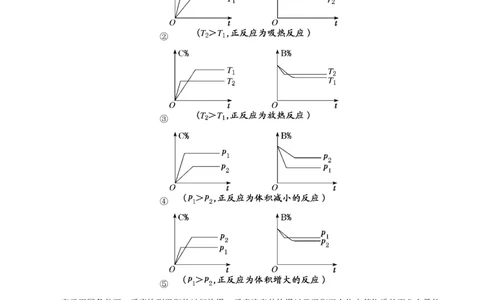
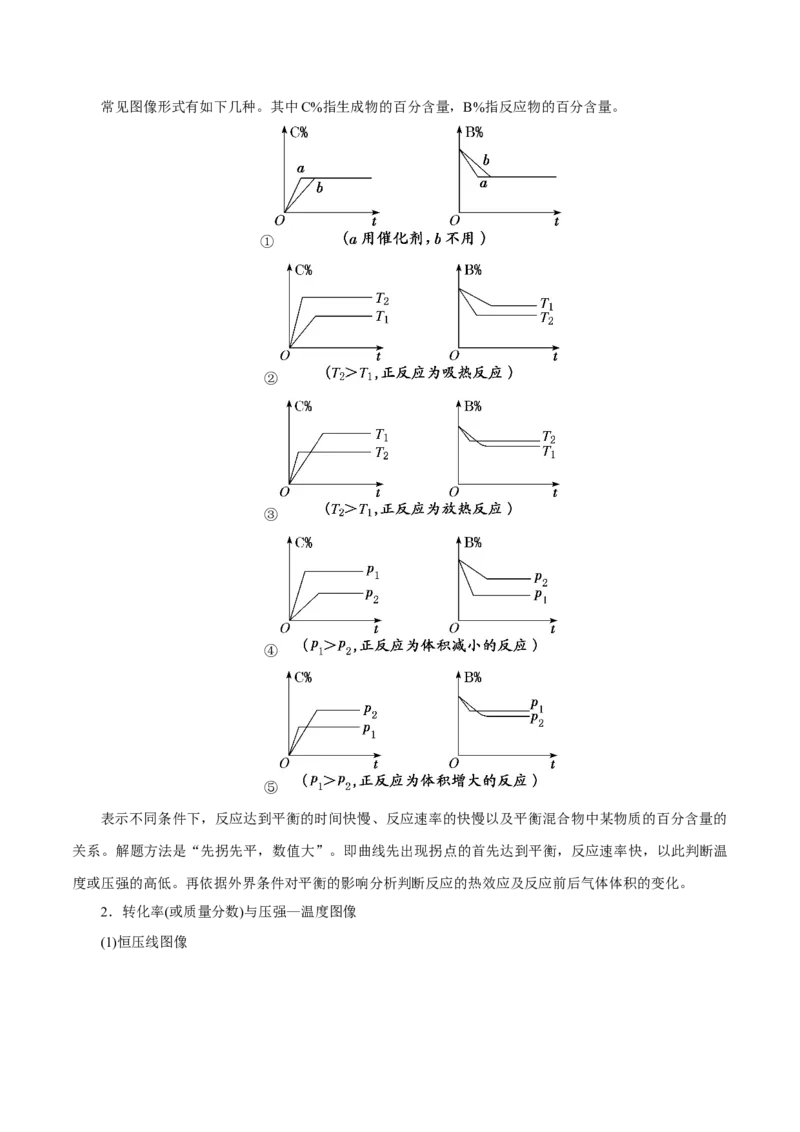
1.含量—时间—温度(压强)图像常见图像形式有如下几种。其中C%指生成物的百分含量,B%指反应物的百分含量。
①
②
③
④
⑤
表示不同条件下,反应达到平衡的时间快慢、反应速率的快慢以及平衡混合物中某物质的百分含量的
关系。解题方法是“先拐先平,数值大”。即曲线先出现拐点的首先达到平衡,反应速率快,以此判断温
度或压强的高低。再依据外界条件对平衡的影响分析判断反应的热效应及反应前后气体体积的变化。
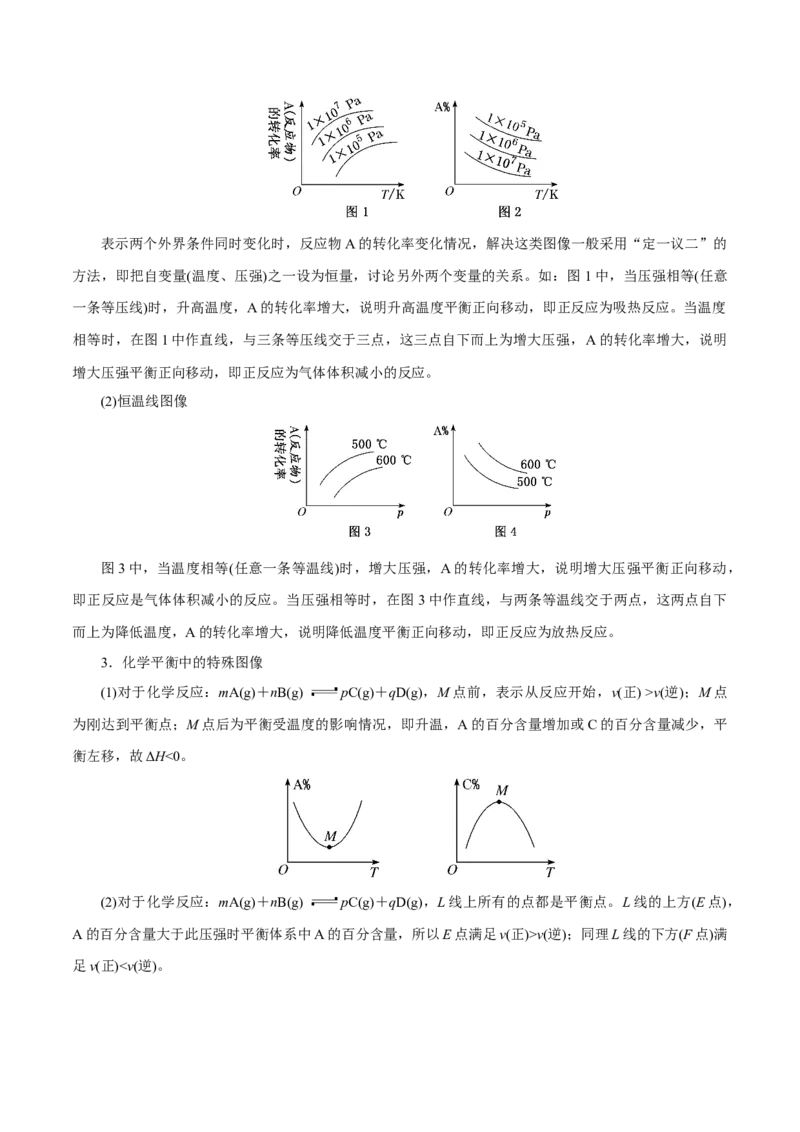
2.转化率(或质量分数)与压强—温度图像
(1)恒压线图像表示两个外界条件同时变化时,反应物A的转化率变化情况,解决这类图像一般采用“定一议二”的
方法,即把自变量(温度、压强)之一设为恒量,讨论另外两个变量的关系。如:图1中,当压强相等(任意
一条等压线)时,升高温度,A的转化率增大,说明升高温度平衡正向移动,即正反应为吸热反应。当温度
相等时,在图1中作直线,与三条等压线交于三点,这三点自下而上为增大压强,A的转化率增大,说明
增大压强平衡正向移动,即正反应为气体体积减小的反应。
(2)恒温线图像
图3中,当温度相等(任意一条等温线)时,增大压强,A的转化率增大,说明增大压强平衡正向移动,
即正反应是气体体积减小的反应。当压强相等时,在图3中作直线,与两条等温线交于两点,这两点自下
而上为降低温度,A的转化率增大,说明降低温度平衡正向移动,即正反应为放热反应。
3.化学平衡中的特殊图像
(1)对于化学反应:mA(g)+nB(g) pC(g)+qD(g),M点前,表示从反应开始,v(正) >v(逆);M点
为刚达到平衡点;M点后为平衡受温度的影响情况,即升温,A的百分含量增加或C的百分含量减少,平
衡左移,故ΔH<0。
(2)对于化学反应:mA(g)+nB(g) pC(g)+qD(g),L线上所有的点都是平衡点。L线的上方(E点),
A的百分含量大于此压强时平衡体系中A的百分含量,所以E点满足v(正)>v(逆);同理L线的下方(F点)满
足v(正)0,在其它条件不变的情况下, 升高温度、增大水蒸
4 2 2
气的浓度均能提高 CH 的平衡转化率
4
D.一定温度下, 恒容密闭容器中充入一定量 NO 发生反应:2NO NO 达到平衡后,再向容器中
2 2 2 4
充入一定量的 NO 并达到新的平衡, 则 NO 体积分数先增大后减小,但比原平衡小
2 2
【变式探究】下列事实不能用平衡移动原理解释的是
A.由 、 、 组成的平衡体系通过缩小体积加压后颜色变深
B.重铬酸钾溶液中存在: ,若滴加少量 溶液,溶
液由橙色变黄色
C.实验室用排饱和食盐水的方法收集D.开启啤酒瓶后,马上泛起大量泡沫