文档内容
训练(三十四) 化学反应速率及影响因素
1.(2021·宁夏银川检测)在2 L的密闭容器中发生以下反应:2A(g)+B(g) 2C(g)+
D(g),若最初加入的A和B都是4 mol,在前5 s内,A的平均反应速率为0.12 mol·L-1·s-1,则
5 s时容器中B的物质的量为( )
A.3.4 mol B.2.4 mol
C.2.8 mol D.1.2 mol
A [前5 s内,A的平均反应速率为0.12 mol·L-1·s-1,则B的反应速率为0.06 mol·L-
1·s-1,故5 s时容器中B的物质的量为4 mol-0.06 mol·L-1·s-1×5 s×2 L=3.4 mol。]
2.(2021·黑龙江哈尔滨六中检测)水煤气是一种绿色环保的气体燃料,极大的提高了煤
炭的燃烧效率。近年来研究推出以生活垃圾热解处理后的残渣为原料生产水煤气的技术工
艺,其主要反应为C(s)+HO(g) CO(g)+H(g)
2 2
ΔH>0。现将一定量的C(s)和水蒸气放在一密闭容器中进行上述反应,则下列有关说法
错误的是( )
A.其他条件不变,升高温度,反应速率增大
B.其他条件不变,将容器体积缩小一半,反应速率减小
C.恒容时,抽出少量H 使反应体系反应速率减小
2
D.其他条件不变,适当增加C(s)的质量,反应速率不变
B [其他条件不变,将容器体积缩小一半,反应混合物的浓度增大,反应速率加快,B项
错误;恒容时,抽出少量H,c(H )减小,反应速率减小,C项正确;碳是固体,增加C(s)的质量,
2 2
其浓度不变,反应速率不变,D项正确。]
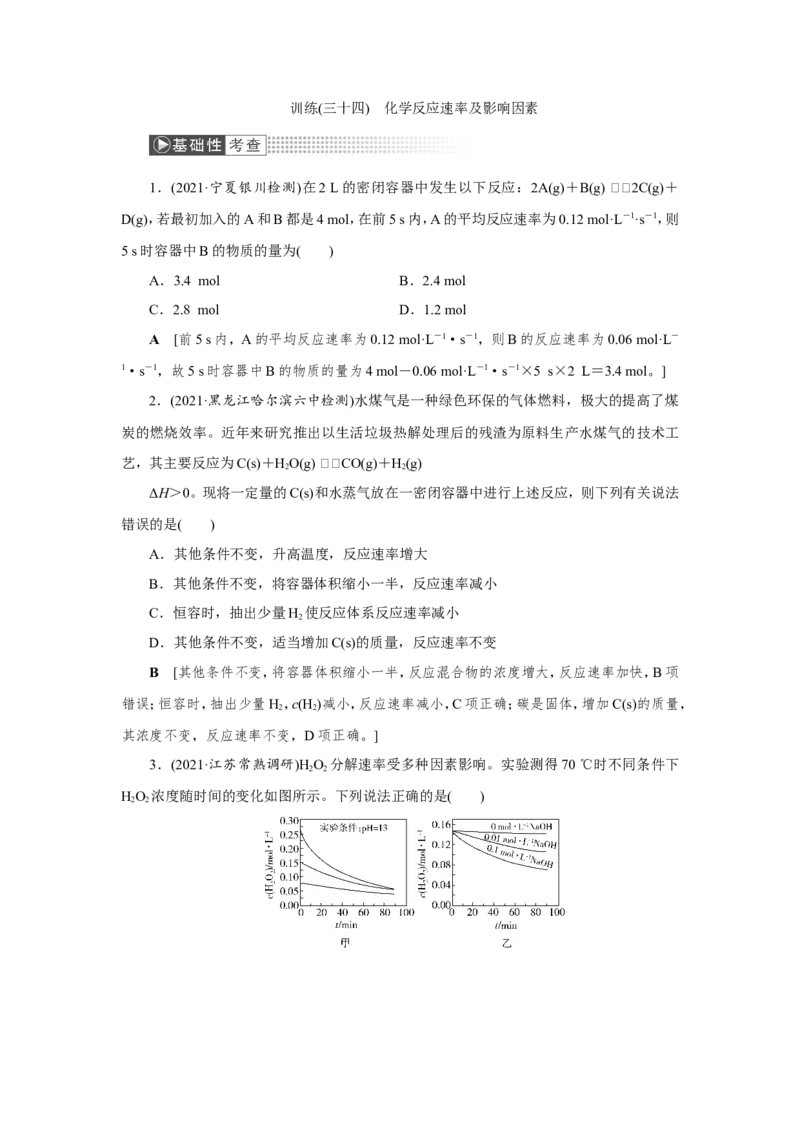
3.(2021·江苏常熟调研)HO 分解速率受多种因素影响。实验测得70 ℃时不同条件下
2 2
HO 浓度随时间的变化如图所示。下列说法正确的是( )
2 2A.图甲表明,其他条件相同时,HO 浓度越小,其分解速率越快
2 2
B.图乙表明,其他条件相同时,溶液pH越小,HO 分解速率越快
2 2
C.图丙表明,少量Mn2+存在时,溶液碱性越强,HO 分解速率越快
2 2
D.图丙和图丁表明,碱性溶液中,Mn2+对HO 分解速率的影响大
2 2
D [浓度对反应速率的影响是浓度越大,反应速率越快,A项错误;NaOH浓度越大,即
pH越大,HO 分解速率越快,B项错误;由图可知,Mn2+存在时,0.1 mol·L-1NaOH中HO
2 2 2 2
的分解速率比1.0 mol·L-1的NaOH中的快,C项错误;由图可知,碱性条件下,Mn2+存在时,
对HO 分解速率影响大,D项正确。]
2 2
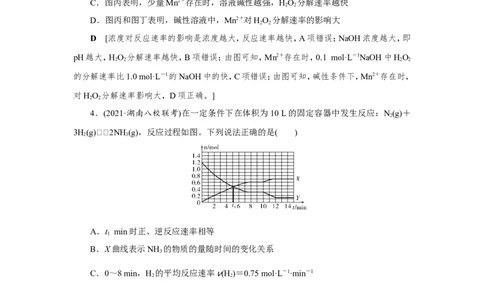
4.(2021·湖南八校联考)在一定条件下在体积为10 L的固定容器中发生反应:N(g)+
2
3H(g)2NH (g),反应过程如图。下列说法正确的是( )
2 3
A.t min时正、逆反应速率相等
1
B.X曲线表示NH 的物质的量随时间的变化关系
3
C.0~8 min,H
2
的平均反应速率 v(H
2
)=0.75 mol·L-1·min-1
D.10~12 min,N
2
的平均反应速率 v(N
2
)=0.25 mol·L-1·min-1
B [t 时刻没有达到平衡状态,正、逆反应速率不相等,A项错误;根据图像,单位时间内
1
X、Y变化量之比为2∶3对比反应的化学计量数,则X为NH 的曲线,B项正确;0~8 min时,
3
v(NH
3
)==0.007 5 mol·L-1·min-1,根据化学反应速率之比等于化学计量数之比得 v(H
2
)==0.011 25 mol·L-1·min-1,C项错误;10~12 min, v(NH
3
)==0.005 mol·L-1·min-1,则
v(N
2
)==0.002 5 mol·L-1·min-1,D项错误。]
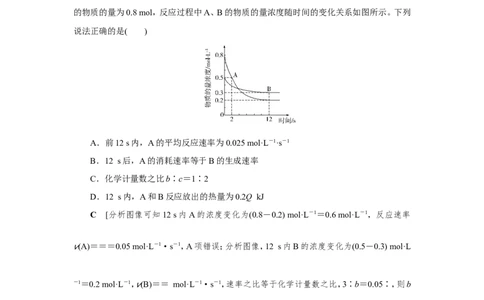
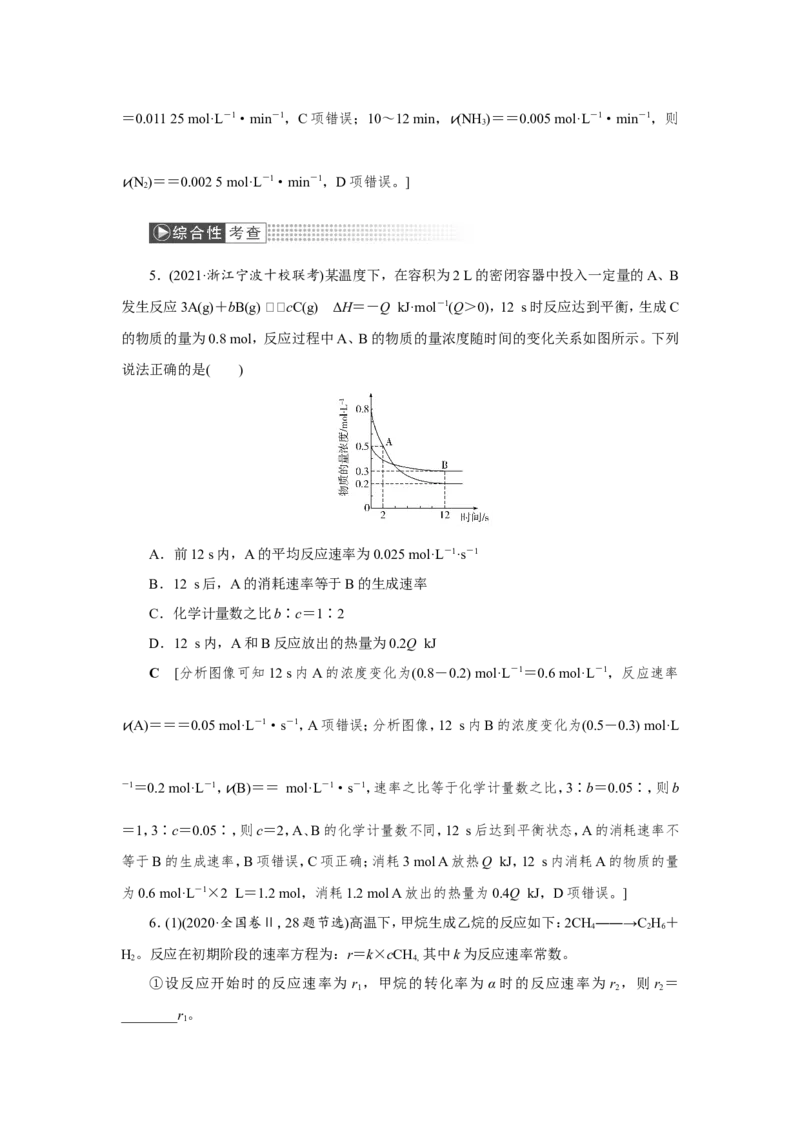
5.(2021·浙江宁波十校联考)某温度下,在容积为2 L的密闭容器中投入一定量的A、B
发生反应3A(g)+bB(g) cC(g) ΔH=-Q kJ·mol-1(Q>0),12 s时反应达到平衡,生成C
的物质的量为0.8 mol,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列
说法正确的是( )
A.前12 s内,A的平均反应速率为0.025 mol·L-1·s-1
B.12 s后,A的消耗速率等于B的生成速率
C.化学计量数之比b∶c=1∶2
D.12 s内,A和B反应放出的热量为0.2Q kJ
C [分析图像可知12 s内A的浓度变化为(0.8-0.2) mol·L-1=0.6 mol·L-1,反应速率
v(A)===0.05 mol·L-1·s-1,A项错误;分析图像,12 s内B的浓度变化为(0.5-0.3) mol·L
-1=0.2 mol·L-1, v(B)== mol·L-1·s-1,速率之比等于化学计量数之比,3∶b=0.05∶,则b
=1,3∶c=0.05∶,则c=2,A、B的化学计量数不同,12 s后达到平衡状态,A的消耗速率不
等于B的生成速率,B项错误,C项正确;消耗3 mol A放热Q kJ,12 s内消耗A的物质的量
为0.6 mol·L-1×2 L=1.2 mol,消耗1.2 mol A放出的热量为0.4Q kJ,D项错误。]
6.(1)(2020·全国卷Ⅱ,28题节选)高温下,甲烷生成乙烷的反应如下:2CH――→C H+
4 2 6
H。反应在初期阶段的速率方程为:r=k×cCH 其中k为反应速率常数。
2 4,
①设反应开始时的反应速率为 r ,甲烷的转化率为 α时的反应速率为 r ,则r =
1 2 2
________r。
1②对于处于初期阶段的该反应,下列说法正确的是________。
A.增加甲烷浓度,r增大
B.增加H 浓度,r增大
2
C.乙烷的生成速率逐渐增大
D.降低反应温度,k减小
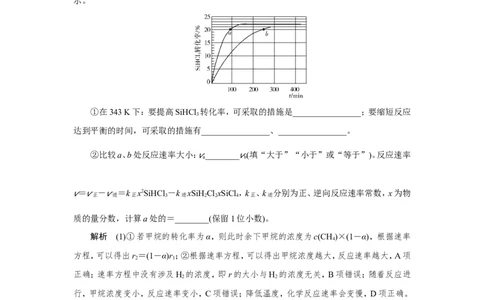
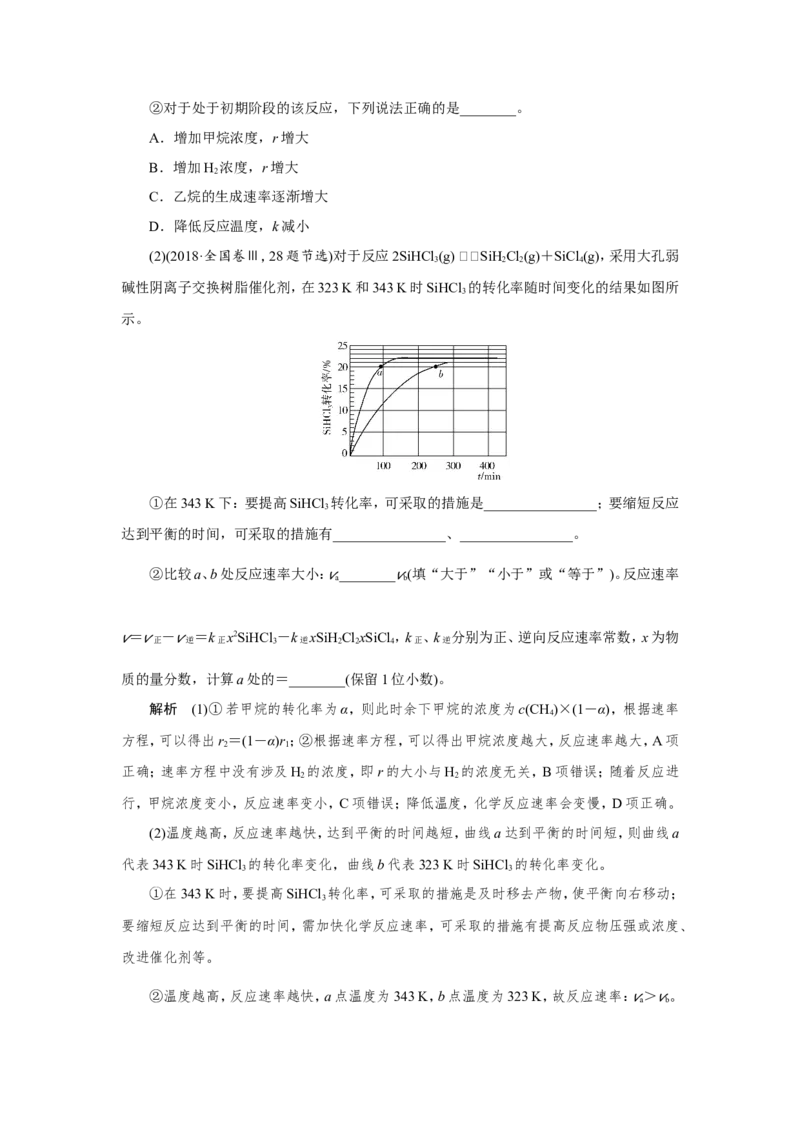
(2)(2018·全国卷Ⅲ,28题节选)对于反应2SiHCl (g) SiHCl(g)+SiCl (g),采用大孔弱
3 2 2 4
碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl 的转化率随时间变化的结果如图所
3
示。
①在343 K下:要提高SiHCl 转化率,可采取的措施是________________;要缩短反应
3
达到平衡的时间,可采取的措施有________________、________________。
②比较a、b处反应速率大小: va ________vb (填“大于”“小于”或“等于”)。反应速率
v = v正 - v逆 =k 正 x2SiHCl 3 -k 逆 xSiH 2 Cl 2 xSiCl 4 ,k 正 、k 逆 分别为正、逆向反应速率常数,x为物
质的量分数,计算a处的=________(保留1位小数)。
解析 (1)①若甲烷的转化率为α,则此时余下甲烷的浓度为c(CH)×(1-α),根据速率
4
方程,可以得出r=(1-α)r;②根据速率方程,可以得出甲烷浓度越大,反应速率越大,A项
2 1
正确;速率方程中没有涉及H 的浓度,即r的大小与H 的浓度无关,B项错误;随着反应进
2 2
行,甲烷浓度变小,反应速率变小,C项错误;降低温度,化学反应速率会变慢,D项正确。
(2)温度越高,反应速率越快,达到平衡的时间越短,曲线a达到平衡的时间短,则曲线a
代表343 K时SiHCl 的转化率变化,曲线b代表323 K时SiHCl 的转化率变化。
3 3
①在343 K时,要提高SiHCl 转化率,可采取的措施是及时移去产物,使平衡向右移动;
3
要缩短反应达到平衡的时间,需加快化学反应速率,可采取的措施有提高反应物压强或浓度、
改进催化剂等。
②温度越高,反应速率越快,a点温度为343 K,b点温度为323 K,故反应速率:
va
>
vb
。反应速率 v = v正 - v逆 =k 正 x2SiHCl 3 -k 逆 ·xSiH 2 Cl 2 ·xSiCl 4 ,则有 v正 =k 正 ·x2SiHCl 3 , v逆 =
k 逆 xSiH 2 Cl 2 ·xSiCl 4 ,343 K 下反应达到平衡状态时 v正 = v逆 ,即 k 正 x2SiHCl 3 =k
·xSiHCl·xSiCl ,此时SiHCl 的平衡转化率α=22%,经计算可得SiHCl 、SiHCl、SiCl
逆 2 2 4 3 3 2 2 4
的物质的量分数分别为0.78、0.11、0.11,则有k ×0.782=k ×0.112,=≈0.02。a处SiHCl 的
正 逆 3
平衡转化率α=20%,此时SiHCl 、SiHCl、SiCl 的物质的量分数分别为0.8、0.1、0.1,则有=
3 2 2 4
=·=0.02×≈1.3。
答案 (1)①1-α ②AD
(2)①及时移去产物 改进催化剂 提高反应物压强(浓度) ②大于 1.3