文档内容
第一讲 物质的量 气体摩尔体积
一、选择题
1、(2023·全国甲卷)N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A.0.5mol异丁烷分子中共价键的数目为6.5N
A
B.标准状况下,22.4L SO 中电子的数目为4.00 N
3 A
C.1.0L pH = 2的 HSO 溶液中H+的数目为0.02N
2 4 A
D.1.0L 1.0mol/L 的NaCO 溶液中CO2-的数目为1.00 N
2 3 3 A
【答案】A
【解析】异丁烷的结构式为 ,烷烃的共价键的数目符合3n+1(n:碳原子数),0.5mol异丁烷的共
3
价键为0.5×(3×4+1)×N = 6.5N ,故A正确;标准状况下,SO 的状态固态,SO 的粒子个数、电子数不
A A 3 3
可求,故B错误;pH=2 的HSO ,C(H+)=10-2mol/L 1.0L的N(H+)= 10-2mol/L ×1.0L ×N = 10-2N ,故C错误;
2 4 A A
NaCO 溶液中CO2-要发生水解,水解程度未知,粒子个数不可求,故D错误。
2 3 3
2、(2023·渭南市一模)近日,中科院上海高研院在二氧化碳电催化转化研究中取得重要进展。通过调控
的孔道结构和表面活性位构型,成功实现了直接转化生成乙醇。用 表示阿伏加德罗常数的值,
下列说法正确的是
的
A. 标准状况下,5.6L CO 中所含电子 数目为4N
2 A
B. 25℃时,CHOH所含共价键的数目为8N
2 5 A
C. 0.1mol乙醇和0.2mol乙酸发生酯化反应,最多可生成0.1N 乙酸乙酯
A
D. CO 电催化过程中,每生成 乙醇,转移电子的数目为
2
【答案】D
【解析】A.标准状况下 5.6L CO 的物质的量为 mol,1mol CO 中含
2 2
(6+8+8)mol=22mol电子,所以标准状况下5.6L CO 中含电子的数目为5.5 N,A错误;B.不确定乙醇的
2 A
资料整理【淘宝店铺:向阳百分百】物质的量,不能计算其共价键数目,B错误;C.乙醇和乙酸发生的酯化反应是可逆反应,不能进行到底,
生成小于0.1 N 乙酸乙酯,C错误;D.电催化过程中由CO 生成乙醇的过程中碳元素由+4价降低到-2价,
A 2
所以每生成1mol乙醇,转移电子的数目为12 N,D正确。答案选D。
A
3.(2023.咸阳一模)N 代表阿伏加德罗常数的值。下列说法正确的是
A
A.18g H 18O含有的中子数为10N
2 A
B.22.4L乙烯和乙烷的混合气体中所含的分子数为N
A
C.2mol NO与1mol O 在密闭容器中充分反应后的分子数小于2N
2 A
D.在1L 0.1mol/L的Na CO 溶液中,由于水解导致溶液中阴离子总数小于0.1N
2 3 A
【答案】C
【详解】A.1个H 18O中含有中子数=18-8=10,18g H 18O的物质的量小于1mol,所以18g H 18O含有的中
2 2 2
子数小于10N ,A错误;B.未说明标准状况,无法利用标况下的气体摩尔体积计算器分子数,B错误;
A
C.2mol NO与1mol O 在密闭容器中发生反应2NO + O =2NO ,产物的分子数为2N ,但同时存在平衡
2 2 2 A
2NO 2 ⇌ N 2 O 4 ,所以分子数小于,C正确;D.Na 2 CO 3 溶液中的水解方程式CO 3 2-+ H 2 O ⇌ HCO 3 - +OH-,消耗
1mol碳酸根时生成2mol阴离子,故阴离子总数大于0.1N ,D错误;答案选C。
A
4、(2021·全国卷Ⅱ)N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A.18 g重水(D O)中含有的质子数为10N
2 A
B.3 mol的NO 与HO完全反应时转移的电子数为4N
2 2 A
C.32 g环状S( )分子中含有的S—S键数为1N
8 A
D.1 L pH=4的0.1 mol·L-1 KCr O 溶液中Cr O离子数为0.1N
2 2 7 2 A
【答案】C
【解析】重水的摩尔质量是20 g·mol-1,1 mol重水中含有10 mol质子,所以18 g重水中含有的质子数为
×10×N mol-1=9N ,A错误;NO 与HO反应的化学方程式为3NO +HO===2HNO +NO,则3 mol NO
A A 2 2 2 2 3 2
与HO完全反应时转移的电子数为2N ,B错误;1 mol S 分子中含有8 mol S—S键,32 g S 分子中含有的
2 A 8 8
S—S键数为×8×N
A
mol-1=1N
A
,C正确;由于K
2
Cr
2
O
7
溶液中存在Cr
2
O+H
2
O ⇌2CrO+2H+平衡,1 L pH
=4的0.1 mol·L-1KCr O 溶液中Cr O离子数小于0.1N ,D错误。
2 2 7 2 A
5.(2023.联盟统考题)N 是阿伏加德罗常数的值。下列说法正确的是( )
A
A.3.9g NaO 固体中含阴、阳离子的总数为0.2N
2 2 A
B.标准状况下,4.48L SO 和足量O 反应,生成的 SO 分子数目为0.2N
2 2 3 A
C.常温常压下,28g乙烯与丙烯的混合物所含的原子数目为6N
A
D.2mol苯中含有碳碳双键的数目为6N
A
【答案】C
资料整理【淘宝店铺:向阳百分百】【解析】A 项, NaO 由 Na+与 O2- 组成,3.9g NaO 的物质的量为 0.05mol,离子的物质的量为
2 2 2 2 2
0.05mol×3=0.15mol,故A错;B项,SO 与O 的反应为可逆反应,生成的分子个数不可求,故A错;;C
2 2
项,乙烯与丙烯的最简式相同均为CH ,可用最简式进行计算,n(CH2)=28g÷14g/mol =2mol,N原子
2
=2mol×3N =6N 不正确;C项正确,苯环中不存在碳碳双键,故D错。
A A
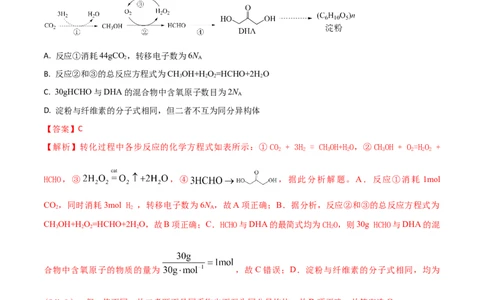
6. 我国在国际上首次实现了二氧化碳到淀粉的从头合成,其中部分核心反应如图所示。设 N 为阿伏加德
A
罗常数的值,下列说法错误的是
A. 反应①消耗44gCO,转移电子数为6N
2 A
B. 反应②和③的总反应方程式为CHOH+H O=HCHO+2H O
3 2 2 2
C. 30gHCHO与DHA的混合物中含氧原子数目为2N
A
D. 淀粉与纤维素的分子式相同,但二者不互为同分异构体
【答案】C
【解析】转化过程中各步反应的化学方程式如表所示:① CO + 3H = CHOH+HO,②CHOH + O=HO +
2 2 3 2 3 2 2 2
HCHO,③ ,④ ,据此分析解题。A.反应①消耗 1mol
CO ,同时消耗3mol H ,转移电子数为6N ,故A项正确;B.据分析,反应②和③的总反应方程式为
2 2 A
CHOH+H O=HCHO+2H O,故B项正确;C.HCHO与DHA的最简式均为CHO,则30g HCHO与DHA的混
3 2 2 2 2
合物中含氧原子的物质的量为 ,故C错误;D.淀粉与纤维素的分子式相同,均为
(CH O),但n值不同,故二者既不是同系物也不互为同分异构体,故D项正确;故答案选C 。
6 10 5 n
7.(2021·浙江6月选考)设N 为阿伏加德罗常数的值,下列说法不正确的是( )
A
A.标准状况下,1.12 L18O 中含有中子数为N
2 A
B.31 g P (分子结构: )中的共价键数目为1.5N
4 A
C.100 mL 0.1 mol·L-1的NaOH水溶液中含有氧原子数为0.01N
A
D.18.9 g三肽C H NO(相对分子质量:189)中的肽键数目为0.2N
6 11 3 4 A
【答案】C
资料整理【淘宝店铺:向阳百分百】【解析】A项,每个18O 中含有20个中子,标准状况下1.12 L18O 的物质的量为0.05 mol,含有中子数为
2 2
0.05×20N =N ,正确;B项,每个P 分子中含有6个共价键,31 g P 的物质的量为0.25 mol,含有共价键
A A 4 4
的数目为0.25×6N =1.5N ,正确;C项,溶液中除溶质NaOH中含氧原子,溶剂HO中也含有氧原子,故
A A 2
溶液中含氧原子数大于0.01N ,不正确;D项,每个该三肽分子中含有2个肽键,18.9 g该三肽的物质的
A
量为0.1 mol,含有肽键数目为0.2N ,正确。
A
8、设N 为阿伏伽德罗常数的值,下列说法错误的是
A
A.50 g质量分数为46%的乙醇水溶液中氧原子数为0.5N
A
B.标准状况下,10.4 g苯乙烯中,含有的碳碳双键总数为0.1N
A
C.0.5 mol C H 和C H O 的混合物完全燃烧,消耗O 分子数目为1.5N
2 4 3 4 2 2 A
D、一定条件下1 mol乙醇与1 mol乙酸充分反应生成的乙酸乙酯分子数小于N
A
【答案】A
【详解】A.在50g46%的乙醇溶液中,乙醇含有的O原子的物质的量n= =0.5mol,而乙醇溶液中
除了乙醇外,水也含O原子,则水中含有的O原子的物质的量n= =1.5mol,故此溶液中共含
O原子为2mol,即2N 个,故A错误;B.标准状况下,10.4g苯乙烯分子中,含有的碳碳双键总数为:
A
×N mol-1=0.1N ,故B正确;C.0.5 mol C H 和C H O (可看做C H •H O)混合物完全燃烧,消
A A 2 4 3 4 2 2 4 2
耗O 分子数目为1.5N ,故C正确;D.乙醇和乙酸的酯化反应为可逆反应,反应物不能完全转化为生成物,
2 A
一定条件下1 mol乙醇与1 mol乙酸充分反应生成的乙酸乙酯分子数小于N ,故D正确;故选A。
A
9、(改编)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A. 1mol苯分子中含碳碳双键的数目为3N
A
B. 14gCO和N 的混合物中含有的质子数为7N
2 A
C. 标准状况下,22.4L CHCl 分子中所含Cl原子数为3N
3 A
D. 0.1mol H 和0.1mol I 于密闭容器中充分反应,转移的电子总数为0.2N
2 2 A
【答案】B
【解析】A.苯分子中的碳碳键是介于碳碳单键和碳碳双键之间的特殊的化学键,苯中不含有碳碳双键,A
错误;B.1个CO和1个N 分子中均含有14个质子,CO、N 的摩尔质量均为28g/mol,所以14gCO和N
2 2 2
资料整理【淘宝店铺:向阳百分百】的混合物中含有的质子数为 ,B正确;C.标准状况下,CHCl 不是气体,
3
无法计算22.4L CHCl 的物质的量及所含C1原子数,C错误;D.H 和I 的反应H(g)+I (g) 2HI(g)为可
3 2 2 2 2
逆反应,0.1molH 和0.1molI 不能全部反应,则转移的电子总数小于0.2N ,D错误;故选B。
2 2 A
10、(2023. 成都市第二次模拟) 设N 表示阿伏加德罗常数值,下列叙述一定正确的是
A
A. 28g14CO中含有中子数为14N
A
B. 1mol O 与一定量甲烷反应转移电子数目为4N
2 A
C. 1L浓度为0.1 mol∙L−1NaCO 溶液中阴离子数目为0.1N
2 3 A
D. 28g C H 和C H 混合物中含有共用电子对数目6N
2 4 3 6 A
【答案】D
【解析】A.28g 14CO中含有中子数为 ,故A错误;B.1mol O 与一
2
定量甲烷反应,甲烷若量很少,则转移电子数目小于4N ,故B错误;C.1L浓度为0.1 mol∙L−1NaCO 溶
A 2 3
液中碳酸钠物质的量为0.1mol,由于碳酸根水解生成碳酸氢根和氢氧根,则阴离子数目大于0.1N ,故C
A
错误;D.28g C H 和C H 混合物,若全部是乙烯,则含有共用电子对数目 ,
2 4 3 6
若是C H ,则含有共用电子对数目 ,共用电子数目相同,故D正确。综上所述,
3 6
答案为D。
11、(2023 成都市蓉城名校联盟第二次联考)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A. 0.25 mol∙L−1NH Cl溶液中,NH +的数目为0.25N
4 4 A
B. 2.24LN 与足量H 充分反应后,生成NH 的数目为0.2N
2 2 3 A
C. 0.2mol环氧乙烷( )中,含有共价键总数为1.4N
A
D. 2molCH 与足量Cl 在光照条件下充分反应后,生成CHCl的数目为2N
4 2 3 A
【答案】C
【解析】A.0.25 mol·L-1NH Cl溶液,体积未知,无法计算NH +的数目,故A错误;B.2.24LN 与足量H
4 4 2 2
充分反应后,不清楚是否在标准状况下,无法计算氮气物质的量,而且氮气和氢气反应是可逆反应,因此
资料整理【淘宝店铺:向阳百分百】生成NH 的数目也无法计算,故B错误;C.环氧乙烷( )中含有4个碳氢键,2个碳氧键,1个碳碳
3
键,因此0.2mol环氧乙烷( )中,含有共价键总数为1.4N ,故C正确;D.甲烷和氯气反应是一系列
A
的反应,产物有一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳,则生成CHCl的数目小于2N ,故D错误。
3 A
综上所述,答案为C。
12.(2023 泸州市第二次诊断性考试)N 为阿伏加德罗常数的值。下列说法正确的是
A
A. 18gH 18O中含有的质子数为10N
2 A
B. 1mL2mol/LH PO 溶液中H+离子数小于0.002N
3 4 A
C. 2.3g钠用铝箔包裹与足量水反应,生成H 分子数为0.05N
2 A
D. 标准状况下,2.24L乙烯与Br 完全反应,断裂共价键总数为0.1N
2 A
【答案】B
【解析】A.H18O的摩尔质量为20g/mol,18gH18O为0.9mol,含有的质子数为9N ,A错误;B.磷酸为
2 2 A
弱酸,不能完全电离,1mL2mol/LH PO 溶液含有磷酸的物质的量为 0.002mol,电离产生的氢离子小于
3 4
0.002mol,B正确;C.铝箔能与钠和水的反应产物氢氧化钠反应放氢气,因此生成氢气的分子数大于
0.05N ,C错误;D.标准状况下2.24L乙烯为0.1mol,与溴单质完全反应,乙烯和溴单质中的共价键都会
A
断裂,断裂共价键的数目不是0.1mol,D错误;故选B。
13、利用电催化实现CO 到C HOH的转化,反应原理:6H+2CO C HOH+3H O。设N 为阿伏加德罗
2 2 5 2 2 2 5 2 A
常数的值,下列有关说法正确的是
A. 11.2L CO 中含分子的数目为0.5 N B. 23gC HOH中含共价键的数目为4 N
2 A 2 5 A
C. 生成1 mol C HOH转移电子的数目为8 N D. 4gH 与4gD 所含中子的数目相差N
2 5 A 2 2 A
【答案】B
【解析】A.没有明确是否是标准状况,所以无法通过体积求出二氧化碳所含分子数目,A错误;B.
C HOH的结构式为 ,则23gC HOH中含共价键的数目为 =4 N ,B正确;
2 5 2 5 A
C.根据上述方程式可知,生成1 mol C HOH,转移的电子数为 =12 N ,C错误;D.
2 5 A
H 无中子,4gD 的中子数为 =2N ,所以4gH 与4gD 所含中子的数目相差2N ,D错误;
2 2 A 2 2 A
资料整理【淘宝店铺:向阳百分百】故选B。
14. (2023.北京市昌平区第二次统考)N 表示阿伏伽德罗常数的值。下列说法正确的是
A
A.1 mol/L的H SO 溶液中含2 N 个H+ B.46g NO 所含氧原子数为 N
2 4 A 2 A
C.1mol 中含 键的个数为10 N D.22.4 L O 的分子个数为 N
A 2 A
【答案】10.C
【详解】A.没有给定溶液的体积,无法计算所含有H+的数目,选项A错误;B.46gNO 中含有1molNO ,
2 2
含有2mol氧原子,含有氧原子数为2N ,选项B错误;C. 中含有2个C-C键,1个C=C、一个C-N、
A
一个C=N、5个C-H,故所含有的 键为10个,故1mol 中含 键的个数为10O ,选项C正确;D.没
2
有说明标准状况下,22.4 L O 的物质的量不一定为1mol,故分子个数不一定为O ,选项D错误;答案选
2 2
C。
15、(2023.广州一模)2021年,我国科学家利用CO 为原料人工合成淀粉,合成过程中发生反应:
2
,设N 为阿伏伽德罗常数,下列有关说法正确的是
A
A.17g H O 分子中含有 键数目为1.5N B.标况下,22.4L CH OH中含有的羟基数为N
2 2 A 3 A
C.反应过程中HCHO为还原产物 D.1mol O 参与反应转移电子数为4N
2 A
【答案】A
【详解】A.17g H O 的物质的量为0.5mol,每个分子含有3个 键,故17克过氧化氢分子中含有 键数
2 2
目为1.5N ,A正确;B.标况下甲醇不是气体,不能使用气体摩尔体积进行计算,B错误;C.该反应中氧
A
气为氧化剂,甲醇为还原剂,甲醛为氧化产物,C错误;D.该反应中1mol氧气反应转移2mol电子,D错
误;故选A。
16、(2023.汕头市二模)工业上制备硫酸的流程: ,设
为阿伏伽德罗常数,下列有关说法正确的是
A. 中 的未成对电子数目为6
资料整理【淘宝店铺:向阳百分百】B. 的中心原子孤对电子数为1,其空间构型为V型
C.标准状况下,22.4L 中含有氧原子数目为
D. 作催化剂,能降低该反应的活化能,提高 的平衡转化率
【答案】B
【详解】A.Fe2+的电子排布式为1s22s22p63s23p63d6,未成对电子数目为4,故A错误;B.SO2的中心原子
价层电子对数为 ,孤对电子数为1,其空间构型为V型;故B正确;C.标准状况下SO 为液
3
态,所以22.4LSO 的物质的量大于1mol,所以含有氧原子数目大于为3N ,故C错误;D.V O 作催化剂,
3 A 2 5
能降低该反应的活化能,但不能提高SO 的平衡转化率;故D错误;故答案选B。
2
二、填空题
17.标准状况下,在乙室中充入1.2 mol HCl,甲室中充入NH 、H 的混合气体,静止时活塞如图。已知甲
3 2
室中气体的质量比乙室中气体的质量少33.8 g。
请回答下列问题:
(1)甲室中气体的物质的量为______________________ mol。
(2)甲室中气体的质量为____________ g。
(3)甲室中NH 、H 的物质的量之比为____________,质量之比为____________。
3 2
(4)如果将活塞a去掉,当HCl与NH 完全反应后,活塞b将静止于刻度“____________”(填数字)处。
3
【答案】(1)2 (2)10 (3)1∶4 17∶8 (4)6
【解析】(1)由题图可知甲、乙两室气体的体积之比为5∶3,故其物质的量之比也为5∶3,所以甲室中气体为
2 mol。(2)HCl气体的质量为1.2 mol ×36.5 g·mol-1=43.8 g,则甲室中气体的质量为43.8 g -33.8 g =10
g。(3)设氨气的物质的量为x,氢气的物质的量为y,可得
解得x=0.4 mol,y=1.6 mol,所以氨气和氢气的物质的量之比=0.4 mol ∶1.6 mol =1∶4,其质量之比=
1×17∶4×2=17∶8。(4)甲室中NH 的物质的量为0.4 mol,能与0.4 mol HCl反应,剩余气体为2.4 mol,相同
3
条件下,气体的体积之比等于其物质的量之比,所以活塞b会移至“6”处。
资料整理【淘宝店铺:向阳百分百】18、某中学有甲、乙两个探究性学习小组,他们拟用小颗粒的铝铜合金与足量的稀硫酸反应测定通常状况
(约20 ℃、1.01×105 Pa)下的气体摩尔体积(V )。
m
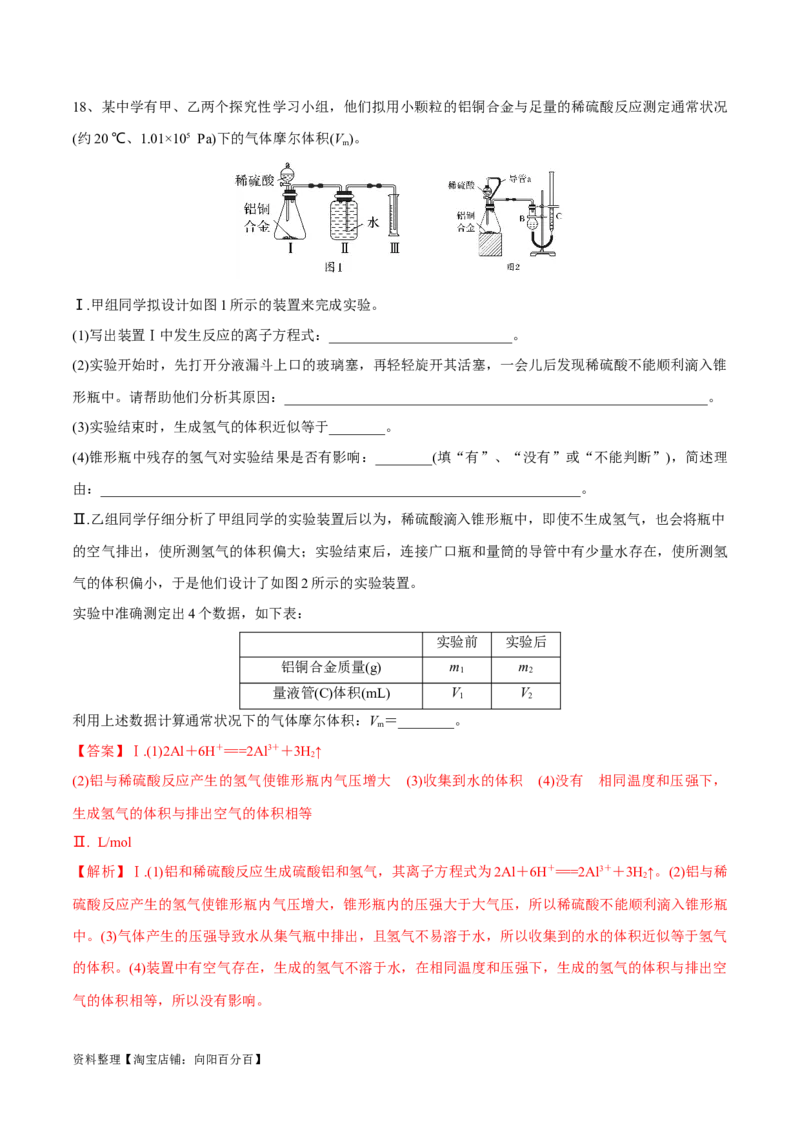
Ⅰ.甲组同学拟设计如图1所示的装置来完成实验。
(1)写出装置Ⅰ中发生反应的离子方程式:__________________________。
(2)实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻旋开其活塞,一会儿后发现稀硫酸不能顺利滴入锥
形瓶中。请帮助他们分析其原因:____________________________________________________________。
(3)实验结束时,生成氢气的体积近似等于________。
(4)锥形瓶中残存的氢气对实验结果是否有影响:________(填“有”、“没有”或“不能判断”),简述理
由:____________________________________________________________________。
Ⅱ.乙组同学仔细分析了甲组同学的实验装置后以为,稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶中
的空气排出,使所测氢气的体积偏大;实验结束后,连接广口瓶和量筒的导管中有少量水存在,使所测氢
气的体积偏小,于是他们设计了如图2所示的实验装置。
实验中准确测定出4个数据,如下表:
实验前 实验后
铝铜合金质量(g) m m
1 2
量液管(C)体积(mL) V V
1 2
利用上述数据计算通常状况下的气体摩尔体积:V =________。
m
【答案】Ⅰ.(1)2Al+6H+===2Al3++3H↑
2
(2)铝与稀硫酸反应产生的氢气使锥形瓶内气压增大 (3)收集到水的体积 (4)没有 相同温度和压强下,
生成氢气的体积与排出空气的体积相等
Ⅱ. L/mol
【解析】Ⅰ.(1)铝和稀硫酸反应生成硫酸铝和氢气,其离子方程式为2Al+6H+===2Al3++3H↑。(2)铝与稀
2
硫酸反应产生的氢气使锥形瓶内气压增大,锥形瓶内的压强大于大气压,所以稀硫酸不能顺利滴入锥形瓶
中。(3)气体产生的压强导致水从集气瓶中排出,且氢气不易溶于水,所以收集到的水的体积近似等于氢气
的体积。(4)装置中有空气存在,生成的氢气不溶于水,在相同温度和压强下,生成的氢气的体积与排出空
气的体积相等,所以没有影响。
资料整理【淘宝店铺:向阳百分百】V = L/mol。
m
资料整理【淘宝店铺:向阳百分百】