文档内容
训练(十七) 碳、硅及其重要化合物
1.(2021·湖北沙市中学检测)改革开放40多年以来,我国的“科学技术”取得了令人瞩
目的成就。下列有关材料的说法不正确的是( )
A.5G芯片“巴龙5000”的主要材料是SiO
2
B.“玉兔二号”的太阳能电池帆板的材料是高纯硅
C.光导纤维传导光的能力很强,是非常好的通信材料
D.碳化硅陶瓷耐高温且不易传热,可用于制造柴油机
A [5G芯片“巴龙5000”的主要材料是Si,A项错误;太阳能电池帆板的主要材料是
高纯硅,B项正确;光导纤维的主要成分是SiO,传导光的能力很强,是非常好的通信材料,C
2
项正确;碳化硅陶瓷耐高温且不易传热,可作耐高温材料,用于制造柴油机等,D项正确。]
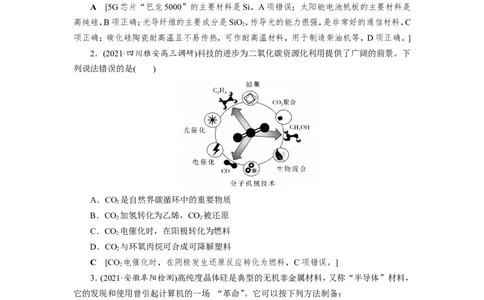
2.(2021·四川雅安高三调研)科技的进步为二氧化碳资源化利用提供了广阔的前景。下
列说法错误的是( )
A.CO 是自然界碳循环中的重要物质
2
B.CO 加氢转化为乙烯,CO 被还原
2 2
C.CO 电催化时,在阳极转化为燃料
2
D.CO 与环氧丙烷可合成可降解塑料
2
C [CO 电催化时,在阴极发生还原反应转化为燃料,C项错误。]
2
3.(2021·安徽阜阳检测)高纯度晶体硅是典型的无机非金属材料,又称“半导体”材料,
它的发现和使用曾引起计算机的一场 “革命”。它可以按下列方法制备:
SiO――→Si(粗)――→SiHCl ――→Si(纯)
2 3
下列说法正确的是( )
A.步骤①的化学方程式为SiO+C=====Si+CO↑
2 2
B.灼烧熔融的NaCO 固体,可用石英坩埚
2 3
C.二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应
D.反应①③中硅元素均被还原
D [步骤①中焦炭过量,反应生成Si和CO,A项错误;石英坩埚中含有SiO,高温熔融
2
NaCO 固体时反应生成NaSiO,B项错误;硅、二氧化硅都能与氢氟酸反应生成SiF 气体,
2 3 2 3 4C项错误;反应①、③中Si均由+4价降低到0价,硅元素均被还原,D项正确。]
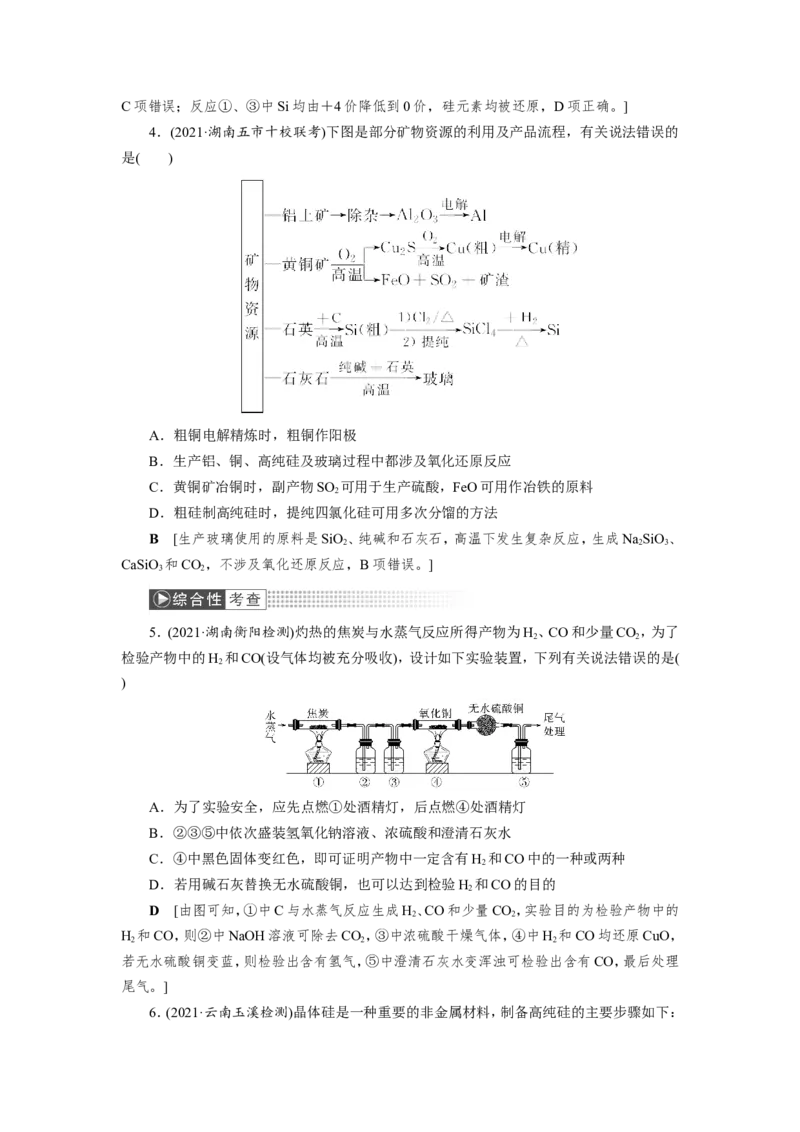
4.(2021·湖南五市十校联考)下图是部分矿物资源的利用及产品流程,有关说法错误的
是( )
A.粗铜电解精炼时,粗铜作阳极
B.生产铝、铜、高纯硅及玻璃过程中都涉及氧化还原反应
C.黄铜矿冶铜时,副产物SO 可用于生产硫酸,FeO可用作冶铁的原料
2
D.粗硅制高纯硅时,提纯四氯化硅可用多次分馏的方法
B [生产玻璃使用的原料是SiO、纯碱和石灰石,高温下发生复杂反应,生成NaSiO、
2 2 3
CaSiO 和CO,不涉及氧化还原反应,B项错误。]
3 2
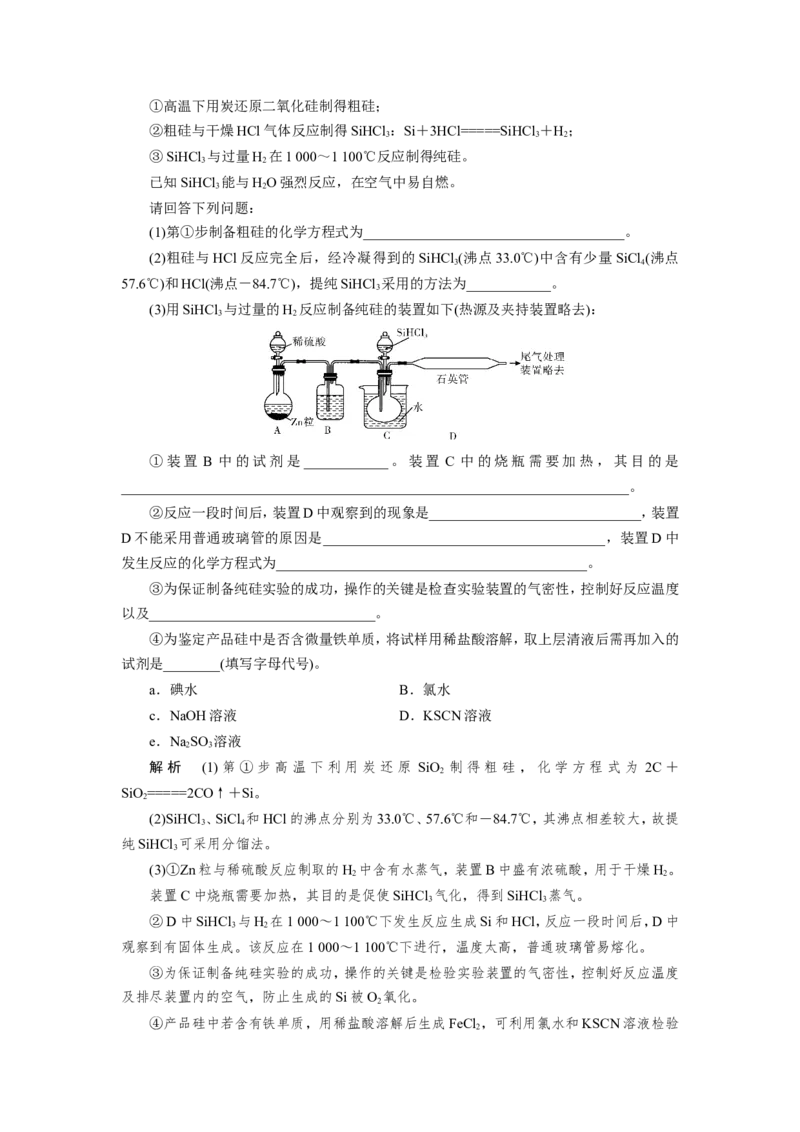
5.(2021·湖南衡阳检测)灼热的焦炭与水蒸气反应所得产物为H、CO和少量CO,为了
2 2
检验产物中的H 和CO(设气体均被充分吸收),设计如下实验装置,下列有关说法错误的是(
2
)
A.为了实验安全,应先点燃①处酒精灯,后点燃④处酒精灯
B.②③⑤中依次盛装氢氧化钠溶液、浓硫酸和澄清石灰水
C.④中黑色固体变红色,即可证明产物中一定含有H 和CO中的一种或两种
2
D.若用碱石灰替换无水硫酸铜,也可以达到检验H 和CO的目的
2
D [由图可知,①中C与水蒸气反应生成H、CO和少量CO,实验目的为检验产物中的
2 2
H 和CO,则②中NaOH溶液可除去CO,③中浓硫酸干燥气体,④中H 和CO均还原CuO,
2 2 2
若无水硫酸铜变蓝,则检验出含有氢气,⑤中澄清石灰水变浑浊可检验出含有CO,最后处理
尾气。]
6.(2021·云南玉溪检测)晶体硅是一种重要的非金属材料,制备高纯硅的主要步骤如下:①高温下用炭还原二氧化硅制得粗硅;
②粗硅与干燥HCl气体反应制得SiHCl :Si+3HCl=====SiHCl +H;
3 3 2
③SiHCl 与过量H 在1 000~1 100℃反应制得纯硅。
3 2
已知SiHCl 能与HO强烈反应,在空气中易自燃。
3 2
请回答下列问题:
(1)第①步制备粗硅的化学方程式为_____________________________________。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl (沸点33.0℃)中含有少量SiCl (沸点
3 4
57.6℃)和HCl(沸点-84.7℃),提纯SiHCl 采用的方法为____________。
3
(3)用SiHCl 与过量的H 反应制备纯硅的装置如下(热源及夹持装置略去):
3 2
①装置 B 中的试剂是____________。装置 C 中的烧瓶需要加热,其目的是
________________________________________________________________________。
②反应一段时间后,装置D中观察到的现象是______________________________,装置
D不能采用普通玻璃管的原因是________________________________________,装置D中
发生反应的化学方程式为____________________________________________。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度
以及________________________________。
④为鉴定产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需再加入的
试剂是________(填写字母代号)。
a.碘水 B.氯水
c.NaOH溶液 D.KSCN溶液
e.NaSO 溶液
2 3
解析 (1)第①步高温下利用炭还原 SiO 制得粗硅,化学方程式为 2C+
2
SiO=====2CO↑+Si。
2
(2)SiHCl 、SiCl 和HCl的沸点分别为33.0℃、57.6℃和-84.7℃,其沸点相差较大,故提
3 4
纯SiHCl 可采用分馏法。
3
(3)①Zn粒与稀硫酸反应制取的H 中含有水蒸气,装置B中盛有浓硫酸,用于干燥H。
2 2
装置C中烧瓶需要加热,其目的是促使SiHCl 气化,得到SiHCl 蒸气。
3 3
②D中SiHCl 与H 在1 000~1 100℃下发生反应生成Si和HCl,反应一段时间后,D中
3 2
观察到有固体生成。该反应在1 000~1 100℃下进行,温度太高,普通玻璃管易熔化。
③为保证制备纯硅实验的成功,操作的关键是检验实验装置的气密性,控制好反应温度
及排尽装置内的空气,防止生成的Si被O 氧化。
2
④产品硅中若含有铁单质,用稀盐酸溶解后生成FeCl ,可利用氯水和KSCN溶液检验
2是否含有FeCl 。
2
答案 (1)2C+SiO=====2CO↑+Si (2)分馏法
2
(3)①浓硫酸 使滴入烧瓶的SiHCl 气化 ②有固体物质生成 在反应温度下,普通玻
3
璃会软化 SiHCl +H=====Si+3HCl ③排尽装置内的空气 ④bd
3 2