文档内容
第 20 练 化学反应原理综合题
一、考情分析
该题型通常以元素化合物知识为载体,以工业生产为背景,综合考查:化学反应中的
能量转化、盖斯定律及其应用、热化学方程式的书写、化学反应速率、化学平衡及其影响
因素、原电池、电解池原理及其电极反应式的书写、水溶液中的离子平衡等知识,甚至还
融合考查氧化还原反应、离子反应,涉及知识点较多,但各个小题又比较相对独立。题目
的综合性强,化学信息较多,设问角度灵活多变,侧重考查考生接受、整合信息的能力、
应用化学知识解决实际问题的能力。
二、高频考点及应对策略
1.热化学方程式的书写及反应热计算方法
首先根据要求书写目标热化学方程式的反应物、产物并配平,其次在反应物和生成物
的后面的括号内注明其状态,再次将目标热化学方程式与已有的热化学方程式比对(主要是
反应物和生成物的位置、化学计量数),最后根据盖斯定律进行适当运算得出目标热化学方
程式的反应热ΔH。
2.反应速率和化学平衡问题的分析思路
(1)熟练“三段式”,准确计算反应速率、转化率和平衡常数。
①明确三种量的意义:一是起始量(物质的量或浓度),二是变化量,三是平衡量;
②用变化量求反应速率和转化率,用平衡浓度求平衡常数(平衡时生成物浓度化学计量
数次幂的乘积与反应物浓度化学计量数次幂的乘积的比值)。
(2)化学平衡状态的比较分析时,要审清两个条件:①恒温恒容;②恒温恒压。
(3)平衡常数的计算
①固体和纯液体的浓度视为常数(不出现在平衡常数表达式中);
②理解气体分压的意义以及气体压强平衡常数 Kp的计算(用分压代表浓度带入平衡常
数公式)。
(4)对于可逆反应,温度变化对正、逆反应速率均产生影响,且影响趋势相同,但影响
程度不同。
①升温对吸热反应影响较大,对放热反应影响较小,故平衡向吸热反应方向移动;
②降温对吸热反应影响较小,对放热反应影响较大,故平衡向放热反应方向移动。
3.分析图表时应注意的事项
(1)对于图像分析要明确三步:“一看”“二想”“三判断”
①“一看”——看图像。a.看面:弄清纵、横坐标的含义。b.看线:弄清线的走向、
变化趋势及线的陡与平。c.看点:弄清曲线上点的含义,特别是一些特殊点,如与坐标轴
的交点、曲线的交点、拐点、最高点与最低点等。d.看量的变化:弄清是浓度变化、温度
变化还是转化率的变化。e.看要不要作辅助线:如等温线、等压线等。
②“二想”——想规律。看完线后联想外界条件对化学反应速率和化学平衡的影响规
律。③“三判断”——得结论。通过对比分析,作出正确判断。
(2) 分析表格数据时,找出数据大小的变化规律。
4.对于电化学类试题,首先判断是原电池还是电解池,然后分析电极类别,书写电极
反应式,最后按电极反应式进行相关计算。
电化学中的电极反应式的书写要做到以下几点:
(1)根据题意、装置图分清“原电池”“电解池”或“电镀池”。
(2)定电极:阴极、阳极;正极、负极。
(3)根据电极反应物和介质确定产物进而写出电极反应式。
①配平(原子守恒、电荷守恒、电子守恒);
②产物粒子在介质中存在的形式;
③得、失电子要表达准确,得电子写+ne-,失电子写-ne-。
(4)对电化学计算要利用各电极转移的电子数相等求未知量。
5.对于电解质溶液类试题,要明确溶液中的物质类型及其可能存在的平衡类型,然后
进行解答。
(1)在守恒式中要注意系数不能遗漏。
①在列电荷守恒式时,注意离子所带电荷的多少,不要简单地认为只是各离子浓度的
相加,如2c(CO)的系数“2”不可漏掉;
②在列物料守恒式时,离子浓度系数不能漏写或颠倒。如NaCO 溶液中的物料守恒式
2 3
中,“2”表示c(Na+)是溶液中各种碳元素存在形式的碳原子总浓度的2倍。
(2)在比较溶液中某些离子大小时①不要忽略水的微弱电离,②不能违背电荷守恒和物
料守恒,如氨水溶液与盐酸混合液中不能出现c(NH)>c(Cl-)>c(H+)>c(OH-)。
1.(2023·河北石家庄·校联考模拟预测)二甲醚是重要的化工原料,采用二氧化碳的有效
转化,既是生成二甲醚的简便方法,又是实现“碳中和”的重要途径。
Ⅰ. 催化加氢合成二甲醚是一种 转化方法,其过程中发生副反应:
①
已知反应:
②
(1) 催化加氢合成二甲醚的热化学方程式为___________,该反应自发进行的条件为
___________。
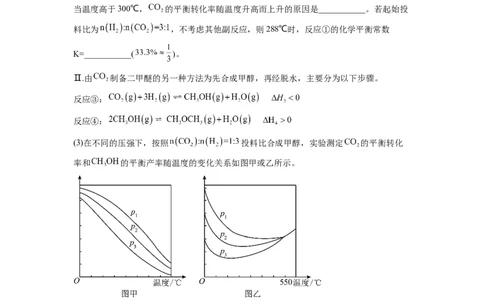
(2)在恒压、 和 的起始量一定的条件下, 的平衡转化率和平衡时 的选择
性随温度变化如图。其中,当温度高于300℃, 的平衡转化率随温度升高而上升的原因是___________。若起始投
料比为 ,不考虑其他副反应,则288℃时,反应①的化学平衡常数
K=___________( )。
Ⅱ.由 制备二甲醚的另一种方法为先合成甲醇,再经脱水,主要分为以下步骤。
反应③:
反应④:
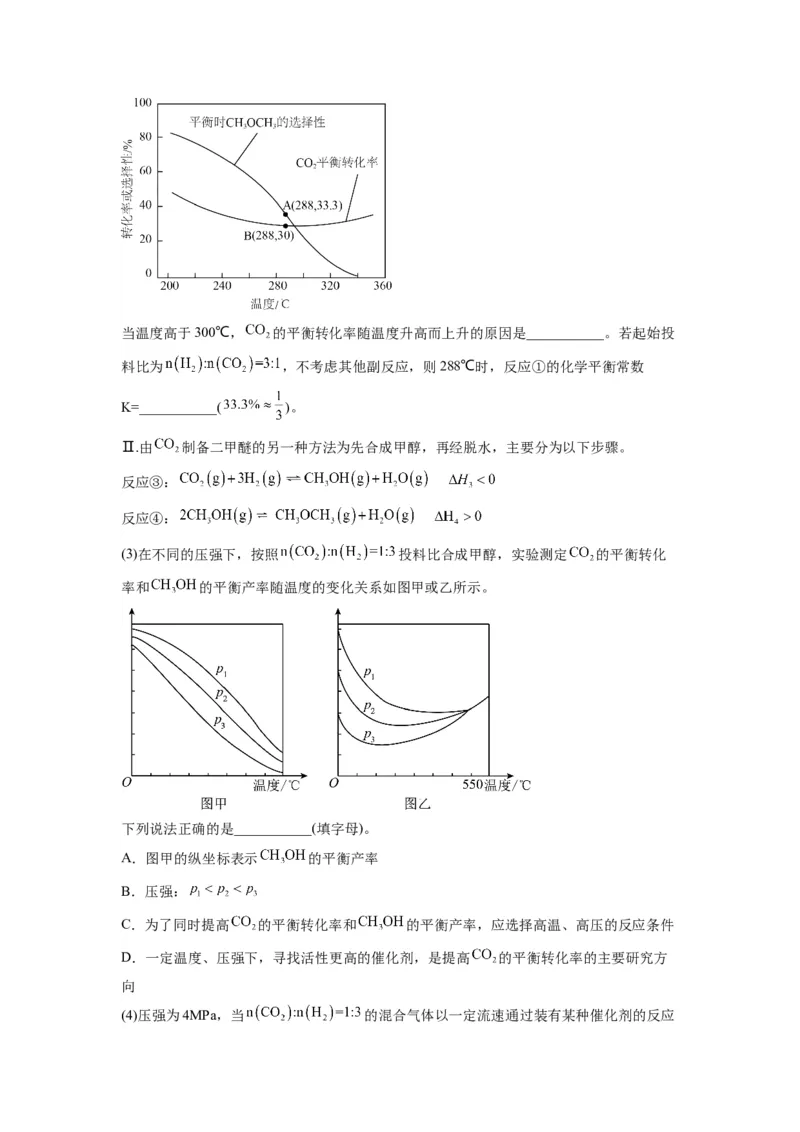
(3)在不同的压强下,按照 投料比合成甲醇,实验测定 的平衡转化
率和 的平衡产率随温度的变化关系如图甲或乙所示。
下列说法正确的是___________(填字母)。
A.图甲的纵坐标表示 的平衡产率
B.压强:
C.为了同时提高 的平衡转化率和 的平衡产率,应选择高温、高压的反应条件
D.一定温度、压强下,寻找活性更高的催化剂,是提高 的平衡转化率的主要研究方
向
(4)压强为4MPa,当 的混合气体以一定流速通过装有某种催化剂的反应器。在280℃时,若 的平衡转化率为7.00%,甲醇的选择性为95.0%,则甲醇的收率为
___________
( )。
(5)甲醇脱水若条件控制不当可生成丙烯,反应为 ,反应
的Arrhenius经验公式的实验数据如图曲线所示,已知Arrhenius经验公式为
(其中, 为活化能,k为速率常数,R和C为常数)。该反应的活化能
___________ 。
2.(2023·广东佛山·统考二模)工业利用 、 催化合成氨实现了人类“向空气中要面
包”的梦想。
(1)原料气(含 、 、CO)中的CO能被催化剂吸附,需经过铜氨液处理除去,反应为:
。
①除去原料气中CO的理由是___________。
②为提高CO吸收率,应选择的条件为___________。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
③ 中的配体为____________
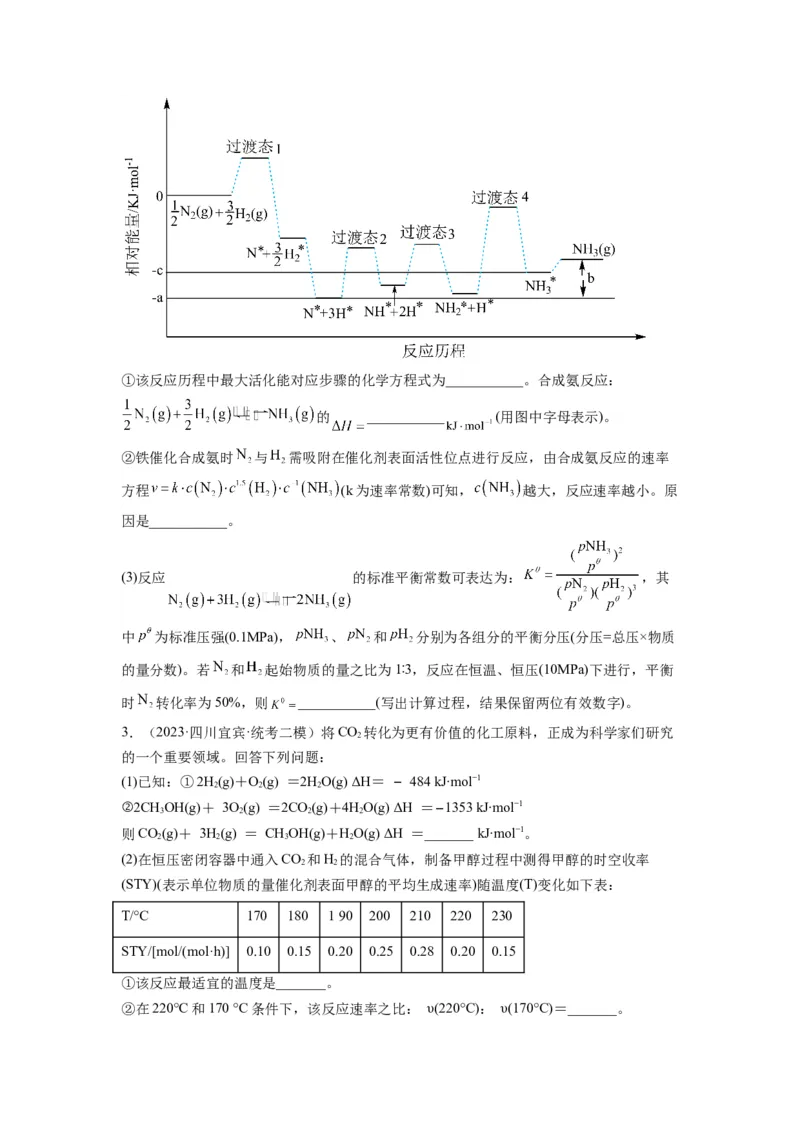
(2)研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的物
种用*标注。①该反应历程中最大活化能对应步骤的化学方程式为___________。合成氨反应:
的 ___________ (用图中字母表示)。
②铁催化合成氨时 与 需吸附在催化剂表面活性位点进行反应,由合成氨反应的速率
方程 (k为速率常数)可知, 越大,反应速率越小。原
因是___________。
(3)反应 的标准平衡常数可表达为: ,其
中 为标准压强(0.1MPa), 、 和 分别为各组分的平衡分压(分压=总压×物质
的量分数)。若 和 起始物质的量之比为1∶3,反应在恒温、恒压(10MPa)下进行,平衡
时 转化率为50%,则 ___________(写出计算过程,结果保留两位有效数字)。
3.(2023·四川宜宾·统考二模)将CO 转化为更有价值的化工原料,正成为科学家们研究
2
的一个重要领域。回答下列问题:
(1)已知:①2H(g)+O(g) =2HO(g) ΔH= − 484 kJ∙mol−1
2 2 2
②2CH OH(g)+ 3O(g) =2CO(g)+4HO(g) ΔH =−1353 kJ∙mol−1
3 2 2 2
则CO(g)+ 3H(g) = CHOH(g)+HO(g) ΔH =_______ kJ∙mol−1。
2 2 3 2
(2)在恒压密闭容器中通入CO 和H 的混合气体,制备甲醇过程中测得甲醇的时空收率
2 2
(STY)(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度(T)变化如下表:
T/°C 170 180 1 90 200 210 220 230
STY/[mol/(mol·h)] 0.10 0.15 0.20 0.25 0.28 0.20 0.15
①该反应最适宜的温度是_______。
②在220°C和170 °C条件下,该反应速率之比: υ(220°C): υ(170°C)=_______。③随温度升高,甲醇的时空收率先增大后减小,可能的原因是_______。
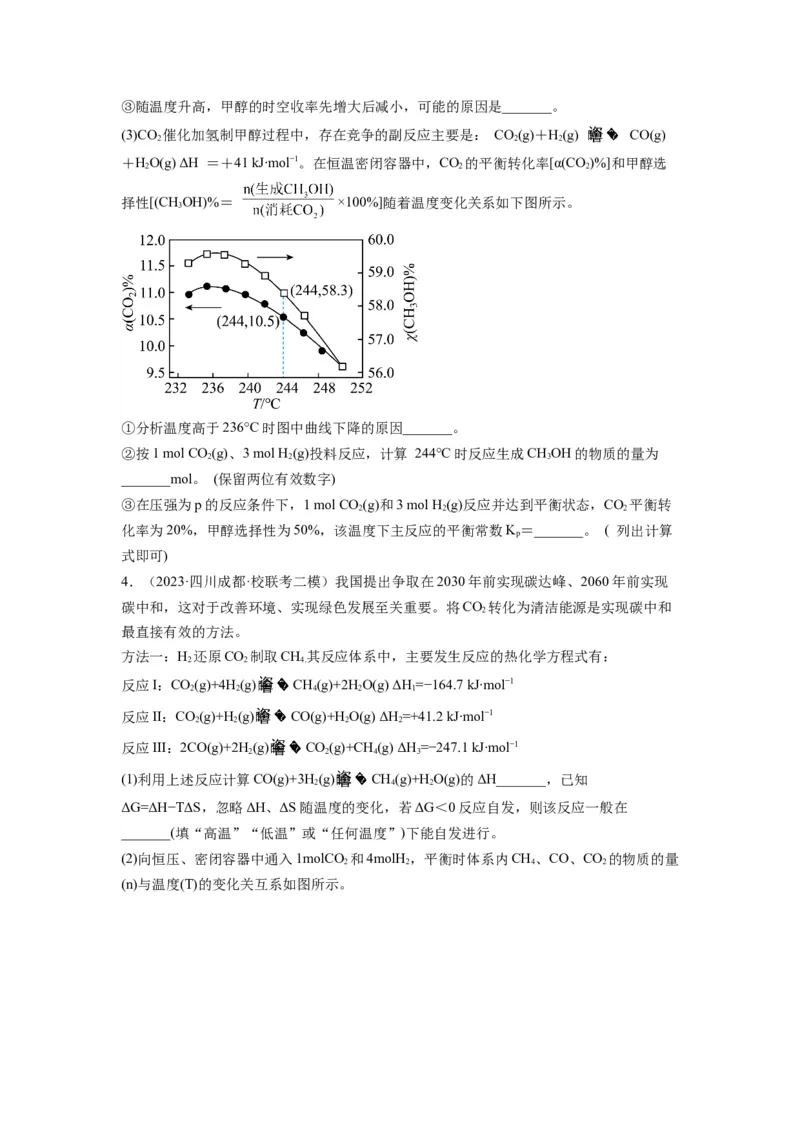
(3)CO 催化加氢制甲醇过程中,存在竞争的副反应主要是: CO(g)+H(g) CO(g)
2 2 2
+HO(g) ΔH =+41 kJ∙mol−1。在恒温密闭容器中,CO 的平衡转化率[α(CO )%]和甲醇选
2 2 2
择性[(CH OH)%= ×100%]随着温度变化关系如下图所示。
3
①分析温度高于236°C时图中曲线下降的原因_______。
②按1 mol CO (g)、3 mol H (g)投料反应,计算 244°C时反应生成CHOH的物质的量为
2 2 3
_______mol。 (保留两位有效数字)
③在压强为p的反应条件下,1 mol CO (g)和3 mol H (g)反应并达到平衡状态,CO 平衡转
2 2 2
化率为20%,甲醇选择性为50%,该温度下主反应的平衡常数K=_______。 ( 列出计算
p
式即可)
4.(2023·四川成都·校联考二模)我国提出争取在2030年前实现碳达峰、2060年前实现
碳中和,这对于改善环境、实现绿色发展至关重要。将CO 转化为清洁能源是实现碳中和
2
最直接有效的方法。
方法一:H 还原CO 制取CH 其反应体系中,主要发生反应的热化学方程式有:
2 2 4.
反应I:CO(g)+4H(g) CH(g)+2HO(g) ΔH=−164.7 kJ∙mol−1
2 2 4 2 1
反应II:CO(g)+H(g) CO(g)+HO(g) ΔH=+41.2 kJ∙mol−1
2 2 2 2
反应III:2CO(g)+2H(g) CO(g)+CH (g) ΔH =−247.1 kJ∙mol−1
2 2 4 3
(1)利用上述反应计算CO(g)+3H(g) CH(g)+HO(g)的ΔH_______,已知
2 4 2
ΔG=ΔH−TΔS,忽略ΔH、ΔS随温度的变化,若ΔG<0反应自发,则该反应一般在
_______(填“高温”“低温”或“任何温度”)下能自发进行。
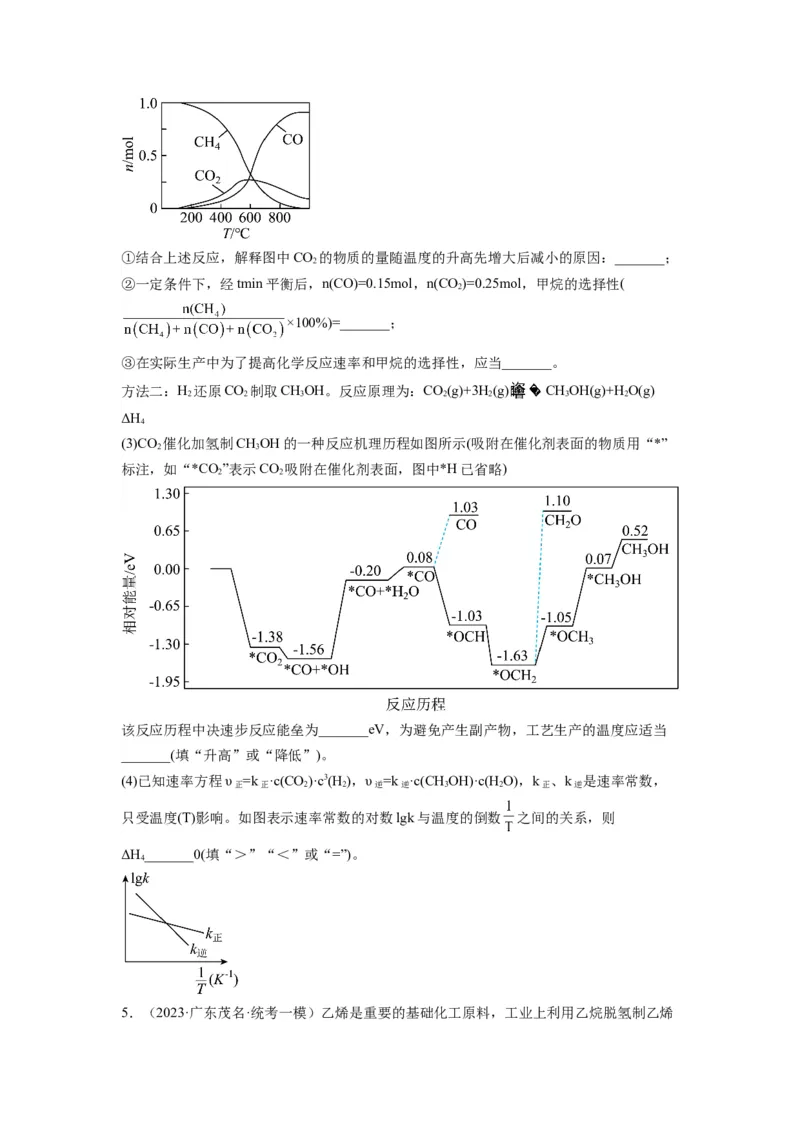
(2)向恒压、密闭容器中通入1molCO 和4molH ,平衡时体系内CH、CO、CO 的物质的量
2 2 4 2
(n)与温度(T)的变化关互系如图所示。①结合上述反应,解释图中CO 的物质的量随温度的升高先增大后减小的原因:_______;
2
②一定条件下,经tmin平衡后,n(CO)=0.15mol,n(CO)=0.25mol,甲烷的选择性(
2
×100%)=_______;
③在实际生产中为了提高化学反应速率和甲烷的选择性,应当_______。
方法二:H 还原CO 制取CHOH。反应原理为:CO(g)+3H(g) CHOH(g)+H O(g)
2 2 3 2 2 3 2
ΔH
4
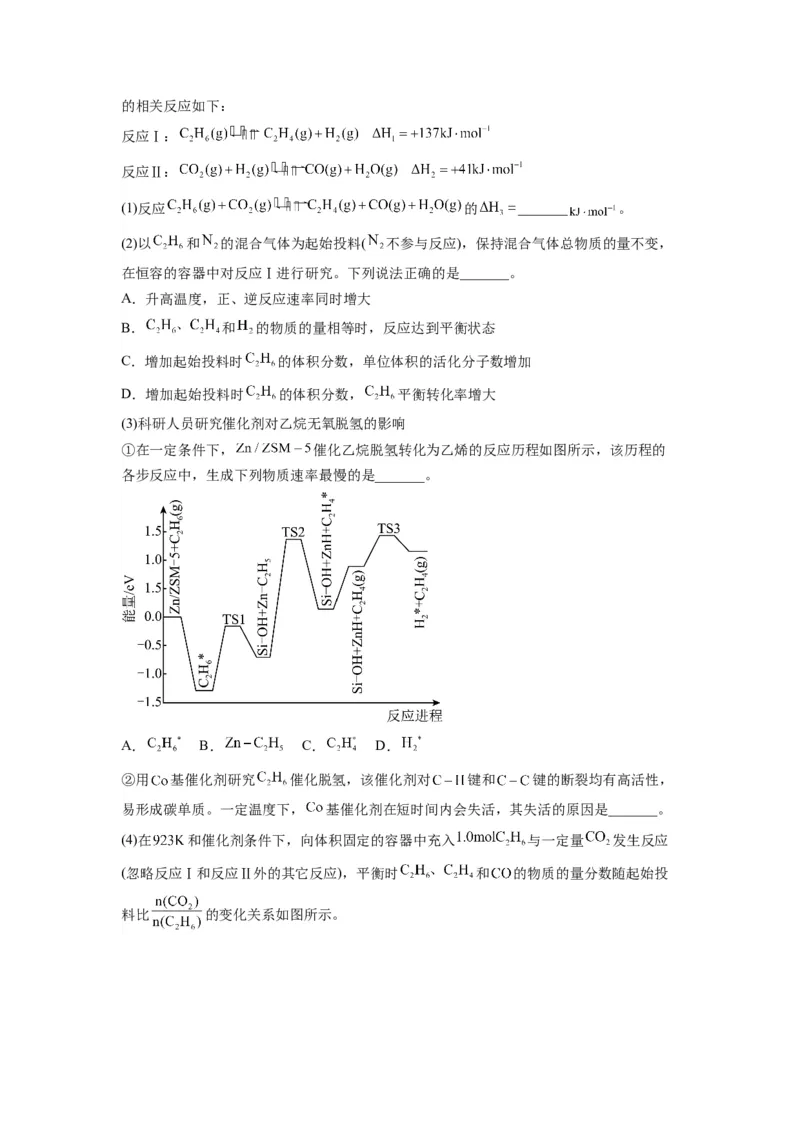
(3)CO 催化加氢制CHOH的一种反应机理历程如图所示(吸附在催化剂表面的物质用“*”
2 3
标注,如“*CO”表示CO 吸附在催化剂表面,图中*H已省略)
2 2
该反应历程中决速步反应能垒为_______eV,为避免产生副产物,工艺生产的温度应适当
_______(填“升高”或“降低”)。
(4)已知速率方程υ =k ·c(CO)·c3(H ),υ =k ·c(CHOH)·c(HO),k 、k 是速率常数,
正 正 2 2 逆 逆 3 2 正 逆
只受温度(T)影响。如图表示速率常数的对数lgk与温度的倒数 之间的关系,则
ΔH_______0(填“>”“<”或“=”)。
4
5.(2023·广东茂名·统考一模)乙烯是重要的基础化工原料,工业上利用乙烷脱氢制乙烯的相关反应如下:
反应Ⅰ:
反应Ⅱ:
(1)反应 的 _______ 。
(2)以 和 的混合气体为起始投料( 不参与反应),保持混合气体总物质的量不变,
在恒容的容器中对反应Ⅰ进行研究。下列说法正确的是_______。
A.升高温度,正、逆反应速率同时增大
B. 和 的物质的量相等时,反应达到平衡状态
C.增加起始投料时 的体积分数,单位体积的活化分子数增加
D.增加起始投料时 的体积分数, 平衡转化率增大
(3)科研人员研究催化剂对乙烷无氧脱氢的影响
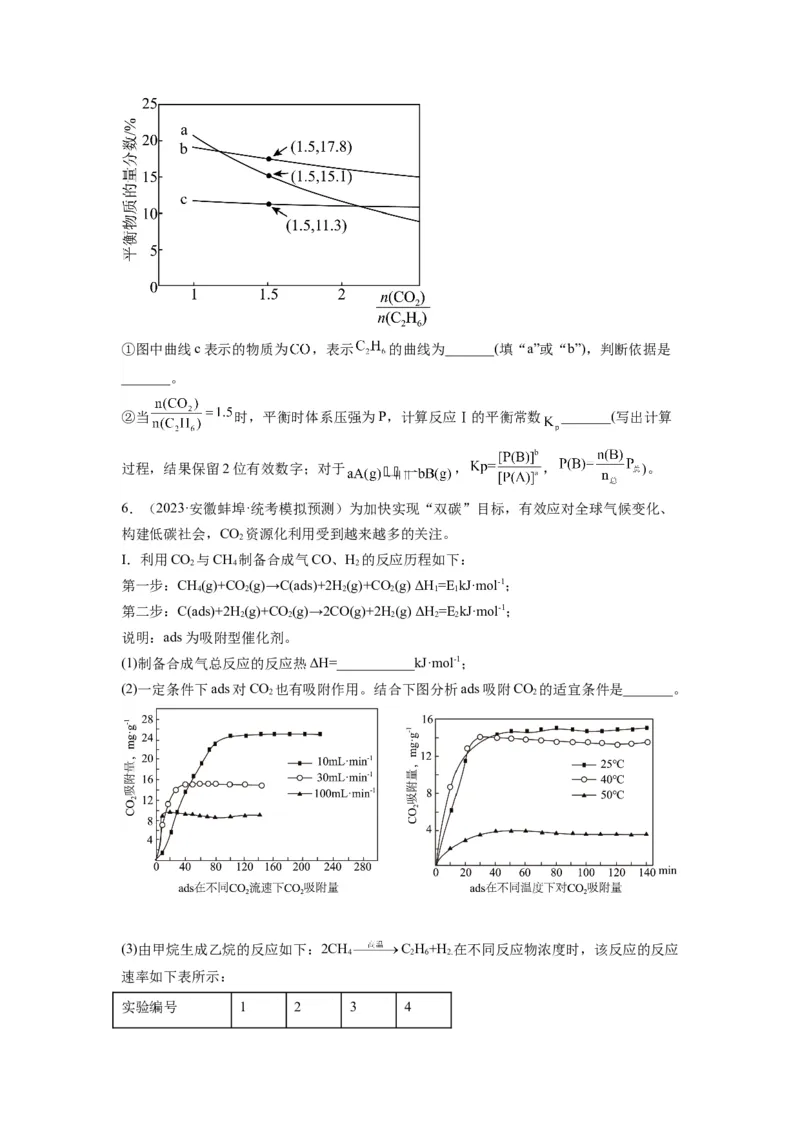
①在一定条件下, 催化乙烷脱氢转化为乙烯的反应历程如图所示,该历程的
各步反应中,生成下列物质速率最慢的是_______。
A. B. C. D.
②用 基催化剂研究 催化脱氢,该催化剂对 键和 键的断裂均有高活性,
易形成碳单质。一定温度下, 基催化剂在短时间内会失活,其失活的原因是_______。
(4)在 和催化剂条件下,向体积固定的容器中充入 与一定量 发生反应
(忽略反应Ⅰ和反应Ⅱ外的其它反应),平衡时 和 的物质的量分数随起始投
料比 的变化关系如图所示。①图中曲线c表示的物质为 ,表示 的曲线为_______(填“a”或“b”),判断依据是
_______。
②当 时,平衡时体系压强为P,计算反应Ⅰ的平衡常数 _______(写出计算
过程,结果保留2位有效数字;对于 , , )。
6.(2023·安徽蚌埠·统考模拟预测)为加快实现“双碳”目标,有效应对全球气候变化、
构建低碳社会,CO 资源化利用受到越来越多的关注。
2
I.利用CO 与CH 制备合成气CO、H 的反应历程如下:
2 4 2
第一步:CH(g)+CO (g)→C(ads)+2H(g)+CO (g) ΔH =EkJ·mol-1;
4 2 2 2 1 1
第二步:C(ads)+2H(g)+CO (g)→2CO(g)+2H (g) ΔH =EkJ·mol-1;
2 2 2 2 2
说明:ads为吸附型催化剂。
(1)制备合成气总反应的反应热ΔH=___________kJ·mol-1;
(2)一定条件下ads对CO 也有吸附作用。结合下图分析ads吸附CO 的适宜条件是_______。
2 2
(3)由甲烷生成乙烷的反应如下:2CH C H+H 在不同反应物浓度时,该反应的反应
4 2 6 2.
速率如下表所示:
实验编号 1 2 3 4c(CH)/(mol·L-1) 0.1000 0.2000 0.3000 0.4000
4
/(mol·L-1·min-1) 0.0076 0.0153 0.0227 0.0306
①该反应的速率方程为: =___________mol·L-1·min-1[用含c(CH)的代数式表示]。
4
②若开始时该反应速率为 mol·L-1·min-1,α表示任一时刻甲烷的转化率,则该反应的速率
1
方程为: =___________mol·L-1·min-1(用含 和α的代数式表示)。
1
③实验测得甲烷浓度由0.400mol·L-1变化到0.200mol·L-1需9.2min,则甲烷浓度由
0.200mol·L-1变化到0.100mol·L-1所需时间___________9.2min。(填“>”、“<”或“=”)
Ⅱ.CO 在固体催化剂表面加氢合成甲烷过程中发生如下反应:
2
反应1:CO
2
(g)+4H
2
(g)⇌CH
4
(g)+2H
2
O(g)
反应2:CO
2
(g)+H
2
(g)⇌CO(g)+H
2
O(g)
(4)已知温度为T时,向0.5L恒容密闭容器中充入2molCO 和6molH ,一段时间后达到平
2 2
衡,测得体系中生成2.5molHO,压强变为原来的75%,反应1的平衡常数
2
K=___________(用分数表示),CH 选择性=___________(CH 选择性= ,
4 4
保留三位有效数字)。
7.(2023·湖北·校联考模拟预测)氨气在农业和国防工业都有很重要的作用,历史上诺贝
尔奖曾经有三次颁给研究合成氨的科学家。
(1)反应的能量变化如图所示。则N(g)与H(g)制备NH (1)的热化学方程式为_____。
2 2 3
(2)关于合成氨工艺的理解,下列正确的是_____。
A.合成氨工业常采用的反应温度为400~500℃左右,可用勒夏特列原理解释
B.使用更高效的催化剂,可以提高平衡时NH 的量
3
C.合成氨工业采用10MPa~30MPa,是因常压下N 和H 的转化率不高
2 2
D.用铜氨溶液处理原料气中CO杂质的反应为:[Cu(NH )]++CO+NH [Cu(NH )CO]+
3 2 3 3 3
ΔH<0,其适宜的生产条件为低温高压
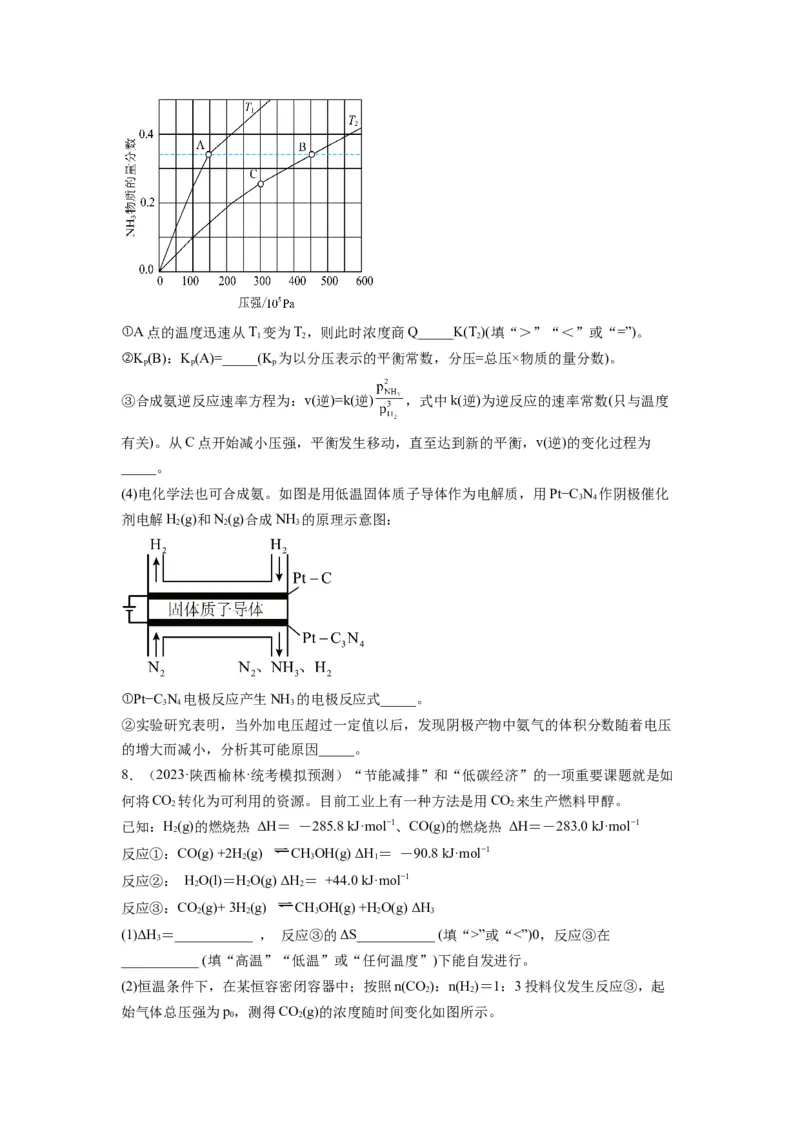
(3)恒压密闭容器中,起始时n(H ):n(N )=3:1,不同温度(T)下平衡混合物中NH (g)物质
2 2 3
的量分数随压强的变化曲线如图所示:①A点的温度迅速从T 变为T,则此时浓度商Q_____K(T )(填“>”“<”或“=”)。
1 2 2
②K (B):K(A)=_____(K 为以分压表示的平衡常数,分压=总压×物质的量分数)。
p p p
③合成氨逆反应速率方程为:v(逆)=k(逆) ,式中k(逆)为逆反应的速率常数(只与温度
有关)。从C点开始减小压强,平衡发生移动,直至达到新的平衡,v(逆)的变化过程为
_____。
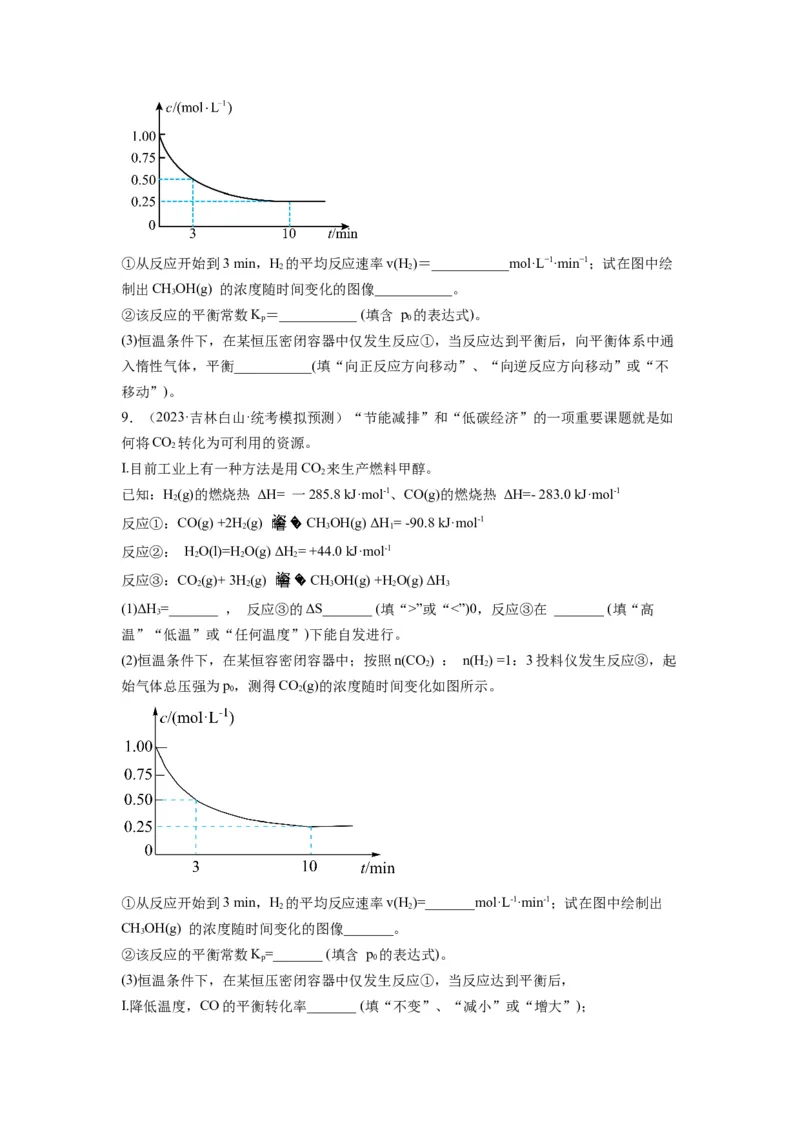
(4)电化学法也可合成氨。如图是用低温固体质子导体作为电解质,用Pt−C N 作阴极催化
3 4
剂电解H(g)和N(g)合成NH 的原理示意图:
2 2 3
①Pt−C N 电极反应产生NH 的电极反应式_____。
3 4 3
②实验研究表明,当外加电压超过一定值以后,发现阴极产物中氨气的体积分数随着电压
的增大而减小,分析其可能原因_____。
8.(2023·陕西榆林·统考模拟预测)“节能减排”和“低碳经济”的一项重要课题就是如
何将CO 转化为可利用的资源。目前工业上有一种方法是用CO 来生产燃料甲醇。
2 2
已知:H(g)的燃烧热 ΔH= -285.8 kJ·mol−1、CO(g)的燃烧热 ΔH=-283.0 kJ·mol−1
2
反应①:CO(g) +2H (g) CHOH(g) ΔH = -90.8 kJ·mol−1
2 3 1
反应②: HO(l)=HO(g) ΔH= +44.0 kJ·mol−1
2 2 2
反应③:CO(g)+ 3H (g) CHOH(g) +HO(g) ΔH
2 2 3 2 3
(1)ΔH =___________ , 反应③的ΔS___________ (填“>”或“<”)0,反应③在
3
___________ (填“高温”“低温”或“任何温度”)下能自发进行。
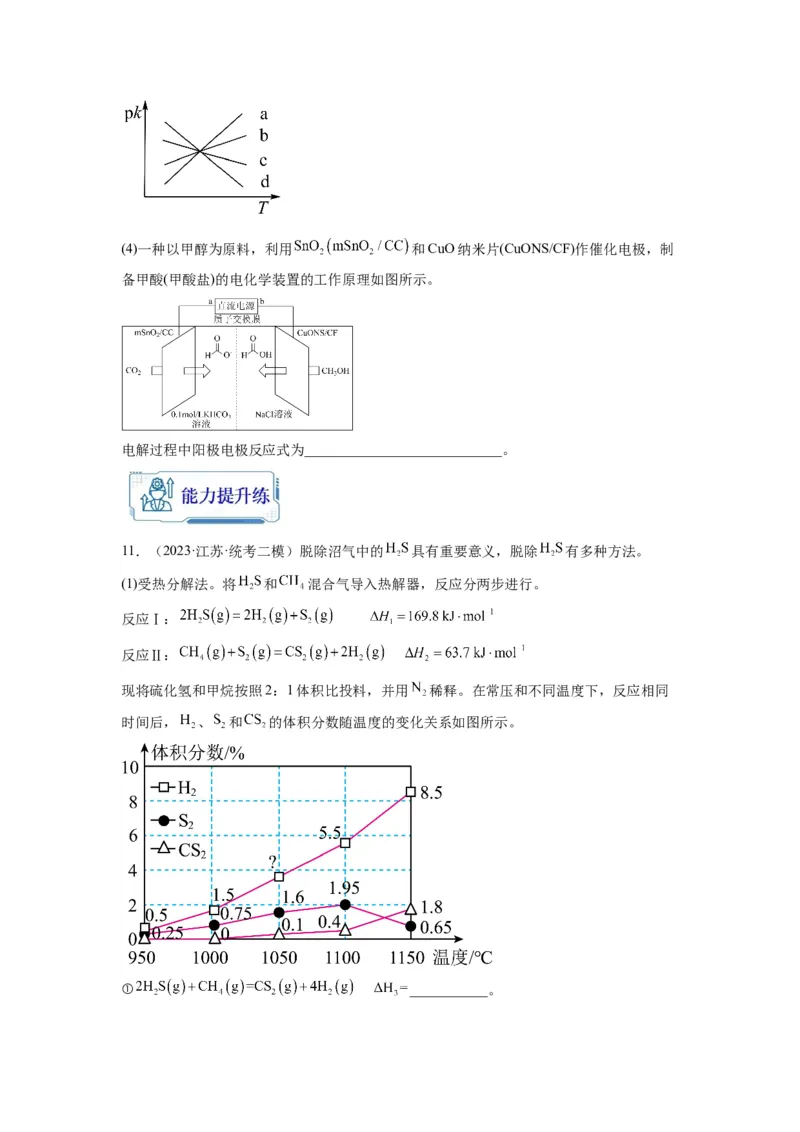
(2)恒温条件下,在某恒容密闭容器中;按照n(CO):n(H )=1:3投料仪发生反应③,起
2 2
始气体总压强为p,测得CO(g)的浓度随时间变化如图所示。
0 2①从反应开始到3 min,H 的平均反应速率v(H )=___________mol·L−1·min−1;试在图中绘
2 2
制出CHOH(g) 的浓度随时间变化的图像___________。
3
②该反应的平衡常数K=___________ (填含 p 的表达式)。
p 0
(3)恒温条件下,在某恒压密闭容器中仅发生反应①,当反应达到平衡后,向平衡体系中通
入惰性气体,平衡___________(填“向正反应方向移动”、“向逆反应方向移动”或“不
移动”)。
9.(2023·吉林白山·统考模拟预测)“节能减排”和“低碳经济”的一项重要课题就是如
何将CO 转化为可利用的资源。
2
I.目前工业上有一种方法是用CO 来生产燃料甲醇。
2
已知:H(g)的燃烧热 ΔH= 一285.8 kJ·mol-1、CO(g)的燃烧热 ΔH=- 283.0 kJ·mol-1
2
反应①:CO(g) +2H (g) CHOH(g) ΔH = -90.8 kJ·mol-1
2 3 1
反应②: HO(l)=HO(g) ΔH= +44.0 kJ·mol-1
2 2 2
反应③:CO(g)+ 3H (g) CHOH(g) +HO(g) ΔH
2 2 3 2 3
(1)ΔH =_______ , 反应③的ΔS_______ (填“>”或“<”)0,反应③在 _______ (填“高
3
温”“低温”或“任何温度”)下能自发进行。
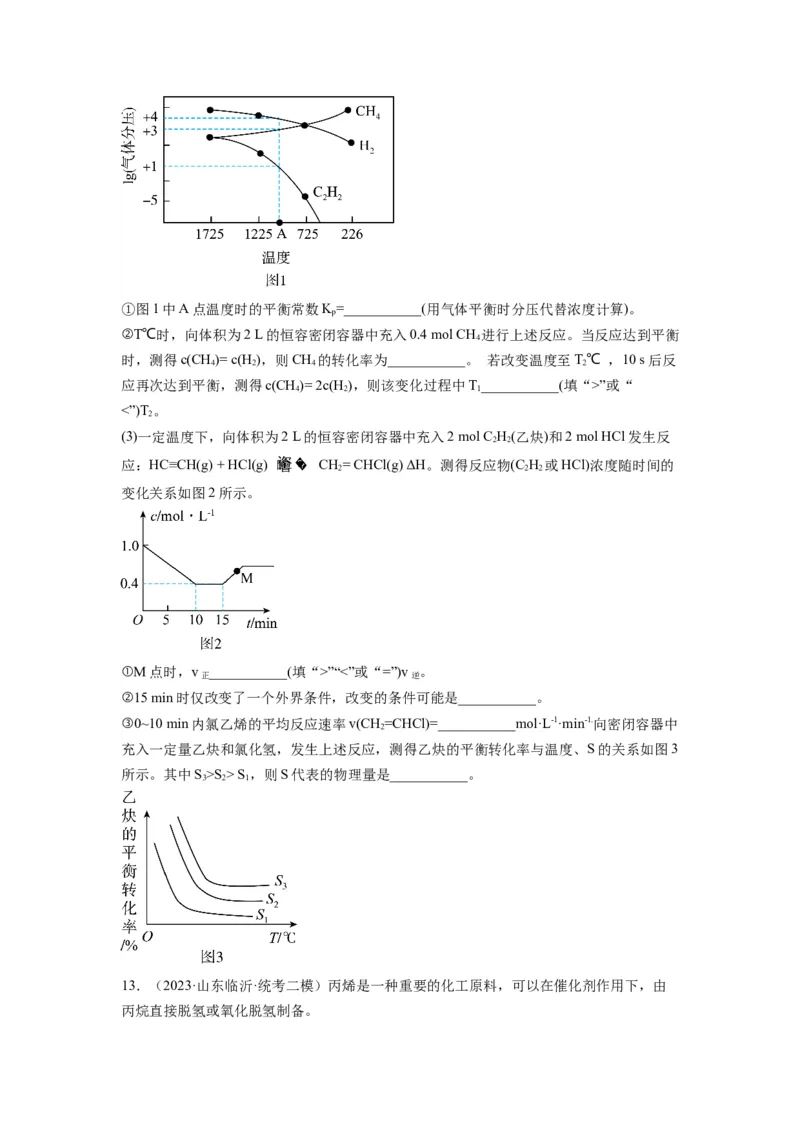
(2)恒温条件下,在某恒容密闭容器中;按照n(CO) : n(H ) =1:3投料仪发生反应③,起
2 2
始气体总压强为p,测得CO(g)的浓度随时间变化如图所示。
0 2
①从反应开始到3 min,H 的平均反应速率v(H )=_______mol·L-1·min-1;试在图中绘制出
2 2
CHOH(g) 的浓度随时间变化的图像_______。
3
②该反应的平衡常数K=_______ (填含 p 的表达式)。
p 0
(3)恒温条件下,在某恒压密闭容器中仅发生反应①,当反应达到平衡后,
I.降低温度,CO的平衡转化率_______ (填“不变”、“减小”或“增大”);II.向平衡体系中通入惰性气体,平衡_______(填“向正反应方向移动”、“向逆反应方向
移动”或“不移动”)。
10.(2023·广东·汕头市澄海中学校联考模拟预测)研发二氧化碳和有机物的利用技术对
治理生态环境具有重要意义。
(1)已知:
则催重整反应 的 _______ 。
(2)催化重整反应 中,测得 的平衡转化率与温度
及压强的关系如图所示:
①判断该反应的 _____ 0(填“>”、“<”或“=”),比较压强的大小: ______ (填“>”、
“<”或“=”) 。
② 在恒容容器中进行该催化重整反应(不考虑其他反应),下列能说明该反应处于化学平衡
状态的是__________(填字母)。
A. 的质量分数保持不变 B.容器中 与H 的百分含量之比保持不变
2
C. D.容器中混合气体的平均相对分子质量保持不
变
③X点对应的初始投料比 ,平衡压强为 ,温度为950℃,则X点平
衡常数 _____________________。
(3)反应 的正、逆反应速率可分
别表示为 、 ,其中k 、k 分别为正、逆反应
正 逆
速率常数,仅受温度影响。则如图所示的四条斜线中,有两条分别为 和pk
随T变化斜线,能表示pk 随T变化关系的是_______(填字母)。
逆 正(4)一种以甲醇为原料,利用 和CuO纳米片(CuONS/CF)作催化电极,制
备甲酸(甲酸盐)的电化学装置的工作原理如图所示。
电解过程中阳极电极反应式为____________________________。
11.(2023·江苏·统考二模)脱除沼气中的 具有重要意义,脱除 有多种方法。
(1)受热分解法。将 和 混合气导入热解器,反应分两步进行。
反应Ⅰ:
反应Ⅱ:
现将硫化氢和甲烷按照2:1体积比投料,并用 稀释。在常压和不同温度下,反应相同
时间后, 、 和 的体积分数随温度的变化关系如图所示。
① ___________。②1050℃时, 的体积分数为___________。
③在950℃~1150℃范围内,其他条件不变,随着温度的升高, (g)的体积分数先增大而
后减小,其原因可能是___________。
(2)光电催化法。某光电催化法脱除 的原理如图所示。
①光电催化法脱除 的离子方程式为___________。
②与受热分解法相比,光电催化法的优点是___________。
(3)催化重整法。Fe O 可以用作脱除 的催化剂,脱除过程如图所示。
2 3
①Fe O 脱除 时需先进行吸附。利用如图乙进行吸附,比如图甲吸附能力强的原因是
2 3
______。
②脱除一段时间后,催化剂的活性降低,原因是___________。
12.(2023·江西赣州·统考模拟预测)甲烷和乙炔(CH≡CH)在有机合成中有着广泛的用途。
回答下列问题:
(1)已知:
①H(g)+ O(g) =H O(g) ΔH= - 198 kJ·mol-1;
2 2 2 1
②CO(g)+ O(g)=CO (g) ΔH = - 283 kJ·mol-1;
2 2 2
③CH (g)+ 2O (g)=CO (g)+2HO(g) ΔH=-846.3 kJ·mol-1。
4 2 2 2 3
写出甲烷与水蒸气在高温下制备合成气(CO、H )的热化学方程式:___________。
2
(2)用甲烷在高温下气相裂解制取乙炔和氢气,其反应原理为2CH(g) C H(g) +3H (g)
4 2 2 2
ΔH >0。几种气体平衡时分压(Pa)的对数与温度(K)的关系如图1所示。①图1中A点温度时的平衡常数K=___________(用气体平衡时分压代替浓度计算)。
p
②T℃时,向体积为2 L的恒容密闭容器中充入0.4 mol CH 进行上述反应。当反应达到平衡
4
时,测得c(CH)= c(H),则CH 的转化率为___________。 若改变温度至T℃ ,10 s后反
4 2 4 2
应再次达到平衡,测得c(CH)= 2c(H),则该变化过程中T___________(填“>”或“
4 2 1
<”)T。
2
(3)一定温度下,向体积为2 L的恒容密闭容器中充入2 mol C H(乙炔)和2 mol HCl发生反
2 2
应:HC≡CH(g) + HCl(g) CH= CHCl(g) ΔH。测得反应物(C H 或HCl)浓度随时间的
2 2 2
变化关系如图2所示。
①M点时,v ___________(填“>”“<”或“=”)v 。
正 逆
②15 min时仅改变了一个外界条件,改变的条件可能是___________。
③0~10 min内氯乙烯的平均反应速率v(CH=CHCl)=___________mol·L-1·min-1.向密闭容器中
2
充入一定量乙炔和氯化氢,发生上述反应,测得乙炔的平衡转化率与温度、S的关系如图3
所示。其中S>S > S ,则S代表的物理量是___________。
3 2 1
13.(2023·山东临沂·统考二模)丙烯是一种重要的化工原料,可以在催化剂作用下,由
丙烷直接脱氢或氧化脱氢制备。反应Ⅰ:
反应Ⅱ:
回答下列问题:
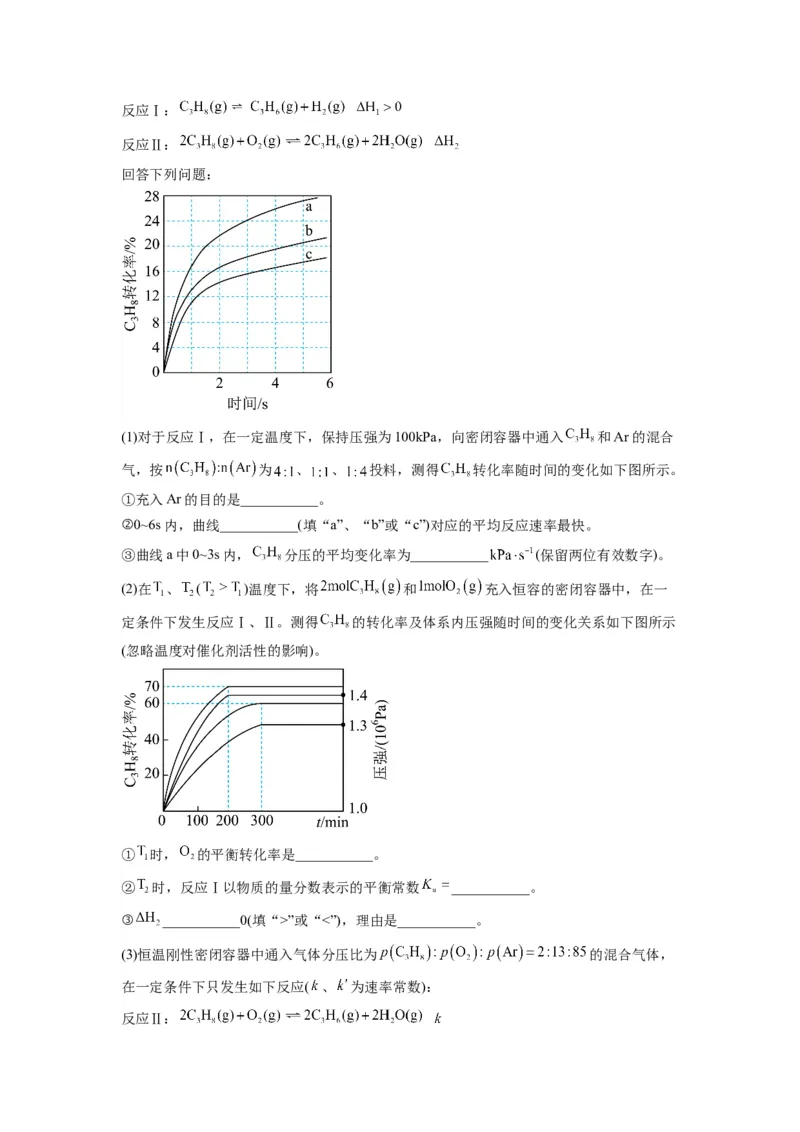
(1)对于反应Ⅰ,在一定温度下,保持压强为100kPa,向密闭容器中通入 和Ar的混合
气,按 为 、 、 投料,测得 转化率随时间的变化如下图所示。
①充入Ar的目的是___________。
②0~6s内,曲线___________(填“a”、“b”或“c”)对应的平均反应速率最快。
③曲线a中0~3s内, 分压的平均变化率为___________ (保留两位有效数字)。
(2)在 、 ( )温度下,将 和 充入恒容的密闭容器中,在一
定条件下发生反应Ⅰ、Ⅱ。测得 的转化率及体系内压强随时间的变化关系如下图所示
(忽略温度对催化剂活性的影响)。
① 时, 的平衡转化率是___________。
② 时,反应Ⅰ以物质的量分数表示的平衡常数 ___________。
③ ___________0(填“>”或“<”),理由是___________。
(3)恒温刚性密闭容器中通入气体分压比为 的混合气体,
在一定条件下只发生如下反应( 、 为速率常数):
反应Ⅱ:反应Ⅲ:
实验测得丙烯的净生成速率方程为 ,可推测丙烯的浓度随
时间的变化趋势为___________,理由是___________。
14.(2023·江苏南京·统考二模)以 还原 的选择性催化还原( -SCR)技术广泛应
用于烟气(含NO、 、 等)脱硝。
(1) 大量排放造成的环境问题主要有:___________(填一种)。
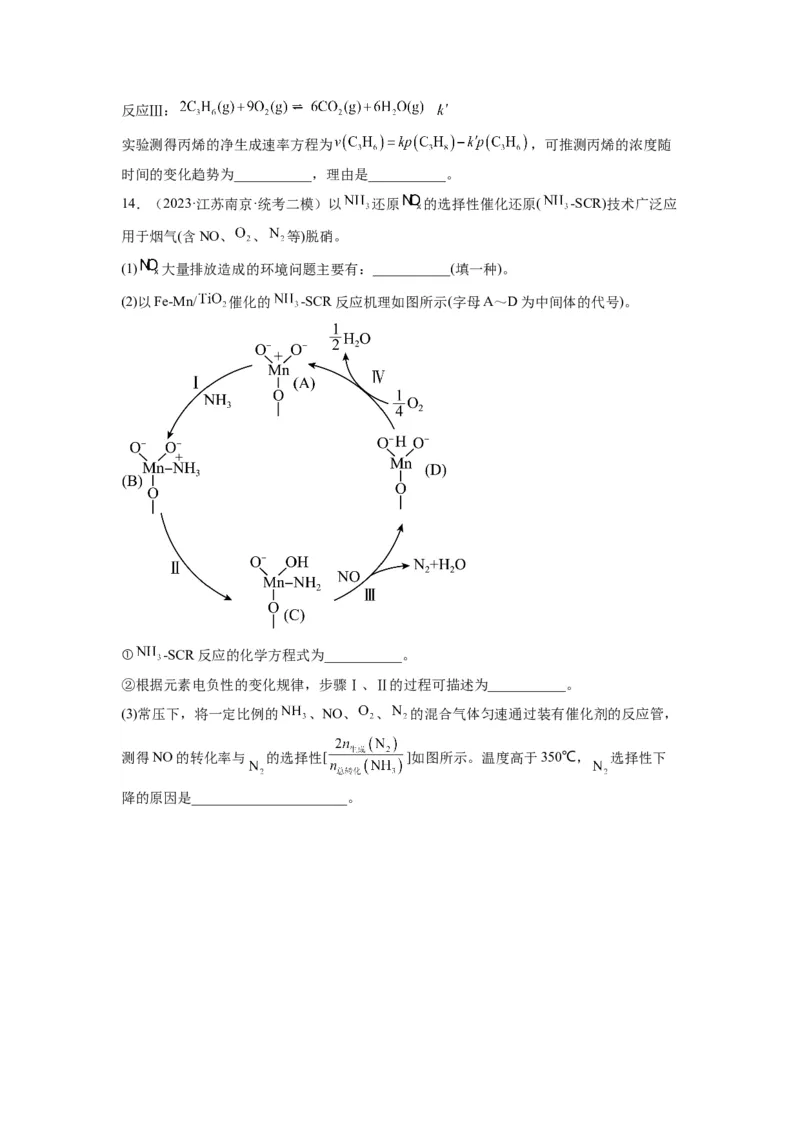
(2)以Fe-Mn/ 催化的 -SCR反应机理如图所示(字母A~D为中间体的代号)。
① -SCR反应的化学方程式为___________。
②根据元素电负性的变化规律,步骤Ⅰ、Ⅱ的过程可描述为___________。
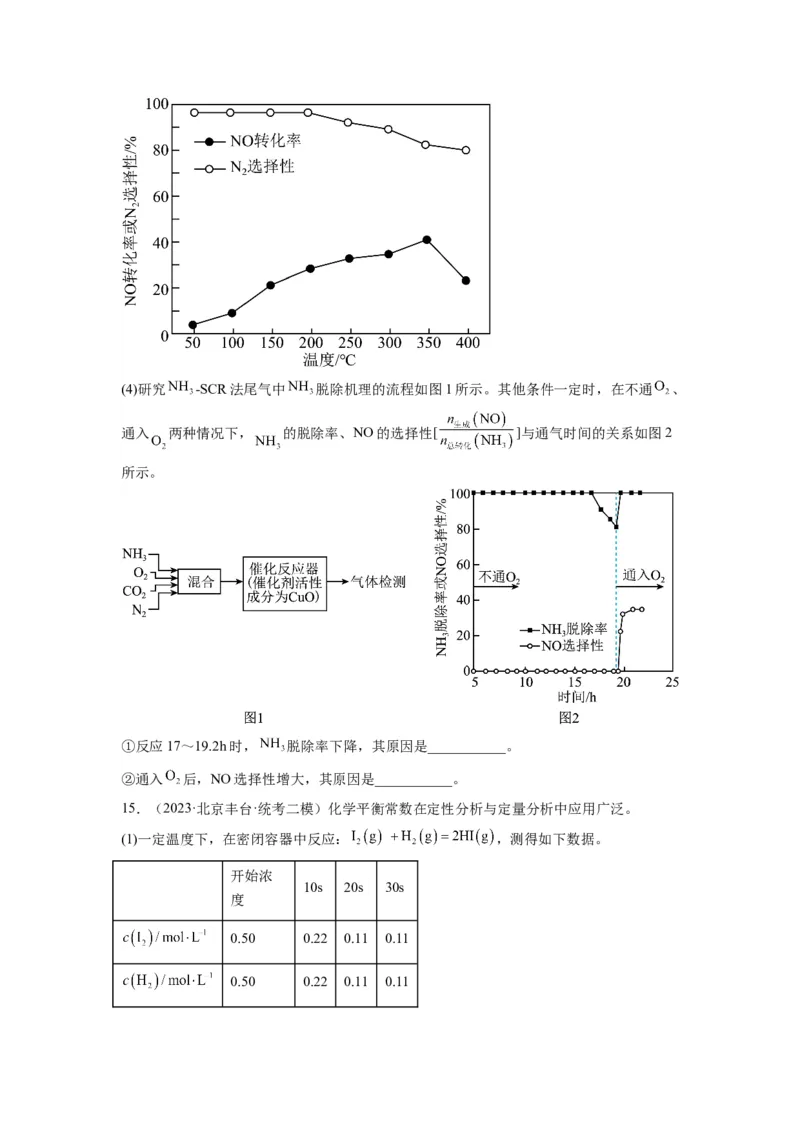
(3)常压下,将一定比例的 、NO、 、 的混合气体匀速通过装有催化剂的反应管,
测得NO的转化率与 的选择性[ ]如图所示。温度高于350℃, 选择性下
降的原因是______________________。(4)研究 -SCR法尾气中 脱除机理的流程如图1所示。其他条件一定时,在不通 、
通入 两种情况下, 的脱除率、NO的选择性[ ]与通气时间的关系如图2
所示。
①反应17~19.2h时, 脱除率下降,其原因是___________。
②通入 后,NO选择性增大,其原因是___________。
15.(2023·北京丰台·统考二模)化学平衡常数在定性分析与定量分析中应用广泛。
(1)一定温度下,在密闭容器中反应: ,测得如下数据。
开始浓
10s 20s 30s
度
0.50 0.22 0.11 0.11
0.50 0.22 0.11 0.110.00 0.56 0.78 0.78
①该温度下, 的平衡转化率为___________。
②该温度下,当初始投入浓度为 , ,
时,进行实验,反应进行的方向为___________(填“正反应方向”或
“逆反应方向”)。
(2)已知:25℃时, 、 、 、 的电离平衡常数。
物质
电离平
衡常数
①25℃时,相同物质的量浓度的 、 、 、 溶液, 由大到
小的顺序为___________。
②25℃时,向 溶液中加入 溶液达到滴定终点,再向溶液中加入
溶液,使溶液中 ,溶液中 ___________
。
③结合电离平衡常数分析 与 溶液反应的产物___________。
④将足量 通入 溶液中,迅速反应得到无色溶液和白色沉淀( )。放置一段
时间,有 和 生成。先产生白色沉淀,后生成 和 的可能原因是___________。
16.(2023·全国甲卷·统考高考真题)甲烷选择性氧化制备甲醇是一种原子利用率高的方
法。回答下列问题:
(1)已知下列反应的热化学方程式:
①
②
反应③ 的 _______ ,平衡常数
_______(用 表示)。
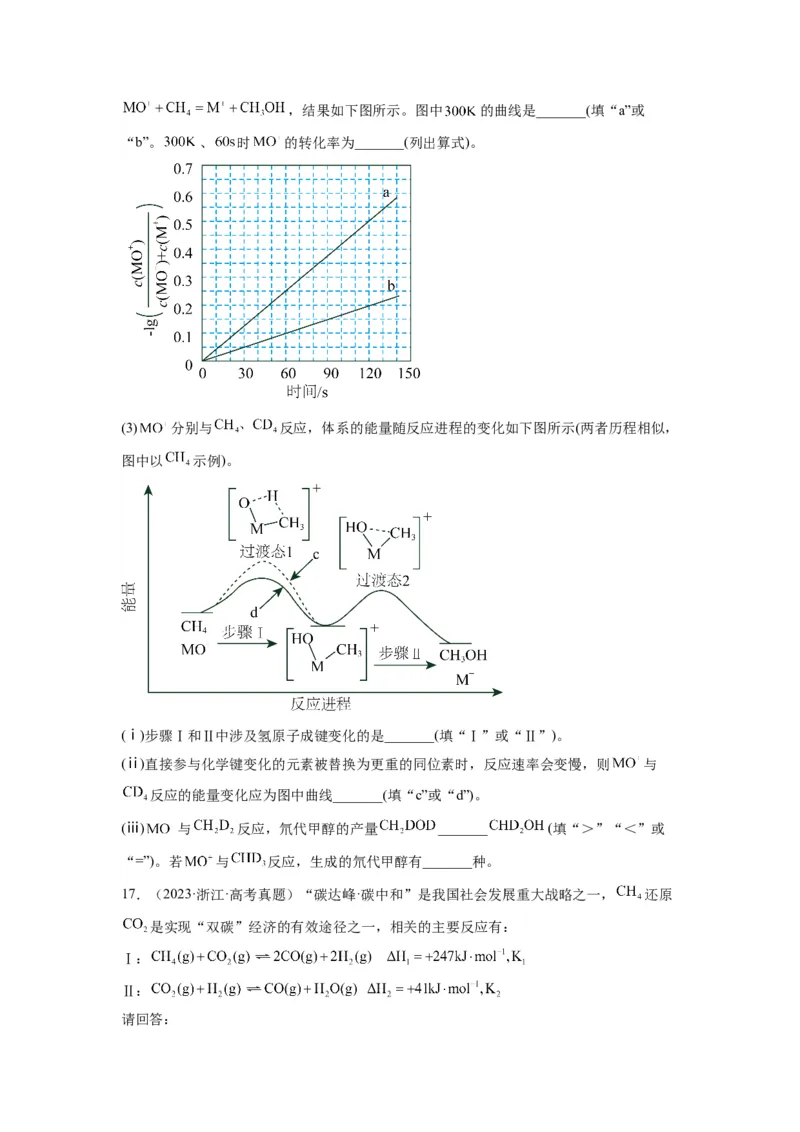
(2)电喷雾电离等方法得到的 ( 等)与 反应可得 。 与 反应
能高选择性地生成甲醇。分别在 和 下(其他反应条件相同)进行反应,结果如下图所示。图中 的曲线是_______(填“a”或
“b”。 、 时 的转化率为_______(列出算式)。
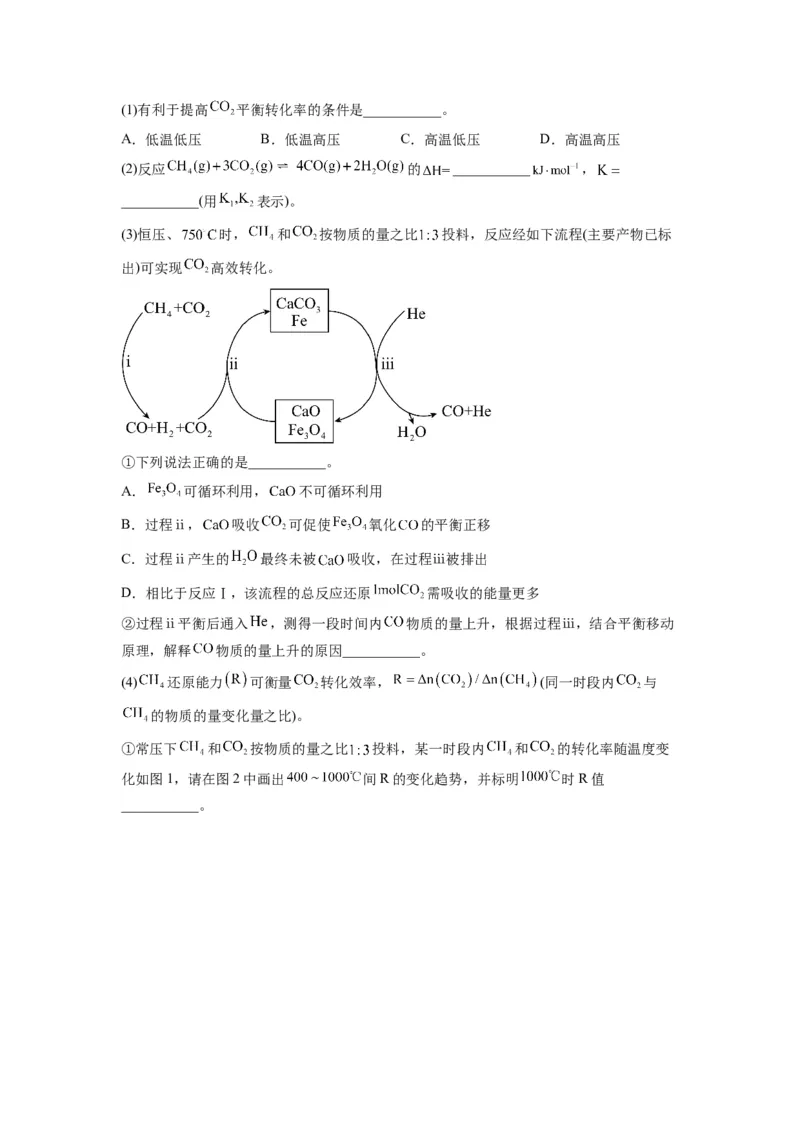
(3) 分别与 反应,体系的能量随反应进程的变化如下图所示(两者历程相似,
图中以 示例)。
(ⅰ)步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是_______(填“Ⅰ”或“Ⅱ”)。
(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则 与
反应的能量变化应为图中曲线_______(填“c”或“d”)。
(ⅲ) 与 反应,氘代甲醇的产量 _______ (填“>”“<”或
“=”)。若 与 反应,生成的氘代甲醇有_______种。
17.(2023·浙江·高考真题)“碳达峰·碳中和”是我国社会发展重大战略之一, 还原
是实现“双碳”经济的有效途径之一,相关的主要反应有:
Ⅰ:
Ⅱ:
请回答:(1)有利于提高 平衡转化率的条件是___________。
A.低温低压 B.低温高压 C.高温低压 D.高温高压
(2)反应 的 ___________ ,
___________(用 表示)。
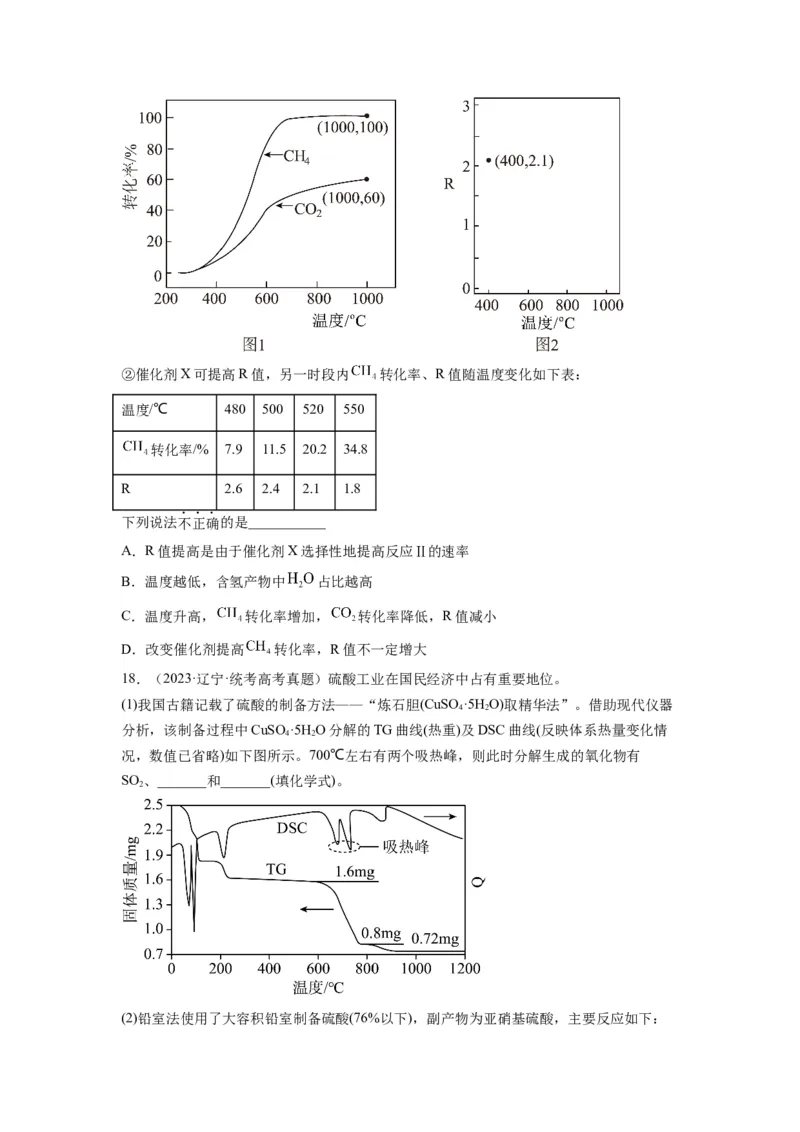
(3)恒压、 时, 和 按物质的量之比 投料,反应经如下流程(主要产物已标
出)可实现 高效转化。
①下列说法正确的是___________。
A. 可循环利用, 不可循环利用
B.过程ⅱ, 吸收 可促使 氧化 的平衡正移
C.过程ⅱ产生的 最终未被 吸收,在过程ⅲ被排出
D.相比于反应Ⅰ,该流程的总反应还原 需吸收的能量更多
②过程ⅱ平衡后通入 ,测得一段时间内 物质的量上升,根据过程ⅲ,结合平衡移动
原理,解释 物质的量上升的原因___________。
(4) 还原能力 可衡量 转化效率, (同一时段内 与
的物质的量变化量之比)。
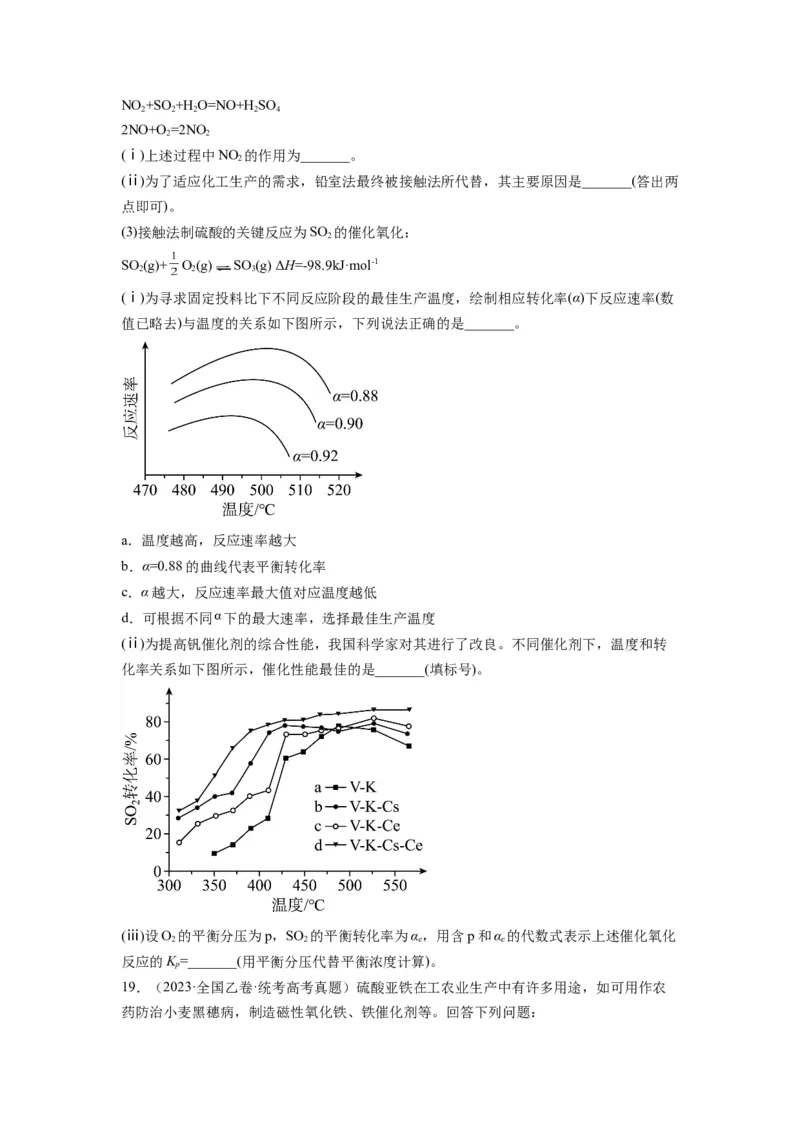
①常压下 和 按物质的量之比 投料,某一时段内 和 的转化率随温度变
化如图1,请在图2中画出 间R的变化趋势,并标明 时R值
___________。②催化剂X可提高R值,另一时段内 转化率、R值随温度变化如下表:
温度/℃ 480 500 520 550
转化率/% 7.9 11.5 20.2 34.8
R 2.6 2.4 2.1 1.8
下列说法不正确的是___________
A.R值提高是由于催化剂X选择性地提高反应Ⅱ的速率
B.温度越低,含氢产物中 占比越高
C.温度升高, 转化率增加, 转化率降低,R值减小
D.改变催化剂提高 转化率,R值不一定增大
18.(2023·辽宁·统考高考真题)硫酸工业在国民经济中占有重要地位。
(1)我国古籍记载了硫酸的制备方法——“炼石胆(CuSO ·5H O)取精华法”。借助现代仪器
4 2
分析,该制备过程中CuSO ·5H O分解的TG曲线(热重)及DSC曲线(反映体系热量变化情
4 2
况,数值已省略)如下图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有
SO 、_______和_______(填化学式)。
2
(2)铅室法使用了大容积铅室制备硫酸(76%以下),副产物为亚硝基硫酸,主要反应如下:NO +SO+H O=NO+H SO
2 2 2 2 4
2NO+O =2NO
2 2
(ⅰ)上述过程中NO 的作用为_______。
2
(ⅱ)为了适应化工生产的需求,铅室法最终被接触法所代替,其主要原因是_______(答出两
点即可)。
(3)接触法制硫酸的关键反应为SO 的催化氧化:
2
SO (g)+ O(g) SO (g) ΔH=-98.9kJ·mol-1
2 2 3
(ⅰ)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数
值已略去)与温度的关系如下图所示,下列说法正确的是_______。
a.温度越高,反应速率越大
b.α=0.88的曲线代表平衡转化率
c.α越大,反应速率最大值对应温度越低
d.可根据不同 下的最大速率,选择最佳生产温度
(ⅱ)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转
化率关系如下图所示,催化性能最佳的是_______(填标号)。
(ⅲ)设O 的平衡分压为p,SO 的平衡转化率为α,用含p和α 的代数式表示上述催化氧化
2 2 e e
反应的K =_______(用平衡分压代替平衡浓度计算)。
p
19.(2023·全国乙卷·统考高考真题)硫酸亚铁在工农业生产中有许多用途,如可用作农
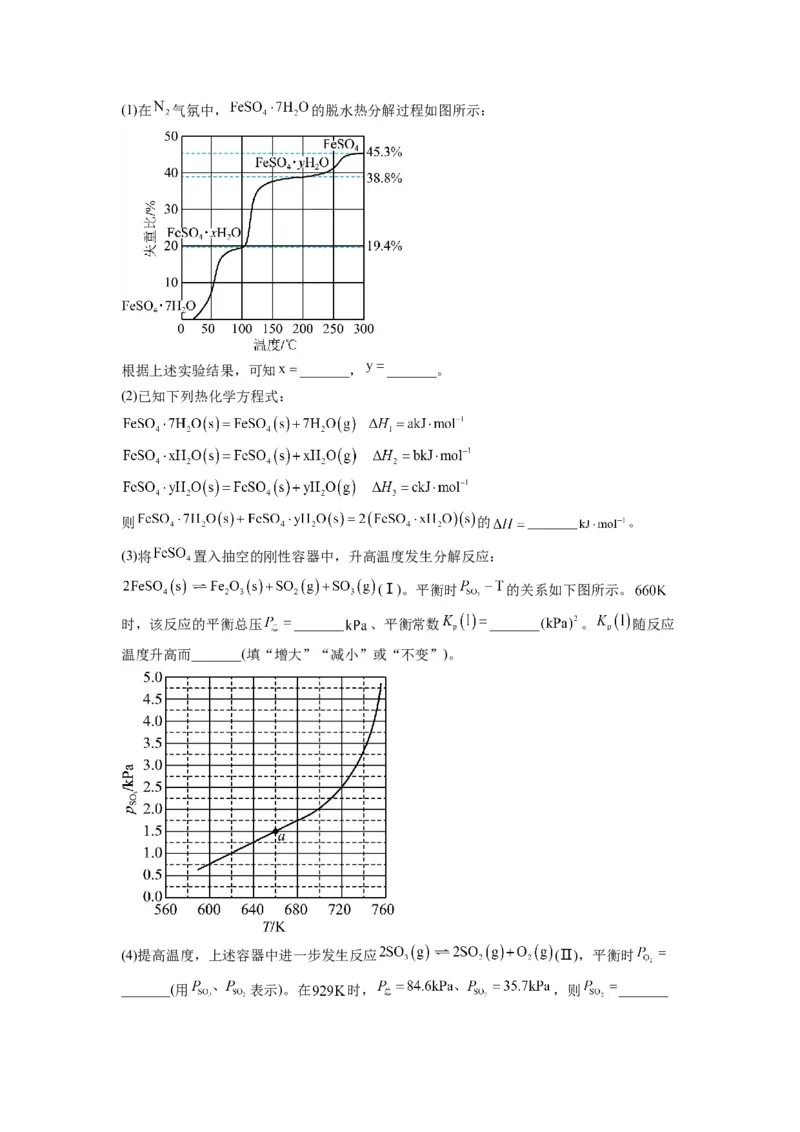
药防治小麦黑穗病,制造磁性氧化铁、铁催化剂等。回答下列问题:(1)在 气氛中, 的脱水热分解过程如图所示:
根据上述实验结果,可知 _______, _______。
(2)已知下列热化学方程式:
则 的 _______ 。
(3)将 置入抽空的刚性容器中,升高温度发生分解反应:
(Ⅰ)。平衡时 的关系如下图所示。
时,该反应的平衡总压 _______ 、平衡常数 _______ 。 随反应
温度升高而_______(填“增大”“减小”或“不变”)。
(4)提高温度,上述容器中进一步发生反应 (Ⅱ),平衡时
_______(用 表示)。在 时, ,则 _______, _______ (列出计算式)。
20.(2023·山东·统考高考真题)一定条件下,水气变换反应 的中间
产物是 。为探究该反应过程,研究 水溶液在密封石英管中的分子反应:
Ⅰ.
Ⅱ.
研究发现,在反应Ⅰ、Ⅱ中, 仅对反应Ⅰ有催加速作用;反应Ⅰ速率远大于反应Ⅱ,近
似认为反应Ⅰ建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问
题:
(1)一定条件下,反应Ⅰ、Ⅱ的焓变分别为 、 ,则该条件下水气变换反应的焓变
_____(用含 的代数式表示)。
(2)反应Ⅰ正反应速率方程为: ,k为反应速率常数。 温度下,
电离平衡常数为 ,当 平衡浓度为 时, 浓度为_____
,此时反应Ⅰ应速率 _____ (用含 和k的代数式表示)。
(3) 温度下,在密封石英管内完全充满 水溶液,使 分解,分
解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存
在形式)。 时刻测得 的浓度分别为 ,反应Ⅱ达平衡时,
测得 的浓度为 。体系达平衡后 _____(用含y的代数式表示,下同),
反应Ⅱ的平衡常数为_____。
相同条件下,若反应起始时溶液中同时还含有 盐酸,则图示点 中,
的浓度峰值点可能是_____(填标号)。与不同盐酸相比, 达浓度峰值时, 浓度
_____(填“增大”“减小”或“不变”), 的反应_____(填“增大”“减小”或
“不变”)。
21.(2022·天津·统考高考真题)天津地处环渤海湾,海水资源丰富。科研人员把铁的配
合物 (L为配体)溶于弱碱性的海水中,制成吸收液,将气体 转化为单质硫,改进了湿法脱硫工艺。该工艺包含两个阶段:① 的吸收氧化;② 的再生。反应原理如
下:
①
②
回答下列问题:
(1)该工艺的总反应方程式为___________。1mol 发生该反应的热量变化为
___________, 在总反应中的作用是___________。
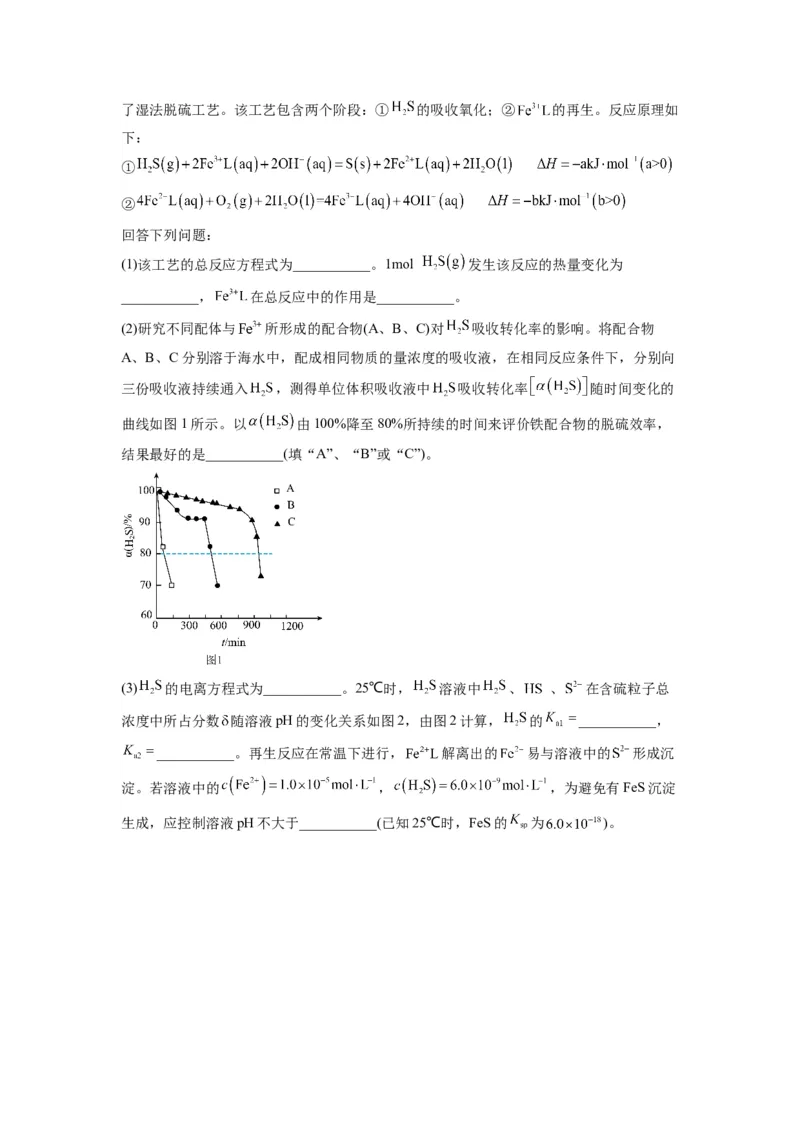
(2)研究不同配体与 所形成的配合物(A、B、C)对 吸收转化率的影响。将配合物
A、B、C分别溶于海水中,配成相同物质的量浓度的吸收液,在相同反应条件下,分别向
三份吸收液持续通入 ,测得单位体积吸收液中 吸收转化率 随时间变化的
曲线如图1所示。以 由100%降至80%所持续的时间来评价铁配合物的脱硫效率,
结果最好的是___________(填“A”、“B”或“C”)。
(3) 的电离方程式为___________。25℃时, 溶液中 、 、 在含硫粒子总
浓度中所占分数 随溶液pH的变化关系如图2,由图2计算, 的 ___________,
___________。再生反应在常温下进行, 解离出的 易与溶液中的 形成沉
淀。若溶液中的 , ,为避免有FeS沉淀
生成,应控制溶液pH不大于___________(已知25℃时,FeS的 为 )。22.(2022·重庆·统考高考真题)反应 在工业上有
重要应用。
(1)该反应在不同温度下的平衡常数如表所示。
温度/℃ 700 800 830 1000
平衡常
1.67 1.11 1.00 0.59
数
①反应的 H_____0(填“>”“<”或“=”)。
②反应常在较高温度下进行,该措施的优缺点是_____。
△
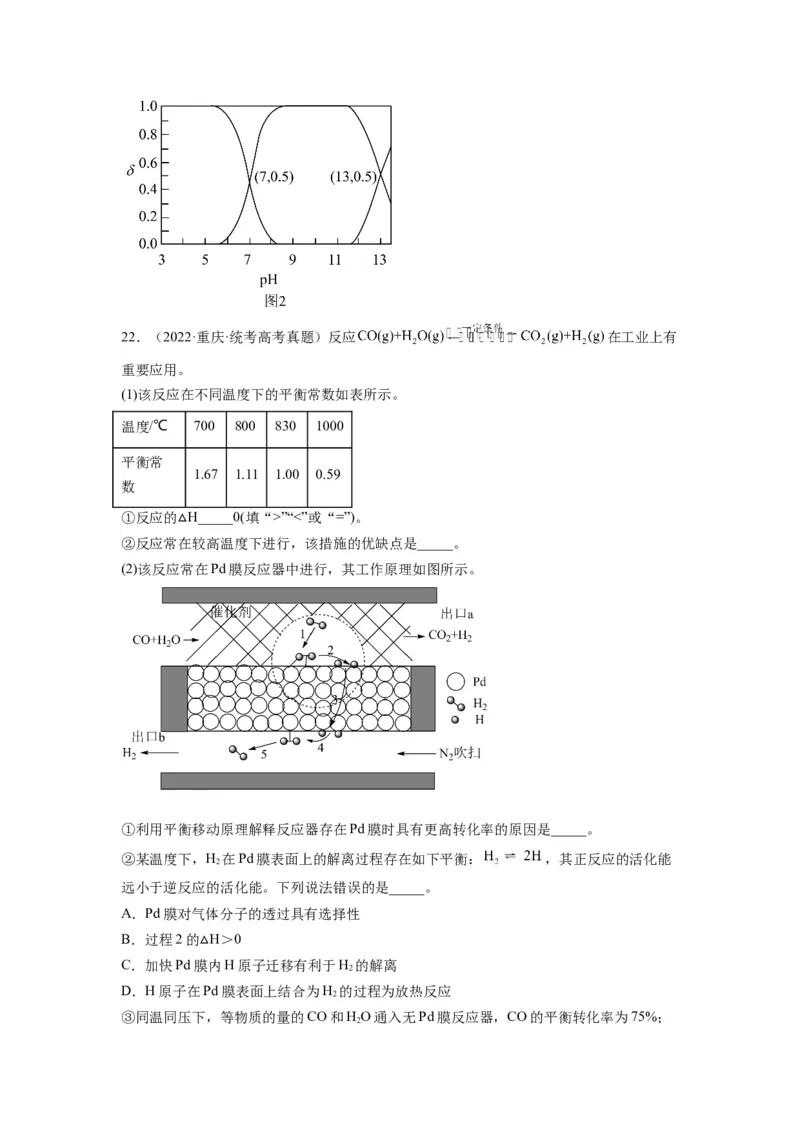
(2)该反应常在Pd膜反应器中进行,其工作原理如图所示。
①利用平衡移动原理解释反应器存在Pd膜时具有更高转化率的原因是_____。
②某温度下,H 在Pd膜表面上的解离过程存在如下平衡: ,其正反应的活化能
2
远小于逆反应的活化能。下列说法错误的是_____。
A.Pd膜对气体分子的透过具有选择性
B.过程2的 H>0
C.加快Pd膜内H原子迁移有利于H 的解离
△ 2
D.H原子在Pd膜表面上结合为H 的过程为放热反应
2
③同温同压下,等物质的量的CO和HO通入无Pd膜反应器,CO的平衡转化率为75%;
2若换成Pd膜反应器,CO的平衡转化率为90%,则相同时间内出口a和出口b中H 的质量
2
比为_____。
(3)该反应也可采用电化学方法实现,反应装置如图所示。
①固体电解质采用______(填“氧离子导体”或“质子导体”)。
②阴极的电极反应式为______。
③同温同压下,相同时间内,若进口Ⅰ处n(CO):n(H O)=a:b,出口Ⅰ处气体体积为进口
2
Ⅰ处的y倍,则CO的转化率为_____(用a,b,y表示)。
23.(2022·江苏·高考真题)氢气是一种清洁能源,绿色环保制氢技术研究具有重要意义。
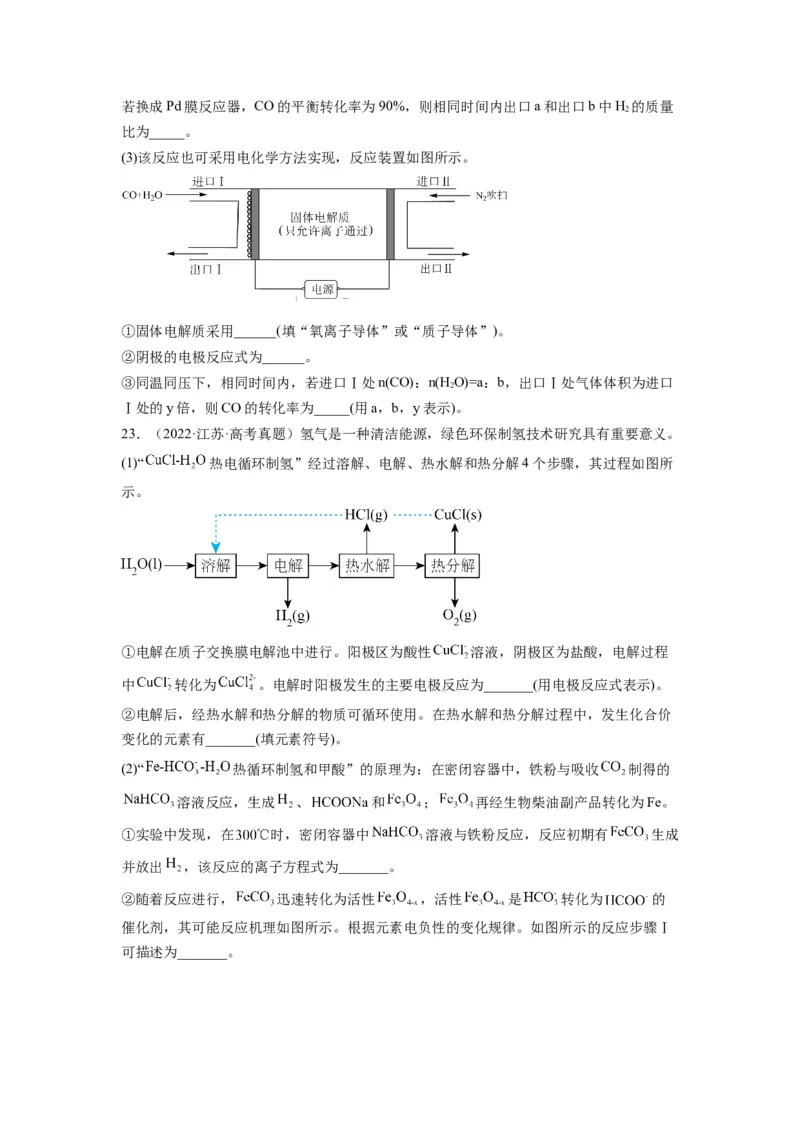
(1)“ 热电循环制氢”经过溶解、电解、热水解和热分解4个步骤,其过程如图所
示。
①电解在质子交换膜电解池中进行。阳极区为酸性 溶液,阴极区为盐酸,电解过程
中 转化为 。电解时阳极发生的主要电极反应为_______(用电极反应式表示)。
②电解后,经热水解和热分解的物质可循环使用。在热水解和热分解过程中,发生化合价
变化的元素有_______(填元素符号)。
(2)“ 热循环制氢和甲酸”的原理为:在密闭容器中,铁粉与吸收 制得的
溶液反应,生成 、 和 ; 再经生物柴油副产品转化为Fe。
①实验中发现,在 时,密闭容器中 溶液与铁粉反应,反应初期有 生成
并放出 ,该反应的离子方程式为_______。
②随着反应进行, 迅速转化为活性 ,活性 是 转化为 的
催化剂,其可能反应机理如图所示。根据元素电负性的变化规律。如图所示的反应步骤Ⅰ
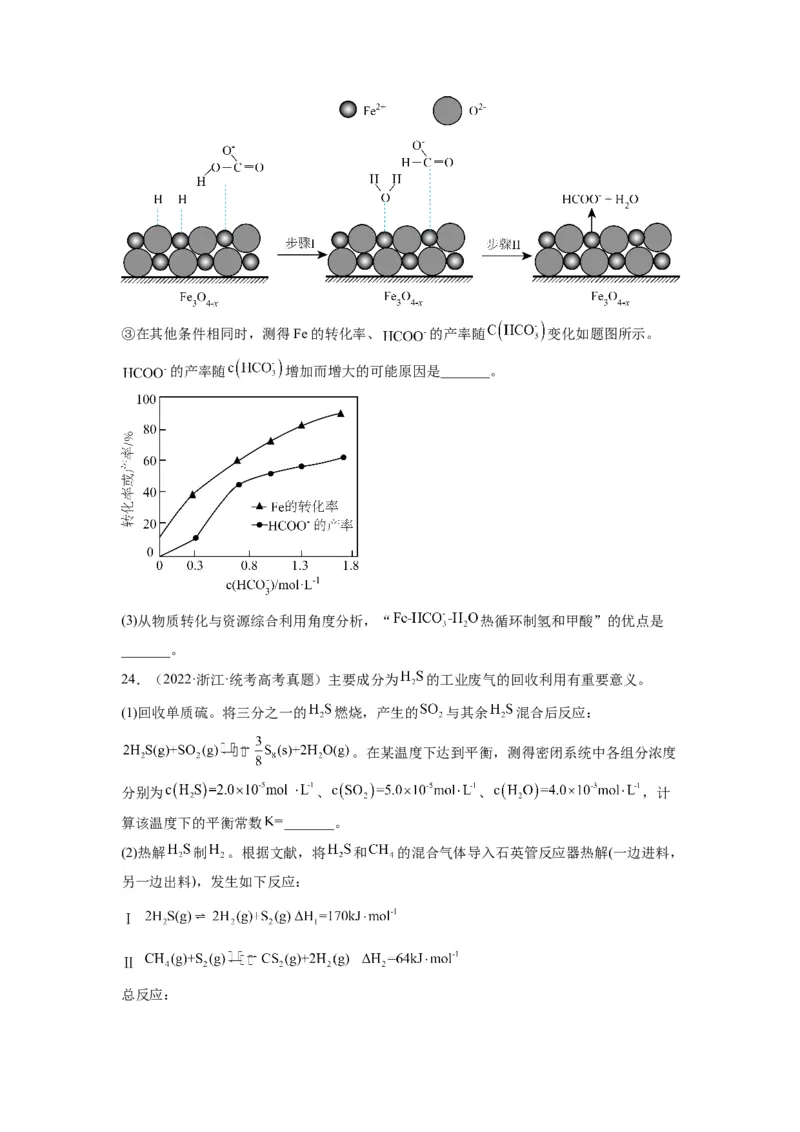
可描述为_______。③在其他条件相同时,测得Fe的转化率、 的产率随 变化如题图所示。
的产率随 增加而增大的可能原因是_______。
(3)从物质转化与资源综合利用角度分析,“ 热循环制氢和甲酸”的优点是
_______。
24.(2022·浙江·统考高考真题)主要成分为 的工业废气的回收利用有重要意义。
(1)回收单质硫。将三分之一的 燃烧,产生的 与其余 混合后反应:
。在某温度下达到平衡,测得密闭系统中各组分浓度
分别为 、 、 ,计
算该温度下的平衡常数 _______。
(2)热解 制 。根据文献,将 和 的混合气体导入石英管反应器热解(一边进料,
另一边出料),发生如下反应:
Ⅰ
Ⅱ
总反应:Ⅲ
投料按体积之比 ,并用 稀释;常压,不同温度下反应相同时间后,
测得 和 体积分数如下表:
温度/ 950 1000 1050 1100 1150
0.5 1.5 3.6 5.5 8.5
0.0 0.0 0.1 0.4 1.8
请回答:
①反应Ⅲ能自发进行的条件是_______。
②下列说法正确的是_______。
A.其他条件不变时,用Ar替代 作稀释气体,对实验结果几乎无影响
B.其他条件不变时,温度越高, 的转化率越高
C.由实验数据推出 中的 键强于 中的 键
D.恒温恒压下,增加 的体积分数, 的浓度升高
③若将反应Ⅲ看成由反应Ⅰ和反应Ⅱ两步进行,画出由反应原料经两步生成产物的反应过
程能量示意图_______。
④在 ,常压下,保持通入的 体积分数不变,提高投料比 ,
的转化率不变,原因是_______。
⑤在 范围内(其他条件不变), 的体积分数随温度升高发生变化,写出该
变化规律并分析原因_______。
25.(2022·湖南·高考真题)2021年我国制氢量位居世界第一,煤的气化是一种重要的制
氢途径。回答下列问题:
(1)在一定温度下,向体积固定的密闭容器中加入足量的 和 ,起始压强为
时,发生下列反应生成水煤气:Ⅰ.
Ⅱ.
①下列说法正确的是_______;
A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.平衡时 的体积分数可能大于
D.将炭块粉碎,可加快反应速率
②反应平衡时, 的转化率为 ,CO的物质的量为 。此时,整个体系
_______(填“吸收”或“放出”)热量_______kJ,反应Ⅰ的平衡常数 _______(以分压表
示,分压=总压×物质的量分数)。
(2)一种脱除和利用水煤气中 方法的示意图如下:
①某温度下,吸收塔中 溶液吸收一定量的 后, ,则该溶
液的 _______(该温度下 的 );
②再生塔中产生 的离子方程式为_______;
③利用电化学原理,将 电催化还原为 ,阴极反应式为_______。