文档内容
第 21 讲 电离平衡
1.下列关于电解质的叙述正确的是( )
A.电解质溶液的浓度越大,其导电性能一定越强
B.强酸和强碱一定是强电解质,不管其水溶液浓度的大小,都能完全电离
C.强极性共价化合物不一定都是强电解质
D.多元酸、多元碱的导电性一定比一元酸、一元碱的导电性强
【答案】C
【解析】A、D项,导电性取决于离子浓度及所带电荷数的多少,错误;B项,98.3%浓硫酸是强酸溶
液,由于水太少,硫酸大部分以硫酸分子的形式存在,错误;C项,HF是强极性共价化合物,但是弱电解
质,正确。
2.下列事实能证明HCOOH为弱酸的是( )
A.可与NaCO 反应生成CO
2 3 2
B.常温时HCOONa溶液的pH大于7
C.导电能力低于同浓度的硫酸
D.0.1 mol·L-1 HCOOH溶液可以使甲基橙变红
【答案】B
【解析】HCOOH能与NaCO 反应产生CO ,只能说明甲酸的酸性比碳酸强(同理盐酸也可),故A不
2 3 2
能证明其为弱酸;常温时HCOONa溶液的pH大于7,溶液显碱性,说明HCOONa为强碱弱酸盐,故B能
证明其为弱酸;导电性强弱与离子浓度有关,HCOOH为一元酸,硫酸为二元强酸,同浓度时,比较导电
性,即使HCOOH是强酸,导电性也比硫酸低,故C不能证明其为弱酸;0.1 mol·L-1 HCOOH溶液可以使
甲基橙变红只能说明HCOOH溶液显酸性,故D不能证明其为弱酸。
3.将0.1 mol·L-1的氨水加水稀释至0.01 mol·L-1,稀释过程中温度不变,下列叙述正确的是( )
A.稀释后溶液中c(H+)和c(OH-)均减小
B.稀释后溶液中c(OH-)变为稀释前的
C.稀释过程中氨水的电离平衡向左移动
D.稀释过程中溶液中增大
【答案】D
【解析】温度不变,水的电离常数不变,稀释后 c(OH-)减小,c(H+)增大,A错误;NH ·H O为弱电
3 2解质,稀释后溶液中c(OH-)大于稀释前的,B错误;NH ·H O为弱电解质,稀释过程中电离平衡向右移动,
3 2
C错误;同一溶液中,=,稀释过程中电离平衡向右移动,故n(OH-)增大,n(NH ·H O)减小,故增大,D
3 2
正确。
4.HS水溶液中存在电离平衡H S H++HS-和HS- H++S2-。下列说法正确的是( )
2 2
A.加水,平衡向右移动,溶液中氢离子浓度增大
B.通入过量SO 气体,平衡向左移动,溶液pH增大
2
C.滴加新制氯水,平衡向左移动,溶液pH减小
D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
【答案】C
【解析】向HS溶液中加水,平衡向右移动,但溶液体积增大,溶液中 H+浓度减小,A错误;通入SO,
2 2
可发生反应:2HS+SO===3S↓+2HO,SO 过量时,SO 与水反应生成的HSO 酸性比氢硫酸强,因此溶液pH
2 2 2 2 2 2 3
减小,B错误;滴加新制氯水,发生反应:HS+Cl===2HCl+S↓,HS浓度减小,平衡向左移动,反应生成的
2 2 2
盐酸为强酸,溶液酸性增强,pH减小,C正确;加入少量CuSO 固体,发生反应:CuSO +HS===CuS↓+
4 4 2
HSO,溶液中S2-浓度减小,H+浓度增大,D错误。
2 4
5.稀氨水中存在着电离平衡:NH·HO NH+OH-,若要使平衡向左移动,同时使 c(OH-) 增大,应
3 2
加入的适量物质或采取的措施是( )
①NHCl固体 ②硫酸 ③NaOH固体 ④水 ⑤加热
4
⑥加入少量MgSO 固体
4
A.①②③⑤ B.③⑥
C.③ D.③⑤
【答案】C
【解析】若在氨水中加入NHCl固体,c(NH)增大,平衡向左移动,c(OH-)减小,①不符合题意;硫酸中的
4
H+与OH-反应,使c(OH-)减小,平衡向右移动,②不符合题意;当在氨水中加入NaOH固体后,c(OH-)增大,
平衡向左移动,③符合题意;若在氨水中加入水,稀释溶液,平衡向右移动,c(OH-)减小,④不符合题意;电
离属于吸热过程,加热平衡向右移动,c(OH-)增大,⑤不符合题意;加入MgSO 固体发生反应:Mg2++2OH-
4
===Mg(OH)↓,溶液中c(OH-)减小,平衡向右移动,⑥不符合题意。
2
6.常温下,0.2 mol·L-1的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓
度如图所示。下列说法正确的是( )A.HA为强酸
B.该混合溶液pH=7.0
C.该混合溶液中:c(A-)+c(Y)=c(Na+)
D.图中X表示HA,Y表示OH-,Z表示H+
【答案】C
【解析】若HA为强酸,按题意两溶液混合后,所得溶液中c(A-)=0.1 mol·L-1,由图知A-浓度小于0.1
mol·L-1,表明A-发生水解,则HA为弱酸,根据水解原理,溶液中主要微粒的浓度大小关系应为c(Na+)>c(A
-)>c(OH-)>c(HA)>c(H+),可以判断X表示OH-,Y表示HA,Z表示H+,则A、B、D错误,C项满足物料守
恒,正确。
7.已知数据:7.2×10-4、4.6×10-4、4.9×10-10分别是三种酸的电离平衡常数,若已知这些酸可发生如下反
应:
①NaCN+HNO===HCN+NaNO
2 2
②NaCN+HF===HCN+NaF
③NaNO+HF===HNO+NaF
2 2
由此可判断下列叙述中不正确的是( )
A.HF的电离平衡常数为7.2×10-4
B.HNO 的电离平衡常数为4.9×10-10
2
C.根据①③两个反应即可知三种酸的相对强弱
D.HNO 的电离平衡常数比HCN大,比HF小
2
【答案】B
【解析】该题中涉及三个反应,由题中三个化学反应方程式(强酸制弱酸)可以得出:HF、HNO、HCN的酸
2
性依次减弱。酸性越强,电离平衡常数越大,据此将三个K值与酸对应起来,故A正确,B错误;反应①说明
酸性HNO>HCN,反应③说明酸性HF>HNO,故C、D正确。
2 2
8.电离度是描述弱电解质电离程度的物理量,电离度=×100%。现取20 mL c(H+)=1×10-3 mol·L-1的
CHCOOH溶液,加入0.2 mol·L-1的氨水,测得溶液导电能力的变化如图所示,则加入氨水前CHCOOH的电
3 3
离度为( )A.0.5% B.1.5%
C.0.1% D.1%
【答案】D
【解析】由题图可知,当加入10 mL氨水时,溶液的导电能力最强,即此时二者恰好完全反应,则有20
mL×c(CHCOOH)=0.2 mol·L-1×10 mL,则c(CHCOOH)=0.1 mol·L-1,故CHCOOH的电离度为×100%=1%。
3 3 3
9.相同温度下,关于盐酸和醋酸两种溶液的比较,下列说法正确的是( )
A.pH相等的两溶液中:c(CHCOO-)=c(Cl-)
3
B.分别中和pH相等、体积相等的两溶液,所需NaOH的物质的量相同
C.相同浓度的两溶液,分别与金属镁反应,反应速率相同
D.相同浓度的两溶液,分别与NaOH固体反应后呈中性的溶液中(忽略溶液体积变化):c(CHCOO-)=c(Cl
3
-)
【答案】A
【解析】在盐酸中存在电荷守恒:c(Cl-)+c(OH-)=c(H+),可推得c(Cl-)=c(H+)-c(OH-),同理在醋酸溶
液中存在:c(CHCOO-)=c(H+)-c(OH-),由于两者pH相等,即c(H+)-c(OH-)相同,故c(Cl-)=c(CHCOO
3 3
-),A项正确;由于盐酸为强酸,在水溶液中完全电离,醋酸为弱酸,在水溶液中部分电离,故 pH相等、体积
相等的两溶液,n(CHCOOH)>n(HCl),故醋酸溶液所需NaOH的物质的量较大,B项错误;相同浓度的两溶液
3
中醋酸溶液的c(H+)小于盐酸的c(H+),故与金属镁反应,反应速率不同,C项错误;取相同体积两溶液,所含
n(HCl)=n(CHCOOH),则恰好反应时需NaOH的物质的量相等,生成NaCl和CHCOONa,NaCl溶液呈中性,
3 3
由于CHCOO-的水解而使CHCOONa溶液呈碱性,为使溶液呈中性需要NaOH的物质的量应小于中和盐酸的
3 3
物质的量,存在c(CHCOO-)+c(OH-)=c(H+)+c(Na+)和c(Cl-)+c(OH-)=c(H+)+c(Na+),又因c(OH-)=c(H
3
+),故c(CHCOO-)=c(Na+)和c(Cl-)=c(Na+)。由于呈中性时,CHCOOH溶液中c(Na+)小于盐酸中c(Na+),
3 3
再由物料守恒可得c(CHCOO-)n
B.取等体积的两种酸溶液分别与完全一样的足量锌粒反应,开始时反应速率盐酸大于醋酸
C.取等体积的两种酸溶液分别中和NaOH溶液,醋酸消耗NaOH的物质的量比盐酸多
D.两种酸溶液中c(CHCOO-)=c(Cl-)
3
【答案】B
【解析】A项,由于弱酸溶液中存在电离平衡,故稀释相同倍数时,弱酸的 pH变化小,现pH变化相等,
则弱酸稀释的倍数大,正确;B项,由于两者的pH相同,故开始时反应速率相等,不正确;C项,pH相同的
情况下,醋酸的浓度远大于盐酸,故等体积时醋酸消耗的氢氧化钠多,正确;D项,根据电离关系可知,正确。
2.相同体积、相同pH的某一元强酸溶液①和某一元弱酸溶液②分别与足量的锌粉发生反应,下列关于氢
气体积(V)随时间(t)变化的示意图正确的是( )
【答案】C
【解析】强酸完全电离,弱酸部分电离,随着反应的进行,弱酸会继续电离出H+,所以溶液②产生氢气的
体积多,在相同时间内,②的反应速率比①快,故选C。
2.醋酸为一元弱酸,25 ℃时,其电离常数K=1.75×10-5。下列说法错误的是( )
a
A.0.1 mol·L-1 CHCOOH溶液的pH在2~3范围内
3
B.CHCOONa溶液中,c(CHCOOH)+c(H+)=c(OH-)
3 3
C.将0.1 mol·L-1 CHCOOH溶液加水稀释,其电离常数和均不变
3D.等体积的 0.1 mol·L-1 NaOH 溶液和 0.1 mol·L-1 CHCOOH 溶液混合后,溶液 pH>7,且 c(Na
3
+)>c(CHCOO-)>c(OH-)>c(H+)
3
【答案】C
【解析】K==1.75×10-5,c(H+)≈c(CHCOO-),则c(H+)== mol·L-1=×10-3 mol·L-1,pH=-lg(×10-
a 3
3)=3-lg,因2=3-lg<3-lg<3-lg=3,则溶液的pH在2~3范围内,故A正确;CHCOONa溶液中,根据
3
质子守恒得:c(CHCOOH)+c(H+)=c(OH-),故 B 正确;温度不变,则电离常数不变,将 0.1 mol·L-1
3
CHCOOH溶液加水稀释,c(CHCOO-)减小,K=,增大,故C错误;等体积的0.1 mol·L-1 NaOH溶液和0.1
3 3 a
mol·L-1 CHCOOH溶液混合后,溶液溶质为CHCOONa,pH>7,则c(Na+)>c(CHCOO-)>c(OH-)>c(H+),故D
3 3 3
正确。
4.一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是
( )
A.a、b、c三点溶液的pH:c<a<b
B.a、b、c三点CHCOOH的电离程度:c<a<b
3
C.用湿润的pH试纸测量a处溶液的pH,测量结果偏小
D.a、b、c三点溶液用1 mol·L-1NaOH溶液中和,消耗NaOH溶液体积:c<a<b
【答案】C
【解析】A项,由导电能力知c(H+):b>a>c,故pH:c>a>b,错误;B项,加水体积越大,越利于
CHCOOH电离,故电离程度:c>b>a,错误;C项,用湿润的pH试纸测量a处溶液的pH,相当于稀释a点溶
3
液,c(H+)增大,pH偏小,正确;D项,a、b、c三点n(CHCOOH)相同,用NaOH溶液中和时消耗n(NaOH)相
3
同,故消耗V(NaOH):a=b=c,错误。
5.已知室温时,0.1 mol·L-1某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )
A.该溶液的pH=4
B.升高温度,溶液的pH增大
C.此酸的电离平衡常数约为1×10-7
D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
【答案】B
【解析】根据HA在水中的电离度可算出c(H+)=0.1%×0.1 mol·L-1=10-4 mol·L-1,所以pH=4,故A正确;因HA在水中有电离平衡,升高温度,促进平衡向电离的方向移动,所以 c(H+)将增大,pH会减小,故B错误;
由平衡常数表达式算出K==1×10-7,故C正确;c(H+)=10-4 mol·L-1,所以c(H+)HO=10-10 mol·L-1,前者
a 2
是后者的106倍,故D正确。
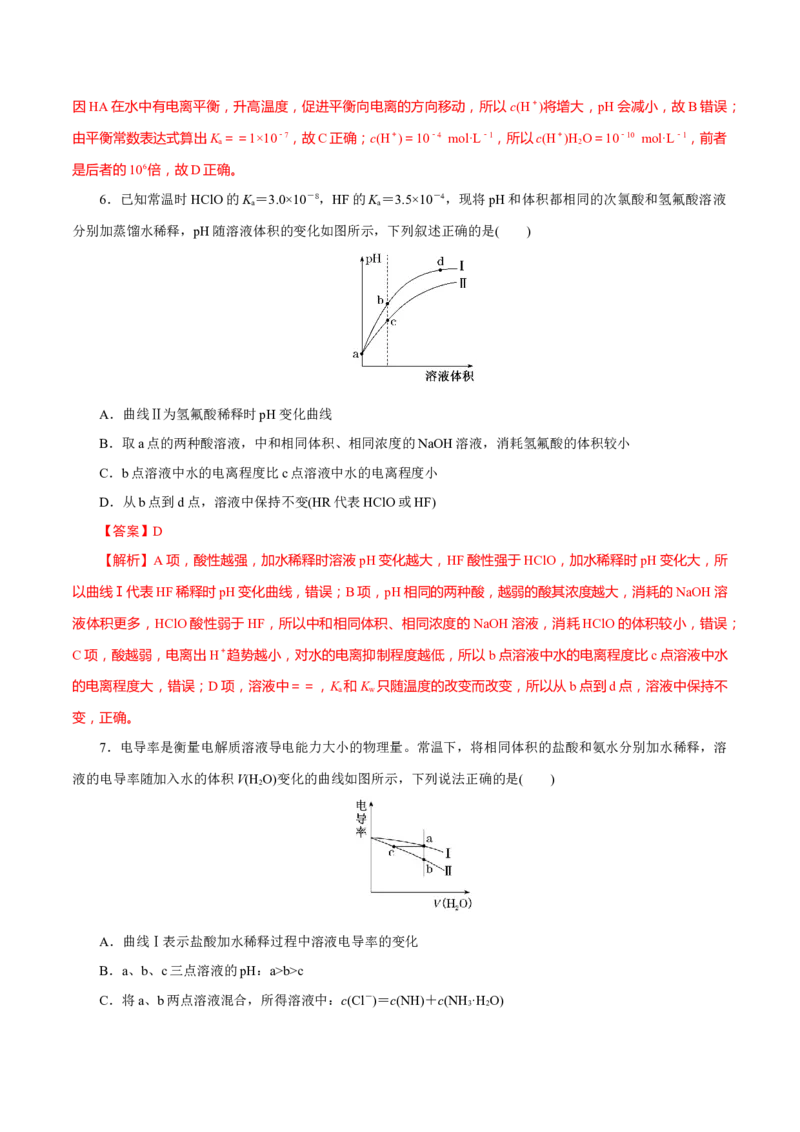
6.已知常温时HClO的K=3.0×10-8,HF的K=3.5×10-4,现将pH和体积都相同的次氯酸和氢氟酸溶液
a a
分别加蒸馏水稀释,pH随溶液体积的变化如图所示,下列叙述正确的是( )
A.曲线Ⅱ为氢氟酸稀释时pH变化曲线
B.取a点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗氢氟酸的体积较小
C.b点溶液中水的电离程度比c点溶液中水的电离程度小
D.从b点到d点,溶液中保持不变(HR代表HClO或HF)
【答案】D
【解析】A项,酸性越强,加水稀释时溶液pH变化越大,HF酸性强于HClO,加水稀释时pH变化大,所
以曲线Ⅰ代表HF稀释时pH变化曲线,错误;B项,pH相同的两种酸,越弱的酸其浓度越大,消耗的NaOH溶
液体积更多,HClO酸性弱于HF,所以中和相同体积、相同浓度的NaOH溶液,消耗HClO的体积较小,错误;
C项,酸越弱,电离出H+趋势越小,对水的电离抑制程度越低,所以b点溶液中水的电离程度比c点溶液中水
的电离程度大,错误;D项,溶液中==,K 和K 只随温度的改变而改变,所以从b点到d点,溶液中保持不
a w
变,正确。
7.电导率是衡量电解质溶液导电能力大小的物理量。常温下,将相同体积的盐酸和氨水分别加水稀释,溶
液的电导率随加入水的体积V(HO)变化的曲线如图所示,下列说法正确的是( )
2
A.曲线Ⅰ表示盐酸加水稀释过程中溶液电导率的变化
B.a、b、c三点溶液的pH:a>b>c
C.将a、b两点溶液混合,所得溶液中:c(Cl-)=c(NH)+c(NH·HO)
3 2D.氨水稀释过程中,不断减小
【答案】B
【解析】加水稀释时,一水合氨进一步电离,导电能力变化较小,则曲线Ⅰ为氨水稀释曲线,故 A错误;
盐酸显酸性,氨水显碱性,导电能力越大,说明离子浓度越大,则a、b、c三点溶液的pH:a>b>c,故B正确;
将a、b两点溶液混合,由于氨水浓度大于盐酸浓度,反应后氨水过量,所以溶液显碱性,c(Cl-)c点
C.从c点到d点,溶液中保持不变(其中HA、A-分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
【答案】C
【解析】根据HNO 和CHCOOH的电离常数,可知酸性:HNO>CHCOOH,相同pH的两种酸溶液,稀
2 3 2 3
释相同倍数时,弱酸的pH变化较小,故曲线Ⅰ代表CHCOOH溶液,A项错误;两种酸溶液中水的电离受到抑
3
制,b点溶液pH小于c点溶液pH,则b点对应酸电离出的c(H+)大,对水的电离抑制程度大,故水的电离程度:
b点c(HNO),故n(CHCOOH)>n(HNO),因此与NaOH恰
3 2 3 2
好中和后,溶液中n(Na+)不同,D项错误。
4.(2019·江苏卷)室温下,反应 +H O HCO+OH−的平衡常数K=2.2×10−8。将NH HCO 溶
2 2 3 4 3
液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室温时下列指
定溶液中微粒物质的量浓度关系正确的是
A.0.2 mol·L−1氨水:c (NH ·H O)>c( )> c (OH−)> c (H+)
3 2
B.0.2 mol·L−1NH HCO 溶液(pH>7):c ( )> c ( )> c (H CO)> c (NH ·H O)
4 3 2 3 3 2
C.0.2 mol·L−1氨水和0.2 mol·L−1NH HCO 溶液等体积混合:c( )+c(NH ·H O)=c(H CO)+c (
4 3 3 2 2 3
)+c( )D.0.6 mol·L−1氨水和0.2 mol·L−1 NH HCO 溶液等体积混合:c (NH ·H O)+ c( )+ c(OH−)=
4 3 3 2
0.3 mol·L−1+ c (H CO)+ c (H+)
2 3
【答案】BD
【解析】NH ∙H O属于弱碱,部分电离,氨水中存在的电离平衡有:NH ∙H O NH ++OH-,HO
3 2 3 2 4 2
H++OH-,所以c(OH-)>c(NH+),A错误;NH HCO 溶液显碱性,说明HCO -的水解程度大于NH +的
4 4 3 3 4
水解,所以c(NH +)>c(HCO-),HCO -水解:HO+HCO - HCO+OH-,NH +水解:NH ++H O
4 3 3 2 3 2 3 4 4 2
NH ∙H O+H+,前者水解程度大且水解都是微弱的,则c(HCO)>c(NH∙H O),B正确;由物料守恒,
3 2 2 3 3 2
n(N):n(C)=2:1,则有c(NH +)+c(NH∙H O)=2[c(HCO)+c(HCO-)+c(CO 2-)],C错误;由物料守恒,
4 3 2 2 3 3 3
n(N):n(C)=4:1,则有c(NH +)+c(NH∙H O)=
4 3 2
4[c(HCO)+c(HCO-)+c(CO 2-)]①;电荷守恒有:c(NH +)+c(H+)=c(HCO-)+2c(CO 2-)+c(OH-)②;结合①②消
2 3 3 3 4 3 3
去c(NH +)得:c(NH ∙H O)+c(OH-)=c(H+)+4c(H CO)+3c(HCO-)+2c(CO 2-)③,0.2mol/LNH HCO 与0.6mol/L
4 3 2 2 3 3 3 4 3
氨水等体积混合后瞬间c(NH HCO )=0.1mol/L,由碳守恒有,c(HCO)+c(HCO-)+c(CO 2-)=0.1mol/L④,将
4 3 2 3 3 3
③等式两边各加一个c(CO2-),则有c(NH ∙H O)+c(OH-)+c(CO 2-)=c(H+)+c(H CO)+3c(H CO)+3c(HCO-)
3 3 2 3 2 3 2 3 3
+3c(CO 2-),将④带入③中得,c(NH ∙H O)+c(OH-)+c(CO 2-)=c(H+)+c(H CO)+0.3mol/L,故D正确;故选
3 3 2 3 2 3
BD。