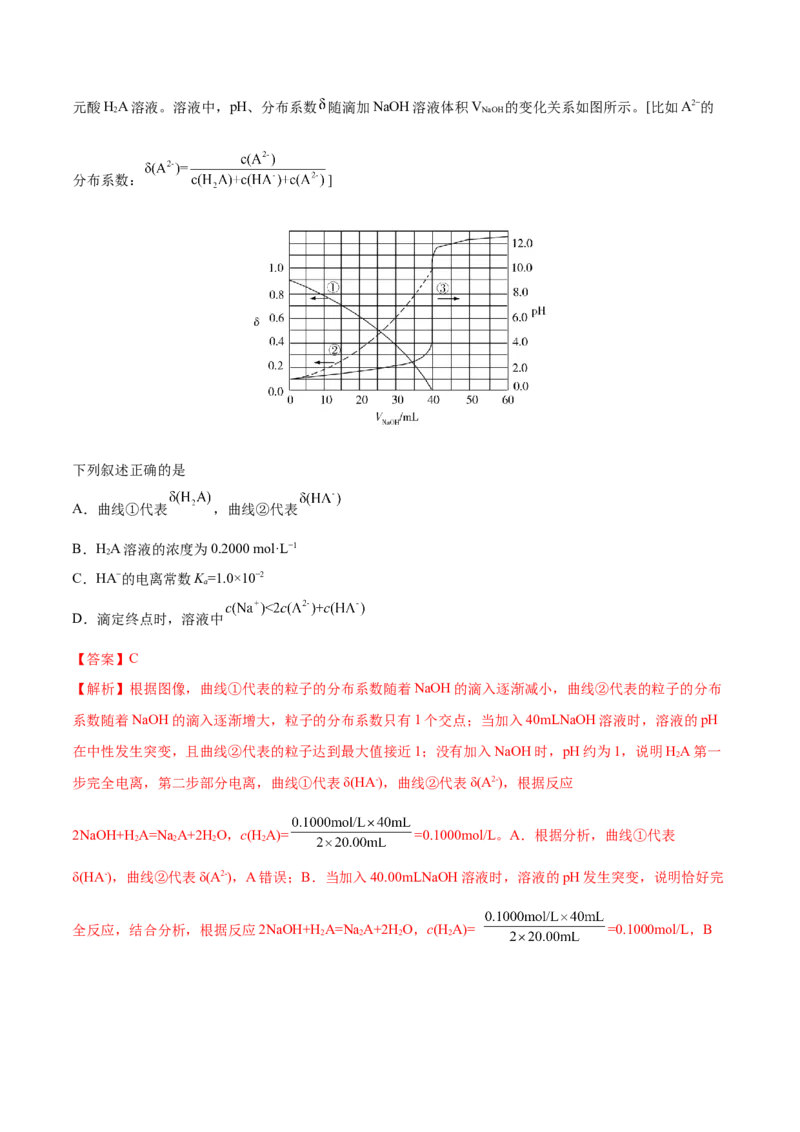
文档内容
第 24 讲 水的电离和溶液的 pH
第一部分:高考真题感悟
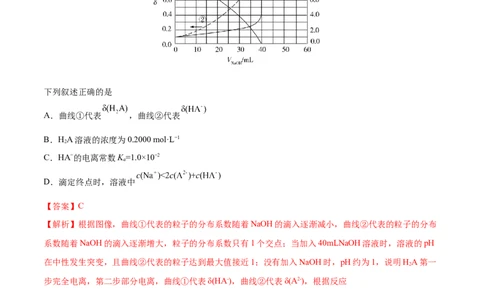
1.(2022·浙江·高考真题)已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说法正确的是
2 a1 a2
A.在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为0.013%
2 2
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
【答案】B
【解析】A.在等浓度的NaA、NaHA溶液中,A2-的水解程度大于HA-,水的电离程度前者大于后者,故
2
A错误;B.溶液中c(H+)=10-3mol/L,HA电离程度较小,溶液中c(HA)≈0.1mol/L,K =
2 2 a1
,c(HA-)=1.3×10-5mol/L,c(HA-)≈c(HA) ,则HA的电离度
2 电离 2
0.013%,故B正确;C.向HA溶液中加入NaOH溶液至pH=11,
2
,则c(A2-)T
1 2
B.K :b>c>a>d=e
w
C.b→c点可通过在水中加入适量的CHCOONa(s)实现
3
D.T 时,将pH=10的NaOH(aq)与pH=3的HSO (aq)等体积混合,溶液呈碱性
2 2 4
【答案】D
【解析】A.水的电离是吸热反应,温度升高电离平衡正向移动,c(H+)和c(OH-)都增大,由图可知,
T>T,A错误;B.K 只受温度影响,温度不变,K 不变,ade点都处于同一温度下,则三点的Kw相等,
2 1 w w
b点c(H+)和c(OH-)都大于a点的,由K =c(H+)∙c(OH-)可知,b点Kw大于c点大于a点,则K :
w w
b>c>a=d=e,B错误;C.b→c点K 变小,是降温导致的,在水中加入适量的CHCOONa(s)但温度不变,
w 3
不能改变K ,C错误;D.T 时,K =c(H+)∙c(OH-)=10-6×10-6=10-12,pH=10的NaOH(aq)其c(OH-)=
w 2 w
,pH=3的HSO (aq)其c(H+)=10-3mol/L,两者等体积混合,n(OH-)过量,则溶液呈
2 4
碱性,D正确;故选:D。
9.(2022·河南河南·模拟预测)常温下,在体积均为10.0mL、浓度均为0.10mol·L-1的HX、HY溶液中分
别滴加某浓度的NaOH溶液,pOH [pOH =-lgc( ),c( )表示溶液中水电离出的OH-的浓度]与滴
水 水
加NaOH溶液的体积的关系如图所示,下列说法正确的是
A.HX、HY均为弱酸,HY的酸性更强
B.NaOH溶液浓度c(NaOH)=0.1mol·L-1
C.M、N两点的溶液中:c(X-)与c(Y-)不相等
D.常温下HY的电离常数K≈5.4×10-6
a
【答案】C
【解析】酸、碱对水的电离均起到抑制作用,pOH 越小,说明水的电离程度越大,根据图像可知,当加
水入20mLNaOH溶液时,pOH 达到最低,说明酸与NaOH完全反应,此时溶液的pH≠7,推出两种酸为弱
水
酸,利用“越弱越水解”,推出酸性HX>HY;A.当加入20mLNaOH溶液时,两条曲线均达到最低点,
pOH 最小,且不为7,说明此时水的电离程度最大,即恰好完全中和,同时说明HX、HY为弱酸,利用
水
“越弱越水解”,推出酸性HX>HY,故A说法错误;B.根据A选项分析,当加入20mLNaOH溶液时,
两种酸与NaOH恰好完全中和,NaOH物质的量浓度是酸的一半,即为0.050mol/L,故B说法错误;C.
根据电荷守恒,推出c(Na+)+c(H+)=c(OH-)+c(Y-)、c(Na+)+c(H+)=c(OH-)+c(X-),M、N点溶液显中性,即有
c(Na+)= c(Y-)、c(Na+)= c(X-),因为两点c(Na+)不同,则c(Y-)≠c(X-),故C说法正确;D.取M点计算HY的
电离平衡常数,c(Na+)= c(Y-)= ,根据物料守恒,c(HY)=
,Ka= =5.4×10-8,故D说
法错误;答案为C。
10.(2022·黑龙江绥化·模拟预测)已知pOH=-lgc(OH-)。初始温度20℃时,向20mL0.1mol·L-1氨水中滴加
0.05mol·L-1的稀硫酸,测得混合溶液的温度T、pOH随加入稀硫酸体积V的变化如图所示。
下列说法正确的是
A.a、b、c三点对应NH 的水解平衡常数:K(c)>K (b)>K(a)
h h h
B.a点溶液中水电离产生的c <(OH-)=0.001mol·L-1
水
C.图中x=7,b点溶液中,c(NH )>2c(SO )
D.若V=40,则c点对应溶液中c(H+)=c(OH-)+c(NH )+2c(NH·H O)
3 3 2
【答案】D【解析】A.升高温度能促进NH 的水解,水解平衡常数增大,由题图可知,温度T(b)>T(a)>T(c),则a、
b、c三点对应NH 的水解平衡常数:K(b)>K(a)>K (c),A项错误;B.a点溶液的pOH==3,
h h h
c(OH-)=0.001mol.·L-1,pH=11,溶液的溶质为NH ·H O和(NH )SO ,NH ·H O过量且抑制水的电离,水电
3 2 4 2 4 3 2
离产生的H+的物质的量浓度为10-11mol·L-1,故水电离产生的OH-的物质的量浓度为10-11mol·L-1,B项错误;
C.根据电荷平衡,在b点c(NH )+c(H+)=2c(SO )+c(OH-),b点时温度高于25°C,故K >10-14,当
w
c(OH-)=10-7时,c(H+)>c(OH-),C项错误;D.c点溶液中,加入稀硫酸的体积为40mL,则原氨水中的
NH ·H O和加入的稀硫酸中的HSO 的物质的量相等,溶液的溶质是HSO 和(NH )SO ,根据电荷守恒:
3 2 2 4 2 4 4 2 4
c(NH )+c(H+)=2c(SO )+c(OH-),物料守恒:c(NH ·H O)+c(NH )=c(SO ),可得:c(H+)=c(OH-)+c(NH )
3 2
+2c(NH·H O),D项正确;答案选D。
3 2
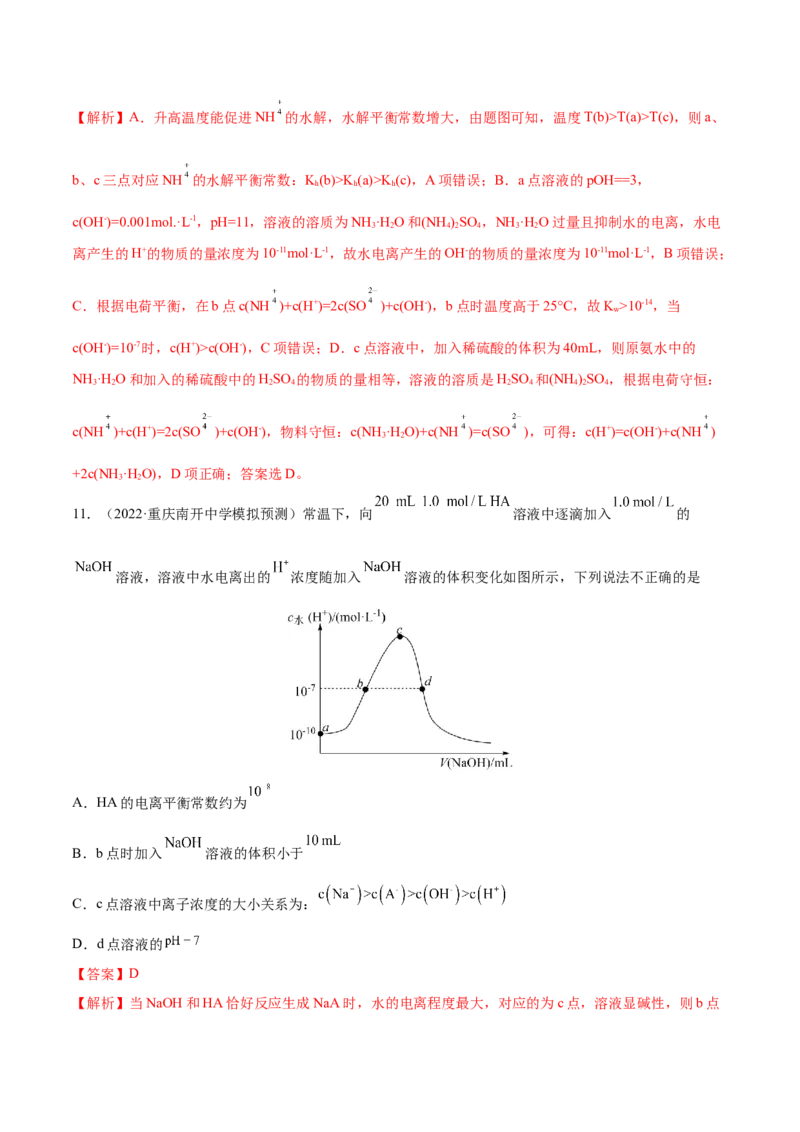
11.(2022·重庆南开中学模拟预测)常温下,向 溶液中逐滴加入 的
溶液,溶液中水电离出的 浓度随加入 溶液的体积变化如图所示,下列说法不正确的是
A.HA的电离平衡常数约为
B.b点时加入 溶液的体积小于
C.c点溶液中离子浓度的大小关系为:
D.d点溶液的
【答案】D
【解析】当NaOH和HA恰好反应生成NaA时,水的电离程度最大,对应的为c点,溶液显碱性,则b点为HA和NaA的混合溶液,溶液显中性,d点为NaA和NaOH的混合溶液,溶液显碱性。A. a点表示
中水电离出氢离子浓度为10-10mol/L,则c(OH-)=10-10mol/L,c(H+)=10-4mol/L,则HA的电离
平衡常数约为 ,故A正确;B. 当加入 溶液时,溶液中为等物质的量浓度的
NaA和HA,HA的电离常数为10-8,A-的水解常数为 ,则A-的水解程度大于HA的电离程度,
此时溶液显碱性,而b点溶液显中性,则b点时加入 溶液的体积小于 ,故B正确;C. c点恰
好为NaA溶液,A-水解使溶液显碱性,此时溶液中离子浓度的大小关系为:
,故C正确;D. d点溶液显碱性, ,故D错误;故选C。
12.(2022·浙江·模拟预测)下列说法不正确的是
A.任何水溶液的
B.25℃,1 ml pH=5的 溶液稀释到 ,所得溶液的 接近7
C.25℃时, 与 的电离平衡常数相等,某浓度的 溶液的pH=4.3,则相同浓度的
溶液的
D.25℃时,当 和 的物质的量之比为1∶2溶于水得到的溶液 ,则溶液中
【答案】A
【解析】A.K 只与温度有关,温度不同K 值不同,故应为25℃时,任何水溶液的 ,A项错
w w
误;B.25℃,1 ml pH=5的 溶液稀释1000倍,但酸溶液再稀释也不可能稀释成中性溶液或者
碱性溶液,故所得溶液的 接近7,B项正确;C.25℃时, 与 的电离平衡常数相等,说明 和CHCOO-水解能力相同,某浓度的 溶液的pH=4.3,说明 水解生成的c(H+)约为10-
3
4.3mol/L,故相同浓度的 溶液,CHCOO-水解生成的c(OH-)约为10-4.3mol/L,故 ,C项正
3
确;D.pH=7,根据电荷守恒可得c(Na+)=c(X-),再根据物料守恒3c(Na+)= c(HX)+c(X-),故可得
c(X-)∶c(HX)=1∶2,D项正确;答案选A。
二、主观题(共3小题,共40分)
13.(2020·江苏南通·一模)(10分)KI和KBr都具有感光性,可以用来制作感光材料。某感光材料主要
成分为KBr和KI,测定其中KBr含量的方法如下:
①称取试样1.000 g,溶解后制备成200.0 mL溶液。
②取50 mL上述溶液,用Br 水将I-氧化成IO -,除去过量Br ,加入过量KI,酸化溶液,加入指示剂,以
2 3 2
0.100 0 mol·L-1 Na SO 溶液滴定析出的I,终点时消耗30 mL。
2 2 3 2
③另取50.00 mL试液,酸化后加入足量KCr O 溶液处理,将释放出的I 和Br 蒸馏收集于含有过量KI的
2 2 7 2 2
溶液中,反应完全后,加入指示剂,以0.100 0 mol·L-1的NaSO 溶液滴定其中的I 至终点,消耗15.00
2 2 3 2
mL 。
(1)写出第②步中用Br 水氧化I-的离子方程式:________。
2
(2)第②步除去过量Br 最简单的物理方法是________;若未除去过量的Br ,对KBr含量测定结果的影响是
2 2
________(填“偏大”“偏小”或“无影响”)。
(3)计算试样中KBr的质量分数_______ (写出计算过程)。
【答案】(1、2问每空2分、第3问4分)(1)3H O+3Br +I-=IO -+6Br-+6H+
2 2 3
(2)煮沸 偏小
(3)由题意可得关系: I- ~ IO - ~ 3I ~ 6SO2-
3 2 2 3
n(I-) 0.100 0 mol·L-1×30×10-3 L
2.5 g(50 mL)样品中n(I-)=0.5×10-3 mol
用KCr O 溶液处理后,该部分I-氧化为I,其物质的量为n(I) =0.5n(I-)=2.5×10-4 mol
2 2 7 2 2
该部分溶液中总的n(I) =0.5×0.100 0 mol·L-1×15×10-3 L=7.5×10-4 mol
2 总
被Br 氧化产生的I 的物质的量为7.5×10-4 mol-2.5×10-4 mol=5×10-4 mol
2 2
2Br- ~ Br ~ I
2 2
n(Br-) 5×10-4 mol
n(KBr)=n(Br-)=1×10-3 mol
则KBr的质量分数为KBr%=119 g·mol-1×1×10-3 mol÷0.250 0 g×100%=47.60%【解析】(1)根据题目,反应的离子方程式为3HO+3Br +I-=IO -+6Br-+6H+;
2 2 3
(2)Br 易蒸发,故为最简单的物理方法;若未除尽过量的Br ,加入过量KI后溴单质继续和KI中的I-发
2 2
生反应,使滴定析出的I 量减小,导致最后对KBr的测定结果偏小;
2
(3)计算过程如下:
由题意可得关系:I-~IO -~3I~6SO2-
3 2 2 3
n(I-)=0.100 0 mol·L-1×30×10-3 L
50 mL样品中n(I-)=0.5×10-3 mol
用KCr O 溶液处理后,该部分I-氧化为I,其物质的量为n(I)=0.5n(I-)=2.5×10-4 mol
2 2 7 2 2
该部分溶液中总的n(I) =0.5×0.100 0 mol·L-1×15×10-3 L=7.5×10-4 mol
2 总
被Br 氧化产生的I 的物质的量为7.5×10-4 mol-2.5×10-4 mol=5×10-4 mol
2 2
2Br-~Br ~I
2 2
n(Br-)=5×10-4 mol
n(KBr)=n(Br-)=1×10-3 mol
则KBr的质量分数为KBr%=119 g·mol-1×1×10-3 mol÷0.2500 g×100%=47.60%
14.(2021·河南·模拟预测)(16分)草酸、KMnO 均是重要的化学分析试剂,某次实验中需要使用
4
480mL0.2000mol/L的草酸溶液,回答下列问题。
(1)实验中需要称取___________g草酸晶体(H C O•2H O),称量后___________(填“需要”或“不需要”)
2 2 4 2
加热除去相应的结晶水;配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管及___________。
(2)假设称取草酸时使用的是托盘天平,称量中试剂与砝码位置错放,则所配制溶液中c(HC O)0.2000
2 2 4
___________ (填“>”、“=”或“<”,下同);若定容时俯视刻度线,则所配溶液中
c(HC O)___________0.2000 。
2 2 4
(3)若配置溶液时所取草酸晶体不纯(杂质无还原性),为测定草酸的纯度,某同学量取20.00mL,上述所配
溶液放入锥形瓶中,然后用0.1000 的酸性KMnO 标准溶液滴定(氧化产物是CO),滴定终点时消耗
4 2
VmL标准溶液。
①标准溶液应使用___________(填“酸”或“碱”)式滴定管取用,合理的V值可能是___________。
A. 15.8 B. 16.20 C. 15.82 D. 16.18
②滴定终点时溶液颜色的变化为___________,样品中草酸品体的质量分数为___________(用含V的式子
表示)。【答案】(每空2分)(1)12.6 不需要 500mL容量瓶、烧杯
(2)
(3)①酸 C ②由无色变成浅红色且在30S内保持不变 6.25V%
【解析】(1)因没有480mL的容量瓶,故实际配制的是500mL溶液,因此所需要的溶质是
,结晶水不需要加热除去,因为溶解后结晶水转化为溶剂。配制过程中
需要使用的玻璃仪器有玻璃棒、胶头滴管及500mL容量瓶、烧杯。
(2)配制溶液时还需要500mL容量瓶、烧杯。当试剂与砝码位置错放时,称量的试剂质量小于12.6g,故最
后所配溶液浓度肯定小于0.2000 。定容俯视刻度时,实际液面在刻度线下,故所配溶液浓度大于
0.2000mol/L。
(3)①应使用酸式滴定管量取KMNO 溶液。当样品为纯净物时,由得失电子守恒及元素化合价变化可得
4
, ,由于草酸晶体不纯(杂质无还原性)故实际
消耗的KMnO 溶液不可能大于16.00mL,B、D项错误;以“mL”为单位时应保留两位小数,C项合理。
4
②滴定终点时溶液颜色的变化为由无色变成浅红色且在30S内保持不变,设所配溶液中
,则有 , ,故样品
中草酸晶体纯度为 。
14.(2022·黑龙江实验中学高三阶段练习)(14分)酸与碱作用生成盐和水的反应叫做中和反应,它在
工农业生产和日常生活中有广泛应用。
Ⅰ.某实验小组用50mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在图示的装置中进行中和反应。通过
测定反应过程中所放出的热量可计算中和热。
(1)测定中和热实验。从实验装置上看,图中尚缺少的一种玻璃用品是___,烧杯间填满碎纸条的作用是___。(2)实验数据如表:
起始温度℃
实验序数 终止温度℃
盐酸 NaOH溶液
1 25.1 25.3 26.2
2 25.1 25.5 28.6
3 25.2 25.4 28.5
4 25.2 25.6 28.8
近似认为0.50mol·L-1盐酸与0.55mol·L-1NaOH溶液的密度都是1g/cm3,中和反应后生成溶液的比热容
c=4.18J/(g·℃)。则中和热ΔH=___(取小数点后一位)。
(3)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会___(填“偏大”“偏
小”“无影响”),原因是___。
Ⅱ.实验室中有一未知浓度的稀盐酸,某学生应用中和反应测定盐酸的浓度在实验室中进行实验。
(4)取20.00mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用0.1000mol/LNaOH标准溶液
进行滴定,滴定前排气泡时,应选择图中的___(填字母);简述排气泡的操作___。
a. b. c. d.
(5)滴定达到终点的标志是___。
(6)若滴定开始和结束时,碱式滴定管中的液面如图所示,所用NaOH标准溶液的体积为___mL。根据上述
数据,可计算出该盐酸的浓度约为___mol/L。
(7)在上述实验中,下列操作(其他操作正确)会造成测定结果偏低的有___。A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C.锥形瓶水洗后未干燥D.碱式滴定管尖嘴部分有气泡,滴定后消失
【答案】(除标注外,每空2分)(1)环形玻璃搅拌棒(1分) 保温、隔热、减少实验过程中热量损失(1
分)
(2)-55.2kJ·mol-1
(3)偏小(1分) NH •H O电离吸热(1分)
3 2
(4)c(1分) 将胶管弯曲使玻璃尖嘴向上倾斜,用两指捏住胶管,轻轻挤压玻璃珠的中上部,使液体从尖
嘴流出
(5)滴入最后一滴标准液,溶液由无色变为浅粉红色,且半分钟内不褪色(1分)
(6)26.10(1分) 0.1300(1分)
(7)AB
【解析】(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒,烧杯间填满碎纸条的作用是
保温、隔热、减少实验过程中热量损失。
(2)第一次数值偏差太大,舍去,后三次的平均温度差为 ℃,Q=cm
T=4.18×100×3.3J=1.3794kJ,生成水的物质的量为0.5mol/L×0.05L=0.025mol, H=- =- kJ/
mol=-55.2kJ·mol-1。
(3)由于氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量小于
57.3kJ,用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会偏小,故答案为:
偏小;氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量小于
57.3kJ。
(4)排去碱式滴定管中气泡的方法应采用如图所示操作中的c操作,将胶管弯曲使玻璃尖嘴向上倾斜,用两
指捏住胶管,轻轻挤压玻璃珠的中上部,使液体从尖嘴流出。
(5)滴定达到终点的标志是滴入最后一滴标准液,溶液由无色变为浅粉红色,且半分钟内不褪色。
(6)碱式滴定管中的液面如图所示,所用NaOH标准溶液的体积为26.10mL,盐酸的浓度约为
mol/L=0.1300mol/L。
(7)根据 ,V(NaOH)偏大,则c(HCl)偏高,反之,偏低。A.滴定终点读数时俯视
读数,V(NaOH)偏小,则c(HCl)偏低;B.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗,所需V(NaOH)偏小,则c(HCl)偏低;C.锥形瓶水洗后未干燥,无影响;D.碱式滴定管尖嘴部分有气泡,滴定后
消失,则V(NaOH)读数偏大,则c(HCl)偏高;故选AB。