文档内容
第 31 讲 晶体结构与性质
1.下列关于化学式为[TiCl(H O) ]Cl ·H O的配合物的说法正确的是( )
2 5 2 2
A.配体是Cl-和HO,配位数是9
2
B.中心离子是Ti4+,配离子是[TiCl(H O) ]2+
2 5
C.内界和外界中的Cl-的数目比是1∶2
D.加入足量AgNO 溶液,所有Cl-均被完全沉淀
3
2.下列说法错误的是( )
A.分子晶体中一定存在分子间作用力,不一定存在共价键
B.原子晶体中只含有共价键
C.任何晶体中,若含有阳离子就一定含有阴离子
D.单质的晶体中一定不存在离子键
3.利用反应CCl +4Na=====C(金刚石)+4NaCl可实现人工合成金刚石。下列关于该反应的说法错
4
误的是( )
A.C(金刚石)属于共价晶体
B.该反应利用了Na的强还原性
C.CCl 和C(金刚石)中的C的杂化方式相同
4
D.NaCl晶体中每个Cl-周围有8个Na+
4.根据下表中给出的有关数据,判断下列说法错误的是( )
AlCl SiCl 晶体硼 金刚石 晶体硅
3 4
熔点/℃ 190 -68 2 300 >3 550 1 415
沸点/℃ 178 57 2 550 4 827 2 355
A.SiCl 是分子晶体
4
B.晶体硼是原子晶体
C.AlCl 是分子晶体,加热能升华
3
D.金刚石中的C—C键比晶体硅中的Si—Si键弱
5.许多过渡金属离子对多种配体有很强的结合力,能形成种类繁多的配合物。下列说法不正确的是(
)
A.向配合物[CoBr(NH )]SO 的溶液中加入BaCl 溶液,有白色沉淀生成
3 5 4 2
B.配离子[Cu(HO)]2+中的Cu2+提供接受孤电子对的空轨道,HO中的O提供孤电子对
2 6 2C.配合物[Cu(NH )]SO ·H O的配体为NH 和HO
3 4 4 2 3 2
D.配合物[Ag(NH )]OH的配位数为2
3 2
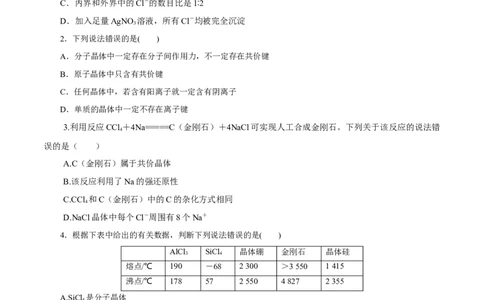
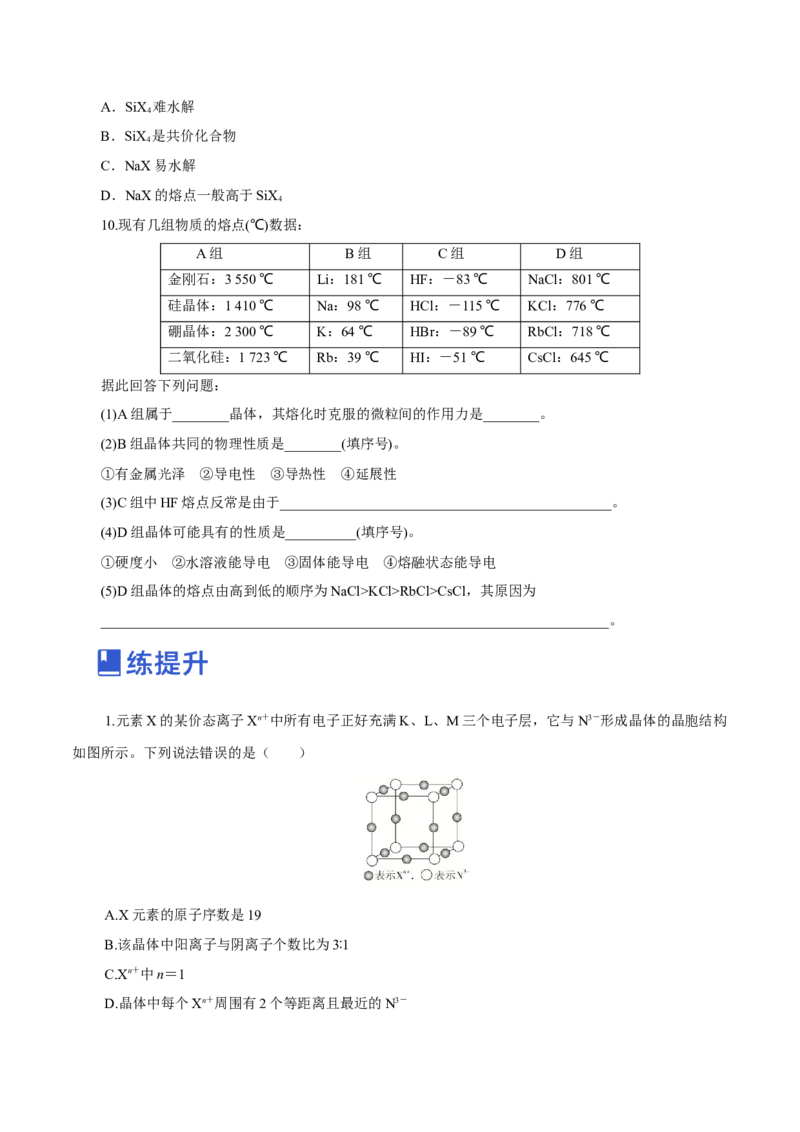
6.某晶体的一部分如图所示,这种晶体中A、B、C三种粒子数之比是( )
A.3∶9∶4 B.1∶4∶2 C.2∶9∶4 D.3∶8∶4
7.如图为甲、乙、丙三种晶体的晶胞:
试写出:
(1)甲晶体化学式(X为阳离子)为________。
(2)乙晶体中A、B、C三种微粒的个数比是________。
(3)丙晶体中每个D周围结合E的个数是________。
(4)乙晶体中每个A周围结合B的个数是________。
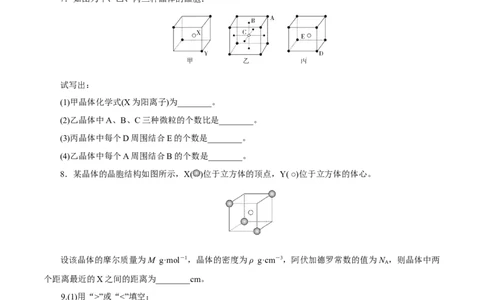
8.某晶体的晶胞结构如图所示,X( )位于立方体的顶点,Y( ○)位于立方体的体心。
设该晶体的摩尔质量为M g·mol-1,晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为N ,则晶体中两
A
个距离最近的X之间的距离为________cm。
9.(1)用“>”或“<”填空:
第一电离能 离子半径 熔点 酸性
Si____S O2-____Na+ NaCl____Si HSO ____HClO
2 4 4
(2)MgCl 在工业上应用广泛,可由MgO制备。
2
①MgO的熔点比BaO的熔点________(填“高”或“低”)。
②SiO 的晶体类型为________________。
2
(3)对于钠的卤化物(NaX)和硅的卤化物(SiX),下列叙述正确的是________。
4A.SiX 难水解
4
B.SiX 是共价化合物
4
C.NaX易水解
D.NaX的熔点一般高于SiX
4
10.现有几组物质的熔点(℃)数据:
A组 B组 C组 D组
金刚石:3 550 ℃ Li:181 ℃ HF:-83 ℃ NaCl:801 ℃
硅晶体:1 410 ℃ Na:98 ℃ HCl:-115 ℃ KCl:776 ℃
硼晶体:2 300 ℃ K:64 ℃ HBr:-89 ℃ RbCl:718 ℃
二氧化硅:1 723 ℃ Rb:39 ℃ HI:-51 ℃ CsCl:645 ℃
据此回答下列问题:
(1)A组属于________晶体,其熔化时克服的微粒间的作用力是________。
(2)B组晶体共同的物理性质是________(填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于_______________________________________________。
(4)D组晶体可能具有的性质是__________(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)D组晶体的熔点由高到低的顺序为NaCl>KCl>RbCl>CsCl,其原因为
________________________________________________________________________。
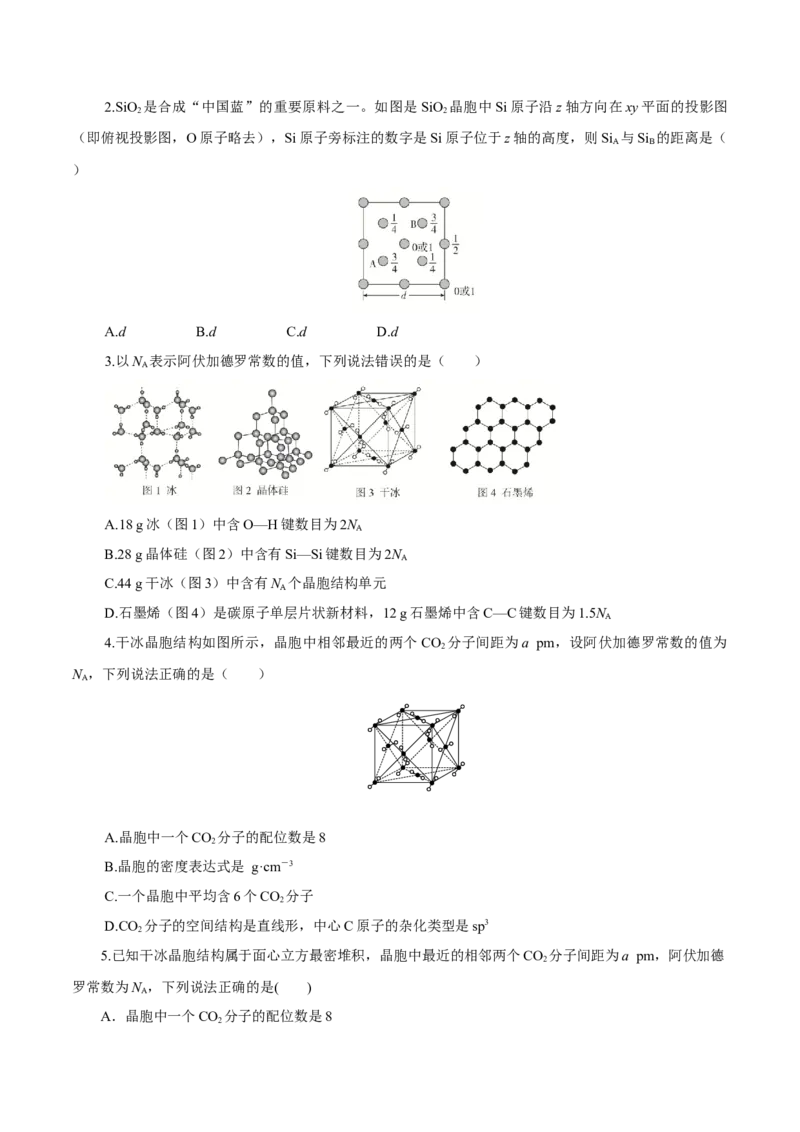
1.元素X的某价态离子Xn+中所有电子正好充满K、L、M三个电子层,它与N3-形成晶体的晶胞结构
如图所示。下列说法错误的是( )
A.X元素的原子序数是19
B.该晶体中阳离子与阴离子个数比为3∶1
C.Xn+中n=1
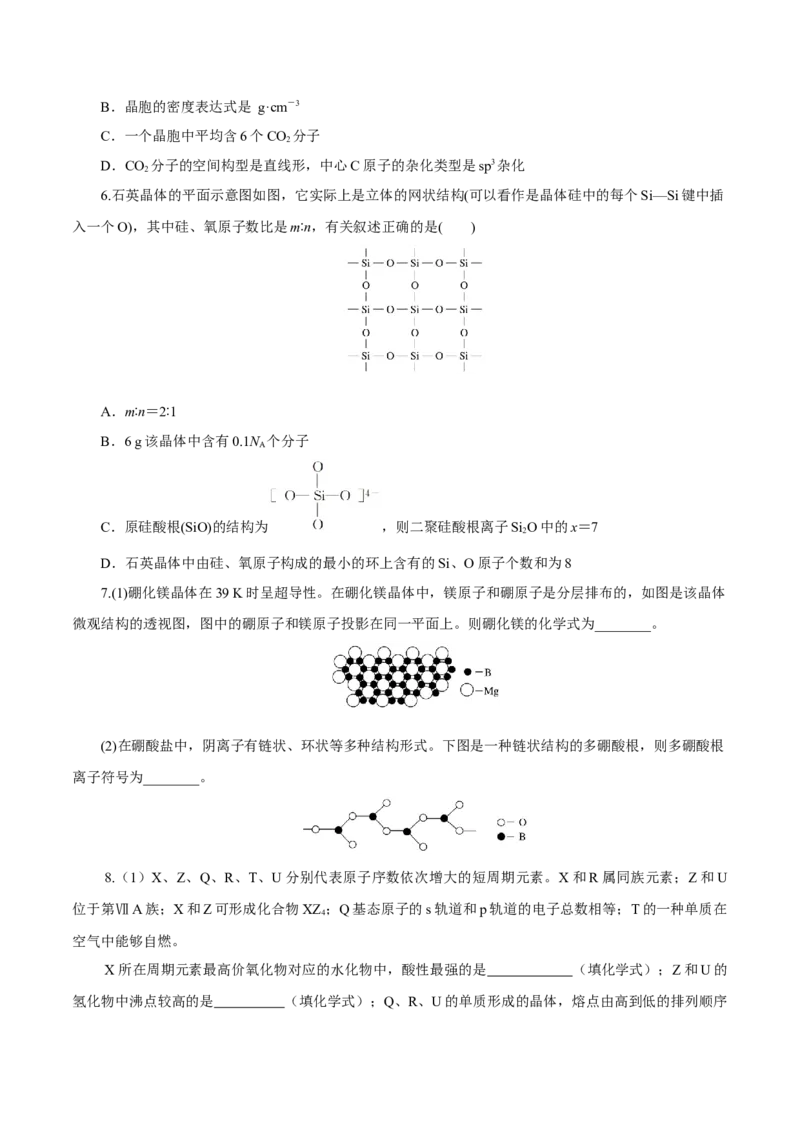
D.晶体中每个Xn+周围有2个等距离且最近的N3-2.SiO 是合成“中国蓝”的重要原料之一。如图是SiO 晶胞中Si原子沿z轴方向在xy平面的投影图
2 2
(即俯视投影图,O原子略去),Si原子旁标注的数字是Si原子位于z轴的高度,则Si 与Si 的距离是(
A B
)
A.d B.d C.d D.d
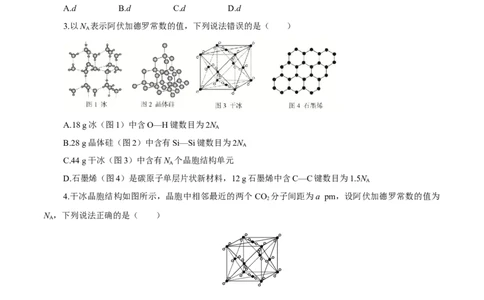
3.以N 表示阿伏加德罗常数的值,下列说法错误的是( )
A
A.18 g冰(图1)中含O—H键数目为2N
A
B.28 g晶体硅(图2)中含有Si—Si键数目为2N
A
C.44 g干冰(图3)中含有N 个晶胞结构单元
A
D.石墨烯(图4)是碳原子单层片状新材料,12 g石墨烯中含C—C键数目为1.5N
A
4.干冰晶胞结构如图所示,晶胞中相邻最近的两个 CO 分子间距为a pm,设阿伏加德罗常数的值为
2
N ,下列说法正确的是( )
A
A.晶胞中一个CO 分子的配位数是8
2
B.晶胞的密度表达式是 g·cm-3
C.一个晶胞中平均含6个CO 分子
2
D.CO 分子的空间结构是直线形,中心C原子的杂化类型是sp3
2
5.已知干冰晶胞结构属于面心立方最密堆积,晶胞中最近的相邻两个CO 分子间距为a pm,阿伏加德
2
罗常数为N ,下列说法正确的是( )
A
A.晶胞中一个CO 分子的配位数是8
2B.晶胞的密度表达式是 g·cm-3
C.一个晶胞中平均含6个CO 分子
2
D.CO 分子的空间构型是直线形,中心C原子的杂化类型是sp3杂化
2
6.石英晶体的平面示意图如图,它实际上是立体的网状结构(可以看作是晶体硅中的每个Si—Si键中插
入一个O),其中硅、氧原子数比是m∶n,有关叙述正确的是( )
A.m∶n=2∶1
B.6 g该晶体中含有0.1N 个分子
A
C.原硅酸根(SiO)的结构为 ,则二聚硅酸根离子Si O中的x=7
2
D.石英晶体中由硅、氧原子构成的最小的环上含有的Si、O原子个数和为8
7.(1)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体
微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为________。
(2)在硼酸盐中,阴离子有链状、环状等多种结构形式。下图是一种链状结构的多硼酸根,则多硼酸根
离子符号为________。
8.(1)X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素。X和R属同族元素;Z和U
位于第ⅦA族;X和Z可形成化合物XZ;Q基态原子的s轨道和p轨道的电子总数相等;T的一种单质在
4
空气中能够自燃。
X所在周期元素最高价氧化物对应的水化物中,酸性最强的是 (填化学式);Z和U的
氢化物中沸点较高的是 (填化学式);Q、R、U的单质形成的晶体,熔点由高到低的排列顺序是 (填化学式)。
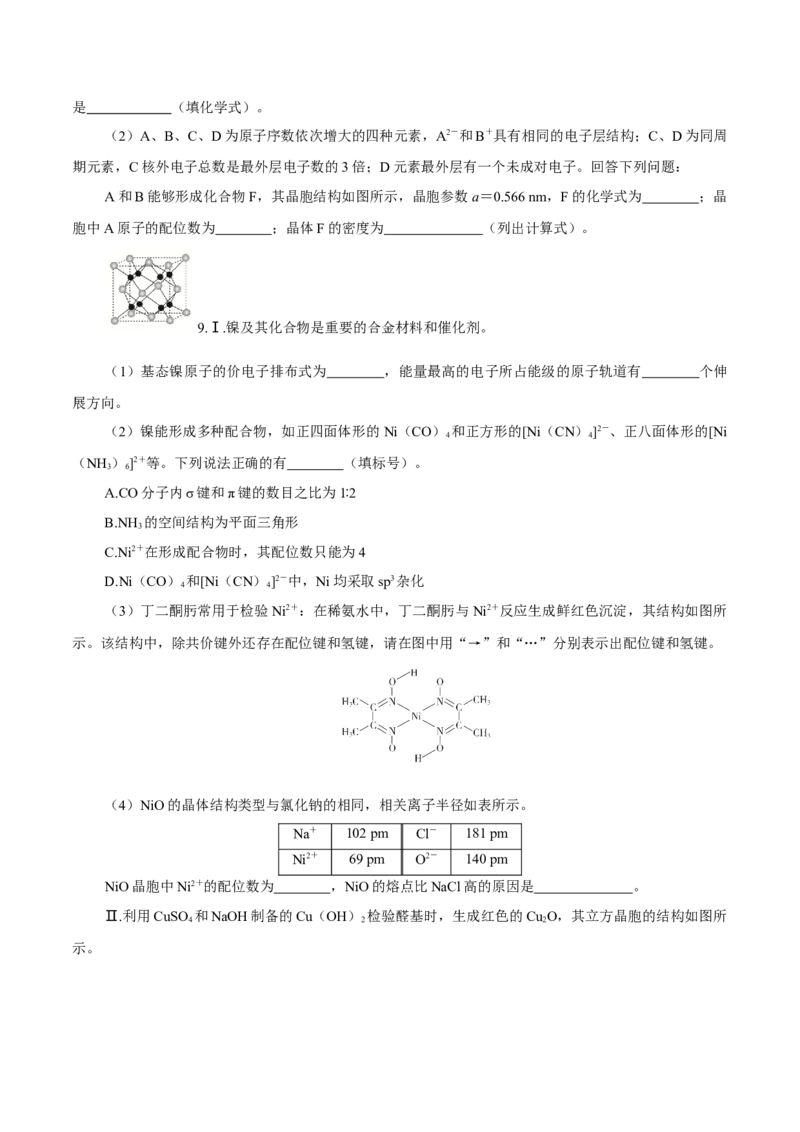
(2)A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子层结构;C、D为同周
期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566 nm,F的化学式为 ;晶
胞中A原子的配位数为 ;晶体F的密度为 (列出计算式)。
9.Ⅰ.镍及其化合物是重要的合金材料和催化剂。
(1)基态镍原子的价电子排布式为 ,能量最高的电子所占能级的原子轨道有 个伸
展方向。
(2)镍能形成多种配合物,如正四面体形的Ni(CO) 和正方形的[Ni(CN)]2-、正八面体形的[Ni
4 4
(NH )]2+等。下列说法正确的有 (填标号)。
3 6
A.CO分子内σ键和π键的数目之比为1∶2
B.NH 的空间结构为平面三角形
3
C.Ni2+在形成配合物时,其配位数只能为4
D.Ni(CO) 和[Ni(CN)]2-中,Ni均采取sp3杂化
4 4
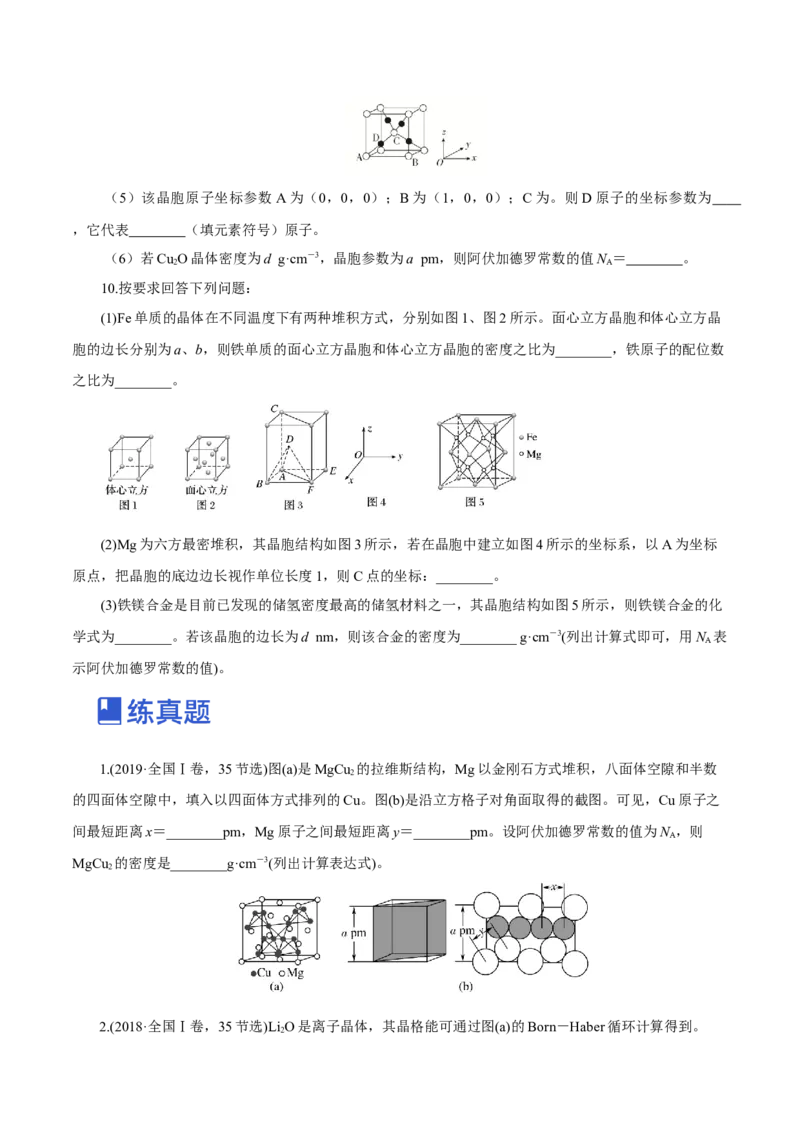
(3)丁二酮肟常用于检验Ni2+:在稀氨水中,丁二酮肟与Ni2+反应生成鲜红色沉淀,其结构如图所
示。该结构中,除共价键外还存在配位键和氢键,请在图中用“→”和“…”分别表示出配位键和氢键。
(4)NiO的晶体结构类型与氯化钠的相同,相关离子半径如表所示。
Na+ 102 pm Cl- 181 pm
Ni2+ 69 pm O2- 140 pm
NiO晶胞中Ni2+的配位数为 ,NiO的熔点比NaCl高的原因是 。
Ⅱ.利用CuSO 和NaOH制备的Cu(OH) 检验醛基时,生成红色的Cu O,其立方晶胞的结构如图所
4 2 2
示。(5)该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);C为。则D原子的坐标参数为
,它代表 (填元素符号)原子。
(6)若Cu O晶体密度为d g·cm-3,晶胞参数为a pm,则阿伏加德罗常数的值N = 。
2 A
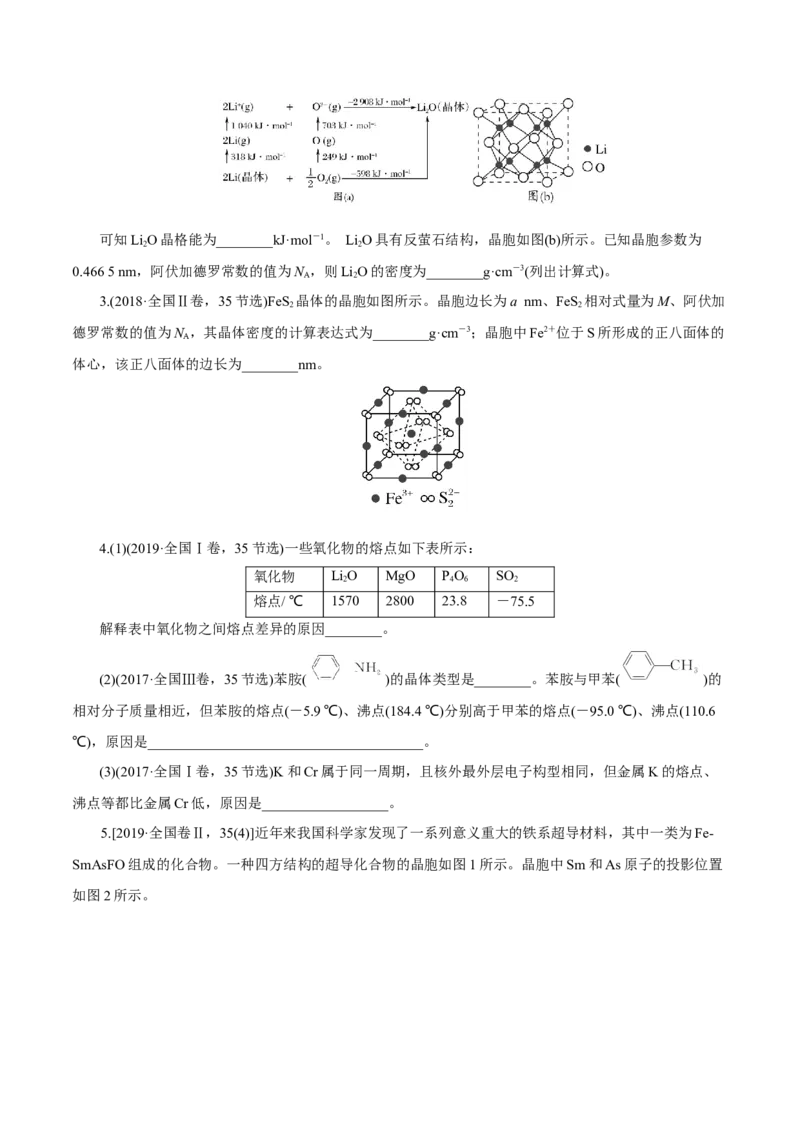
10.按要求回答下列问题:
(1)Fe单质的晶体在不同温度下有两种堆积方式,分别如图1、图2所示。面心立方晶胞和体心立方晶
胞的边长分别为a、b,则铁单质的面心立方晶胞和体心立方晶胞的密度之比为________,铁原子的配位数
之比为________。
(2)Mg为六方最密堆积,其晶胞结构如图3所示,若在晶胞中建立如图4所示的坐标系,以A为坐标
原点,把晶胞的底边边长视作单位长度1,则C点的坐标:________。
(3)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图5所示,则铁镁合金的化
学式为________。若该晶胞的边长为d nm,则该合金的密度为________ g·cm-3(列出计算式即可,用N 表
A
示阿伏加德罗常数的值)。
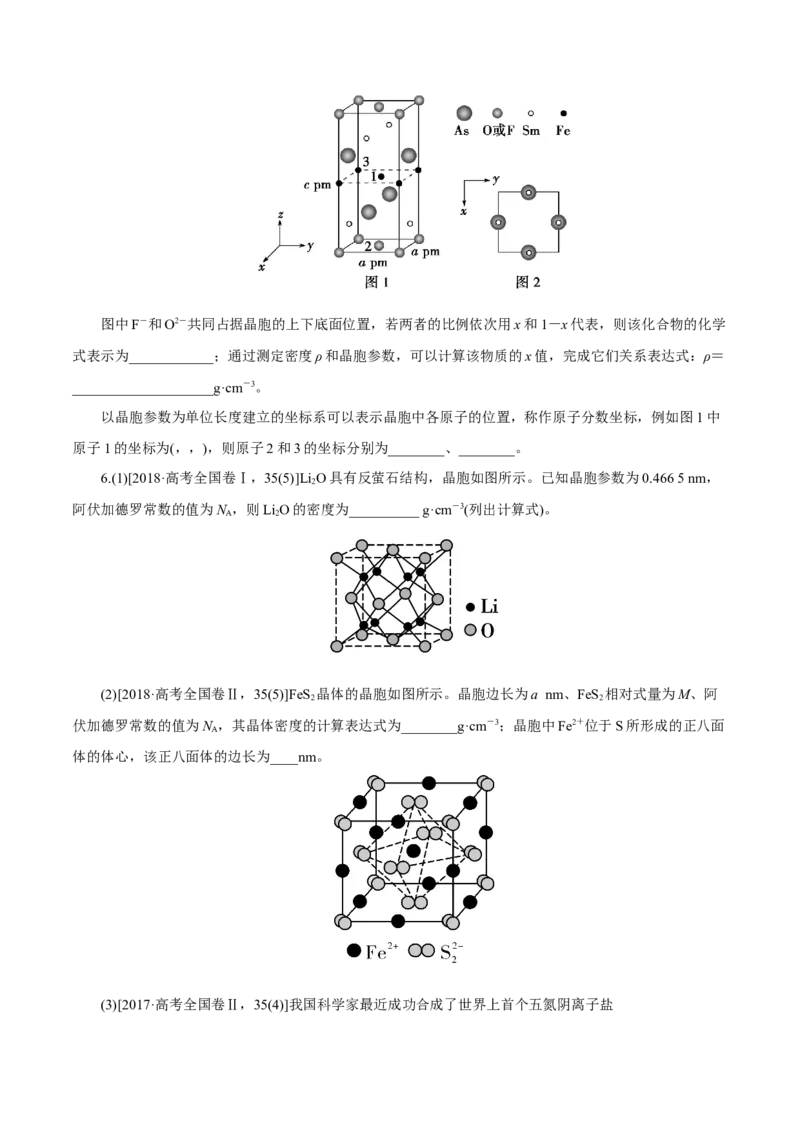
1.(2019·全国Ⅰ卷,35节选)图(a)是MgCu 的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数
2
的四面体空隙中,填入以四面体方式排列的Cu。图(b)是沿立方格子对角面取得的截图。可见,Cu原子之
间最短距离x=________pm,Mg原子之间最短距离y=________pm。设阿伏加德罗常数的值为N ,则
A
MgCu 的密度是________g·cm-3(列出计算表达式)。
2
2.(2018·全国Ⅰ卷,35节选)Li O是离子晶体,其晶格能可通过图(a)的Born-Haber循环计算得到。
2可知LiO晶格能为________kJ·mol-1。 LiO具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为
2 2
0.466 5 nm,阿伏加德罗常数的值为N ,则LiO的密度为________g·cm-3(列出计算式)。
A 2
3.(2018·全国Ⅱ卷,35节选)FeS 晶体的晶胞如图所示。晶胞边长为a nm、FeS 相对式量为M、阿伏加
2 2
德罗常数的值为N ,其晶体密度的计算表达式为________g·cm-3;晶胞中Fe2+位于S所形成的正八面体的
A
体心,该正八面体的边长为________nm。
4.(1)(2019·全国Ⅰ卷,35节选)一些氧化物的熔点如下表所示:
氧化物 LiO MgO PO SO
2 4 6 2
熔点/ ℃ 1570 2800 23.8 -75.5
解释表中氧化物之间熔点差异的原因________。
(2)(2017·全国Ⅲ卷,35节选)苯胺( )的晶体类型是________。苯胺与甲苯( )的
相对分子质量相近,但苯胺的熔点(-5.9 ℃)、沸点(184.4 ℃)分别高于甲苯的熔点(-95.0 ℃)、沸点(110.6
℃),原因是_______________________________________。
(3)(2017·全国Ⅰ卷,35节选)K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、
沸点等都比金属Cr低,原因是__________________。
5.[2019·全国卷Ⅱ,35(4)]近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe-
SmAsFO组成的化合物。一种四方结构的超导化合物的晶胞如图1所示。晶胞中Sm和As原子的投影位置
如图2所示。图中F-和O2-共同占据晶胞的上下底面位置,若两者的比例依次用x和1-x代表,则该化合物的化学
式表示为____________;通过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=
____________________g·cm-3。
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中
原子1的坐标为(,,),则原子2和3的坐标分别为________、________。
6.(1)[2018·高考全国卷Ⅰ,35(5)]Li O具有反萤石结构,晶胞如图所示。已知晶胞参数为0.466 5 nm,
2
阿伏加德罗常数的值为N ,则LiO的密度为__________ g·cm-3(列出计算式)。
A 2
(2)[2018·高考全国卷Ⅱ,35(5)]FeS 晶体的晶胞如图所示。晶胞边长为a nm、FeS 相对式量为M、阿
2 2
伏加德罗常数的值为N ,其晶体密度的计算表达式为________g·cm-3;晶胞中Fe2+位于S所形成的正八面
A
体的体心,该正八面体的边长为____nm。
(3)[2017·高考全国卷Ⅱ,35(4)]我国科学家最近成功合成了世界上首个五氮阴离子盐(N )(H O) (NH )Cl(用R代表)。R的晶体密度为d g·cm-3,其立方晶胞参数为a nm,晶胞中含有y个
5 6 3 3 4 4
[(N )(H O) (NH )Cl]单元,该单元的相对质量为M,则y的计算表达式为
5 6 3 3 4 4
_____________________________。
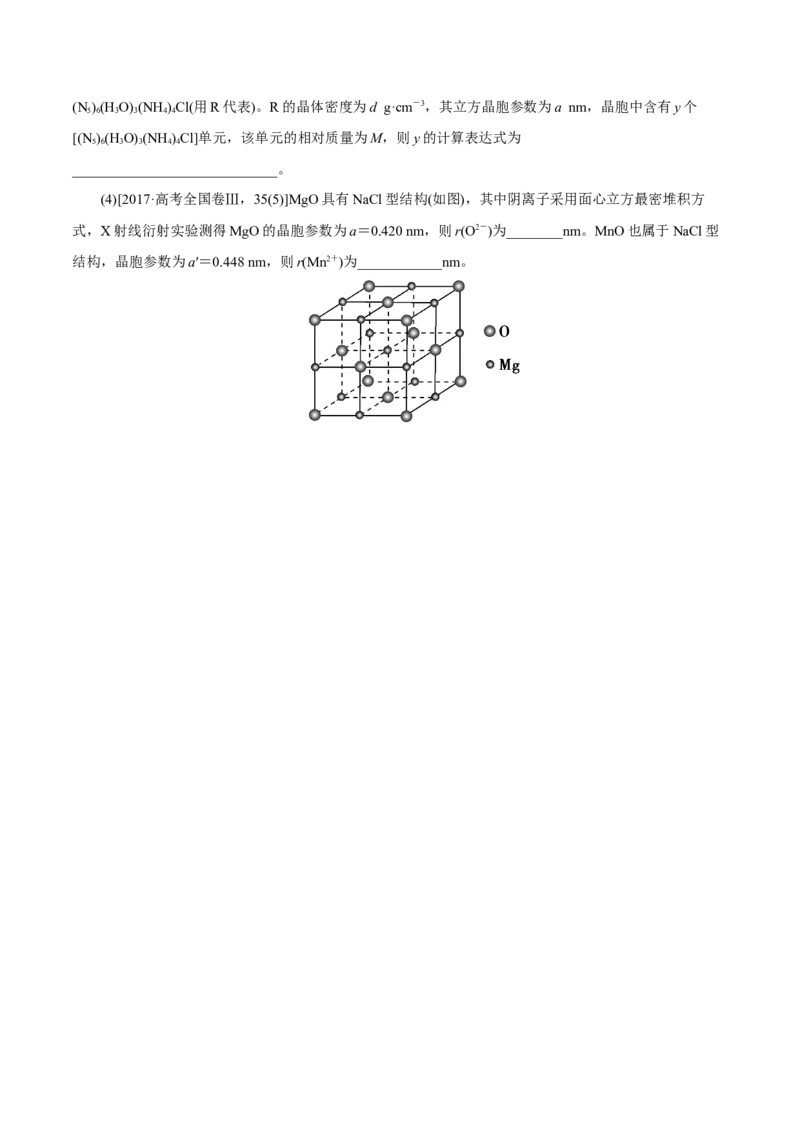
(4)[2017·高考全国卷Ⅲ,35(5)]MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方
式,X射线衍射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为________nm。MnO也属于NaCl型
结构,晶胞参数为a′=0.448 nm,则r(Mn2+)为____________nm。