文档内容
第 31 讲 难溶电解质的溶解平衡与应用
目录
考情分析
考点三 溶度积常数及应用
网络构建
【夯基·必备基础知识梳理】
考点一 沉淀溶解平衡及影响因素
知识点1 溶度积及其应用
【夯基·必备基础知识梳理】 知识点2 溶度积的影响因素
知识点1 沉淀溶解平衡 【提升·必考题型归纳】
知识点2 影响沉淀溶解平衡的因素 考向1 考查溶度积及其应用
【提升·必考题型归纳】 考向2 考查溶度积的影响因素
考向1 考查沉淀溶解平衡的特点
考向2 考查沉淀溶解平衡的影响因素 考点四 沉淀溶解平衡图像分析
【夯基·必备基础知识梳理】
考点二 沉淀溶解平衡的应用
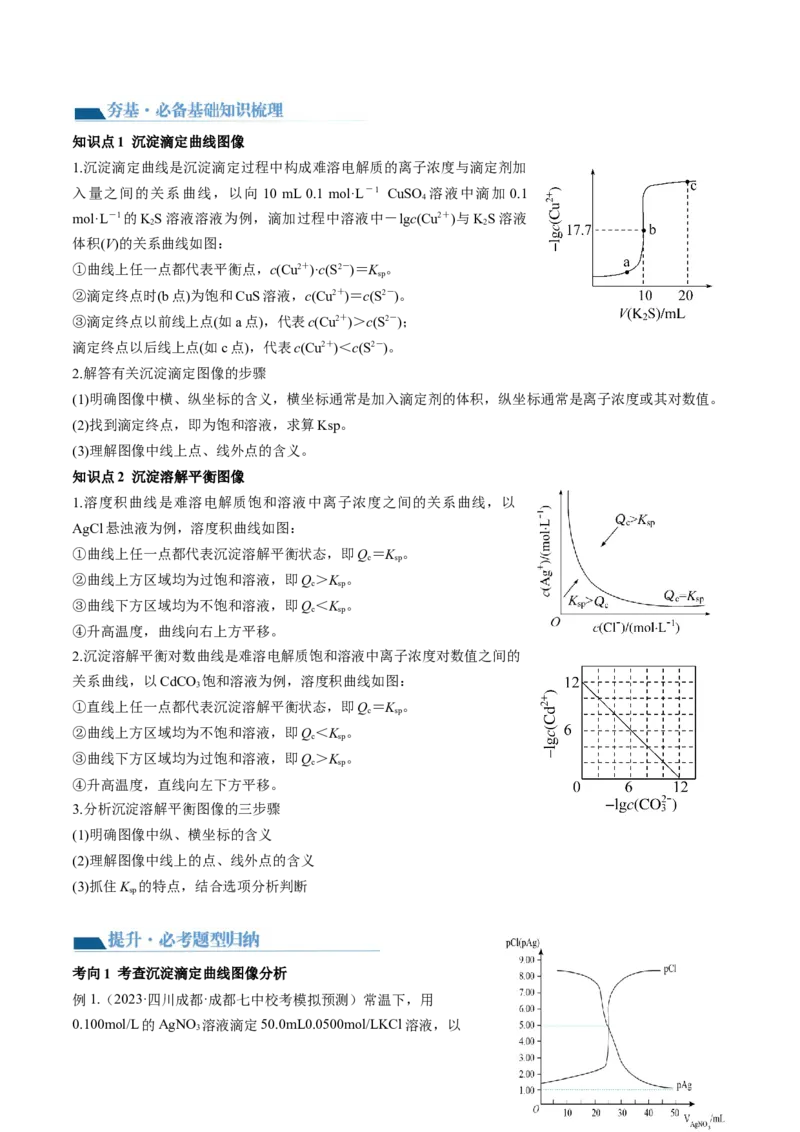
知识点1 沉淀滴定曲线图像
【夯基·必备基础知识梳理】 知识点2 沉淀溶解平衡图像
知识点1 沉淀的生成
【提升·必考题型归纳】
知识点2 沉淀的溶解 考向1 滴定曲线图像
知识点3 沉淀的转化 考向2 沉淀溶解平衡图像分析
【提升·必考题型归纳】
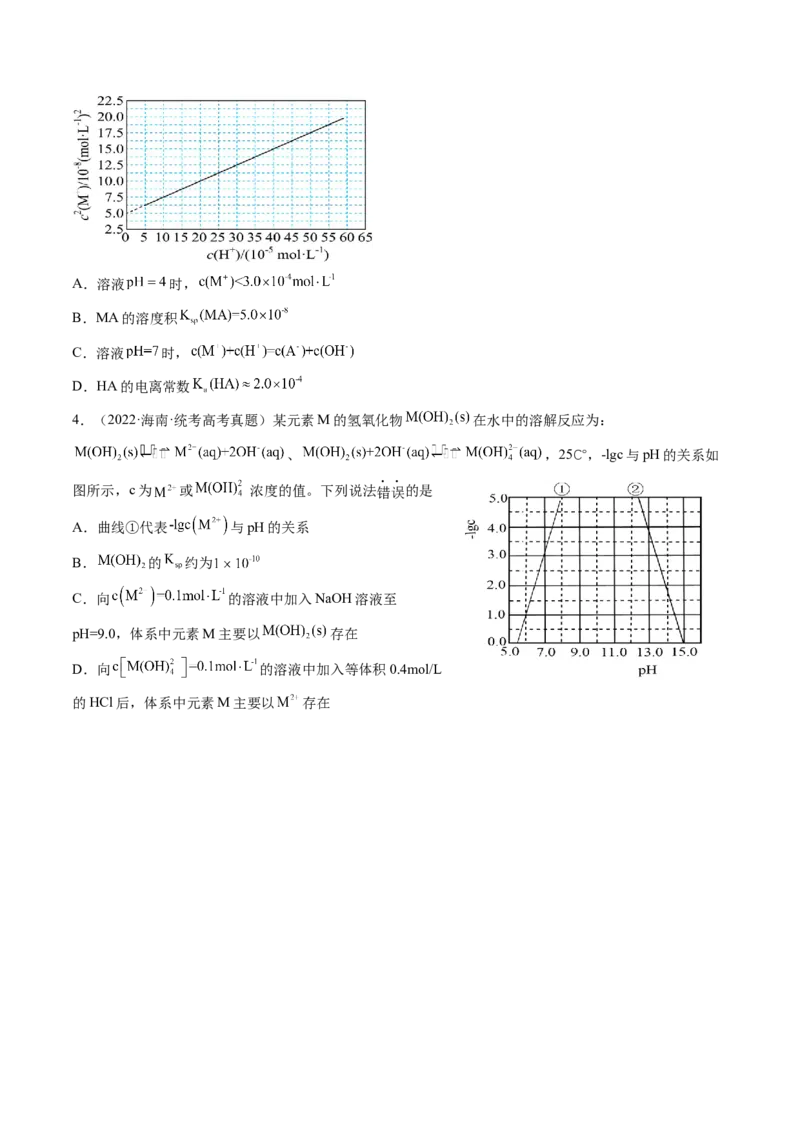
真题感悟
考向1 考查沉淀的生成与溶解
考向2 考查沉淀的转化
考点要求 考题统计 考情分析
2023山东卷15题,4分 分析近三年高考试题,高考命题在本讲有以下沉淀溶解平衡及影 2022山东卷14题,4分 规律:
响因素 2021广东卷17题,4分 1.从考查题型和内容上看,高考命题以选择题
2023新课标卷13题,6分 和非选择题呈现,考查内容主要有以下四个方
沉淀溶解平衡的
面:
2022**卷**题,**分
应用
(1)以具体探究实验为依托,考查沉淀溶解平衡
2021**卷**题,**分
在外界因素影响下的移动;
2023全国甲卷13题,6分
(2)以工艺流程形式考查沉淀溶解平衡的应用,
溶度积常数及应用 2022海南卷14题,3分
包括沉淀的生成、溶解和转化;
2021全国甲卷12题,6分
(3)以具体情境为背景,综合考查溶度积的计算
和应用;
(4)以溶解曲线和滴定曲线的形式考查沉淀溶解
平衡。
2.从命题思路上看,侧重以实际工艺生产为背
景,考查溶度积的计算和沉淀溶解平衡图像。
(1)选择题:常以溶解曲线和滴定曲线为依托,
综合考查沉淀溶解平衡的影响因素、溶度积计
2023全国乙卷卷13题,6分
沉淀溶解平衡图像
算和溶解平衡的移动;
2022湖南卷10题,3分
分析
(2)非选择题:与工艺流程相结合,考查沉淀的
2021全国乙卷13题,6分
生成、溶解和转化等在工业生产中的应用。
3.根据高考命题的特点和规律,复习时要注意以
下几个方面:
(1)沉淀溶解平衡在工业生产中的应用
(2)溶度积的表达式和相关计算
(3)溶解曲线和滴定曲线考点一 沉淀溶解平衡及影响因素
知识点1 沉淀溶解平衡
1.从宏观角度理解溶解度
(1)定义:在一定温度下,某固体物质在100 g溶剂中形成饱和溶液时,溶解的溶质质量为该物质在该温
度下的溶解度,用S表示。
(2)溶解度与溶解性的关系——难溶、可溶、易溶界定:
20 ℃时,电解质在水中的溶解度与溶解性存在如下关系:
2.从微观角度理解沉淀溶解平衡
(1)含义:在一定温度下的水溶液中,当难溶电解质沉淀溶解和生成的速率相等时,即建立了沉淀溶解平衡
状态。
(2)溶解平衡的建立
溶质溶解的过程是一个可逆过程:固体溶质 溶液中的溶质
(3)表达式
难溶电解质(s) 溶质离子(aq)
如AgCl的溶解平衡表达式为AgCl(s) Ag+(aq)+Cl-(aq)
(4)特点(同其他化学平衡):逆、等、定、动、变(适用平衡移动原理)
知识点2 影响沉淀溶解平衡的因素
1.内因:难溶电解质本身的性质,这是决定因素。
①绝对不溶的电解质是没有的。
②同是难溶电解质,溶解度差别也很大。
③易溶电解质作溶质时只要是饱和溶液也可存在溶解平衡。
2.外因
①浓度:加水稀释,平衡向沉淀溶解的方向移动;
②温度:绝大多数难溶电解质的溶解是吸热过程,升高温度,平衡向沉淀溶解的方向移动;
③同离子效应:向平衡体系中加入难溶电解质溶解产生的离子,平衡向生成沉淀的方向移动;
④其他:向平衡体系中加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子时,平衡向沉淀
溶解的方向移动。
3.实例:以AgCl(s) Ag+(aq)+Cl-(aq)为例,填写外界条件对溶解平衡的影响。
外界条件 移动方向 平衡后c(Ag+) 平衡后c(Cl-) K
sp
升高温度 正向 增大 增大 增大
加水稀释 正向 不变 不变 不变
加入少量AgNO(s) 逆向 增大 减小 不变
3
通入HCl(g) 逆向 减小 增大 不变
通入HS(g) 正向 减小 增大 不变
2
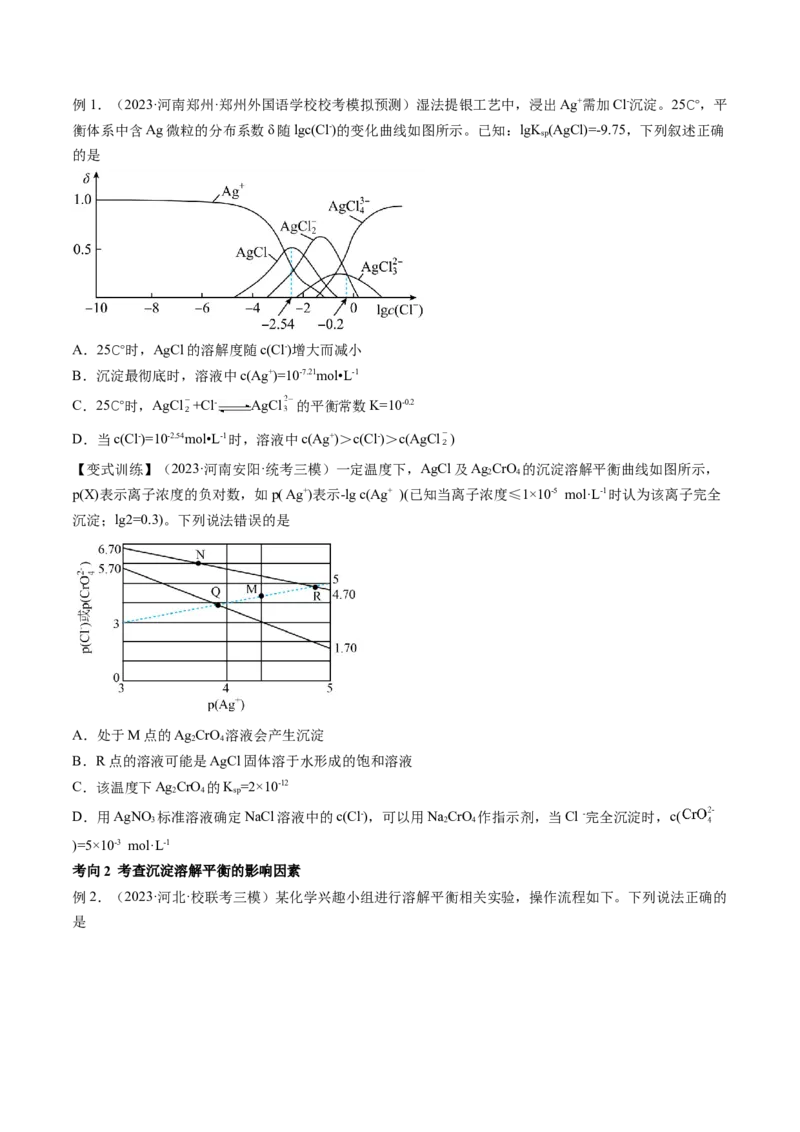
考向1 考查沉淀溶解平衡的特点例1.(2023·河南郑州·郑州外国语学校校考模拟预测)湿法提银工艺中,浸出Ag+需加Cl-沉淀。25℃,平
衡体系中含Ag微粒的分布系数δ随lgc(Cl-)的变化曲线如图所示。已知:lgK (AgCl)=-9.75,下列叙述正确
sp
的是
A.25℃时,AgCl的溶解度随c(Cl-)增大而减小
B.沉淀最彻底时,溶液中c(Ag+)=10-7.21mol•L-1
C.25℃时,AgCl +Cl- AgCl 的平衡常数K=10-0.2
D.当c(Cl-)=10-2.54mol•L-1时,溶液中c(Ag+)>c(Cl-)>c(AgCl )
【变式训练】(2023·河南安阳·统考三模)一定温度下,AgCl及Ag CrO 的沉淀溶解平衡曲线如图所示,
2 4
p(X)表示离子浓度的负对数,如p( Ag+)表示-lg c(Ag+ )(已知当离子浓度≤1×10-5 mol·L-1时认为该离子完全
沉淀;lg2=0.3)。下列说法错误的是
A.处于M点的Ag CrO 溶液会产生沉淀
2 4
B.R点的溶液可能是AgCl固体溶于水形成的饱和溶液
C.该温度下Ag CrO 的K =2×10-12
2 4 sp
D.用AgNO 标准溶液确定NaCl溶液中的c(Cl-),可以用NaCrO 作指示剂,当Cl -完全沉淀时,c(
3 2 4
)=5×10-3 mol·L-1
考向2 考查沉淀溶解平衡的影响因素
例2.(2023·河北·校联考三模)某化学兴趣小组进行溶解平衡相关实验,操作流程如下。下列说法正确的
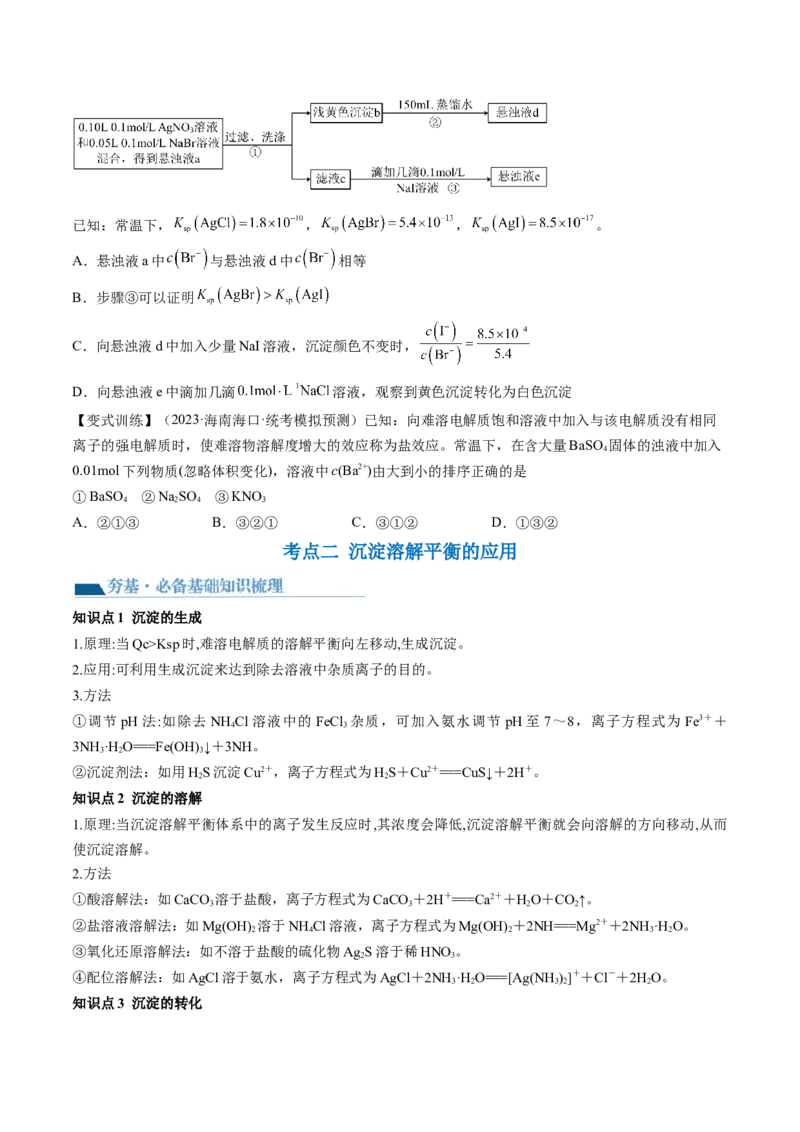
是已知:常温下, , , 。
A.悬浊液a中 与悬浊液d中 相等
B.步骤③可以证明
C.向悬浊液d中加入少量NaI溶液,沉淀颜色不变时,
D.向悬浊液e中滴加几滴 溶液,观察到黄色沉淀转化为白色沉淀
【变式训练】(2023·海南海口·统考模拟预测)已知:向难溶电解质饱和溶液中加入与该电解质没有相同
离子的强电解质时,使难溶物溶解度增大的效应称为盐效应。常温下,在含大量BaSO 固体的浊液中加入
4
0.01mol下列物质(忽略体积变化),溶液中c(Ba2+)由大到小的排序正确的是
①BaSO ②NaSO ③KNO
4 2 4 3
A.②①③ B.③②① C.③①② D.①③②
考点二 沉淀溶解平衡的应用
知识点1 沉淀的生成
1.原理:当Qc>Ksp时,难溶电解质的溶解平衡向左移动,生成沉淀。
2.应用:可利用生成沉淀来达到除去溶液中杂质离子的目的。
3.方法
①调节pH法:如除去NH Cl溶液中的FeCl 杂质,可加入氨水调节 pH至7~8,离子方程式为 Fe3++
4 3
3NH ·H O===Fe(OH) ↓+3NH。
3 2 3
②沉淀剂法:如用HS沉淀Cu2+,离子方程式为HS+Cu2+===CuS↓+2H+。
2 2
知识点2 沉淀的溶解
1.原理:当沉淀溶解平衡体系中的离子发生反应时,其浓度会降低,沉淀溶解平衡就会向溶解的方向移动,从而
使沉淀溶解。
2.方法
①酸溶解法:如CaCO 溶于盐酸,离子方程式为CaCO +2H+===Ca2++HO+CO↑。
3 3 2 2
②盐溶液溶解法:如Mg(OH) 溶于NH Cl溶液,离子方程式为Mg(OH) +2NH===Mg2++2NH ·H O。
2 4 2 3 2
③氧化还原溶解法:如不溶于盐酸的硫化物Ag S溶于稀HNO。
2 3
④配位溶解法:如AgCl溶于氨水,离子方程式为AgCl+2NH ·H O===[Ag(NH )]++Cl-+2HO。
3 2 3 2 2
知识点3 沉淀的转化1.实质:沉淀溶解平衡的移动(沉淀的溶解度差别越大,越容易转化,易溶的转化为难溶的)。
如AgNO 溶液――→AgCl(白色沉淀)――→AgBr(浅黄色沉淀)――→AgI(黄色沉淀)――→Ag S(黑色沉淀)。
3 2
2.沉淀转化的规律
1)难溶的物质转化为更难溶的物质较易实现。
2)K 相差不大时,K 小的物质可以转化为K 大的物质。如K (BaCO)=5.1×10-9>K (BaSO)=1.1×10-
sp sp sp sp 3 sp 4
10,通过增大CO的浓度,可以实现BaSO(s)+CO(aq) BaCO (s)+SO(aq)。
4 3
3)K 相差很大时,K 小的物质不能转化为K 大的物质。
sp sp sp
3.应用
a.锅炉除垢:将 CaSO 转化为易溶于酸的 CaCO ,离子方程式为 CaSO(s)+CO(aq) CaCO (s)+
4 3 4 3
SO(aq)。
b.矿物转化:CuSO 溶液遇PbS转化为CuS,离子方程式为Cu2+(aq)+PbS(s) CuS(s)+Pb2+(aq)。
4
【易错提醒】(1)沉淀溶解平衡移动过程是固体溶解和析出的相互转化过程,属于物理变化,但遵循勒夏特
列原理。
(2)沉淀溶解达到平衡时,再加入该难溶物对平衡无影响。
(3)用沉淀法除杂不可能将杂质离子全部通过沉淀除去。一般认为残留在溶液中的离子浓度小于 1×10-5
mol·L-1时,沉淀已经完全。
(4)对于化学式中阴、阳离子个数比不同的难溶物,不能直接根据 K 的大小来确定其溶解能力的大小,需
sp
通过计算转化为溶解度。
4.分步沉淀
若一种沉淀剂可使溶液中多种离子产生沉淀时,则可控制反应条件,使这些离子先后分别沉淀。
(1)对同一类型的沉淀,Ksp越小越先沉淀,且Ksp相差越大分步沉淀效果越好。如在Cl-、Br-、I-的混合溶液
中,由于AgCl、AgBr、AgI的Ksp相差较大,逐滴加入Ag+可按I-、Br-、Cl-的顺序先后沉淀,即Ksp最小的首
先沉淀出来。
(2)对不同类型的沉淀,其沉淀先后顺序要利用Ksp计算溶液中离子的浓度,根据离子浓度的大小来判断沉淀
的先后顺序,如AgCl和Ag CrO 的分步沉淀,可通过控制Ag+浓度来完成。
2 4
考向1 考查沉淀的生成与溶解
例1.(2023·湖南常德·常德市一中校考模拟预测)25℃时,难溶盐CaSO、CaCO 、MnCO 溶液中阳离子
4 3 3
浓度的负对数 和阴离子浓度的负对数
的关系如图所示。下列说法错误的是
A.25℃,
B.向A点对应的溶液中加入固体CaCl ,可得到Y点对应
2
的溶液
C.25℃,三种物质的溶解度:MnCO K :溶液过饱和,有沉淀析出
c sp
应用
②Q=K :溶液饱和,处于平衡状态
c sp
③Q<K :溶液未饱和,无沉淀析出
c sp
2.对“Ksp”的理解
(1)Ksp只与温度有关,与浓度无关,升高温度,大多数固体难溶电解质的Ksp增大,但Ca(OH) 却相反。
2
(2)对于Ksp表达式类型相同的物质,如Mg(OH) 和Zn(OH) ,Ksp的大小反映了难溶电解质在溶液中的溶解能
2 2
力的大小,一般Ksp越小,溶解度越小。
(3)对于阴、阳离子的个数比不同的难溶电解质,它们的溶解度不能直接用 Ksp 的大小来比较,如
AgCl(Ksp=1.8×10-10)、Ag CrO(Ksp=1.0×10-12),Ag CrO 溶液中的c(Ag+)大于AgCl溶液中的c(Ag+)。
2 4 2 4
3.溶度积常数的计算
(1)溶度积原则
①K 只与难溶电解质的性质和温度有关,而与沉淀的量和溶液中离子浓度无关。
sp
②同温条件时,对于同类型物质,K 数值越大,难溶电解质在水中的溶解能力越强。如由K 数值可知,
sp sp溶解能力:AgCl>AgBr>AgI,Cu(OH) <Mg(OH) 。
2 2
③不同类型的物质,K 差距不大时不能直接作为比较依据。如(25 ℃):
sp
AgCl(s) Ag+(aq)+Cl-(aq),K =1.8×10-10,
sp
Mg(OH) (s) Mg2+(aq)+2OH-(aq),K =1.8×10-11,
2 sp
虽然Mg(OH) 的K 较小,但不能认为Mg(OH) 比AgCl更难溶。
2 sp 2
(2)沉淀开始和沉淀完全时溶液pH的计算方法:
[以Cu(OH) 为例]室温下,向2 mol·L-1 CuSO 溶液中逐滴加入NaOH溶液调节溶液的pH至多少时开始沉
2 4
淀?调节溶液pH至多少时Cu2+沉淀完全?
(已知:室温下K [Cu(OH) ]=2.0×10-20,离子浓度小于10-5 mol·L-1时视为Cu2+沉淀完全)
sp 2
①沉淀开始时pH的求算。
K [Cu(OH) ]=c(Cu2+)·c2(OH-)=2×c2(OH-)=2.0×10-20,
sp 2
c(OH-)==10-10(mol·L-1),
c(H+)===10-4(mol·L-1),
pH=-lgc(H+)=-lg10-4=4。
②沉淀完全时pH的求算。
K [Cu(OH) ]=c(Cu2+)·c2(OH-)=10-5·c2(OH-)=2.0×10-20,c(OH-)==×10-8≈4.47×10-8(mol·L-1),c(H+)
sp 2
==≈2.24×10-7(mol·L-1),pH=-lgc(H+)=-lg(2.24×10-7)=7-lg2.24≈6.6。
知识点2 溶度积的影响因素
1.内因:难溶物质本身的性质,这是主要决定因素。
2.外因
①浓度:加水稀释,平衡向溶解方向移动,但K 不变。
sp
②温度:绝大多数难溶盐的溶解是吸热过程,升高温度,平衡向溶解方向移动,K 增大。
sp
③其他:向平衡体系中加入可与体系中某些离子反应生成更难溶物质或更难电离物质或气体的离子时,平
衡向溶解方向移动,但K 不变。
sp
【易错提醒】(1)K 只与难溶电解质的性质和温度有关,与沉淀的量无关。
sp
(2)溶液中离子浓度的变化只能使溶解平衡移动,并不能改变溶度积。
(3)沉淀的生成和溶解相互转化的条件是离子浓度的大小,改变反应所需的离子浓度,可使反应向着所需的
方向转化。
(4)K 小的难溶电解质也能向K 大的难溶电解质转化,需看溶液中生成沉淀的离子浓度的大小。
sp sp
考向1 考查溶度积及其计算
例1.(2023·新疆·统考三模)常温下,CaCO 和CaF 的沉淀溶解平衡曲线如图[ pX=-lgc(Xn-)、pCa=-
3 2
lgc( Ca2+)],已知K ( CaCO )>K ( CaF ),下列说法正确的是
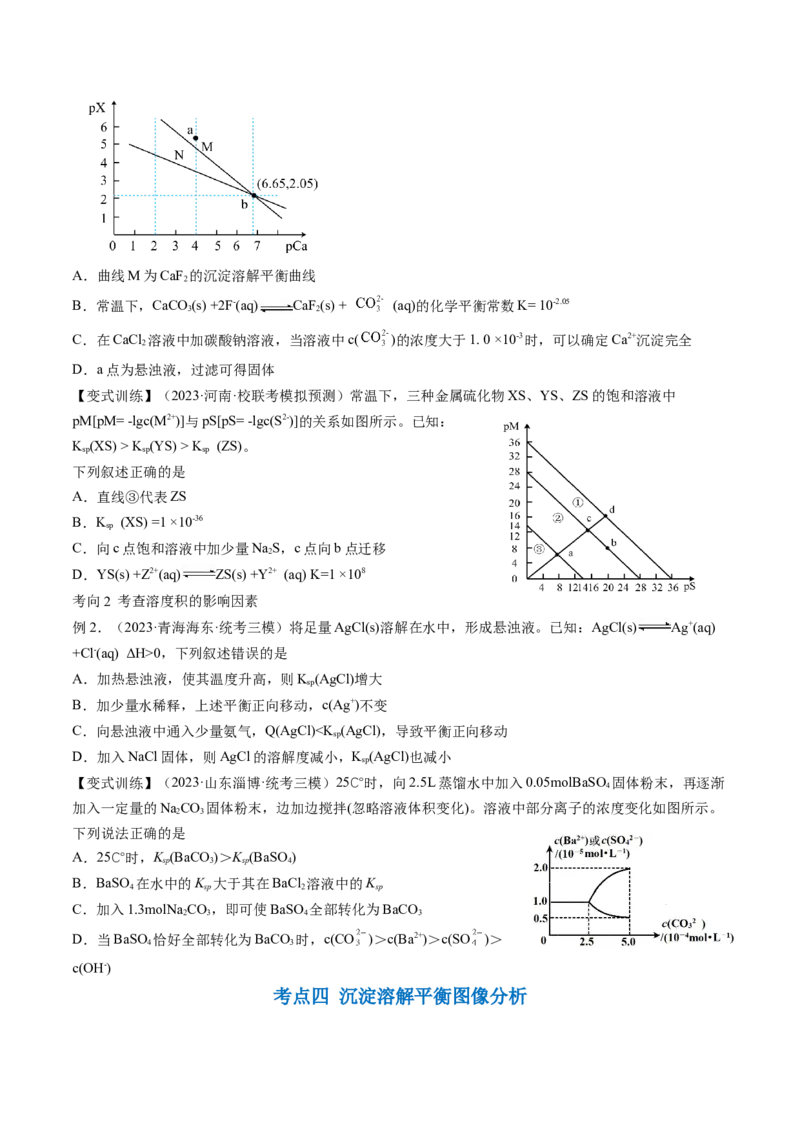
sp 3 sp 2A.曲线M为CaF 的沉淀溶解平衡曲线
2
B.常温下,CaCO (s) +2F-(aq) CaF (s) + (aq)的化学平衡常数K= 10-2.05
3 2
C.在CaCl 溶液中加碳酸钠溶液,当溶液中c( )的浓度大于1. 0 ×10-3时,可以确定Ca2+沉淀完全
2
D.a点为悬浊液,过滤可得固体
【变式训练】(2023·河南·校联考模拟预测)常温下,三种金属硫化物XS、YS、ZS的饱和溶液中
pM[pM= -lgc(M2+)]与pS[pS= -lgc(S2-)]的关系如图所示。已知:
K (XS) > K (YS) > K (ZS)。
sp sp sp
下列叙述正确的是
A.直线③代表ZS
B.K (XS) =1 ×10-36
sp
C.向c点饱和溶液中加少量NaS,c点向b点迁移
2
D.YS(s) +Z2+(aq) ZS(s) +Y2+ (aq) K=1 ×108
考向2 考查溶度积的影响因素
例2.(2023·青海海东·统考三模)将足量AgCl(s)溶解在水中,形成悬浊液。已知:AgCl(s) Ag+(aq)
+Cl-(aq) ΔH>0,下列叙述错误的是
A.加热悬浊液,使其温度升高,则K (AgCl)增大
sp
B.加少量水稀释,上述平衡正向移动,c(Ag+)不变
C.向悬浊液中通入少量氨气,Q(AgCl)c(NO )>c(Ag+)>c(H+)>c(OH-)
D.相同实验条件下,若改为 0.05 mol/L NaCl和NaCrO 溶液,则曲线L 中N点移到P点
2 4 2
考向2 考查沉淀溶解平衡图像分析
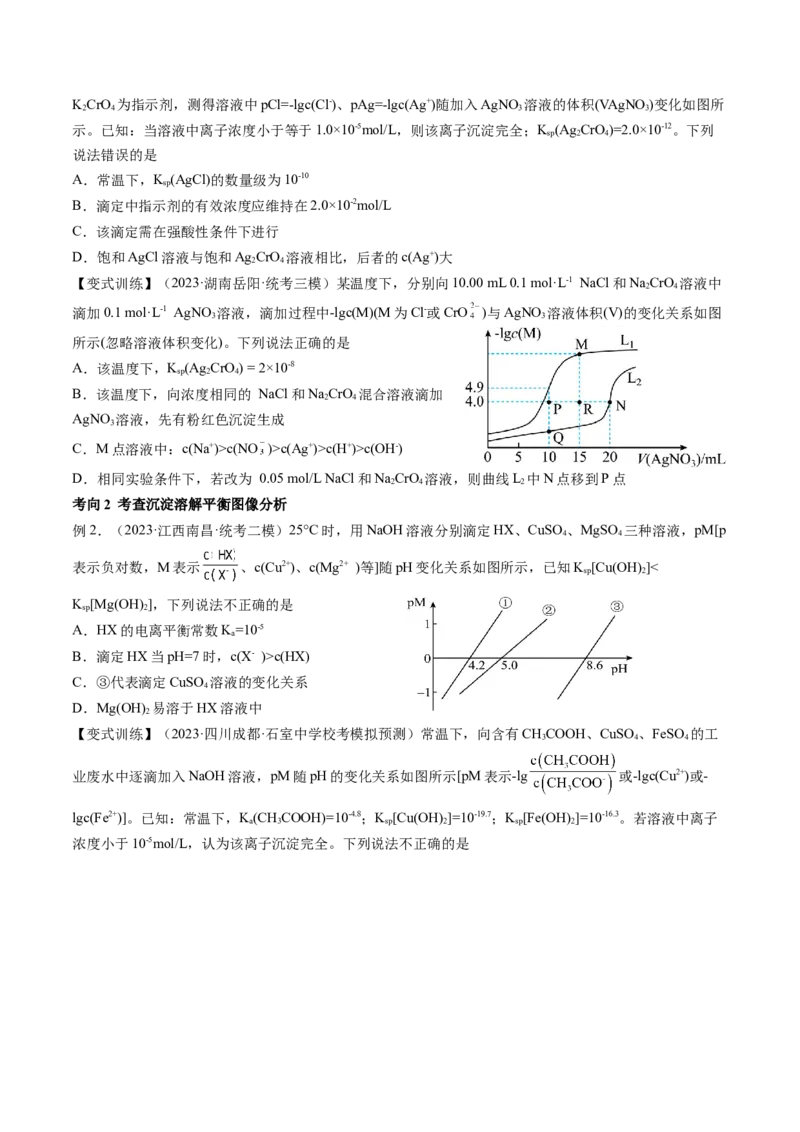
例2.(2023·江西南昌·统考二模)25°C时,用NaOH溶液分别滴定HX、CuSO 、MgSO 三种溶液,pM[p
4 4
表示负对数,M表示 、c(Cu2+)、c(Mg2+ )等]随pH变化关系如图所示,已知K [Cu(OH) ]<
sp 2
K [Mg(OH) ],下列说法不正确的是
sp 2
A.HX的电离平衡常数K=10-5
a
B.滴定HX当pH=7时,c(X- )>c(HX)
C.③代表滴定CuSO 溶液的变化关系
4
D.Mg(OH) 易溶于HX溶液中
2
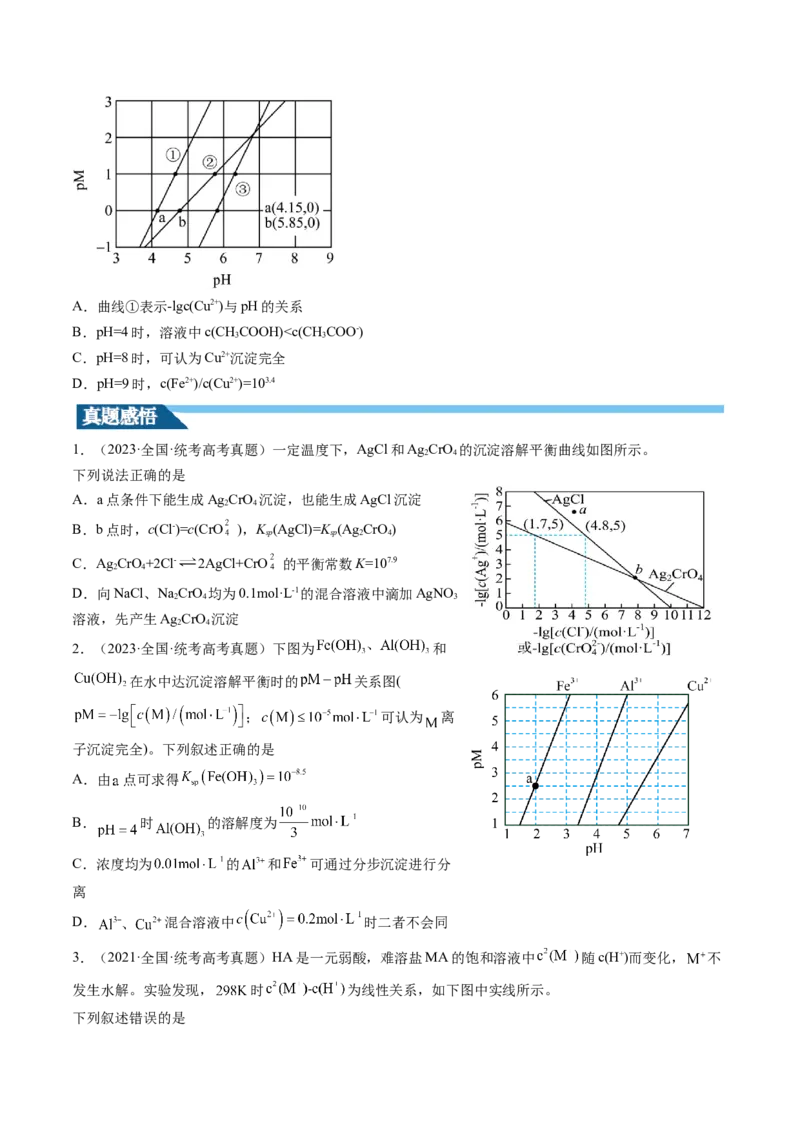
【变式训练】(2023·四川成都·石室中学校考模拟预测)常温下,向含有CHCOOH、CuSO 、FeSO 的工
3 4 4
业废水中逐滴加入NaOH溶液,pM随pH的变化关系如图所示[pM表示-lg 或-lgc(Cu2+)或-
lgc(Fe2+)]。已知:常温下,K(CHCOOH)=10-4.8;K [Cu(OH) ]=10-19.7;K [Fe(OH) ]=10-16.3。若溶液中离子
a 3 sp 2 sp 2
浓度小于10-5mol/L,认为该离子沉淀完全。下列说法不正确的是A.曲线①表示-lgc(Cu2+)与pH的关系
B.pH=4时,溶液中c(CHCOOH)