文档内容
第 4 讲 氧化还原反应的基本概念和规律
课 程 标 准 知 识 建 构
1.认识有化合价变化的反应是氧化还原
反应,了解氧化还原反应的本质是电子
的转移。
2.知道常见的氧化剂和还原剂。
3.认识元素在物质中可以具有不同的价
态,可以通过氧化还原反应实现含有不
同价态同种元素的物质的相互转化。
一、氧化还原反应
1.氧化还原反应的本质和特征
2.对立统一的氧化还原反应基本概念及关系
3.氧化还原反应中电子转移的表示方法
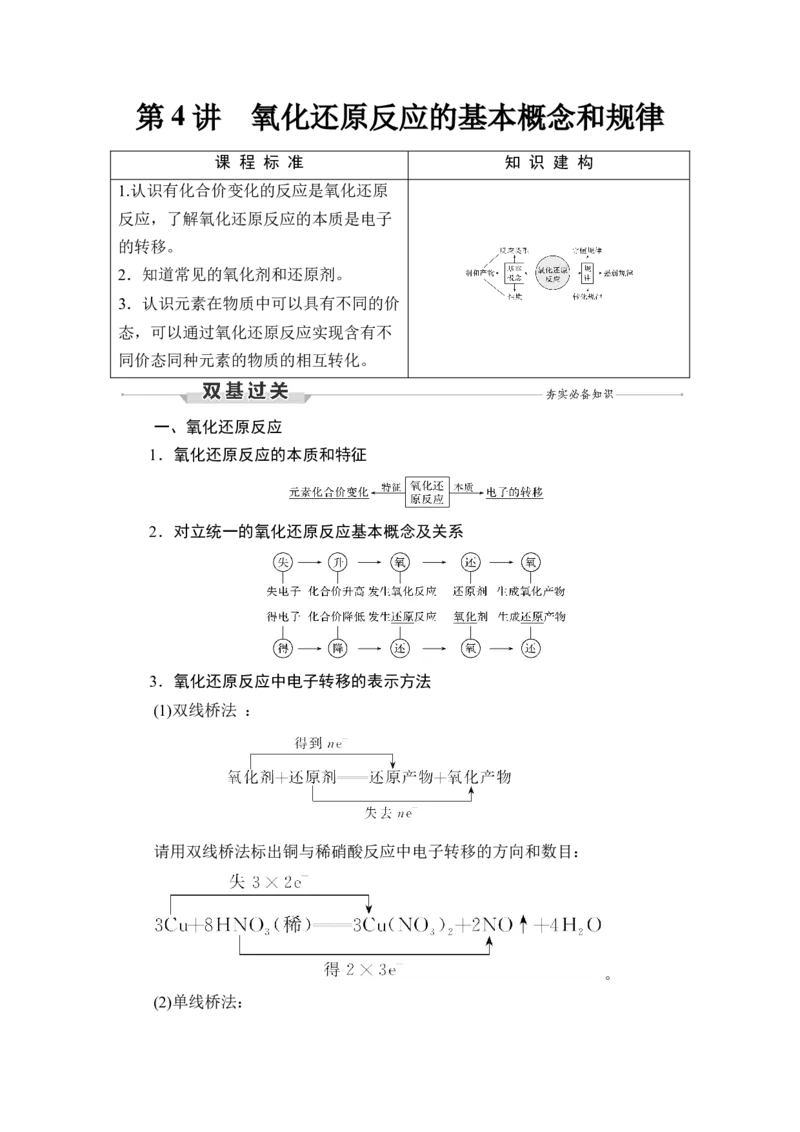
(1)双线桥法 :
请用双线桥法标出铜与稀硝酸反应中电子转移的方向和数目:
。
(2)单线桥法:请用单线桥法标出铜与稀硝酸反应中电子转移的方向和数目:
。
4.氧化还原反应与四种基本反应类型的关系
【诊断1】 标出下列反应中化合价变化元素的化合价,并用双线桥法表示电
子转移的方向和数目:
2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl ↑+8H O
4 2 2 2
上述反应中________是氧化剂,________元素被氧化,氧化产物是________,
生成1 mol Cl 时转移电子数目为________,盐酸表现的性质是________。
2
答案
KMnO 氯 Cl 2N 还原性、酸性
4 2 A
二、氧化剂和还原剂
1.常见氧化剂和还原剂
(1)常见氧化剂及其还原产物
物质类别 实例 还原产物
X (卤素单质) X -
2
活泼非金属单质
O (H+) H O
2 2
氧化物 MnO Mn 2 +
2
浓硫酸 SO
2
含氧酸
高价化合物或离子 硝酸 NO 或 NO
2
KMnO (H+) Mn 2 +
4
盐
Cr O(H+) Cr 3 +
2FeCl Fe 2 +
3
(2)常见还原剂及其氧化产物
物质类别 实例 氧化产物
活泼金属单质 Zn Zn 2 +
H H O
2 2
非金属单质
C CO
2
氧化物 CO CO
2
低价化合物或离子 氢化物 H S S
2
盐 KI I
2
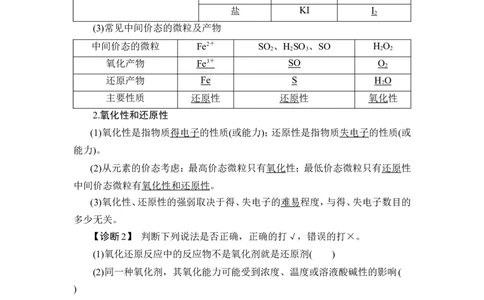
(3)常见中间价态的微粒及产物
中间价态的微粒 Fe2+ SO 、H SO 、SO H O
2 2 3 2 2
氧化产物 Fe 3 + SO O
2
还原产物 Fe S H O
2
主要性质 还原性 还原性 氧化性
2.氧化性和还原性
(1)氧化性是指物质得电子的性质(或能力);还原性是指物质失电子的性质(或
能力)。
(2)从元素的价态考虑:最高价态微粒只有氧化性;最低价态微粒只有还原性
中间价态微粒有氧化性和还原性。
(3)氧化性、还原性的强弱取决于得、失电子的难易程度,与得、失电子数目的
多少无关。
【诊断2】 判断下列说法是否正确,正确的打√,错误的打×。
(1)氧化还原反应中的反应物不是氧化剂就是还原剂( )
(2)同一种氧化剂,其氧化能力可能受到浓度、温度或溶液酸碱性的影响(
)
(3)实现“Cl → Cl-”的变化过程一定要加入还原剂( )
2
(4)阳离子只有氧化性,阴离子只有还原性( )
(5)SO、NO中非氧元素的化合价均为最高价,一定能表现出强氧化性( )
(6)物质越易失电子,还原性越强,越易被氧化,氧化性越强( )
答案 (1)× (2)√ (3)× (4)× (5)× (6)×
三、氧化还原反应的规律
1.守恒规律(得失电子守恒)在氧化还原反应中,氧化剂得到的电子总数与还原剂失去的电子总数相等。
2.转化规律(价态归中, 互不交叉)
如H S和H SO (浓)反应生成S和SO 的反应中,H S转化为S。
2 2 4 2 2
3.先后规律(强易弱难, 先强后弱)
一种氧化剂与多种还原剂反应时,将按照还原性由强到弱的顺序依次反应;
一种还原剂与多种氧化剂反应时,将按照氧化性由强到弱的顺序依次反应。
【诊断3】 向含有1 mol Fe3+和1 mol Cu2+的溶液中逐渐加入铁粉,溶液中的
________________先参加反应,当加入 0.6 mol 铁粉时,溶液中的金属离子有
________________,其物质的量分别为________________。
答案 Fe3+ Cu2+、Fe2+ 0.9 mol、1.6 mol
考点一 基于“双线桥”理解氧化还原反应的基本概念和规律
【典例1】 关于反应2KI+O +H O===2KOH+I +O ,下列说法正确的是(
3 2 2 2
)
A.当有2 mol KI被还原时,1 mol氧原子被氧化
B.O 是还原产物
2
C.若消耗2.24 L O ,则转移0.2 mol电子
3
D.氧化剂与还原产物的物质的量之比为1∶1
答案 D
解析 反应中电子转移情况为:
,1 mol氧原子被还原,A项错误;KOH是
还原产物,B项错误;未说明O 所处的状况,C项错误;氧化剂是O ,还原产物为
3 3
KOH,1 mol O 参加反应,共得2 mol电子,只有1 mol KOH是还原产物,故D项
3
正确。
【对点练1】 (电子转移的表示方法)饮用水中的NO对人类健康会产生危害,
为了降低饮用水中NO的浓度,某饮用水研究人员指出,在碱性条件下用铝粉将
NO还原为N ,其化学方程式为:10Al+6NaNO +4NaOH===10NaAlO +3N ↑
2 3 2 2
+2H O。
2
下列有关该反应的说法中,正确的是( )A.反应中铝元素的化合价升高,被还原
B.若有10 mol铝原子参与反应,则转移的电子总数为30
C.用双线桥表示的电子转移为:
D.可以用单线桥将电子转移表示为
答案 C
解析 由化学方程式可知,铝元素的化合价升高,被氧化,A项错误;10 mol
铝原子参加反应转移电子为10 mol× 3=30 mol,数目为30N ,B项错误;用双线
A
桥法表示的电子转移如下:
C项正确;单线桥上应标注电子总数,并且不注明得失,D项错误。
【对点练2】 (双线桥在电子转移计算的应用)三氟化氮(NF )是微电子工业中
3
优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF +5H O===2NO+
3 2
HNO +9HF,下列有关该反应的说法正确的是 ( )
3
A.NF 是氧化剂,H O是还原剂
3 2
B.HF是还原产物
C.还原剂和氧化剂的物质的量之比是2∶1
D.3 mol NF 参加反应转移电子2 mol
3
答案 D
解析 ,该反应中3 mol NF 参
3
加反应时,2 mol NF 被还原成NO,1 mol NF 被氧化成HNO ,即NF 既是氧化剂
3 3 3 3
又是还原剂,还原剂和氧化剂的物质的量之比为1∶2,NO为还原产物,HNO 为
3氧化产物,HF既不是氧化产物也不是还原产物,B、C项错误。
【对点练3】 (“双线桥”法的定量分析)
(1)湿法制备 K FeO 反应的离子方程式为:2Fe(OH) +3ClO-+4OH-
2 4 3
===2FeO+3Cl-+5H O,当有 3 mol FeO 生成时,转移电子的物质的量为
2
________。
(2)对于NaNO +NH Cl===NaCl+N ↑+2H O反应,生成0.5 mol N ,转移电
2 4 2 2 2
子的物质的量为________。
答案 (1)9 mol (2)1.5 mol
解析 (1)反应中电子转移情况为
可知,当有3 mol FeO生成时,转移电子的物质的量为 mol=9 mol。
(2)此反应电子转移表示为
故生成0.5 mol N 时转移电子0.5 mol×3=1.5 mol。
2
特殊物质中元素化合价的判断
(1)CuFeS :Cu+2 Fe+2 S-2
2
(2)K FeO :Fe+6 FeO:Fe+(8-n)
2 4
(3)Li NH、LiNH 、AlN:N-3
2 2
(4)Na S O :S+2 S O:S+2.5
2 2 3 4
(5)C O:C+3 HCN:C+2 N-3
2
考点二 物质氧化性、还原性强弱的比较
【典例2】 SO 气体与足量Fe (SO ) 溶液完全反应后,再加入K Cr O 溶液,
2 2 4 3 2 2 7
发生如下化学反应:①SO +2Fe3++2H O===SO+2Fe2++4H+;②Cr O+6Fe2+
2 2 2
+14H+===2Cr3++6Fe3++7H O。则下列有关说法不正确的是( )
2
A.氧化性:Cr O>Fe3+>SO
2 2B.标准状况下,若有6.72 L SO 参加反应,则最终消耗0.2 mol K Cr O
2 2 2 7
C.反应②中,每有1 mol K Cr O 参加反应,转移电子的数目为6N
2 2 7 A
D.由上述反应原理推断:K Cr O 能将Na SO 氧化成Na SO
2 2 7 2 3 2 4
答案 B
解析 由①可知,Fe元素的化合价降低,则氧化性为Fe3+>SO ,由②可知,
2
Cr元素的化合价降低,则氧化性为Cr O>Fe3+,A项正确;6.72 L SO (标准状况)
2 2
参加反应,n(SO )=6.72 L÷22.4 L·mol-1=0.3 mol,由题述两个反应可知,存在
2
3SO ~Cr O,则最终消耗0.1 mol K Cr O ,B项错误;每有1 mol K Cr O 参加反
2 2 2 2 7 2 2 7
应,转移电子的物质的量为1 mol×2×(6-3)=6 mol,即转移电子的数目为6N ,
A
C项正确;因氧化性Cr O>SO ,则K Cr O 能将Na SO 氧化成Na SO ,D项正确
2 2 2 2 7 2 3 2 4
【对点练4】 (应用方程式判断性质的强弱)现有下列三个氧化还原反应:
①2FeCl +2KI===2FeCl +2KCl+I
3 2 2
②2FeCl +Cl ===2FeCl
2 2 3
③2KMnO +16HCl===2KCl+2MnCl +5Cl ↑+8H O
4 2 2 2
若某溶液中含有Fe2+、Cl-和I-,要除去I-而不氧化Fe2+和Cl-,可以加入的
试剂是( )
A.Cl B.KMnO
2 4
C.FeCl D.HCl
3
答案 C
解析 由①知氧化性:Fe3+>I ,还原性:I->Fe2+;由②知氧化性:Cl >Fe3+,还
2 2
原性:Fe2+>Cl-;由③知氧化性:MnO>Cl ,还原性:Cl->Mn2+;由此推知氧化性
2
强弱顺序为KMnO >Cl >FeCl >I ,还原性强弱顺序为I->Fe2+>Cl->Mn2+。所以
4 2 3 2
KMnO 可氧化Cl-、Fe2+及I-,Cl 可氧化Fe2+及I-,FeCl 只能氧化I-。
4 2 3
【对点练5】 (性质强弱的判断)已知H SO +I +H O===H SO +2HI,将0.1
2 3 2 2 2 4
mol Cl 通入100 mL含等物质的量的HI与H SO 的混合溶液中,有一半的HI被
2 2 3
氧化,则下列说法正确的是( )
A.物质的还原性:HI>H SO >HCl
2 3
B.H SO 的物质的量浓度为0.6 mol·L-1
2 3
C.若再通入0.05 mol Cl ,恰好能将HI和H SO 完全氧化
2 2 3
D.通入 0.1 mol Cl 发生反应的离子方程式为:5Cl +4H SO +2I-+
2 2 2 3
4H O===4SO+I +10Cl-+16H+
2 2
答案 D解析 根据H SO +I +H O===H SO +2HI可知,H SO 还原性强于HI;将
2 3 2 2 2 4 2 3
0.1 mol Cl 通入100 mL含等物质的量的HI与H SO 的混合溶液中,氯气先氧化
2 2 3
H SO ,再氧化HI;物质的还原性:H SO >HI>HCl,故A错误;设H SO 的物质
2 3 2 3 2 3
的量为x mol,则H SO 消耗氯气为x mol;有 mol的HI被氧化,消耗氯气 mol,x
2 3
mol+ mol=0.1 mol,x=0.08 mol,所以H SO 的物质的量浓度为0.8 mol·L-1,故
2 3
B错误;0.08 mol H SO 消耗氯气为0.08 mol,0.08 mol HI消耗氯气为0.04 mol,共
2 3
消耗氯气0.12 mol,所以若再通入0.02 mol Cl ,恰好能将HI和H SO 完全氧化,
2 2 3
故C错误;通入0.1 mol Cl 被氧化的HI只有H SO 的一半,发生反应的离子方程
2 2 3
式为:5Cl +4H SO +2I-+4H O===4SO+I +10Cl-+16H+,故D正确。
2 2 3 2 2
【对点练6】 (信息型反应的性质强弱判断)某学生做如下实验:第一步,在淀
粉-KI溶液中,滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;第二
步,在上述蓝色溶液中,滴加足量的Na SO 溶液,蓝色逐渐消失。下列有关该同
2 3
学对实验原理的解释和所得结论的叙述不正确的是( )
A.氧化性:ClO->I >SO
2
B.蓝色消失的原因是Na SO 溶液具有漂白性
2 3
C.淀粉-KI溶液变蓝是因为I-被ClO-氧化为I ,I 使淀粉变蓝
2 2
D.若将Na SO 溶液加入氯水中,氯水褪色
2 3
答案 B
解析 由NaClO+2KI+H SO ===I +NaCl+K SO +H O,ClO-的氧化性强
2 4 2 2 4 2
于I 的氧化性,由Na SO +I +H O===Na SO +2HI,I 的氧化性强于SO的氧化
2 2 3 2 2 2 4 2
性,所以氧化性强弱为:ClO->I >SO,故A正确;由第二步反应可知,S元素的
2
化合价升高,则蓝色消失的原因是Na SO 溶液具有还原性,故B错误;由第一步
2 3
反应可知,淀粉-KI溶液变蓝是因为I-被氧化为I ,淀粉遇I 变蓝,故C正确;氯
2 2
气的氧化性强于碘单质,碘单质将亚硫酸钠氧化为硫酸钠,所以氯气更能将亚硫
酸钠氧化,而使氯水褪色,故D正确。
判断物质氧化性、还原性强弱的常用方法
(1)根据化学方程式判断
①氧化性: 氧化剂>氧化产物。
②还原性: 还原剂>还原产物。
(2)根据反应条件和产物价态高低判断。(3)熟记常见物质氧化性、还原性顺序
①氧化性:KMnO >Cl >Br >Fe3+ >I >S
4 2 2 2
②还原性:Cl- Fe2+,氯气先和I-反应,过量的氯气再和Fe2+反应,B正确; Co O 的氧化性强
2 3
于Cl ,反应中有氯气生成,C正确; Fe3+的氧化性强于I ,因此两者发生反应,D
2 2
正确。
【对点练7】 (2020·福建福州市高三模拟)在含有FeCl 、CuCl 的混合溶液中
3 2
加入铁粉,充分反应后仍有固体存在,下列判断正确的是( )
A.加入KSCN溶液可能变红色
B.溶液中一定含有Fe2+
C.溶液中一定不含Cu2+
D.剩余固体中一定含有Fe
答案 B
解析 由于金属有剩余,溶液中一定不存在Fe3+,所以加入KSCN溶液一定
不变红色,故A错误;固体有剩余,Fe3+、Cu2+的氧化性强弱为:Fe3+>Cu2+,Fe3+
优先反应,溶液中一定存在Fe2+,故B正确;若Fe不足,溶液中可能有Cu2+,故C错误;根据以上分析可知如果铁不足,剩余的固体没有铁,故D错误。
【对点练8】 (转化规律的应用)已知G、Q、X、Y、Z均为含氯元素的化合物,在
一定条件下有下列转化关系(未配平):
①G―→Q+NaCl
②Q+H O――→X+H
2 2
③Y+NaOH―→G+Q+H O
2
④Z+NaOH―→Q+X+H O
2
这五种化合物中Cl元素化合价由低到高的顺序是( )
A.G、Y、Q、Z、X B.X、Z、Q、G、Y
C.X、Z、Q、Y、G D.G、Q、Y、Z、X
答案 A
解析 由①得出Q中价态高于G,因为G必介于Q和-1价的氯元素之间,
-1价为氯元素的最低价;将该结论引用到③,Y介于Q与G之间,故有Q价态
高于Y,Y价态高于G;分析②:H O中的H元素化合价降低,则Q中的氯元素转
2
变为X中的氯元素,化合价必升高,则得出X价态高于Q;最后分析④:Z介于
Q、X之间,则X价态高于Z,Z价态高于Q,所以五种化合物中Cl元素化合价由
低到高的顺序为G、Y、Q、Z、X,故选A。
【对点练9】 (电子守恒的应用)NSR技术能有效降低柴油发动机在空气过量
条件下的NO (氮氧化物)的排放,其工作原理:NO 的储存和还原在不同时段交替
x x
进行,如图所示。下列说法不正确的是( )
A.储存过程中化合价发生改变的元素有两种
B.还原过程中,Ba(NO ) 转化为BaO
3 2
C.在储存过程中,参加反应的NO和O 的物质的量之比为2∶1
2
D.还原过程中,若还原性气体为H ,则参加反应的H 与生成的N 的物质的
2 2 2
量之比是5∶1
答案 C
解析 在储存过程中,只有氮、氧元素的化合价发生变化,A正确;还原过程
中,Ba(NO ) 与还原性气体反应生成氧化钡、氮气和水,B正确;储存过程中,NO
3 2与O 、BaO反应生成Ba(NO ) 1 mol NO完全反应化合价升高了3 mol,1 mol O 完
2 3 2, 2
全反应得到4 mol电子,根据电子守恒可知,参加反应的NO和O 的物质的量之
2
比=4 mol∶3 mol=4∶3,故C错误;还原过程中,若还原性气体为H 1 mol氢气
2,
完全反应失去2 mol电子,Ba(NO ) 中+5价N转化成N 得到10 mol电子,根据
3 2 2
电子守恒可知,参加反应的H 与生成的N 的物质的量之比=10 mol∶2 mol=
2 2
5∶1,故D正确。
价态归中(转化)规律思维模型
含不同价态的同种元素的物质间发生氧化还原反应时,该元素价态的变化一
定遵循“高价+低价→中间价”,而不会出现交叉现象。简记为“两相靠,不相
交”。
例如,不同价态硫元素之间可以发生的氧化还原反应是
注:H S与浓H SO 反应可以是③、④或H S转化为S、H SO 转化为SO ,但
2 2 4 2 2 4 2
⑤不会发生。
1.(2020·山东学业水平等级考试)下列叙述不涉及氧化还原反应的是( )
A.谷物发酵酿造食醋
B.小苏打用作食品膨松剂
C.含氯消毒剂用于环境消毒
D.大气中NO 参与酸雨形成
2
答案 B
解析 谷物发酵酿造食醋过程中 CH CH OH转化为CH COOH属于氧化还
3 2 3
原反应,A项不符合题意;小苏打用作食品膨松剂利用的是NaHCO 受热分解会
3
放出CO 的性质,不涉及氧化还原反应,B项符合题意;含氯消毒剂具有较强的氧
2
化性,消毒时发生氧化还原反应,C项不符合题意;大气中的NO 形成酸雨时发
2
生反应3NO +H O===2HNO +NO,该反应属于氧化还原反应,D项不符合题意
2 2 3
2.(2020·北京等级考)下列物质的应用中,利用了氧化还原反应的是( )A.用石灰乳脱除烟气中的SO
2
B.用明矾[KAl(SO ) ·12H O]处理污水
4 2 2
C.用盐酸去除铁锈(主要成分Fe O ·xH O)
2 3 2
D.用84消毒液(有效成分NaClO)杀灭细菌
答案 D
解析 石灰乳脱除烟气中的SO 的原理为Ca(OH) +SO ===CaSO +H O,发
2 2 2 3 2
生非氧化还原反应,A项错误;用明矾处理污水的原理是明矾溶于水,铝离子水
解生成的氢氧化铝胶体能吸附水中的悬浮物质,发生非氧化还原反应,B项错误
盐酸去除铁锈的原理为Fe O ·xH O+6HCl===2FeCl +(3+x)H O,发生非氧化还
2 3 2 3 2
原反应,C项错误;84消毒液中的有效成分NaClO与空气中的水、二氧化碳反应
生成次氯酸,次氯酸具有强氧化性,可使蛋白质氧化变性,从而起到杀灭细菌的
作用,发生了氧化还原反应,D项正确。
3.(2020·北京卷)水与下列物质反应时,水表现出氧化性的是( )
A.Na B.Cl
2
C.NO D.Na O
2 2
答案 A
解析 A.2Na+2H O===2NaOH+H ↑,H O中H元素化合价由+1降为0
2 2 2
价,得电子被还原,做氧化剂,在反应中表现出氧化性,故 A正确;B.Cl +
2
H OHCl+HClO,H O中的元素没有发生化合价的变化,水在反应中既不是氧
2 2
化剂也不是还原剂,既不表现氧化性也不表现还原性,故 B错误;C.3NO +
2
H O===2HNO +NO,H O中的元素没有发生化合价的变化,水在反应中既不是
2 3 2
氧化剂也不是还原剂,既不表现氧化性也不表现还原性,故C错误;D.Na O+
2
H O===2NaOH,该反应没有元素化合价变化,不是氧化还原反应,水在反应中既
2
不表现氧化性也不表现还原性,故D错误。
4.(双选)(2020·海南高考)含有下列有害组分的尾气,常用NaOH溶液吸收以
保护环境。吸收过程中发生歧化反应的是( )
A.SO B.Cl
3 2
C.NO D.HBr
2
答案 BC
解析 A.三氧化硫与氢氧化钠反应生成硫酸钠和水,为非氧化还原反应,A
不符合题意;B.氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,氯气中Cl元素
的化合价既升高又降低,发生氧化还原反应,属于歧化反应,B符合题意;C.二氧化氮与氢氧化钠反应生成亚硝酸钠、硝酸钠和水,N元素化合价既升高又降低,
发生氧化还原反应,属于歧化反应,C符合题意;D.溴化氢与氢氧化钠反应生成溴
化钠和水,为非氧化还原反应,D不符合题意。
5.(2021·1 月 湖 南 普 高 校 招 生 适 应 性 考 试 , 8) 已 知 反 应 : 2NaClO +
3
4HCl===2ClO ↑+Cl ↑+2NaCl+2H O,下列关于该反应说法错误的是( )
2 2 2
A.氧化性:NaClO >Cl
3 2
B.当反应中有2 mol e-转移时,被氧化的HCl为4 mol
C.氧化产物和还原产物的物质的量之比为1∶2
D.产物ClO 和Cl 都可以用于自来水消毒杀菌
2 2
答案 B
解析 由分析可知,氯酸钠是氧化剂,氯气是氧化产物,在同一个氧化还原反应
中氧化剂的氧化性大于氧化产物的氧化性,则氧化性:NaClO >Cl ,故A不选;当
3 2
反应中有2 mol e-转移时,氯化氢中氯元素的化合价由-1升高到0,则被氧化的
HCl为2 mol,故B选;由分析可知,Cl 是氧化产物,ClO 是还原产物,由化学方
2 2
程式2NaClO +4HCl===2ClO ↑+Cl ↑+2NaCl+2H O可知,氧化产物和还原
3 2 2 2
产物的物质的量之比为1∶2,故C不选;产物ClO 和Cl 都具有氧化性,可以用
2 2
于自来水消毒杀菌,故D不选。
6.(2020·海南高考改编)以黄铁矿(主要成分FeS )为原料生产硫酸,应将产出
2
的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所
示。
回答下列问题:
(1)黄铁矿中硫元素的化合价为________。
(2)由炉渣制备还原铁粉的化学方程式为___________________________。
(3)欲得到更纯的 NaHSO ,反应①应通入________(填 “过量”或“不足
3
量”)的SO 气体。
2
(4)因为 Na S O 具有________性, 导致商品 Na S O 中不可避免地存在
2 2 5 2 2 5
Na SO 。检验其中含有SO的方法是_______________________________。
2 4(5)一般用K Cr O 滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样
2 2 7
品,用过量稀硫酸溶解,用标准K Cr O 溶液滴定其中的Fe2+。反应离子方程式为:
2 2 7
__________________________________________________________。
(6)①H O 的强氧化性使其对大多数致病菌和病毒具有消杀功能。用3%医用
2 2
H O 对传染病房喷洒消毒时,地板上有气泡冒出,该气体是________。
2 2
②H O 的一种衍生物K S O ,阴离子结构式为( )。其中性溶液加
2 2 2 2 8
热至沸后,溶液pH降低,用离子方程式表明原因:___________________。
答案 (1)-1 (2)Fe O +3CO=====2Fe+ 3CO (3)过量 (4)还原 先加
2 3 2
入盐酸,再加入氯化钡溶液,生成白色沉淀,说明含有 SO (5)Cr O+6Fe2+ +
2
14H+===2Cr3++6Fe3+ +7H O (6)①氧气 ②S O+H OHSO+H++SO
2 2 2
解析 (1)黄铁矿的主要成分是二硫化亚铁(FeS ),其中铁元素的化合价是+2
2
价,因此硫元素的化合价为-1价;(2)炉渣的主要成分为Fe O ,由炉渣制备还原
2 3
铁粉的化学方程式为Fe O +3CO=====2Fe+ 3CO ;(3)Na SO 溶液能够与SO
2 3 2 2 3 2
反应生成 NaHSO ,欲得到更纯的 NaHSO ,反应①应通入过量的 SO 气体;
3 3 2
(4)Na S O 转化为Na SO 过程中S元素的化合价升高,被氧化,体现了Na S O
2 2 5 2 4 2 2 5
的还原性;检验其中含有SO的方法是首先用盐酸酸化,除去S O,再加入氯化钡
2
溶液,看有无白色沉淀生成,若生成白色沉淀,证明含有 SO,否则没有SO;
(5)K Cr O 溶液滴定溶液中Fe2+,反应的离子方程式为:Cr O+6Fe2+ +14H+
2 2 7 2
===2Cr3++6Fe3++7H O;(6)①利用双氧水消毒的时候会有气泡放出,是由于双
2
氧水分解生成的氧气的缘故,故放出的气体是氧气;②过硫酸根在水中易发生水
解生成过一硫酸氢根、硫酸根和氢离子,加热升高温度有助于加速水解,其溶液
pH降低,故过硫酸根水解的方程式为S O+H OHSO+H++SO。
2 2
一、选择题(每小题只有一个选项符合题意)
1.化学与生活密切相关。下列应用中利用了物质氧化性的是( )
A.明矾净化水 B.纯碱去油污
C.食醋除水垢 D.漂白粉漂白织物
答案 D
2.(2020·山西太原市实验中学高三月考)下列实验中,颜色的变化与氧化还
原反应有关的是( )
A.往紫色石蕊溶液中加入盐酸,溶液变红B.饱和FeCl 溶液在沸水中变成红褐色胶体
3
C.向FeSO 溶液中滴加NaOH溶液,生成的沉淀由白色变成灰绿色,最后变
4
成红褐色
D.SO 使有酚酞的NaOH溶液褪色
2
答案 C
解析 酸遇紫色石蕊变红,只与酸性有关,与氧化还原反应无关,A错误;铁
离子水解生成胶体,只与水解有关,B错误;硫酸亚铁与氢氧化钠发生复分解反
应生成氢氧化亚铁,氢氧化亚铁被氧化为红褐色的氢氧化铁,涉及了氧化还原反
应,C正确;SO 与氢氧化钠溶液发生复分解反应生成亚硫酸钠和水,NaOH在反
2
应中消耗,则溶液褪色,只与复分解反应和碱溶液的性质有关,D错误。
3.宋代著名法医学家宋慈所著的《洗冤集录》中有“银针验毒”的记载。“银
针验毒”的原理是4Ag+2H S+O ===2Ag S+2H O,下列有关该反应的说法正
2 2 2 2
确的是( )
A.Ag是氧化剂 B.O 被氧化
2
C.H S发生氧化反应 D.Ag S是氧化产物
2 2
答案 D
解析 该反应中银元素化合价从0变为+1,化合价升高被氧化,作还原剂,
故A错误;在反应中氧元素化合价从0变为-2,化合价降低被还原,故B错误;
反应中H S含有的H、S元素化合价没有变化,则H S既不是氧化剂又不是还原
2 2
剂,故C错误;在反应中Ag被氧化,则Ag S为氧化产物,故D正确。
2
4.(2020·浙江1月选考)反应MnO +4HCl(浓)=====MnCl +Cl ↑+2H O中,
2 2 2 2
氧化产物是( )
A.MnO B.HCl
2
C.MnCl D.Cl
2 2
答案 D
解析 氧化产物是由还原剂经氧化反应而得到的,化合价升高后的产物,分
析方程式,HCl中Cl元素的化合价为-1价,而Cl 中Cl元素的化合价为0价,化
2
合价升高,Cl 是氧化产物。
2
5.ClO 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下
2
反应制得 ClO :2KClO +H C O +H SO =====2ClO ↑+K SO +2CO ↑+
2 3 2 2 4 2 4 2 2 4 2
2H O。下列说法正确的是( )
2
A.ClO 是氧化产物
2B.KClO 在反应中得到电子
3
C.H C O 在反应中被还原
2 2 4
D.1 mol KClO 完全参与反应有2 mol电子转移
3
答案 B
解析 Cl元素的化合价由+5价降低为+4价,KClO 在反应中得到电子,
3
ClO 是还原产物,A项错误,B项正确;H C O 为还原剂,在反应中被氧化,C项
2 2 2 4
错误;1 mol KClO 完全参与反应,转移的电子有1 mol×(5-4)=1 mol,D项错误。
3
6.O F 可以发生反应:H S+4O F ===SF +2HF+4O ,下列说法正确的是(
2 2 2 2 2 6 2
)
A.氧气是氧化产物
B.O F 既是氧化剂又是还原剂
2 2
C.若生成4.48 L HF,则转移0.8 mol电子
D.还原剂与氧化剂的物质的量之比为1∶4
答案 D
解析 A项,O元素的化合价由反应前的+1价变为反应后的0价,化合价降
低,获得电子,所以氧气是还原产物,错误;B项,在反应中O F 中的O元素的化
2 2
合价降低,获得电子,所以该物质是氧化剂,而H S中的S元素的化合价是-2价,
2
反应后变为SF 中的+6价,所以H S是还原剂,错误;C项,外界条件不明确,不
6 2
能确定HF的物质的量,所以不能确定转移电子的数目,错误;D项,根据反应化
学方程式可知还原剂H S与氧化剂O F 的物质的量之比是1∶4,正确。
2 2 2
7.已知下列反应:
反应Ⅰ:Co O +6HCl(浓)===2CoCl +Cl ↑+3H O
2 3 2 2 2
反应Ⅱ:5Cl +I +6H O===10HCl+2HIO
2 2 2 3
下列说法正确的是( )
A.反应Ⅰ中HCl是氧化剂
B.反应Ⅱ中Cl 发生氧化反应
2
C.氧化性:Co O >Cl >HIO
2 3 2 3
D.还原性:CoCl >HCl>I
2 2
答案 C
解析 反应Ⅰ中Cl元素的化合价部分升高,则HCl为还原剂,故A项错误;
反应Ⅱ中Cl元素的化合价降低,则Cl 发生还原反应,故B项错误;由氧化剂的
2
氧化性强于氧化产物的氧化性可知,反应Ⅰ中氧化性:Co O >Cl ,反应Ⅱ中氧化
2 3 2性:Cl >HIO ,则氧化性:Co O >Cl >HIO ,故C项正确;由还原剂的还原性强
2 3 2 3 2 3
于还原产物的还原性,反应Ⅰ中还原性:HCl>CoCl ,反应Ⅱ中还原性:I >HCl,
2 2
故还原性:I >HCl>CoCl ,D项错误。
2 2
8.(2021·广东惠州高三第一次调研)为防止废弃的硒单质(Se)造成环境污染,
通常用浓硫酸将其转化成二氧化硒(SeO ),再用KI溶液处理回收Se。发生的反应
2
为 ① Se + 2H SO ( 浓 )===2SO ↑ + SeO + 2H O ; ② SeO + 4KI +
2 4 2 2 2 2
4HNO ===4KNO +Se+2I +2H O,下列说法错误的是( )
3 3 2 2
A.①中SO 是还原产物,SeO 是氧化产物
2 2
B.②中KI是还原剂,HNO 是氧化剂
3
C.②中每生成0.2 mol I 共转移0.4 mol电子
2
D.氧化性由强到弱的顺序是:H SO (浓)>SeO >I
2 4 2 2
答案 B
解析 反应①中Se是还原剂,对应的生成物SeO 是氧化产物,浓硫酸是氧
2
化剂,对应的生成物SO 是还原产物,A项正确;反应②中Se由+4价变为0价,
2
SeO 是氧化剂,I由-1价变为0价,KI是还原剂,N在反应前后化合价没有变化
2
HNO 既不是氧化剂也不是还原剂,B项错误;反应②中I由-1价变为0价,则生
3
成0.2 mol I 转移0.4 mol电子,C项正确;由氧化剂的氧化性大于氧化产物的氧
2
化性可得氧化性:H SO (浓)>SeO >I ,D项正确。
2 4 2 2
9.(2020·湖南株洲质检)向CuSO 溶液中逐滴加入KI溶液至过量,观察到有
4
沉淀(CuI)生成,且溶液变为棕色。再向反应后的混合物中不断通入SO 气体,溶
2
液逐渐变成无色。下列有关分析中正确的是( )
A.上述实验条件下,物质的氧化性:Cu2+>SO >I
2 2
B.在SO 与I 反应中得到的还原产物为H SO
2 2 2 4
C.通入SO 后溶液逐渐变成无色,体现了SO 的漂白性
2 2
D.滴加KI溶液时,每转移2 mol e-会生成2 mol CuI沉淀
答案 D
解析 由题干信息可知,向 CuSO 溶液中加入 KI 溶液时发生反应:
4
,当转移2 mol e-时生成2 mol CuI沉
淀,故D项正确;向反应后的混合物中再通入SO 气体,又发生反应:I +SO +
2 2 2
2H O===H SO +2HI②,该反应中SO 作还原剂,体现了SO 的还原性,得到的还
2 2 4 2 2
原产物是HI,故B、C均不正确;根据氧化剂的氧化性强于氧化产物的氧化性可知,反应①中氧化性:Cu2+>I ,反应②中I 将SO 氧化,说明氧化性:I >SO ,故A
2 2 2 2 2
项错误。
10.已知下列实验事实:①Cr O 固体既能溶于KOH溶液得到KCrO 溶液,
2 3 2
又能溶于硫酸得到Cr (SO ) 溶液;②将K Cr O 溶液滴加到淀粉KI溶液中,溶液
2 4 3 2 2 7
变蓝;③向KCrO 溶液中滴加H O 溶液,再酸化,可得K Cr O 溶液。下列判断不
2 2 2 2 2 7
正确的是( )
A.化合物KCrO 中Cr为+3价
2
B.实验①证明Cr O 是两性氧化物
2 3
C.实验②证明氧化性:Cr O>I
2 2
D.实验③证明H O 既有氧化性又有还原性
2 2
答案 D
解析 A项,化合物KCrO 中,K为+1价,O为-2价,由化合物中正、负化
2
合价的代数和为0知,Cr为+3价,正确;B项,由反应①可知,氧化铬与酸、碱反
应均生成盐和水,为两性氧化物,正确;C项,由②中溶液变蓝,生成碘单质,发生
了氧化还原反应,Cr的化合价降低,I的化合价升高,由氧化剂的氧化性大于氧化
产物的氧化性知,氧化性:Cr O>I ,正确;D项,实验③中发生氧化还原反应,Cr
2 2
的化合价由+3价升高为+6价,则过氧化氢中O的化合价降低,证明H O 有氧
2 2
化性,错误。
11.(2020·四川成都摸底)在酸性条件下,黄铁矿(FeS )催化氧化的反应方程式
2
为2FeS +7O +2H O===2Fe2++4SO+4H+,实现该反应的物质间转化如图所示
2 2 2
下列分析错误的是( )
A.反应Ⅰ的离子方程式为4Fe(NO)2++O +4H+===4Fe3++4NO+2H O
2 2
B.反应Ⅱ的氧化剂是Fe3+
C.反应Ⅲ是氧化还原反应
D.黄铁矿催化氧化中NO作催化剂
答案 C
解析 结合题图和元素守恒可知,反应Ⅰ在酸性条件下进行,其反应的离子
方程式为4Fe(NO)2++4H++O ===4Fe3++4NO+2H O,A项正确;反应Ⅱ是Fe3
2 2+与 FeS 反应生成 SO 和 Fe2+,其反应的离子方程式为 14Fe3++FeS +
2 2
8H O===15Fe2++2SO+16H+,该反应中Fe3+将FeS 中-1价的硫氧化为+6价
2 2
的 SO,本身被还原为 Fe2+,Fe3+作氧化剂,B 项正确;反应Ⅲ为 Fe2++
NO===Fe(NO)2+,该反应中各元素的化合价均无变化,属于非氧化还原反应,C
项错误;结合总反应2FeS +7O +2H O===2Fe2++4SO+4H+和转化关系图可知
2 2 2
NO为该反应的催化剂,D项正确。
12.(2019·山东泰安二模)工业废水中含有的Cr O和CrO会对水体产生很大
2
的危害,这种工业废水必须净化处理。一种处理含铬废水的工艺流程如下:
CrO(黄色)――→Cr O(橙色)――→Cr3+――→Cr(OH) ↓
2 3
下列说法不正确的是( )
A.①中,酸化后发生反应为2CrO+2H+Cr O+H O
2 2
B.②中,反应的氧化剂与还原剂的物质的量之比为1∶6
C.③中,所得沉淀只有Cr(OH)
3
D.③中调pH所用物质可以是NH 或Fe O
3 2 3
答案 C
解析 酸化后,2CrO(黄色)+2H+Cr O(橙色)+H O正向移动,橙色加深,
2 2
A项正确;②中Cr元素的化合价降低,Fe元素的化合价升高,反应的离子方程式
为Cr O+6Fe2++14H+===2Cr3++6Fe3++7H O,可知氧化剂与还原剂的物质的
2 2
量之比为1∶6,B项正确;③中Fe3+在pH=4时会以氢氧化物形式沉淀,则③中
所得沉淀Cr(OH) 中含有Fe(OH) ,C项错误;①中酸化后,溶液显强酸性,③中可
3 3
以选用NH 或Fe O 与酸反应调节pH,D项正确。
3 2 3
二、非选择题(本题包括3小题)
13.HNO 是一种弱酸,且不稳定,易分解生成NO和NO ;它能被常见的强氧
2 2
化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO 是
2
一种难溶于水、易溶于酸的化合物,试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO ),则导致血红
2
蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
________(填字母)。
A.亚硝酸盐被还原
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂(2)某同学把新制的氯水加到 NaNO 溶液中,观察到氯水褪色,同时生成
2
NaNO 和HCl,请写出反应的离子方程式:
3
_______________________________________________________________。
(3)Fe与过量稀硫酸反应可以制取FeSO ,若将反应所得的酸性溶液中的Fe2+
4
转化为Fe3+,要求产物纯净,可选用的最佳试剂是________(填字母)。
a.Cl b.Fe
2
c.H O d.HNO
2 2 3
(4)FeSO 可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾
4
(K FeO ),氧化性比 Cl 、O 、ClO 、KMnO 更强,主要反应:2FeSO +
2 4 2 2 2 4 4
6Na O ===2Na FeO +2Na O+2Na SO +O ↑
2 2 2 4 2 2 4 2
①该反应中的氧化剂是________,还原剂是________。
②简要说明K FeO 作为水处理剂时所起的作用_____________________。
2 4
答案 (1)D
(2)NO+Cl +H O===NO+2H++2Cl- (3)c
2 2
(4)①Na O Na O 、FeSO
2 2 2 2 4
②高铁酸钾具有强氧化性,能杀菌消毒,消毒过程中自身被还原为Fe3+,Fe3+
水解生成Fe(OH) 胶体能吸附水中悬浮杂质而沉降
3
解析 (1)服用维生素C可以解毒,说明在维生素C作用下Fe3+又转化为Fe2
+,Fe元素化合价降低,被还原,则维生素C具有还原性,而亚硝酸盐会导致Fe2+
转化为Fe3+,说明亚硝酸盐具有氧化性,在反应中亚硝酸盐为氧化剂,维生素C
是还原剂。(3)Cl 、HNO 都能氧化亚铁离子,但能引入新的杂质;铁不能氧化亚铁
2 3
离子;双氧水的还原产物是水,不引入杂质,所以最佳试剂是双氧水。(4)该反应中
Fe元素化合价由+2价变为+6价,O元素化合价由-1价变为0价、-2价。①得
Na O 是氧化剂,Na O 、FeSO 是还原剂;②K FeO 中Fe元素的化合价为+6价,
2 2 2 2 4 2 4
具有强氧化性,且还原产物铁离子能水解生成氢氧化铁胶体,胶体具有吸附性,
能吸附除去水中的悬浮杂质。
14.过氧化氢俗名双氧水,医疗上利用它杀菌消毒的作用来清洗伤口。根据
下列反应回答问题:
A.Na O +2HCl===2NaCl+H O
2 2 2 2
B.Ag O+H O ===2Ag+O ↑+H O
2 2 2 2 2
C.2H O =====2H O+O ↑
2 2 2 2
D.3H O +Cr (SO ) +10KOH===2K CrO +3K SO +8H O
2 2 2 4 3 2 4 2 4 2(1)上述反应中,H O 仅体现氧化性的反应是(填字母,下同)________,H O 既
2 2 2 2
体现氧化性又体现还原性的反应是________,H O 体现酸性的反应是________。
2 2
(2)上述反应说明H O 、Ag O、K CrO 的氧化性由强到弱的顺序是________。
2 2 2 2 4
(3)储存过氧化氢的试剂瓶上最适合贴上的一个标签是________(填字母)。
(4)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六
种微粒:O 、MnO、H O、Mn2+、H O 、H+。已知该反应中H O 只发生了如下过程:
2 2 2 2 2 2
H O →O 。
2 2 2
①反应体系选择的酸是________(填字母)。
A.盐酸 B.浓硫酸
C.稀硫酸 D.醋酸
②如果上述反应中有 6.72 L(标准状况)气体生成,转移的电子为________
mol。
答案 (1)D C A
(2)Ag O>H O >K CrO
2 2 2 2 4
(3)B (4)①C ②0.6
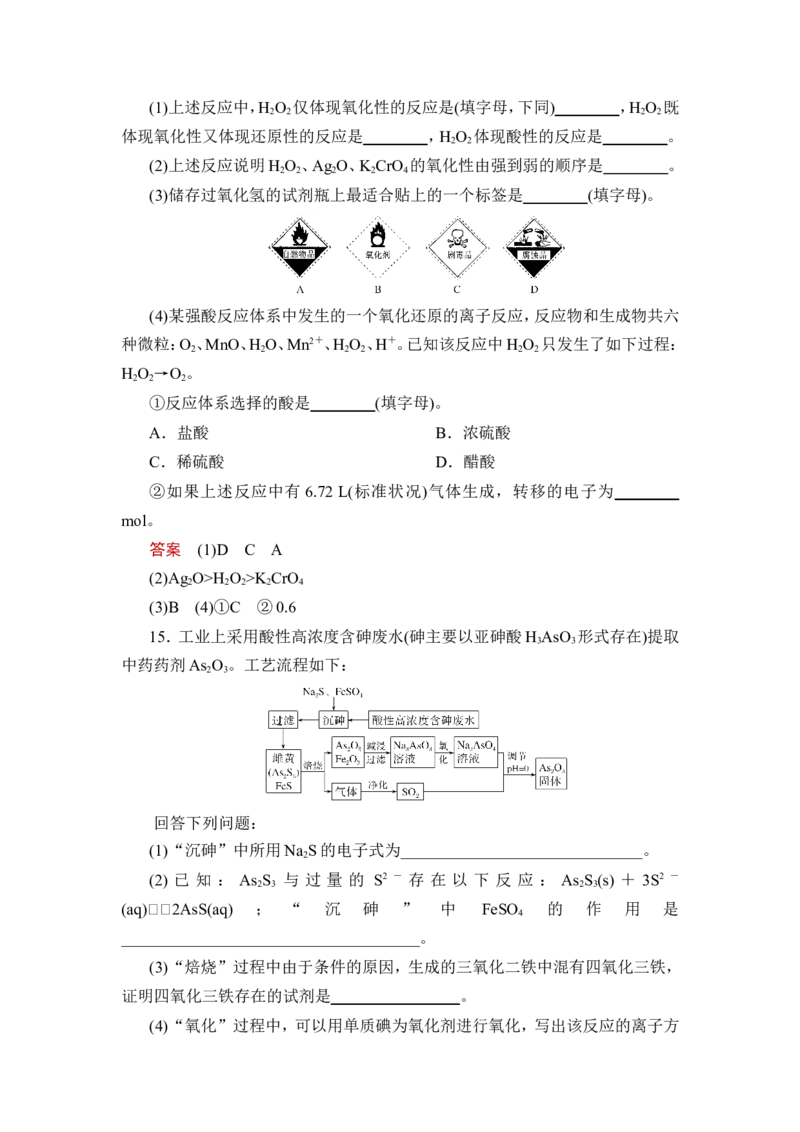
15.工业上采用酸性高浓度含砷废水(砷主要以亚砷酸H AsO 形式存在)提取
3 3
中药药剂As O 。工艺流程如下:
2 3
回答下列问题:
(1)“沉砷”中所用Na S的电子式为______________________________。
2
(2) 已 知 : As S 与 过 量 的 S2 - 存 在 以 下 反 应 : As S (s) + 3S2 -
2 3 2 3
(aq)2AsS(aq) ; “ 沉 砷 ” 中 FeSO 的 作 用 是
4
_____________________________________。
(3)“焙烧”过程中由于条件的原因,生成的三氧化二铁中混有四氧化三铁,
证明四氧化三铁存在的试剂是________________。
(4)“氧化”过程中,可以用单质碘为氧化剂进行氧化,写出该反应的离子方程式:_________________________________________________________。
(5)调节pH=0时,请写出由Na AsO 制备As O 的离子方程式:
3 4 2 3
_______________________________________________________________。
(6)一定条件下,用雄黄(As S )制备As O 的转化关系如图所示。若反应中,1
4 4 2 3
mol As S (其中As元素的化合价为+2价)参加反应时,转移28 mol e-,则物质a
4 4
为________。
答案 (1)
(2)S2-与Fe2+生成沉淀,使平衡As S (s)+3S2-(aq)2AsS(aq)左移,提高沉
2 3
砷效果
(3)稀硫酸、高锰酸钾溶液(或其他合理答案)
(4)AsO+I +2OH-===2I-+AsO+H O
2 2
(5)2AsO+2SO +2H+===As O +2SO+H O
2 2 3 2
(6)SO
2
解析 (1)硫化钠为离子化合物,电子式为 。(2)FeSO 的
4
作用是除去过量的S2-,使平衡As S (s)+3S2-(aq)2AsS(aq)逆向移动,提高沉
2 3
砷效果。(3)四氧化三铁含有+2价铁,具有还原性,可在酸性条件下与高锰酸钾
反应,使溶液褪色,则可用硫酸、高锰酸钾溶液检验四氧化三铁。(6)1 mol As S 参
4 4
加反应时,转移28 mol e-,As S 中As为+2价、S为-2价,且生成As O ,则
4 4 2 3
As S 中S元素化合价升高 6,生成物中 S元素的化合价为+4,则物质 a应为
4 4
SO 。
2