文档内容
INCLUDEPICTURE "F:\\方正文件\\2019 文
件\\课件\\2020 版 创新设计 高考总复习
化 学 人 教 版 \\ 第 五 章 .tif" \*
MERGEFORMATINET
第1讲 原子结构 化学键
【2020·备考】
最新考纲:1.了解元素、核素和同位素的含义。2.了解原子的构成;了解原子序数、
核电荷数、质子数、中子数、核外电子数以及它们之间的相互关系。3.了解原子核
外电子排布。4.掌握原子结构示意图。5.了解化学键的定义。6.了解离子键、共价键
的形成。7.掌握电子式的表示方法。
核心素养:1.变化观念与平衡思想:认识化学键的本质是原子间的静电作用,能多
角度、动态的分析化学键。2.证据推理与模型认知:能运用原子结构模型解释化学
现象,揭示现象的本质与规律。3.科学探究与创新意识:能发现和提出有探究价值
的原子结构与化学键的问题,确定探究目的,设计研究方案。考点一 原子构成
(频数:★☆☆ 难度:★☆☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 原
子结构高考考查力度不是很大,注意有关概念辨析,重点掌握常见原子核外电子
排布特点,根据排布特点推断元素种类,熟知常见的等电子微粒。
1.原子的构成
(1)原子的定义:原子是化学变化中的最小微粒。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
①破坏原子结构的核变不属于化学变化。
②化学反应前后原子守恒。
(2)原子的构成
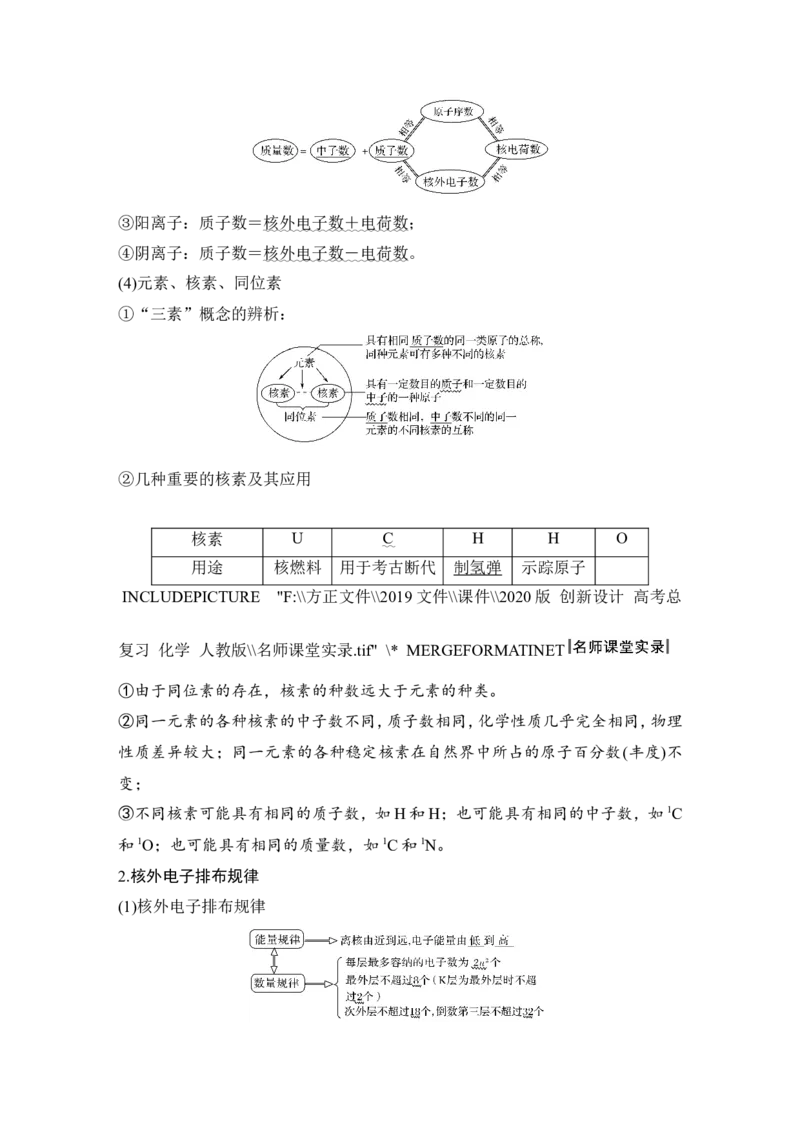
(3)原子内的等量关系
①质量数(A)= 质子数 ( Z )+ 中子数 ( N );
②质子数=原子序数=核电荷数=核外电子数;
图示:③阳离子:质子数=核外电子数+电荷数;
④阴离子:质子数=核外电子数-电荷数。
(4)元素、核素、同位素
①“三素”概念的辨析:
②几种重要的核素及其应用
核素 U C H H O
用途 核燃料 用于考古断代 制氢弹 示踪原子
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
①由于同位素的存在,核素的种数远大于元素的种类。
②同一元素的各种核素的中子数不同,质子数相同,化学性质几乎完全相同,物理
性质差异较大;同一元素的各种稳定核素在自然界中所占的原子百分数(丰度)不
变;
③不同核素可能具有相同的质子数,如H和H;也可能具有相同的中子数,如1C
和1O;也可能具有相同的质量数,如1C和1N。
2.核外电子排布规律
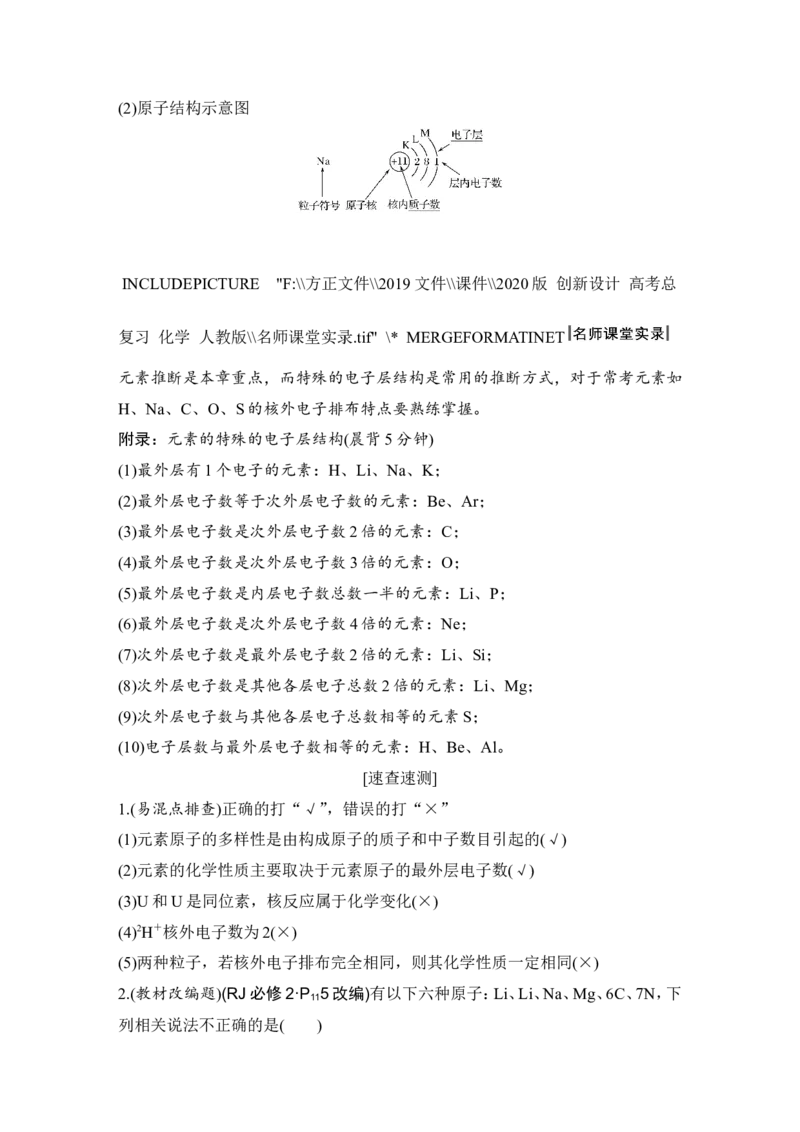
(1)核外电子排布规律(2)原子结构示意图
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
元素推断是本章重点,而特殊的电子层结构是常用的推断方式,对于常考元素如
H、Na、C、O、S的核外电子排布特点要熟练掌握。
附录:元素的特殊的电子层结构(晨背5分钟)
(1)最外层有1个电子的元素:H、Li、Na、K;
(2)最外层电子数等于次外层电子数的元素:Be、Ar;
(3)最外层电子数是次外层电子数2倍的元素:C;
(4)最外层电子数是次外层电子数3倍的元素:O;
(5)最外层电子数是内层电子数总数一半的元素:Li、P;
(6)最外层电子数是次外层电子数4倍的元素:Ne;
(7)次外层电子数是最外层电子数2倍的元素:Li、Si;
(8)次外层电子数是其他各层电子总数2倍的元素:Li、Mg;
(9)次外层电子数与其他各层电子总数相等的元素S;
(10)电子层数与最外层电子数相等的元素:H、Be、Al。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)元素原子的多样性是由构成原子的质子和中子数目引起的(√)
(2)元素的化学性质主要取决于元素原子的最外层电子数(√)
(3)U和U是同位素,核反应属于化学变化(×)
(4)2H+核外电子数为2(×)
(5)两种粒子,若核外电子排布完全相同,则其化学性质一定相同(×)
2.(教材改编题)(RJ必修2·P 5改编)有以下六种原子:Li、Li、Na、Mg、6C、7N,下
11
列相关说法不正确的是( )A.Li和Li在元素周期表中所处的位置相同
B.6C和7N质量数相等,二者互为同位素
C.Na和Mg的中子数相同但不属于同种元素
D.Li的质量数和7N的中子数相等
答案 B
3.(思维探究题)等质量的H O和D O:
2 2
物质的量之比:________________ 。
中子数之比:________________ 。
质子数之比:________________ 。
电子数之比:________________ 。
答案 10∶9 8∶9 10∶9 10∶9
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(2019·福建厦门一中期中)在陆地生态系统研究中,2H、13C、15N、18O、34S等常用
作环境分析指示物。下列说法中正确的是( )
A.34S原子核内中子数为16
B.2H+的酸性比1H+的酸性更强
C.13C和15N原子核内的质子数相差2
D.1HO在相同条件下比1HO更易蒸发
解析 34S原子核内的中子数为34-16=18,A项错误;2H+与1H+都是氢离子,化
学性质相同,即2H+的酸性与1H+的酸性相同,B项错误;13C原子的质子数为6,
15N原子的质子数为7,则13C和15N原子核内的质子数相差1,C项错误;因1HO的
相对分子质量为1×2+16=18,1HO的相对分子质量为1×2+18=20,则1HO的
沸点低,1HO在相同条件下比1HO更易蒸发,D项正确。
答案 D
2.(2019·上海同济中学月考)月球上的每百吨He聚变所释放出的能量相当于目前
人类一年消耗的能量,地球上氦元素主要以He的形式存在。已知一个12C原子的质量为a g,一个He原子的质量为b g,N 为阿伏加德罗常数。下列说法正确的是(
A
)
A.He比He多一个中子
B.氦元素的近似相对原子质量为3.5
C.He的相对原子质量为
D.He的摩尔质量为bN
A
解析 He比He少一个中子,A错误;不能确定核素的原子百分含量,因此不能计
算氦元素的近似相对原子质量,B错误;一个原子的真实质量与一个1C原子质量
的的比值是该核素的相对原子质量,因此He的相对原子质量为,C正确;He的摩
尔质量为bN g·mol-1,D错误。
A
答案 C
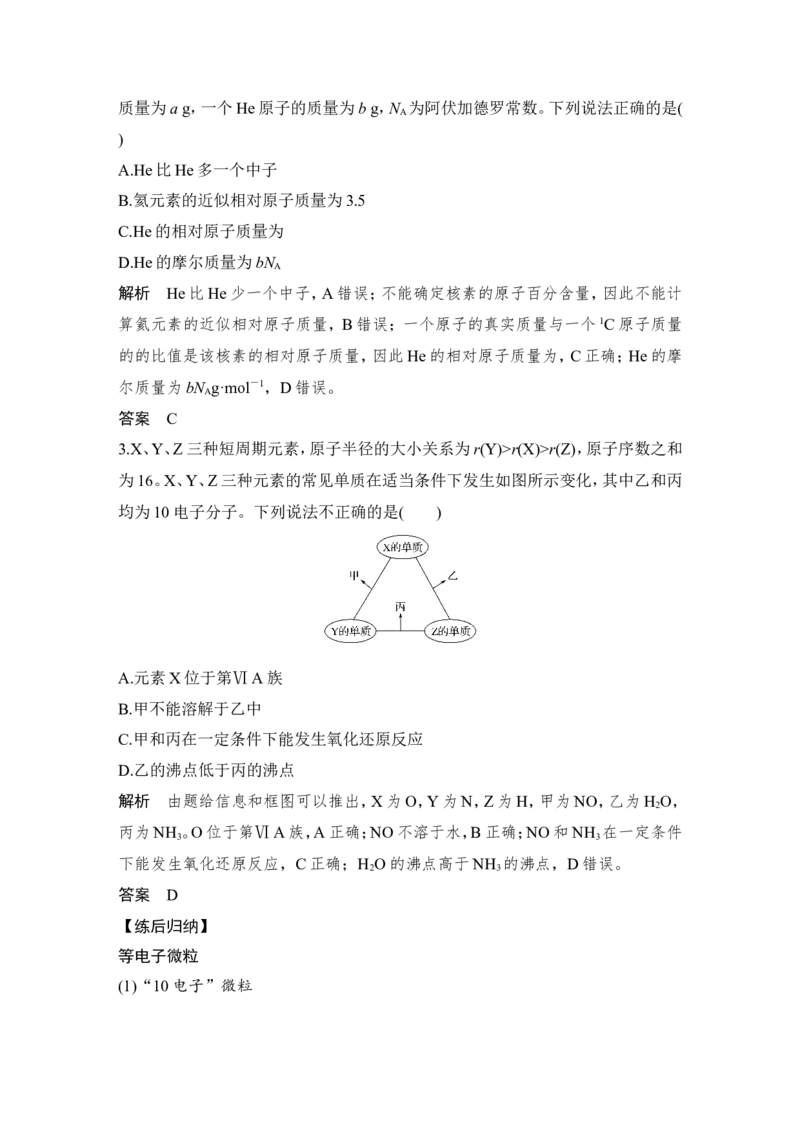
3.X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和
为16。X、Y、Z三种元素的常见单质在适当条件下发生如图所示变化,其中乙和丙
均为10电子分子。下列说法不正确的是( )
A.元素X位于第ⅥA族
B.甲不能溶解于乙中
C.甲和丙在一定条件下能发生氧化还原反应
D.乙的沸点低于丙的沸点
解析 由题给信息和框图可以推出,X为O,Y为N,Z为H,甲为NO,乙为H O,
2
丙为NH 。O位于第ⅥA族,A正确;NO不溶于水,B正确;NO和NH 在一定条件
3 3
下能发生氧化还原反应,C正确;H O的沸点高于NH 的沸点,D错误。
2 3
答案 D
【练后归纳】
等电子微粒
(1)“10电子”微粒(2)“14电子”微粒:Si、N 、CO、C H 、C。
2 2 2
(3)“16电子”微粒:S、O 、C H 、HCHO。
2 2 4
(4)“18电子”微粒
CH —CH 、H N—NH 、HO—OH、F—F、F—CH 、CH —OH……
3 3 2 2 3 3
[B组 考试能力过关]
4.(2017· 北 京 卷 )2016 年 IUPAC 命 名 117 号 元 素 为 Ts( 中 文 名 “
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\田.tif" \* MERGEFORMATINET ”,tián),Ts的原子核外最
外层电子数是7,下列说法不正确的是( )
A.Ts是第七周期第ⅦA族元素
B.Ts的同位素原子具有相同的电子数
C.Ts在同族元素中非金属性最弱
D.中子数为176的Ts核素符号是 Ts
解析 A.117号元素Ts的原子核外最外层电子数是7,可知Ts是第七周期第ⅦA
族元素,正确;B.同位素是同种元素不同原子之间的互称,因此Ts的同位素原子具
有相同的电子数,正确;C.根据元素周期律可知,同一主族元素从上往下非金属性
依次减弱,所以Ts在同族元素中非金属性最弱,正确;D.中子数为176的Ts核素
符号是Ts,错误。
答案 D
5.(海南化学)重水(D O)是重要的核工业原料,下列说法错误的是( )
2
A.氘(D)原子核外有1个电子
B.1H与D互称同位素C.H O与D O互称同素异形体
2 2
D.1HO与DO的相对分子质量相同
解析 A项,氘表示为H,核外有1个电子;D项,1HO的相对分子质量为20,DO
的相对分子质量也为20;C项,H O、D O均为化合物。
2 2
答案 C
6.(新课标全国卷)短周期元素W、X、Y、Z的原子序数依次增大,其简单离子都能
破坏水的电离平衡的是( )
A.W2-、X+ B.X+、Y3+
C.Y3+、Z2- D.X+、Z2-
解析 结合原子序数依次增大和简单离子的电荷数,确定W、X、Y、Z分别为O、
Na、Al、S四种元素,能发生水解的离子为Al3+、S2-,故C项正确。
答案 C考点二 化学键
(频数:★★☆ 难度:★☆☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 本
考点主要考查对两种常见化学键类型的理解与判断;以及对离子化合物和共价化
合物两种物质类别的判断;另外电子式的书写在二卷中也是一个重要的考查角度,
特别是在理解结构的基础上对陌生物质的电子式的书写方法,要重点掌握。
1.化学键
(1)定义:相邻原子间强烈的相互作用。
(2)分类
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
(1)分子间作用力、氢键不属于化学键。
(2)物质中并不一定都存在化学键,如He等稀有气体分子。
2.离子键与共价键
(1)概念
①离子键:阴、阳离子通过静电作用形成的化学键。
②共价键:原子间通过共用电子对所形成的化学键。
(2)对比
离子键 共价键
成键粒子 阴、阳离子 原子成键方式 得失电子形成阴、阳离子 形成共用电子对
活泼金属元素与活泼非金
成键条件 一般在非金属原子之间
属元素
作用力实质 静电作用
(1)非金属单质,如H 、O
2 2
等;
存在于离子化合物中,如
(2)共价化合物,如HCl、
存在举例 NaCl、KCl、MgCl 、CaCl 、
2 2 CO 、CH 等;
ZnSO 、NaOH等 2 4
4
(3)某些离子化合物,如
NaOH、Na O 等
2 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
(1)离子键中的“静电作用”既包括静电吸引力又包括静电排斥力。
(2)由活泼金属与活泼非金属形成的化学键不一定都是离子键,如AlCl 中Al—Cl
3
键为共价键。
(3)非金属元素的两个原子之间一定形成共价键,但多个原子间也可能形成离子键
如NH Cl等。
4
3.化学键的表示方法——电子式
(1)概念:在元素符号周围用“·”或“×”来代表原子的最外层电子(价电子)的式
子。
(2)书写
4.化学键与物质类别的关系
(1)化学键与物质类别的关系(2)离子化合物与共价化合物
与物质分
化合物类型 定 义 举例
类的关系
NaCl、Na O 、
包括强碱、绝大多数 2 2
含有离子键的化合
离子化合物 盐及活泼金属的氧 NaOH、Na O、
物 2
化物
NH Cl等
4
H S、SO 、
2 2
包括酸、弱碱、极少
CH COOH、
只含有共价键的化 数盐、气态氢化物、 3
共价化合物
合物 非金属氧化物、大多
H SO 、
2 4
数有机物等
NH ·H O等
3 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
(1)不同元素的两个非金属原子构成的物质一定是共价化合物,如HCl;两种非金
属元素多个原子可构成离子化合物,如NH H。
4
(2)离子化合物溶于水或熔化后均电离成自由移动的阴、阳离子,离子键被破坏;共
价化合物在液态下不电离,所以熔化时导电的化合物一定是离子化合物。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)所有物质中都存在化学键(×)
(2)由活泼金属元素与活泼非金属元素形成的化学键都是离子键(×)
(3)原子最外层只有一个电子的元素原子跟卤素原子结合时,所形成的化学键一定
是离子键(×)
(4)共价化合物溶于水,分子内共价键被破坏,单质溶于水,分子内共价键不被破
坏(×)(5)共价化合物熔点都低于离子化合物(×)
2.(教材改编题)(RJ必修2·P 9改编)有以下9种物质:
25
①Ne ② NH Cl ③ KNO ④ NaOH ⑤ Cl ⑥ SO ⑦ H S ⑧ Na O
4 3 2 2 2 2 2
⑨MgCl
2
(1)既存在离子键又存在共价键的是________。
(2)不存在化学键的是________。
(3)属于共价化合物的是________。
(4)属于离子化合物的是________。
答案 (1)②③④⑧ (2)① (3)⑥⑦ (4)②③④⑧⑨
3.(思维探究题)对于反应:2Na O +2CO ===2Na CO +O
2 2 2 2 3 2
断裂的化学键为:__________________________________________________。
形成的化学键为:____________________________________________________。
答案 离子键、极性和非极性共价键 离子键、极性和非极性共价键
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(2018·陕西西安模拟)在下列变化过程中,既有离子键被破坏又有共价键被破坏
的是( )
A.将SO 通入水中 B.烧碱溶于水
2
C.将HCl通入水中 D.硫酸氢钠溶于水
解析 SO 、HCl不含有离子键,所以不会有离子键的破坏过程,A、C错误;烧碱在
2
水溶液中电离产生了钠离子和氢氧根离子,没有共价键的破坏过程,B错误;硫酸
氢钠既含有离子键又含有共价键,溶于水时钠离子与硫酸氢根离子之间的离子键
被破坏,同时硫酸氢根离子中的共价键也被破坏。
答案 D
2.(2018·浙江温州模拟)下列说法正确的是( )
A.碘晶体受热转变为碘蒸气,吸收的热量用于克服碘原子间的作用力
B.硫酸钾和硫酸溶于水都电离出硫酸根离子,所以它们在熔融状态下都能导电C.N 、CO 和SiO 中都存在共价键,它们都是由分子构成
2 2 2
D.H 和Cl 在光照条件下反应生成HCl,反应中一定有共价键的断裂和形成
2 2
解析 A项,碘晶体受热转变为碘蒸气,吸收的热量用于克服分子间作用力,碘原
子间是共价键,错误;B项,硫酸是共价化合物,在熔融状态下不能导电,错误;C
项,N 、CO 和SiO 中都存在共价键,N 、CO 都是由分子构成,SiO 是由原子构成,
2 2 2 2 2 2
错误;D项,氢气、氯气和氯化氢中均含有共价键,因此反应中一定有共价键的断
裂和形成,正确。
答案 D
3.a、b、c、d为短周期元素,a的M电子层有1个电子,b的最外层电子数为内层电
子数的2倍,c的最高化合价为最低化合价绝对值的3倍,c与d同周期,d的原子
半径小于c。下列叙述错误的是( )
A.d元素的非金属性最强
B.它们均存在两种或两种以上的氧化物
C.只有a与其他元素生成的化合物都是离子化合物
D.b、c、d分别与氢形成的化合物中化学键均为极性共价键
解析 根据题意,短周期元素中,a的M层电子数为1个,则a为钠元素,b的最外
层电子数为内层电子数的2倍,则b为碳元素,c的最高化合价为最低化合价绝对
值的3倍,则c为硫元素,结合c与d同周期,d的原子半径小于c,故d为氯元素。
A项,上述元素中非金属性最强的元素是氯元素,正确;B项,钠可以形成Na O、
2
Na O 两种氧化物,碳元素可以形成CO、CO 两种氧化物,S元素可以形成SO 、
2 2 2 2
SO 两种氧化物,氯元素可以形成Cl O、ClO 、Cl O 等多种价态的氧化物,B项正
3 2 2 2 7
确;C项,钠为活泼金属元素,可以与非金属元素C、S、Cl等形成离子化合物,正确
D项,碳元素可以与氢元素形成只含有极性键的化合物,如CH ,也可形成含有极
4
性键和非极性键的化合物,如CH CH 等,硫元素形成的H S只含极性键,氯元素
3 3 2
与氢元素形成的HCl也只含极性键,错误。
答案 D
4.已知:
化合物 MgO Al O MgCl AlCl
2 3 2 3类型 离子化合物 离子化合物 离子化合物 共价化合物
熔点/℃ 2 800 2 050 714 191
工 业 制 镁 时 , 电 解 MgCl 而 不 电 解 MgO 的 原 因 是
2
_____________________________________________________________________;
制 铝 时 , 电 解 Al O 而 不 电 解 AlCl 的 原 因 是
2 3 3
____________________________________________________________________。
答案 MgO的熔点高,熔融时耗费更多资源,增加生产成本 AlCl 为共价化合物
3
熔融态难导电
【归纳总结】
化学键对物质性质的影响
1.对物理性质的影响
(1)金刚石、晶体硅、石英、金刚砂等物质硬度大、熔点高,就是因为其中的共价键
很强,破坏时需消耗很多的能量。
(2)NaCl等部分离子化合物,也有很强的离子键,故熔点也较高。
2.对化学性质的影响
(1)N 分子中有很强的共价键,故在通常状况下,N 性质很稳定。
2 2
(2)H S、HI等分子中的共价键较弱,故它们受热时易分解。
2
[B组 考试能力过关]
5.(全国卷)下列有关化学键的叙述,正确的是( )
A.离子化合物中一定含有离子键
B.单质分子中均不存在化学键
C.含有极性键的分子一定是极性分子
D.含有共价键的化合物一定是共价化合物
解析 特别注意:离子化合物中一定含有离子键,共价化合物中一定含有共价键;
含有离子键的化合物一定是离子化合物,但含有共价键的化合物不一定为共价化
合物,如NaOH、NH Cl等,故A项正确,D项错误;化学键既可以存在于化合物中,
4
也可以存在于双原子或多原子的单质分子中,如O 、O ,故B项错误;C项中,含
2 3
有极性键的分子不一定是极性分子,若分子结构对称,则为非极性分子,如CO 、
2
CH 等为非极性分子。
4
答案 A6.(2015·全国卷Ⅱ,9)原子序数依次增大的元素a、b、c、d,它们的最外层电子数分
别为1、6、7、1。a-的电子层结构与氦相同,b和c的次外层有8个电子,c-和d+的
电子层结构相同。下列叙述错误的是( )
A.元素的非金属性次序为c>b>a
B.a和其他3种元素均能形成共价化合物
C.d和其他3种元素均能形成离子化合物
D.元素a、b、c各自最高和最低化合价的代数和分别为0、4、6
解析 a-的电子层结构与氦相同,则a为氢元素;b和c的次外层有8个电子,且
最外层电子数分别为6、7,则b为硫元素,c为氯元素;d的最外层电子数为1,且c
-和d+的电子层结构相同,则d为钾元素。A项,元素的非金属性次序为Cl>S>H,
正确;H S和HCl是共价化合物,KH、K S和KCl是离子化合物,B项错误,C项正
2 2
确;D项,氢、硫、氯三种元素的最高和最低化合价分别为+1和-1、+6和-2、+
7和-1,因此它们各自最高和最低化合价的代数和分别为0、4、6,正确。
答案 B
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\分层课时作业.TIF" \* MERGEFORMATINET
[A级 全员必做题]
1.(2018·漳州八校高三联考)下列表示物质结构的化学用语或模型正确的是( )
A.HF的电子式:
B.HClO的结构式:H—O—Cl
C.S2-的结构示意图:
D.CH 分子的球棍模型:
4解析 HF是共价化合物,不存在离子键,分子中氟原子与氢原子形成1个共用电
子对,电子式为 ,A错误;次氯酸的中心原子为O,HClO的结构式
正确,B正确,硫离子质子数为16,核外电子数为18,有3个电子层,由里到外各
层电子数分别为2、8、8,离子结构示意图为 ,C错误;球棍模型可以表示
原子之间的成键形式、分子的空间结构等, 不能表示甲烷中原子之间的成键
情况,是甲烷的比例模型,甲烷的球棍模型为 ,D错误。
答案 B
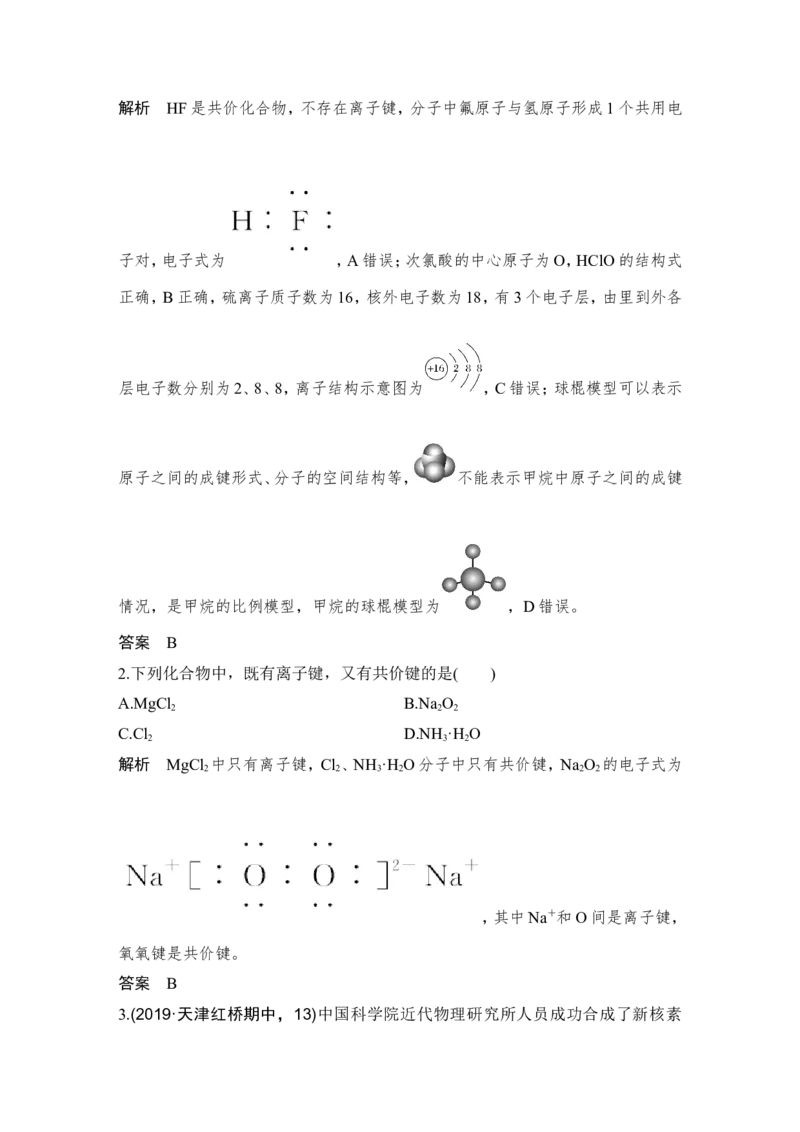
2.下列化合物中,既有离子键,又有共价键的是( )
A.MgCl B.Na O
2 2 2
C.Cl D.NH ·H O
2 3 2
解析 MgCl 中只有离子键,Cl 、NH ·H O分子中只有共价键,Na O 的电子式为
2 2 3 2 2 2
,其中Na+和O间是离子键,
氧氧键是共价键。
答案 B
3.(2019·天津红桥期中,13)中国科学院近代物理研究所人员成功合成了新核素2Ac,主要用于宇航飞行器的热源。205Ac可由207Ac转化而成,下列有关205Ac、207Ac
的说法中正确的是( )
A.核外电子数分别为116、118
B.205Ac、207Ac化学性质相同
C.205Ac、207Ac在周期表中的位置不同
D.物质的量相等的205Ac、207Ac质量相同
解析 205Ac、207Ac为同位素,核外电子都是89个,A项错误;205Ac、207Ac的核外电
子排布相同,故二者的化学性质相同,B项正确;205Ac、207Ac互为同位素,在元素
周期表中的位置相同,C项错误;205Ac、207Ac的质量数不同,其摩尔质量不同,则
相同物质的量的二者质量不同,D项错误。
答案 B
4.用N 表示阿伏加德罗常数的值,35Cl和37Cl是Cl元素的两种核素,下列说法正
A
确的是( )
A.71 g 35Cl 和71 g 37Cl 均含2N 个Cl原子
2 2 A
B.35Cl和37Cl间的相互转化是化学变化
C.35Cl和37Cl核外电子排布方式相同
D.35Cl 、H 形成的燃料电池,35Cl 在负极放电
2 2 2
解析 35Cl 和37Cl 的摩尔质量不同,A项错误。发生化学变化的最小微粒是原子,
2 2
原子的种类和数目不发生变化,而35Cl和37Cl间的相互转化是原子核内部的变化,
B项错误。35Cl和37Cl核外均为17个电子,核外电子排布方式相同,C项正确。35Cl
2
与H 反应生成H35Cl,35Cl 是氧化剂,在正极放电,D项错误。
2 2
答案 C
5.下列说法正确的是( )
A.13C和14N质子数相差1,中子数也相差1
B.一种元素可以有多种核素,有几种核素就有几种原子
C.钴Co、Co、Co、Co等几种原子,他们是同素异形体,其物理性质几乎相同,化学
性质不同
D.核聚变如H+H→He+n,由于有新粒子生成,该变化是化学变化
解析 13C和14N质子数相差1,中子数相等,均为7,A项错误;一种元素可以有多
种核素,一种核素就是一种原子,B项正确;钴Co、Co、Co、Co等几种原子,他们是同位素,C项错误;核聚变如H+H→He+n,由于原子核发生了变化,该变化属
于核反应,不是化学变化,D项错误。
答案 B
6.(2018·东北五校联考)下列说法不正确的是( )
A.干冰升华和液氯汽化时,都只需克服分子间作用力
B.N 和Cl O两种分子中,每个原子的最外层都具有8电子稳定结构
2 2
C.HF、HCl、HBr、HI的热稳定性和还原性均依次减弱
D.石墨转化为金刚石,既有化学键的断裂,又有化学键的形成
解析 干冰升华、液氯汽化,都只需克服分子间作用力,A项正确;N 的电子式为
2
∶N⋮⋮N∶,Cl O的电子式为 ,每个原子的最外层都
2
具有8电子稳定结构,B项正确;非金属性:F>Cl>Br>I,HF、HCl、HBr、HI的热稳
定性依次减弱,还原性依次增强,C项错误;石墨转化为金刚石,为化学变化,既有
化学键的断裂,又有化学键的形成,D项正确。
答案 C
7.某元素的一个原子形成的离子可表示为Xn-,下列说法正确的是( )
A.Xn-含有的中子数为a+b
B.Xn-含有的电子数为a-n
C.X原子的质量数为a+b+n
D.1个X原子的质量约为 g
解析 Xn-中a表示质子数,b表示质量数,“n-”表示X得到n个电子,则其含
有的中子数为b-a,电子数为a+n,A、B、C项错误;1 mol X的质量约为b g,则1
个X原子的质量约为 g,D项正确。
答案 D
8.“神舟六号”所用动力燃料之一为氢化锂三兄弟:LiH、LiD、LiT。其中Li的质
量数为7,有关下列叙述中正确的是( )
A.等物质的量的三种物质质子数之比为1∶2∶3B.等物质的量的三种物质中子数之比为1∶1∶1
C.等物质的量的三种物质的摩尔质量之比为8∶9∶10
D.三种物质的化学性质不相同
解析 等物质的量的三种物质质子数之比为1∶1∶1,中子数之比为4∶5∶6,质
量数之比为8∶9∶10,A、B错,C正确;化学性质与原子的核外电子排布有关,三
种物质的化学性质相同,D错。
答案 C
9.下列说法中正确的是( )
A.在化合物CaCl 中,除了有Ca2+与Cl-之间的离子键外,还有两个Cl-之间的共
2
价键
B.碘受热升华时共价键被破坏
C.熔化状态下能导电的化合物中一定存在离子键
D.离子化合物中可能含有共价键,共价化合物中可能含有离子键
解析 本题考查微粒之间的相互作用力。熔化状态下能导电的化合物是离子化合
物,C项正确。在化合物CaCl 中,两个Cl-之间无化学键,A项错误;碘受热升华
2
时分子间作用力被破坏,共价键未被破坏,B项错误;共价化合物中不可能含有离
子键,D项错误。
答案 C
10.(2018·宁夏银川一中高三考前适应性训练)下列各项表达中正确的是( )
A.用酸性KMnO 溶液可以检验绿矾(FeSO ·7H O)是否变质
4 4 2
B.非极性键只存在于双原子的单质分子(如Cl )中
2
C.在共价化合物分子内,可能存在离子键
D.在氮原子中,质子数为7而中子数不一定为7
解析 A项,绿矾变质后,仍有部分Fe2+,绿矾不变质,绿矾中也含有Fe2+,都能使
酸性高锰酸钾溶液褪色,因此不能用酸性高锰酸钾溶液检验绿矾是否变质,应用
KSCN溶液检验,如果溶液变红,说明绿矾变质,错误;B项,非极性键也可存在于
化合物中,如Na O 和H O 中,错误;C项,共价化合物中一定不含离子键,错误;
2 2 2 2
D项,氮原子中质子数为7,但中子数不一定为7,正确。
答案 D
11.现有a~h 8种短周期元素,它们在元素周期表中的位置如图,请据此回答下列问题:
(1)下列元素的原子间反应最容易形成离子键的是________(填选项字母,下同),容
易形成共价键的是________。
A.c和f B.b和h
C.d和h D.b和e
(2)下列由 a~h 形成的各分子中所有原子都满足最外层为 8 电子结构的是
________(双选)。
A.ea B.ah
3
C.fh D.dh
3 4
(3)均由a、b、g和氧四种元素形成的两种离子化合物,相互反应可生成有刺激性气
味的气体。这两种化合物中有一种相对分子质量为120,该化合物熔化时破坏的是
________(填化学键类型,下同),溶于水时破坏的是________。
解析 由元素在周期表中的位置可推知:a为H,b为Na,c为Mg,d为C,e为N,f
为P,g为S,h为Cl。
(1)非金属性最强的Cl和金属性最强的Na最易形成离子键,故选B项。非金属元
素间易形成共价键,而四个组合中只有碳、氯都为非金属元素,故选C项。
(2)写出各选项所对应的分子,其中NH 和HCl中的氢不是8电子结构,只有C、D
3
项符合题意。
(3)均由 H、Na、S、O四种元素构成的能相互反应的离子化合物是 NaHSO 和
3
NaHSO ,其中相对分子质量为120的为NaHSO ,熔化时破坏的是离子键,电离方
4 4
程式为 NaHSO ===Na++HSO;溶于水时破坏的是离子键和共价键:
4
NaHSO ===Na++H++SO。
4
答案 (1)B C (2)CD
(3)离子键 离子键和共价键
12.(2018·河北邢台质量检测,10)硒的原子序数为34,与硫处于同一主族,硒的单
质及其化合物用途非常广泛。
(1)硫的原子结构示意图为________。
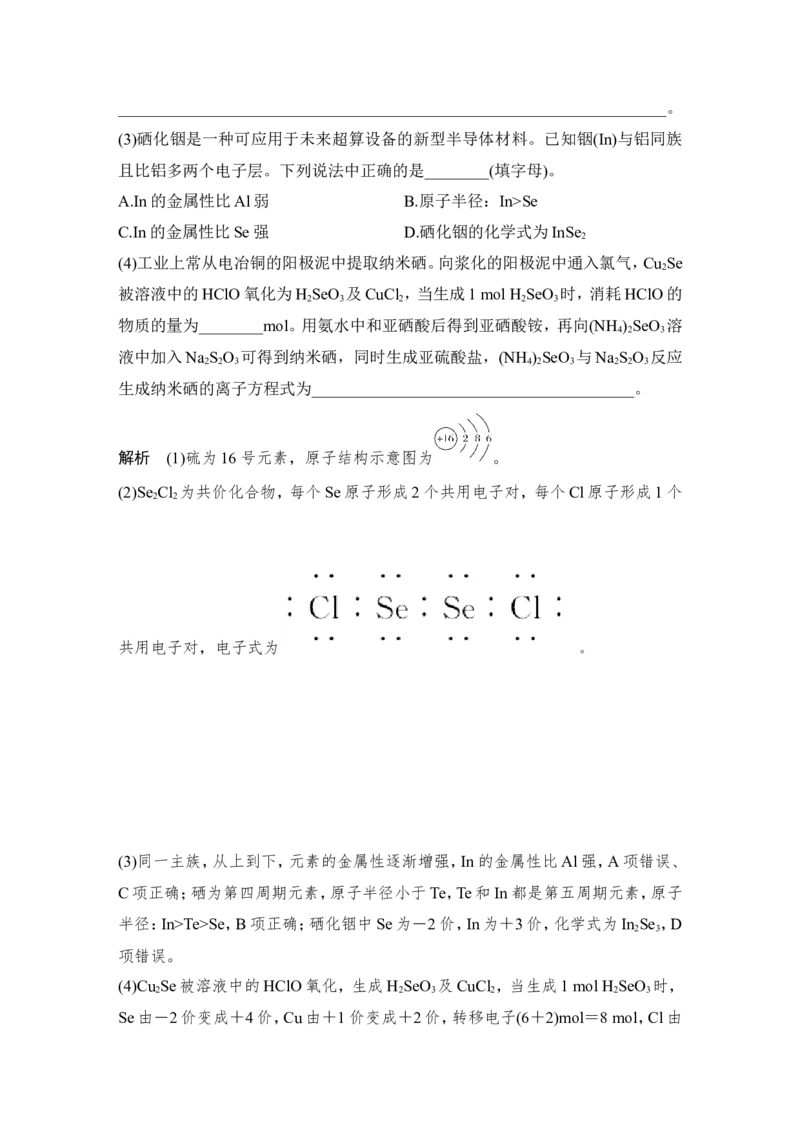
(2)Se Cl 常 用 作 分 析 试 剂 , 其 电 子 式 为
2 2____________________________________________________________________。
(3)硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族
且比铝多两个电子层。下列说法中正确的是________(填字母)。
A.In的金属性比Al弱 B.原子半径:In>Se
C.In的金属性比Se强 D.硒化铟的化学式为InSe
2
(4)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu Se
2
被溶液中的HClO氧化为H SeO 及CuCl ,当生成1 mol H SeO 时,消耗HClO的
2 3 2 2 3
物质的量为________mol。用氨水中和亚硒酸后得到亚硒酸铵,再向(NH ) SeO 溶
4 2 3
液中加入Na S O 可得到纳米硒,同时生成亚硫酸盐,(NH ) SeO 与Na S O 反应
2 2 3 4 2 3 2 2 3
生成纳米硒的离子方程式为________________________________________。
解析 (1)硫为16号元素,原子结构示意图为 。
(2)Se Cl 为共价化合物,每个Se原子形成2个共用电子对,每个Cl原子形成1个
2 2
共用电子对,电子式为 。
(3)同一主族,从上到下,元素的金属性逐渐增强,In的金属性比Al强,A项错误、
C项正确;硒为第四周期元素,原子半径小于Te,Te和In都是第五周期元素,原子
半径:In>Te>Se,B项正确;硒化铟中Se为-2价,In为+3价,化学式为In Se ,D
2 3
项错误。
(4)Cu Se被溶液中的HClO氧化,生成H SeO 及CuCl ,当生成1 mol H SeO 时,
2 2 3 2 2 3
Se由-2价变成+4价,Cu由+1价变成+2价,转移电子(6+2)mol=8 mol,Cl由+1价变为-1价,因此消耗HClO的物质的量为4 mol。(NH ) SeO 与Na S O 反
4 2 3 2 2 3
应生成纳米硒的离子方程式为SeO+S O===Se↓+2SO。
2
答案 (1) (2)
(3)BC (4)4 SeO+S O===Se↓+2SO
2
[B级 拔高选做题]
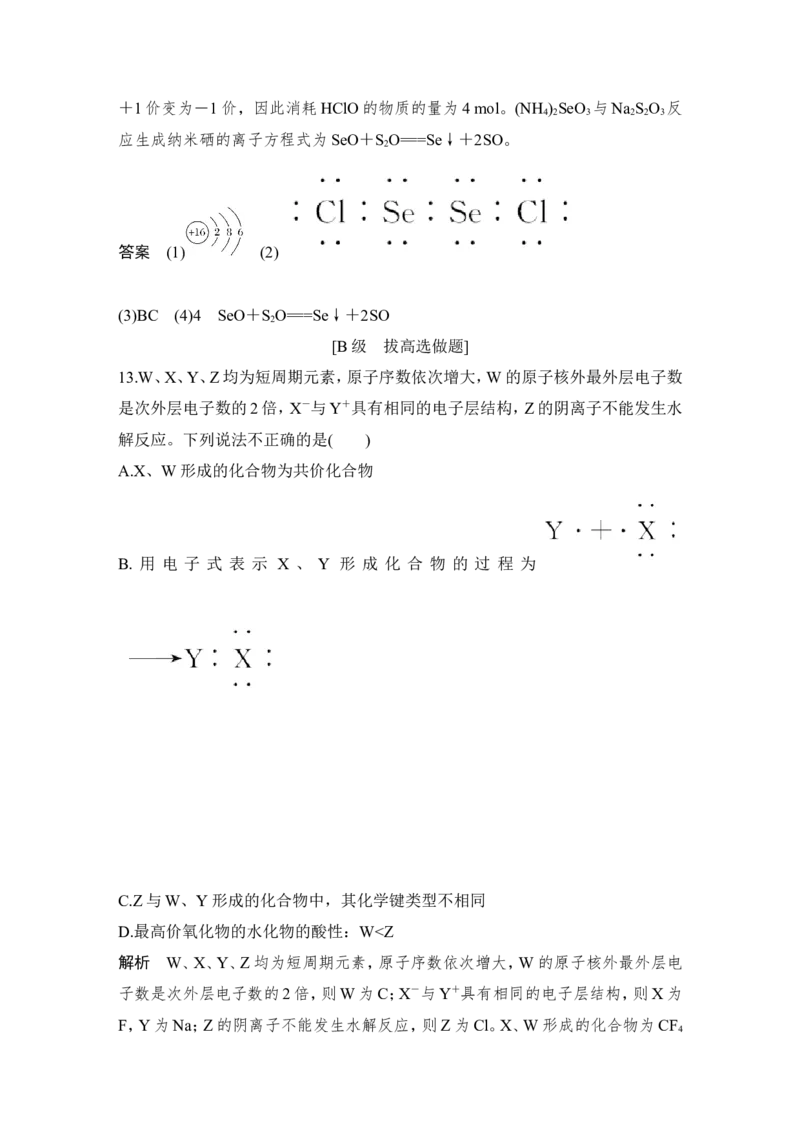
13.W、X、Y、Z均为短周期元素,原子序数依次增大,W的原子核外最外层电子数
是次外层电子数的2倍,X-与Y+具有相同的电子层结构,Z的阴离子不能发生水
解反应。下列说法不正确的是( )
A.X、W形成的化合物为共价化合物
B. 用 电 子 式 表 示 X 、 Y 形 成 化 合 物 的 过 程 为
C.Z与W、Y形成的化合物中,其化学键类型不相同
D.最高价氧化物的水化物的酸性:WP,故最高价氧化物对
3 2 2
应水化物的酸性:HClO >H PO 。
4 3 4
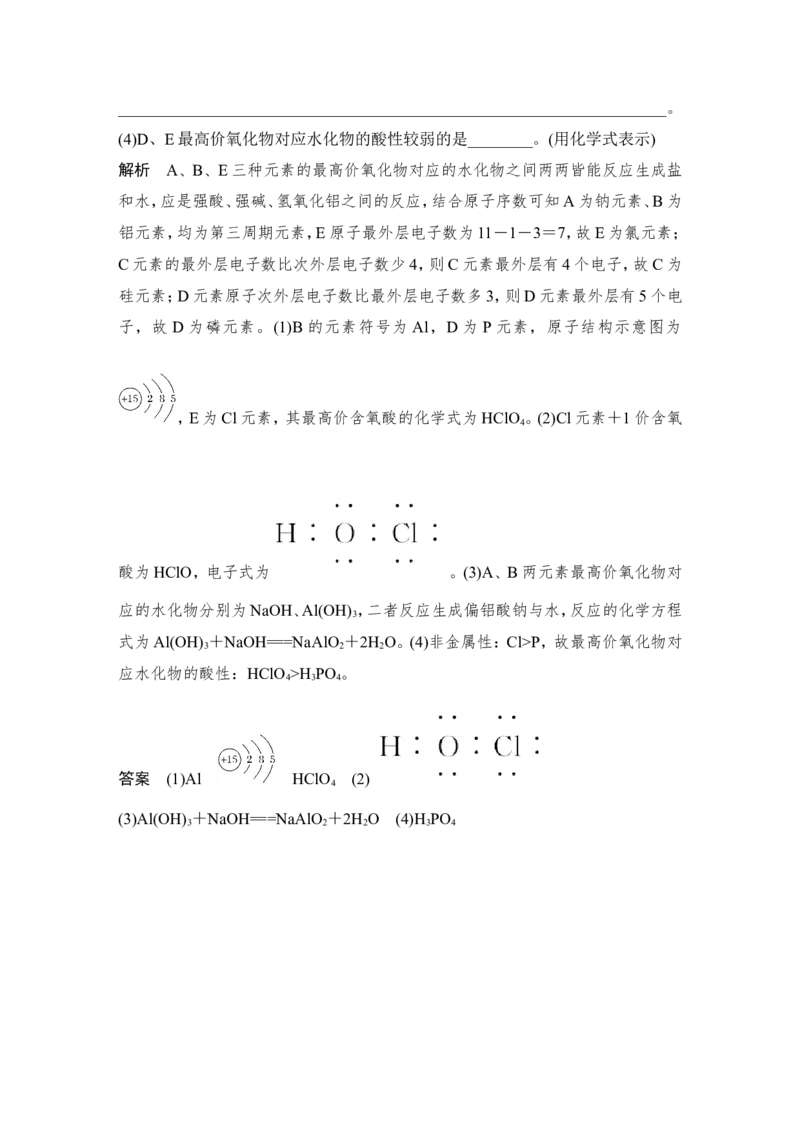
答案 (1)Al HClO (2)
4
(3)Al(OH) +NaOH===NaAlO +2H O (4)H PO
3 2 2 3 4