文档内容
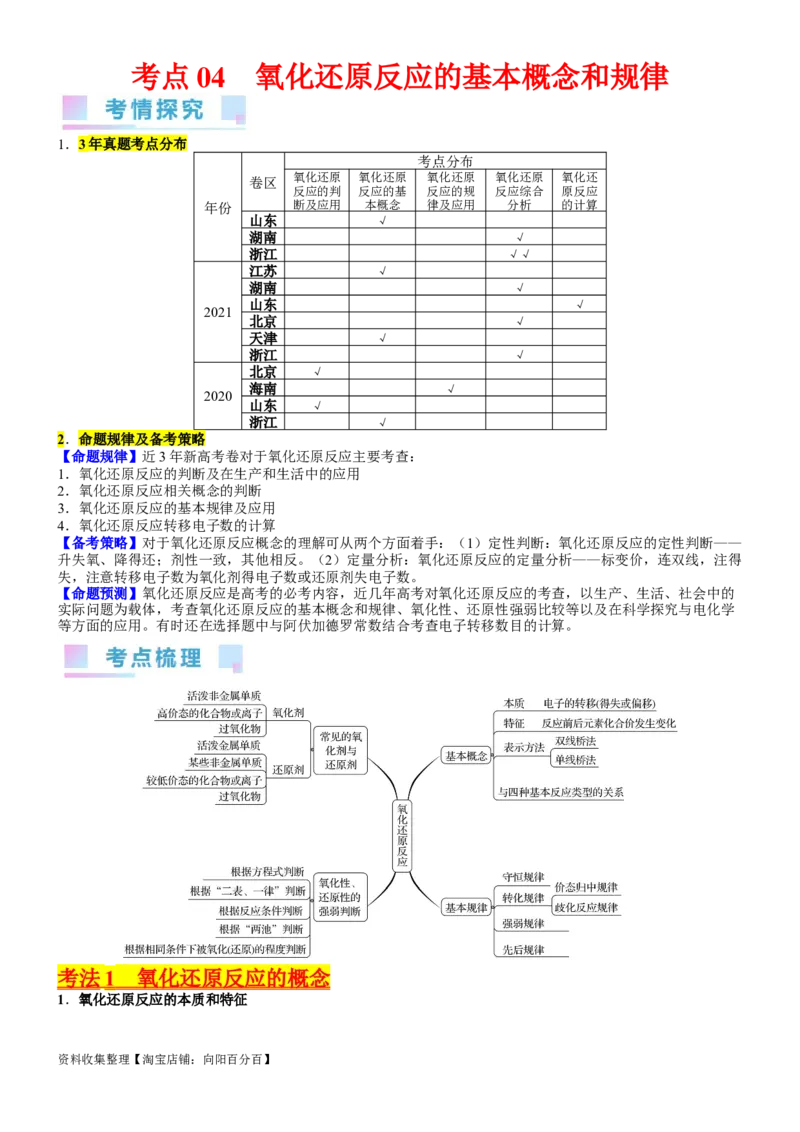
考点 04 氧化还原反应的基本概念和规律
1.3年真题考点分布
考点分布
氧化还原 氧化还原 氧化还原 氧化还原 氧化还
卷区
反应的判 反应的基 反应的规 反应综合 原反应
年份 断及应用 本概念 律及应用 分析 的计算
山东 √
湖南 √
浙江 √√
江苏 √
湖南 √
山东 √
2021
北京 √
天津 √
浙江 √
北京 √
海南 √
2020
山东 √
浙江 √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于氧化还原反应主要考查:
1.氧化还原反应的判断及在生产和生活中的应用
2.氧化还原反应相关概念的判断
3.氧化还原反应的基本规律及应用
4.氧化还原反应转移电子数的计算
【备考策略】对于氧化还原反应概念的理解可从两个方面着手:(1)定性判断:氧化还原反应的定性判断——
升失氧、降得还;剂性一致,其他相反。(2)定量分析:氧化还原反应的定量分析——标变价,连双线,注得
失,注意转移电子数为氧化剂得电子数或还原剂失电子数。
【命题预测】氧化还原反应是高考的必考内容,近几年高考对氧化还原反应的考查,以生产、生活、社会中的
实际问题为载体,考查氧化还原反应的基本概念和规律、氧化性、还原性强弱比较等以及在科学探究与电化学
等方面的应用。有时还在选择题中与阿伏加德罗常数结合考查电子转移数目的计算。
考法 1 氧化还原反应的概念
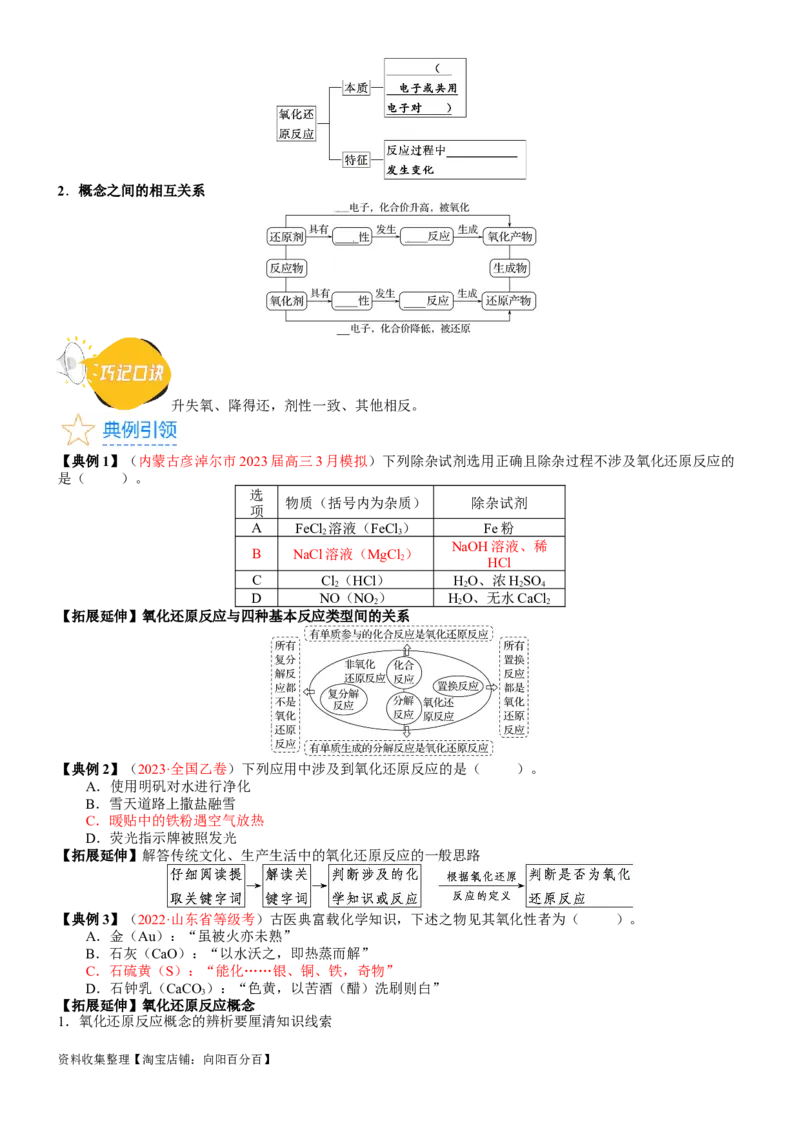
1.氧化还原反应的本质和特征
资料收集整理【淘宝店铺:向阳百分百】2.概念之间的相互关系
升失氧、降得还,剂性一致、其他相反。
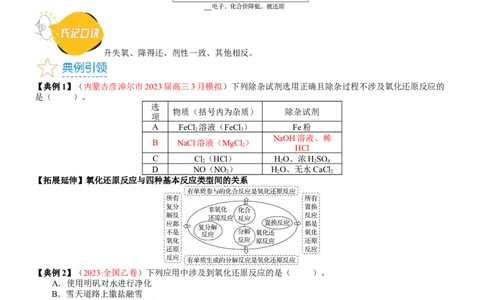
【典例1】(内蒙古彦淖尔市2023届高三3月模拟)下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的
是( )。
选
物质(括号内为杂质) 除杂试剂
项
A FeCl 溶液(FeCl ) Fe粉
2 3
NaOH溶液、稀
B NaCl溶液(MgCl )
2 HCl
C Cl(HCl) HO、浓HSO
2 2 2 4
D NO(NO ) HO、无水CaCl
2 2 2
【拓展延伸】氧化还原反应与四种基本反应类型间的关系
【典例2】(2023·全国乙卷)下列应用中涉及到氧化还原反应的是( )。
A.使用明矾对水进行净化
B.雪天道路上撒盐融雪
C.暖贴中的铁粉遇空气放热
D.荧光指示牌被照发光
【拓展延伸】解答传统文化、生产生活中的氧化还原反应的一般思路
【典例3】(2022·山东省等级考)古医典富载化学知识,下述之物见其氧化性者为( )。
A.金(Au):“虽被火亦未熟”
B.石灰(CaO):“以水沃之,即热蒸而解”
C.石硫黄(S):“能化……银、铜、铁,奇物”
D.石钟乳(CaCO ):“色黄,以苦酒(醋)洗刷则白”
3
【拓展延伸】氧化还原反应概念
1.氧化还原反应概念的辨析要厘清知识线索
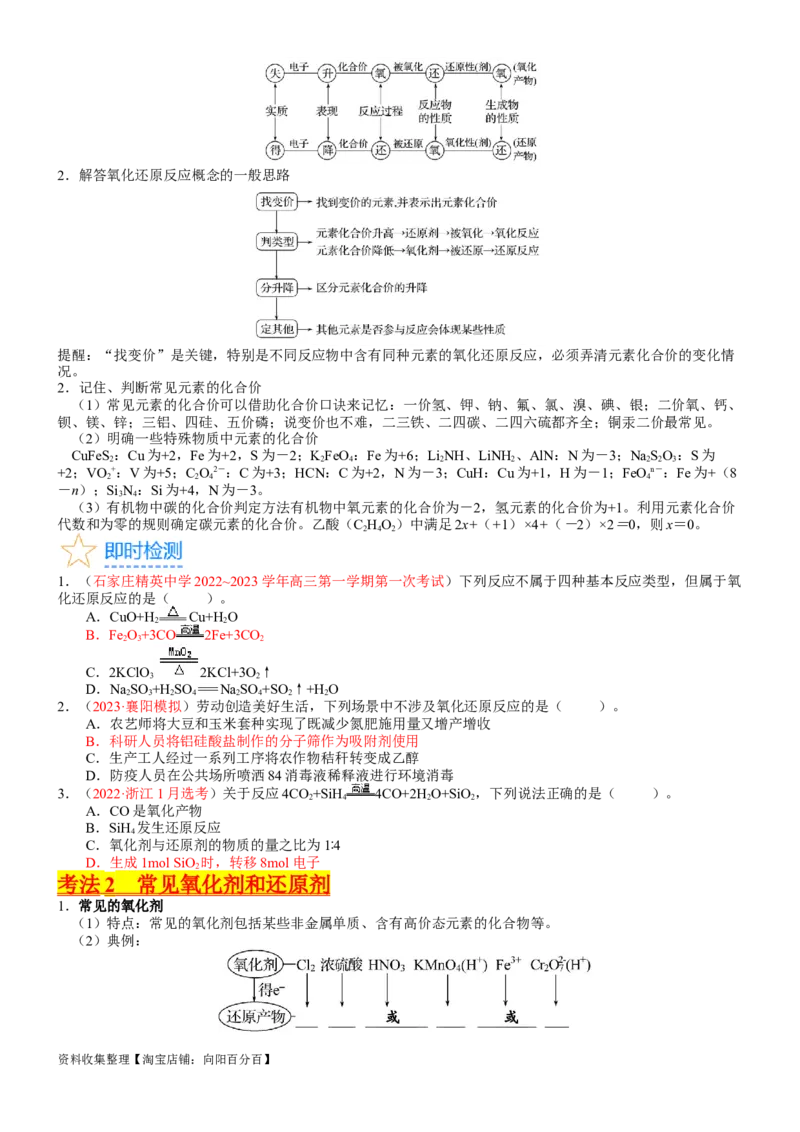
资料收集整理【淘宝店铺:向阳百分百】2.解答氧化还原反应概念的一般思路
提醒:“找变价”是关键,特别是不同反应物中含有同种元素的氧化还原反应,必须弄清元素化合价的变化情
况。
2.记住、判断常见元素的化合价
(1)常见元素的化合价可以借助化合价口诀来记忆:一价氢、钾、钠、氟、氯、溴、碘、银;二价氧、钙、
钡、镁、锌;三铝、四硅、五价磷;说变价也不难,二三铁、二四碳、二四六硫都齐全;铜汞二价最常见。
(2)明确一些特殊物质中元素的化合价
CuFeS:Cu为+2,Fe为+2,S为-2;KFeO:Fe为+6;LiNH、LiNH、AlN:N为-3;NaSO:S为
2 2 4 2 2 2 2 3
+2;VO +:V为+5;C O2-:C为+3;HCN:C为+2,N为-3;CuH:Cu为+1,H为-1;FeOn-:Fe为+(8
2 2 4 4
-n);Si N:Si为+4,N为-3。
3 4
(3)有机物中碳的化合价判定方法有机物中氧元素的化合价为-2,氢元素的化合价为+1。利用元素化合价
代数和为零的规则确定碳元素的化合价。乙酸(C HO)中满足2x+(+1)×4+(-2)×2=0,则x=0。
2 4 2
1.(石家庄精英中学2022~2023学年高三第一学期第一次考试)下列反应不属于四种基本反应类型,但属于氧
化还原反应的是( )。
A.CuO+H Cu+H O
2 2
B.Fe O+3CO 2Fe+3CO
2 3 2
C.2KClO 2KCl+3O ↑
3 2
D.NaSO +H SO NaSO +SO↑+H O
2 3 2 4 2 4 2 2
2.(2023·襄阳模拟)劳动创造美好生活,下列场景中不涉及氧化还原反应的是( )。
A.农艺师将大豆和玉米套种实现了既减少氮肥施用量又增产增收
B.科研人员将铝硅酸盐制作的分子筛作为吸附剂使用
C.生产工人经过一系列工序将农作物秸秆转变成乙醇
D.防疫人员在公共场所喷洒84消毒液稀释液进行环境消毒
3.(2022·浙江1月选考)关于反应4CO+SiH 4CO+2HO+SiO,下列说法正确的是( )。
2 4 2 2
A.CO是氧化产物
B.SiH 发生还原反应
4
C.氧化剂与还原剂的物质的量之比为1∶4
D.生成1mol SiO 时,转移8mol电子
2
考法 2 常见氧化剂和还原剂
1.常见的氧化剂
(1)特点:常见的氧化剂包括某些非金属单质、含有高价态元素的化合物等。
(2)典例:
资料收集整理【淘宝店铺:向阳百分百】2.常见的还原剂
(1)特点:活泼的金属单质、非金属阴离子及含低价态元素的化合物、低价金属阳离子、某些非金属单质及
其氢化物等。
(2)典例:
3.元素化合价处于中间价态的物质既有氧化性,又有还原性。如
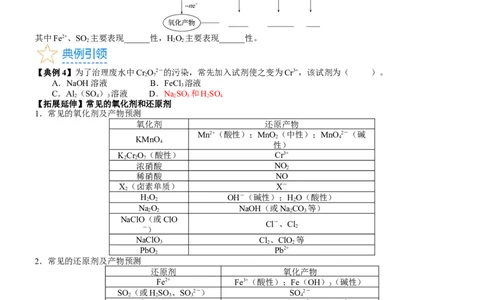
其中Fe2+、SO 主要表现______性,HO 主要表现______性。
2 2 2
【典例4】为了治理废水中Cr O2-的污染,常先加入试剂使之变为Cr3+,该试剂为( )。
2 7
A.NaOH溶液 B.FeCl 溶液
3
C.Al (SO ) 溶液 D.NaSO 和HSO
2 4 3 2 3 2 4
【拓展延伸】常见的氧化剂和还原剂
1.常见的氧化剂及产物预测
氧化剂 还原产物
Mn2+(酸性);MnO (中性);MnO 2-(碱
KMnO 2 4
4 性)
KCr O(酸性) Cr3+
2 2 7
浓硝酸 NO
2
稀硝酸 NO
X(卤素单质) X-
2
HO OH-(碱性);HO(酸性)
2 2 2
NaO NaOH(或NaCO 等)
2 2 2 3
NaClO(或ClO
Cl-、Cl
-) 2
NaClO Cl、ClO 等
3 2 2
PbO Pb2+
2
2.常见的还原剂及产物预测
还原剂 氧化产物
Fe2+ Fe3+(酸性);Fe(OH)(碱性)
3
SO (或HSO 、SO 2-) SO 2-
2 2 3 3 4
S2-(或HS) S、SO (或SO 2-)、SO 2-
2 2 3 4
HC O CO(酸性);CO2-(碱性)
2 2 4 2 3
HO O
2 2 2
I-(或HI) I、IO -
2 3
CO CO(酸性);CO2-(碱性)
2 3
Zn2+、Fe2+(与强氧化剂反应生成Fe3+)
金属单质(Zn、Fe、Cu等)
Cu2+(与弱氧化剂反应生成Cu+)
1.随着人们生活节奏的加快,方便的小包装食品已被广泛接受.为了防止仲秋月饼等富脂食品氧化变质,延长
食品的保质期,在包装袋中常加入抗氧化物质,下列不属于抗氧化物质的是( )。
A.生石灰 B.还原铁粉 C.亚硫酸钠 D.维生素C
2.以KI为碘剂的加碘食盐,由于受空气作用,容易引起碘的损失,工业生产中需添加稳定剂以减少碘的损失。
资料收集整理【淘宝店铺:向阳百分百】下列物质中可能做稳定剂的是( )。
A.NaSO B.FeCl C.NaHCO D.CaO
2 2 3 3 3
3.下列物质属于常见氧化剂的一组是( )。
A.Cl、O、FeCl 、KMnO
2 2 3 4
B.O、KMnO 、C、H
2 4 2
C.Na、K、FeCl 、H、CO
2 2
D.CuO、CO、Fe O、H
2 3 2
考法 3 氧化还原反应的表示方法
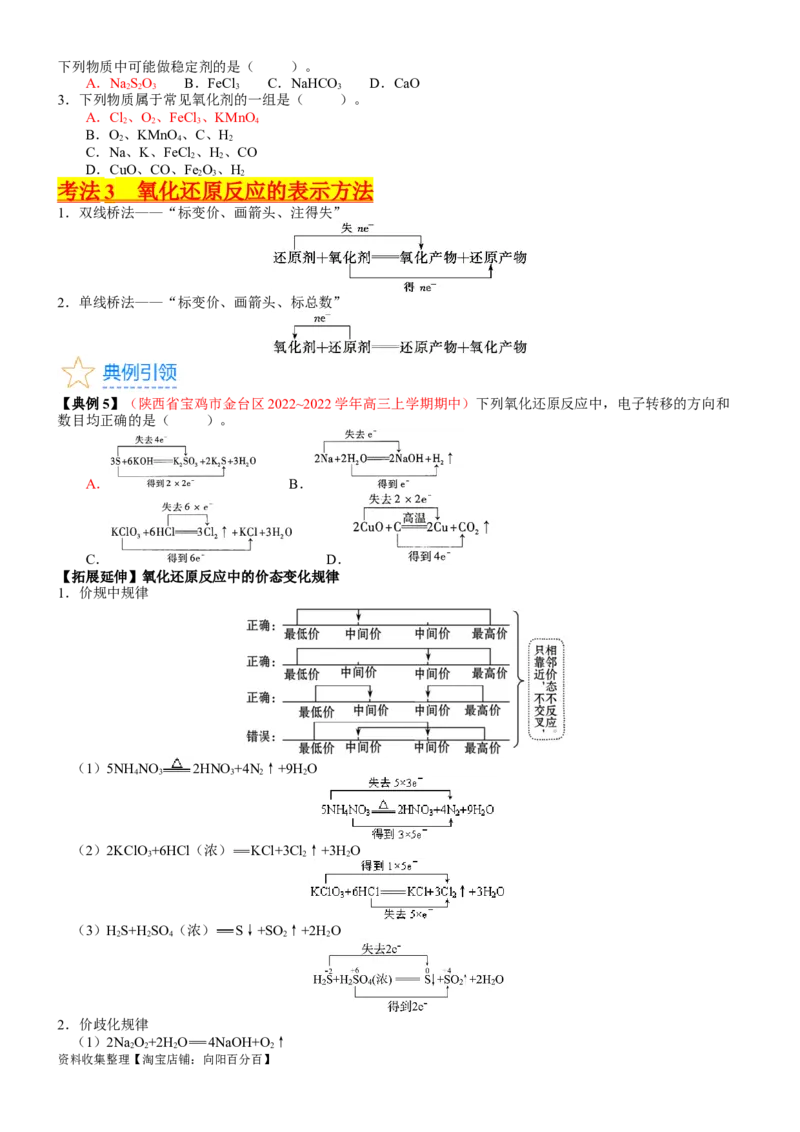
1.双线桥法——“标变价、画箭头、注得失”
2.单线桥法——“标变价、画箭头、标总数”
【典例5】(陕西省宝鸡市金台区2022~2022学年高三上学期期中)下列氧化还原反应中,电子转移的方向和
数目均正确的是( )。
A. B.
C. D.
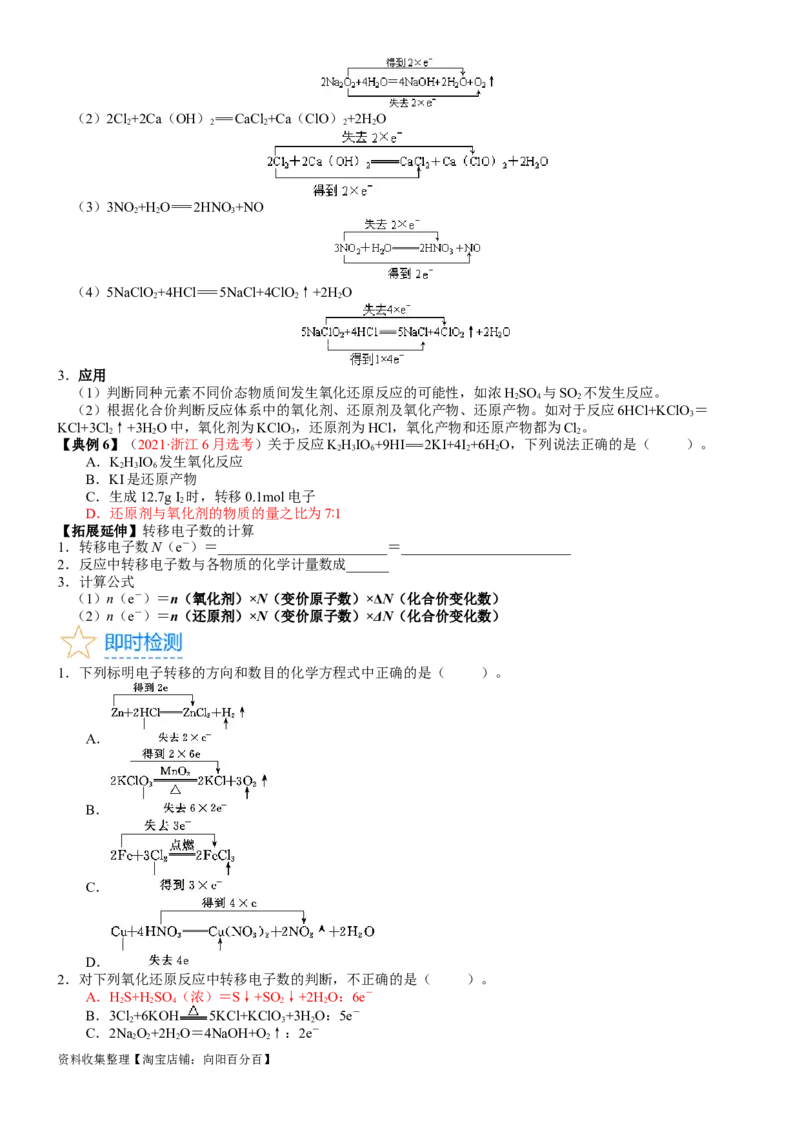
【拓展延伸】氧化还原反应中的价态变化规律
1.价规中规律
(1)5NH NO 2HNO+4N ↑+9H O
4 3 3 2 2
(2)2KClO+6HCl(浓) KCl+3Cl↑+3HO
3 2 2
(3)HS+HSO (浓) S↓+SO↑+2H O
2 2 4 2 2
2.价歧化规律
(1)2NaO+2H O 4NaOH+O ↑
2 2 2 2
资料收集整理【淘宝店铺:向阳百分百】(2)2Cl+2Ca(OH) CaCl +Ca(ClO)+2HO
2 2 2 2 2
(3)3NO +HO 2HNO+NO
2 2 3
(4)5NaClO+4HCl 5NaCl+4ClO ↑+2HO
2 2 2
3.应用
(1)判断同种元素不同价态物质间发生氧化还原反应的可能性,如浓HSO 与SO 不发生反应。
2 4 2
(2)根据化合价判断反应体系中的氧化剂、还原剂及氧化产物、还原产物。如对于反应6HCl+KClO =
3
KCl+3Cl ↑+3H O中,氧化剂为KClO,还原剂为HCl,氧化产物和还原产物都为Cl。
2 2 3 2
【典例6】(2021·浙江6月选考)关于反应KHIO +9HI 2KI+4I+6H O,下列说法正确的是( )。
2 3 6 2 2
A.KHIO 发生氧化反应
2 3 6
B.KI是还原产物
C.生成12.7g I 时,转移0.1mol电子
2
D.还原剂与氧化剂的物质的量之比为7∶1
【拓展延伸】转移电子数的计算
1.转移电子数N(e-)=________________________=________________________
2.反应中转移电子数与各物质的化学计量数成______
3.计算公式
(1)n(e-)=n(氧化剂)×N(变价原子数)×ΔN(化合价变化数)
(2)n(e-)=n(还原剂)×N(变价原子数)×ΔN(化合价变化数)
1.下列标明电子转移的方向和数目的化学方程式中正确的是( )。
A.
B.
C.
D.
2.对下列氧化还原反应中转移电子数的判断,不正确的是( )。
A.HS+HSO (浓)=S↓+SO↓+2H O:6e-
2 2 4 2 2
B.3Cl+6KOH 5KCl+KClO +3H O:5e-
2 3 2
C.2NaO+2H O=4NaOH+O ↑:2e-
2 2 2 2
资料收集整理【淘宝店铺:向阳百分百】D.2HS+SO=3S+2HO:4e-
2 2 2
3.工业生产中对空气中的CO进行监测,粉红色的PdCl 溶液可以检验空气中少量的CO。若空气中含CO,则
2
溶液中会产生黑色的Pd沉淀(反应中只有PdCl 作氧化剂)。每生成5.3gPd沉淀,反应转移的电子数为(
2
)。
A.0.05N B.0.1N C.0.2N D.0.4N
A A A A
4.(2023•上海杨浦区一模)N 代表阿伏加德罗常数。常温常压下二氧化碳和过氧化钠反应后,若固体质量增
A
加了28g,对该反应的分析,错误的是( )。
A.反应前后物质中阴、阳离子数目保持不变
B.反应前后总物质的量减少0.5mol
C.反应中转移了N 电子并生成了11.2L氧气
A
D.反应的二氧化碳和生成的氧气体积比为2∶1
考法 4 氧化 性、 还原 性
1.氧化性、还原性强弱规律
(1)氧化性、还原性的概念
①氧化性:指得电子的性质(或能力);还原性:指失电子的性质(或能力)。
②氧化性、还原性的强弱取决于得、失电子的难易程度,与得、失电子数目的多少无关。
(2)从元素的价态和氧化性、还原性的关系
①最高价态——只有氧化性,如:HSO 、KMnO 等;
2 4 4
②最低价态——只有还原性,如:金属单质、Cl-、S2-等;
③中间价态——既有氧化性又有还原性,如:Fe2+、S、Cl 等。
2
(3)依据氧化还原反应方程式判断
①氧化性:氧化剂>氧化产物
②还原性:还原剂>还原产物
2.价态规律:含不同价态的同种元素的物质间发生氧化还原反应时。该元素价态的变化
(1)遵循“高价+低价→中间价”,如4NH +6NO 5N+6H O
3 2 2
(2)遵循“中间价→高价+低价”,如Cl+2NaOH NaCl+NaClO+H O。
2 2
3.先后规律
(1)同时含有几种还原剂时 将按照还原性由强到弱的顺序依次反应。如:在FeBr 溶液中通入少
2
量Cl 时,因为还原性Fe2+>Br-,所以Fe2+先与Cl 反应。
2 2
(2)同时含有几种氧化剂时 将按照氧化性由强到弱的顺序依次反应。如:在含有Fe3+、Cu2+、
H+的溶液中加入铁粉,因为氧化性Fe3+>Cu2+>H+,所以铁粉先与Fe3+反应,然后依次为Cu2+、H+。
4.电子守恒规律:即氧化剂得电子的总数等于还原剂失电子的总数
【典例7】(2021·天津等级考)关于反应HSO +Na SO NaSO +SO↑+H O所涉及的物质,下列说法错误的
2 4 2 3 2 4 2 2
是( )。
A.HSO 在该反应中为氧化剂
2 4
B.NaSO 容易被空气中的O 氧化变质
2 3 2
C.NaSO 是含有共价键的离子化合物
2 4
D.SO 是导致酸雨的主要有害污染物
2
【拓展延伸】化合价和氧化性、还原性的关系
①金属单质只有还原性
②非金属单质既有氧化性又有还原性,F 除外
2
③从理论上讲任何一种化合物既有氧化性又有还原性
资料收集整理【淘宝店铺:向阳百分百】(2)常见元素的最高价态和最低价态
元素 Cl S N C H
最高
+7 +6 +5 +4 +1
价
最低
- 1 - 2 - 3 - 4 - 1
价
1.下列说法错误的是( )。
A.某金属元素从化合态变为游离态时,该金属元素一定被还原
B.有单质参加或有单质生成的反应一定是氧化还原反应
C.高效火箭推进剂N(NO ) 既有氧化性又有还原性
2 3
D.磁性材料Fe(FeO) 既有氧化性又有还原性
2 2
2.(2023·咸阳高三上学期期中)在下列变化中,一定要加入合适的氧化剂才能实现的是( )。
A.NaO→O B.Cl→Cl-
2 2 2 2
C.Fe(OH)→Fe(OH) D.NO →HNO
2 3 2 3
【典例8】(2020·北京市等级考)水与下列物质反应时,水表现出氧化性的是( )。
A.Na B.Cl C.NO D.NaO
2 2 2
【拓展延伸】氧化还原反应中某微粒的作用
1.氧化还原反应中酸或碱的作用
(1)氧化性:所含元素的化合价降低
(2)还原性:所含元素的化合价升高
(3)酸或碱性:所含元素的化合价不变,有相应的盐生成
(4)具体反应分析
①Zn+2HCl ZnCl+H ↑,盐酸表现酸性和氧化性
2 2
②CuO+2HCl CuCl +H O,盐酸表现酸性
2 2
③MnO +4HCl(浓) MnCl+Cl↑+2H O,盐酸表现酸性和还原性
2 2 2 2
④2HCl H↑+Cl↑,盐酸表现氧化性和还原性
2 2
⑤3Cl+8NH N+6NH Cl,NH 表现碱性和还原性
2 3 2 4 3
⑥Cu O+6HNO(浓) 2Cu(NO )+2NO ↑+3HO,硝酸表现酸性和氧化性
2 3 3 2 2 2
2.氧化还原反应中水的作用
(1)氧化性:有H 产生
2
(2)还原性:有O 产生
2
(3)氧化性和还原性:同时有H 和 O 产生
2 2
(4)水既不表现氧化性又不表现还原性的氧化还原反应
①2NaO+2H O 4NaOH+O ↑
2 2 2 2
②Cl+H O HCl+HClO
2 2
③3NO +H O 2HNO+NO
2 2 3
1.(2023·上海青浦区一模)亚硝酸(HNO)参加反应时,既可作氧化剂,也可作还原剂。当它作还原剂时,
2
可能生成的产物是( )。
A.NH B.N C.NO D.HNO
3 2 2 3 3
2.某危险品仓库中存放有化工原料氰化钠(NaCN)。该物质有剧毒,一旦进入城市排水系统,后果不堪设想。
当仓库发生火灾爆炸事故时,工作人员一方面封堵氰化钠泄漏渠道,另一方面对已经泄漏的少量氰化钠做无害
化处理。根据NaCN的化合价,推测它可能有的性质是( )。
A.NaCN中N元素的化合价为+3价既能升高又能降低,因此该物质既有氧化性又有还原性
B.NaCN中N元素的化合价为-3价只能升高,因此该物质具有还原性;C元素的化合价为+2价既能升高
又能降低,因此该物质既有氧化性又有还原性
C.NaCN中C元素的化合价为+4价既能升高又能降低,因此该物质既有氧化性又有还原性
D.NaCN中CN-的化合价为-1价既能升高又能降低,因此该物质既有氧化性又有还原性
3.针对以下A~D四个涉及HO 的反应(未配平),填写空白:
2 2
A.NaO +HCl→NaCl+H O
2 2 2 2
B.Ag O+HO→Ag+O↑+H O
2 2 2 2 2
C.HO→HO+O↑
2 2 2 2
D.HO+Cr (SO )+KOH→KCrO+K SO +H O
2 2 2 4 3 2 4 2 4 2
(1)仅体现HO 的氧化性的反应是(填代号)_________,配平化学该方程式___________________________。
2 2
资料收集整理【淘宝店铺:向阳百分百】