文档内容
★秘密·2022年9月29日10:00前
重庆市 2022-2023 学年(上)9 月月度质量检测
高三化学
2022.09
【命题单位:重庆缙云教育联盟】
注意事项:
1.答题前,考生务必用黑色签字笔将自己的姓名、准考证号、座位号在答题卡上填写清楚;
2.每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,在试卷上作答无效;
3.考试结束后,请将本试卷和答题卡一并交回;
4.全卷共8页,满分100分,考试时间75分钟。
一、选择题(共14小题,每题3分,共42分)
1.下列说法不正确的是
A.“可燃冰”的主要成分是甲烷水合物 B.煤的液化是物理变化
C.聚四氟乙烯可制成化工行业使用的耐腐蚀制品 D.硫化后的橡胶可用于制造轮胎
2.下列叙述正确的是
A. 的结构示意图为 B. 的电子式为
C.硫离子的电子式为 D. 的电子式为
3.常温下,在溶液中可发生如下反应:① ;② 。下列说法正确的是
A.反应①中 作为还原剂 B.Z元素在反应②中被氧化
C.还原性由强到弱的顺序是 D.反应 可以进行
4.某烃的结构简式为 ,有关它的分析正确的是
A.分子式为 B.一氯代物有8种
C.能发生取代、氧化、加聚反应 D.最多有7个碳原子在一条直线上
5.下列说法不正确的是A.用pH试纸测溶液的pH和用红色石蕊试纸检测气体时均不需要润湿
B.液溴保存时常加少量的水液封
C.可用分液漏斗分离乙酸乙酯和饱和碳酸钠溶液
D.NaBr溶液中加少量新制的氯水,再加少量CCl 充分振荡后静置,下层为橙红色
4
6.我国科研人员研究了在Cu-ZnO-ZrO 催化剂上CO 加氢
2 2
制甲醇过程中水的作用机理,其主反应历程如图所示下列
说法错误的是
A.二氧化碳加氢制甲醇的过程中原子利用率达100%
B.带*标记的物质是该反应历程中的中间产物
C.向该反应体系中加入少量的水能增加甲醇的产率
D.第③步的反应式为*H CO+H O →CH OH+*HO
3 2 3
7.已知反应S O (aq)+2I-(aq) 2SO (aq)+I (aq),若
2 2
向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列
有关该反应的说法不正确的是
①2Fe3+(aq)+2I-(aq) I (aq)+2Fe2+(aq)
2
② 2Fe2+(aq)+S O (aq) 2Fe3+(aq)+2SO (aq)
2
A.Fe2+是该反应的催化剂
B.该反应正反应活化能小于逆反应活化能
C.该反应可设计成原电池
D.加入Fe3+后降低了该反应的活化能
8.短周期主族元素 ,原子序数依次增大,原子半径 。X与Z同主族,Y与W
同主族,Y原子最外层电子数是次外层电子数的3倍。下列说法正确的是
A.Y与X形成的化合物一定只含极性键
B. 离子半径由大到小的顺序为:
C.Y和W分别形成的氢化物中,沸点较高的是W的氢化物
D.由这四种元素只能形成一种化合物
9.设 为阿伏加德罗常数的值,下列说法正确的是A. 甲醚中含有 键的数目为3
B. 的 分子中的质子数是2.8
C. 的酸性 溶液中含有的氧原子数为14
D. 的 溶液中,阴离子总数大于0.1
10.已知反应 ,反应中相关的化学键键能数据
如表所示,则1mol 中的化学键完全断裂时需要的能量为
化学键 C—H H—H C—O
键能/( ) 414 802 436 326
A.432kJ B.464kJ C.864kJ D.928kJ
11.微生物燃料电池是指在微生物的作用下将化学能转
化为电能的装置,其工作原理如图所示。下列有关微生物
电池的说法错误的是( )
A.负极反应中有CO 生成
2
B.微生物促进了反应中电子的转移
C.正极反应式为O +4e-+2H O=4OH-
2 2
D.电池总反应为C H O +6O =6CO +6H O
6 12 6 2 2 2
12.下列实验操作、现象和结论都正确的是
实验操作 现象 结论
室温下,向 溶液中滴加少量 溶液,再滴
A 溶液变蓝色 的氧化性比 的强
加几滴淀粉溶液
B 常温下将铜、铁分别加入浓硫酸中 均不溶解 常温下铜、铁均不与浓硫酸反应
上层显紫红 在 中的溶解度大于在水中
C 向 碘水中加入少量 ,振荡后静置
色 的溶解度
向浓度均为 的 、 混合溶液中 有黄色沉淀
D
生成
滴加少量 液A.A B.B C.C D.D
13.常温下,用 盐酸滴定 某弱碱
溶液,所得溶液 、 和 的物质的量分数与滴加盐酸
体积的关系如图所示。下列叙述正确的是
A. 的电离平衡常数为
B.曲线①代表 ,曲线②代表
C.b点溶液中存在
D.a、b、c三点的溶液,水的电离程度
14.废旧光盘金属层中含有Ag(其他金属微量忽略不计),从光盘中提取金属Ag的工艺流程如下。下列说法
不正确的是( )
A.“氧化”阶段会产生使带火星木条复燃的气体,则发生的反应方程式为:
B.“过滤I”得到的滤渣中含有 和其他不溶性杂质
C.过滤阶段得到的滤液中Ag元素主要以 存在
D.“还原阶段每消耗 ,理论上可得到Ag 21.6g
二、非选择题(共4小题,共58分,其中15-17题为必做题,18-19题为选做题)
15.(12分)富马酸亚铁又称反丁烯二酸亚铁,是良好的动物铁营养元素补充剂,它以富马酸、碳酸钠
和硫酸亚铁作为反应单体,先由富马酸和碳酸钠合成富马酸二钠再与硫酸亚铁反应所得,某化学兴趣小组
在实验室中模拟制备富马酸亚铁,实验流程及装置如下图:(1)仪器A的名称是_______,仪器A的作用是_______。
(2)称取 富马酸(反丁烯二酸 ,式量为116)置于右边
的三颈烧瓶中,根据计算的浓度,称取一定量的水加入三颈烧瓶中,开启
搅拌桨搅拌,并开启调温型电热套使温度达到 时,加入预先溶解好
的 溶液,在生成富马酸二钠约 后,调节 在6.8~7.0之间,继续加热升温,反应 ,
即可得到富马酸二钠溶液。写出碳酸钠与富马酸反应的化学方程式:_______;富马酸二钠溶液中离子浓
度由大到小的顺序是_______(除 )。
(3)在富马酸二钠溶液中,缓慢加入 溶液,维持温度 ,充分搅拌 ;在回流过程中一直
通入氮气的目的是_______。冷却、过滤,洗涤沉淀,然后水浴干燥,得到粗产品 。若(2)中调节的
太小,最后得到的粗产品的质量会_______(填“不变”“偏大”或“偏小”,下同),若不通氮气,最
后得到的粗产品的质量会_______。
(4)洗涤沉淀时的操作为_______。
(5)准确称取粗产品 ,加入煮沸过的 硫酸溶液 ,待样品完全溶解后,加煮沸过的冷水
配制成 溶液,取溶液 滴入3滴邻二氮菲-亚铁指示剂,立即用 硫酸高铈铵)
标准溶液进行滴定。平行3次实验,用去标准液的体积平均值 (反应方程式为
)。计算产品中富马酸亚铁(相对分子质量为170)的质量分数为_______。16.(14分)钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。
(1)CoNi Fe O (其中Co、Ni均为+2)可用作H O 分解的催化剂,具有较高的活性。
x (1-x) 2 4 2 2
①该催化剂中铁元素的化合价为______。
②图1表示两种不同方法制得的催化剂CoNi Fe O 在10℃时催化分解6%的H O 溶液的相对初始速率随x
x (1-x) 2 4 2 2
变化曲线。由图中信息可知:______________法制取得到的催化剂活性更高;Co2+、Ni2+两种离子中催化效
果更好的是______。
(2)草酸钴是制备钴的氧化物的重要原料。下图2为二水合草酸钴(CoC O ·2H O)在空气中受热的质量
2 4 2
变化曲线,曲线中300℃及以上所得固体均为钴氧化物。
①通过计算确定A点剩余固体的化学成分为________________(填化学式)。试写出B点对应的物质与O
2
在225℃~300℃发生反应的化学方程式:_________________________________________。
②取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480 mL 5 mol/L盐酸
恰好完全溶解固体,得到CoCl 溶液和4.48 L(标准状况)黄绿色气体。试确定该钴氧化物中Co、O的物
2
质的量之比为___________。
17.(17分)回答下列问题:
(1)化学反应的过程都是旧键断裂、新键形成的过程。对于反应: ,已知断开 键,
键分别需要吸收的能量是 和 ,形成 键需要放出的能量是 。
① 和 完全反应共_______(填“放出”或“吸收”)能量_______ 。
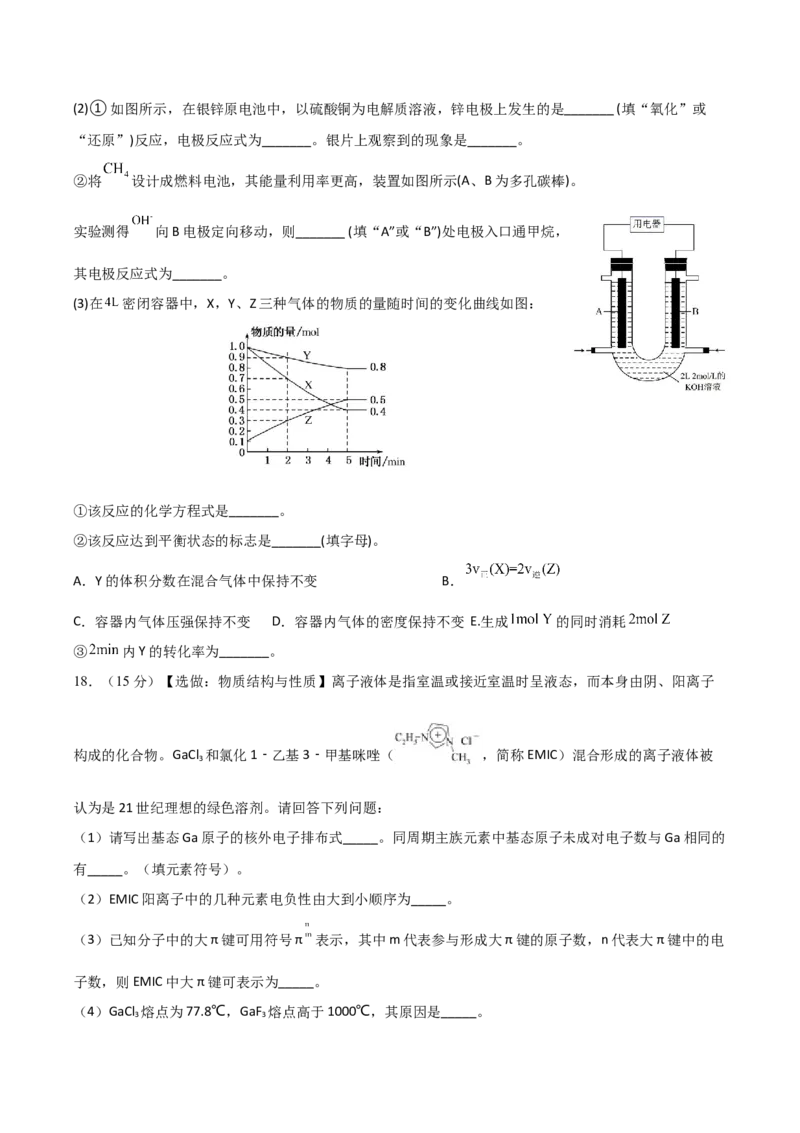
②如图,能够反映该反应能量变化的图像是_______(填“A”或“B”)。(2)①如图所示,在银锌原电池中,以硫酸铜为电解质溶液,锌电极上发生的是_______ (填“氧化”或
“还原”)反应,电极反应式为_______。银片上观察到的现象是_______。
②将 设计成燃料电池,其能量利用率更高,装置如图所示(A、B为多孔碳棒)。
实验测得 向B电极定向移动,则_______ (填“A”或“B”)处电极入口通甲烷,
其电极反应式为_______。
(3)在 密闭容器中,X,Y、Z三种气体的物质的量随时间的变化曲线如图:
①该反应的化学方程式是_______。
②该反应达到平衡状态的标志是_______(填字母)。
A.Y的体积分数在混合气体中保持不变 B.
C.容器内气体压强保持不变 D.容器内气体的密度保持不变 E.生成 的同时消耗
③ 内Y的转化率为_______。
18.(15分)【选做:物质结构与性质】离子液体是指室温或接近室温时呈液态,而本身由阴、阳离子
构成的化合物。GaCl 和氯化1﹣乙基3﹣甲基咪唑( ,简称EMIC)混合形成的离子液体被
3
认为是21世纪理想的绿色溶剂。请回答下列问题:
(1)请写出基态Ga原子的核外电子排布式_____。同周期主族元素中基态原子未成对电子数与Ga相同的
有_____。(填元素符号)。
(2)EMIC阳离子中的几种元素电负性由大到小顺序为_____。
(3)已知分子中的大π键可用符号π 表示,其中m代表参与形成大π键的原子数,n代表大π键中的电
子数,则EMIC中大π键可表示为_____。
(4)GaCl 熔点为77.8℃,GaF 熔点高于1000℃,其原因是_____。
3 3(5)GaCl 和EMIC混合形成离子液体的过程中会存在以下转变:GaCl GaCl Ga Cl 请写出
3 3 4 2 7
Ga Cl 的结构式_____。
2
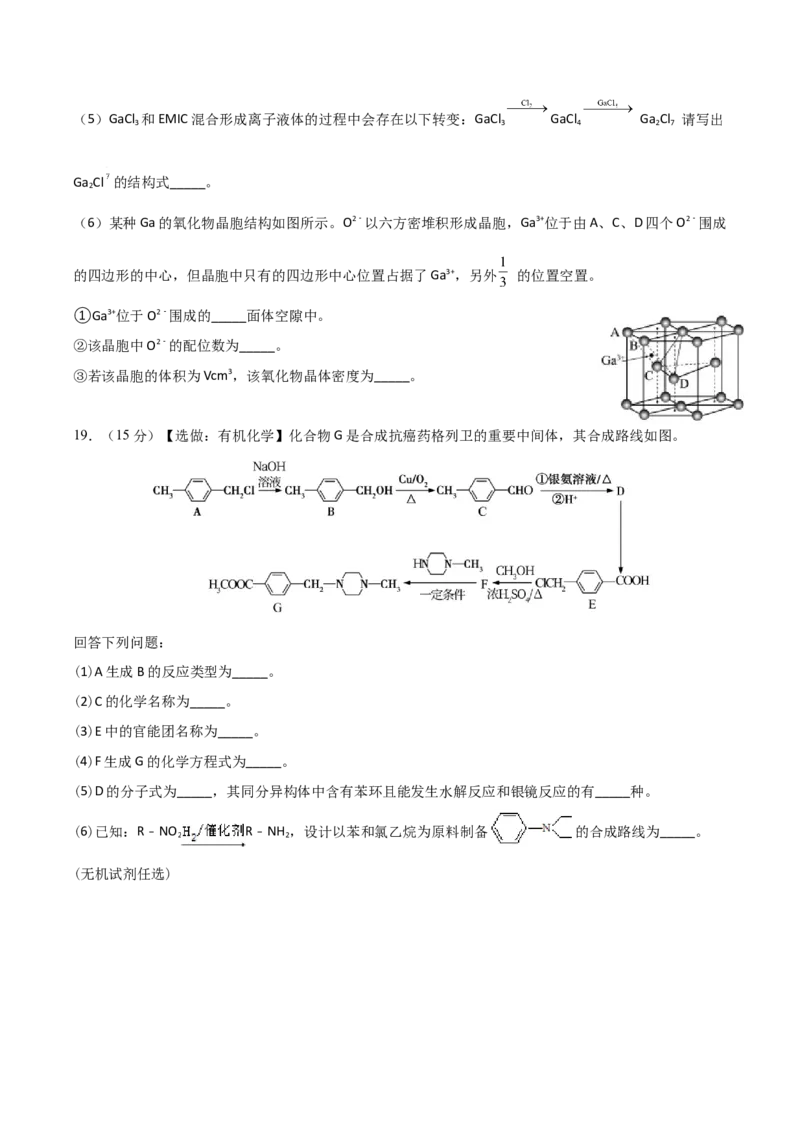
(6)某种Ga的氧化物晶胞结构如图所示。O2﹣以六方密堆积形成晶胞,Ga3+位于由A、C、D四个O2﹣围成
的四边形的中心,但晶胞中只有的四边形中心位置占据了Ga3+,另外 的位置空置。
①Ga3+位于O2﹣围成的_____面体空隙中。
②该晶胞中O2﹣的配位数为_____。
③若该晶胞的体积为Vcm3,该氧化物晶体密度为_____。
19.(15分)【选做:有机化学】化合物G是合成抗癌药格列卫的重要中间体,其合成路线如图。
回答下列问题:
(1)A生成B的反应类型为_____。
(2)C的化学名称为_____。
(3)E中的官能团名称为_____。
(4)F生成G的化学方程式为_____。
(5)D的分子式为_____,其同分异构体中含有苯环且能发生水解反应和银镜反应的有_____种。
(6)已知:R﹣NO R﹣NH ,设计以苯和氯乙烷为原料制备 的合成路线为_____。
2 2
(无机试剂任选)下载最新免费模拟卷,到公众号:一枚试卷君