文档内容
重难点 03 离子方程式的正误判断、离子共存、检验和推断
►命题趋势►解题策略►真题回眸►限时检测
考向一 离子方程式的正误判断
考向二 无限定条件的离子共存
离子方程式的正误判断、
考向三 限定条件下的离子共存
离子共存、检验和推断
考向四 离子的检验
考向五 离子的推断
离子反应是高中化学中的重要反应类型,在工农业生产与社会发展中发挥着重要作用,因此成为高考
考查的重要内容。
预计2024年高考对离子反应的考查,选择题仍主要涉及离子方程式的书写和正误判断、离子共存、离
子的检验与推断三个角度,题目考查内容主要是元素化合物的性质、化学过程的解释。
因此,要求考生对离子反应常见的错误类型进行归纳总结,注意特殊的离子反应方程式书写;对于离
子共存问题,要多关注双水解和氧化还原不共存的情况;离子的检验要多加留意试剂的添加顺序,以及杂
质离子的干扰。
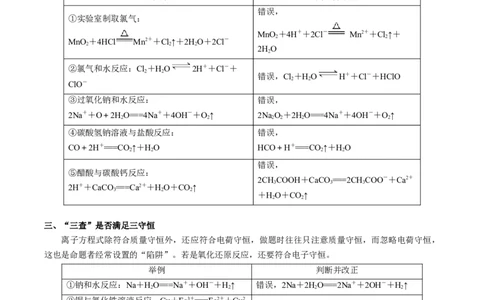
【策略1】“六查法”突破离子方程式的正误判断
一、“一查”是否符合反应事实。
看是否符合客观事实。如Fe和稀盐酸反应的离子方程式写成2Fe+6H+===2Fe3++3H↑是错误的,Fe
2
和稀盐酸反应生成Fe2+。
举例 判断并改正
①铁与稀硫酸反应:2Fe+6H+===2Fe3++3H↑ 错误,Fe+2H+===Fe2++H↑
2 2
②铜与稀硝酸反应: 错误,
Cu+4H++2NO===Cu2++2NO ↑+2HO 3Cu+8H++2NO===3Cu2++2NO↑+4HO
2 2 2
③电解饱和食盐水:2Cl-+2Na+=====2Na+Cl↑ 错误,2Cl-+2HO=====2OH-+H↑+Cl↑
2 2 2 2
错误,
④KClO碱性溶液与Fe(OH) 反应:
3
3ClO-+4OH-+2Fe(OH) ===2FeO+3Cl-+
3
3ClO-+2Fe(OH) ===2FeO+3Cl-+4H++HO
3 2
5HO
2
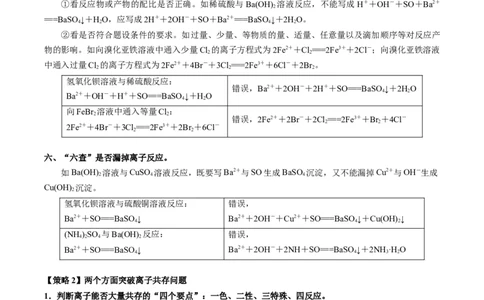
二、“二查”电解质拆分是否正确。
离子方程式的正误判断中,常常设置物质是否能“拆分”陷阱,氧化物、弱电解质、沉淀、多元弱酸
的酸式酸根(HSO除外)在离子方程式中均不能拆分。在复习时,应熟记常见的弱电解质、溶解度表及常见
多元弱酸的酸式酸根。a.弱酸的酸式酸根离子不能拆开,如HCO、HS-、HSO等;
b.强酸的酸式酸根离子(如HSO)在水溶液中写成拆分形式,如NaHSO 应写成Na+、H+和SO;而
4
NaHSO 在熔融状态下HSO不能拆开,应写成Na+和HSO。
4
c.微溶物出现在反应物中时,澄清溶液可以拆,悬浊液不可拆;微溶物出现在生成物中时当沉淀处
理,不可拆。如澄清石灰水与盐酸反应的离子方程式:H++OH-===H O;用石灰乳制漂白粉的离子方程
2
式:Ca(OH) +Cl===Ca2++Cl-+ClO-+HO。
2 2 2
d.氨水作为反应物,书写成NH ·H O;氨水作为生成物,若有加热条件或在浓溶液中生成,则书写
3 2
成NH ↑+HO,若无加热条件或在稀溶液中生成,则书写成NH ·H O。
3 2 3 2
举例 判断并改正
错误,
①实验室制取氯气:
MnO +4H++2Cl- Mn2++Cl↑+
2 2
MnO +4HCl Mn2++Cl↑+2HO+2Cl-
2 2 2
2HO
2
②氯气和水反应:Cl+HO 2H++Cl-+
2 2
错误,Cl+HO H++Cl-+HClO
2 2
ClO-
③过氧化钠和水反应: 错误,
2Na++O+2HO===4Na++4OH-+O↑ 2NaO+2HO===4Na++4OH-+O↑
2 2 2 2 2 2
④碳酸氢钠溶液与盐酸反应: 错误,
CO+2H+===CO ↑+HO HCO+H+===CO ↑+HO
2 2 2 2
错误,
⑤醋酸与碳酸钙反应:
2CHCOOH+CaCO ===2CH COO-+Ca2+
3 3 3
2H++CaCO ===Ca2++HO+CO↑
3 2 2
+HO+CO↑
2 2
三、“三查”是否满足三守恒
离子方程式除符合质量守恒外,还应符合电荷守恒,做题时往往只注意质量守恒,而忽略电荷守恒,
这也是命题者经常设置的“陷阱”。若是氧化还原反应,还要符合电子守恒。
举例 判断并改正
①钠和水反应:Na+HO===Na++OH-+H↑ 错误,2Na+2HO===2Na++2OH-+H↑
2 2 2 2
②铜与氯化铁溶液反应:Cu+Fe3+===Fe2++Cu2
错误,Cu+2Fe3+===2Fe2++Cu2+
+
③铝与氢氧化钠溶液反应:
错误,2Al+2HO+2OH-===2AlO+3H↑
2 2
Al+2OH-===AlO+H↑
2
四、“四查”“===”“ ”“↓”“↑”是否使用恰当。
用饱和FeCl 溶液制备胶体:
3
错误,Fe3++3HO Fe(OH) (胶体)+
2 3
Fe3++3HO Fe(OH) ↓+3H+ 3H+
2 3NaHCO 溶液因水解呈碱性:
3
错误,HCO+HO HCO+OH-
HCO+HO===H CO+OH- 2 2 3
2 2 3
向NH Cl溶液中滴入烧碱溶液并加热:
4
错误,NH+OH- NH ↑+HO
3 2
NH+OH- NH ·H O
3 2
五、“五查”反应物的用量:如过量、少量、足量、等物质的量等。
在离子方程式正误判断中,做题时往往忽略相对量的影响,命题者往往设置“离子方程式正确,但不
符合相对量”的陷阱。突破“陷阱”的方法一是审准“相对量”的多少,二是看离子反应是否符合该量。
①看反应物或产物的配比是否正确。如稀硫酸与Ba(OH) 溶液反应,不能写成H++OH-+SO+Ba2+
2
===BaSO ↓+HO,应写成2H++2OH-+SO+Ba2+===BaSO ↓+2HO。
4 2 4 2
②看是否符合题设条件的要求。如过量、少量、等物质的量、适量、任意量以及滴加顺序等对反应产
物的影响。如向溴化亚铁溶液中通入少量Cl 的离子方程式为2Fe2++Cl===2Fe3++2Cl-;向溴化亚铁溶液
2 2
中通入过量Cl 的离子方程式为2Fe2++4Br-+3Cl===2Fe3++6Cl-+2Br 。
2 2 2
氢氧化钡溶液与稀硫酸反应:
错误,Ba2++2OH-+2H++SO===BaSO ↓+2HO
4 2
Ba2++OH-+H++SO===BaSO ↓+HO
4 2
向FeBr 溶液中通入等量Cl:
2 2
错误,2Fe2++2Br-+2Cl===2Fe3++Br +4Cl-
2 2
2Fe2++4Br-+3Cl===2Fe3++2Br +6Cl-
2 2
六、“六查”是否漏掉离子反应。
如Ba(OH) 溶液与CuSO 溶液反应,既要写Ba2+与SO生成BaSO 沉淀,又不能漏掉Cu2+与OH-生成
2 4 4
Cu(OH) 沉淀。
2
氢氧化钡溶液与硫酸铜溶液反应: 错误,
Ba2++SO===BaSO ↓ Ba2++2OH-+Cu2++SO===BaSO ↓+Cu(OH) ↓
4 4 2
(NH )SO 与Ba(OH) 反应: 错误,
4 2 4 2
Ba2++SO===BaSO ↓ Ba2++2OH-+2NH+SO===BaSO ↓+2NH ·H O
4 4 3 2
【策略2】两个方面突破离子共存问题
1.判断离子能否大量共存的“四个要点”:一色、二性、三特殊、四反应。
(1)一色——溶液颜色
离子 Cu2+ Fe3+ Fe2+ MnO
溶液颜色 蓝色 棕黄色 浅绿色 紫红色
(2)二性——溶液的酸碱性
①在强酸性溶液中,OH-及弱酸根阴离子(如CO、ClO-、SO、S2-、CHCOO-等)不能大量存在。
3
②在强碱性溶液中,H+及弱碱阳离子(如NH、Al3+、Cu2+、Mg2+、Zn2+、Fe3+等)不能大量存在。
③如HCO、HS-、HSO、HPO、HPO等,在强酸性或强碱性溶液中均不能大量存在。
2
(3)三特殊——三种特殊情况:①AlO与HCO不能大量共存:AlO+HCO+HO===Al(OH) ↓+CO。
2 3
②“NO+H+”组合具有强氧化性,能与S2-、Fe2+、I-、SO等还原性的离子发生氧化还原反应而不
能大量共存。
③NH与CHCOO-、CO,Mg2+与HCO等组合中,虽然两种离子都能水解且水解相互促进,但总的
3
水解程度仍很小,它们在溶液中仍能大量共存。
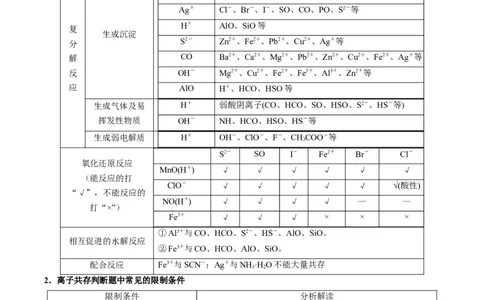
(4)四反应——四种反应类型
反应类型
离子 不能大量共存的离子
Ba2+、Ca2+ SO、CO、SO、SiO、PO等
Ag+ Cl-、Br-、I-、SO、CO、PO、S2-等
H+ AlO、SiO等
复
生成沉淀
分
S2- Zn2+、Fe2+、Pb2+、Cu2+、Ag+等
解 CO Ba2+、Ca2+、Mg2+、Pb2+、Zn2+、Cu2+、Fe2+、Ag+等
反 OH- Mg2+、Cu2+、Fe2+、Fe3+、Al3+、Zn2+等
应 AlO H+、HCO、HSO等
生成气体及易 H+ 弱酸阴离子(CO、HCO、SO、HSO、S2-、HS-等)
挥发性物质 OH- NH、HCO、HSO、HS-等
生成弱电解质 H+ OH-、ClO-、F-、CHCOO-等
3
S2- SO I- Fe2+ Br- Cl-
氧化还原反应
MnO(H+) √ √ √ √ √ √
(能反应的打
ClO- √ √ √ √ √ √(酸性)
“√”,不能反应的
NO(H+) √ √ √ √ — —
打“×”)
Fe3+ √ √ √ × × ×
①Al3+与CO、HCO、S2-、HS-、AlO、SiO。
相互促进的水解反应
②Fe3+与CO、HCO、AlO、SiO。
配合反应 Fe3+与SCN-;Ag+与NH ·H O不能大量共存
3 2
2.离子共存判断题中常见的限制条件
限制条件 分析解读
无色溶液 有色离子不能大量共存(透明溶液可能含有色离子)
使甲基橙呈红色或pH=1 溶液显酸性,OH-及弱酸的酸根离子不能大量共存
溶液呈碱性,H+及弱碱的阳离子、弱酸的酸式酸根离子不能
遇酚酞呈红色或pH=13
大量共存
与Al反应放出H 溶液可能显酸性,也可能显强碱性,显酸性时不能含NO
2
由水电离出的c(H+)=1×10-13 mol·L-
溶液可能显酸性,也可能显碱性
1
通入足量的CO(或NH ) 溶液呈酸性(或碱性)
2 3因发生氧化还原反应而不能大量共存 能发生氧化还原反应的氧化性离子和还原性离子不能大量共存
“一定”“可能”还是“不能”大量
确定是“可能性”还是“肯定性”
共存
说明该溶液呈酸性[稀释的是溶质,溶质c(H+)减小,而c(OH
加水稀释,减小
-)增大]
某溶液的lg =12 该溶液呈酸性
【策略3】牢记常见离子检验的特征反应及注意事项
(1)常见阳离子的检验
【易错提醒】阳离子检验的注意事项
NaOH溶液可以同时鉴别出若干种阳离子,包括Al3+、Fe3+、Fe2+、Cu2+、NH、Mg2+等多种离子,在阳
离子鉴别中,NaOH溶液是一种应用较广的试剂。若先使用NaOH溶液(必要时可加热)检验出几种离子,
再用其他方法鉴别用NaOH溶液鉴别不出来的离子,整个问题可以较快解决。
(2)常见阴离子的检验【易错提醒】阴离子检验的注意事项
①AgNO 溶液与稀硝酸、BaCl 溶液与稀盐酸这两组试剂,可以鉴别出若干种阴离子,是阴离子鉴别
3 2
最常用的试剂组合。一般说来,若待检的若干种离子中有SO,最好先用BaCl 溶液和盐酸这组试剂,检出
2
包括SO在内的一些离子,其他离子再用AgNO 溶液与稀硝酸等去鉴别。
3
②为了检验某盐中含SO或CO,可以直接加酸(非氧化性酸,如盐酸),根据放出气体的气味等特征现
象判断气体是CO 或SO ,进而确定物质中含CO或SO。
2 2
③灵活运用阴离子检验的知识,有时可以解决某些阳离子的鉴别问题。例如,在一定条件下,可考虑
用卤素离子(如Cl-)检出Ag+,用SO检出Ba2+。
【策略4】坚持“四项基本原则”突破离子推断
1.离子推断的“四项基本原则”
(1)肯定原则:根据实验现象推出溶液中肯定存在或肯定不存在的离子(记住几种常见的有色离子:Fe2
+、Fe3+、Cu2+、MnO、CrO、Cr O)。
2
(2)互斥原则:在肯定某些离子存在的同时,结合离子共存规律,否定一些离子的存在(注意题目中的隐
含条件,如酸性、碱性、指示剂的颜色变化、与铝反应产生H、水的电离情况等)。
2
(3)电中性原则:溶液呈电中性,溶液中有阳离子,必有阴离子,且溶液中阳离子所带正电荷总数与阴
离子所带负电荷总数相等(这一原则可帮助我们确定一些隐含的离子)。
(4)进出原则:通常是在实验过程中使用,是指在实验过程中反应生成的离子或引入的离子对后续实验
的干扰。
2.电荷守恒在定量型离子推断试题中的应用
离子定量推断试题常根据离子的物质的量(或浓度)定量推断最后一种离子的存在:如果多种离子共存,
且只有一种离子的物质的量未知,可以用电荷守恒来确定最后一种离子是否存在,即阳离子所带的正电荷
总数等于阴离子所带的负电荷总数。
考向一 离子方程式的正误判断
1.(2023·重庆·统考高考真题)下列离子方程式中,错误的是
A. 通入水中:
B. 通入石灰乳中:
C. 放入 溶液中:
D. 放入 溶液中:
2.(2023·浙江·统考高考真题)下列反应的离子方程式正确的是
A.碘化亚铁溶液与等物质的量的氯气:
B.向次氯酸钙溶液通入足量二氧化碳:C.铜与稀硝酸:
D.向硫化钠溶液通入足量二氧化硫:
3.(2022·湖南·高考真题)下列离子方程式正确的是
A. 通入冷的 溶液:
B.用醋酸和淀粉 溶液检验加碘盐中的 :
C. 溶液中加入 产生沉淀:
D. 溶液与少量的 溶液混合:
考向二 无限定条件的离子共存
4.(2022·天津·统考高考真题)25℃时,下列各组离子中可以在水溶液中大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
5.(2021·湖南·统考高考真题)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
粒子组 判断和分析
A 、 、 、 不能大量共存,因发生反应:
B 、 、 、 不能大量共存,因发生反应:
C 、 、 、 能大量共存,粒子间不反应
D 、 、 、 能大量共存,粒子间不反应
考向三 限定条件下的离子共存
6.(2021·重庆·统考高考真题)25°时, 下列各组离子在指定溶液中一定能大量共存的是
A.1.0 mol·L-1氯化钡溶液中:Mg2+、K+、Br-、
B.1.0 mol·L-1硫酸中:A13+、Na+、Cl-、
C.pH=1l 的氨水中:Fe2+、Na+、 、ClO-
D.pH=1的硝酸中:Fe3+、K+、I-、
7.(2021·福建·统考高考真题)室温下,下列各组离子一定能与指定溶液共存的是
A. 的 溶液: 、 、 、
B. 的 溶液: 、 、 、
C. 的 溶液: 、 、 、
D. 的 溶液: 、 、 、8.(2021·天津·统考高考真题)常温下,下列各组离子在给定溶液中能大量共存的是
A.pH=1的溶液:Fe2+、Mg2+、 、
B.pH=12的溶液:K+、Na+、 、
C.pH=7的溶液:Na+、Cu2+、S2-、Cl-
D.pH=7的溶液:Al3+、K+、Cl-、
考向四 离子的检验
9.(2023·辽宁·统考高考真题)下列鉴别或检验不能达到实验目的的是
A.用石灰水鉴别NaCO 与NaHCO
2 3 3
B.用KSCN溶液检验FeSO 是否变质
4
C.用盐酸酸化的BaCl 溶液检验NaSO 是否被氧化
2 2 3
D.加热条件下用银氨溶液检验乙醇中是否混有乙醛
10.(2021·海南·统考高考真题)一次性鉴别等浓度的 、 、 三种溶液,下列方法不可
行的是
A.测定 B.焰色试验
C.滴加 溶液 D.滴加饱和 溶液,微热
考向五 离子的推断
11.(2022·全国·统考高考真题)某白色粉末样品,可能含有 、 、 和 。取
少量样品进行如下实验:
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加 溶液有沉淀生成。
该样品中确定存在的是
A. B.
C. D.
(建议用时:35分钟)
1.(2023·陕西商洛·一模)下列反应的离子方程式书写正确的是
A.金属Na与 溶液反应:
B. 溶于过量HI溶液:
C.澄清石灰水与过量小苏打溶液混合:
D.草酸( )与酸性 溶液反应:2.(2023·四川绵阳·统考模拟预测)常温下,下列各组离子在给定溶液中一定能大量共存的是
A.由水电离出的c(OH⁻)=10⁻⁴molL⁻¹的溶液中:
B. 溶液中: ⋅
C.加入过量明矾 后的溶液中:
D.通入CO 后的溶液中:
2
3.(2022·新疆乌鲁木齐·校联考一模)某澄清溶液含有下列离子: 、 、 、 、 、 、
、 中的若干种,且离子浓度相等,为了确定其组成,进行了下列实验:
①取10mL溶液,向其中加入盐酸,无现象;
②另取10mL溶液,向其中逐滴加入NaOH溶液,得到白色沉淀,继续滴加NaOH溶液,沉淀溶解;
对溶液成分的叙述正确的是
A.由“澄清”可推断 一定不存在 B.一定含有 、 、
C.可能含有 D. 的存在无法判断
4.(2022·陕西宝鸡·统考三模)某100mL溶液可能含有K+、 、Al3+、 、 、Cl-中的若干种,
取该溶液进行连续实验,实验过程如下图所示(所加试剂均过量,气体全部逸出):下列说法错误的是
A.原溶液中一定含有 、 ,无Al3+
B.原溶液中一定存在K+,可能存在Cl-
C.是否存在K+只有通过焰色反应才能确定
D.若原溶液中不存在C1-,则c(K+)=0.1mol·L-1
5.(2023·海南省·统考模拟预测)常温下,下列粒子在指定溶液中能大量共存的是
A. 溶液中: 、 、 、
B. 溶液中: 、 、 、
C. 酸性 溶液中: 、 、 、
D. 溶液中: 、 、 、
6.(2023·河南·校联考模拟预测)某溶液中可能含有 、 、 、 、 、 和 ,取该
溶液 ,加入过量 溶液,加热,得到 气体,同时产生红褐色沉淀,过滤、洗涤、灼烧,
得到 固体;向上述滤液中加足量 溶液,得到 不溶于盐酸的沉淀,由此可知原溶液中
A.至少存在3种离子B. 一定存在,且
C. 、 一定存在, 不能确定
D. 、 一定不存在, 可能存在
7.(2023·吉林长春·校考一模)下列各组离子能大量共存,且加入相应试剂后发生反应的离子方程式正确
的是
选项 离子组 加入试剂 加入试剂后发生的离子反应
A 、 、 溶液
、 、
B 溶液
、 、
C 气体
、 、
D 酸性 溶液
8.(2023·四川绵阳·统考一模)实验室用化学沉淀法除去粗盐中的Ca2+、Mg2+、 获得精制盐。下列叙
述有误的是
A.杂质离子除去顺序可确定为:SO 、Mg2+、Ca2+
B.加入试剂顺序可依次为:NaOH、NaCO、BaCl 、盐酸四种溶液
2 3 2
C.杂质离子沉淀完后,采取的分离操作用到的仪器是a、b、c、d
D.沉淀分离完成后,调整溶液pH时用到的全部仪器为a、c、e、f
9.(2023·四川雅安·统考模拟预测)常温下,下列各组粒子在指定溶液中一定能大量共存的是
A.澄清透明溶液:K+、Na+、SO 、MnO
B.遇KSCN变红色的溶液:Na+、Mg2+、I-、Cl-
C.pH=0的溶液: 、Fe2+、SO 、ClO-
2
D.通入足量NH 的溶液:K+、Cu2+、SO 、Cl-
3
10.(2023·海南省·统考模拟预测)下列实验操作能达到相应实验目的的是选项 实验操作 实验目的
向某无色溶液中滴加过量稀盐酸,将产生的气体通入
A 检验该溶液中是否含有
澄清石灰水中
B 用玻璃棒蘸取新制氯水,滴在 试纸上 测定新制氯水的
C 向 样品溶液中滴加 溶液 探究 是否变质
D 将化合物X溶于水并测定所得溶液的导电性 判断X是否为电解质
11.(2023·浙江宁波·统考模拟预测)下列过程中对应的离子方程式正确的是
A.向苯酚钠溶液中通入少量 :
B.酚酞滴入碳酸钠溶液中变红:
C.同浓度同体积明矾 溶液与 溶液混合:
D.用醋酸和淀粉 溶液检验加碘盐中的 :
12.(2023·河北唐山·统考模拟预测)下列离子方程式书写正确的是
A.向AlCl 溶液中滴加氨水:
3
B.向Fe(SCN) 溶液中滴加入铁粉:
3
C.向苯酚钠溶液通入少量二氧化碳: +HCO
D.向Ba(OH) 溶液中滴加NaHSO 至Ba2+沉淀完全:
2 4
13.(2023·吉林长春·东北师大附中校考一模)下列实验设计、现象和结论都正确的是
选项 实验操作及现象 实验结论
取少量 样品溶于水,加入 溶液,再加
A 原样品已变质
入足量盐酸,产生白色沉淀
向某溶液中滴加浓盐酸,将产生气体通入石蕊试液,溶液
B 溶液中含有 或
先变红后褪色
C 向溶有 的 溶液中通入气体X,出现白色沉淀 气体X不一定是氧化性气体
在某固体试样加水后的溶液中,滴加 溶液,没有产
D 该固体试样中不可能存在
生使湿润红色石蕊试纸变蓝的气体
14.(2023·河南·校联考一模)下列离子方程式书写正确的是
A.向 溶液中通入过量 :B.CuO溶于 溶液:
C.向 溶液中通入 :
D.Fe与稀硝酸反应,当 时:
15.(2023·内蒙古赤峰·统考一模)某无色透明溶液中可能含有
中的几种、取 100mL溶液,向其中加入少量溴水,溶液仍呈无色,继续滴加足量盐酸和Ba(NO ) 混合,
3 2
产生沉淀,沉淀经洗涤、高温干燥后质量为4.66g。滤液加足量NaOH、加热、生成气体在标准状况下体积
为 1120mL。以下推测正确的是
A.原溶液中肯定存在
B.原溶液中一定不含
C.原溶液中可能存在 Na⁺、
D.另取试液滴加足量盐酸、BaCl 溶液,即可确定离子组成
2
16.某固体混合物可能由SiO、Fe O、Fe、NaSO 、NaCO、BaCl 中的若干种物质组成,设计部分实验
2 2 3 2 3 2 3 2
方案探究该固体混合物的成分,所加试剂均过量,下列说法正确的是
A.气体A是SO 和CO 的混合气体
2 2
B.固体A一定含有SiO,可能含有BaSO
2 4
C.该固体混合物中Fe O 和Fe至少有其中一种
2 3
D.该固体混合物一定含有NaCO、NaSO 、BaCl
2 3 2 3 2
17.(2024上·陕西宝鸡·高三校联考阶段练习)A、B、C、D、E五种常见的可溶性盐都是由下表中的离
子组成:
阳离子 、 , 、 、
阴离子 、 、 、
为了鉴别上述化合物,做了以下实验(已知AgOH能溶于氨水形成银氨溶液):
①灼烧D,火焰呈现黄色。
②A的水溶液呈中性,B、C、E的水溶液均呈酸性,D的水溶液呈碱性。
③若在这五种盐的水溶液中,分别加入 溶液,只有A、C的水溶液均不产生沉淀。
④若在这五种盐的水溶液中,分别加入氨水,E和C的水溶液中均有沉淀产生;继续分别加入氨水,C的
水溶液中的沉淀消失。
⑤把A的水溶液分别加入到B、C、E的水溶液中,均能生成不溶于稀硝酸的沉淀。回答下列问题:
(1)A的化学式是 ,B的化学式是 。
(2)D中含有金属元素,该金属元素的单质在工业上的冶炼原理为 (写化学方程式)。
(3)D的水溶液和E的水溶液混合,发生反应的离子方程式为 。
(4)C的水溶液和过量氨水反应的总的离子方程式是 。
18.(2023上·甘肃平凉·高三校联考阶段练习)有一包白色固体,可能含有 、 、KCl、
和无水 ,按下列步骤做实验:
①将该白色固体溶于水,得到无色溶液;
②向所得的无色溶液中加入足量 溶液,得到白色沉淀,再加稀硝酸,白色沉淀部分溶解并有气泡产
生,将气体通入澄清石灰水中,石灰水变浑浊。
回答下列问题:
(1)该白色固体中一定存在的物质是 ,一定不存在的物质是 ,可能存在的物质是
。
(2)称取该白色固体3.53 g,将其溶于水得到溶液A,在A中加入50 mL未知的 溶液恰好完全反应,
过滤得沉淀B,向B中加入足量稀硝酸,充分反应后剩余沉淀2.87g,同时放出0.224 L气体(标准状况)。
①该白色固体中 的质量分数为 (保留2位有效数字,下同)。
② 溶液中溶质的物质的量浓度为 。
③该白色固体的成分是 。
19.(2023上·河南·高三周口市文昌中学校联考阶段练习)写出符合下列情况的离子方程式。
(1)向 溶液中加入 溶液生成 和 : 。
(2)BaS溶液与硫酸锌溶液混合生成立德粉( ): 。
(3)向 溶液中加入 生成 : 。
(4)已知 不溶于水,但可溶于醋酸铵溶液,反应方程式如下:
,将硫化钠溶液与醋酸铅溶液混合,可生成沉淀,写
出反应的离子方程式: 。
(5)新制的氯水加到 溶液中,观察到氯水褪色,同时生成 和HCl,请写出反应的离子方程式:
。
(6) 能与热的经硫酸酸化的 溶液反应,生成 和 ,该反应的离子方程式:
。
20.(2023上·福建泉州·高三泉州五中校考阶段练习)
Ⅰ.某溶液中只可能含有 、 、 、 、 、 、 、 。当加入一种淡黄色固体
并加热时,有刺激性气体放出和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生
气体的物质的量(纵坐标)的关系如下图所示。(1)该淡黄色物质做焰色反应实验显黄色。可知溶液中含有的离子是 ;所含离子的物质的量浓度之
比为 ;所加的淡黄色固体是 。
Ⅱ.湿法制备高铁酸钾 的反应体系中有六种粒子: 、 、 、 、 、
。
(2)写出并配平湿法制高铁酸钾反应的离子方程式: 。
(3)每生成 转移 电子,若反应过程中转移了0.3mol电子,则还原产物的物质
的量为 。
Ⅲ.已知在稀硫酸中, 和 能发生以下反应(均未配平):
(4)试比较在酸性条件下 、 、 、 氧化性的强弱: 。
(5)以下离子方程式错误的是 (选填答案编号)。
a.
b.
c.d.